 МЫ РАССМОТРИМ Окисление различных классов органических соединений Примеры заданий
МЫ РАССМОТРИМ Окисление различных классов органических соединений Примеры заданий
 ОПРЕДЕЛЕНИЯ
ОПРЕДЕЛЕНИЯ
 ОПРЕДЕЛЕНИЯ
ОПРЕДЕЛЕНИЯ
 ОПРЕДЕЛЕНИЯ
ОПРЕДЕЛЕНИЯ
 КЛАССЫ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Алканы и циклоалканы Алкены Алкины Ароматические соединения Спирты и простые эфиры Альдегиды и кетоны Карбоновые кислоты
КЛАССЫ ОРГАНИЧЕСКИХ СОЕДИНЕНИЙ Алканы и циклоалканы Алкены Алкины Ароматические соединения Спирты и простые эфиры Альдегиды и кетоны Карбоновые кислоты
 ТИПЫ РЕАКЦИЙ ОКИСЛЕНИЯ Полное окисление (горение) Каталитическое окисление кислородом Препаративное окисление
ТИПЫ РЕАКЦИЙ ОКИСЛЕНИЯ Полное окисление (горение) Каталитическое окисление кислородом Препаративное окисление
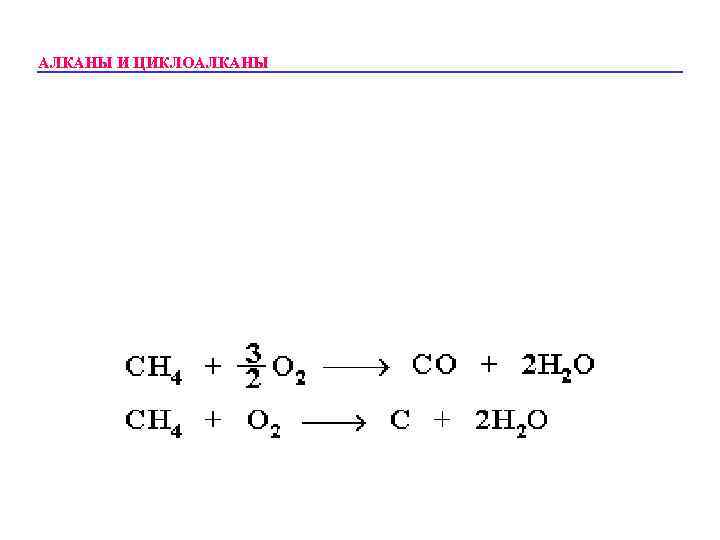
 АЛКАНЫ И ЦИКЛОАЛКАНЫ Уравнение реакции горения алканов в общем виде:
АЛКАНЫ И ЦИКЛОАЛКАНЫ Уравнение реакции горения алканов в общем виде:
 АЛКАНЫ И ЦИКЛОАЛКАНЫ
АЛКАНЫ И ЦИКЛОАЛКАНЫ
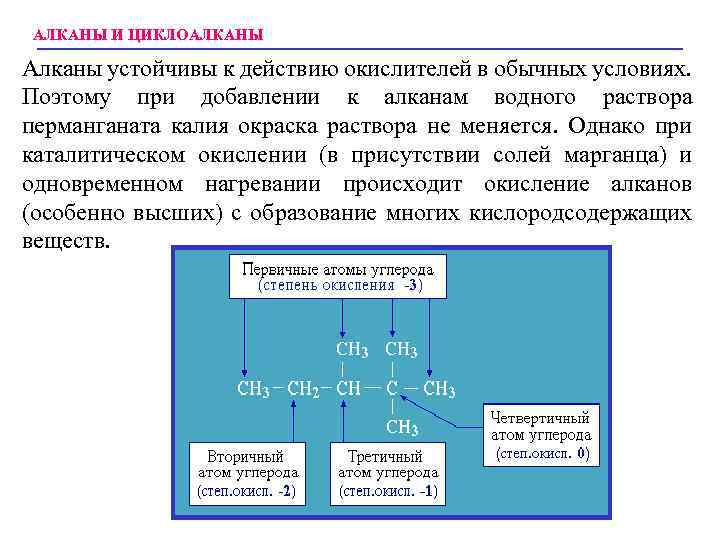 АЛКАНЫ И ЦИКЛОАЛКАНЫ Алканы устойчивы к действию окислителей в обычных условиях. Поэтому при добавлении к алканам водного раствора перманганата калия окраска раствора не меняется. Однако при каталитическом окислении (в присутствии солей марганца) и одновременном нагревании происходит окисление алканов (особенно высших) с образование многих кислородсодержащих веществ.
АЛКАНЫ И ЦИКЛОАЛКАНЫ Алканы устойчивы к действию окислителей в обычных условиях. Поэтому при добавлении к алканам водного раствора перманганата калия окраска раствора не меняется. Однако при каталитическом окислении (в присутствии солей марганца) и одновременном нагревании происходит окисление алканов (особенно высших) с образование многих кислородсодержащих веществ.
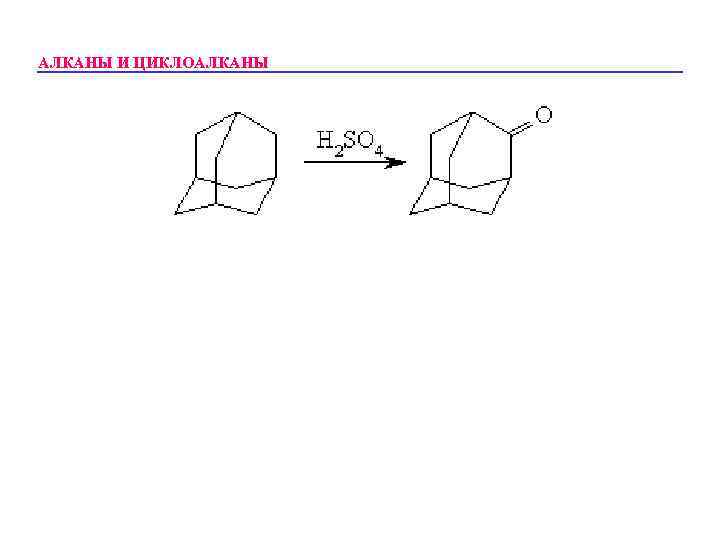
 АЛКАНЫ И ЦИКЛОАЛКАНЫ Частичное окисление алканов при относительно невысокой температуре и с применением катализаторов сопровождается разрывом только части связей С–С и С–Н и используется для получения ценных продуктов: карбоновых кислот, кетонов, альдегидов, спиртов. Например, при повышенной Т на медном катализаторе метан окисляется до метанола:
АЛКАНЫ И ЦИКЛОАЛКАНЫ Частичное окисление алканов при относительно невысокой температуре и с применением катализаторов сопровождается разрывом только части связей С–С и С–Н и используется для получения ценных продуктов: карбоновых кислот, кетонов, альдегидов, спиртов. Например, при повышенной Т на медном катализаторе метан окисляется до метанола:
 АЛКАНЫ И ЦИКЛОАЛКАНЫ
АЛКАНЫ И ЦИКЛОАЛКАНЫ
 АЛКАНЫ И ЦИКЛОАЛКАНЫ
АЛКАНЫ И ЦИКЛОАЛКАНЫ
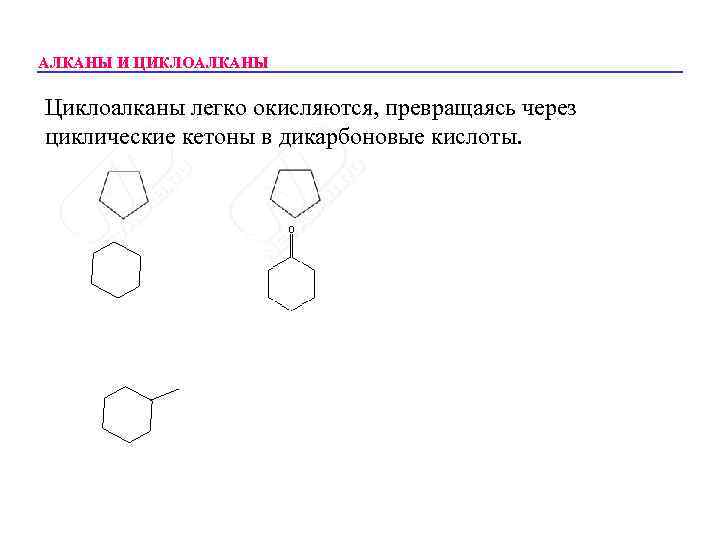 АЛКАНЫ И ЦИКЛОАЛКАНЫ Циклоалканы легко окисляются, превращаясь через циклические кетоны в дикарбоновые кислоты.
АЛКАНЫ И ЦИКЛОАЛКАНЫ Циклоалканы легко окисляются, превращаясь через циклические кетоны в дикарбоновые кислоты.
 АЛКЕНЫ
АЛКЕНЫ
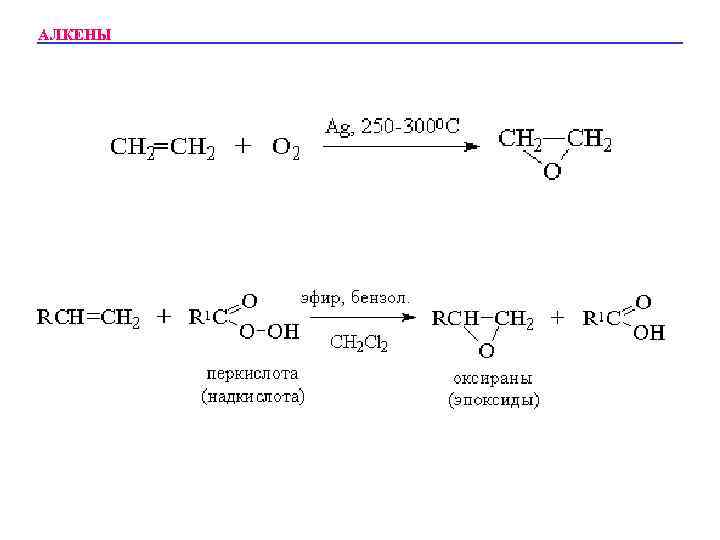 АЛКЕНЫ
АЛКЕНЫ
 АЛКЕНЫ
АЛКЕНЫ
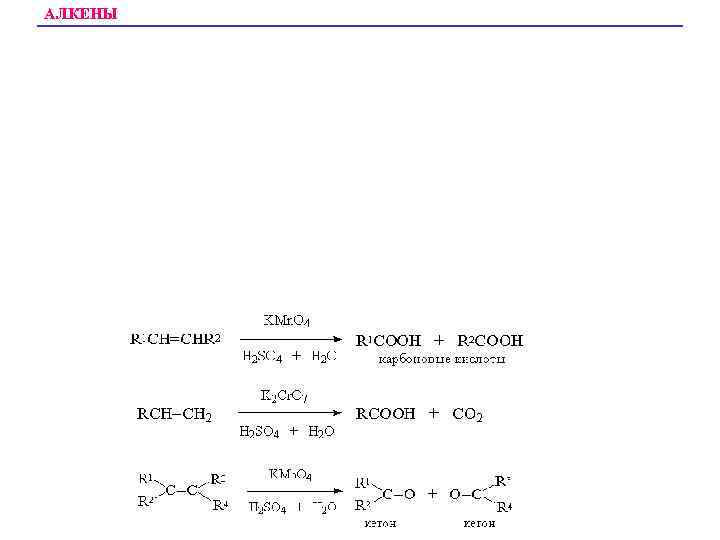 АЛКЕНЫ
АЛКЕНЫ
 АЛКЕНЫ
АЛКЕНЫ
 АЛКЕНЫ
АЛКЕНЫ
 АЛКИНЫ
АЛКИНЫ
 АЛКИНЫ
АЛКИНЫ
 АЛКИНЫ
АЛКИНЫ
 ВАЖНОЕ ЗАМЕЧАНИЕ В кислой среде: В нейтральной среде: В щелочной среде:
ВАЖНОЕ ЗАМЕЧАНИЕ В кислой среде: В нейтральной среде: В щелочной среде:
 АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
АРОМАТИЧЕСКИЕ СОЕДИНЕНИЯ
 СПИРТЫ И ПРОСТЫЕ ЭФИРЫ
СПИРТЫ И ПРОСТЫЕ ЭФИРЫ
 СПИРТЫ И ПРОСТЫЕ ЭФИРЫ
СПИРТЫ И ПРОСТЫЕ ЭФИРЫ
 ПРОСТЫЕ ЭФИРЫ
ПРОСТЫЕ ЭФИРЫ
 АЛЬДЕГИДЫ И КЕТОНЫ
АЛЬДЕГИДЫ И КЕТОНЫ
 АЛЬДЕГИДЫ И КЕТОНЫ
АЛЬДЕГИДЫ И КЕТОНЫ
 КАРБОНОВЫЕ КИСЛОТЫ
КАРБОНОВЫЕ КИСЛОТЫ
 МЫ РАССМОТРЕЛИ Окисление различных классов органических соединений Примеры заданий
МЫ РАССМОТРЕЛИ Окисление различных классов органических соединений Примеры заданий