4205c73b75bbf0dd77a9377794bbfe71.ppt
- Количество слайдов: 32


Муниципальное казенное общеобразовательное учреждение «Шарнутовская средняя общеобразовательная школа имени Б. С. Санджарыкова» Тема урока: «Железо и его соединения» Ниджляева Е. В. , учитель химии, I квалификационная категория

Начало железного века Каменный век Медный Бронзовый Железный век век IV – III тысячелетие до н. э. Конец IV – начало I тысячелетия до н. э. I тысячелетие до н. э.
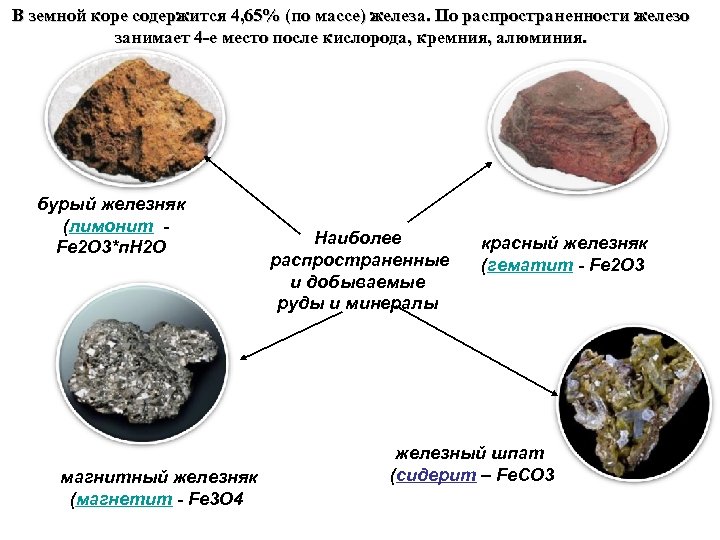
В земной коре содержится 4, 65% (по массе) железа. По распространенности железо занимает 4 -е место после кислорода, кремния, алюминия. бурый железняк (лимонит Fe 2 О 3*п. Н 2 О магнитный железняк (магнетит - Fe 3 O 4 Наиболее распространенные и добываемые руды и минералы красный железняк (гематит - Fe 2 O 3 железный шпат (сидерит – Fe. CO 3

Памятник «Танк Т-34»


Характеристика железа как химического элемента • 1. Химический символ и название элемента • Fe – железо • 2. Положение в Периодической системе(атомный номер, номер периода и группы) • 26, 4 период, VIII В группа • 3. Строение атома (заряд ядра, число электронов, число уровней, распределение электронов по уровням) • (+26; 4; 2 е, 8 е, 14 е, 2 е)

Выводы: 1. В атоме железа электронами заполняется предвнешний энергетический уровень; 2. Валентными являются электроны внешнего и, частично, предвнешнего энергетических уровней; 3. Атомы железа проявляют переменную степень окисления (+2 и + 3).
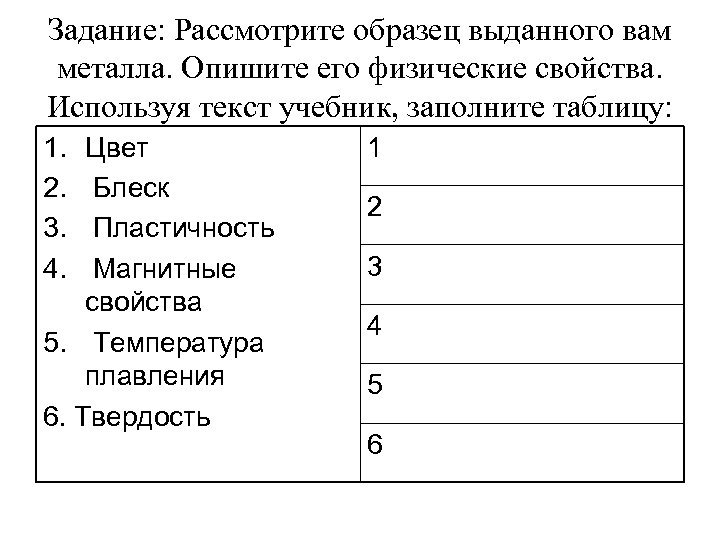
Задание: Рассмотрите образец выданного вам металла. Опишите его физические свойства. Используя текст учебник, заполните таблицу: 1. 2. 3. 4. Цвет Блеск Пластичность Магнитные свойства 5. Температура плавления 6. Твердость 1 2 3 4 5 6

• Железо дает два ряда соединений, соответствующих степени окисления +2, +3. Степень окисления Fe зависит от окислительной способности реагирующего вещества. • У сильных окислителей железо принимает степень окисления +3, у более слабых +2.
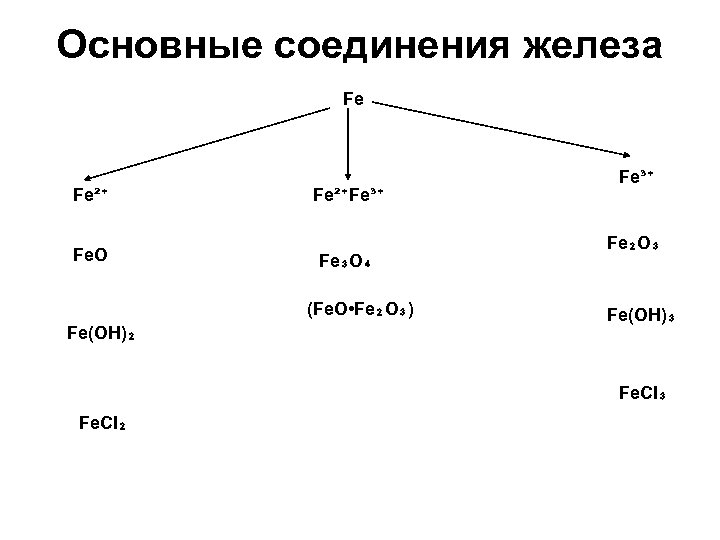
Основные соединения железа Fe Fe²⁺ Fe. O Fe²⁺Fe³⁺ Fe₃O₄ (Fe. O • Fe₂O₃) Fe(OH)₂ Fe³⁺ Fe₂O₃ Fe(OH)₃ Fe. CI₂



Химические свойства железа Взаимодействие железа с кислородом:

Химические свойства железа Взаимодействие железа с кислородом: 3 Fe + 2 O 2 = Fe 3 O 4 (Fe. O*Fe 2 O 3)

Химические свойства железа Взаимодействие железа с кислородом:

Химические свойства железа Взаимодействие железа с хлором: 2 Fe + 3 Cl 2 = 2 Fe. Cl 3

• Железо + соляная кислота Fe + 2 HCl = Fe. Cl 2 + H 2 • Железо + сульфат меди(II) Fe + Cu. SO 4 = Fe. SO 4 + Cu

Получение гидроксидов железа Fe. CI₂ + 2 Na. OH = Fe(OH)₂↓ +2 Na. CI Fe. CI₃ + 3 Na. OH = Fe(OH)₃↓ + 3 Na. CI Fe(OH)₂ окисляется на воздухе: сначала зеленеет, потом приобретает бурую окраску 4 Fe(OH)₂ + 2 H₂O + O₂ = 4 Fe(OH)₃

Качественные реакции на ионы Fe²⁺ и Fe³⁺ реактив – роданид калия KSCN Fe³⁺ реактив – желтая кровяная соль Fe²⁺ реактив – красная кровяная соль - – K₄[Fe(CN)₆] K₃[Fe(CN)₆]

Биологическая роль железа. • Какое значение имеет железо для жизнедеятельности растений? • Какое значение имеет железо для жизни животных и человека? • К каким последствия для здоровья человека может привести снижение его содержания в крови? • Как восполнить недостаток железа в организме? • Какие продукты богаты этим элементом?
«Железо в живых организмах» Большая часть железа (около 70%) сосредоточена в гемоглобине крови. Гемоглобин — красный пигмент эритроцитов. В 100 мл крови в норме содержится около 15 г гемоглобина.

Важнейшие источники железа • • • Содержание железа в 100 г продукта Печень 9 мг Персики 4 мг Хлеб 2 мг Грибы свежие 5 мг Грибы сушёные 35 мг Яблоки 3 мг

Тест • • • • 1. На Земле химически чистое железо: а) не встречается; б) встречается самородное; в) содержится в морской воде; г) встречается метеоритного происхождения. 2. Какое из утверждений верно: а) атомы железа в химических процессах могут проявлять окислительные или восстановительные свойства; б) во всех соединениях железо проявляет степень окисления +2; в) на внешнем энергетическом уровне атома железа два электрона, следовательно, это элемент II группы; г) число энергетических уровней у атома железа равно четырем, следовательно, это элемент 4 периода. 3. Железо, в отличие от алюминия, магния обладает особым свойством: а) электропроводностью; б) теплопроводностью; в) магнитными свойствами; г) ковкостью. 4. Для производства чугуна в качестве сырья не применяется руда: а) бурый железняк; б) железный колчедан; в) красный железняк; г) магнитный железняк. 5. Ионы железа входят в состав: а) костной ткани; б) гемоглобина крови; в) серого вещества мозга; г) эмали зубов.

Вопрос. Что здесь лишнее? Fe. Cl 3 Fe(NO 3)2 Fe. S Fe O 2 3 Fe. SO 4 Fe. CO 3

Блиц по теме «Железо» • • • • Число электронов на внешнем уровне в атоме железа Число d-электронов в атоме железа в основном состоянии Число энергетических уровней у атома элемента № 26 Количество протонов в изотопе железа с относительной атомной массой 57 Общее число электронов в ионе Fe 2+ Место железа среди металлов по распространенности в природе При горении железа в чистом кислороде образуется Продукт окисления в реакции между железом и конц. азотной кислотой при нагревании Продукт взаимодействия железа с молекулярным хлором Характер оксида железа (II) Какие свойства оксида железа (III) доказывает реакция его взаимодействия и расплавом гидроксида натрия? Как изменяются основные свойства оксидов с возрастанием степени окисления железа? Белок, содержащий железо и участвующий в газообмене в животном организме Заболевание, вызываемое недостатком железа в крови человека

Генетические связи Fe Пройдите, составив соответствующую схему реакций, от одного указанного в задании вещества к другому: - ОТ ОКСИДА ЖЕЛЕЗА (II) ДО ЖЕЛЕЗА - ОТ ЖЕЛЕЗА ДО ОКСИДА ЖЕЛЕЗА (III) Fe. Cl 2 Fe Fe. Cl 3 Fe O Fe 3 O 4 Fe(OH)3 Fe(OH)2 Fe. SO 4 Fe 2 O 3
Трубопроводы для воды, нефти и газа Железо сегодня Автомобили , Тракторы, Подводные лодки, Бытовые приборы, Другие предметы Гидроэлектростанции и опоры линий электропередач

Железный век продолжается… Железо не только основа всего мира, самый главный металл окружающей нас природы, оно – основа культуры и промышленности, оно – орудие войны и мирного труда. И трудно во всей таблице Менделеева найти другой элемент, который был бы так связан с прошлым, настоящим и будущими судьбами человечества. А. Е. Ферсман.

Домашнее задание

Интернет-источники • www. catalogmineralov. ru – сайт содержит каталог минералов, большую коллекцию фотографий и описание минералов. • http: //. elementy. ru – сайт “ Элементы большой науки”, содержит каталоги и статьи науно-популярных журналов “Химия и жизнь”, “ Наука и жизнь”, “Природа” и др. • http: //www. ovitanah. com - сайт посвящен витаминам и микроэлементам, содержит интересную информацию. • http: //alhimik. ru – сайт “Алхимик” содержит самую разнообразную информацию по химии.

4205c73b75bbf0dd77a9377794bbfe71.ppt