Мультимедийный курс «Оборудование и технологии фармацевтического


Мультимедийный курс «Оборудование и технологии фармацевтического производства» Лекция 16 Основы обеспечения качества при производстве лекарственных средств. GMPстандарты. Валидация.

Обеспечение качества – это всеобъемлющее понятие, охватывающее все планируемые и систематически осуществляемые, а также подтверждаемые (если это требуется), виды деятельности в рамках системы качества, необходимые для создания гарантии того, что лекарственное средство соответствует своему назначению (определение, приведенное в руководстве по GMP) Обеспечение качества – часть менеджмента качества, направленное на создание уверенности в том, что требования к качеству выполняются и будут выполнены (определение, приведенное в стандарте ГОСТ Р ИСО 9000: 2001) Обеспечение качества лежит в основе всех документов в сфере обращения лекарственных средств 2
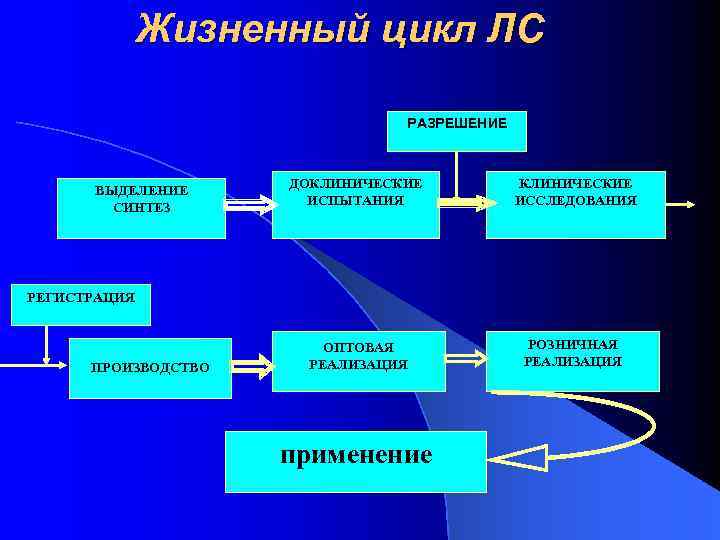
Жизненный цикл ЛС РАЗРЕШЕНИЕ ВЫДЕЛЕНИЕ ДОКЛИНИЧЕСКИЕ СИНТЕЗ ИСПЫТАНИЯ ИССЛЕДОВАНИЯ РЕГИСТРАЦИЯ ОПТОВАЯ РОЗНИЧНАЯ ПРОИЗВОДСТВО РЕАЛИЗАЦИЯ применение
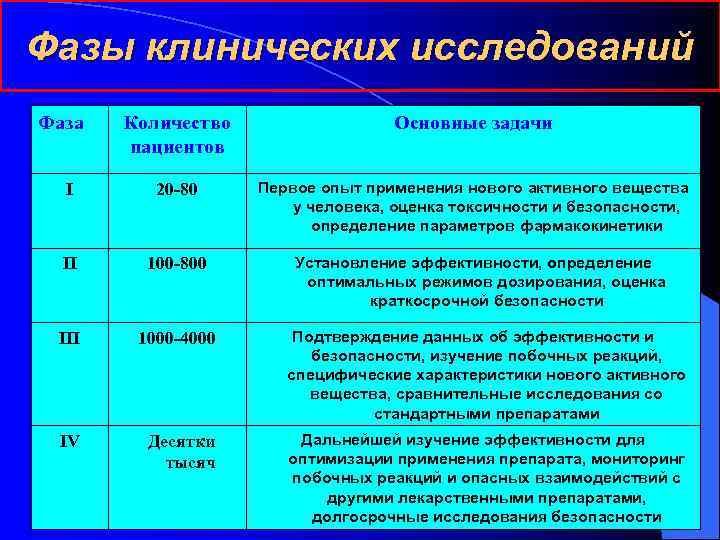
Фазы клинических исследований Фаза Количество Основные задачи пациентов I 20 -80 Первое опыт применения нового активного вещества у человека, оценка токсичности и безопасности, определение параметров фармакокинетики II 100 -800 Установление эффективности, определение оптимальных режимов дозирования, оценка краткосрочной безопасности III 1000 -4000 Подтверждение данных об эффективности и безопасности, изучение побочных реакций, специфические характеристики нового активного вещества, сравнительные исследования со стандартными препаратами IV Десятки Дальнейшей изучение эффективности для тысяч оптимизации применения препарата, мониторинг побочных реакций и опасных взаимодействий с другими лекарственными препаратами, 4 долгосрочные исследования безопасности

Доклинические испытания Испытания проводятся на животных (не менее двух видов) Цель: изучение механизма действия нового потенциального лекарственного препарата, его фармакокинетики, токсичности (острой, хронической, мутагенности, онкогенности). После завершения: выдача разрешения на проведение клинических исследований 5

Фаза I клинических исследований I фаза клинических испытаний (клиническая фармакология) — исследуемая группа состоит из 20– 80 человек. Первые испытания потенциального лекарственного препарата на человеке. В исследовании принимают участие здоровые добровольцы. Показатели, оцениваемые на фазе I - предварительная оценка препарата • безопасность • влияние на физиологические показатели • фармакокинетические и фармакодинамические показатели • активность • константы скорости элиминации, абсорбции, экскреции • пиковая концентрация в сыворотке крови • время достижения максимальной концентрации • метаболизм и лекарственное взаимодействие • активность • площадь под кривой «концентрация – время» (AUC) 6

Фаза II клинических исследований II фаза клинических испытаний (пилотные терапевтические исследования) — исследуемая группа состоит из 100– 800 человек. Оцениваются факторы сходные с теми, которые исследовались в I фазе. Проводятся обследование пациентов с конкретными заболеваниями. Показатели, оцениваемые на фазе II • безопасность (получение дополнительных данных) • доказательство клинической эффективности ЛС • определение возможных режимов дозирования ЛС (оценка соотношения доза-эффект) • определение минимальных и максимальных режимов дозирования • контроль возможной токсичности 7

Фаза III клинических исследований III фаза клинических испытаний (официальное клиническое испытание) — группа состоит из 1000– 4000 человек и и более. Испытание проводится на больших группах пациентов. Исследования проводятся в условиях, приближенным к тем, в которых препарат будет использован в случае получения разрешения и выпуска на фармацевтический рынок. Обычно принимают участие тысячи пациентов с определенным заболеванием. Показатели, оцениваемые на фазе III • оценка безопасности и эффективности ЛС при его длительном применении • доказательство клинической эффективности ЛС • изучение профиля и характера наиболее часто встречающихся побочных реакций • факторы, изменяющие действие активного вещества (взаимодействие с другими ЛП, возраст больных, сопутствующие заболевания) • сравнительные исследования со стандартными препаратами Результаты исследований в III фазе – точка опоры для регистрации лекарства 8

Фаза IV клинических исследований IV фаза клинических испытаний (постмаркетинговое исследование) — группа состоит десяток тысяч человек. Проводится при наличии регистрации на ЛС и после начала его широкого применения. Показатели, оцениваемые на фазе IV • мониторинг побочных реакций и опасных взаимодействий с другими препаратами, которые не были выявлены в III фазе • оценка различных дозировок ЛП • сроки лечения • взаимодействие с пищевыми продуктами • сравнительный анализ стандартных курсов лечения • анализ применения в различных возрастных группах • отдаленные результаты лечения (снижение или увеличение уровня смертности у пациентов, длительно получающих данный препарат) 9

Этапы создания лекарственного средства I. Научно-исследовательский этап Ш поиск схемы синтеза Ш наработка лабораторных образцов Ш биологические испытания Ш составление лабораторной прописи Ш уточнение и оптимизация схемы синтеза Ш предварительная оценка показателей качества II. Производственные этапы Ш Создание лабораторного регламента Ш Создание опытно-промышленного регламента Ш Разработка нормативной документации (фармакопейной статьи, фармакопейные статьи предприятия) 10

Этапы создания лекарственного средства I. Научно-исследовательский этап - химико-фармацевтические исследования. Используется полный набор аналитических методов для получения максимальной информации о превращениях исходного продукта в целевой Лабораторная пропись – итоговый документ научно-исследовательского этапа. Лабораторная пропись содержит исходные данные для составления технологических регламентов по сырью, описание всех стадий процесса получения конечного продукта и условий их проведения, показатели качества конечного продукта, характеристики полупродуктов и др. II. Производственные этапы - на основе полученной научно- исследовательской информации разрабатываются конкретные оптимальные методики аналитического контроля производства и показателей качества ЛС. На всех этих этапах необходимо проведение аналитического контроля с применение надежных методов исследования и анализа. 11

Технологические регламенты производства Технологический регламент производства - нормативный документ, устанавливающий методы производства, технологические нормативы, технические средства, условия и порядок проведения технологического процесса в производстве фармацевтической продукции, обеспечивающий получение лекарственного средства с показателями качества, отвечающими требованиям фармакопейной статьи, а также устанавливающий безопасность ведения работ и достижение оптимальных технико - экономических показателей конкретного производства. v Лабораторный регламент v Опытно-промышленный регламент v Пусковой регламент v Промышленный регламент 12

Лабораторный регламент производства Лабораторный регламент - технологический документ, которым завершаются научные исследования в лабораторных условиях при разработке метода производства новых лекарственных средств Проводятся исследования по окончательному выбору схемы синтеза ЛС на основании исходных данных лабораторной прописи § Рассматриваются различные варианты сырья и полупродуктов § Подбираются методы анализа, позволяющие по ходу процесса исследовать химические превращения, устанавливать структуру побочных и промежуточных продуктов § Оптимизируются технологические параметры (температура, p. H) § Определяется максимальное число контрольных точек § Исследуется влияние природы и количество примесей на последующие стадии процесса § Определяется требуемая степень очистки полупродуктов и исходного сырья 13

Опытно-промышленный регламент производства Опытно-промышленный регламент - технологический документ, которым завершается отработка новой технологии производства лекарственного средства на опытно - промышленной установке Параметры технологических процессов, записанные в лабораторной регламенте, проверяются на пилотной установке § уточняется состав реакционных смесей, требующих контроля; § устанавливаются более узкие диапазоны измеряемых концентраций; § определяются окончательные контрольные точки; § определяется периодичность анализов На основе полученных результатов предварительно разработанные методики адаптируются к условиям опытно-промышленного производства. При обработке технологии в этом масштабе используется в основном оборудование и КИП промышленного исполнения (р. Н-датчики, 14 расходометры, термометры и т. д. ).

Промышленный регламент производства Промышленный регламент - технологический документ действующего серийного производства лекарственного средства Это производственная и нормативно-техническая документация 1. Устанавливаются технико-экономические нормативы (расход сырья и материалов). 2. Составляются производственные инструкции. 3. Разрабатываются мероприятия по экологической безопасности Промышленный регламент утверждается руководителем промышленного предприятия и направляется на согласование в Минздрав РФ. 15

Стандарты качества Стандарт качества ЛС – это нормативный документ, содержащий перечень нормируемых показателей и методов контроля качества ЛС, утверждаемый Минздравом России Категории стандартов качества l Государственные стандарты качества Общая фармакопейная статья – перечень нормируемых показателей и методов контроля качества для конкретной лекарственной формы, описание физических, физико -химических, биохимических, биологических, микробиологических методов анализа, требования к используемым реактивам. Фармакопейная статья – разрабатывается на лекарственное средство и содержит обязательный перечень нормируемых показателей и методов контроля качества с учетом лекарственной формы, соответствующих требованиям ведущих зарубежных фармакопей. l Фармакопейная статья предприятия - перечень нормируемых показателей и методов контроля качества ЛС производства конкретного предприятия 16

Перечень разделов ФС и ФСП Лекарственное вещество (субстанция) 1. Название препарата на русском языке 2. Международное непатентованное название (МНН) на русском языке 3. Химическое название в соответствии с требованиями ИЮПАК 4. Структурная и эмпирическая формулы и молекулярная масса 5. Содержание действующего вещества (в процентах) 6. Описание 7 Растворимость 8. Подлинность 9. Температура плавления (разложения), или Температура затвердевания, или Температура кипения 10. Плотность 11. Удельное вращение 12. Удельный показатель поглощения 13. Показатель преломления 14. Прозрачность раствора 15. Цветность раствора 16. p. H или кислотность или щелочность 17. Механические включения 17

Перечень разделов ФС и ФСП Лекарственное вещество (субстанция) 18. Посторонние примеси (родственные соединения) 19. Показатели чистоты (хлориды, сульфатная зола и тяжелые металлы и т. п. ) 20. Потеря в массе при высушивании или вода, определяемая методом К. Фишера 21. Остаточные органические растворители (в случае их использования на последней стадии технологического процесса) 22. Пирогенность или содержание бактериальных эндотоксинов 23. Токсичность 24. Содержание веществ гистаминоподобного действия 25. Микробиологическая чистота или стерильность 26. Количественное определение 27. Упаковка 28. Маркировка 29. Транспортирование 30. Хранение 31. Срок годности 32. Фармакологическая группа 18

ГОСТ Р 52249 -2004 НАЦИОНАЛЬНЫЙ СТАНДАРТ РОССИЙСКОЙ ФЕДЕРАЦИИ ПРАВИЛА ПРОИЗВОДСТВА И КОНТРОЛЯ КАЧЕСТВА ЛЕКАРСТВЕННЫХ СРЕДСТВ GOOD MANUFACTURING PRACTICE FOR MEDICINAL PRODUCTS (GMP) Направлены на обеспечение высокого уровня качества и безопасности лекарственных средств и гарантирование того, что ЛС изготовлено в соответствии со своей формулой (составом), не содержит посторонних включений, маркировано надлежащим образом, упаковано и сохраняет свои свойства в течении всего срока 19 годности

ГОСТ Р 52249 -2004 Основные требования: 1. Управление качеством 2. Персонал 3. Помещения и оборудование 4. Документация 5. Производство 6. Контроль качества 7. Работа по контрактам на производство продукции и проведение анализов 8. Рекламации и отзыв продукции 9. Самоинспекция 20

Надлежащая производственная практика (GMP) - введение GMP - унифицированные правила производства лекарственных препаратов, которые производитель обязан выполнять, чтобы выпускать качественную фармацевтическую продукцию. Производитель работает на высококачественном дорогостоящем оборудовании, имеет систему внутреннего контроля на каждом этапе технологической цепочки. l Концепция была разработана в начале 70 -х годов XX века и впервые была введена в Великобритании в 1978 году. l GMP – система требований к порядку организации производства и контроля качества лекарственных средств, относящаяся к: - помещениям - оборудованию - персоналу - ведению документации - производственным отношениям l В РФ компетенция по установлению порядка организации производства и контроля качества лекарственных средств закреплена Минздравсоцразвития России 21

Надлежащая производственная практика (GMP) - введение Правила GMP направлены на обеспечение высокого уровня качества и безопасности лекарственных средств и гарантировании того, что лекарственное средство изготовлено в соответствии со своей формулой (составом) не содержит посторонних включений, маркировано надлежащим образом, упаковано и сохраняет свои свойства в течение всего срока годности. Стандарт распространяется на все виды лекарственных средств и устанавливает общие требования к их производству и контролю качества, а также специальные требования к производству отдельных видов лекарственных средств (Приложения 1 -18). Стандарт не распространяется на обеспечение промышленной безопасности, пожарной безопасности, взрывобезопасности, химической безопасности и безопасности других видов при производстве лекарственных средств, требования к которым приведены в других нормативных документах. 22

Основные требования GMP 1. Управление качеством - принципы - обеспечение качества - требования к производству и контролю качества ЛС - контроль качества 2. Персонал - принципы и общие положения - руководящие работники - обучение - гигиена персонала 3. Помещения и оборудование - принципы - помещения - производственная зона - зона складирования - зона контроля качества - вспомогательные зоны - оборудование 23

Основные требования GMP 4. Документация - принципы и общие положения - обязательная документация: - спецификации на исходные и упаковочные материалы, спецификации на промежуточную и нерасфасованную продукцию, спецификации на готовую продукцию - технологический регламент и технологические инструкции - инструкции по упаковке - протоколы на серию продукции - протоколы на упаковку серии продукции - инструкции и протоколы - отбор проб - проведение испытаний 5. Производство - принципы и общие положения - предотвращение перекрестного загрязнения при производстве - аттестация (валидация) - исходные материалы - промежуточная и нерасфасованная продукция - упаковочные материалы - операции по упаковке - готовая продукция - отклоненные, повторно использованные и возвращенные материалы 24

Основные требования GMP 6. Контроль качества - принципы и общие положения - организация работы контрольных лабораторий - документация - отбор проб - проведение испытаний 7. Работа по контрактам на производство продукции и проведение анализов - принципы и общие положения - заказчик - исполнитель - контракт 8. Рекламация и отзыв продукта - принципы - рекламации - отзыв продукции 9. Самоинспекция - принципы 25
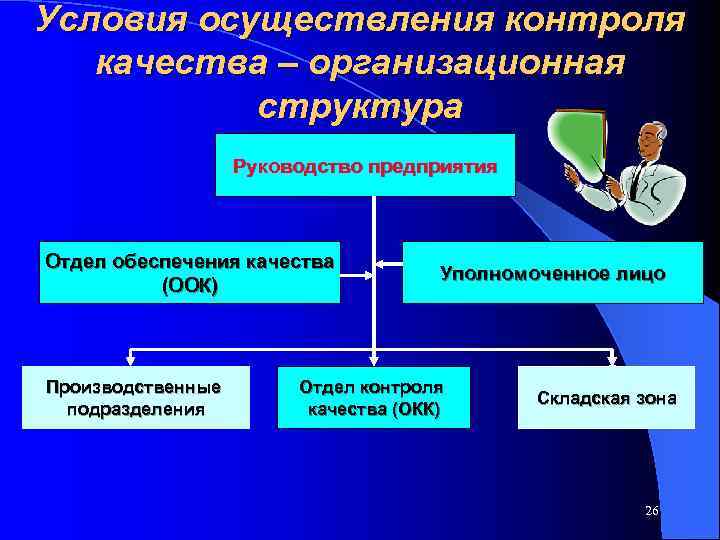
Условия осуществления контроля качества – организационная структура Руководство предприятия Отдел обеспечения качества Уполномоченное лицо (ООК) Производственные Отдел контроля Складская зона подразделения качества (ОКК) 26

Контроль качества Основная цель, преследуемая подобной структурой подчинения в СМК – формирование у Уполномоченного лица уверенности в том, что «каждая серия продукции произведена и проверена в соответствие с установленными требованиями» (ГОСТ Р 52249 -2004, п. 1. 2, VIII, п. 2. 4, а) Подпись на разрешении – Письменное гарантия соответствия качества разрешение на выпуск данной серии ЛС регистрационному досье 27
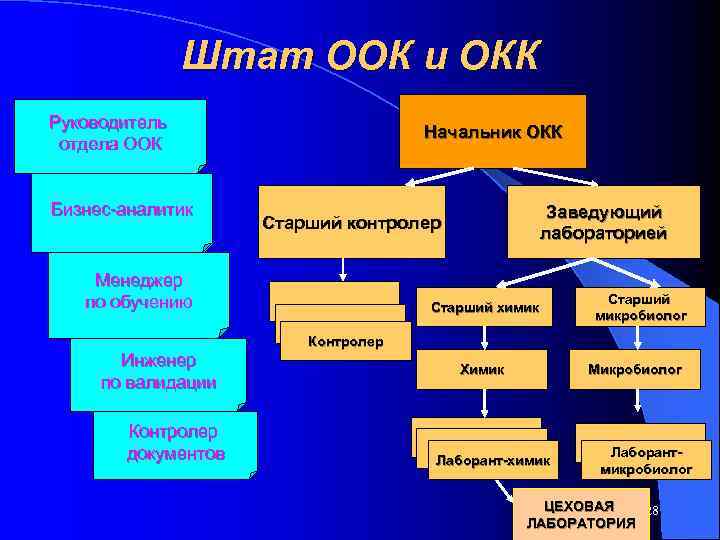
Штат ООК и ОКК Руководитель Начальник ОКК отдела ООК Бизнес-аналитик Заведующий Старший контролер лабораторией Менеджер по обучению Старший химик микробиолог Контролер Инженер Химик Микробиолог по валидации Контролер документов Лаборант-химик Лаборант- микробиолог ЦЕХОВАЯ 28 ЛАБОРАТОРИЯ

Контроль качества включает в себя отбор проб, проведение испытаний (анализов) и оформление соответствующей документации. Уровни контроля: l Входной контроль – контроль качества сырья, материалов и полупродуктов, поступивших от поставщика на предприятие для использовании в производстве. Цель процедур входного контроля – установить единый порядок проведения контроля их качества с тем, чтобы несоответствующие исходные компоненты не поступили на производство. l Оперативный контроль – это первый (низший) уровень контроля, когда измерение параметров (испытания) осуществляется в отношении наибольшего количества объектов (проб, отдельных стадий, операций и т. д. ). В свою очередь оперативный контроль подразделяется на предварительный, текущий и заключительный, основным компонентом каждого из которых является выборочный контроль. l Управленческий контроль – это второй уровень контроля, где на первое место выступает не качество измерения, а качество оценки и краткосрочного прогноза. Этот уровень контроля обеспечивает устранение возможных дефектов на промежуточных стадиях изготовления продукта, а не в готовом изделии, с предупреждением 29 возможности появления дефекта в данной точке в следующий раз.

Персонал Организация и функционирование производства и системы обеспечения качества лекарственных средств зависят от персонала. Предприятие должно быть укомплектовано персоналом необходимой численности и квалификации. Должностные обязанности каждого сотрудника должны быть оформлены документально и усвоены каждым сотрудником. Все сотрудники также должны знать требования настоящего стандарта (Правил GMP), относящиеся к сфере их деятельности, и проходить начальное и повторное обучение в необходимом объеме, в т. ч. по правилам личной гигиены. 30

Помещения и оборудование Место расположения, проект, строительство, монтаж, оснащение и обслуживание помещений и оборудования должны соответствовать характеру выполняемых работ. Планировка помещений и конструкция оборудования должны минимизировать риск ошибок, предусматривать проведение эффективной уборки и обслуживания с целью предотвращения перекрестного загрязнения, появления пыли или грязи и, в общем случае, устранения любого фактора, ухудшающего качество продукции. 31

Документация Правильно составленная документация является важной частью системы обеспечения качества. Четкое оформление документации позволяет предотвратить ошибки, возможные при устном общении, и проследить все этапы производства конкретной серии продукции. Спецификации, промышленные регламенты, инструкции, методики и протоколы серии продукции должны быть оформлены надлежащим образом и не должны содержать ошибок. Виды документов: l спецификация: документ, содержащий требования к материалам и продуктам, используемым или получаемым при производстве, являющийся основой для оценки качества лекарственных средств; l промышленный регламент, технологическая инструкция и инструкция по упаковке: документы, определяющие все используемые исходные материалы и операции по производству и упаковке продукции; l инструкция, методика, процедура: документ, содержащий указания по выполнению отдельных видов операций (например, по очистке, переодеванию, контролю окружающей среды, отбору проб, проведению испытаний, эксплуатации оборудования); l протокол на серию: документ, отражающий ход производства каждой серии продукции, в т. ч. разрешение на ее реализацию, и все факторы, влияющие на качество готовой продукции. 32

Другие документы системы обеспечения качества l Стандарты предприятия – документы, создаваемые и утверждаемые непосредственно на предприятии и определяющие его политику в той или иной области. l Стандартные операционные процедуры (СОП) – санкционированная на данном предприятии конкретная письменная методика осуществления определенной производственной, контрольной или вадидационной операции (процедуры). l Рабочие инструкции – это указание, описывающее порядок работы с технологическим, контрольным (аналитическим) или валидационным оборудованием. l Регистрационная документация (заполняемые формы) – это журналы, протоколы, акты, отчеты, списки, разработанные и используемые на предприятии с целью протоколирования (регистрации) любых действий, в результате которых создается ЛС. Регистрационная документация является надежным инструментом расследования несоответствий, управления ими, назначения корректирующих действий, предупреждения несоответствий - всего того, что регламентировано СМК. 33

Производство Для получения продукции требуемого качества технологические операции следует выполнять согласно промышленному регламенту и соответствующим инструкциям, требованиям настоящего стандарта, нормативных документов и регистрационного досье. Валидация (от англ. validation - проверка достоверности; подтверждение правильности) – это акт доказательства и документирования того, что процедура осуществляется эффективно. Валидация – важная часть системы обеспечения и контроля качества. Валидация – раздел правил GMP, касающийся надежности условий производства и их способности приводить к ожидаемым результатам по показателям качества продукции. 34
Валидация – документированная процедура, дающая высокую степень уверенности в том, что конкретный процесс, метод или система будет последовательно приводить к результатам, отвечающим заранее установленным критериям приемлемости. Повышение степени Необходимость ВАЛИДАЦИЯ гарантии качества совершенствования условий производства Валидация должна проводиться для: l Каждого технологического процесса перед его внедрением в производство; l Существующих процессов производства стерильных лекарственных средств (валидация технологического процесса и оборудования). 35

Объекты валидации Валидации подлежат: l Технологические процессы; l Аналитические методы; l Процессы очистки оборудования, коммуникаций и т. д. ; l Процессы санитарной обработки помещений и др. ; l Технологическое и лабораторное оборудование; l Инженерные системы, непосредственно влияющие на качество полупродукта и готового продукта (обеспечение чистым воздухом, паром, сжатым воздухом/ и др. ) l «Чистые» помещения и зоны l Компьютерный системы, связанные с процессом и контролем производства 36

Основные элементы валидации Оценка монтажа и работоспособности основного и вспомогательного оборудования, в том числе компьютерных систем Оценка условий и параметров технологического процесса Оценка предела возможного отклонения в ведении процесса Оценка методов анализа Составление протоколов и отчета, аттестующих технологический процесс 37
Обеспечение качества.GMP.Валидация.ppt
- Количество слайдов: 37

