МОУ «Гимназия «Дмитров» » , г. Дмитров, Московской










Основы квантовой теории.ppt
- Количество слайдов: 12
 МОУ «Гимназия «Дмитров» » , г. Дмитров, Московской области Приложение к работе Виртуальная периодическая система химических элементов двухмерного пространства «ОСНОВЫ КВАНТОВОЙ ТЕОРИИ» Авторы: Исмакова Анастасия и Першина Анастасия, 11 класс Научный руководитель: Першина Ольга Геннадьевна Дмитров, 2008
МОУ «Гимназия «Дмитров» » , г. Дмитров, Московской области Приложение к работе Виртуальная периодическая система химических элементов двухмерного пространства «ОСНОВЫ КВАНТОВОЙ ТЕОРИИ» Авторы: Исмакова Анастасия и Першина Анастасия, 11 класс Научный руководитель: Першина Ольга Геннадьевна Дмитров, 2008
 Квантовые числа – это энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится. Квантовые числа необходимы для описания состояния каждого электрона в атоме. Существует 5 квантовых чисел: v Главное v Побочное (орбитальное) v Магнитное v Спиновое v Проекция спина
Квантовые числа – это энергетические параметры, определяющие состояние электрона и тип атомной орбитали, на которой он находится. Квантовые числа необходимы для описания состояния каждого электрона в атоме. Существует 5 квантовых чисел: v Главное v Побочное (орбитальное) v Магнитное v Спиновое v Проекция спина
 Для энергетических уровней электрона в атоме приняты буквенные обозначения: Главное квантовое число n 1 2 3 4 5 6 7 Обозначение энергетического уровня K L M N O P Q Главное квантовое число – n – определяет vэнергетический уровень электрона, vудалённость энергетического уровня от ядра, vразмер электронного облака. Количество орбиталей - n 2 максимальное количество электронов на энергетическом уровне - 2 n². Главное квантовое число n 1 2 3 4 5 6 7 Число орбиталей 1 4 9 16 25 36 49 Максимальное количество e 2 8 18 32 50 72 98
Для энергетических уровней электрона в атоме приняты буквенные обозначения: Главное квантовое число n 1 2 3 4 5 6 7 Обозначение энергетического уровня K L M N O P Q Главное квантовое число – n – определяет vэнергетический уровень электрона, vудалённость энергетического уровня от ядра, vразмер электронного облака. Количество орбиталей - n 2 максимальное количество электронов на энергетическом уровне - 2 n². Главное квантовое число n 1 2 3 4 5 6 7 Число орбиталей 1 4 9 16 25 36 49 Максимальное количество e 2 8 18 32 50 72 98
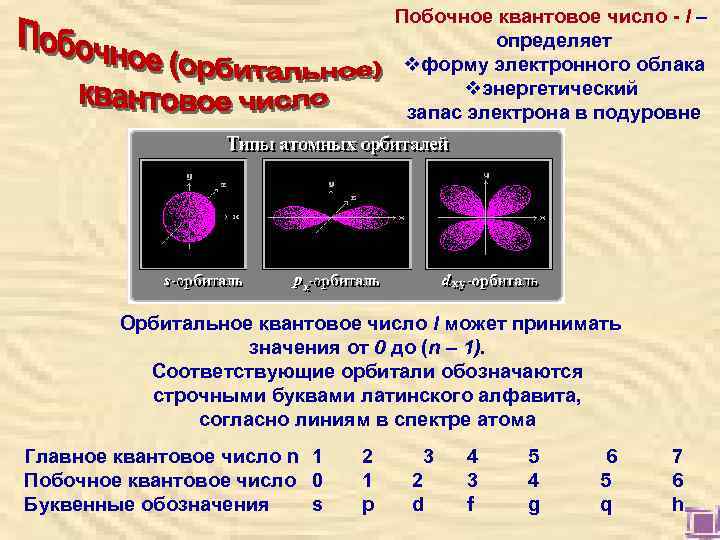
 Побочное квантовое число - l – определяет vформу электронного облака vэнергетический запас электрона в подуровне Орбитальное квантовое число l может принимать значения от 0 до (n – 1). Соответствующие орбитали обозначаются строчными буквами латинского алфавита, согласно линиям в спектре атома Главное квантовое число n 1 2 3 4 5 6 7 Побочное квантовое число 0 1 2 3 4 5 6 Буквенные обозначения s p d f g q h
Побочное квантовое число - l – определяет vформу электронного облака vэнергетический запас электрона в подуровне Орбитальное квантовое число l может принимать значения от 0 до (n – 1). Соответствующие орбитали обозначаются строчными буквами латинского алфавита, согласно линиям в спектре атома Главное квантовое число n 1 2 3 4 5 6 7 Побочное квантовое число 0 1 2 3 4 5 6 Буквенные обозначения s p d f g q h
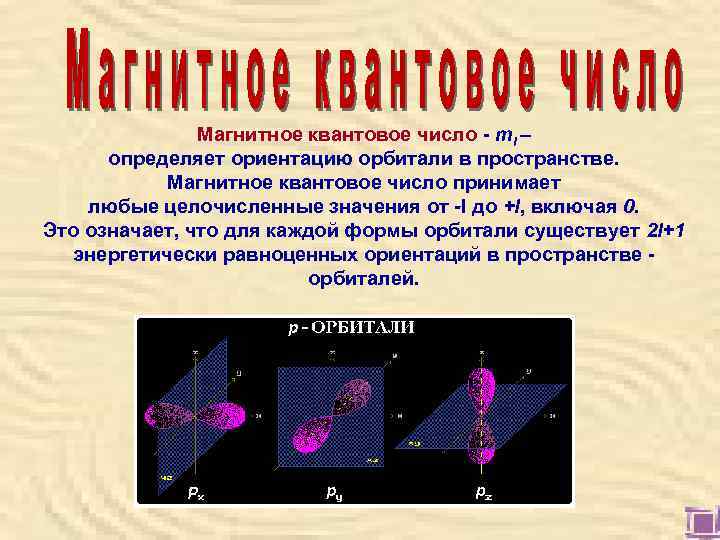
 Магнитное квантовое число - ml – определяет ориентацию орбитали в пространстве. Магнитное квантовое число принимает любые целочисленные значения от -l до +l, включая 0. Это означает, что для каждой формы орбитали существует 2 l+1 энергетически равноценных ориентаций в пространстве - орбиталей.
Магнитное квантовое число - ml – определяет ориентацию орбитали в пространстве. Магнитное квантовое число принимает любые целочисленные значения от -l до +l, включая 0. Это означает, что для каждой формы орбитали существует 2 l+1 энергетически равноценных ориентаций в пространстве - орбиталей.
 Спин — это собственный момент импульса электрона, не связанный с движением в пространстве. Проекция спина (магнитное спиновое число ms) может иметь лишь два значения: ms = + ½ или ms = - ½. Это соответствует двум возможным и противоположным другу направлениям собственного магнитного момента электрона. Для обозначения электронов с различной проекцией спина используются символы: ↑ и ↓.
Спин — это собственный момент импульса электрона, не связанный с движением в пространстве. Проекция спина (магнитное спиновое число ms) может иметь лишь два значения: ms = + ½ или ms = - ½. Это соответствует двум возможным и противоположным другу направлениям собственного магнитного момента электрона. Для обозначения электронов с различной проекцией спина используются символы: ↑ и ↓.
 При заполнении атомных орбиталей электронами соблюдаются три основные правила: 1. Принцип Паули 2. Правило Гунда (Хунда) 3. Принцип наименьшей энергии (правило Клечковского)
При заполнении атомных орбиталей электронами соблюдаются три основные правила: 1. Принцип Паули 2. Правило Гунда (Хунда) 3. Принцип наименьшей энергии (правило Клечковского)
 В 1925 году В. Паули установил правило: В атоме не может быть двух электронов, обладающих одинаковыми свойствами Или В атоме не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковы. Два электрона, находящиеся на одной орбитали (и характеризующиеся противоположно направленными спинами), называются спаренными. Спины одного направления называют параллельными, а противоположно направленные — антипараллельными.
В 1925 году В. Паули установил правило: В атоме не может быть двух электронов, обладающих одинаковыми свойствами Или В атоме не может быть двух электронов, у которых все четыре квантовых числа были бы одинаковы. Два электрона, находящиеся на одной орбитали (и характеризующиеся противоположно направленными спинами), называются спаренными. Спины одного направления называют параллельными, а противоположно направленные — антипараллельными.
 В 1927 г. на основе анализа атомных спектров было выведено немецким физиком-теоретиком Ф. Гундом (Хундом) правило Гунда (Хунда) : Устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня (подгруппы), при котором абсолютное значение суммарного спина атома максимально. Оно определяет порядок заселения электронами орбиталей, имеющих одинаковую энергию
В 1927 г. на основе анализа атомных спектров было выведено немецким физиком-теоретиком Ф. Гундом (Хундом) правило Гунда (Хунда) : Устойчивому состоянию атома соответствует такое распределение электронов в пределах энергетического подуровня (подгруппы), при котором абсолютное значение суммарного спина атома максимально. Оно определяет порядок заселения электронами орбиталей, имеющих одинаковую энергию
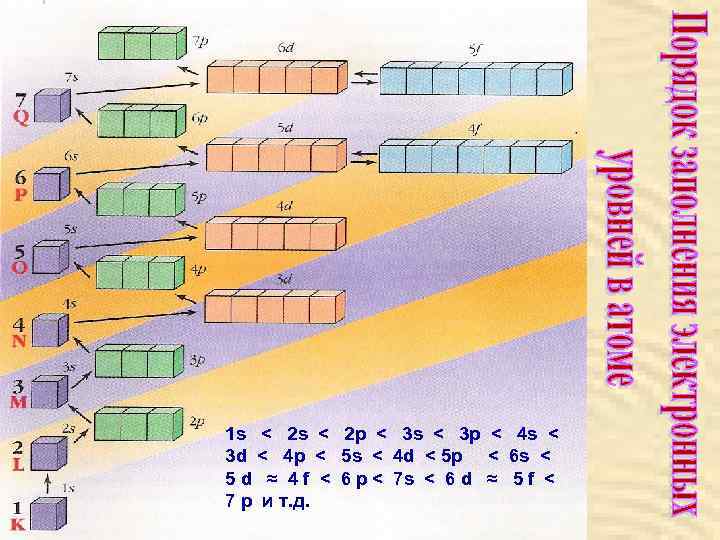
 Русский учёный В. М. Клечковский (1961 год) установил, что энергия электрона возрастает по мере увеличения суммы главного и орбитального квантовых чисел: а) В порядке увеличения сумм главного и орбитального квантовых чисел ( n + l ). б) Если для двух орбиталей суммы (n + l) имеют одинаковые значения, то вначале электронами заполняется орбиталь с меньшим значением главного квантового числа. При заполнении электронных слоёв атома в стационарном (невозбуждённом) состоянии выдерживается принцип наименьшей энергии электрона, в соответствии с которым, наиболее устойчивому состоянию электрона в атоме отвечает минимальная из возможных энергия этого электрона.
Русский учёный В. М. Клечковский (1961 год) установил, что энергия электрона возрастает по мере увеличения суммы главного и орбитального квантовых чисел: а) В порядке увеличения сумм главного и орбитального квантовых чисел ( n + l ). б) Если для двух орбиталей суммы (n + l) имеют одинаковые значения, то вначале электронами заполняется орбиталь с меньшим значением главного квантового числа. При заполнении электронных слоёв атома в стационарном (невозбуждённом) состоянии выдерживается принцип наименьшей энергии электрона, в соответствии с которым, наиболее устойчивому состоянию электрона в атоме отвечает минимальная из возможных энергия этого электрона.
 1 s < 2 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s < 5 d ≈ 4 f < 6 p < 7 s < 6 d ≈ 5 f < 7 p и т. д.
1 s < 2 s < 2 p < 3 s < 3 p < 4 s < 3 d < 4 p < 5 s < 4 d < 5 p < 6 s < 5 d ≈ 4 f < 6 p < 7 s < 6 d ≈ 5 f < 7 p и т. д.
 Расположение электронов по слоям и орбиталям называется электронной конфигурацией. Схемы электронного строения атомов показывают распределение электронов по электронным слоям (энергетическим уровням). Электронную конфигурацию атома хлора можно записать так: 17 Cl 2, 8, 7 Различают несколько видов написания электронных конфигураций: Электронная формула Электронная схема Электронно-графическая 2 2 6 2 5 формула 1 s 2 s 2 p 3 s 3 p K L M 3 +17 2 d 1 p 2 8 7 s
Расположение электронов по слоям и орбиталям называется электронной конфигурацией. Схемы электронного строения атомов показывают распределение электронов по электронным слоям (энергетическим уровням). Электронную конфигурацию атома хлора можно записать так: 17 Cl 2, 8, 7 Различают несколько видов написания электронных конфигураций: Электронная формула Электронная схема Электронно-графическая 2 2 6 2 5 формула 1 s 2 s 2 p 3 s 3 p K L M 3 +17 2 d 1 p 2 8 7 s

