2_Химия p-элементов_Галогены.pptx
- Количество слайдов: 42
 Московский Государственный Университет Тонких Химических Технологий им. М. В. Ломоносова ХИМИЯ ЭЛЕМЕНТОВ Лектор: ст. преп. , к. х. н. Дорохов Андрей Викторович
Московский Государственный Университет Тонких Химических Технологий им. М. В. Ломоносова ХИМИЯ ЭЛЕМЕНТОВ Лектор: ст. преп. , к. х. н. Дорохов Андрей Викторович
 ЛЕКЦИЯ № 2 1. Химия p-элементов. Общие сведения. 2. Химия галогенов. 3. 1. Общая характеристика галогенов. Свойства простых веществ. 3. 2. Галогеноводороды. 3. 3. Кислородные соединения галогенов. Лекция 2 1
ЛЕКЦИЯ № 2 1. Химия p-элементов. Общие сведения. 2. Химия галогенов. 3. 1. Общая характеристика галогенов. Свойства простых веществ. 3. 2. Галогеноводороды. 3. 3. Кислородные соединения галогенов. Лекция 2 1
 I. Химия p-элементов. Общие сведения Радиус атома, металличность ns 2 np 1 Лекция 2 Электроотрицательность, потенциал ионизации ns 2 np 5 2
I. Химия p-элементов. Общие сведения Радиус атома, металличность ns 2 np 1 Лекция 2 Электроотрицательность, потенциал ионизации ns 2 np 5 2
 II. Химия галогенов φθόρος - разрушение Галогены – «рождающие соль» άλός- соль γεννάω - рождать χλωρός - зелёный βρῶμος - зловоние ἰώδης- фиолетовый ἄστατος- неустойчивый Лекция 2 3
II. Химия галогенов φθόρος - разрушение Галогены – «рождающие соль» άλός- соль γεννάω - рождать χλωρός - зелёный βρῶμος - зловоние ἰώδης- фиолетовый ἄστατος- неустойчивый Лекция 2 3
 II. Химия галогенов 1. Общая характеристика галогенов. 2. Галогеноводороды. 3. Кислородные соединения галогенов. Лекция 2 4
II. Химия галогенов 1. Общая характеристика галогенов. 2. Галогеноводороды. 3. Кислородные соединения галогенов. Лекция 2 4
 II. Галогены. Общая характеристика 1. Общая характеристика элементов 1. 1. Строение атома (электронное). 1. 2. Физико-химические свойства простых веществ. 1. 3. Химические свойства, общие для всех элементов группы. 1. 4. Различия в химических свойствах элементов одной группы. 1. 5. Химические свойства простых веществ (отношение к H 2 O, H 3 O+, OH-, O 2, Hal 2). 1. 6. Распространённость в природе. История открытия. Методы получения. 1. 7. Применение. Лекция 2 5
II. Галогены. Общая характеристика 1. Общая характеристика элементов 1. 1. Строение атома (электронное). 1. 2. Физико-химические свойства простых веществ. 1. 3. Химические свойства, общие для всех элементов группы. 1. 4. Различия в химических свойствах элементов одной группы. 1. 5. Химические свойства простых веществ (отношение к H 2 O, H 3 O+, OH-, O 2, Hal 2). 1. 6. Распространённость в природе. История открытия. Методы получения. 1. 7. Применение. Лекция 2 5
 II. Химия галогенов. Общая характеристика. 1. 1. Строение атома (валентные подуровни). E XVII (VIIA) F, Cl, Br. I, At Характерные степени окисления: F: -I, 0 Cl: -I, 0, +III, +IV, +VI, +VII Br: -I, 0, +III, +IV, +VII I: -I, 0, +III, +VII At: -I, 0, +V 2 np 5 ns 1. Степени окисления: все от -I до +VII (кроме F); устойчивые – нечётные; наиболее устойчивая степень окисления: -I. 2. До завершения подуровня не хватает одного электрона склонность принимать электроны. Простые вещества – очень сильные окислители! Простые вещества – неметаллы! 3. Простые вещества – двухатомные (Hal 2). 4. Соединения Э-I – как правило, ионные. Лекция 2 6
II. Химия галогенов. Общая характеристика. 1. 1. Строение атома (валентные подуровни). E XVII (VIIA) F, Cl, Br. I, At Характерные степени окисления: F: -I, 0 Cl: -I, 0, +III, +IV, +VI, +VII Br: -I, 0, +III, +IV, +VII I: -I, 0, +III, +VII At: -I, 0, +V 2 np 5 ns 1. Степени окисления: все от -I до +VII (кроме F); устойчивые – нечётные; наиболее устойчивая степень окисления: -I. 2. До завершения подуровня не хватает одного электрона склонность принимать электроны. Простые вещества – очень сильные окислители! Простые вещества – неметаллы! 3. Простые вещества – двухатомные (Hal 2). 4. Соединения Э-I – как правило, ионные. Лекция 2 6
 II. Химия галогенов. Общая характеристика 1. 2. Физико-химические свойства простых веществ F 2 tк = -188 o. C d = 1. 693 г/см 3 Cl 2 tк = -33. 6 o. C d = 3. 214 г/см 3 Br 2 tк = 58. 8 o. C d = 3. 102 г/см 3 Период полураспада: ~ 8 ч. Максимальное количество: ~ 2∙ 10 -9 г Лекция 2 I 2 tпл = 113. 5 o. C d = 4. 940 г/см 3 At 2 tпл = 302 o. C 7
II. Химия галогенов. Общая характеристика 1. 2. Физико-химические свойства простых веществ F 2 tк = -188 o. C d = 1. 693 г/см 3 Cl 2 tк = -33. 6 o. C d = 3. 214 г/см 3 Br 2 tк = 58. 8 o. C d = 3. 102 г/см 3 Период полураспада: ~ 8 ч. Максимальное количество: ~ 2∙ 10 -9 г Лекция 2 I 2 tпл = 113. 5 o. C d = 4. 940 г/см 3 At 2 tпл = 302 o. C 7
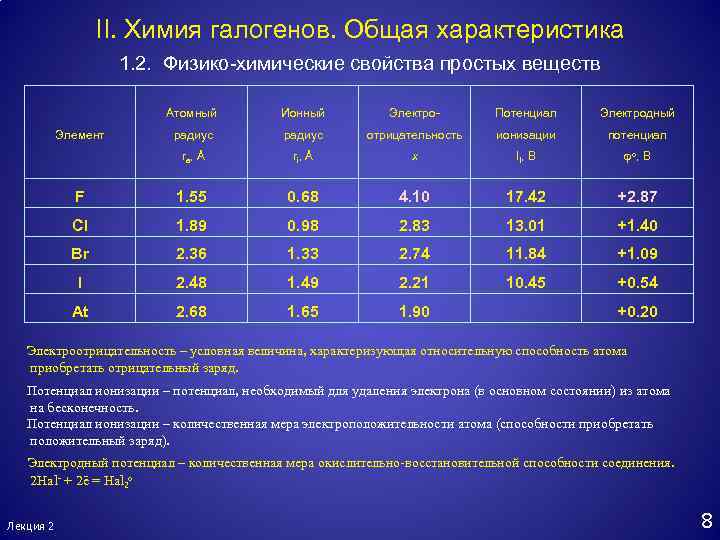 II. Химия галогенов. Общая характеристика 1. 2. Физико-химические свойства простых веществ Атомный Ионный Электро- Потенциал Электродный радиус отрицательность ионизации потенциал ra, Å ri, Å x II, В о, В F 1. 55 0. 68 4. 10 17. 42 +2. 87 Cl 1. 89 0. 98 2. 83 13. 01 +1. 40 Br 2. 36 1. 33 2. 74 11. 84 +1. 09 I 2. 48 1. 49 2. 21 10. 45 +0. 54 At 2. 68 1. 65 1. 90 Элемент +0. 20 Электроотрицательность – условная величина, характеризующая относительную способность атома приобретать отрицательный заряд. Потенциал ионизации – потенциал, необходимый для удаления электрона (в основном состоянии) из атома на бесконечность. Потенциал ионизации – количественная мера электроположительности атома (способности приобретать положительный заряд). Электродный потенциал – количественная мера окислительно-восстановительной способности соединения. 2 Hal- + 2ē = Hal 2 о Лекция 2 8
II. Химия галогенов. Общая характеристика 1. 2. Физико-химические свойства простых веществ Атомный Ионный Электро- Потенциал Электродный радиус отрицательность ионизации потенциал ra, Å ri, Å x II, В о, В F 1. 55 0. 68 4. 10 17. 42 +2. 87 Cl 1. 89 0. 98 2. 83 13. 01 +1. 40 Br 2. 36 1. 33 2. 74 11. 84 +1. 09 I 2. 48 1. 49 2. 21 10. 45 +0. 54 At 2. 68 1. 65 1. 90 Элемент +0. 20 Электроотрицательность – условная величина, характеризующая относительную способность атома приобретать отрицательный заряд. Потенциал ионизации – потенциал, необходимый для удаления электрона (в основном состоянии) из атома на бесконечность. Потенциал ионизации – количественная мера электроположительности атома (способности приобретать положительный заряд). Электродный потенциал – количественная мера окислительно-восстановительной способности соединения. 2 Hal- + 2ē = Hal 2 о Лекция 2 8
 II. Химия галогенов. Общая характеристика 1. 3. Химические свойства, общие для всех элементов групп A). Сильные окислительные свойства простых веществ окисление металлов: t Cl 2 + Cu = Cu. Cl 2 HO Br 2 + Al = Al. Br 3 2 (с воспламенением) окисление неметаллов (кроме O 2 и N 2): 5 Cl 2 + 2 P = 2 PCl 5 5 Cl 2 + 2 Sb = 2 Sb. Cl 5 2 S + Br 2 = S 2 Br 2 (хлор, бром - с воспламенением, фтор – со взрывом!) окисление других веществ: Hal 2 + H 2 S = S + 2 HHal SO 32 - + 2 Hal 2 + H 2 O = SO 42 - + 2 Hal- + 2 H+ окисление некоторых органических веществ (например, скипидар) – с воспламенением, фтор – со взрывом!) Лекция 2 9
II. Химия галогенов. Общая характеристика 1. 3. Химические свойства, общие для всех элементов групп A). Сильные окислительные свойства простых веществ окисление металлов: t Cl 2 + Cu = Cu. Cl 2 HO Br 2 + Al = Al. Br 3 2 (с воспламенением) окисление неметаллов (кроме O 2 и N 2): 5 Cl 2 + 2 P = 2 PCl 5 5 Cl 2 + 2 Sb = 2 Sb. Cl 5 2 S + Br 2 = S 2 Br 2 (хлор, бром - с воспламенением, фтор – со взрывом!) окисление других веществ: Hal 2 + H 2 S = S + 2 HHal SO 32 - + 2 Hal 2 + H 2 O = SO 42 - + 2 Hal- + 2 H+ окисление некоторых органических веществ (например, скипидар) – с воспламенением, фтор – со взрывом!) Лекция 2 9
 II. Химия галогенов. Общая характеристика. 1. 3. Химические свойства, общие для всех элементов групп Б). Кислотные свойства растворов галогеноводородов HHal + H 2 O = Hal- + H 3 O+ (Hal = Cl, Br, I) HF + H 2 O F- + H 3 O+ В). Кислотные свойства оксидов Сl 2 O 7 + 2 Na. OH = Na. Cl. O 4 + H 2 O Лекция 2 10
II. Химия галогенов. Общая характеристика. 1. 3. Химические свойства, общие для всех элементов групп Б). Кислотные свойства растворов галогеноводородов HHal + H 2 O = Hal- + H 3 O+ (Hal = Cl, Br, I) HF + H 2 O F- + H 3 O+ В). Кислотные свойства оксидов Сl 2 O 7 + 2 Na. OH = Na. Cl. O 4 + H 2 O Лекция 2 10
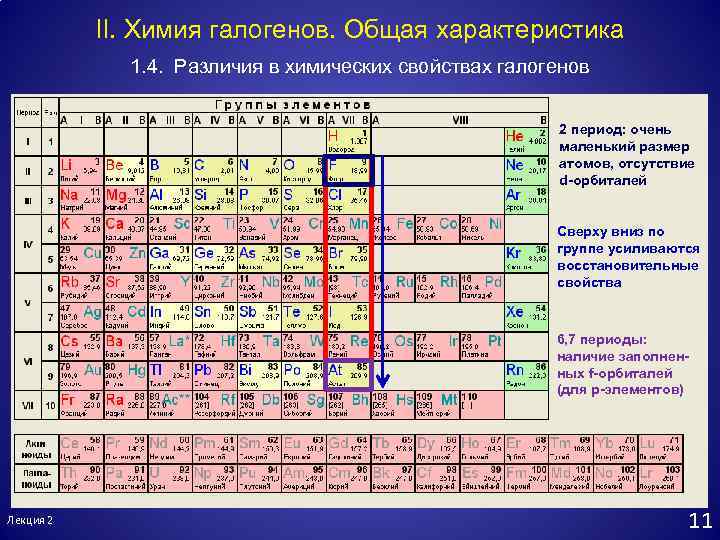 II. Химия галогенов. Общая характеристика 1. 4. Различия в химических свойствах галогенов 2 период: очень маленький размер атомов, отсутствие d-орбиталей Сверху вниз по группе усиливаются восстановительные свойства 6, 7 периоды: наличие заполненных f-орбиталей (для p-элементов) Лекция 2 11
II. Химия галогенов. Общая характеристика 1. 4. Различия в химических свойствах галогенов 2 период: очень маленький размер атомов, отсутствие d-орбиталей Сверху вниз по группе усиливаются восстановительные свойства 6, 7 периоды: наличие заполненных f-орбиталей (для p-элементов) Лекция 2 11
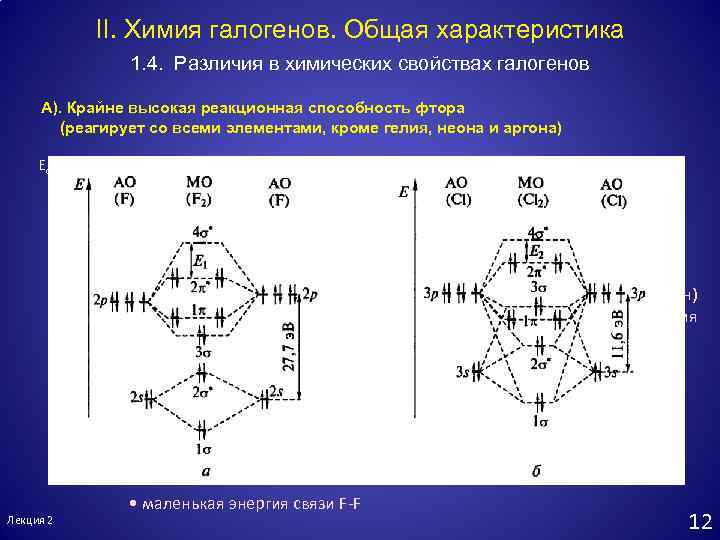 II. Химия галогенов. Общая характеристика 1. 4. Различия в химических свойствах галогенов A). Крайне высокая реакционная способность фтора (реагирует со всеми элементами, кроме гелия, неона и аргона) Eсв, к. Дж/моль 300 • очень маленький размер атомов F (сильное отталкивание электронов) Энергия связи Hal-Hal • большая разница в энергии между s- и p- орбиталями фтора (2 s – орбитали фтора не участвуют в образовании связи галоген-галоген) • отсутствие дативного взаимодействия между атомами F. 250 200 150 100 с ростом длины связи её прочность падает F 2 Cl 2 Br 2 I 2 • высокая электроотрицательность F Лекция 2 • маленькая энергия связи F-F 12
II. Химия галогенов. Общая характеристика 1. 4. Различия в химических свойствах галогенов A). Крайне высокая реакционная способность фтора (реагирует со всеми элементами, кроме гелия, неона и аргона) Eсв, к. Дж/моль 300 • очень маленький размер атомов F (сильное отталкивание электронов) Энергия связи Hal-Hal • большая разница в энергии между s- и p- орбиталями фтора (2 s – орбитали фтора не участвуют в образовании связи галоген-галоген) • отсутствие дативного взаимодействия между атомами F. 250 200 150 100 с ростом длины связи её прочность падает F 2 Cl 2 Br 2 I 2 • высокая электроотрицательность F Лекция 2 • маленькая энергия связи F-F 12
 II. Химия галогенов. Общая характеристика 1. 4. Различия в химических свойствах галогенов Б). Взаимодействие с водой 2 F 2 + H 2 O(ж) = фторид + 2 HF (от 0 до 90 о. С) OF 2 кислорода 2 F 2 + 2 H 2 O(г) = O 2 + 4 HF (выше 90 о. С) окисление воды F 2 + H 2 O(к) = HOF + HF (ниже 0 о. С) фторооксигенат (0) водорода Cl 2 + H 2 O(ж) HCl. O + HCl (на холоду) хлорноватистая кислота 3 Cl 2 + 3 H 2 O(ж) = HCl. O 3 + 5 HCl (при нагревани) дисмутация галогена хлорноватая кислота Бром – аналогично хлору. Иод с водой практически не взаимодействует. Лекция 2 Раствор хлора в воде – хлорная вода. Cl 2(aq) 13
II. Химия галогенов. Общая характеристика 1. 4. Различия в химических свойствах галогенов Б). Взаимодействие с водой 2 F 2 + H 2 O(ж) = фторид + 2 HF (от 0 до 90 о. С) OF 2 кислорода 2 F 2 + 2 H 2 O(г) = O 2 + 4 HF (выше 90 о. С) окисление воды F 2 + H 2 O(к) = HOF + HF (ниже 0 о. С) фторооксигенат (0) водорода Cl 2 + H 2 O(ж) HCl. O + HCl (на холоду) хлорноватистая кислота 3 Cl 2 + 3 H 2 O(ж) = HCl. O 3 + 5 HCl (при нагревани) дисмутация галогена хлорноватая кислота Бром – аналогично хлору. Иод с водой практически не взаимодействует. Лекция 2 Раствор хлора в воде – хлорная вода. Cl 2(aq) 13
 II. Химия галогенов. Общая характеристика 1. 4. Различия в химических свойствах галогенов В). Вытеснение более электроположительного галогена более электроотрицательным из галогенидов Cl 2 + 2 Na. Br = Br 2 + 2 Na. Cl Br 2 + Na. I = I 2 + 2 Na. Br восстановительные свойства Галоген, стоящий в группе выше, вытесняет нижестоящий. Г). Фтор разъедает стекло F 2 + Si. O 2 = Si. F 4 + O 2 Изделия для работы со фтором изготовляют из никеля и его сплавов, меди, нержавеющей стали. Лекция 2 14
II. Химия галогенов. Общая характеристика 1. 4. Различия в химических свойствах галогенов В). Вытеснение более электроположительного галогена более электроотрицательным из галогенидов Cl 2 + 2 Na. Br = Br 2 + 2 Na. Cl Br 2 + Na. I = I 2 + 2 Na. Br восстановительные свойства Галоген, стоящий в группе выше, вытесняет нижестоящий. Г). Фтор разъедает стекло F 2 + Si. O 2 = Si. F 4 + O 2 Изделия для работы со фтором изготовляют из никеля и его сплавов, меди, нержавеющей стали. Лекция 2 14
 II. Химия галогенов. Общая характеристика 1. 5. Химические свойства простых веществ А). С компонентами воздуха не взаимодействуют (кроме фтора) Б). Реагируют с водой и растворами щелочей Cl 2 + H 2 O(ж) HCl. O + HCl (на холоду) 3 Cl 2 + 3 H 2 O(ж) = HCl. O 3 + 5 HCl (при нагревани) Бром – аналогично хлору. Иод с водой практически не взаимодействует. Но растворяется в иодиде калия: I 2 (т) + KI = K[I(I 2)] Cl 2 + Na. OH = Na. Cl. O + Na. Cl + H 2 O (на холоду) гипохлорит натрия 3 Cl 2 + 6 KOH = KCl. O 3 + 5 KCl + 3 H 2 O (при нагревани) хлорат калия Бром – аналогично хлору. 3 I 2 + 6 Na. OH = Na. IO 3 + 5 Na. I + 3 H 2 O (при любой температуре) Лекция 2 иодат натрия 15
II. Химия галогенов. Общая характеристика 1. 5. Химические свойства простых веществ А). С компонентами воздуха не взаимодействуют (кроме фтора) Б). Реагируют с водой и растворами щелочей Cl 2 + H 2 O(ж) HCl. O + HCl (на холоду) 3 Cl 2 + 3 H 2 O(ж) = HCl. O 3 + 5 HCl (при нагревани) Бром – аналогично хлору. Иод с водой практически не взаимодействует. Но растворяется в иодиде калия: I 2 (т) + KI = K[I(I 2)] Cl 2 + Na. OH = Na. Cl. O + Na. Cl + H 2 O (на холоду) гипохлорит натрия 3 Cl 2 + 6 KOH = KCl. O 3 + 5 KCl + 3 H 2 O (при нагревани) хлорат калия Бром – аналогично хлору. 3 I 2 + 6 Na. OH = Na. IO 3 + 5 Na. I + 3 H 2 O (при любой температуре) Лекция 2 иодат натрия 15
 II. Химия галогенов. Общая характеристика 1. 5. Химические свойства простых веществ В). С кислотами-неокислителями не взаимодействуют Г). Энергично реагируют с металлами Cl 2 + Cu = Cu. Cl 2 Br 2 + Al = Al. Br 3 (с воспламенением) и неметаллами 5 Cl 2 + 2 P = 2 PCl 5 5 Cl 2 + 2 Sb = 2 Sb. Cl 5 (с воспламенением) 3 Cl 2 + I 2 = 2 ICl 3 Д). Галогены крайне токсичны! Обращение с галогенами требует неукоснительного соблюдения правил техники безопасности! Лекция 2 16
II. Химия галогенов. Общая характеристика 1. 5. Химические свойства простых веществ В). С кислотами-неокислителями не взаимодействуют Г). Энергично реагируют с металлами Cl 2 + Cu = Cu. Cl 2 Br 2 + Al = Al. Br 3 (с воспламенением) и неметаллами 5 Cl 2 + 2 P = 2 PCl 5 5 Cl 2 + 2 Sb = 2 Sb. Cl 5 (с воспламенением) 3 Cl 2 + I 2 = 2 ICl 3 Д). Галогены крайне токсичны! Обращение с галогенами требует неукоснительного соблюдения правил техники безопасности! Лекция 2 16
 II. Химия галогенов. Общая характеристика 1. 6. Нахождение в природе ФТОР: 0. 065% Основные минералы: флюорит (Ca. F 2), фторапатит (Ca 5(PO 4)3), криолит (Na 3 Al. F 6). Незаменимый элемент для животных (входит в состав костной ткани). ХЛОР: 0. 045% Основные минералы: галит (Na. Cl), сильвин (КCl), сильвинит (Na. Cl ·KCl) карналлит (KCl·Mg. Cl 2· 6 H 2 O), каинит (КСд·Mg. SO 4· 3 H 2 O), бишофит (Mg. Cl 2· 6 H 2 O) и др. В виде хлоридов – основной компонент морской воды. Незаменимый элемент для жизнедеятельности живых организмов. БРОМ: 1. 6· 10 -4 %, редкий элемент, в рассеянном виде. Собственных минералов не образует. Присутствует в природных и буровых водах; концентрируется в некоторых водорослях. ИОД: 3· 10 -5 %, редкий элемент, в рассеянном виде. Собственных минералов не образует. Встречается в буровых водах; концентрируется некоторыми организмами (например, водорослями). Незаменимый микроэлемент для жизнедеятельности человека. Лекция 2 17
II. Химия галогенов. Общая характеристика 1. 6. Нахождение в природе ФТОР: 0. 065% Основные минералы: флюорит (Ca. F 2), фторапатит (Ca 5(PO 4)3), криолит (Na 3 Al. F 6). Незаменимый элемент для животных (входит в состав костной ткани). ХЛОР: 0. 045% Основные минералы: галит (Na. Cl), сильвин (КCl), сильвинит (Na. Cl ·KCl) карналлит (KCl·Mg. Cl 2· 6 H 2 O), каинит (КСд·Mg. SO 4· 3 H 2 O), бишофит (Mg. Cl 2· 6 H 2 O) и др. В виде хлоридов – основной компонент морской воды. Незаменимый элемент для жизнедеятельности живых организмов. БРОМ: 1. 6· 10 -4 %, редкий элемент, в рассеянном виде. Собственных минералов не образует. Присутствует в природных и буровых водах; концентрируется в некоторых водорослях. ИОД: 3· 10 -5 %, редкий элемент, в рассеянном виде. Собственных минералов не образует. Встречается в буровых водах; концентрируется некоторыми организмами (например, водорослями). Незаменимый микроэлемент для жизнедеятельности человека. Лекция 2 17
 II. Химия галогенов. Общая характеристика 1. 6. Получение F 2: впервые получен А. Муассаном в 1886 г. электролизом HF. Современные методы получения: 1. Промышленный метод - электролиз расплава KHF 2 или KH 2 F 3: анод (никелевая сетка): катод (угольный): 2. 2 HF + 2ē = H 2↑ + 2 F 2 F- - 2ē = F 2↑ Лабораторные методы: t 2 Co. F 3 = 2 Co. F 2 + F 2↑ t K 3[Ni. F 6] = 2 KF + Ni. F 2 + F 2↑ K 3[Ni. F 6] + 2 HF(ж) = 2 KHF 2 + Ni. F 2 + F 2↑ t K 3[Mn. F 6] + Ti. F 4 = K 2[Ti. F 6] + Mn. F 2 + F 2 Лекция 2 18
II. Химия галогенов. Общая характеристика 1. 6. Получение F 2: впервые получен А. Муассаном в 1886 г. электролизом HF. Современные методы получения: 1. Промышленный метод - электролиз расплава KHF 2 или KH 2 F 3: анод (никелевая сетка): катод (угольный): 2. 2 HF + 2ē = H 2↑ + 2 F 2 F- - 2ē = F 2↑ Лабораторные методы: t 2 Co. F 3 = 2 Co. F 2 + F 2↑ t K 3[Ni. F 6] = 2 KF + Ni. F 2 + F 2↑ K 3[Ni. F 6] + 2 HF(ж) = 2 KHF 2 + Ni. F 2 + F 2↑ t K 3[Mn. F 6] + Ti. F 4 = K 2[Ti. F 6] + Mn. F 2 + F 2 Лекция 2 18
 II. Химия галогенов. Общая характеристика 1. 6. Получение Cl 2: впервые получен Карлом Шееле в 1774 г. при взаимодействии Mn. O 2 с HCl. Современные методы получения: 1. Промышленный метод - электролиз раствора Na. Cl: анод (графит): катод (сталь или ртуть): 2. 2 H 2 O + 2ē = H 2↑ + 2 OH 2 Cl- -2ē = Cl 2↑ Лабораторные методы: 2 KMn. O 4(т)+ 16 HCl(конц) = 5 Cl 2↑ + 2 Mn. Cl 2 + 2 KCl + 8 H 2 O t Mn. O 2(т) + 4 HCl(конц) = Cl 2↑ + Mn. Cl 2 + 2 H 2 O t Pb. O 2(т) + 4 HCl = Cl 2↑ + Pb. Cl 2 + 2 H 2 O 2 KCl. O 3(т) + 12 HCl = 5 Cl 2↑ + 2 KCl + 6 H 2 O Лекция 2 19
II. Химия галогенов. Общая характеристика 1. 6. Получение Cl 2: впервые получен Карлом Шееле в 1774 г. при взаимодействии Mn. O 2 с HCl. Современные методы получения: 1. Промышленный метод - электролиз раствора Na. Cl: анод (графит): катод (сталь или ртуть): 2. 2 H 2 O + 2ē = H 2↑ + 2 OH 2 Cl- -2ē = Cl 2↑ Лабораторные методы: 2 KMn. O 4(т)+ 16 HCl(конц) = 5 Cl 2↑ + 2 Mn. Cl 2 + 2 KCl + 8 H 2 O t Mn. O 2(т) + 4 HCl(конц) = Cl 2↑ + Mn. Cl 2 + 2 H 2 O t Pb. O 2(т) + 4 HCl = Cl 2↑ + Pb. Cl 2 + 2 H 2 O 2 KCl. O 3(т) + 12 HCl = 5 Cl 2↑ + 2 KCl + 6 H 2 O Лекция 2 19
 II. Химия галогенов. Общая характеристика 1. 6. Получение Br 2: открыт Антуаном Баларом в 1826 г. в рассолах средиземноморских соляных промыслов. Современные методы получения: 1. Промышленный метод - обработка природных и буровых вод хлором: Cl 2 + Br- = Br 2↑ + 2 Cl- 2. Лабораторный метод: Mn. O 2(т) + 2 Na. Br(т) + 3 H 2 SO 4(конц) = Br 2↑ + Mn. SO 4 + 2 Na. HSO 4 + 2 H 2 O I 2: впервые получен Бернаром Куртуа в 1811 г. из золы морских водорослей. Современные методы получения: 1. Промышленный метод: 2 I- + 2 Na. NO 2 + 4 H 3 O+ = I 2↓ + 2 Na+ + 2 NO↑ + 6 H 2 O 2. Лабораторные методы: 2 Na. I + 2 H 2 SO 4(р) + 2 Na. NO 2 = I 2↓ + 2 Na 2 SO 4 + 2 NO↑ + 4 H 2 O 5 KI + KIO 3 + 3 H 2 SO 4(р) = 3 I 2↓ + 3 K 2 SO 4 + 3 H 2 O Лекция 2 20
II. Химия галогенов. Общая характеристика 1. 6. Получение Br 2: открыт Антуаном Баларом в 1826 г. в рассолах средиземноморских соляных промыслов. Современные методы получения: 1. Промышленный метод - обработка природных и буровых вод хлором: Cl 2 + Br- = Br 2↑ + 2 Cl- 2. Лабораторный метод: Mn. O 2(т) + 2 Na. Br(т) + 3 H 2 SO 4(конц) = Br 2↑ + Mn. SO 4 + 2 Na. HSO 4 + 2 H 2 O I 2: впервые получен Бернаром Куртуа в 1811 г. из золы морских водорослей. Современные методы получения: 1. Промышленный метод: 2 I- + 2 Na. NO 2 + 4 H 3 O+ = I 2↓ + 2 Na+ + 2 NO↑ + 6 H 2 O 2. Лабораторные методы: 2 Na. I + 2 H 2 SO 4(р) + 2 Na. NO 2 = I 2↓ + 2 Na 2 SO 4 + 2 NO↑ + 4 H 2 O 5 KI + KIO 3 + 3 H 2 SO 4(р) = 3 I 2↓ + 3 K 2 SO 4 + 3 H 2 O Лекция 2 20
 II. Химия галогенов. Общая характеристика 1. 6. Получение At 2: существование элемента предсказано Д. И. Менделеевым ( «экаиод» ). Впервые получен в 1940 Д. Корсоном, К. Маккензи и Э. Сегре (США). Астат является наиболее редким элементом среди всех, обнаруженных в природе. В поверхностном слое земной коры толщиной 1. 6 км содержится всего 70 мг астата. Современные методы получения: 1. Лекция 2 Облучение висмута или тория высокоэнергетическими α-частицами. 21
II. Химия галогенов. Общая характеристика 1. 6. Получение At 2: существование элемента предсказано Д. И. Менделеевым ( «экаиод» ). Впервые получен в 1940 Д. Корсоном, К. Маккензи и Э. Сегре (США). Астат является наиболее редким элементом среди всех, обнаруженных в природе. В поверхностном слое земной коры толщиной 1. 6 км содержится всего 70 мг астата. Современные методы получения: 1. Лекция 2 Облучение висмута или тория высокоэнергетическими α-частицами. 21
 II. Химия галогенов. Общая характеристика 1. 7. Применение F: Cl: ● необходимый для жизнедеятельности элемент ● органический синтез (полимеры, пестициды, фреоны и т. д. ) ● цветная металлургия (извлечение, разделение и очистка металлов) ● дезинфицирующие и отбеливающие средства (Na. Cl. O, Ca(Cl. O)2) ● производство спичек (KCl. O 3) ● производство пестицидов, гербицидов, дефолиантов ● пиротехника (KCl. O 4, KCl. O 3, Na. Cl. O 3) ● пищевая промышленность, медицина (Na. Cl) ● СДЯВ (БОВ) (например, фосген: COCl 2) Br: ● медицина ( «бром » – KBr) ● производство фотоматериалов (Ag. Br) I: Лекция 2 ● необходимый для жизнедеятельности животных элемент ● ядерная энергетика (UF 6) ● электротехника (SF 6) ● производство фторопластов, хладагентов (фреонов) ● ракетное топливо (фториды галогенов и кислорода) ● необходимый для жизнедеятельности элемент ● медицина ● цветная металлургия (рафинирование металлов) ● галогенные лампы 22
II. Химия галогенов. Общая характеристика 1. 7. Применение F: Cl: ● необходимый для жизнедеятельности элемент ● органический синтез (полимеры, пестициды, фреоны и т. д. ) ● цветная металлургия (извлечение, разделение и очистка металлов) ● дезинфицирующие и отбеливающие средства (Na. Cl. O, Ca(Cl. O)2) ● производство спичек (KCl. O 3) ● производство пестицидов, гербицидов, дефолиантов ● пиротехника (KCl. O 4, KCl. O 3, Na. Cl. O 3) ● пищевая промышленность, медицина (Na. Cl) ● СДЯВ (БОВ) (например, фосген: COCl 2) Br: ● медицина ( «бром » – KBr) ● производство фотоматериалов (Ag. Br) I: Лекция 2 ● необходимый для жизнедеятельности животных элемент ● ядерная энергетика (UF 6) ● электротехника (SF 6) ● производство фторопластов, хладагентов (фреонов) ● ракетное топливо (фториды галогенов и кислорода) ● необходимый для жизнедеятельности элемент ● медицина ● цветная металлургия (рафинирование металлов) ● галогенные лампы 22
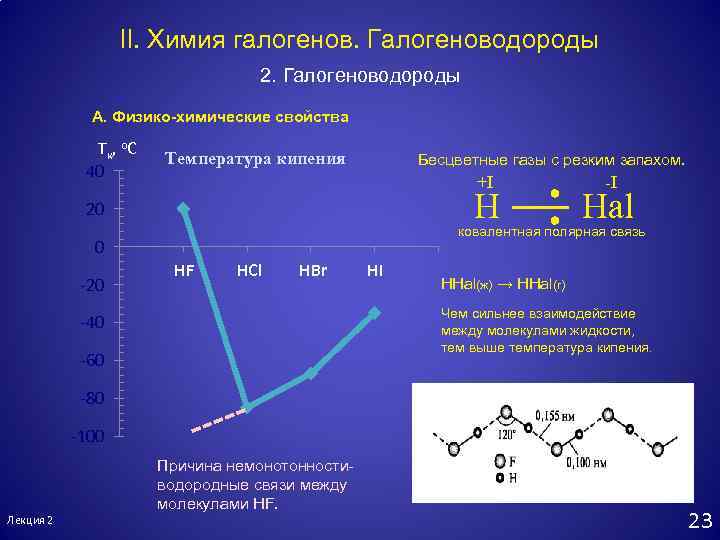 II. Химия галогенов. Галогеноводороды 2. Галогеноводороды А. Физико-химические свойства Tк, o. C 40 Температура кипения Бесцветные газы с резким запахом. +I H 20 HF HCl HBr HI HHal(ж) → HHal(г) Чем сильнее взаимодействие между молекулами жидкости, тем выше температура кипения. -40 -60 -80 -100 Причина немонотонностиводородные связи между молекулами HF. Лекция 2 Hal ковалентная полярная связь 0 -20 -I Дальнейший монотонный рострезультат увеличения массы и размера молекул HHal и, как следствие, усиление взаимодействия между ними. 23
II. Химия галогенов. Галогеноводороды 2. Галогеноводороды А. Физико-химические свойства Tк, o. C 40 Температура кипения Бесцветные газы с резким запахом. +I H 20 HF HCl HBr HI HHal(ж) → HHal(г) Чем сильнее взаимодействие между молекулами жидкости, тем выше температура кипения. -40 -60 -80 -100 Причина немонотонностиводородные связи между молекулами HF. Лекция 2 Hal ковалентная полярная связь 0 -20 -I Дальнейший монотонный рострезультат увеличения массы и размера молекул HHal и, как следствие, усиление взаимодействия между ними. 23
 II. Химия галогенов. Галогеноводороды Б. Получение HF В промышленности: 1. Ca. F 2 + H 2 SO 4(конц) = Ca. SO 4↓ + 2 HF↑ (150 -300 o. C) В лаборатории: 1. 2. HCl t Ca. F 2 + H 2 SO 4 = Ca. SO 4↓ + 2 HF↑ t KHF 2 = KF + HF↑ В промышленности: 1. Cl 2 + H 2 = 2 HCl↑ (сжигание хлора в избытке водорода) 2. Хлорирование углеводородов (побочный продукт) В лаборатории: 1. Na. Cl + H 2 SO 4(конц) = Na. HSO 4 + HCl↑ HBr HI В промышленности и в лаборатории: 2 P + 3 Hal 2 = 2 PHal 3; PHal 3 + 3 H 2 O = 3 HHal↑ + H 2 PHO 3 2. SO 2 + Hal 2 + 2 H 2 O = 2 HHal↑ + H 2 SO 4 3. Лекция 2 1. Ba. S + 4 Hal 2 + 4 H 2 O = 8 HHal↑ + Ba. SO 4↓ 4. H 2 S + Hal 2 = 2 HHal + S↓ (в присутствии воды) 24
II. Химия галогенов. Галогеноводороды Б. Получение HF В промышленности: 1. Ca. F 2 + H 2 SO 4(конц) = Ca. SO 4↓ + 2 HF↑ (150 -300 o. C) В лаборатории: 1. 2. HCl t Ca. F 2 + H 2 SO 4 = Ca. SO 4↓ + 2 HF↑ t KHF 2 = KF + HF↑ В промышленности: 1. Cl 2 + H 2 = 2 HCl↑ (сжигание хлора в избытке водорода) 2. Хлорирование углеводородов (побочный продукт) В лаборатории: 1. Na. Cl + H 2 SO 4(конц) = Na. HSO 4 + HCl↑ HBr HI В промышленности и в лаборатории: 2 P + 3 Hal 2 = 2 PHal 3; PHal 3 + 3 H 2 O = 3 HHal↑ + H 2 PHO 3 2. SO 2 + Hal 2 + 2 H 2 O = 2 HHal↑ + H 2 SO 4 3. Лекция 2 1. Ba. S + 4 Hal 2 + 4 H 2 O = 8 HHal↑ + Ba. SO 4↓ 4. H 2 S + Hal 2 = 2 HHal + S↓ (в присутствии воды) 24
 II. Химия галогенов. Галогеноводороды Б. Получение HBr и HI нельзя получить таким же методом, что и НСl! 2 Na. Br + 3 H 2 SO 4(конц) = Br 2↓ + SO 2↑ + 2 Na. HSO 4 + 2 H 2 O 8 KI + 9 H 2 SO 4(конц) = 4 I 2↓ + H 2 S↑ + 8 KHSO 4 + 4 H 2 O t KHal + H 3 PO 4 = HHal↑ + KH 2 PO 4 (Hal = Cl, Br, I) Лекция 2 25
II. Химия галогенов. Галогеноводороды Б. Получение HBr и HI нельзя получить таким же методом, что и НСl! 2 Na. Br + 3 H 2 SO 4(конц) = Br 2↓ + SO 2↑ + 2 Na. HSO 4 + 2 H 2 O 8 KI + 9 H 2 SO 4(конц) = 4 I 2↓ + H 2 S↑ + 8 KHSO 4 + 4 H 2 O t KHal + H 3 PO 4 = HHal↑ + KH 2 PO 4 (Hal = Cl, Br, I) Лекция 2 25
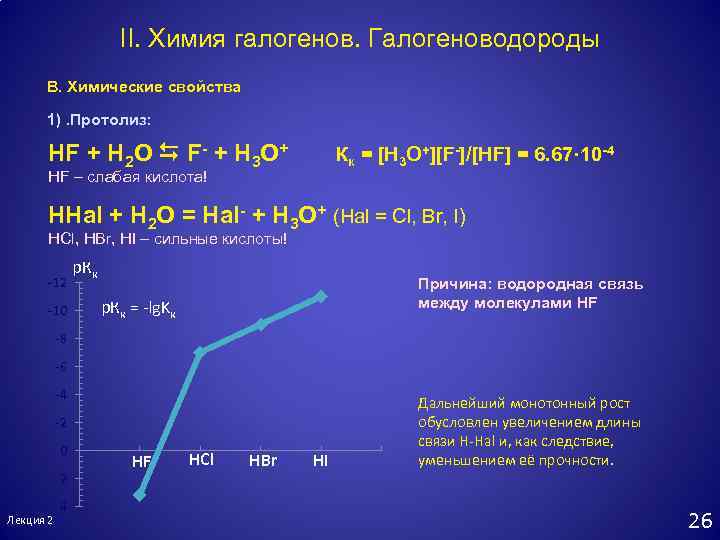 II. Химия галогенов. Галогеноводороды В. Химические свойства 1). Протолиз: HF + H 2 O F- + H 3 O+ Кк = [H 3 O+][F-]/[HF] = 6. 67· 10 -4 HF – слабая кислота! HHal + H 2 O = Hal- + H 3 O+ (Hal = Cl, Br, I) HCl, HBr, HI – сильные кислоты! -12 -10 p. Кк Причина: водородная связь между молекулами HF p. Кк = -lg. Kк -8 -6 -4 -2 0 2 Лекция 2 4 HF HCl HBr HI Дальнейший монотонный рост обусловлен увеличением длины связи H-Hal и, как следствие, уменьшением её прочности. 26
II. Химия галогенов. Галогеноводороды В. Химические свойства 1). Протолиз: HF + H 2 O F- + H 3 O+ Кк = [H 3 O+][F-]/[HF] = 6. 67· 10 -4 HF – слабая кислота! HHal + H 2 O = Hal- + H 3 O+ (Hal = Cl, Br, I) HCl, HBr, HI – сильные кислоты! -12 -10 p. Кк Причина: водородная связь между молекулами HF p. Кк = -lg. Kк -8 -6 -4 -2 0 2 Лекция 2 4 HF HCl HBr HI Дальнейший монотонный рост обусловлен увеличением длины связи H-Hal и, как следствие, уменьшением её прочности. 26
 II. Химия галогенов. Галогеноводороды В. Химические свойства (продолжение) 2). Взаимодействие с металлами: HF + Zn = Zn. F 2 + H 2 6 HCl + 2 Al = 2 Al. Cl 3 + 3 H 2 Галогеноводородные кислоты – неокислители! 4 HI + Hg = H 2[Hg. I 4] + 2 H 2 3). Взаимодействие с основными и амфотерными оксидами и гидроксокомплексами: 3 HF + Al. O(OH) = Al. F 3 + 2 H 2 O 6 HCl + Fe 2 O 3 = 2 Fe. Cl 3 + 3 H 2 O 4 HBr + Na 2[Zn(OH)4] = 2 Na. Br + Zn. Br 2 + 4 H 2 O Лекция 2 27
II. Химия галогенов. Галогеноводороды В. Химические свойства (продолжение) 2). Взаимодействие с металлами: HF + Zn = Zn. F 2 + H 2 6 HCl + 2 Al = 2 Al. Cl 3 + 3 H 2 Галогеноводородные кислоты – неокислители! 4 HI + Hg = H 2[Hg. I 4] + 2 H 2 3). Взаимодействие с основными и амфотерными оксидами и гидроксокомплексами: 3 HF + Al. O(OH) = Al. F 3 + 2 H 2 O 6 HCl + Fe 2 O 3 = 2 Fe. Cl 3 + 3 H 2 O 4 HBr + Na 2[Zn(OH)4] = 2 Na. Br + Zn. Br 2 + 4 H 2 O Лекция 2 27
 II. Химия галогенов. Галогеноводороды В. Химические свойства 4). Восстановительные свойства (кроме HF): t 4 HCl + Mn. O 2(т) = Mn. Cl 2 + 2 H 2 O + Cl 2↑ (аналогично HBr и HI) 6 HBr + H 2 SO 4(конц) = 3 Br 2↑ + S↓ + 4 H 2 O (аналогично HI) 4 HI + O 2 = 2 I 2 + 2 H 2 O (только HI) HF Eo Hal 2/Hal- HCl HBr HI +3. 09 +1. 40 +1. 09 +0. 54 Восстановительные свойства 5). HF разъедает стекло: 4 HF(г) + Si. O 2(т) = Si. F 4↑ + 2 H 2 O 6 HF(р-р) + Si. O 2(т) = H 2[Si. F 6] + 2 H 2 O Лекция 2 гексафторосиликат водорода 28
II. Химия галогенов. Галогеноводороды В. Химические свойства 4). Восстановительные свойства (кроме HF): t 4 HCl + Mn. O 2(т) = Mn. Cl 2 + 2 H 2 O + Cl 2↑ (аналогично HBr и HI) 6 HBr + H 2 SO 4(конц) = 3 Br 2↑ + S↓ + 4 H 2 O (аналогично HI) 4 HI + O 2 = 2 I 2 + 2 H 2 O (только HI) HF Eo Hal 2/Hal- HCl HBr HI +3. 09 +1. 40 +1. 09 +0. 54 Восстановительные свойства 5). HF разъедает стекло: 4 HF(г) + Si. O 2(т) = Si. F 4↑ + 2 H 2 O 6 HF(р-р) + Si. O 2(т) = H 2[Si. F 6] + 2 H 2 O Лекция 2 гексафторосиликат водорода 28
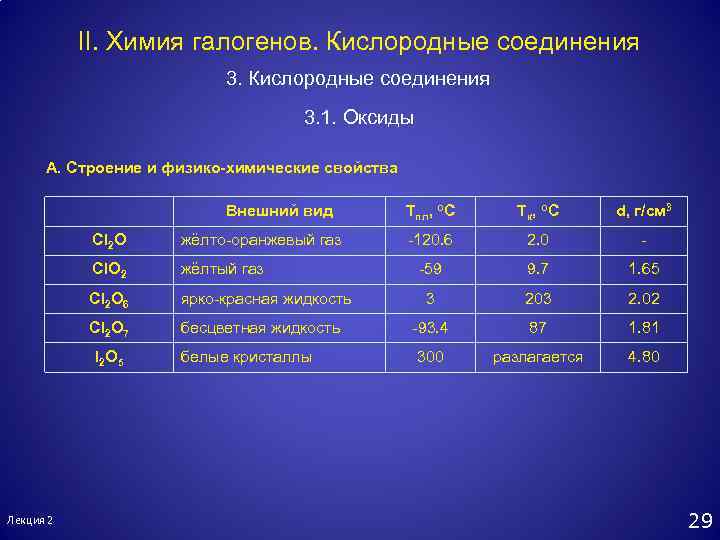 II. Химия галогенов. Кислородные соединения 3. 1. Оксиды А. Строение и физико-химические свойства Внешний вид Cl 2 O жёлто-оранжевый газ Cl. O 2 жёлтый газ Cl 2 O 6 ярко-красная жидкость Cl 2 O 7 бесцветная жидкость I 2 O 5 Лекция 2 белые кристаллы Тпл, о. С Тк, о. С d, г/см 3 -120. 6 2. 0 - -59 9. 7 1. 65 3 203 2. 02 -93. 4 87 1. 81 300 разлагается 4. 80 29
II. Химия галогенов. Кислородные соединения 3. 1. Оксиды А. Строение и физико-химические свойства Внешний вид Cl 2 O жёлто-оранжевый газ Cl. O 2 жёлтый газ Cl 2 O 6 ярко-красная жидкость Cl 2 O 7 бесцветная жидкость I 2 O 5 Лекция 2 белые кристаллы Тпл, о. С Тк, о. С d, г/см 3 -120. 6 2. 0 - -59 9. 7 1. 65 3 203 2. 02 -93. 4 87 1. 81 300 разлагается 4. 80 29
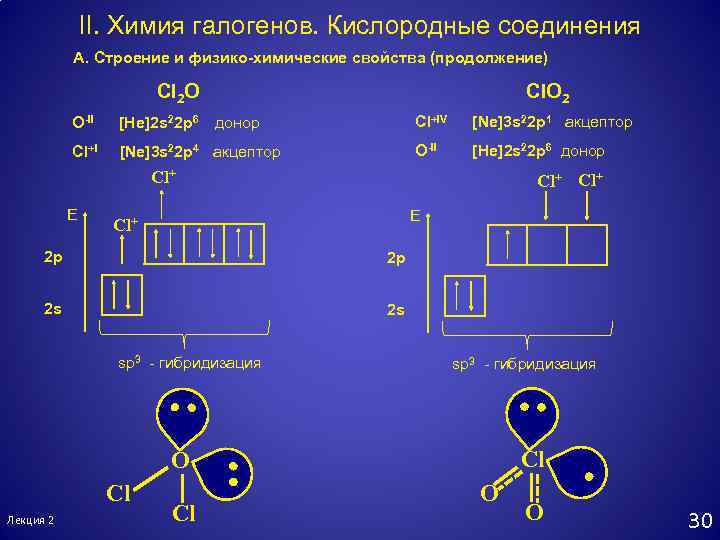 II. Химия галогенов. Кислородные соединения А. Строение и физико-химические свойства (продолжение) Cl 2 O Cl. O 2 O-II [He]2 s 22 p 6 донор Cl+IV [Ne]3 s 22 p 1 акцептор Cl+I [Ne]3 s 22 p 4 акцептор O-II [He]2 s 22 p 6 донор Cl+ E Cl+ 2 p 2 p 2 s 2 s sp 3 - гибридизация Cl O Cl Лекция 2 Cl O O 30
II. Химия галогенов. Кислородные соединения А. Строение и физико-химические свойства (продолжение) Cl 2 O Cl. O 2 O-II [He]2 s 22 p 6 донор Cl+IV [Ne]3 s 22 p 1 акцептор Cl+I [Ne]3 s 22 p 4 акцептор O-II [He]2 s 22 p 6 донор Cl+ E Cl+ 2 p 2 p 2 s 2 s sp 3 - гибридизация Cl O Cl Лекция 2 Cl O O 30
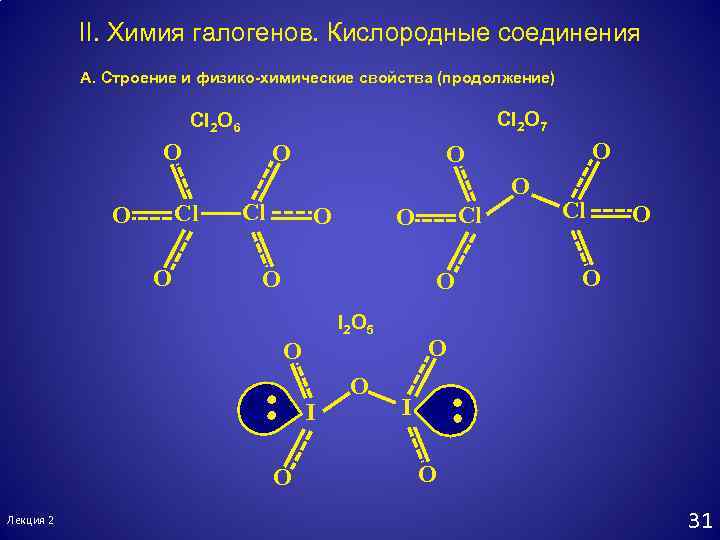 II. Химия галогенов. Кислородные соединения А. Строение и физико-химические свойства (продолжение) Cl 2 O 7 Cl O O I 2 O 5 O I O Cl O O Лекция 2 Cl O O O Cl 2 O 6 31
II. Химия галогенов. Кислородные соединения А. Строение и физико-химические свойства (продолжение) Cl 2 O 7 Cl O O I 2 O 5 O I O Cl O O Лекция 2 Cl O O O Cl 2 O 6 31
 II. Химия галогенов. Оксиды Б. Получение 2 Cl 2(г) + Hg. O(т) = Cl 2 O↑ + Hg. Cl 2 (на холоду) Na. Cl. O 2 + Cl 2 = 2 Na. Cl + Cl. O 2↑ Na. Cl. O 3 + SO 2 + H 2 SO 4 = 2 Na. HSO 4 + Cl. O 2↑ 2 KCl. O 3 + H 2 C 2 O 4 + H 2 SO 4 = K 2 SO 4 + 2 H 2 O + 2 CO 2 + 2 Cl. O 2 2 KCl. O 3 + F 2 = 2 KF + Cl 2 O 6 2 Cl. O 2 + 2 O 3 = Cl 2 O 6 + 2 O 2 4 HCl. O 4 + P 4 O 10 = 4 HPO 3 + 2 Cl 2 O 7 t 2 HIO 3(т) = I 2 O 5 + H 2 O Лекция 2 32
II. Химия галогенов. Оксиды Б. Получение 2 Cl 2(г) + Hg. O(т) = Cl 2 O↑ + Hg. Cl 2 (на холоду) Na. Cl. O 2 + Cl 2 = 2 Na. Cl + Cl. O 2↑ Na. Cl. O 3 + SO 2 + H 2 SO 4 = 2 Na. HSO 4 + Cl. O 2↑ 2 KCl. O 3 + H 2 C 2 O 4 + H 2 SO 4 = K 2 SO 4 + 2 H 2 O + 2 CO 2 + 2 Cl. O 2 2 KCl. O 3 + F 2 = 2 KF + Cl 2 O 6 2 Cl. O 2 + 2 O 3 = Cl 2 O 6 + 2 O 2 4 HCl. O 4 + P 4 O 10 = 4 HPO 3 + 2 Cl 2 O 7 t 2 HIO 3(т) = I 2 O 5 + H 2 O Лекция 2 32
 II. Химия галогенов. Оксиды. В. Химические свойства 1). Оксиды термически неустойчивы: 2 Cl 2 O = Cl 2 + O 2 2 Cl. O 2 = Cl 2 + O 2 Cl 2 O 6 = Cl 2 + 3 O 2 2 Cl 2 O 7 = 2 Cl. O 2 +3 O 2 обычно со взрывом! 2). Взаимодействие с водой и растворами щелочей: Cl 2 O + H 2 O 2 HCl. O 2 +H 2 O = HCl. O 2 + HCl. O 3 Cl 2 O 6 +H 2 O = HCl. O 3 + HCl. O 4 Cl 2 O 7 + H 2 O = 2 HCl. O 4 I 2 O 5 + H 2 O = 2 HIO 3 оксиды с чётными степенями окисления галогенов диспропорционируют В реакциях со щелочами образуются соли соответствующих кислот. 3). Все оксиды галогенов – сильные окислители. Лекция 2 I 2 O 5 + 5 СO = 5 СO 2 + I 2 33
II. Химия галогенов. Оксиды. В. Химические свойства 1). Оксиды термически неустойчивы: 2 Cl 2 O = Cl 2 + O 2 2 Cl. O 2 = Cl 2 + O 2 Cl 2 O 6 = Cl 2 + 3 O 2 2 Cl 2 O 7 = 2 Cl. O 2 +3 O 2 обычно со взрывом! 2). Взаимодействие с водой и растворами щелочей: Cl 2 O + H 2 O 2 HCl. O 2 +H 2 O = HCl. O 2 + HCl. O 3 Cl 2 O 6 +H 2 O = HCl. O 3 + HCl. O 4 Cl 2 O 7 + H 2 O = 2 HCl. O 4 I 2 O 5 + H 2 O = 2 HIO 3 оксиды с чётными степенями окисления галогенов диспропорционируют В реакциях со щелочами образуются соли соответствующих кислот. 3). Все оксиды галогенов – сильные окислители. Лекция 2 I 2 O 5 + 5 СO = 5 СO 2 + I 2 33
 II. Химия галогенов. Кислородные соединения. 3. 2. Кислородные кислоты галогенов А. Номенклатура HCl. O хлорноватистая HCl. O 2 хлористая HCl. O 3 хлорноватая КCl. O гипохлорит калия КCl. O 2 хлорит калия КCl. O 3 КCl. O 4 хлорат перхлорат калия HBr. O бромноватистая - КBr. O гипобромит калия КBr. O 2 бромит калия - Лекция 2 - HBr. O 3 бромноватая HCl. O 4 хлорная HBr. O 4 бромная КBr. O 3 КBr. O 4 бромат пербромат калия HIO 3 иодноватая HIO 4 H 5 IO 6 иодная ортоиодная КIO 3 КIO 4 K 5 IO 6 иодат периодат ортопериодат калия 34
II. Химия галогенов. Кислородные соединения. 3. 2. Кислородные кислоты галогенов А. Номенклатура HCl. O хлорноватистая HCl. O 2 хлористая HCl. O 3 хлорноватая КCl. O гипохлорит калия КCl. O 2 хлорит калия КCl. O 3 КCl. O 4 хлорат перхлорат калия HBr. O бромноватистая - КBr. O гипобромит калия КBr. O 2 бромит калия - Лекция 2 - HBr. O 3 бромноватая HCl. O 4 хлорная HBr. O 4 бромная КBr. O 3 КBr. O 4 бромат пербромат калия HIO 3 иодноватая HIO 4 H 5 IO 6 иодная ортоиодная КIO 3 КIO 4 K 5 IO 6 иодат периодат ортопериодат калия 34
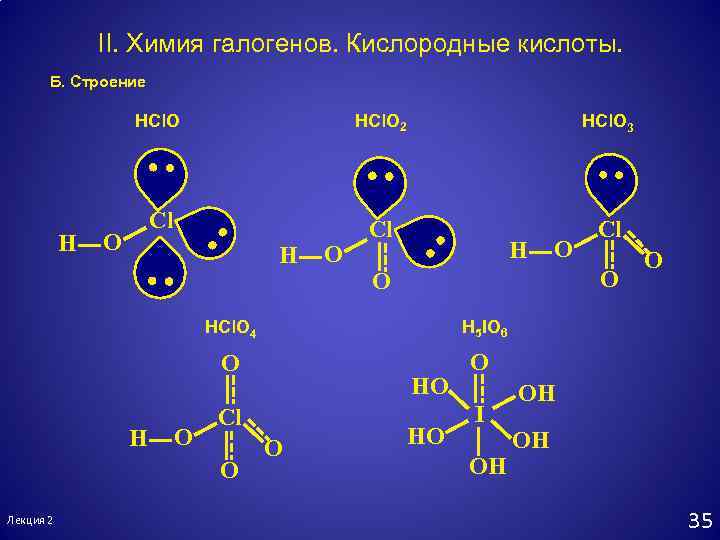 II. Химия галогенов. Кислородные кислоты. Б. Строение HCl. O H HCl. O 2 HCl. O 3 Cl Cl Cl O H O O Лекция 2 HO Cl O O H 5 IO 6 HCl. O 4 H O O HO O I OH OH OH 35
II. Химия галогенов. Кислородные кислоты. Б. Строение HCl. O H HCl. O 2 HCl. O 3 Cl Cl Cl O H O O Лекция 2 HO Cl O O H 5 IO 6 HCl. O 4 H O O HO O I OH OH OH 35
 II. Химия галогенов. Кислородные кислоты. В. Химические свойства 1). Протолитические свойства: HCl. O 2 HCl. O 3 HCl. O 4 сила кислот H+ H+ HCl. O + H 2 O Cl. O- + H 3 O+ Правило Полинга: Если NO – NH ≥ 2 => сильная HCl. O 3: NO – NH = 3 – 1 = 2 => сильная H+ HCl. O 3 + H 2 O = Cl. O- + H 3 O+ 2). Устойчивость, окислительные свойства: HCl. O 2 HCl. O 3 HCl. O 4 устойчивость HCl. O – сильный окислитель! HCl. O 4 в разбавленных растворах окислителем не является! окислительные свойства Лекция 2 HCl. O, HCl. O 2, HCl. O 3 существуют только в разбавленных растворах (<40%) 36
II. Химия галогенов. Кислородные кислоты. В. Химические свойства 1). Протолитические свойства: HCl. O 2 HCl. O 3 HCl. O 4 сила кислот H+ H+ HCl. O + H 2 O Cl. O- + H 3 O+ Правило Полинга: Если NO – NH ≥ 2 => сильная HCl. O 3: NO – NH = 3 – 1 = 2 => сильная H+ HCl. O 3 + H 2 O = Cl. O- + H 3 O+ 2). Устойчивость, окислительные свойства: HCl. O 2 HCl. O 3 HCl. O 4 устойчивость HCl. O – сильный окислитель! HCl. O 4 в разбавленных растворах окислителем не является! окислительные свойства Лекция 2 HCl. O, HCl. O 2, HCl. O 3 существуют только в разбавленных растворах (<40%) 36
 II. Химия галогенов. Кислородные кислоты. В. Химические свойства (продолжение) 2). Устойчивость, окислительные свойства (продолжение): HCl. O, HCl. O 2 – сильные окислители: 2 HCl. O + Na. Cl. O = Na. Cl. O 3 + 2 HCl HCl. O 4 – в растворах не является окислителем: 2 HCl. O 4 + Mg = Mg(Cl. O 4)2 + H 2 Термодинамически: Cl. O 4 - < Br. O 4 - > H 2 IO 63 - Кинетически: Cl. O 4 - и Br. O 4 - реагируют очень медленно! Безводные HCl. O 4 и HBr. O 4– сильнейшие окислители! (реакции протекают со взрывом!) H 5 IO 6 – сильный окислитель: 5 H 5 IO 6 + 2 Mn. SO 4 = 2 HMn. O 4 + 5 HIO 3 + 2 H 2 SO 4 + 7 H 2 O Лекция 2 37
II. Химия галогенов. Кислородные кислоты. В. Химические свойства (продолжение) 2). Устойчивость, окислительные свойства (продолжение): HCl. O, HCl. O 2 – сильные окислители: 2 HCl. O + Na. Cl. O = Na. Cl. O 3 + 2 HCl HCl. O 4 – в растворах не является окислителем: 2 HCl. O 4 + Mg = Mg(Cl. O 4)2 + H 2 Термодинамически: Cl. O 4 - < Br. O 4 - > H 2 IO 63 - Кинетически: Cl. O 4 - и Br. O 4 - реагируют очень медленно! Безводные HCl. O 4 и HBr. O 4– сильнейшие окислители! (реакции протекают со взрывом!) H 5 IO 6 – сильный окислитель: 5 H 5 IO 6 + 2 Mn. SO 4 = 2 HMn. O 4 + 5 HIO 3 + 2 H 2 SO 4 + 7 H 2 O Лекция 2 37
 II. Химия галогенов. Кислородные кислоты. В. Химические свойства 2). Устойчивость, окислительные свойства (продолжение): Соли кислородных кислот – менее сильные окислители, чем сами кислоты (ионное строение, устойчивость выше) Гипогалогениты – сильные окислители: 2 Na. Cl. O + 4 Na. OH + Mn. Cl 2 = Na 2 Mn. O 4 + 4 Na. Cl + 2 H 2 O Hal. O 3 - – окислительные свойства проявляются только в кислотной среде: KCl. O 3 + 6 HCl = 3 Cl 2 + KCl + 3 H 2 O KIO 3 + 5 KI + 3 H 2 SO 4 = 3 I 2 + 3 K 2 SO 4 + 3 H 2 O Перхлораты и перброматы в растворе окислителями не являются. Твёрдые галогенаты и пергалогенаты - сильные окислители! 10 KCl. O 3(т) + 3 P 4(т) = 10 KCl + 3 P 4 O 10 (cо взрывом!) KCl. O 4(т) + K 2 S(т) = K 2 SO 4 + KCl Лекция 2 38
II. Химия галогенов. Кислородные кислоты. В. Химические свойства 2). Устойчивость, окислительные свойства (продолжение): Соли кислородных кислот – менее сильные окислители, чем сами кислоты (ионное строение, устойчивость выше) Гипогалогениты – сильные окислители: 2 Na. Cl. O + 4 Na. OH + Mn. Cl 2 = Na 2 Mn. O 4 + 4 Na. Cl + 2 H 2 O Hal. O 3 - – окислительные свойства проявляются только в кислотной среде: KCl. O 3 + 6 HCl = 3 Cl 2 + KCl + 3 H 2 O KIO 3 + 5 KI + 3 H 2 SO 4 = 3 I 2 + 3 K 2 SO 4 + 3 H 2 O Перхлораты и перброматы в растворе окислителями не являются. Твёрдые галогенаты и пергалогенаты - сильные окислители! 10 KCl. O 3(т) + 3 P 4(т) = 10 KCl + 3 P 4 O 10 (cо взрывом!) KCl. O 4(т) + K 2 S(т) = K 2 SO 4 + KCl Лекция 2 38
 II. Химия галогенов. Кислородные кислоты. В. Химические свойства (продолжение) 2). Термическое разложение кислот и их солей 4 KCl. O 3 2 KCl. O 3 t>400 o. C KCl + 3 KCl. O 4 t>100 o. C, Mn. O 2 2 KCl + 3 O 2 Устойчивость солей выше, чем соответствующих кислот (Cr 2 O 3, Cu. O, Fe 2 O 3 и др. ) KCl. O 4 t>550 o. C H 5 IO 6 t<100 o. C HIO 4 + 2 H 2 O HIO 4 t>120 o. C 2 HIO 3 + O 2 2 HIO 3 300 o. C I 2 O 5 + H 2 O 2 Na. IO 4 Лекция 2 Устойчивость пергалогенатов выше, чем галогенатов 2 Na. IO 3 240 o. C вакуум 600 o. C KCl + 2 O 2 2 Na. IO 3 + O 2 2 Na. I + 3 O 2 39
II. Химия галогенов. Кислородные кислоты. В. Химические свойства (продолжение) 2). Термическое разложение кислот и их солей 4 KCl. O 3 2 KCl. O 3 t>400 o. C KCl + 3 KCl. O 4 t>100 o. C, Mn. O 2 2 KCl + 3 O 2 Устойчивость солей выше, чем соответствующих кислот (Cr 2 O 3, Cu. O, Fe 2 O 3 и др. ) KCl. O 4 t>550 o. C H 5 IO 6 t<100 o. C HIO 4 + 2 H 2 O HIO 4 t>120 o. C 2 HIO 3 + O 2 2 HIO 3 300 o. C I 2 O 5 + H 2 O 2 Na. IO 4 Лекция 2 Устойчивость пергалогенатов выше, чем галогенатов 2 Na. IO 3 240 o. C вакуум 600 o. C KCl + 2 O 2 2 Na. IO 3 + O 2 2 Na. I + 3 O 2 39
 II. Химия галогенов. Кислородные кислоты. Г. Получение Hal 2 + Hg. O + H 2 O = Hg. Hal 2· 2 Hg. O↓ + HHal. O Ca. CO 3 + 2 Cl 2 + H 2 O = 2 HCl. O + Ca. Cl 2 + CO 2 Ca(OH)2 + Cl 2 = Ca. Cl(OCl) + H 2 O хлорная известь 2 Na. OH(р-р) + Cl 2 = Na. Cl + Na. Cl. O + H 2 O (на холоду) жавелевая вода 2 Cl. O 2 + Ba(OH)2 + H 2 O 2 = Ba(Cl. O 2)2 + 2 H 2 O + O 2↑ 2 Cl. O 2 + Pb. O + 2 Na. OH = Pb. O 2↓ + 2 Na. Cl. O 2 + H 2 O Ba(Cl. O 2)2 + H 2 SO 4 = Ba. SO 4↓ + 2 HCl. O 2 Cl- + 3 H 2 O - 5ē = Cl. O 3 - + 6 H+ (электролиз) t - = Cl. O - + 5 Cl- + 3 H O Cl 2 + 6 OH 3 2 Ba(Cl. O 3)2 + H 2 SO 4 = HCl. O 3 + Ba. SO 4 t I 2 + 10 HNO 3(конц) = 2 HIO 3 + 10 NO 2↑ + 4 H 2 O t I 2 + 5 H 2 O 2 = 2 HIO 3 + 4 H 2 O Лекция 2 40
II. Химия галогенов. Кислородные кислоты. Г. Получение Hal 2 + Hg. O + H 2 O = Hg. Hal 2· 2 Hg. O↓ + HHal. O Ca. CO 3 + 2 Cl 2 + H 2 O = 2 HCl. O + Ca. Cl 2 + CO 2 Ca(OH)2 + Cl 2 = Ca. Cl(OCl) + H 2 O хлорная известь 2 Na. OH(р-р) + Cl 2 = Na. Cl + Na. Cl. O + H 2 O (на холоду) жавелевая вода 2 Cl. O 2 + Ba(OH)2 + H 2 O 2 = Ba(Cl. O 2)2 + 2 H 2 O + O 2↑ 2 Cl. O 2 + Pb. O + 2 Na. OH = Pb. O 2↓ + 2 Na. Cl. O 2 + H 2 O Ba(Cl. O 2)2 + H 2 SO 4 = Ba. SO 4↓ + 2 HCl. O 2 Cl- + 3 H 2 O - 5ē = Cl. O 3 - + 6 H+ (электролиз) t - = Cl. O - + 5 Cl- + 3 H O Cl 2 + 6 OH 3 2 Ba(Cl. O 3)2 + H 2 SO 4 = HCl. O 3 + Ba. SO 4 t I 2 + 10 HNO 3(конц) = 2 HIO 3 + 10 NO 2↑ + 4 H 2 O t I 2 + 5 H 2 O 2 = 2 HIO 3 + 4 H 2 O Лекция 2 40
 II. Химия галогенов. Кислородные кислоты. Г. Получение Cl. O 3 - + H 2 O - 2ē = Cl. O 4 - + 2 H+ (электролиз) Na. Br. O 3 + F 2 + 2 Na. OH = Na. Br. O 4 + 2 Na. F + H 2 O t Na. Cl. O 4(конц) + HCl(конц) = HCl. O 4 + Na. Cl↓ t KCl. O 4 + H 2 SO 4 = HCl. O 4 + KHSO 4 Na. IO 3 + 4 Na. OH + Cl 2 = Na 3 H 2 IO 6↓ + 2 Na. Cl + H 2 O 2 Na 3 H 2 IO 6 + Ba(NO 3)2 = Ba 3(H 2 IO 6)2↓ + 6 Na. NO 3 Ba 3(H 2 IO 6)2 + 3 H 2 SO 4 = 2 H 5 IO 6 + 3 Ba. SO 4↓ Лекция 2 41
II. Химия галогенов. Кислородные кислоты. Г. Получение Cl. O 3 - + H 2 O - 2ē = Cl. O 4 - + 2 H+ (электролиз) Na. Br. O 3 + F 2 + 2 Na. OH = Na. Br. O 4 + 2 Na. F + H 2 O t Na. Cl. O 4(конц) + HCl(конц) = HCl. O 4 + Na. Cl↓ t KCl. O 4 + H 2 SO 4 = HCl. O 4 + KHSO 4 Na. IO 3 + 4 Na. OH + Cl 2 = Na 3 H 2 IO 6↓ + 2 Na. Cl + H 2 O 2 Na 3 H 2 IO 6 + Ba(NO 3)2 = Ba 3(H 2 IO 6)2↓ + 6 Na. NO 3 Ba 3(H 2 IO 6)2 + 3 H 2 SO 4 = 2 H 5 IO 6 + 3 Ba. SO 4↓ Лекция 2 41


