W_Mo.ppt
- Количество слайдов: 26

Молибден элемент побочной подгруппы шестой группы пятого периода периодической системы химических элементов Д. И. Менделеева, атомный номер 42. Обозначается символом Mo (лат. Molybdaenum). Простое вещество молибден — переходный металл светло серого цвета.

История открытия 1778 г шведским химиком Карлом Шееле, который, прокаливая молибденовую кислоту, получил Мо. О 3. 1782 г в металлическом состоянии впервые получен П. Гьельмом восстановлением оксида углём: он получил молибден, загрязненный углеродом и карбидом молибдена. В 1817 чистый молибден

Название происходит от др. греч. μόλυβδος, означающего «свинец» . Оно дано из за внешнего сходства молибденита (Mo. S 2), с галенитом (Pb. S). Вплоть до XVIII в. молибденит не отличали от графита и галенита, эти минералы носили общее название «молибден» .

Основные физические характеристики и химические свойства Атомная масса 95, 94 а. е. м. Сидерофильный Электронная конфигурация [Kr] 4 d 5 5 s 1 элемент с переменной Радиус атома 139 пм валентностью Ковалентный радиус 130 пм Радиус иона (+6 e) 62 (+4 e) 70 пм Электроотрицательность 2, 16 (шкала Характерные примеси Полинга) и спутники: Электродный потенциал -0, 2 Re, U, V, Se , Cu и W. Степени окисления 6, 5, 4, 3, 2
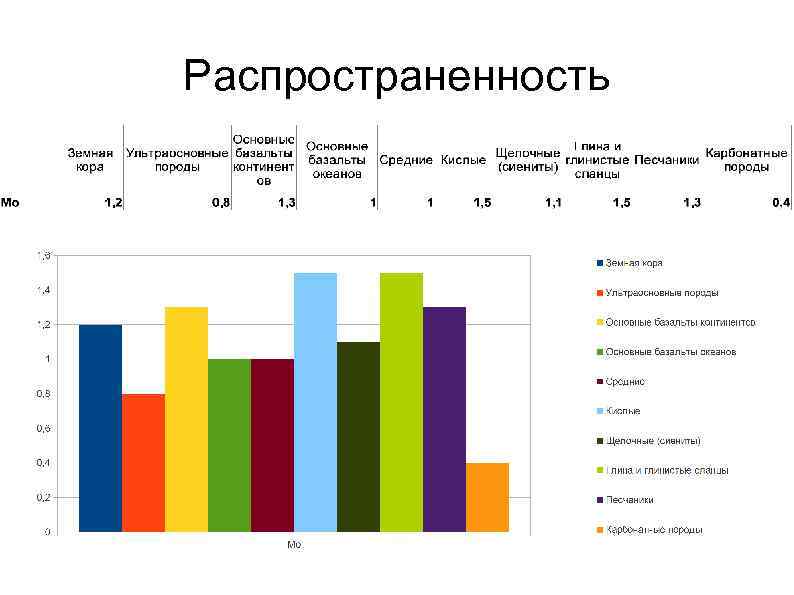
Распространенность

Распространенность в других природных объектах Содержание молибдена в морской воде колеблется от 8, 9 до 12, 2 мкг/л[2] для разных океанов и акваторий. Общим является то, что воды вблизи берега и верхние слои меньше обогащены молибденом, чем воды на глубине и вдали от берега. Молибден в организме растений, животных и человека постоянно присутствует как микроэлемент, участвующий преимущественно в азотном обмене.

Основные минералы носители Известно около 20 минералов молибдена. Наиболее высокие концентрации молибдена в породах связаны с акцессорными минералами (магнетит, ильменит, сфен), однако основная масса его заключена в полевых шпатах и меньше в кварце. Молибден в породах находится в следующих формах: 1. Молибдатной (повеллит Ca [ Mo. O 4 ], вульфенит Pb [ Mo. O 4], ферримолибдит Fe 2[ Mo. O 4]3 8 H O)

2. Сульфидной в виде микроскопических и субмикроскопических выделений, изоморфной и рассеянной (в породообразующих минералах). Молибден обладает большим сродством с серой, чем с кислородом ( молибдит Mo. O 3), и в рудных телах образуется сульфид четырёхвалентного молибдена — молибденит (Mo. S 2)

Поведение в геологических процессах Типы геохимических барьеров Магматический сероводородный барьер Глеевые барьеры Щелочные геохимические барьеры Кислые геохимические барьеры Испарительные геохимические барьеры Накопление химических элементов на щелочном барьере (по Н. С. Касимову): 1 — карбонатизация; 2 — огипсование; 3 — направление движения кислых и слабокислых растворов; 4 — направление движения слабощелочных растворов

Геохимия молибдена в зоне окисления Окисление окисление главного минерала молибденита (Mo. S 2) происходит активно и усиливается при появление Fе 3+. Объясняется это разрушением образующейся на молибдените защитной пленки, которая разрушается также под

Основные типы месторождений 1. Контактово-метасоматические (скарновые) 2. Гидротермальные А. Высокотемпературные (грейзеновые) Б. Среднетемпературные

Вольфрам химический элемент с атомным номером 74 в периодической системе, обозначается символом W (лат. Wolframium), твёрдый серый переходный металл. Вольфрам самый тугоплавкий известный в настоящее время металл. При стандартных условиях химически стоек.

История открытия В 1781 г Шееле получил трехокись вольфрама WO 3 из минерала, который позднее был назван в его честь шеелитом (Ca. WO 4). Открытие Шееле подтвердил Бергман, назвавший минерал "тяжеловесным камнем" (лат. Lapis в 1783 г испанцами братьями де ponderosus); в переводе на шведский язык Эльгуйяр, учениками Бергмана, был получен впервые чистый это тунгстен (Tung Sten тяжелый камень). вольфрам

Название вольфрам существовало, однако, задолго до открытия элемента. Горняки и металлурги XIV XVI вв. , занимавшиеся добычей олова, заметили, что при прокаливании одной из оловянных руд значительное количество олова теряется, уходя в шлак. Эта руда получила название волк (Wolf, или Wolfert), которое с течением времени изменилось на вольфрам; так стали называть минерал, содержащийся в руде

Основные физические характеристики и химические свойства Атомная масса 183, 84 а. е. м. Сидерофильный Электронная конфигурация [Xe] 4 f 14 5 d 4 6 s 2 элемент с Радиус атома 141 пм переменной Химические свойства Ковалентный радиус 170 валентностью пм Радиус иона (+6 e) 62 (+4 e) 70 пм Основные примеси: Sn, Mo, Электроотрицательность 2. 3 (шкала Полинга) Be, Au, Cu, Pb и Zn Электродный потенциал W ← W 3+ 0, 11 В
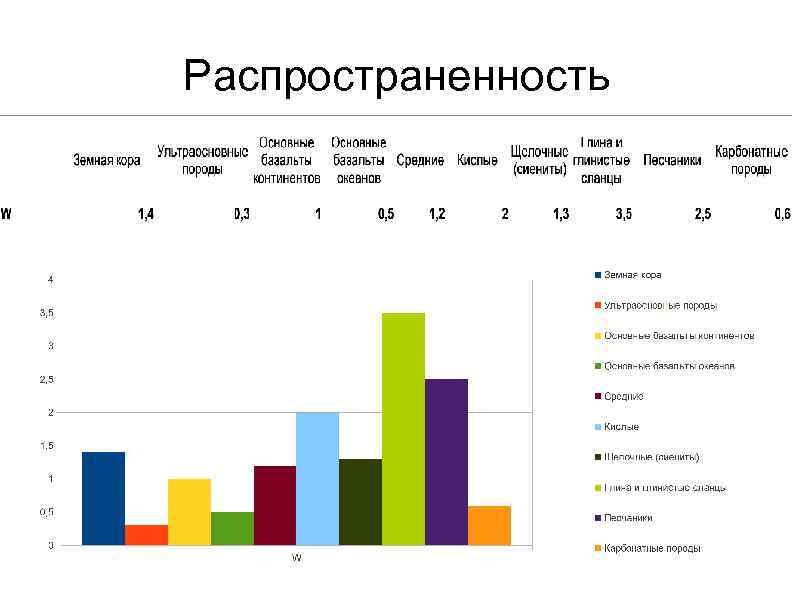
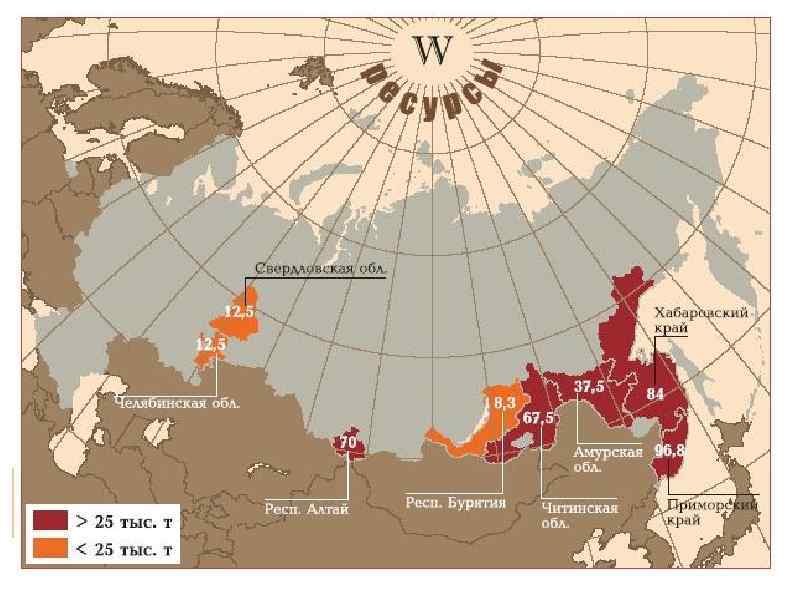
Распространенность

Распространенность в других природных объектах Вольфрам не играет значительной биологической роли. У некоторых архебактерий имеются ферменты, включающие вольфрам в своем активном центре. Существуют облигатно зависимые от вольфрама формы архебактерий гипертермофилов, обитающие вокруг глубоководных гидротермальных источников. Присутствие вольфрама в составе ферментов может рассматриваться как физиологический реликт раннего архея — существуют предположения, что вольфрам играл роль в ранних этапах возникновения жизни.

Основные минералы носители Наиболее распространенными природными соединениями вольфрама являются соли вольфрамовой кислоты. Из них на первом месте по распространенности стоит вольфрамит (Fe, Mn)WO 4, представляющий изоморфную смесь темнокоричневого ферберита Fe. WO 4 и более светлою гюбнерита Mn. WO 4. Окраска вольфрамита зависит от соотношения Fe : Мn
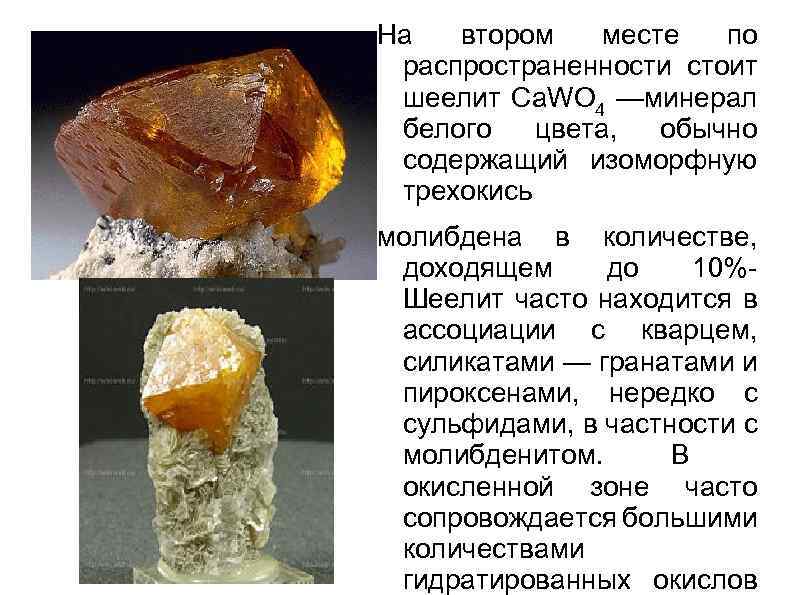
На втором месте по распространенности стоит шеелит Ca. WO 4 —минерал белого цвета, обычно содержащий изоморфную трехокись молибдена в количестве, доходящем до 10% Шеелит часто находится в ассоциации с кварцем, силикатами — гранатами и пироксенами, нередко с сульфидами, в частности с молибденитом. В окисленной зоне часто сопровождается большими количествами гидратированных окислов

Менее распространенным минералом является штольцит Pb. WO 4, связанный со свинцовыми рудами. В зоне окисления вольфраматы частично разлагаются. При разложении вольфрамита железо окисляется до трехвалентного, образуя землистые желто бурые массы. Вольфрам здесь обычно переходит в ферритунгстит — гидратированный окисел вольфрама, содержащий железо, и тунгстит WO 3 • Н 2 О. В виде изоморфной примеси вольфрам входит в молибдаты в небольшом количестве он находится во многих ниобатах и танталатах.

Поведение в геологических процессах Магматические процессы Поведение вольфрама в магматическом процессе обусловлено его переменной валентностью и характером изменения потенциала кристаллизующихся систем. Осадочные процессы Вольфрам накапливается в россыпях в связи со своей высокой плотностью. Гидротермальные процессы По условиям образования месторождения вольфрамовые руды разделяют на эндогенные и экзогенные. Среди эндогенных различают пегматитовые, скарновые, грейзеновые и гидротермальные (прожилково жильные) генетические типы руд.

Основные типы месторождений альбитизированные, грейзенизированные и окварцованные купола и штоки гранитов или гранит порфиров кварц вольфрамитовые прожилки, кварц полевошпатовые, кварц топазовые, кварц флюоритовые и кварцевые жилы кварц шеелитовые жилы; шеелитсодержащие скарны гранат пироксен скаполитового состава с

Основные типы месторождений альбитизированные, грейзенизированные и окварцованные купола и штоки гранитов или гранит порфиров кварц вольфрамитовые прожилки, кварц полевошпатовые, кварц топазовые, кварц флюоритовые и кварцевые жилы кварц шеелитовые жилы; шеелитсодержащие скарны гранат пироксен скаполитового состава с
W_Mo.ppt