10.молек.основы рецепторного взаимодействия.ppt
- Количество слайдов: 28
 Молекулярные основы рецепторного взаимодействия Лекция 10
Молекулярные основы рецепторного взаимодействия Лекция 10
 Рецепторная теория действия лекарств развивается с конца 19 го века, когда Paul Ehrlich выдвинул концепцию о лекарстве как «волшебной пуле» направленной на «поражаемый рецептор» . Многие годы рецепторы характеризовали по эффектам различных эндо- и экзогенных соединений, названия которых определяли номенклатуру рецепторов. Прямая идентификация рецепторов лекарств, гормонов, нейромедиаторов стала возможной в 60 х годах двадцатого века благодаря разработке методов радиолигандного анализа. Несравненно более глубокое понимание структуры и функции рецепторов в последние два десятилетия достигнуто на основе молекулярно-генетических исследований. Большинство рецепторов выделено, определена их аминокислотная последовательность, клонированы сотни кодирующих рецепторы генов.
Рецепторная теория действия лекарств развивается с конца 19 го века, когда Paul Ehrlich выдвинул концепцию о лекарстве как «волшебной пуле» направленной на «поражаемый рецептор» . Многие годы рецепторы характеризовали по эффектам различных эндо- и экзогенных соединений, названия которых определяли номенклатуру рецепторов. Прямая идентификация рецепторов лекарств, гормонов, нейромедиаторов стала возможной в 60 х годах двадцатого века благодаря разработке методов радиолигандного анализа. Несравненно более глубокое понимание структуры и функции рецепторов в последние два десятилетия достигнуто на основе молекулярно-генетических исследований. Большинство рецепторов выделено, определена их аминокислотная последовательность, клонированы сотни кодирующих рецепторы генов.
 В литературе, особенно отечественной, под термином рецепция иногда понимается любое связывание лекарства с биологическим субстратом. Однако, большинство современных исследователей отличает рецепторное связывание от неспецифического, имея ввиду прежде всего, что последнее не ведет к специфическому эффекту. С другой стороны, не все лекарства влияют на рецепторы, имеющие эндогенные лиганды. Фармакологическое действие может опосредоваться ферментами, небелковыми элементами – липидами, изменением содержания ионов и состава воды, другими процессами. Взаимодействие лекарств со специфическими рецепторами обеспечивается различными типами химических связей. Иногда имеет место ковалентное связывание, однако для фармакологических препаратов характерно обратимое связывание за счет комбинации электростатического взаимодействия, водородных связей, Ван дер Ваальсовых сил при высокой комплементарности лиганда к рецептору. Рецептор также должен быть стереоселективен в отношении оптических изомеров лекарств.
В литературе, особенно отечественной, под термином рецепция иногда понимается любое связывание лекарства с биологическим субстратом. Однако, большинство современных исследователей отличает рецепторное связывание от неспецифического, имея ввиду прежде всего, что последнее не ведет к специфическому эффекту. С другой стороны, не все лекарства влияют на рецепторы, имеющие эндогенные лиганды. Фармакологическое действие может опосредоваться ферментами, небелковыми элементами – липидами, изменением содержания ионов и состава воды, другими процессами. Взаимодействие лекарств со специфическими рецепторами обеспечивается различными типами химических связей. Иногда имеет место ковалентное связывание, однако для фармакологических препаратов характерно обратимое связывание за счет комбинации электростатического взаимодействия, водородных связей, Ван дер Ваальсовых сил при высокой комплементарности лиганда к рецептору. Рецептор также должен быть стереоселективен в отношении оптических изомеров лекарств.
 Сигнальные механизмы На сегодняшний день выделяют 4 основных механизма по которым экстраклеточный лиганд регулирует внутриклеточные процессы. Молекулярные основы сигнальных систем трансдукции значительно различаются (рис 1). Первой, наиболее сложной, является рецепторная система, связанная с G белками. Она состоит из трансмембранного рецептора, к которому лиганд присоединяется на поверхности клетки, этот рецептор сопрягается с расположенным на внутренней поверхности мембраны гуанин-нуклеотид связывающим белком ( G белком). G белок в свою очередь регулирует эффекторный фермент, генерирующий внутриклеточный вторичный мессенджер. Второй тип рецепторной системы – рецепторы связанные с тирозинкиназой и гуанилилциклазой. Они состоят из трансмембранных рецепторов, в которых внутриклеточная часть обладает ферментативной активностью, аллостерически регулируемой лигандным связыванием на внешнем, по отношению к мембране, участке рецептора.
Сигнальные механизмы На сегодняшний день выделяют 4 основных механизма по которым экстраклеточный лиганд регулирует внутриклеточные процессы. Молекулярные основы сигнальных систем трансдукции значительно различаются (рис 1). Первой, наиболее сложной, является рецепторная система, связанная с G белками. Она состоит из трансмембранного рецептора, к которому лиганд присоединяется на поверхности клетки, этот рецептор сопрягается с расположенным на внутренней поверхности мембраны гуанин-нуклеотид связывающим белком ( G белком). G белок в свою очередь регулирует эффекторный фермент, генерирующий внутриклеточный вторичный мессенджер. Второй тип рецепторной системы – рецепторы связанные с тирозинкиназой и гуанилилциклазой. Они состоят из трансмембранных рецепторов, в которых внутриклеточная часть обладает ферментативной активностью, аллостерически регулируемой лигандным связыванием на внешнем, по отношению к мембране, участке рецептора.
 Третий тип - более простая система рецептора, это регулируемый лигандом трансмембранный ионный канал. Его открытое состояние определяется прямым связыванием лиганда с экстраклеточным участком каналообразующих белков. Четвертый тип – характерен для жирорастворимых лигандов. В этом случае проникший через мембрану лиганд связывается с внутриклеточным рецептором, далее этот комплекс присоединяется к специфическому участку ДНК в ядре и регулирует транскрипцию. Для понимания фармакогенетического значения лигандрецепторного взаимодействия, механизмы трансдукции следует рассмотреть более подробно. Системы вторичных мессенджеров связанные с G белками В таблице 1 приведены примеры подобных рецепторных систем. Очевидно, что большое число первичных мессенджеров регулируют лишь несколько вторичных, таким образом следует понимать, что специфичность действия первичносвязывающихся лигандов определяется локализацией рецептора на определенных клетках в которых вторичные мессенджеры вызывают экспрессию белков, специфичных для данной клетки.
Третий тип - более простая система рецептора, это регулируемый лигандом трансмембранный ионный канал. Его открытое состояние определяется прямым связыванием лиганда с экстраклеточным участком каналообразующих белков. Четвертый тип – характерен для жирорастворимых лигандов. В этом случае проникший через мембрану лиганд связывается с внутриклеточным рецептором, далее этот комплекс присоединяется к специфическому участку ДНК в ядре и регулирует транскрипцию. Для понимания фармакогенетического значения лигандрецепторного взаимодействия, механизмы трансдукции следует рассмотреть более подробно. Системы вторичных мессенджеров связанные с G белками В таблице 1 приведены примеры подобных рецепторных систем. Очевидно, что большое число первичных мессенджеров регулируют лишь несколько вторичных, таким образом следует понимать, что специфичность действия первичносвязывающихся лигандов определяется локализацией рецептора на определенных клетках в которых вторичные мессенджеры вызывают экспрессию белков, специфичных для данной клетки.
 Рецепторы, связанные с G белками Открыто более 1000 генов, кодирующих рецепторы, связанные с G белками. Эти рецепторы являются мономерными гликопротеинами с относительно сходным аминокислотным составом, внутри которых характерны 7 доменов имеющих гидрофобные аминокислоты в составе полипептидной цепи. Эти домены образуются петлями внутри мембраны с одним концом выступающим наружу, а другим - внутрь цитоплазмы ( рис. 1 -1). Эндогенные лиганды связываются с внешней частью рецептора. Небольшие по размеру, например амины присоединяются к участкам внутри различных трансмембранных областей, тогда как крупные, например, полипептиды, менее способные проникать в гидрофобные регионы, связываются на экстраклеточной петле Nконцевого участка рецептора.
Рецепторы, связанные с G белками Открыто более 1000 генов, кодирующих рецепторы, связанные с G белками. Эти рецепторы являются мономерными гликопротеинами с относительно сходным аминокислотным составом, внутри которых характерны 7 доменов имеющих гидрофобные аминокислоты в составе полипептидной цепи. Эти домены образуются петлями внутри мембраны с одним концом выступающим наружу, а другим - внутрь цитоплазмы ( рис. 1 -1). Эндогенные лиганды связываются с внешней частью рецептора. Небольшие по размеру, например амины присоединяются к участкам внутри различных трансмембранных областей, тогда как крупные, например, полипептиды, менее способные проникать в гидрофобные регионы, связываются на экстраклеточной петле Nконцевого участка рецептора.
 G белки присоединяются к внутриклеточному сегменту рецептора внутри 3 ей петли между 5 ым и 6 ым регионами (рис. 1 -1). Хотя механизм эффекта, возникающего при соединении с агонистом не до конца ясен, предполагается, что этот акт стабилизирует рецептор в конформации, позволяющей его взаимодействие с тримером G белков, активируя их и последующие эффекторные события. Эффект агониста обычно имеет лишь ограниченную продолжительность, что определяется несколькими процессами. Большинство связанных с G белками рецепторов имеют остатки серина и треонина в цитоплазматической петле и в С-концевом участке рецептора, которые могут быть фосфорилированы несколькими киназами, что приводит к снижению взаимодействия между рецептором и G белком. Данный процесс называется десенситезацией рецептора и позволяет клетке ответить на весьма широкие диапазоны концентраций стимулирующих экстраклеточных агентов. После продолжительного воздействия агониста число рецепторов на плазматической мембране может также регулироваться процессом интернационализации (осуществляемым в некоторых случаях катаболизмом), или down регуляцией рецептора. Хотя вызывающие ее сигналы не ясны, представляется, что они отличны от контролирующих десенситезацию.
G белки присоединяются к внутриклеточному сегменту рецептора внутри 3 ей петли между 5 ым и 6 ым регионами (рис. 1 -1). Хотя механизм эффекта, возникающего при соединении с агонистом не до конца ясен, предполагается, что этот акт стабилизирует рецептор в конформации, позволяющей его взаимодействие с тримером G белков, активируя их и последующие эффекторные события. Эффект агониста обычно имеет лишь ограниченную продолжительность, что определяется несколькими процессами. Большинство связанных с G белками рецепторов имеют остатки серина и треонина в цитоплазматической петле и в С-концевом участке рецептора, которые могут быть фосфорилированы несколькими киназами, что приводит к снижению взаимодействия между рецептором и G белком. Данный процесс называется десенситезацией рецептора и позволяет клетке ответить на весьма широкие диапазоны концентраций стимулирующих экстраклеточных агентов. После продолжительного воздействия агониста число рецепторов на плазматической мембране может также регулироваться процессом интернационализации (осуществляемым в некоторых случаях катаболизмом), или down регуляцией рецептора. Хотя вызывающие ее сигналы не ясны, представляется, что они отличны от контролирующих десенситезацию.
 G белки осуществляют трансдукцию сигнала от мембранных рецепторов к эффекторным ферментам и ионным каналам. Каждый из этих белков состоит из 3 х отдельных субъединиц , обозначаемых α, β, γ в порядке снижения молекулярного веса. α субъединица тримера связывает гуанин нуклеотиды и является главным посредником во влиянии G белков на их эффектор. Основной функцией β и γ субъединиц тримера является поддержка взаимодействия α субъединицы с плазматической мембранной и рецепторами, однако, они способны и к прямой регуляции эффектора (табл. 2). G белки, участвующие в трансмембранном переносе сигнала, регулируются общими механизмами. На рисунке 2 представлен цикл активации и инактивации этих белков. В базальном состоянии три субъединицы G белков вместе связаны с гуанозиндифисфатом, присоединенным к α субъединице. Когда агонист соединяется с рецептором, GDP отделяется и освободившиеся на α субъединице место занимается гуанозинтрифосфатом, в избытке присутствующим в цитоплазме.
G белки осуществляют трансдукцию сигнала от мембранных рецепторов к эффекторным ферментам и ионным каналам. Каждый из этих белков состоит из 3 х отдельных субъединиц , обозначаемых α, β, γ в порядке снижения молекулярного веса. α субъединица тримера связывает гуанин нуклеотиды и является главным посредником во влиянии G белков на их эффектор. Основной функцией β и γ субъединиц тримера является поддержка взаимодействия α субъединицы с плазматической мембранной и рецепторами, однако, они способны и к прямой регуляции эффектора (табл. 2). G белки, участвующие в трансмембранном переносе сигнала, регулируются общими механизмами. На рисунке 2 представлен цикл активации и инактивации этих белков. В базальном состоянии три субъединицы G белков вместе связаны с гуанозиндифисфатом, присоединенным к α субъединице. Когда агонист соединяется с рецептором, GDP отделяется и освободившиеся на α субъединице место занимается гуанозинтрифосфатом, в избытке присутствующим в цитоплазме.
 Возникновение этой связи стимулирует G белки в результате α субъединица отделяется от рецептора и от β, γ субъединиц и связывается с эффектором. Спустя несколько секунд, имеющаяся в α субъединице GTPаза гидролизует связанную GTP до GDP, что приводит к инактивации субъединицы. Связанная с GDP α субъединица отделяется от эффектора и вновь ассоциируется с β, γ комплексом G белков, становясь способной к новому циклу активации рецептором. Функциональные различия между членами семейства G белков первично определяются отличиями в α субъединицах, которых на 2000 год было известно более 20 (табл. 3). Номенклатура G белков изначально строилась в соответствии с их функцией. Так обозначения GS и Gi приняты для, соответственно, стимулирующих и ингибирующих аденилатциклазу G белков. Обозначение Gt было введено раньше когда впервые открытый в сетчатке G белок назывался трансдуцином.
Возникновение этой связи стимулирует G белки в результате α субъединица отделяется от рецептора и от β, γ субъединиц и связывается с эффектором. Спустя несколько секунд, имеющаяся в α субъединице GTPаза гидролизует связанную GTP до GDP, что приводит к инактивации субъединицы. Связанная с GDP α субъединица отделяется от эффектора и вновь ассоциируется с β, γ комплексом G белков, становясь способной к новому циклу активации рецептором. Функциональные различия между членами семейства G белков первично определяются отличиями в α субъединицах, которых на 2000 год было известно более 20 (табл. 3). Номенклатура G белков изначально строилась в соответствии с их функцией. Так обозначения GS и Gi приняты для, соответственно, стимулирующих и ингибирующих аденилатциклазу G белков. Обозначение Gt было введено раньше когда впервые открытый в сетчатке G белок назывался трансдуцином.
 Несовершенство этой номенклатуры стало очевидным после выделения и клонирования G белков с невыясненной функцией. Так появились обозначения G 0, Gq, затем G 11, G 12 и тд. Некоторые G белки экспрессируются лишь в определенных типах клеток и высокоспециализированны, например Gt обнаружен только в палочках и колбочках сетчатки, где активирует с. GMP специфичную фосфодиэстеразу. Другие G белки наоборот экспрессируются в большинстве тканей и имеют множественную функцию, например, Gi присутствует в большинстве клеток, ингибируя аденилатциклазу, но Gi способен и к прямому воздействию на некоторые ионные каналы. Влияние большинства G белков на эффекторы – стимулирующее, однако, некоторые их ингибируют. Например, G 0 ингибирует Ca++ каналы в мозге и в сердце, Gs стимулирует, а Gi ингибирует аденилатциклазу. Последние два G белка в свою очередь регулируются различными группами рецепторов, которые часто представлены в одной клетке. Одновременная активация стимулирующих и ингибирующих рецепторов имеет результатом уменьшение, смягчение аденилатциклазного ответа.
Несовершенство этой номенклатуры стало очевидным после выделения и клонирования G белков с невыясненной функцией. Так появились обозначения G 0, Gq, затем G 11, G 12 и тд. Некоторые G белки экспрессируются лишь в определенных типах клеток и высокоспециализированны, например Gt обнаружен только в палочках и колбочках сетчатки, где активирует с. GMP специфичную фосфодиэстеразу. Другие G белки наоборот экспрессируются в большинстве тканей и имеют множественную функцию, например, Gi присутствует в большинстве клеток, ингибируя аденилатциклазу, но Gi способен и к прямому воздействию на некоторые ионные каналы. Влияние большинства G белков на эффекторы – стимулирующее, однако, некоторые их ингибируют. Например, G 0 ингибирует Ca++ каналы в мозге и в сердце, Gs стимулирует, а Gi ингибирует аденилатциклазу. Последние два G белка в свою очередь регулируются различными группами рецепторов, которые часто представлены в одной клетке. Одновременная активация стимулирующих и ингибирующих рецепторов имеет результатом уменьшение, смягчение аденилатциклазного ответа.
 Эта двойная регуляция в дополнение к взаимодействию других следующих за белками компонентов сигнальной системы обеспечивает интегрированный ответ клетки на многочисленные стимулы. Эффекторные ферменты, регулируемые G белками Из трех компонентов, обеспечивающих сопряженное с G белками проведение сигнала, эффекторные звенья наиболее сложно изучать на молекулярном уровне. Только недавно некоторые из ферментов этого звена были изолированы и клонированы. Эффекты гормональных и нейромедиаторных рецепторов чаще всего реализуются через аденилатциклазу и фосфолипазу С (табл. 1). Эти две системы схематически представленные на рис. 1 изучены наиболее подробно. Другие ферменты, такие как фосфолипаза А 2, продуцирующая арахидоновую кислоту, также повидимому регулируются G белками, однако эти реакции до конца не ясны.
Эта двойная регуляция в дополнение к взаимодействию других следующих за белками компонентов сигнальной системы обеспечивает интегрированный ответ клетки на многочисленные стимулы. Эффекторные ферменты, регулируемые G белками Из трех компонентов, обеспечивающих сопряженное с G белками проведение сигнала, эффекторные звенья наиболее сложно изучать на молекулярном уровне. Только недавно некоторые из ферментов этого звена были изолированы и клонированы. Эффекты гормональных и нейромедиаторных рецепторов чаще всего реализуются через аденилатциклазу и фосфолипазу С (табл. 1). Эти две системы схематически представленные на рис. 1 изучены наиболее подробно. Другие ферменты, такие как фосфолипаза А 2, продуцирующая арахидоновую кислоту, также повидимому регулируются G белками, однако эти реакции до конца не ясны.
 Аденилатциклаза и ц. АМФ как вторичный мессенджер Циклический АМФ (ц. АМФ) синтезируется из АТФ встроенными в плазматическую мембрану аденилилциклазными ферментами. Представляется, что эти ферменты являются большими полипептидами, содержащими два кластера из шести трансмембранных сегментов, разделяющих два сходных каталитических домена. Имеется, по крайней мере, 8 форм аденилатциклазы. Все они стимулируются Gsα, но отличаются по чувствительности к ингибирующему влиянию Giα, стимуляции кальций зависимым кальмодулином (calcium/calmodulin) и эффекта βγ субъединиц G белков (табл. 2). Эти дополнительные регуляторы дают возможность интеграции многих сигналов, влияющих на различные системы вторичных месенеджеров внутри одной клетки. Циклический АМФ проявляет свой эффект в клетке в основном активируя ц. АМФ-зависимые протеинкиназы ( протеинкиназа А, РКА). Эти тетрамерные ферменты состоят из двух регуляторных и двух каталитических субъединиц. Ферменты активируются, когда две молекулы ц. АМФ присоединяются к каждой регуляторной субъединице, освобождая каталитические субъединицы из тетрамера.
Аденилатциклаза и ц. АМФ как вторичный мессенджер Циклический АМФ (ц. АМФ) синтезируется из АТФ встроенными в плазматическую мембрану аденилилциклазными ферментами. Представляется, что эти ферменты являются большими полипептидами, содержащими два кластера из шести трансмембранных сегментов, разделяющих два сходных каталитических домена. Имеется, по крайней мере, 8 форм аденилатциклазы. Все они стимулируются Gsα, но отличаются по чувствительности к ингибирующему влиянию Giα, стимуляции кальций зависимым кальмодулином (calcium/calmodulin) и эффекта βγ субъединиц G белков (табл. 2). Эти дополнительные регуляторы дают возможность интеграции многих сигналов, влияющих на различные системы вторичных месенеджеров внутри одной клетки. Циклический АМФ проявляет свой эффект в клетке в основном активируя ц. АМФ-зависимые протеинкиназы ( протеинкиназа А, РКА). Эти тетрамерные ферменты состоят из двух регуляторных и двух каталитических субъединиц. Ферменты активируются, когда две молекулы ц. АМФ присоединяются к каждой регуляторной субъединице, освобождая каталитические субъединицы из тетрамера.
 Освободившиеся субъединицы катализируют перенос фосфатной группы из АТФ на специфические сериновые или треаниновые остатки белков-мишеней. Среди таковых могу быть ферменты, которые участвуют в метаболических процессах клетки и белки, регулирующие транскрипцию гена. Хорошо изучен, например, активируемый ц. АМФ метаболический путь, составляющий каскад ферментативных активаций, ведущий к распаду гликогенов печени. Активированная протеинкиназа А фосфорилирует фосфорилазную киназу (phosphorylase kinase), которая, в свою очередь, фосфорилирует гликогенфосфорилазу, фермент, катализирующий распад гликогена. катализируемым протеинкиназой А фосфорилированием белка, известного под названием c. AMP response element-binding protein (CREB). CREB присоединяется к специфическим коротким последовательностям ДНК известных как c. AMP response elements (CRE). CREB присоединяется к CRE будучи фосфорилированным протеинкиназой А, что стимулирует транскрипцию генов, содержащих CRE в их регуляторных зонах.
Освободившиеся субъединицы катализируют перенос фосфатной группы из АТФ на специфические сериновые или треаниновые остатки белков-мишеней. Среди таковых могу быть ферменты, которые участвуют в метаболических процессах клетки и белки, регулирующие транскрипцию гена. Хорошо изучен, например, активируемый ц. АМФ метаболический путь, составляющий каскад ферментативных активаций, ведущий к распаду гликогенов печени. Активированная протеинкиназа А фосфорилирует фосфорилазную киназу (phosphorylase kinase), которая, в свою очередь, фосфорилирует гликогенфосфорилазу, фермент, катализирующий распад гликогена. катализируемым протеинкиназой А фосфорилированием белка, известного под названием c. AMP response element-binding protein (CREB). CREB присоединяется к специфическим коротким последовательностям ДНК известных как c. AMP response elements (CRE). CREB присоединяется к CRE будучи фосфорилированным протеинкиназой А, что стимулирует транскрипцию генов, содержащих CRE в их регуляторных зонах.
 Фосфолипаза С и фосфолипидные вторичные мессенджеры Представители семейства Gq белков (табл. 3) сопрягают различные рецепторы с группой ферментов, известных как фосфолипаза с-β. Эти ферменты принадлежат к большому семейству фосфолипаз, субстратом для которых являются инозитолфосфолипиды. Сигнальная трансдукция через этот путь влечет последовательность молекулярных событий, сходных с наблюдаемыми при активации аденилатциклазы. Связывание агониста с рецептором активирует Gбелок, который, в свою очередь, присоединяется к фосфолипазе на внутренней поверхности плазматической мембраны. Активированная липаза быстро превращает фосфатидилинозитолбифосфат PIP 2 в инозитолтрифосфат (IP 3) и диацил-глицерол. Обе эти молекулы действовуют как вторичные мессенджеры двумя различными путями. IP 3 небольшая водорастворимая молекула, способна быстро диффундировать в цитоплазму и просоединяться к IP 3 – зависимым кальциевым каналам в гладком эндоплазматическом ретикулуме, освобождая запасы кальция в цитозоль.
Фосфолипаза С и фосфолипидные вторичные мессенджеры Представители семейства Gq белков (табл. 3) сопрягают различные рецепторы с группой ферментов, известных как фосфолипаза с-β. Эти ферменты принадлежат к большому семейству фосфолипаз, субстратом для которых являются инозитолфосфолипиды. Сигнальная трансдукция через этот путь влечет последовательность молекулярных событий, сходных с наблюдаемыми при активации аденилатциклазы. Связывание агониста с рецептором активирует Gбелок, который, в свою очередь, присоединяется к фосфолипазе на внутренней поверхности плазматической мембраны. Активированная липаза быстро превращает фосфатидилинозитолбифосфат PIP 2 в инозитолтрифосфат (IP 3) и диацил-глицерол. Обе эти молекулы действовуют как вторичные мессенджеры двумя различными путями. IP 3 небольшая водорастворимая молекула, способна быстро диффундировать в цитоплазму и просоединяться к IP 3 – зависимым кальциевым каналам в гладком эндоплазматическом ретикулуме, освобождая запасы кальция в цитозоль.
 Увеличение концентрации Са ++ в цитоплазме инициирует волну Са ++ зависимых реакций в клетке, многие из которых опосредуются специфическими Са ++-связывающими белками из которых наиболее распространен калемодулин. Са ++ -кальмодулин регулирует ряд ферментов, включая Са ++ -зависимую АТФ-азу плазматической мембраны, которая выкачивает кальций из клетки, и, как было сказано раньше, (табл. 2), некоторые типы аденилатциклазы. Большинство эффектов кальция в клетке являются результатом активации группы протеинкиназ, известных как Са ++ кальмодулинзависимые протеинкиназы. Эти киназы фосфорилируют сериновые и треониновые остатки различных белков. Таким образом, вновь физиологический ответ на активацию фосфолипидного вторичного мессенджера в каждой клетке зависит именно от экспрессирующихся в ней белков, являющихся мишенью Са ++ / кальмодулин киназ.
Увеличение концентрации Са ++ в цитоплазме инициирует волну Са ++ зависимых реакций в клетке, многие из которых опосредуются специфическими Са ++-связывающими белками из которых наиболее распространен калемодулин. Са ++ -кальмодулин регулирует ряд ферментов, включая Са ++ -зависимую АТФ-азу плазматической мембраны, которая выкачивает кальций из клетки, и, как было сказано раньше, (табл. 2), некоторые типы аденилатциклазы. Большинство эффектов кальция в клетке являются результатом активации группы протеинкиназ, известных как Са ++ кальмодулинзависимые протеинкиназы. Эти киназы фосфорилируют сериновые и треониновые остатки различных белков. Таким образом, вновь физиологический ответ на активацию фосфолипидного вторичного мессенджера в каждой клетке зависит именно от экспрессирующихся в ней белков, являющихся мишенью Са ++ / кальмодулин киназ.
 Другой молекулярный продукт гидролиза PIP 2 фосфолипазой С диацилглицерол. Эта липидная молекула остается в плазматической мембране, где совместно с фосфатидилсерином активирует некоторых членов другого семейства серин-треониновых киназ, известных как протеинкиназа С. Эти растворимые киназы перемещаются в мембрану в ответ на увеличение кальция в цитозоле (вызванного освобождением IP 3) и затем активируются комбинированным воздействием Са ++ , диацилглицерола и фосфатидилсерина. Будучи активированными эти киназы фосфорилируют специфические для клетки группы субстратных белков, которые включают многие ионные каналы, рецепторы и другие киназы, что в конечном счете увеличивает генную транскрипцию.
Другой молекулярный продукт гидролиза PIP 2 фосфолипазой С диацилглицерол. Эта липидная молекула остается в плазматической мембране, где совместно с фосфатидилсерином активирует некоторых членов другого семейства серин-треониновых киназ, известных как протеинкиназа С. Эти растворимые киназы перемещаются в мембрану в ответ на увеличение кальция в цитозоле (вызванного освобождением IP 3) и затем активируются комбинированным воздействием Са ++ , диацилглицерола и фосфатидилсерина. Будучи активированными эти киназы фосфорилируют специфические для клетки группы субстратных белков, которые включают многие ионные каналы, рецепторы и другие киназы, что в конечном счете увеличивает генную транскрипцию.
 Другие процессы сигнальной трансдукции, регулируемые G белками В дополнение к описанным ферментам совсем недавно было показано, что G белки также модулируют и активность вольтаж зависимых ионных каналов. Как видно из табл. 1, многие гормоны и нейромедиаторы регулируют как вторичные мессенджеры, так и ионные каналы, активируя один G белок. Например, GS стимулирует как аденилатциклазу, так и некоторые типы Са ++ каналов. Очевидно, что дальнейшее выяснение механизмов прямой и обратной регуляции рецепторных систем сигнальной трансдукции является одной из важнейших научных задач будущего.
Другие процессы сигнальной трансдукции, регулируемые G белками В дополнение к описанным ферментам совсем недавно было показано, что G белки также модулируют и активность вольтаж зависимых ионных каналов. Как видно из табл. 1, многие гормоны и нейромедиаторы регулируют как вторичные мессенджеры, так и ионные каналы, активируя один G белок. Например, GS стимулирует как аденилатциклазу, так и некоторые типы Са ++ каналов. Очевидно, что дальнейшее выяснение механизмов прямой и обратной регуляции рецепторных систем сигнальной трансдукции является одной из важнейших научных задач будущего.
 Рецепторы, связанные с ферментами Тирозинкиназные рецепторы Эта группа рецепторов опосредует сигнал от ряда эндогенных веществ, включающих инсулин, эпидермальный фактор роста (EGF), тромбоцитарный фактор роста (platelet-derived growth factor) PDGF. Эти рецепторы сформированы одной полипептидной цепью, которая пронизывает цитоплазматическую мембрану, образуя 3 домена: лигандсвязывающий экстрацеллюлярный, трансмембранный и интрацеллюлярный, который содержит участок, обеспечивающий ферментативную активность (рис. 1). Некоторые из этих рецепторов, например инсулиновый, существуют в виде димеров из двух рецепторов, сопряженных друг с другом нековалентными связями. Другие, такие как EGF рецептор, существуют внутри мембраны в единичной форме и образуют димер в ответ на присоединение лиганда к каждой субъединице. В любом случае связывание фактора роста с рецептором приводит к аллостерической активации тирозинкиназной активности в цитоплазматическом домене рецептора.
Рецепторы, связанные с ферментами Тирозинкиназные рецепторы Эта группа рецепторов опосредует сигнал от ряда эндогенных веществ, включающих инсулин, эпидермальный фактор роста (EGF), тромбоцитарный фактор роста (platelet-derived growth factor) PDGF. Эти рецепторы сформированы одной полипептидной цепью, которая пронизывает цитоплазматическую мембрану, образуя 3 домена: лигандсвязывающий экстрацеллюлярный, трансмембранный и интрацеллюлярный, который содержит участок, обеспечивающий ферментативную активность (рис. 1). Некоторые из этих рецепторов, например инсулиновый, существуют в виде димеров из двух рецепторов, сопряженных друг с другом нековалентными связями. Другие, такие как EGF рецептор, существуют внутри мембраны в единичной форме и образуют димер в ответ на присоединение лиганда к каждой субъединице. В любом случае связывание фактора роста с рецептором приводит к аллостерической активации тирозинкиназной активности в цитоплазматическом домене рецептора.
 Представляется, что первый шаг в этой активации включает перекрестное фосфорилирование множественных остатков тирозина 2 -х рецепторных субъединиц внутри интрацеллюлярного домена. Эта автофосфорилирование действует как сигнал к связыванию других внутриклеточных белков тирозиновые остатки которых фосфорилируются рецептором и таким образом активируются. Опять таки специфичность клеточного ответа детерминируется специфичными для данной клетки комбинациями белков, которые присоединяются к рецепторам факторов роста. В последнее время большое число белков, присоединяющихся к активированным рецепторам факторов роста было идентифицировано. Имея различную структуру, эти белки включают 2 консервативных домена, известных как SH 2 и SH 3 (Sre homology region). Впервые они были выявлены в протоонкогене, названном как Sre белок, отсюда и название. SH 2 домены распознают фосфотирозины на рецепторах факторов роста, функции SH 3 пока не ясны.
Представляется, что первый шаг в этой активации включает перекрестное фосфорилирование множественных остатков тирозина 2 -х рецепторных субъединиц внутри интрацеллюлярного домена. Эта автофосфорилирование действует как сигнал к связыванию других внутриклеточных белков тирозиновые остатки которых фосфорилируются рецептором и таким образом активируются. Опять таки специфичность клеточного ответа детерминируется специфичными для данной клетки комбинациями белков, которые присоединяются к рецепторам факторов роста. В последнее время большое число белков, присоединяющихся к активированным рецепторам факторов роста было идентифицировано. Имея различную структуру, эти белки включают 2 консервативных домена, известных как SH 2 и SH 3 (Sre homology region). Впервые они были выявлены в протоонкогене, названном как Sre белок, отсюда и название. SH 2 домены распознают фосфотирозины на рецепторах факторов роста, функции SH 3 пока не ясны.
 Характеристика белков, содержащих SH 2 и SH 3 домены является сегодня предметом многих исследований. Роль некоторых из них показана. Например, одним из механизмов, которым факторы роста регулируют клеточный рост и дифференцировку, является активация каскада протеинкиназ, известных как митоген активируемые протеинкиназы (mitogen activated protein kinas) (МАР kinase pathway). Активация этого пути инициирyется фосфорилированием тирозинов белка Grb 2 , содержащего SH 2 и SH 3 домены. SH 3 домен на Grb 2 присоединяет другой белок, известный как м SOS и совместно, комплекс Grb 2/ м SOS активирует Ras, мономерный G белок. Ras имеет структуру, аналогичную α – субъединице G белков, которая взаимодействует с 7 -трансмембранными (сопряженными с G белками) рецепторами и активируется и инактивируется сходными механизмами (рис. 2). Отсюда, взаимодействие Ras с Grb 2/ м SOS ускоряет обмен GDP на GTP на Ras, стимулируя его активацию. Следующий шаг в этом каскаде менее понят, но, включает, по видимому, активацию Ras серин/треонинкиназы, известной как Raf.
Характеристика белков, содержащих SH 2 и SH 3 домены является сегодня предметом многих исследований. Роль некоторых из них показана. Например, одним из механизмов, которым факторы роста регулируют клеточный рост и дифференцировку, является активация каскада протеинкиназ, известных как митоген активируемые протеинкиназы (mitogen activated protein kinas) (МАР kinase pathway). Активация этого пути инициирyется фосфорилированием тирозинов белка Grb 2 , содержащего SH 2 и SH 3 домены. SH 3 домен на Grb 2 присоединяет другой белок, известный как м SOS и совместно, комплекс Grb 2/ м SOS активирует Ras, мономерный G белок. Ras имеет структуру, аналогичную α – субъединице G белков, которая взаимодействует с 7 -трансмембранными (сопряженными с G белками) рецепторами и активируется и инактивируется сходными механизмами (рис. 2). Отсюда, взаимодействие Ras с Grb 2/ м SOS ускоряет обмен GDP на GTP на Ras, стимулируя его активацию. Следующий шаг в этом каскаде менее понят, но, включает, по видимому, активацию Ras серин/треонинкиназы, известной как Raf.
 Raf затем активирует фосфорилированием другую киназу, МЕК, (известная как МАР киназная киназа), которая, в свою очередь, фосфорилирует МАР киназу. МАР киназа способна проходить через ядерную мембрану и в ядре она фосфорилирует различные факторы транскрипции. Возникающие изменения транскрипции гена инициируют процессы пролиферации или дифференцировки. Другие белки, взаимодействующие с рецепторами факторов роста, способны регулировать внутриклеточные вторичные мессенджеры. Например, члены семейства фосфолипазы с-γ которые регулируют уровень внутриклеточного IP 3 и диацилглицерола так же как PLC-β семейство обсуждавшееся выше, содержат SH 2 и SH 3 домены, и могут быть активированы тирозинкиназными рецепторами. Пока из рецепторов факторов роста только инсулиновые используются как фармакологические мишени у больных диабетом. Однако учитывая роль этих рецепторов в клеточном росте, неконтролируемое проведение через них сигналов при воспалительных и неопластических заболеваниях, они определяют большой интерес для разработки блокирующих их активность агентов. Например, мутантные Ras белки были обнаружены в более чем 30% опухолей человека. Поэтому, в настоящее время в качестве препаратов лечения опухолей разрабатываются вещества, способные ингибировать мутантные белки ras и другие в МАРкиназном пути.
Raf затем активирует фосфорилированием другую киназу, МЕК, (известная как МАР киназная киназа), которая, в свою очередь, фосфорилирует МАР киназу. МАР киназа способна проходить через ядерную мембрану и в ядре она фосфорилирует различные факторы транскрипции. Возникающие изменения транскрипции гена инициируют процессы пролиферации или дифференцировки. Другие белки, взаимодействующие с рецепторами факторов роста, способны регулировать внутриклеточные вторичные мессенджеры. Например, члены семейства фосфолипазы с-γ которые регулируют уровень внутриклеточного IP 3 и диацилглицерола так же как PLC-β семейство обсуждавшееся выше, содержат SH 2 и SH 3 домены, и могут быть активированы тирозинкиназными рецепторами. Пока из рецепторов факторов роста только инсулиновые используются как фармакологические мишени у больных диабетом. Однако учитывая роль этих рецепторов в клеточном росте, неконтролируемое проведение через них сигналов при воспалительных и неопластических заболеваниях, они определяют большой интерес для разработки блокирующих их активность агентов. Например, мутантные Ras белки были обнаружены в более чем 30% опухолей человека. Поэтому, в настоящее время в качестве препаратов лечения опухолей разрабатываются вещества, способные ингибировать мутантные белки ras и другие в МАРкиназном пути.
 Гуанилат циклазные рецепторы Известен только один класс таких рецепторов для семейства пептидных гормонов, называемых предсердными натрийуретическими пептидами (atrial natriuretic peptides, ANPs). Они секретируются мышечными клетками в ответ на увеличение кровяного давления. ANPs связываются с рецепторами в почках, где индуцируют увеличение экскреции натрия и воды и в гладких мышцах сосудов, вызывая их релаксацию. ANP рецептор является одиночным полипептидом, содержащим экстрацеллюлярный ANP связывающий домен, одиночный трансмембранный домен и внутриклеточный каталитический домен с гуанилатциклазой. Активация рецептора ведет к увеличению продукции ц. ГМФ, который, в свою очередь, активирует серин-треонин киназы, ц. ГМФ зависимую протеинкиназу (протеинкиназу G). Белки-мишени для протеинкиназы G и сигнальные каскады, ведущие к ответу на ANP недостаточно изучены.
Гуанилат циклазные рецепторы Известен только один класс таких рецепторов для семейства пептидных гормонов, называемых предсердными натрийуретическими пептидами (atrial natriuretic peptides, ANPs). Они секретируются мышечными клетками в ответ на увеличение кровяного давления. ANPs связываются с рецепторами в почках, где индуцируют увеличение экскреции натрия и воды и в гладких мышцах сосудов, вызывая их релаксацию. ANP рецептор является одиночным полипептидом, содержащим экстрацеллюлярный ANP связывающий домен, одиночный трансмембранный домен и внутриклеточный каталитический домен с гуанилатциклазой. Активация рецептора ведет к увеличению продукции ц. ГМФ, который, в свою очередь, активирует серин-треонин киназы, ц. ГМФ зависимую протеинкиназу (протеинкиназу G). Белки-мишени для протеинкиназы G и сигнальные каскады, ведущие к ответу на ANP недостаточно изучены.
 Ионные каналы, контролируемые лигандным связыванием Синаптические нейромедиаторы связываются с группой рецепторов на постсинаптических мембранах, известных как лиганд-контролируемые ионные каналы (3 на рис. 1). Среди них ацетилхолин, γ-аминомасляная кислота, глицин, глутамат. Лиганд контролируемые ионные каналыважнейшая мишень для действия лекарственных средств, особенно психотропных. Различные ионные каналы сходны по структуре, они состоят из нескольких субъединиц, формирующих в мембране ионный канал. Каждая субъединица канала – полипептид, содержащий 4 перекрывающих мембрану домена. В то же время для них характерна специфичность связывания нейромедиаторов и селективность транспорта ионов (табл. 4). В данном классе лучше всего охарактеризован н-ацетилхолиновый рецептор. Этот ионный канал (3 рис. 1) состоит из 5 субъединиц (2α, δ, β и γ), которые совместно формируют пору, проходящую через плазматическую мембрану. Закрытая позиция двух α-субъединиц внутри мембраны формирует «ворота» , препятствующие прохождению ионов через канал. Ацетилхолин, присоединяясь к экстрацеллюлярным участкам 2 -х α-субъединиц, вызывает в них конформационные изменения ведущие к открытию канала для ионов, в особенности, для Na+, которые идут внутрь клетки, соответственно химическому градиенту.
Ионные каналы, контролируемые лигандным связыванием Синаптические нейромедиаторы связываются с группой рецепторов на постсинаптических мембранах, известных как лиганд-контролируемые ионные каналы (3 на рис. 1). Среди них ацетилхолин, γ-аминомасляная кислота, глицин, глутамат. Лиганд контролируемые ионные каналыважнейшая мишень для действия лекарственных средств, особенно психотропных. Различные ионные каналы сходны по структуре, они состоят из нескольких субъединиц, формирующих в мембране ионный канал. Каждая субъединица канала – полипептид, содержащий 4 перекрывающих мембрану домена. В то же время для них характерна специфичность связывания нейромедиаторов и селективность транспорта ионов (табл. 4). В данном классе лучше всего охарактеризован н-ацетилхолиновый рецептор. Этот ионный канал (3 рис. 1) состоит из 5 субъединиц (2α, δ, β и γ), которые совместно формируют пору, проходящую через плазматическую мембрану. Закрытая позиция двух α-субъединиц внутри мембраны формирует «ворота» , препятствующие прохождению ионов через канал. Ацетилхолин, присоединяясь к экстрацеллюлярным участкам 2 -х α-субъединиц, вызывает в них конформационные изменения ведущие к открытию канала для ионов, в особенности, для Na+, которые идут внутрь клетки, соответственно химическому градиенту.
 Внутриклеточные рецепторы Достаточно жирорастворимые лиганды, способные проникать через плазматическую мембрану, проявляют свое действие, связываясь с группой внутриклеточных белков, называемых суперсемейством стероидных рецепторов (4 на рис. 1). Оно включает рецепторы глюкокортикоидов, минералокортикоидов, половых стероидных гормонов, витамина Д, тиреоидного гормона и ретиноевой кислоты. Активация всех этих рецепторов приводит к увеличению транскрипции в определенных генах клетки-мишени, поэтому, они называются лиганд-зависимыми факторами транскрипции. Общая структура рецептора этого класса (рис1) представляет собой единичный полипептид, который делится на 3 функциональных домена. N-концевой участок рецептора имеет модуляторную функцию и в отсутствие своего лиганда связан с белоком, известным как hsp 90 (90 k. Da heat-shock prоtein).
Внутриклеточные рецепторы Достаточно жирорастворимые лиганды, способные проникать через плазматическую мембрану, проявляют свое действие, связываясь с группой внутриклеточных белков, называемых суперсемейством стероидных рецепторов (4 на рис. 1). Оно включает рецепторы глюкокортикоидов, минералокортикоидов, половых стероидных гормонов, витамина Д, тиреоидного гормона и ретиноевой кислоты. Активация всех этих рецепторов приводит к увеличению транскрипции в определенных генах клетки-мишени, поэтому, они называются лиганд-зависимыми факторами транскрипции. Общая структура рецептора этого класса (рис1) представляет собой единичный полипептид, который делится на 3 функциональных домена. N-концевой участок рецептора имеет модуляторную функцию и в отсутствие своего лиганда связан с белоком, известным как hsp 90 (90 k. Da heat-shock prоtein).
 Домен рецептора связывающийся с ДНК расположен в середине белка и содержит структурный мотив, известный как «zinс finger» , который является общим для связывающихся с ДНК белков. Домен, присоединяющий лиганд, находится на С – концевом участке рецептора. В результате связывания с лигандом hsp 90 белок освобождается, открывая связывающийся с ДНК и активирующий транскрипцию домен рецептора. Поскольку действие лигандов этого класса требует увеличения транскрипции, трансляции и последующего белкового синтеза, ответ формируется медленно, часто в несколько часов. Аналогично, медленный оборот большинства белков, регулируемых этими лигандами, дает длительный эффект, продолжающийся после удаления лиганда. Соответственно, нельзя вывести простые зависимости между содержанием в плазме гормонов или лекарств, действующих на соответствующие рецепторы с их эффектом.
Домен рецептора связывающийся с ДНК расположен в середине белка и содержит структурный мотив, известный как «zinс finger» , который является общим для связывающихся с ДНК белков. Домен, присоединяющий лиганд, находится на С – концевом участке рецептора. В результате связывания с лигандом hsp 90 белок освобождается, открывая связывающийся с ДНК и активирующий транскрипцию домен рецептора. Поскольку действие лигандов этого класса требует увеличения транскрипции, трансляции и последующего белкового синтеза, ответ формируется медленно, часто в несколько часов. Аналогично, медленный оборот большинства белков, регулируемых этими лигандами, дает длительный эффект, продолжающийся после удаления лиганда. Соответственно, нельзя вывести простые зависимости между содержанием в плазме гормонов или лекарств, действующих на соответствующие рецепторы с их эффектом.
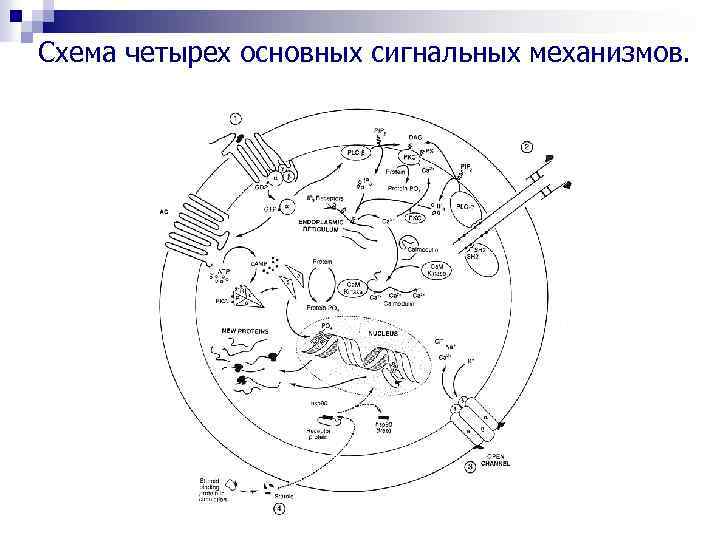 Схема четырех основных сигнальных механизмов.
Схема четырех основных сигнальных механизмов.
 1 – рецепторы, связанные с G-белками, 2 – рецепторы, связанные с тирозинкиназой, 3 – связанные с лигандами ионные каналы, 4 - внутриклеточные рецепторы. Сокращения: α, β, γ (механизм 1) = субъединицы G-белка; α, β, γ, δ (механизм 2) = субъединицы ионного канала; АС – аденилатциклаза, АТР – аденозинтрифосфат, с каталитические субъединицы РКА, Са. М – кальмодулин, с. АМР – циклический аденозин монофосфат, CRE = элемент ц. АМФ ответа, CREB – белок, связывающий элемент ц. АМФ ответа, DAG- диацилглицерол, GDP – гуанозин дифосфат, GTP – гуанозин трифосфат, hsp 90 – heat-shock protein 90, IP 3 – инозитол-1, 4, 5 -трифосфат, PIP 2 – фосфатидилинозитол-4, 5 -бфосфат, РКА – протеинкиназа А, РКС – протеинкиназа С, PLС – фосфолипаза С, PS – фосфатидилсерин, R – регуляторные субъединицы РКА, SH 2 – Src гомологичный участок 2, SRE – элемент стероидного ответа.
1 – рецепторы, связанные с G-белками, 2 – рецепторы, связанные с тирозинкиназой, 3 – связанные с лигандами ионные каналы, 4 - внутриклеточные рецепторы. Сокращения: α, β, γ (механизм 1) = субъединицы G-белка; α, β, γ, δ (механизм 2) = субъединицы ионного канала; АС – аденилатциклаза, АТР – аденозинтрифосфат, с каталитические субъединицы РКА, Са. М – кальмодулин, с. АМР – циклический аденозин монофосфат, CRE = элемент ц. АМФ ответа, CREB – белок, связывающий элемент ц. АМФ ответа, DAG- диацилглицерол, GDP – гуанозин дифосфат, GTP – гуанозин трифосфат, hsp 90 – heat-shock protein 90, IP 3 – инозитол-1, 4, 5 -трифосфат, PIP 2 – фосфатидилинозитол-4, 5 -бфосфат, РКА – протеинкиназа А, РКС – протеинкиназа С, PLС – фосфолипаза С, PS – фосфатидилсерин, R – регуляторные субъединицы РКА, SH 2 – Src гомологичный участок 2, SRE – элемент стероидного ответа.
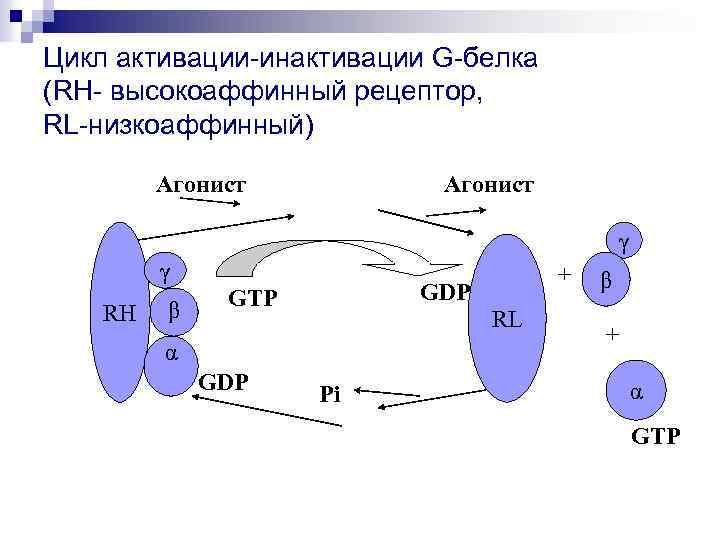 Цикл активации-инактивации G-белка (RH- высокоаффинный рецептор, RL-низкоаффинный) Агонист γ γ RH β GDP GTP RL α GDP + Pi β + α GTP
Цикл активации-инактивации G-белка (RH- высокоаффинный рецептор, RL-низкоаффинный) Агонист γ γ RH β GDP GTP RL α GDP + Pi β + α GTP


