Л2.ppt
- Количество слайдов: 31

МОЛЕКУЛЯРНЫЕ МЕХАНИЗМЫ ПРЕОБРАЗОВАНИЯ ИНФОРМАЦИИ В НЕЙРОНЕ

ВОПРОСЫ: Молекулярный интерфейс. Внутриклеточная интеграция сигналов. Молекулярные механизмы памяти.

МОЛЕКУЛЯРНАЯ СТРУКТУРА ИНТЕРФЕЙСА: В организме клетки являются изолированными объектами, которые взаимодействуют через специализированный молекулярный интерфейс. Молекулярный интерфейс включает сигнальные молекулы, их рецепторы и сопряженные с ними ферменты. Рецепторы сигнальных молекул являются основным компонентом интерфейса, обеспечивающим декодирование информации, содержащейся в пакете сигнальных молекул. Различают пять типов рецепторов : Ядерные и содержащие 1 трансмембранный домен, 2 трансмембранных домена 4 трансмембранных домена и 7 трансмембранных доменов.
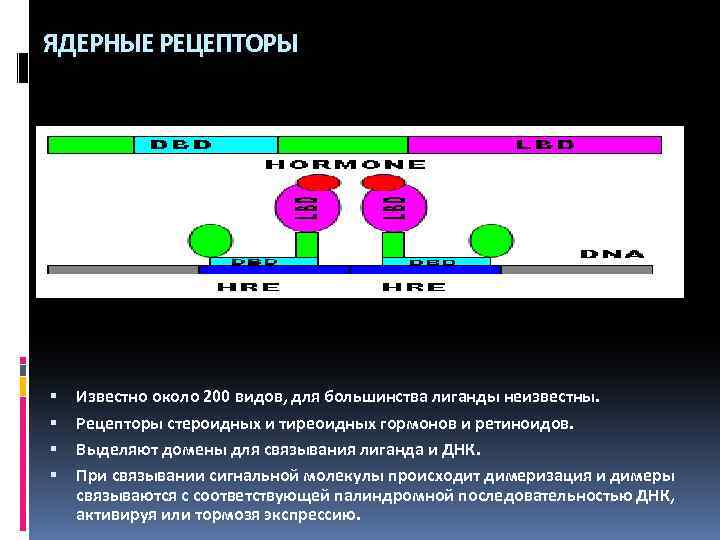
ЯДЕРНЫЕ РЕЦЕПТОРЫ Известно около 200 видов, для большинства лиганды неизвестны. Рецепторы стероидных и тиреоидных гормонов и ретиноидов. Выделяют домены для связывания лиганда и ДНК. При связывании сигнальной молекулы происходит димеризация и димеры связываются с соответствующей палиндромной последовательностью ДНК, активируя или тормозя экспрессию.
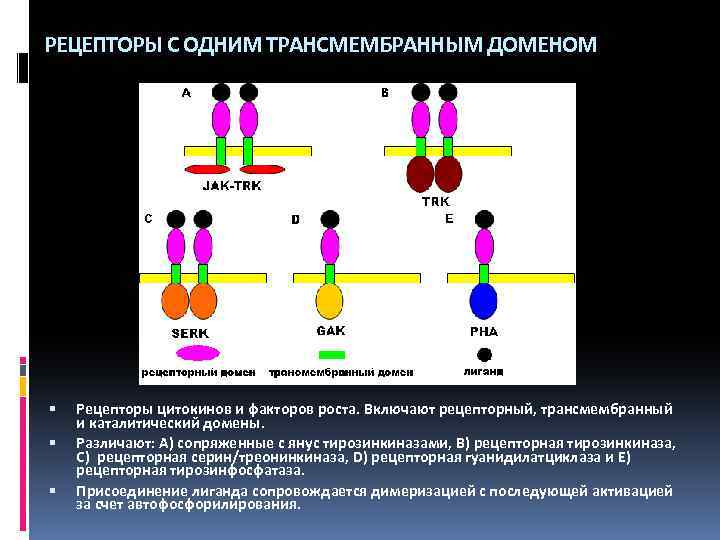
РЕЦЕПТОРЫ С ОДНИМ ТРАНСМЕМБРАННЫМ ДОМЕНОМ Рецепторы цитокинов и факторов роста. Включают рецепторный, трансмембранный и каталитический домены. Различают: A) сопряженные с янус тирозинкиназами, B) рецепторная тирозинкиназа, C) рецепторная серин/треонинкиназа, D) рецепторная гуанидилатциклаза и E) рецепторная тирозинфосфатаза. Присоединение лиганда сопровождается димеризацией с последующей активацией за счет автофосфорилирования.
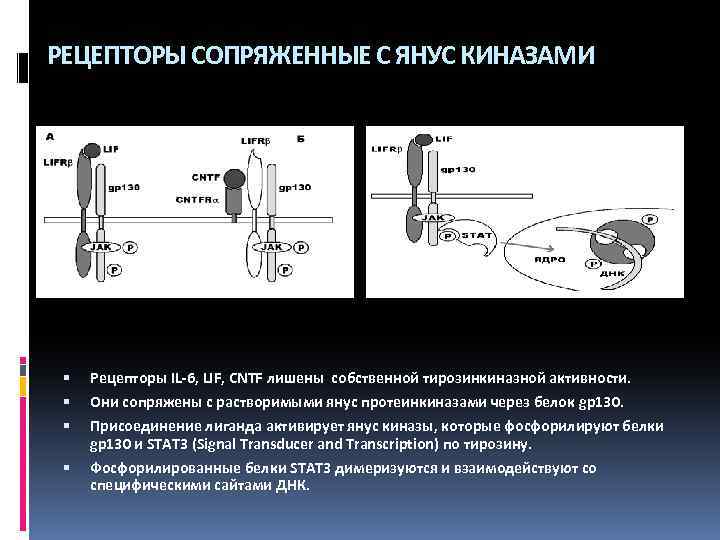
РЕЦЕПТОРЫ СОПРЯЖЕННЫЕ С ЯНУС КИНАЗАМИ Рецепторы IL-6, LIF, CNTF лишены собственной тирозинкиназной активности. Они сопряжены с растворимыми янус протеинкиназами через белок gp 130. Присоединение лиганда активирует янус киназы, которые фосфорилируют белки gp 130 и STAT 3 (Signal Transducer and Transcription) по тирозину. Фосфорилированные белки STAT 3 димеризуются и взаимодействуют со специфическими сайтами ДНК.
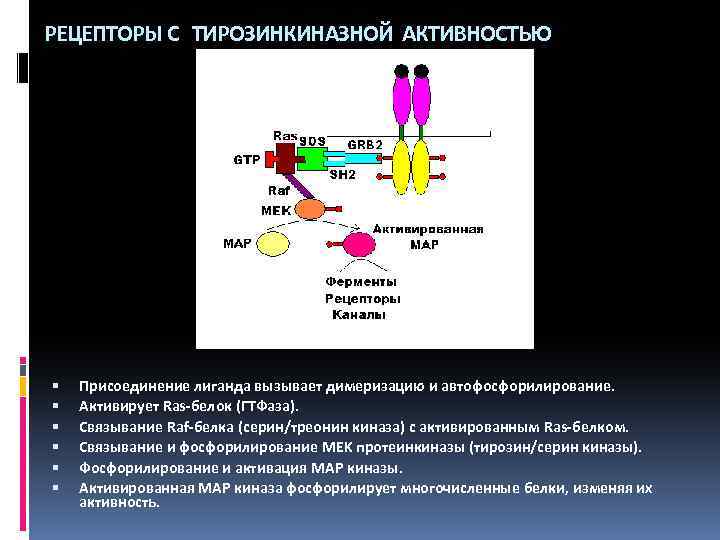
РЕЦЕПТОРЫ С ТИРОЗИНКИНАЗНОЙ АКТИВНОСТЬЮ Присоединение лиганда вызывает димеризацию и автофосфорилирование. Активирует Ras-белок (ГТФаза). Связывание Raf-белка (серин/треонин киназа) с активированным Ras-белком. Связывание и фосфорилирование MEK протеинкиназы (тирозин/серин киназы). Фосфорилирование и активация MAP киназы. Активированная MAP киназа фосфорилирует многочисленные белки, изменяя их активность.

СХЕМА P 2 X ПУРИНОРЕЦЕПТОРА Состоит из 3 или 6 субъединиц, включающих 2 трансмембранных домена. Субъединицы образуют Ca 2+ канал в норме закрытый. Присоединение АТФ вызывает открытие канала и проникновение ионов Ca 2+ внутрь нейрона.
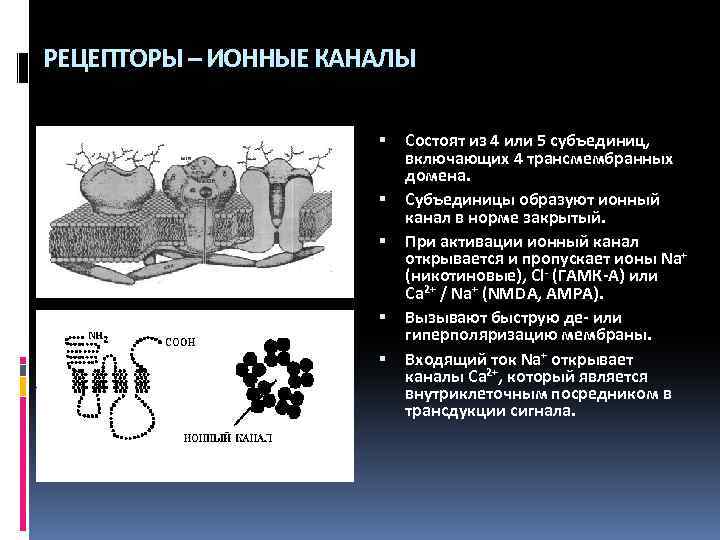
РЕЦЕПТОРЫ – ИОННЫЕ КАНАЛЫ Состоят из 4 или 5 субъединиц, включающих 4 трансмембранных домена. Субъединицы образуют ионный канал в норме закрытый. При активации ионный канал открывается и пропускает ионы Na+ (никотиновые), Cl- (ГАМК-А) или Ca 2+ / Na+ (NMDA, AMPA). Вызывают быструю де- или гиперполяризацию мембраны. Входящий ток Na+ открывает каналы Ca 2+, который является внутриклеточным посредником в трансдукции сигнала.

РЕЦЕПТОРЫ СОПРЯЖЕННЫЕ С G-БЕЛКАМИ Более 1000 рецепторов медиаторов, гормонов, света, вкуса, запаха. Семь трансмембранных доменов. Третья цитоплазматическая петля и COOH конец сопряжены с G-белком. Механизм трансдукции сигнала определяется природой G-белка. Отмечена конститутивная активность рецепторов в отсутствии лиганда. Лиганд только усиливает гидролиз G-белка.
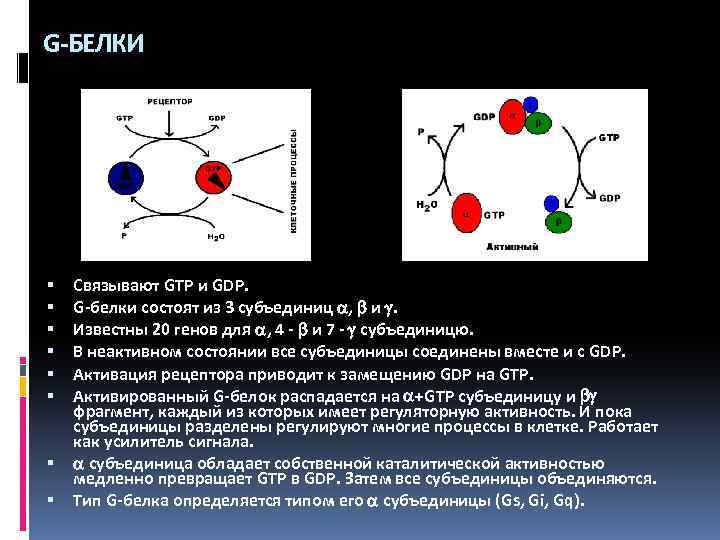
G-БЕЛКИ Связывают GTP и GDP. G-белки состоят из 3 субъединиц , и . Известны 20 генов для , 4 - и 7 - субъединицю. В неактивном состоянии все субъединицы соединены вместе и с GDP. Активация рецептора приводит к замещению GDP на GTP. Активированный G-белок распадается на +GTP субъединицу и фрагмент, каждый из которых имеет регуляторную активность. И пока субъединицы разделены регулируют многие процессы в клетке. Работает как усилитель сигнала. субъединица обладает собственной каталитической активностью медленно превращает GTP в GDP. Затем все субъединицы объединяются. Тип G-белка определяется типом его субъединицы (Gs, Gi, Gq).
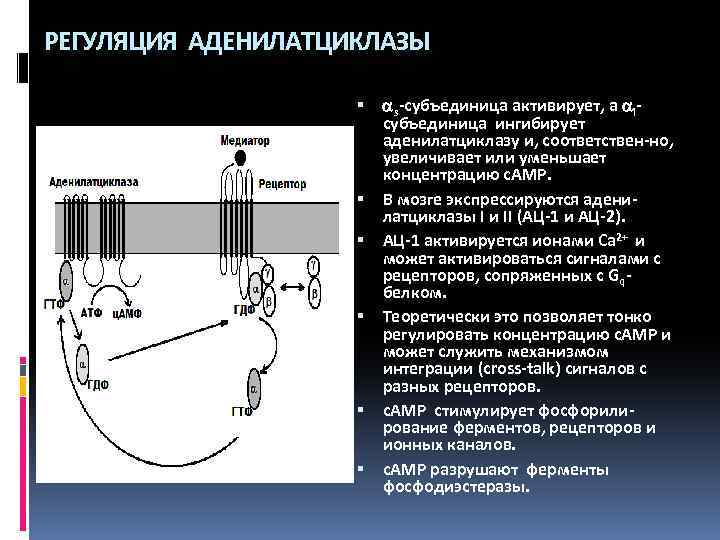
РЕГУЛЯЦИЯ АДЕНИЛАТЦИКЛАЗЫ s-субъединица активирует, а iсубъединица ингибирует аденилатциклазу и, соответствен-но, увеличивает или уменьшает концентрацию c. AMP. В мозге экспрессируются аденилатциклазы I и II (АЦ-1 и АЦ-2). АЦ-1 активируется ионами Ca 2+ и может активироваться сигналами с рецепторов, сопряженных с Gqбелком. Теоретически это позволяет тонко регулировать концентрацию c. AMP и может служить механизмом интеграции (cross-talk) сигналов с разных рецепторов. c. AMP стимулирует фосфорилирование ферментов, рецепторов и ионных каналов. c. AMP разрушают ферменты фосфодиэстеразы.

ФОСФОДИЭСТЕРАЗЫ Гидроксилируют c. AMP и снижают ее концентрацию в клетке. Играют ключевую роль в трансдукции сигнала внутри клетки. У дрозофилы фосфодиэстеразы участвуют в процессе обучения и памяти. Мутации в гене dunce, снижающие активность фосфодиэстеразы, нарушают память и обучение у дрозофилы.
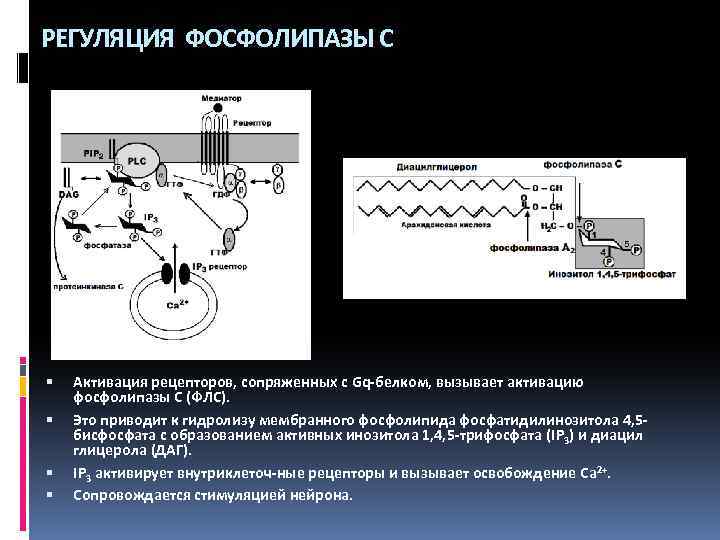
РЕГУЛЯЦИЯ ФОСФОЛИПАЗЫ С Активация рецепторов, сопряженных с Gq-белком, вызывает активацию фосфолипазы С (ФЛС). Это приводит к гидролизу мембранного фосфолипида фосфатидилинозитола 4, 5 бисфосфата с образованием активных инозитола 1, 4, 5 -трифосфата (IP 3) и диацил глицерола (ДАГ). IP 3 активирует внутриклеточ-ные рецепторы и вызывает освобождение Ca 2+. Сопровождается стимуляцией нейрона.
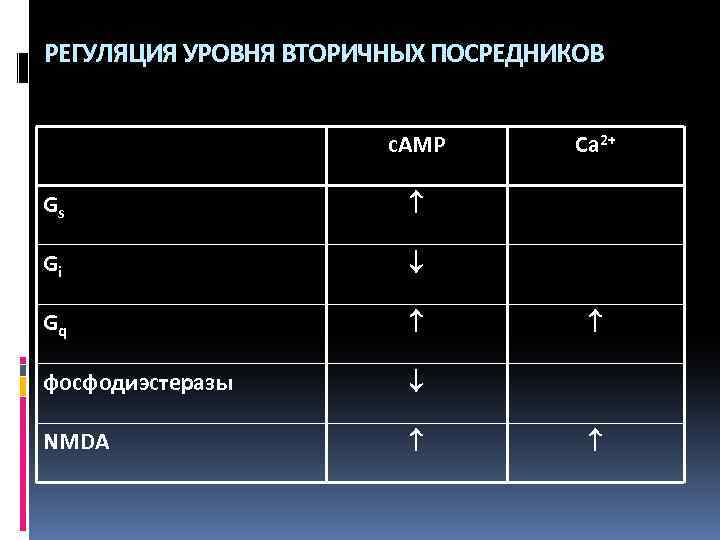
РЕГУЛЯЦИЯ УРОВНЯ ВТОРИЧНЫХ ПОСРЕДНИКОВ c. AMP Gs Gi Gq фосфодиэстеразы NMDA Ca 2+
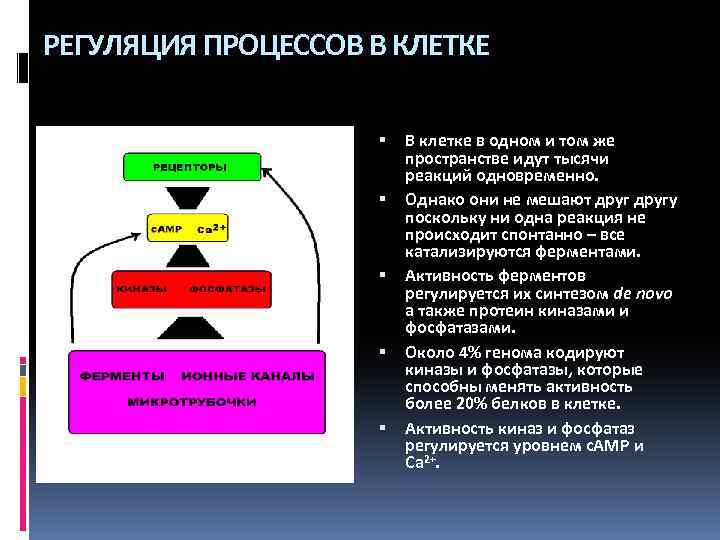
РЕГУЛЯЦИЯ ПРОЦЕССОВ В КЛЕТКЕ В клетке в одном и том же пространстве идут тысячи реакций одновременно. Однако они не мешают другу поскольку ни одна реакция не происходит спонтанно – все катализируются ферментами. Активность ферментов регулируется их синтезом de novo а также протеин киназами и фосфатазами. Около 4% генома кодируют киназы и фосфатазы, которые способны менять активность более 20% белков в клетке. Активность киназ и фосфатаз регулируется уровнем c. AMP и Ca 2+.

ПРОТЕИНКИНАЗЫ Протеинкиназы – ферменты переносящие -фосфатный остаток от ATP на гидроксильные остатки серина/треонина (сериновые киназы) или тирозина (тирозиновые киназы) в молекулах регулируемых белков. Обычно фосфорилирование активирует белки. Основные сериновые протеинкиназы: Протеинкиназа А, регулируемая c. AMP. Протеинкиназа С, регулируемая Ca 2+. Кальций, кальмодулин зависимая протеинкиназа II.
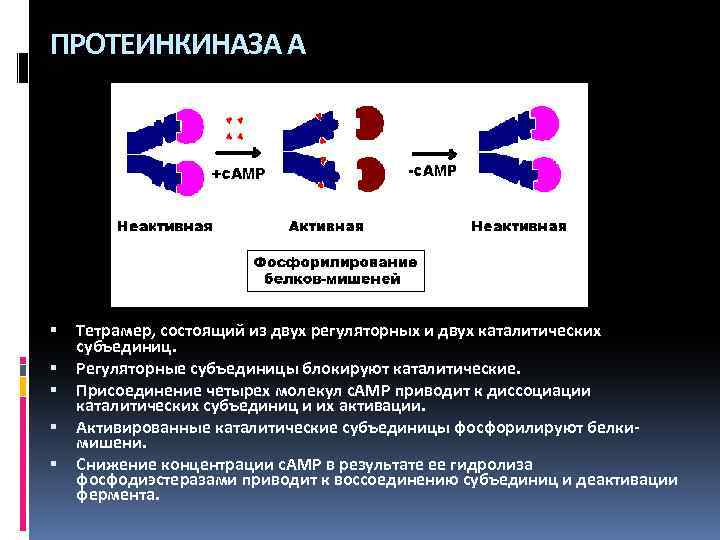
ПРОТЕИНКИНАЗА А Тетрамер, состоящий из двух регуляторных и двух каталитических субъединиц. Регуляторные субъединицы блокируют каталитические. Присоединение четырех молекул c. AMP приводит к диссоциации каталитических субъединиц и их активации. Активированные каталитические субъединицы фосфорилируют белкимишени. Снижение концентрации c. AMP в результате ее гидролиза фосфодиэстеразами приводит к воссоединению субъединиц и деактивации фермента.

ПРОТЕИНКИНАЗЫ С Мономеры, включающие каталитический (на С-конце) и регуляторный (на N-конце) домены. Регуляторный домен включает сайты для связывания Ca 2+ и диацилглицерол (регулятор). Связывание Ca 2+ активирует фермент. Не обладают субстратной специфичностью.

КАЛЬМОДУЛИН Устойчивый к нагреванию белок. Размер 17 к. Д и 4 центра связывания Ca 2+. Концентрация его в клетке высока. Комплекс кальмодулин-Ca 2+ активирует многие ферменты и ионные каналы.

ПРОТЕИНКИНАЗА II Состоит из 10 -12 субъединиц, кодируемых четырьмя гомологичными генами ( , , и ). Гомо- и гетеромультимеры и изоформ встречаются в основном в мозге, а и - повсеместно (и в мозге). Каждая субъединица состоит из каталитического и регуляторного домена. В неактивном состоянии регуляторный домен надвинут (закрывает) каталитический. Присоединение комплекса кальмодулин-(Ca 2+)4 смещает регуляторный домен, открывает каталитический и активирует его. Удаление Ca 2+ закрывает каталитический домен.
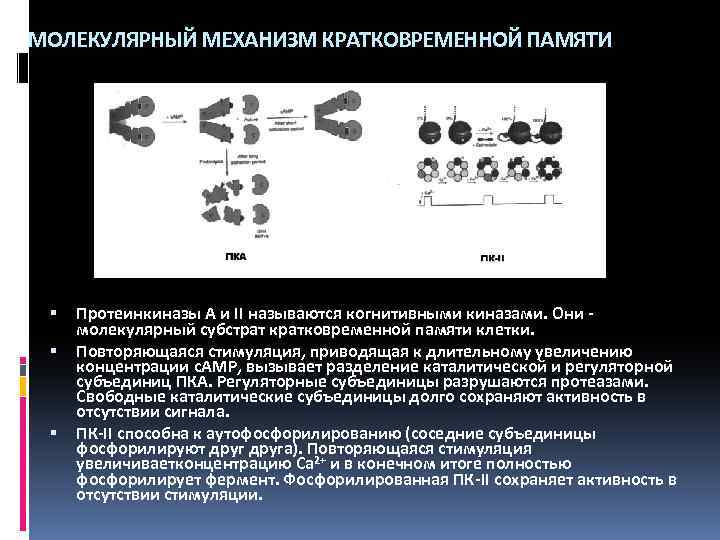
МОЛЕКУЛЯРНЫЙ МЕХАНИЗМ КРАТКОВРЕМЕННОЙ ПАМЯТИ Протеинкиназы А и II называются когнитивными киназами. Они молекулярный субстрат кратковременной памяти клетки. Повторяющаяся стимуляция, приводящая к длительному увеличению концентрации c. AMP, вызывает разделение каталитической и регуляторной субъединиц ПКА. Регуляторные субъединицы разрушаются протеазами. Свободные каталитические субъединицы долго сохраняют активность в отсутствии сигнала. ПК-II способна к аутофосфорилированию (соседние субъединицы фосфорилируют друга). Повторяющаяся стимуляция увеличиваетконцентрацию Ca 2+ и в конечном итоге полностью фосфорилирует фермент. Фосфорилированная ПК-II сохраняет активность в отсутствии стимуляции.

ФОСФАТАЗЫ Ферменты, отщепляющие остатки фосфата (присоединенные киназами) от молекул. Осуществляют функцию противоположную киназам. Отменяют то, что сделали киназы. В клетке прикреплены к белковым регуляторам. Основные фосфатазы в нейроне: Фосфатаза 1. Фосфатаза 2 А. Фосфатаза 2 B или кальценеврин.

СВОЙСТВА ФОСФАТАЗЫ-1 И КАЛЬЦЕНЕВРИНА Фосфатаза-1 имеет натуральный белок-ингибитор: DARPP-32 (дофамин и ц. АМФ регулируемый фосфопротеин). Кальценеврин – тетрамер (2 А и 2 B субъединицы). Имеет центр связывания Ca 2+-КМ комплекса. Частичная активация присоединении Ca 2+, а сильная – при связывании комплекса Ca 2+-КМ. Слабая и низкочастотная стимуляция активирует преимущественно кальценеврин, а сильная и высокочастотная – кальценеврин и ПК-II.

DARPP-32 И МОЛЕКУЛЯРНЫЙ МЕХАНИЗМ ИНТЕГРАЦИИ DARPP-32 фосфопротеин участвует во внутриклеточной интеграции сигналов с рецепторов D 1 и NMDA. Стимуляция D 1 рецептора активирует АЦ, увеличивает уровень ц. АМФ и активность ПКА. Это вызывает фосфорилирование DARPP-32. Стимуляция NMDA рецептора увеличивает уровень Ca 2+ и активирует кальценеврин, который дефосфорилирует DARPP-32 -P. Фосфорилированный белок ингибирует фосфатазу-1 и тем самым регулирует процессы в клетке.

РОЛЬ ВТОРИЧНЫХ ПОСРЕДНИКОВ Вторичные посредники c. AMP и Ca 2+ осуществляют связь между мембранными рецепторами и процессами в цитоплазме. Любой сигнал с рецептора перекодируется в концентрации этих соединений. Регуляторную функцию вторичные посредники осуществляют через активацию протеинкиназ и фосфатаз. Активированные киназы и фосфатазы изменяют функциональные свойства и активность ферментов, рецепторов и ионных каналов. Протеинкиназы и фосфатазы участвуют в клеточных механизмах кратковременной памяти и интеграции.

ИНТЕРФЕЙС МЕЖДУ ЦИТОПЛАЗМОЙ И ЯДРОМ Длительное сохранение изменений, необходимое для долговременной памяти, осуществляется через изменение экспрессии генов. Вторичные посредники, изменяя функцию клетки, не могут непосредственно влиять на экспрессию генов. Имеется интерфейс, передающий изменения в цитоплазме ядру. Он включает третичные посредники – белковые транскрипционные факторы. Эти белки связываются специфическими участками ДНК и взаимодействуя с РНК полимеразой II инициируют транскрипцию. Наиболее известны транскрипционные факторы CREB и AP-1. Белки быстрого ответа Fos, Fra, Jun.
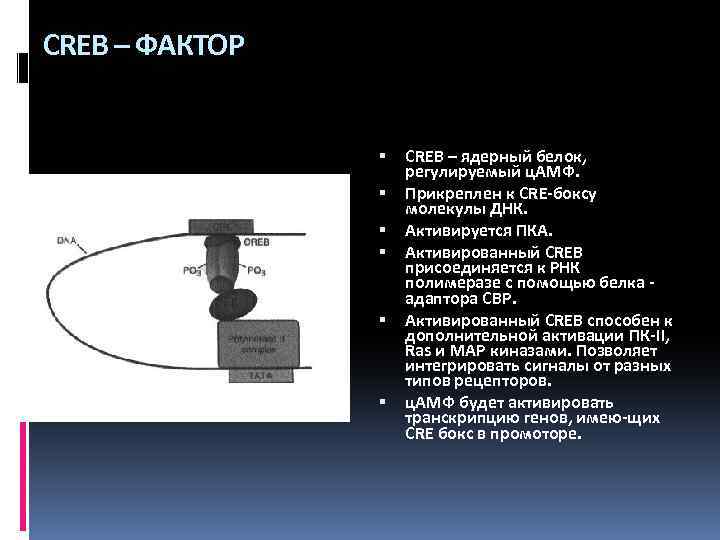
CREB – ФАКТОР CREB – ядерный белок, регулируемый ц. АМФ. Прикреплен к CRE-боксу молекулы ДНК. Активируется ПКА. Активированный CREB присоединяется к РНК полимеразе с помощью белка адаптора CBP. Активированный CREB способен к дополнительной активации ПК-II, Ras и MAP киназами. Позволяет интегрировать сигналы от разных типов рецепторов. ц. АМФ будет активировать транскрипцию генов, имею-щих CRE бокс в промоторе.
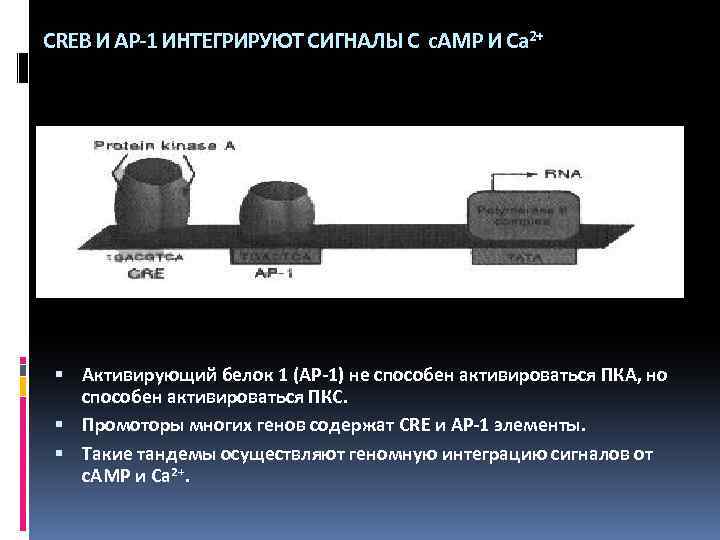
CREB И AP-1 ИНТЕГРИРУЮТ СИГНАЛЫ С c. AMP И Ca 2+ Активирующий белок 1 (AP-1) не способен активироваться ПКА, но способен активироваться ПКС. Промоторы многих генов содержат CRE и AP-1 элементы. Такие тандемы осуществляют геномную интеграцию сигналов от c. AMP и Ca 2+.

ФАКТОРЫ БЫСТРОГО ОТВЕТА В РЕГУЛЯЦИИ ЭКСПРЕССИИ ГЕНОВ Белки быстрого ответа способны регулировать экспрессию генов либо непосредственно связываясь с AP-1 боксом, либо образуя комплексы с CREB.

ЗАКЛЮЧЕНИЕ Интерфейс нейрона перекодирует информацию, содержащуюся в пакетах медиаторов, во внутриклеточную концентрацию вторичных посредников, c. AMP и Ca++. Далее протеинкиназы и фосфатазы преобразуют концентрацию вторичных посредников в интенсивности внутриклеточных процессов. Третичные посредники преобразуют концентрации вторичных посредников в процессы активации и репрессии генов. Взаимодействие регуляторных белков осуществляет интеграцию сигналов на уровне клетки. Изменения активности ферментов, рецепторов и ионных каналов, сохраняются длительное время и служат молекулярным механизмом памяти.
Л2.ppt