Отбор и дрейф-15.ppt
- Количество слайдов: 33
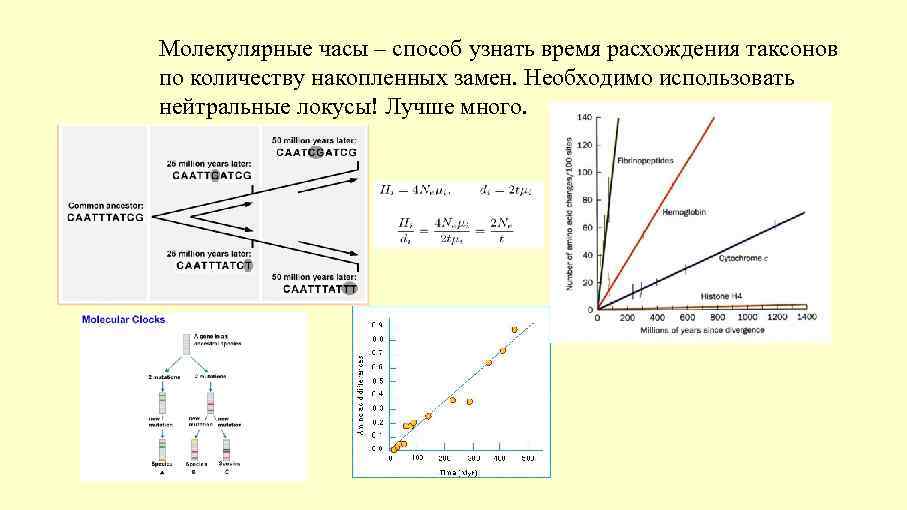
Молекулярные часы – способ узнать время расхождения таксонов по количеству накопленных замен. Необходимо использовать нейтральные локусы! Лучше много.

U 0 Количество мутаций на гамету на локус на поколение, Ne – эффективная численность популяции Тогда количество новых мутаций будет U 0 *2 Ne, поскольку в популяции есть 2 Ne копий генов Вероятность фиксации новой мутации при дрейфе равна ее частоте p, p=1/ 2 Ne Таким образом, количество вновь возникших нейтральных мутаций, которые появляются в каждом Поколении и когда-нибудь зафиксируются
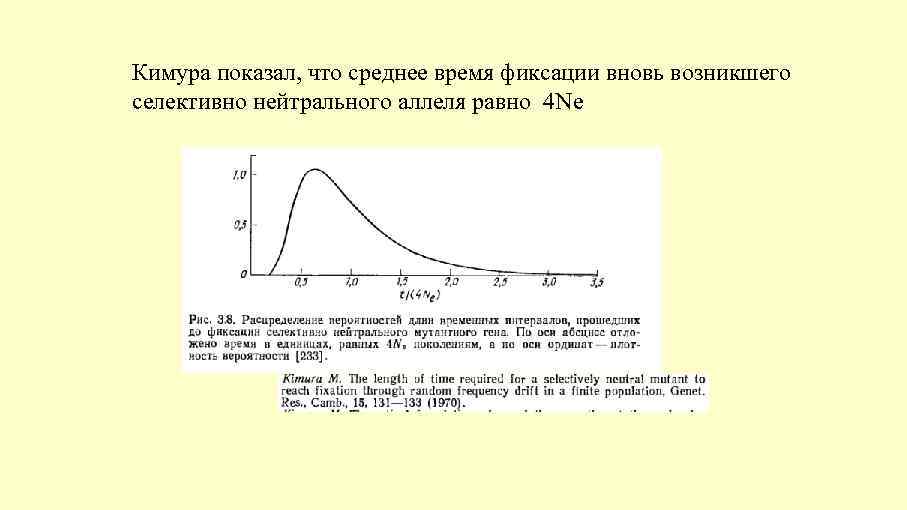
Кимура показал, что среднее время фиксации вновь возникшего селективно нейтрального аллеля равно 4 Ne

Коалесценция Каждая пара аллелей в популяции имеет общего предка – т. е. они являются потомками одной копии аллеля, существовавшей несколько поколений назад. Точка, в которой находится общий предок всех нынешних копий, наз. точкой коалесценции. Потомки всех остальных живших в то время копий вымерли в силу отбора или дрейфа. Точка коалесценции – своя для каждого гена! t=2 Ne – время, за которое два случайно выбранных аллеля придут к одному предку под действием только дрейфа
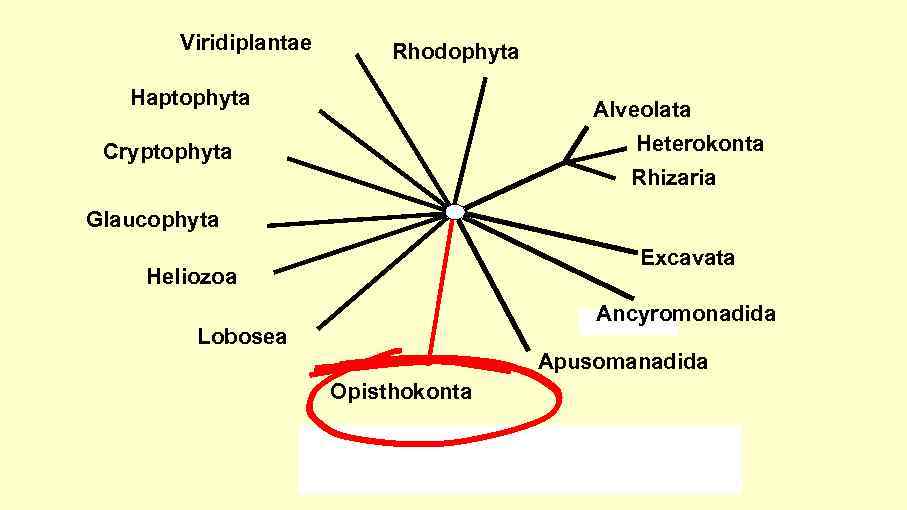
Viridiplantae Rhodophyta Haptophyta Alveolata Heterokonta Cryptophyta Rhizaria Glaucophyta Excavata Heliozoa Ancyromonadida Lobosea Apusomanadida Opisthokonta
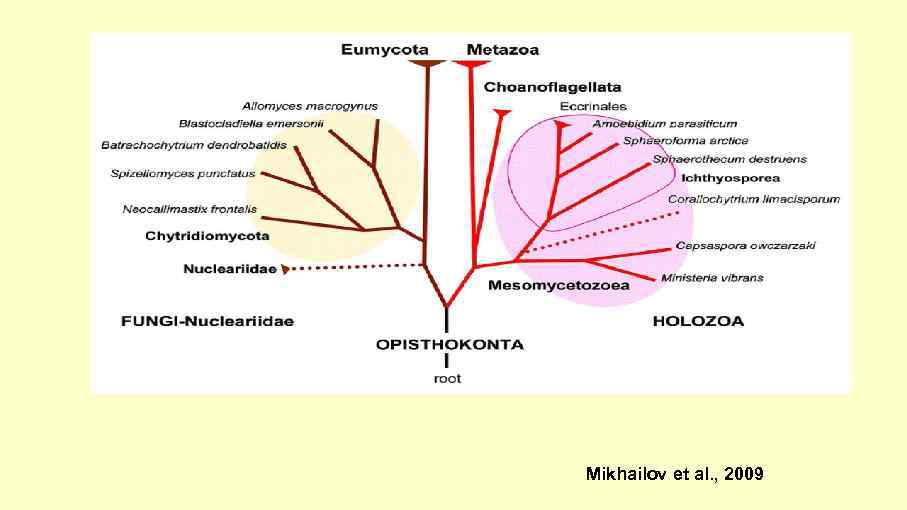
Mikhailov et al. , 2009
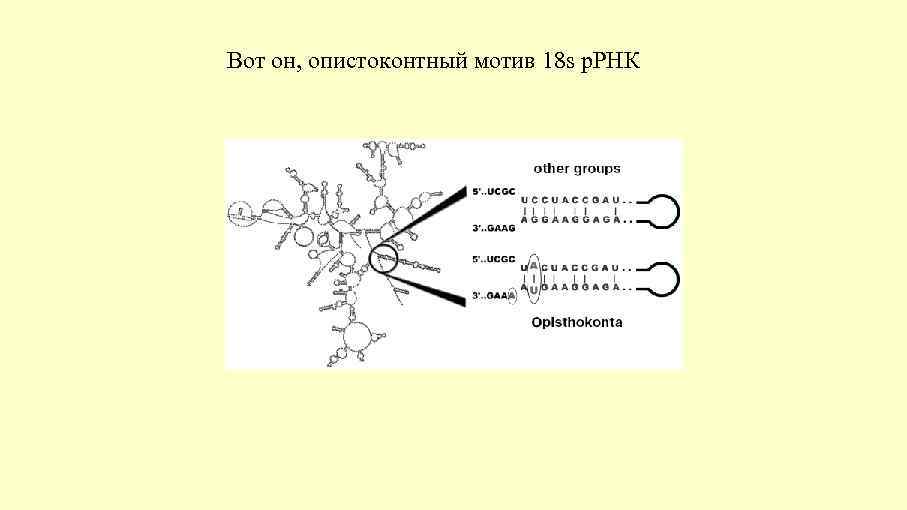
Вот он, опистоконтный мотив 18 s р. РНК
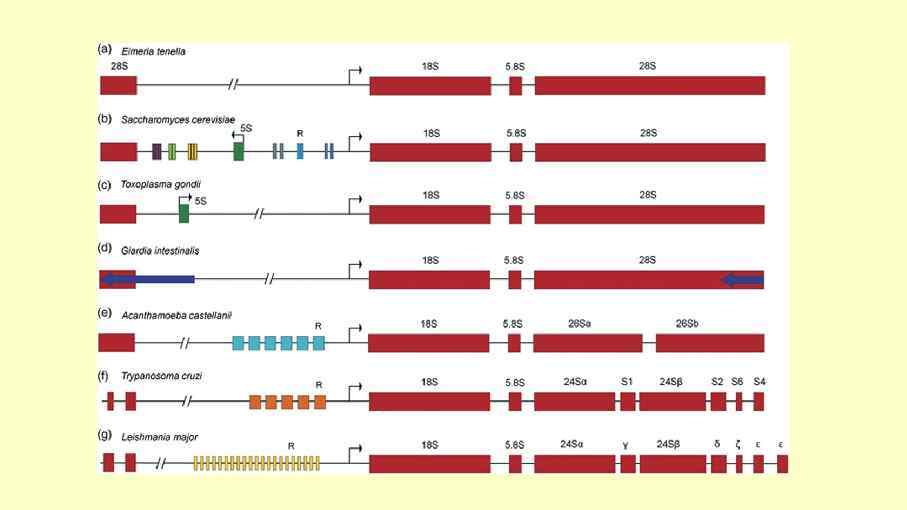
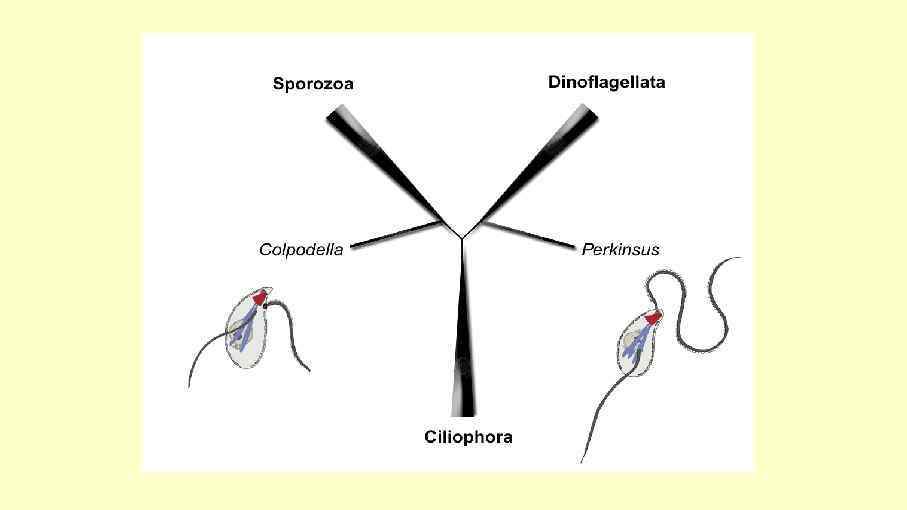
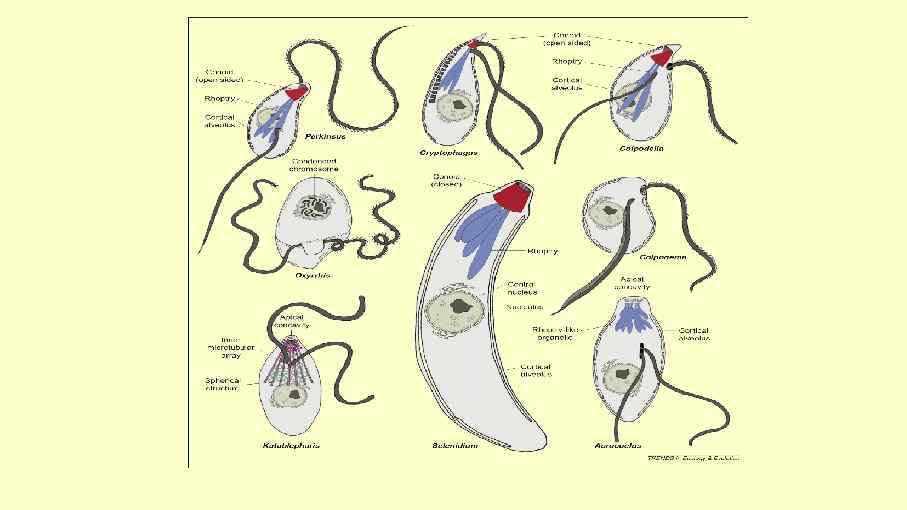

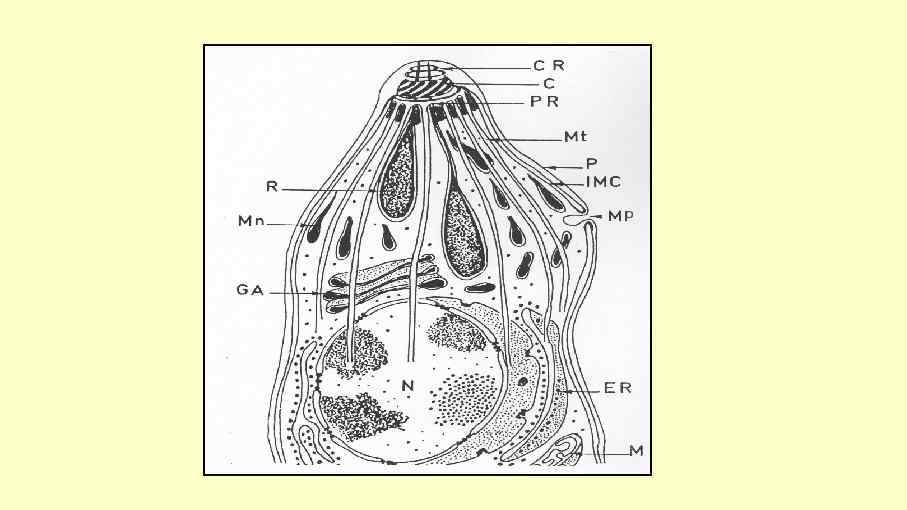
Colpodella pontica
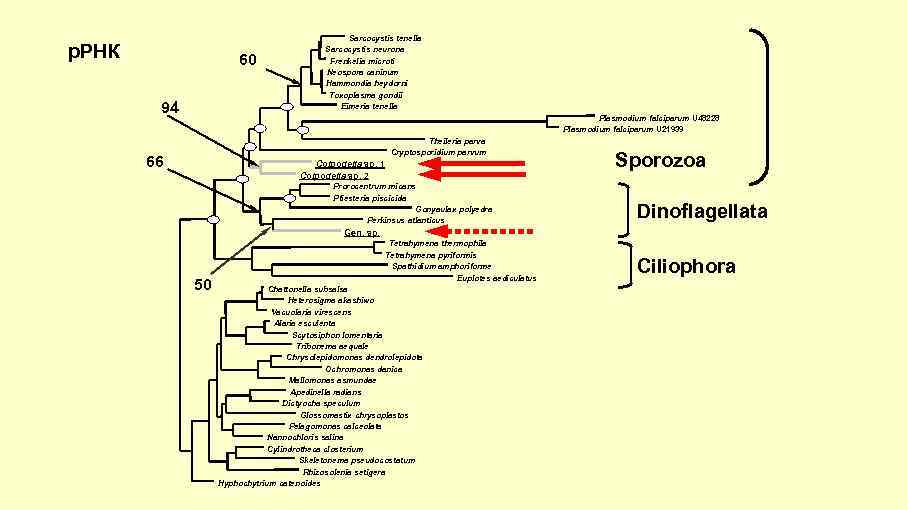
р. РНК 60 94 Sarcocystis tenella Sarcocystis neurona Frenkelia microti Neospora caninum Hammondia heydorni Toxoplasma gondii Eimeria tenella Plasmodium falciparum U 48228 Plasmodium falciparum U 21939 Theileria parva Cryptosporidium parvum 66 Colpodella sp. 1 Colpodella sp. 2 Prorocentrum micans Pfiesteria piscicida Gonyaulax polyedra Perkinsus atlanticus Sporozoa Dinoflagellata Gen. sp. 50 Tetrahymena thermophila Tetrahymena pyriformis Spathidium amphoriforme Euplotes aediculatus Chattonella subsalsa Heterosigma akashiwo Vacuolaria virescens Alaria esculenta Scytosiphon lomentaria Tribonema aequale Chrysolepidomonas dendrolepidota Ochromonas danica Mallomonas asmundae Apedinella radians Dictyocha speculum Glossomastix chrysoplastos Pelagomonas calceolata Nannochloris salina Cylindrotheca closterium Skeletonema pseudocostatum Rhizosolenia setigera Hyphochytrium catenoides Ciliophora
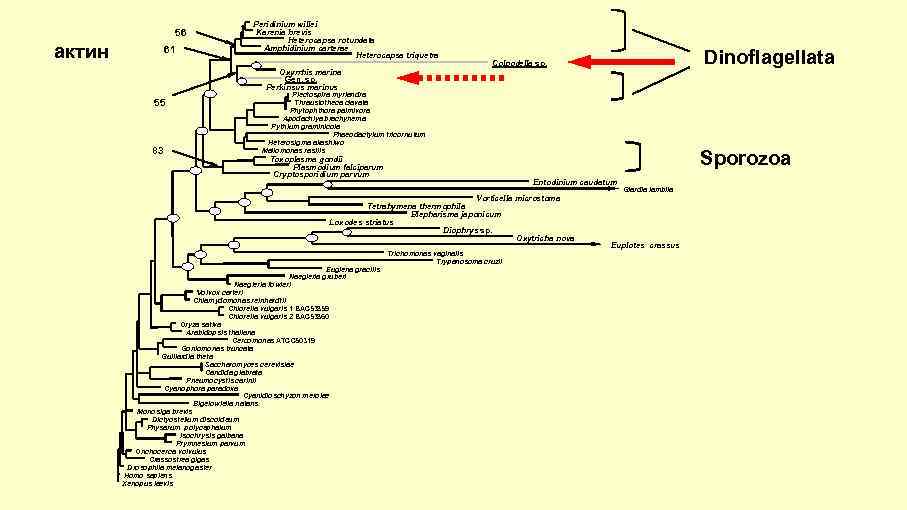
56 актин 61 Peridinium willei Karenia brevis Heterocapsa rotundata Amphidinium carterae Heterocapsa triquetra Oxyrrhis marina Gen. sp. Perkinsus marinus 55 83 Dinoflagellata Colpodella sp. Plectospira myriandra Thraustotheca clavata Phytophthora palmivora Apodachlya brachynema Pythium graminicola Phaeodactylum tricornutum Heterosigma akashiwo Mallomonas rasilis Sporozoa Toxoplasma gondii Plasmodium falciparum Cryptosporidium parvum Entodinium caudatum Giardia lamblia Vorticella microstoma Tetrahymena thermophila Blepharisma japonicum Loxodes striatus Diophrys sp. Trichomonas vaginalis Trypanosoma cruzii Euglena gracilis Naegleria gruberi Naegleria fowleri Volvox carteri Chlamydomonas reinhardtii Chlorella vulgaris 1 BAC 53859 Chlorella vulgaris 2 BAC 53860 Oryza sativa Arabidopsis thaliana Cercomonas ATCC 50319 Goniomonas truncata Guillardia theta Saccharomyces cerevisiae Candida glabrata Pneumocystis carinii Cyanophora paradoxa Cyanidioschyzon merolae Bigelowiella natans Monosiga brevis Dictyostelium discoideum Physarum polycephalum Isochrysis galbana Prymnesium parvum Onchocerca volvulus Crassostrea gigas Drosophila melanogaster Homo sapiens Xenopus laevis Oxytricha nova Euplotes crassus
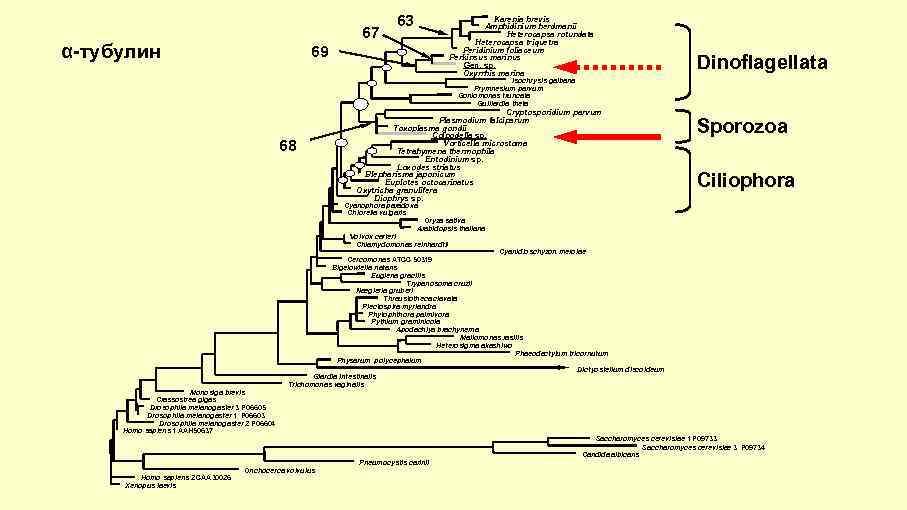
67 α-тубулин 63 Karenia brevis Amphidinium herdmanii Heterocapsa rotundata Heterocapsa triquetra Peridinium foliaceum Perkinsus marinus Gen. sp. Oxyrrhis marina 69 Dinoflagellata Isochrysis galbana Prymnesium parvum Goniomonas truncata Guillardia theta 68 Cryptosporidium parvum Plasmodium falciparum Toxoplasma gondii Colpodella sp. Vorticella microstoma Tetrahymena thermophila Entodinium sp. Loxodes striatus Blepharisma japonicum Euplotes octocarinatus Oxytricha granulifera Diophrys sp. Sporozoa Ciliophora Cyanophora paradoxa Chlorella vulgaris Oryza sativa Arabidopsis thaliana Volvox carteri Chlamydomonas reinhardtii Monosiga brevis Crassostrea gigas Drosophila melanogaster 3 P 06605 Drosophila melanogaster 1 P 06603 Drosophila melanogaster 2 P 06604 Homo sapiens 1 AAH 50637 Cyanidioschyzon merolae Cercomonas ATCC 50319 Bigelowiella natans Euglena gracilis Trypanosoma cruzii Naegleria gruberi Thraustotheca clavata Plectospira myriandra Phytophthora palmivora Pythium graminicola Apodachlya brachynema Mallomonas rasilis Heterosigma akashiwo Phaeodactylum tricornutum Physarum polycephalum Dictyostelium discoideum Giardia intestinalis Trichomonas vaginalis Pneumocystis carinii Homo sapiens 2 CAA 30026 Xenopus laevis Onchocerca volvulus Saccharomyces cerevisiae 1 P 09733 Saccharomyces cerevisiae 3 P 09734 Candida albicans
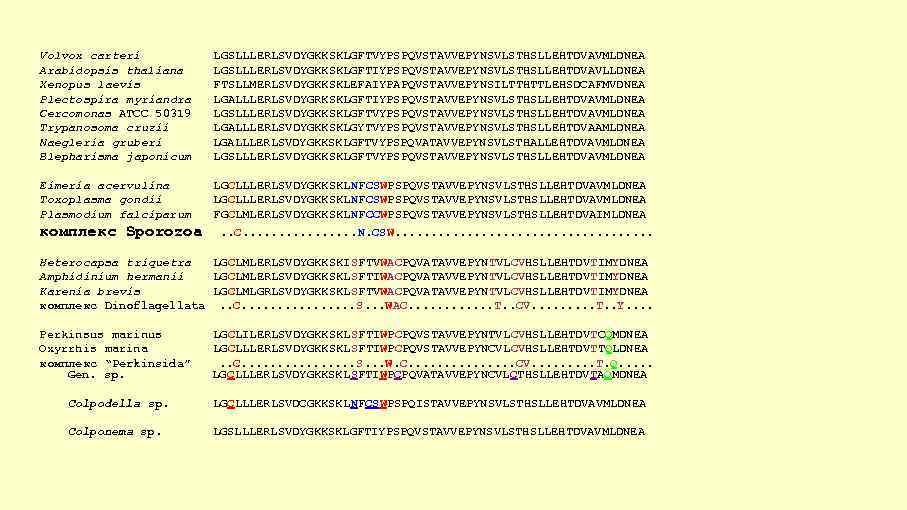
Volvox carteri Arabidopsis thaliana Xenopus laevis Plectospira myriandra Cercomonas ATCC 50319 Trypanosoma cruzii Naegleria gruberi Blepharisma japonicum LGSLLLERLSVDYGKKSKLGFTVYPSPQVSTAVVEPYNSVLSTHSLLEHTDVAVMLDNEA LGSLLLERLSVDYGKKSKLGFTIYPSPQVSTAVVEPYNSVLSTHSLLEHTDVAVLLDNEA FTSLLMERLSVDYGKKSKLEFAIYPAPQVSTAVVEPYNSILTTHTTLEHSDCAFMVDNEA LGALLLERLSVDYGRKSKLGFTIYPSPQVSTAVVEPYNSVLSTHSLLEHTDVAVMLDNEA LGSLLLERLSVDYGKKSKLGFTVYPSPQVSTAVVEPYNSVLSTHSLLEHTDVAVMLDNEA LGALLLERLSVDYGKKSKLGYTVYPSPQVSTAVVEPYNSVLSTHSLLEHTDVAAMLDNEA LGALLLERLSVDYGKKSKLGFTVYPSPQVATAVVEPYNSVLSTHALLEHTDVAVMLDNEA LGSLLLERLSVDYGKKSKLGFTVYPSPQVSTAVVEPYNSVLSTHSLLEHTDVAVMLDNEA Eimeria acervulina Toxoplasma gondii Plasmodium falciparum LGCLLLERLSVDYGKKSKLNFCSWPSPQVSTAVVEPYNSVLSTHSLLEHTDVAVMLDNEA FGCLMLERLSVDYGKKSKLNFCCWPSPQVSTAVVEPYNSVLSTHSLLEHTDVAIMLDNEA. . C. . . . N. CSW. . . . . комплекс Sporozoa Heterocapsa triquetra LGCLMLERLSVDYGKKSKISFTVWACPQVATAVVEPYNTVLCVHSLLEHTDVTIMYDNEA Amphidinium hermanii LGCLMLERLSVDYGKKSKLSFTIWACPQVATAVVEPYNTVLCVHSLLEHTDVTIMYDNEA Karenia brevis LGCLMLGRLSVDYGKKSKLSFTVWACPQVATAVVEPYNTVLCVHSLLEHTDVTIMYDNEA комплекс Dinoflagellata. . C. . . . S. . . WAC. . . T. . CV. . T. . Y. . Perkinsus marinus Oxyrrhis marina комплекс “Perkinsida” Gen. sp. LGCLILERLSVDYGKKSKLSFTIWPCPQVSTAVVEPYNTVLCVHSLLEHTDVTCQMDNEA LGCLLLERLSVDYGKKSKLSFTIWPCPQVSTAVVEPYNCVLCVHSLLEHTDVTTQLDNEA. . C. . . . S. . . W. C. . . . CV. . T. Q. . . LGCLLLERLSVDYGKKSKLSFTIWPCPQVATAVVEPYNCVLCTHSLLEHTDVTAQMDNEA Colpodella sp. LGCLLLERLSVDCGKKSKLNFCSWPSPQISTAVVEPYNSVLSTHSLLEHTDVAVMLDNEA Colponema sp. LGSLLLERLSVDYGKKSKLGFTIYPSPQVSTAVVEPYNSVLSTHSLLEHTDVAVMLDNEA
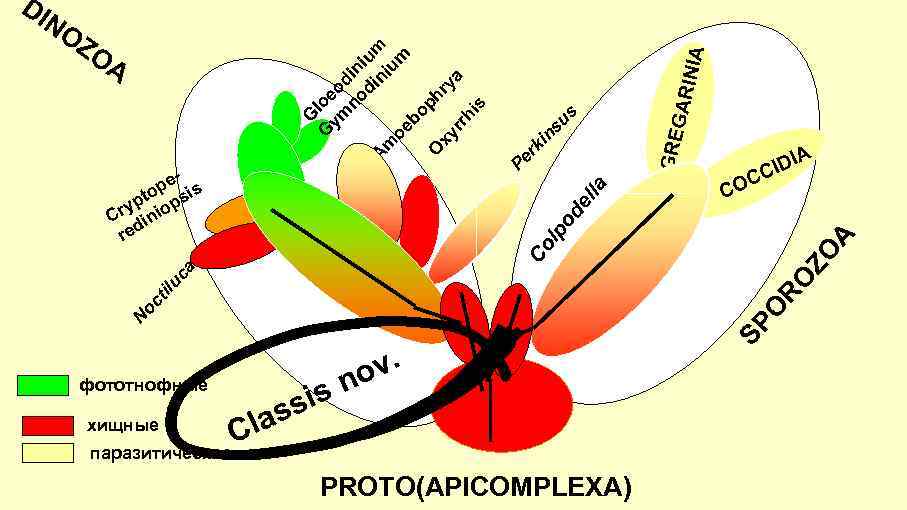
DI IA su s in A IDI C C CO фототнофные хищные паразитические v. o sn si las C PROTO(APICOMPLEXA) SP N O oc til RO uc a ZO Co A lp od el la pe is pto ops y Cr ini d re GRE GAR IN A m oe G rk n ym Pe di o eo di G m u ni bo ph O ry xy a rr hi s ni u A lo ZO m NO

Генетический дрейф ненаправленное случайное изменение частот генов в общем генофонде популяции, происходящее исключительно в силу вероятностных причин (ошибка выборки) Дрейф или отбор – вот какой вопрос всегда есть Кn/Ks test Mc. Donald-Kreitman test Tajima’s D test
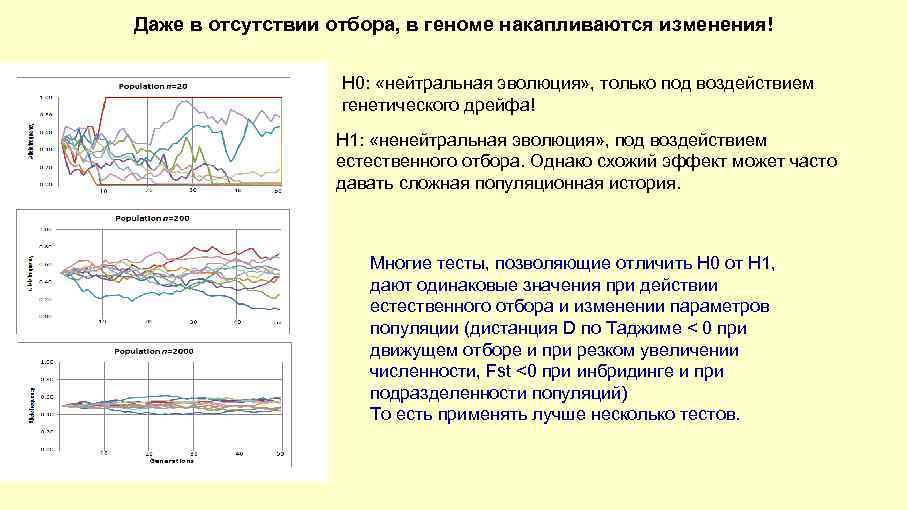
Даже в отсутствии отбора, в геноме накапливаются изменения! H 0: «нейтральная эволюция» , только под воздействием генетического дрейфа! H 1: «ненейтральная эволюция» , под воздействием естественного отбора. Однако схожий эффект может часто давать сложная популяционная история. Многие тесты, позволяющие отличить Н 0 от Н 1, дают одинаковые значения при действии естественного отбора и изменении параметров популяции (дистанция D по Таджиме < 0 при движущем отборе и при резком увеличении численности, Fst <0 при инбридинге и при подразделенности популяций) То есть применять лучше несколько тестов.
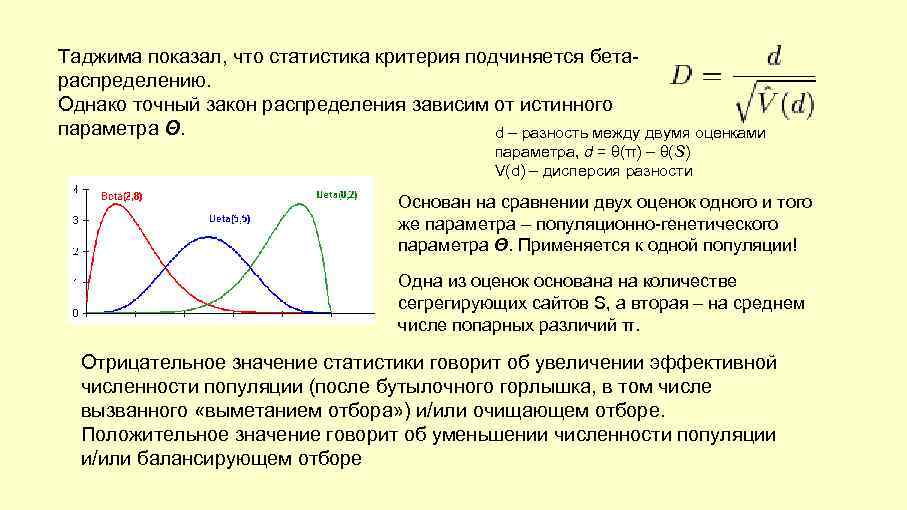
Таджима показал, что статистика критерия подчиняется бетараспределению. Однако точный закон распределения зависим от истинного параметра Θ. d – разность между двумя оценками параметра, d = θ(π) – θ(S) V(d) – дисперсия разности Основан на сравнении двух оценок одного и того же параметра – популяционно-генетического параметра Θ. Применяется к одной популяции! Одна из оценок основана на количестве сегрегирующих сайтов S, а вторая – на среднем числе попарных различий π. Отрицательное значение статистики говорит об увеличении эффективной численности популяции (после бутылочного горлышка, в том числе вызванного «выметанием отбора» ) и/или очищающем отборе. Положительное значение говорит об уменьшении численности популяции и/или балансирующем отборе

Мутационно-дрейфовое равновесие Гетерозиготность популяции – вероятность того, что два случайно выбранных аллеля различаются. H=1 -G Гомозиготность – вероятность того, что они одинаковы. Из-за дрейфа гетерозиготность теряется со скоростью 1/2 N за поколение Gt+1=1/2 N+(1 -1/2 N)Gt ΔG=1/2 N-G/2 N=H/2 N ΔH=-H/2 N – на столько уменьшается гетерозиготность за поколение НО ЕСТЬ МУТАЦИИ! ΔH=-H/2 N+2 u. G При больших u H стремится к 1
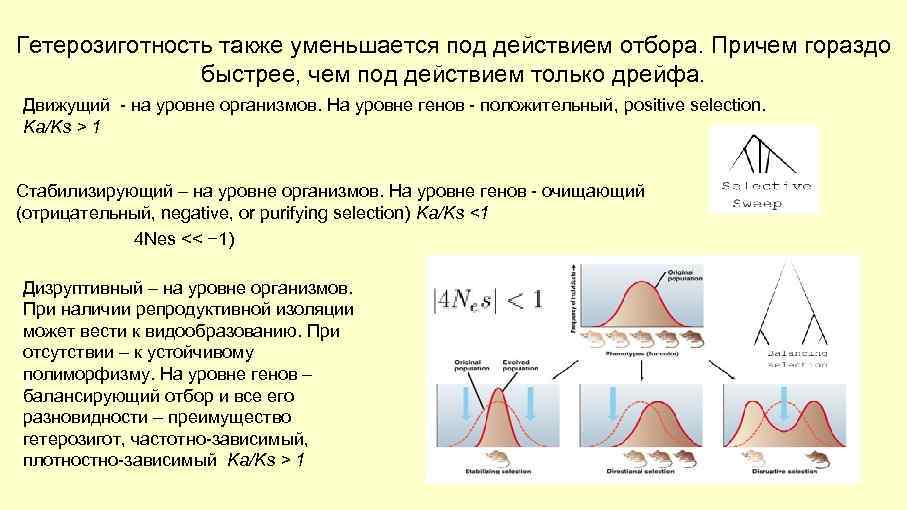
Гетерозиготность также уменьшается под действием отбора. Причем гораздо быстрее, чем под действием только дрейфа. Движущий - на уровне организмов. На уровне генов - положительный, positive selection. Ka/Ks > 1 Стабилизирующий – на уровне организмов. На уровне генов - очищающий (отрицательный, negative, or purifying selection) Ka/Ks <1 4 Nes << − 1) Дизруптивный – на уровне организмов. При наличии репродуктивной изоляции может вести к видообразованию. При отсутствии – к устойчивому полиморфизму. На уровне генов – балансирующий отбор и все его разновидности – преимущество гетерозигот, частотно-зависимый, плотностно-зависимый Ka/Ks > 1

Как определить наличие отбора и его разновидность Отношение несинонимичных замен к синонимичным (Ka/Ks) Ka (или KN) – среднее число несинонимичных замен, меняющих аминокислоту Ks – среднее число синонимичных замен Ka/Ks > 1 – положительный отбор Ka/Ks = 1 – нет отбора Ka/Ks <1 – очищающий отбор 4 Nes << − 1) Применяется при сравнении разошедшихся последовательностей – ортологов или паралогов. Сравниваются обычно разные виды или разные копии одного гена в одном виде.
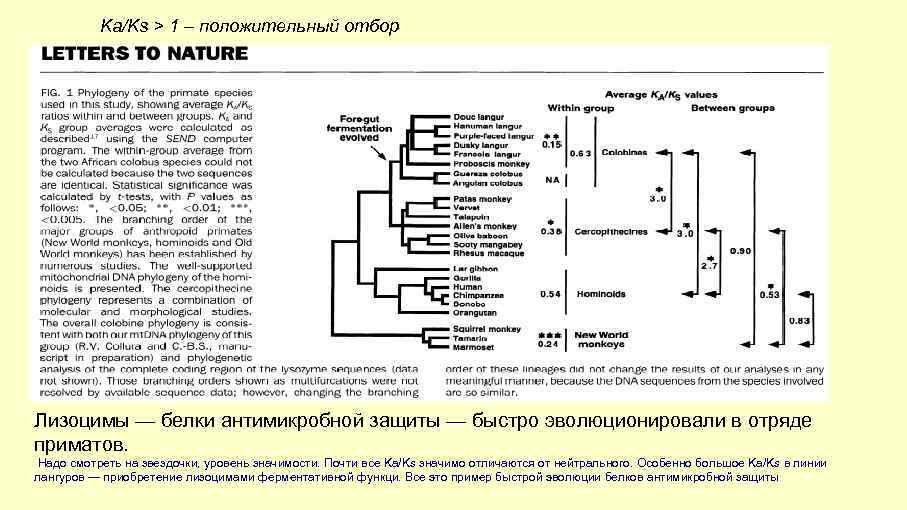
Ka/Ks > 1 – положительный отбор Лизоцимы — белки антимикробной защиты — быстро эволюционировали в отряде приматов. Надо смотреть на звездочки, уровень значимости. Почти все Ka/Ks значимо отличаются от нейтрального. Особенно большое Ka/Ks в линии лангуров — приобретение лизоцимами ферментативной функци. Все это пример быстрой эволюции белков антимикробной защиты

Тест Мак. Дональда-Крейтмана – сравнение доли синонимичных и несинонимичных точечных мутаций среди полиморфных и дивергировавших локусов. Фиксированные Полиморфные Синонимичные Ds Ps Несинонимичные Dn Pn Dn/Ds>Pn/Ps – указание на положительный отбор Фиксированные Полиморфные Синонимичные 17 42 Несинонимичные 7 7/17>2/42 2 Данные из статьи Mc. Donald, Kreitman, 1991 по заменам в гене алкогольдегидрогеназы у дрозофил.
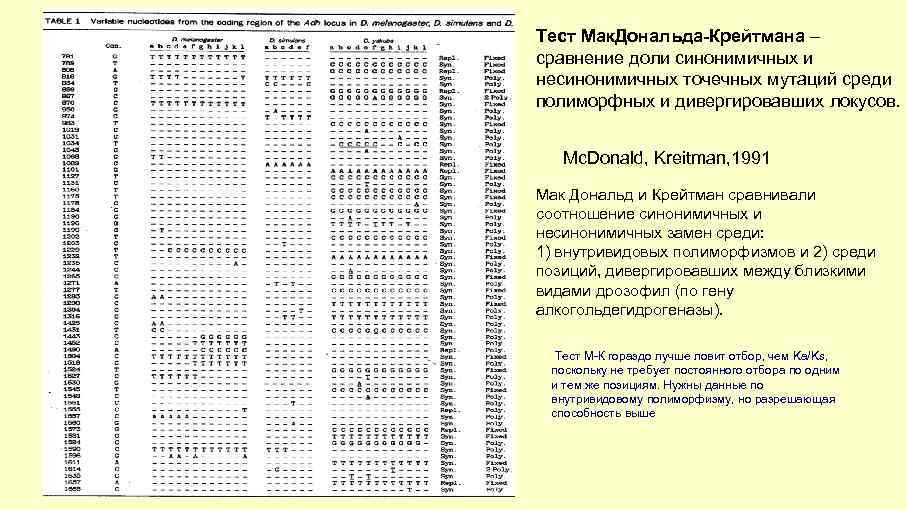
Тест Мак. Дональда-Крейтмана – сравнение доли синонимичных и несинонимичных точечных мутаций среди полиморфных и дивергировавших локусов. Mc. Donald, Kreitman, 1991 Мак Дональд и Крейтман сравнивали соотношение синонимичных и несинонимичных замен среди: 1) внутривидовых полиморфизмов и 2) среди позиций, дивергировавших между близкими видами дрозофил (по гену алкогольдегидрогеназы). Тест М-К гораздо лучше ловит отбор, чем Ka/Ks, поскольку не требует постоянного отбора по одним и тем же позициям. Нужны данные по внутривидовому полиморфизму, но разрешающая способность выше
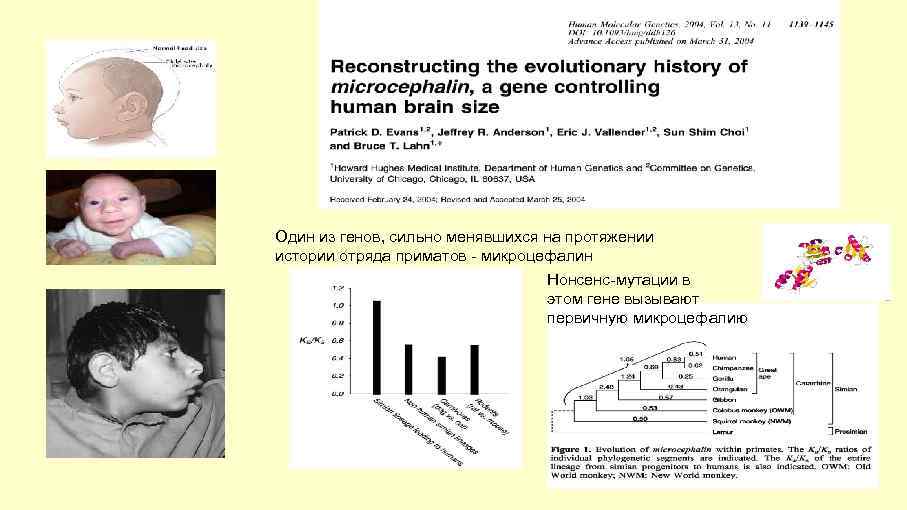
Один из генов, сильно менявшихся на протяжении истории отряда приматов - микроцефалин Нонсенс-мутации в этом гене вызывают первичную микроцефалию
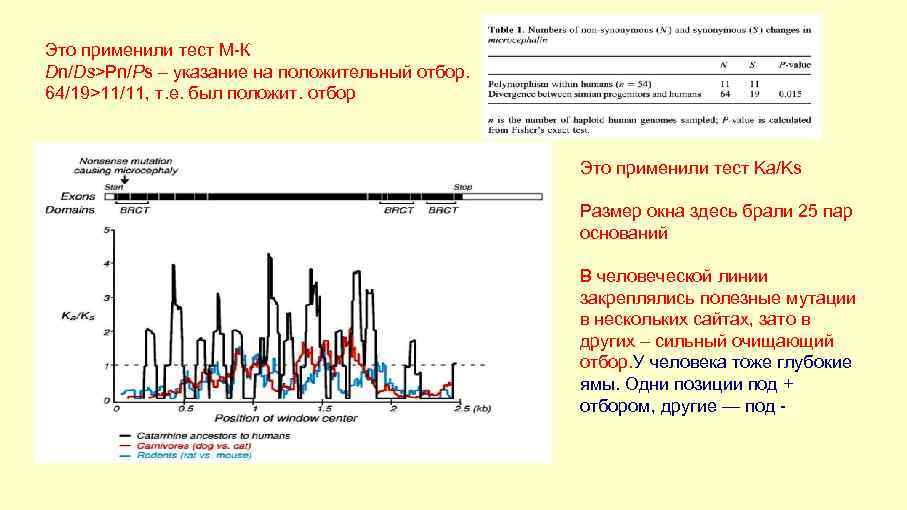
Это применили тест М-К Dn/Ds>Pn/Ps – указание на положительный отбор. 64/19>11/11, т. е. был положит. отбор Это применили тест Ka/Ks Размер окна здесь брали 25 пар оснований В человеческой линии закреплялись полезные мутации в нескольких сайтах, зато в других – сильный очищающий отбор. У человека тоже глубокие ямы. Одни позиции под + отбором, другие — под -
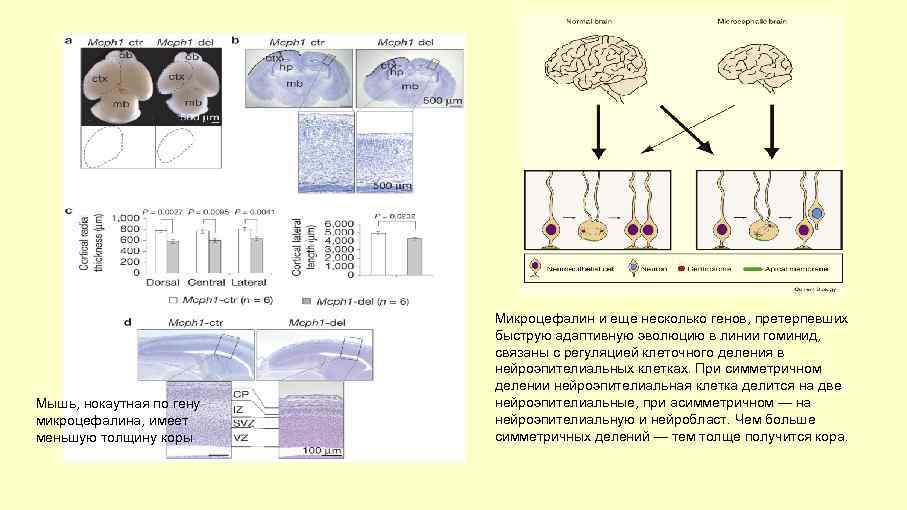
Мышь, нокаутная по гену микроцефалина, имеет меньшую толщину коры Микроцефалин и еще несколько генов, претерпевших быструю адаптивную эволюцию в линии гоминид, связаны с регуляцией клеточного деления в нейроэпителиальных клетках. При симметричном делении нейроэпителиальная клетка делится на две нейроэпителиальные, при асимметричном — на нейроэпителиальную и нейробласт. Чем больше симметричных делений — тем толще получится кора.
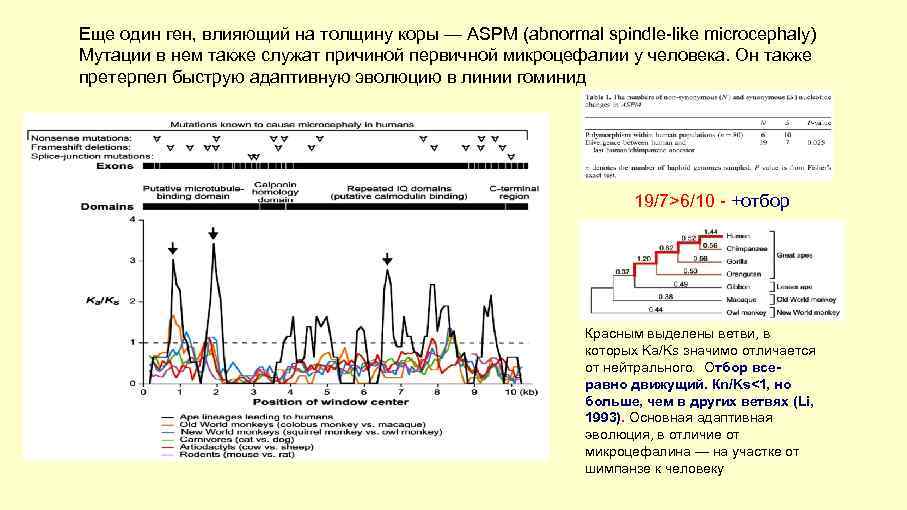
Еще один ген, влияющий на толщину коры — ASPM (abnormal spindle-like microcephaly) Мутации в нем также служат причиной первичной микроцефалии у человека. Он также претерпел быструю адаптивную эволюцию в линии гоминид 19/7>6/10 - +отбор Красным выделены ветви, в которых Ka/Ks значимо отличается от нейтрального. Отбор всеравно движущий. Кn/Ks<1, но больше, чем в других ветвях (Li, 1993). Основная адаптивная эволюция, в отличие от микроцефалина — на участке от шимпанзе к человеку
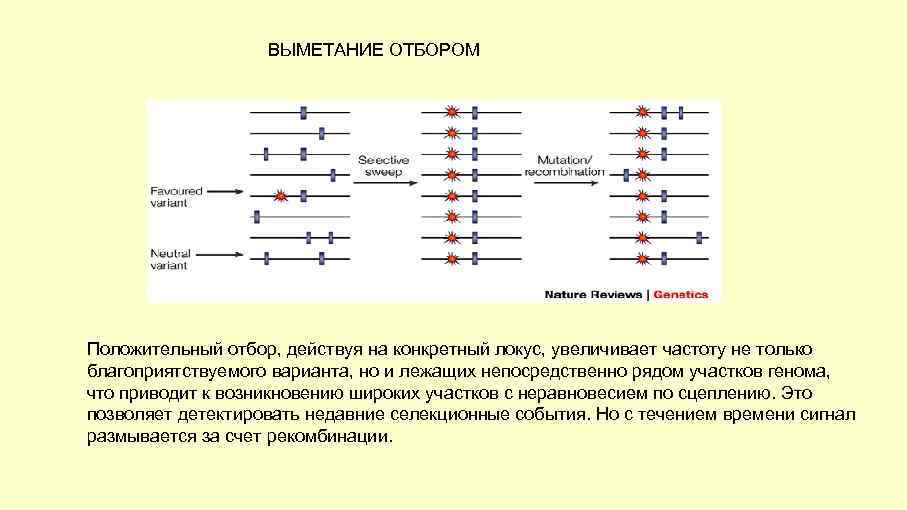
ВЫМЕТАНИЕ ОТБОРОМ Положительный отбор, действуя на конкретный локус, увеличивает частоту не только благоприятствуемого варианта, но и лежащих непосредственно рядом участков генома, что приводит к возникновению широких участков с неравновесием по сцеплению. Это позволяет детектировать недавние селекционные события. Но с течением времени сигнал размывается за счет рекомбинации.
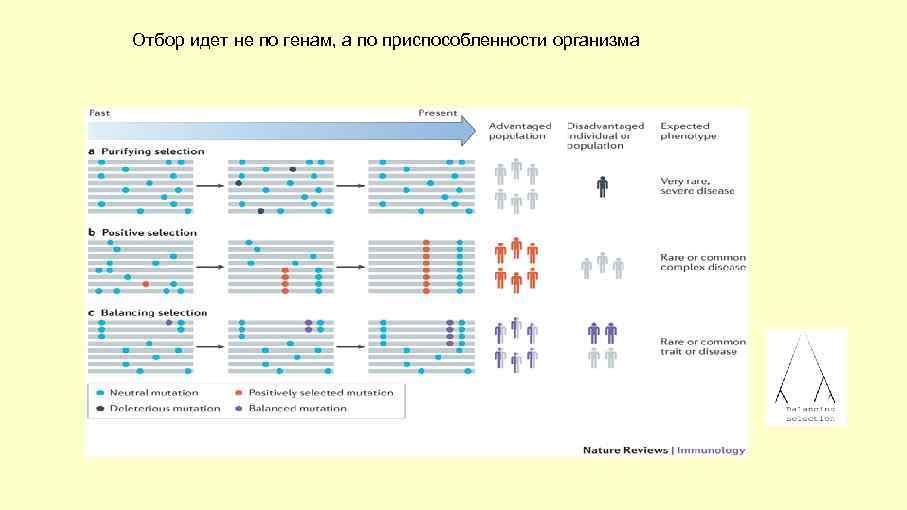
Отбор идет не по генам, а по приспособленности организма
Отбор и дрейф-15.ppt