13.pptx
- Количество слайдов: 48
 Молекулярнокинетическая теория (МКТ) 1
Молекулярнокинетическая теория (МКТ) 1
 Все вещества – жидкие, твердые и газообразные – образованы из мельчайших частиц – молекул, которые сами состоят из атомов ( «элементарных молекул» ). Молекулы химического вещества могут быть простыми и сложными и состоять из одного или нескольких атомов. Молекулы и атомы представляют собой электрически 2
Все вещества – жидкие, твердые и газообразные – образованы из мельчайших частиц – молекул, которые сами состоят из атомов ( «элементарных молекул» ). Молекулы химического вещества могут быть простыми и сложными и состоять из одного или нескольких атомов. Молекулы и атомы представляют собой электрически 2
 Атомы и молекулы находятся в непрерывном хаотическом движении. Частицы взаимодействуют друг с другом силами, имеющими электрическую природу. Гравитационное взаимодействие между частицами пренебрежимо мало. 3
Атомы и молекулы находятся в непрерывном хаотическом движении. Частицы взаимодействуют друг с другом силами, имеющими электрическую природу. Гравитационное взаимодействие между частицами пренебрежимо мало. 3
 В МКТ существуют два метода изучения: статистический и термодинамический. Оба метода предполагают, что рассматриваемая макросистема состоит из огромного числа элементов. 4
В МКТ существуют два метода изучения: статистический и термодинамический. Оба метода предполагают, что рассматриваемая макросистема состоит из огромного числа элементов. 4
 Относительной молекулярной (или атомной) массой вещества Мr называют отношение массы молекулы (или атома) m 0 данного вещества к 1/12 массы атома углерода m 0 c. В молекулярно-кинетической теории количество вещества принято считать пропорциональным числу частиц. Единица количества вещества называется молем (моль). 5
Относительной молекулярной (или атомной) массой вещества Мr называют отношение массы молекулы (или атома) m 0 данного вещества к 1/12 массы атома углерода m 0 c. В молекулярно-кинетической теории количество вещества принято считать пропорциональным числу частиц. Единица количества вещества называется молем (моль). 5
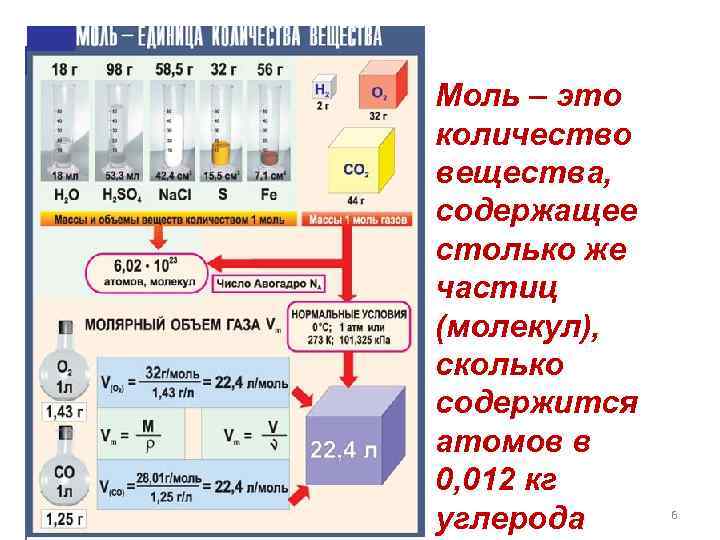 Моль – это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов в 0, 012 кг углерода 6
Моль – это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов в 0, 012 кг углерода 6
 В одном моле любого вещества содержится одно и то же число частиц (молекул). Это число называется постоянной Авогадро NA=6. 02 1023 моль1. Количество вещества ν определяется как отношение числа N частиц (молекул) вещества к постоянной Авогадро NA 7
В одном моле любого вещества содержится одно и то же число частиц (молекул). Это число называется постоянной Авогадро NA=6. 02 1023 моль1. Количество вещества ν определяется как отношение числа N частиц (молекул) вещества к постоянной Авогадро NA 7
 8
8
 Молярной массой μ вещества называют массу вещества, взятого в количестве 1 моля. Молярная масса равна произведению массы m 0 одной молекулы данного вещества на постоянную Авогадро: 9
Молярной массой μ вещества называют массу вещества, взятого в количестве 1 моля. Молярная масса равна произведению массы m 0 одной молекулы данного вещества на постоянную Авогадро: 9
 Идеальным газом называется газ: молекулы - материальные точки, то есть расстояния между ними намного превосходят их размеры; молекулы между собой не взаимодействуют; единственный вид их взаимодействий – абсолютно упругий удар; между столкновениями молекулы движутся прямолинейно и равномерно. Модель идеального газа достаточно хорошо описывает поведение реальных 10
Идеальным газом называется газ: молекулы - материальные точки, то есть расстояния между ними намного превосходят их размеры; молекулы между собой не взаимодействуют; единственный вид их взаимодействий – абсолютно упругий удар; между столкновениями молекулы движутся прямолинейно и равномерно. Модель идеального газа достаточно хорошо описывает поведение реальных 10
 Равновесным состоянием системы называется такое состояние, при котором все параметры системы имеют определенные значения, остающиеся при неизменных внешних условиях постоянными сколь угодно долго. Процесс, состоящий из непрерывной последовательности равновесных состояний, называется, равновесны процессом. 11
Равновесным состоянием системы называется такое состояние, при котором все параметры системы имеют определенные значения, остающиеся при неизменных внешних условиях постоянными сколь угодно долго. Процесс, состоящий из непрерывной последовательности равновесных состояний, называется, равновесны процессом. 11
 Состояние некоторой массы газа определятся значениями трех параметров: давления р, объема V и температуры T. Эти параметры связаны друг с другом, так что изменение одного из них влечет за собой изменение других. Данная связь может быть задана аналитически в виде функции: 12
Состояние некоторой массы газа определятся значениями трех параметров: давления р, объема V и температуры T. Эти параметры связаны друг с другом, так что изменение одного из них влечет за собой изменение других. Данная связь может быть задана аналитически в виде функции: 12
 Для идеального газа уравнение состояния принимает следующий вид: 13
Для идеального газа уравнение состояния принимает следующий вид: 13
 По закону Авогадро одинаковые количества различных идеальных газов при одинаковых условиях (давление, температура) занимают одинаковый объем. Следовательно, если количество газа равно одному молю, постоянная одинакова для всех газов. Обозначим ее Это – как R: уравнение Клайперона 14
По закону Авогадро одинаковые количества различных идеальных газов при одинаковых условиях (давление, температура) занимают одинаковый объем. Следовательно, если количество газа равно одному молю, постоянная одинакова для всех газов. Обозначим ее Это – как R: уравнение Клайперона 14
 Величина R называется универсальной газовой постоянной. Ее значение можно вычислить, подставив атмосферное давление, объем 22. 4 л и температуру 273 К: 15
Величина R называется универсальной газовой постоянной. Ее значение можно вычислить, подставив атмосферное давление, объем 22. 4 л и температуру 273 К: 15
 Уравнение состояния идеального газа, написанное для любой массы газа m: 16
Уравнение состояния идеального газа, написанное для любой массы газа m: 16
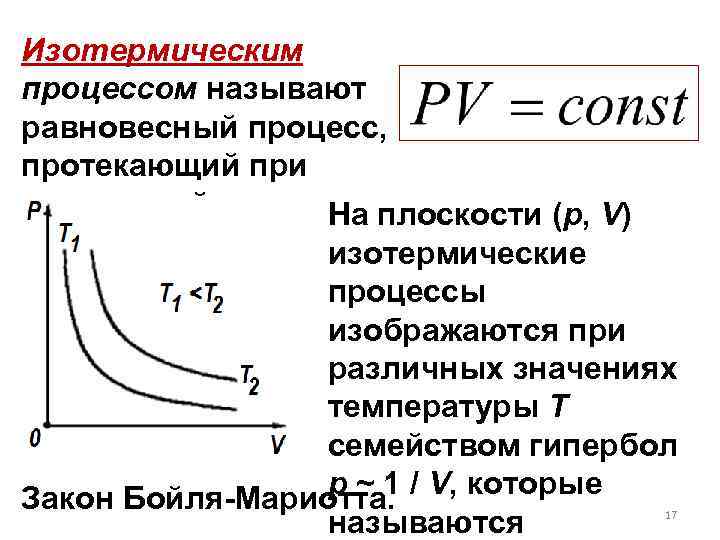 Изотермическим процессом называют равновесный процесс, протекающий при постоянной На плоскости (p, V) температуре T. изотермические процессы изображаются при различных значениях температуры T семейством гипербол p ~ 1 / V, которые Закон Бойля-Мариотта. называются 17
Изотермическим процессом называют равновесный процесс, протекающий при постоянной На плоскости (p, V) температуре T. изотермические процессы изображаются при различных значениях температуры T семейством гипербол p ~ 1 / V, которые Закон Бойля-Мариотта. называются 17
 Изохорный процесс: равновесное нагревание или охлаждение газа при постоянном объеме V и неизменном количество На плоскости (Т, р) вещества ν. изохорные процессы для заданного количества вещества ν при различных значениях объема V изображаются семейством прямых линий, которые называются изохорами. Закон Шарля 18
Изохорный процесс: равновесное нагревание или охлаждение газа при постоянном объеме V и неизменном количество На плоскости (Т, р) вещества ν. изохорные процессы для заданного количества вещества ν при различных значениях объема V изображаются семейством прямых линий, которые называются изохорами. Закон Шарля 18
 Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид: На плоскости (V, T) изобарные процессы при разных значениях давления p изображаются семейством прямых линий, которые Закон Гей-Люссака называются изобарами. 19
Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид: На плоскости (V, T) изобарные процессы при разных значениях давления p изображаются семейством прямых линий, которые Закон Гей-Люссака называются изобарами. 19
 МКТ устанавливает связи между макро- и микропараметрами идеального газа. Давление газа на стенки сосуда является результатом многочисленных ударов молекул. При каждом ударе стенка получает силовой импульс, величина которого зависит от скорости молекул и, следовательно, от энергии их движения. При огромном числе ударов создается постоянное давление газа на стенку. Число ударов зависит от 20
МКТ устанавливает связи между макро- и микропараметрами идеального газа. Давление газа на стенки сосуда является результатом многочисленных ударов молекул. При каждом ударе стенка получает силовой импульс, величина которого зависит от скорости молекул и, следовательно, от энергии их движения. При огромном числе ударов создается постоянное давление газа на стенку. Число ударов зависит от 20
 Введем некоторые упрощения: 1) все молекулы движутся по взаимно перпендикулярным направлениям; 2) скорости всех молекул Каждый элемент поверхности d. S одинаковы. непрерывно подвергается бомбардировке большим количеством молекул. В результате за время dt поверхность получает суммарный импульс dp направленный по нормали к d. S. Отношение dр к dt дает, как известно из второго закона Ньютона, силу, действующую на d. S, а отношение этой силы к 21 d. S дает давление Р.
Введем некоторые упрощения: 1) все молекулы движутся по взаимно перпендикулярным направлениям; 2) скорости всех молекул Каждый элемент поверхности d. S одинаковы. непрерывно подвергается бомбардировке большим количеством молекул. В результате за время dt поверхность получает суммарный импульс dp направленный по нормали к d. S. Отношение dр к dt дает, как известно из второго закона Ньютона, силу, действующую на d. S, а отношение этой силы к 21 d. S дает давление Р.
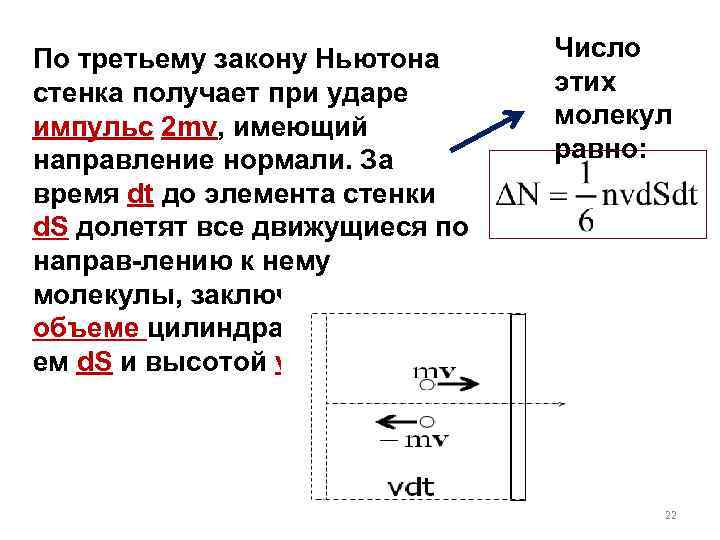 По третьему закону Ньютона стенка получает при ударе импульс 2 mv, имеющий направление нормали. За время dt до элемента стенки d. S долетят все движущиеся по направ-лению к нему молекулы, заключен-ные в объеме цилиндра с основанием d. S и высотой vdt. Число этих молекул равно: 22
По третьему закону Ньютона стенка получает при ударе импульс 2 mv, имеющий направление нормали. За время dt до элемента стенки d. S долетят все движущиеся по направ-лению к нему молекулы, заключен-ные в объеме цилиндра с основанием d. S и высотой vdt. Число этих молекул равно: 22
 n – число молекул в единице объема. Таким образом, число ударов о единицу поверхности за единицу времени будет равно: Суммарный импульс dp, сообщаемый элементу стенки d. S за время dt: 23
n – число молекул в единице объема. Таким образом, число ударов о единицу поверхности за единицу времени будет равно: Суммарный импульс dp, сообщаемый элементу стенки d. S за время dt: 23
 Отнеся импульс dp к промежутку времени dt, получим силу, действующую на d. S. Отнеся затем полученную силу к площадке d. S, получим давление газа, оказываемое им на стенки сосуда. 24
Отнеся импульс dp к промежутку времени dt, получим силу, действующую на d. S. Отнеся затем полученную силу к площадке d. S, получим давление газа, оказываемое им на стенки сосуда. 24
 Учтем выражение для кинетической энергии поступательного движения молекулы 25
Учтем выражение для кинетической энергии поступательного движения молекулы 25
 Получим ОСНОВНОЕ УРАВНЕНИЕ МКТ 26
Получим ОСНОВНОЕ УРАВНЕНИЕ МКТ 26
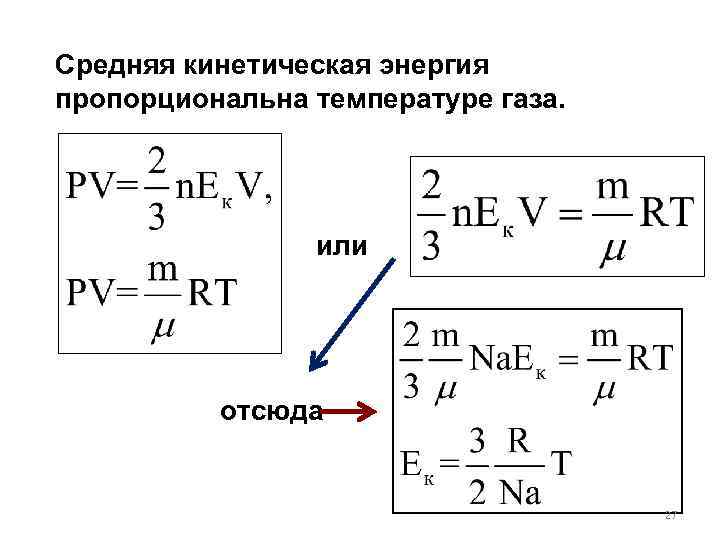 Средняя кинетическая энергия пропорциональна температуре газа. или отсюда 27
Средняя кинетическая энергия пропорциональна температуре газа. или отсюда 27
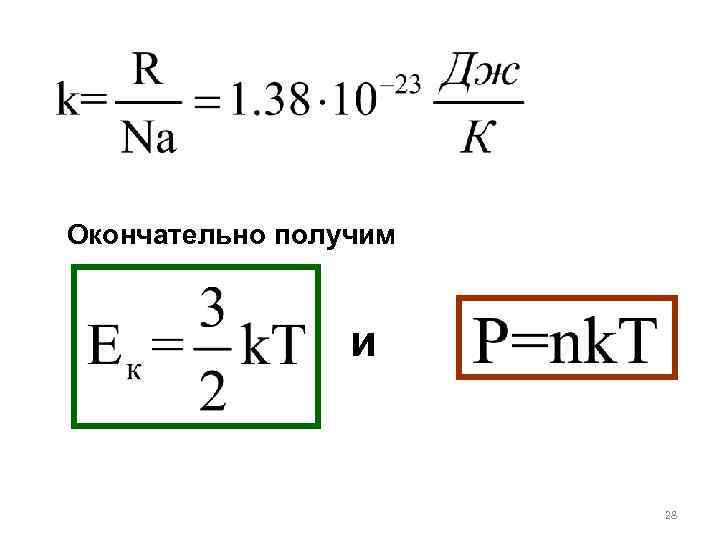 Окончательно получим и 28
Окончательно получим и 28
 Для смеси газов справедлив закон Дальтона: давление смеси идеальных газов равно сумме парциальных давлений входящих в нее газов: где k – номер газовой компоненты в смеси, Pk – ее парциальное давление, т. е. то давление, которое имел бы k–ый газ, если бы только он один занимал весь объём, занимаемый смесью. 29
Для смеси газов справедлив закон Дальтона: давление смеси идеальных газов равно сумме парциальных давлений входящих в нее газов: где k – номер газовой компоненты в смеси, Pk – ее парциальное давление, т. е. то давление, которое имел бы k–ый газ, если бы только он один занимал весь объём, занимаемый смесью. 29
 Джон Дальтон (1766 — 1844) — английский провинциальный учитель-самоучка, химик, метеоролог и естествоиспытатель. Впервые (1794) провёл исследования и описал дефект зрения, названный дальтонизмом; открыл закон парциальных давлений (1801), закон равномерного расширения газов при нагревании (1802), закон растворимости газов в жидкостях, установил закон кратных отношений (1803), обнаружил явление полимеризации, ввёл понятие 30
Джон Дальтон (1766 — 1844) — английский провинциальный учитель-самоучка, химик, метеоролог и естествоиспытатель. Впервые (1794) провёл исследования и описал дефект зрения, названный дальтонизмом; открыл закон парциальных давлений (1801), закон равномерного расширения газов при нагревании (1802), закон растворимости газов в жидкостях, установил закон кратных отношений (1803), обнаружил явление полимеризации, ввёл понятие 30
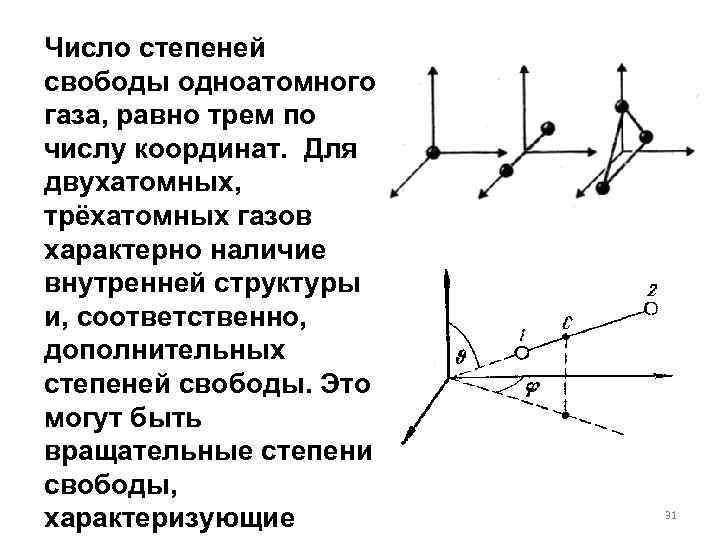 Число степеней свободы одноатомного газа, равно трем по числу координат. Для двухатомных, трёхатомных газов характерно наличие внутренней структуры и, соответственно, дополнительных степеней свободы. Это могут быть вращательные степени свободы, характеризующие 31
Число степеней свободы одноатомного газа, равно трем по числу координат. Для двухатомных, трёхатомных газов характерно наличие внутренней структуры и, соответственно, дополнительных степеней свободы. Это могут быть вращательные степени свободы, характеризующие 31
 i – сумма числа поступательных, числа вращательных и удвоенного числа колебательных степеней свободы молекулы: i=nпост + nвращ + 2 nколеб Для молекулы с жесткой связью между атомами i совпадает с числом степеней молекулы. 32
i – сумма числа поступательных, числа вращательных и удвоенного числа колебательных степеней свободы молекулы: i=nпост + nвращ + 2 nколеб Для молекулы с жесткой связью между атомами i совпадает с числом степеней молекулы. 32
 Средняя кинетическая энергия, приходящаяся при тепловом равновесии на одну степень свободы молекулы равна Таким образом, средняя энергия молекулы должна равняться: 33
Средняя кинетическая энергия, приходящаяся при тепловом равновесии на одну степень свободы молекулы равна Таким образом, средняя энергия молекулы должна равняться: 33
 В сосуде, содержащем большое число молекул, устанавливается некоторое статистическое распределение молекул по скоростям, зависящее от абсолютной температуры T. Все направления векторов скоростей молекул равноправны (равновероятны). Величины скоростей подчиняются определенной закономерности. Распределение молекул газа по величине скоростей называется распределением Максвелла. 34
В сосуде, содержащем большое число молекул, устанавливается некоторое статистическое распределение молекул по скоростям, зависящее от абсолютной температуры T. Все направления векторов скоростей молекул равноправны (равновероятны). Величины скоростей подчиняются определенной закономерности. Распределение молекул газа по величине скоростей называется распределением Максвелла. 34
 Джеймс Клерк Ма ксвелл (James Clerk Maxwell, 1831 — 1879) — британский физик и математик. Максвелл заложил основы современной классической электродинамики, ввёл в физику понятия тока смещения и электромагнитного поля, электромаг-нитной волны, кинетической давления газов, Он является теории света. установил распределение одним из основателей молекул газа по скоростям (распределение Максвелла). Максвелл одним из первых ввёл в физику статисти-ческие представления. 35
Джеймс Клерк Ма ксвелл (James Clerk Maxwell, 1831 — 1879) — британский физик и математик. Максвелл заложил основы современной классической электродинамики, ввёл в физику понятия тока смещения и электромагнитного поля, электромаг-нитной волны, кинетической давления газов, Он является теории света. установил распределение одним из основателей молекул газа по скоростям (распределение Максвелла). Максвелл одним из первых ввёл в физику статисти-ческие представления. 35
 Функция распределения молекул по скоростям обозначается f(v). Эта формула представляет собой закон распределения Максвелла по модулю скорости. Эта функция может быть нормирована на единицу: 36
Функция распределения молекул по скоростям обозначается f(v). Эта формула представляет собой закон распределения Максвелла по модулю скорости. Эта функция может быть нормирована на единицу: 36
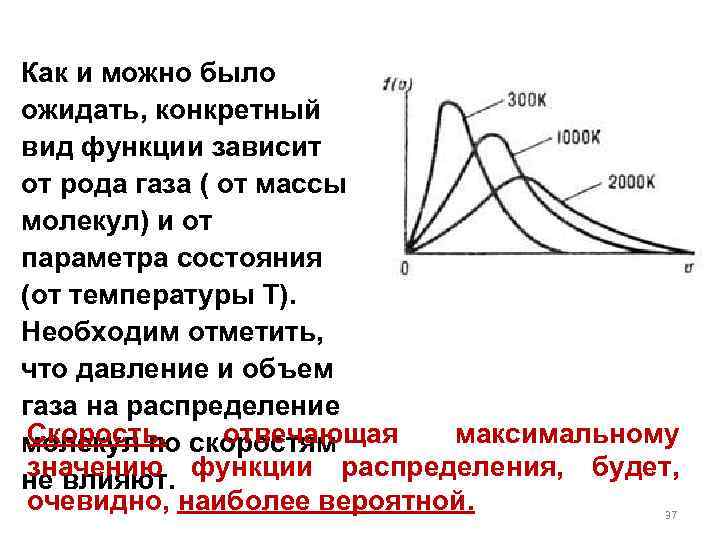 Как и можно было ожидать, конкретный вид функции зависит от рода газа ( от массы молекул) и от параметра состояния (от температуры Т). Необходим отметить, что давление и объем газа на распределение Скорость, отвечающая максимальному молекул по скоростям значению не влияют. функции распределения, будет, очевидно, наиболее вероятной. 37
Как и можно было ожидать, конкретный вид функции зависит от рода газа ( от массы молекул) и от параметра состояния (от температуры Т). Необходим отметить, что давление и объем газа на распределение Скорость, отвечающая максимальному молекул по скоростям значению не влияют. функции распределения, будет, очевидно, наиболее вероятной. 37
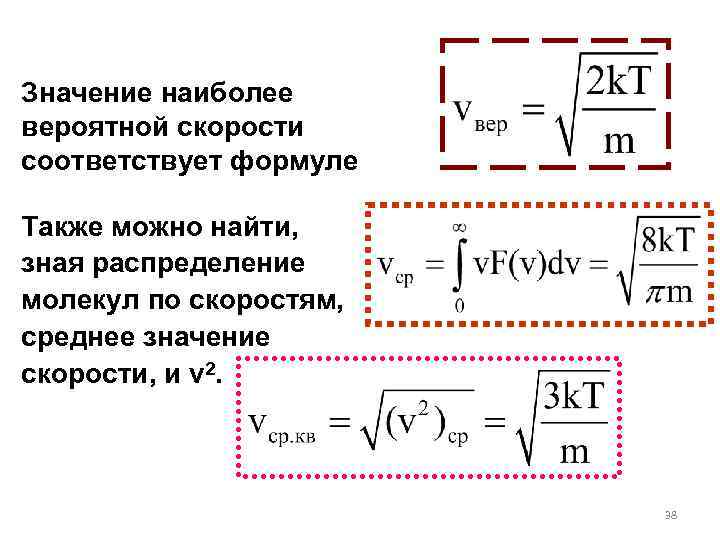 Значение наиболее вероятной скорости соответствует формуле Также можно найти, зная распределение молекул по скоростям, среднее значение скорости, и v 2. 38
Значение наиболее вероятной скорости соответствует формуле Также можно найти, зная распределение молекул по скоростям, среднее значение скорости, и v 2. 38
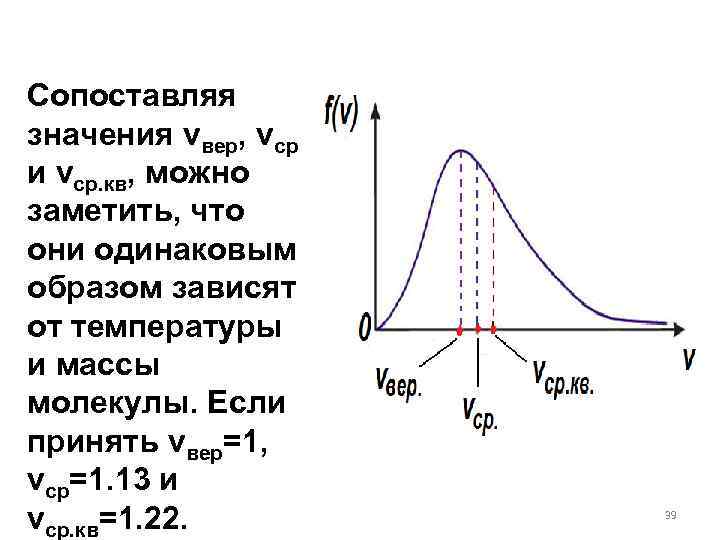 Сопоставляя значения vвер, vср и vср. кв, можно заметить, что они одинаковым образом зависят от температуры и массы молекулы. Если принять vвер=1, vср=1. 13 и vср. кв=1. 22. 39
Сопоставляя значения vвер, vср и vср. кв, можно заметить, что они одинаковым образом зависят от температуры и массы молекулы. Если принять vвер=1, vср=1. 13 и vср. кв=1. 22. 39
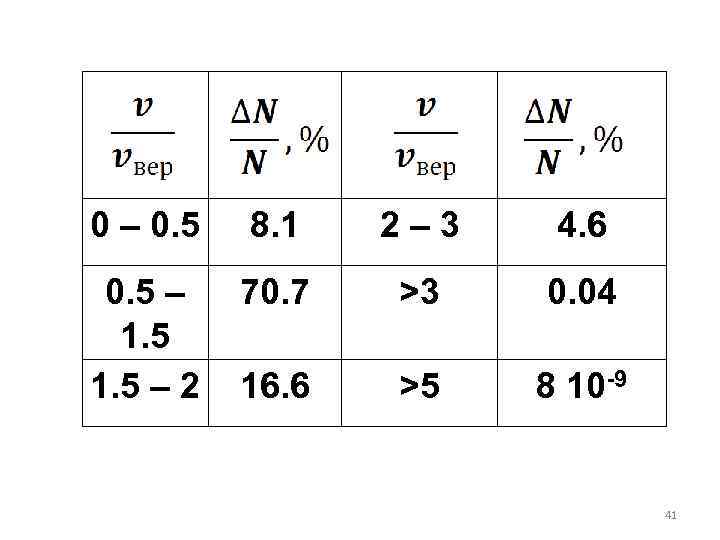
 Относительное число молекул, скорость которых превышает некоторое значение v 0, сильно растет с температурой. В таблице приведены относительные количества молекул скорости которых лежат в определенных интервалов относительно наиболее вероятной скорости. 40
Относительное число молекул, скорость которых превышает некоторое значение v 0, сильно растет с температурой. В таблице приведены относительные количества молекул скорости которых лежат в определенных интервалов относительно наиболее вероятной скорости. 40
 0 – 0. 5 8. 1 2 – 3 4. 6 0. 5 – 1. 5 – 2 70. 7 >3 0. 04 16. 6 >5 8 10 -9 41
0 – 0. 5 8. 1 2 – 3 4. 6 0. 5 – 1. 5 – 2 70. 7 >3 0. 04 16. 6 >5 8 10 -9 41
 Как видно из таблицы, более чем у 70% всех молекул скорость отличается от наиболее вероятной не больше чем на 50%. Скоростью, более чем в 3 раза превышающей vвер, обладает в среднем только 0. 04% молекул. 42
Как видно из таблицы, более чем у 70% всех молекул скорость отличается от наиболее вероятной не больше чем на 50%. Скоростью, более чем в 3 раза превышающей vвер, обладает в среднем только 0. 04% молекул. 42
 • Барометрическая формула 43
• Барометрическая формула 43
 • 44
• 44
 • 45
• 45
 • 46
• 46
 Барометрическую формулу для оценки можно использовать и в случае, когда температура не является постоянной, а слабо зависит от высоты. Такая ситуация имеет место в атмосфере до высоты примерно 100 км, когда давление падает на несколько порядков. На таких высотах выделяют несколько слоев атмосферы. Нижний слой – тропосфера – простирается до высоты примерно 12 км, содержит 80% массы атмосферы Земли и характеризуется почти линейным 47
Барометрическую формулу для оценки можно использовать и в случае, когда температура не является постоянной, а слабо зависит от высоты. Такая ситуация имеет место в атмосфере до высоты примерно 100 км, когда давление падает на несколько порядков. На таких высотах выделяют несколько слоев атмосферы. Нижний слой – тропосфера – простирается до высоты примерно 12 км, содержит 80% массы атмосферы Земли и характеризуется почти линейным 47
 Контрольные вопросы 1. Назовите два подхода для изучения МКТ 2. Определите, что такое идеальный газ 3. Назовите законы идеального газа 4. Напишите формулу основного закона МКТ 5. Распределение Максвелла 6. Формулы для наиболее вероятной, средней и среднеквадратичной 48
Контрольные вопросы 1. Назовите два подхода для изучения МКТ 2. Определите, что такое идеальный газ 3. Назовите законы идеального газа 4. Напишите формулу основного закона МКТ 5. Распределение Максвелла 6. Формулы для наиболее вероятной, средней и среднеквадратичной 48


