 МОЛЕКУЛЯРНОКИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗА
МОЛЕКУЛЯРНОКИНЕТИЧЕСКАЯ ТЕОРИЯ ГАЗА
 Основное уравнение молекулярно-кинетической теории (МКТ) газа Модель идеального газа: - молекулы газа рассматриваются как идеально упругие шарики, взаимодействующие между собой и со стенками только во время упругих столкновений, - суммарный объем всех молекул предполагается малым по сравнению с объемом сосуда Задача МКТ состоит в том, чтобы установить связь между микроскопическими (масса, скорость, кинетическая энергия молекул) и макроскопическими параметрами (давление, температура).
Основное уравнение молекулярно-кинетической теории (МКТ) газа Модель идеального газа: - молекулы газа рассматриваются как идеально упругие шарики, взаимодействующие между собой и со стенками только во время упругих столкновений, - суммарный объем всех молекул предполагается малым по сравнению с объемом сосуда Задача МКТ состоит в том, чтобы установить связь между микроскопическими (масса, скорость, кинетическая энергия молекул) и макроскопическими параметрами (давление, температура).
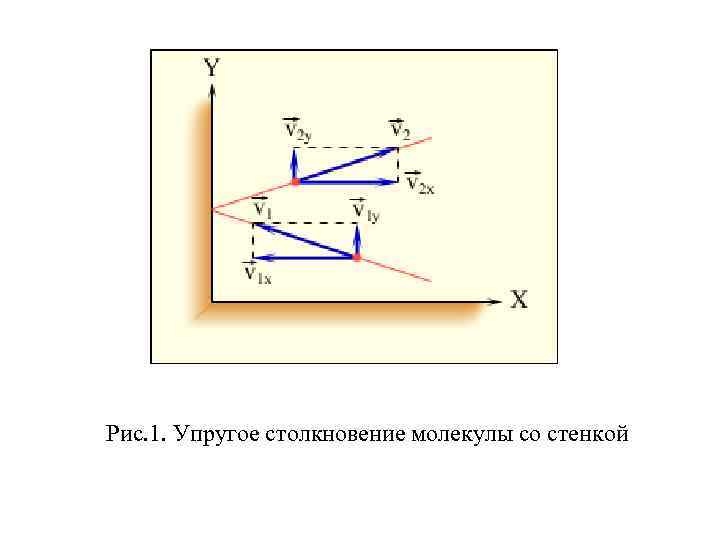 Рис. 1. Упругое столкновение молекулы со стенкой
Рис. 1. Упругое столкновение молекулы со стенкой
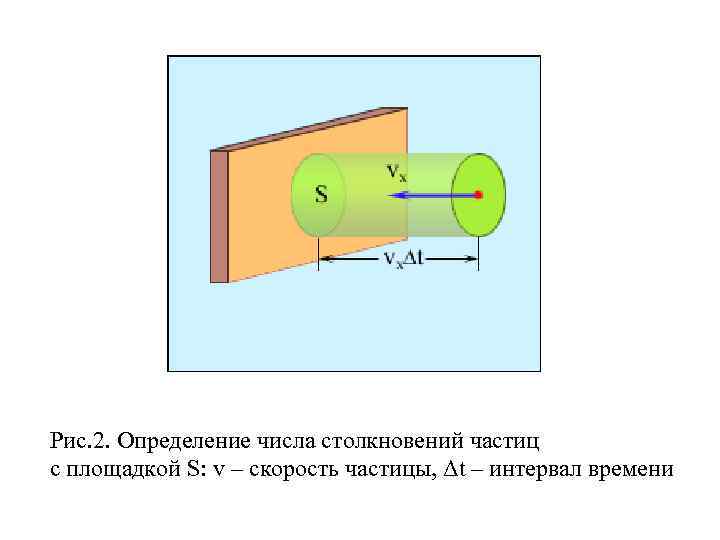 Рис. 2. Определение числа столкновений частиц с площадкой S: v – скорость частицы, Δt – интервал времени
Рис. 2. Определение числа столкновений частиц с площадкой S: v – скорость частицы, Δt – интервал времени
 Изменение импульса молекулы в результате удара m 0 – масса молекулы Число ударов молекул о площадку S за время Δt n - число молекул в единице объема газа
Изменение импульса молекулы в результате удара m 0 – масса молекулы Число ударов молекул о площадку S за время Δt n - число молекул в единице объема газа
 Полное изменение импульса всех молекул, столкнувшихся за время Δt с площадкой S Изменение импульса всех столкнувшихся со стенкой молекул соответствует действию импульса силы со стороны стенки на площадке S. F – некоторая средняя сила
Полное изменение импульса всех молекул, столкнувшихся за время Δt с площадкой S Изменение импульса всех столкнувшихся со стенкой молекул соответствует действию импульса силы со стороны стенки на площадке S. F – некоторая средняя сила
 Давление газа на стенку сосуда Замечания. 1. При выводе этого соотношения предполагалось, что все молекулы, содержащихся в единице объема газа, имеют одинаковые проекции скоростей на ось X. 2. В результате многочисленных соударений молекул газа между собой и со стенками в сосуде, содержащем большое число молекул, устанавливается некоторое статистическое распределение молекул по скоростям.
Давление газа на стенку сосуда Замечания. 1. При выводе этого соотношения предполагалось, что все молекулы, содержащихся в единице объема газа, имеют одинаковые проекции скоростей на ось X. 2. В результате многочисленных соударений молекул газа между собой и со стенками в сосуде, содержащем большое число молекул, устанавливается некоторое статистическое распределение молекул по скоростям.
 Распределение молекул газа по скоростям (распределение Максвелла) Основные идеи. 1. Все направления векторов скоростей молекул оказываются равноправными (равновероятными). 2. Модули скоростей и их проекции на координатные оси подчиняются статистическим закономерностям.
Распределение молекул газа по скоростям (распределение Максвелла) Основные идеи. 1. Все направления векторов скоростей молекул оказываются равноправными (равновероятными). 2. Модули скоростей и их проекции на координатные оси подчиняются статистическим закономерностям.
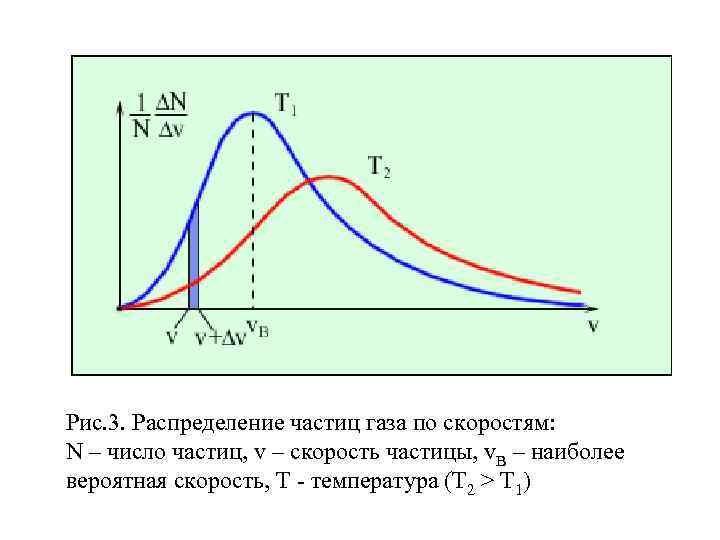 Рис. 3. Распределение частиц газа по скоростям: N – число частиц, v – скорость частицы, v. B – наиболее вероятная скорость, Т - температура (T 2 > T 1)
Рис. 3. Распределение частиц газа по скоростям: N – число частиц, v – скорость частицы, v. B – наиболее вероятная скорость, Т - температура (T 2 > T 1)
 Уточним формулу для давления газа на стенку сосуда. Предположим, что все молекулы, содержащиеся в единице объема, разбиты на группы, содержащие n 1, n 2 и т. д. молекул с проекциями скоростей υx 1, υx 2 и т. д. Каждая группа молекул вносит свой вклад в давление газа.
Уточним формулу для давления газа на стенку сосуда. Предположим, что все молекулы, содержащиеся в единице объема, разбиты на группы, содержащие n 1, n 2 и т. д. молекул с проекциями скоростей υx 1, υx 2 и т. д. Каждая группа молекул вносит свой вклад в давление газа.
 v. СР 2 - среднее квадратичное значение скорости частиц Введем понятие средней кинетической энергии частиц газа
v. СР 2 - среднее квадратичное значение скорости частиц Введем понятие средней кинетической энергии частиц газа
 Температура газа Тепловое равновесие. Состояние системы тел, находящихся в тепловом контакте, при котором не происходит теплопередачи от одного тела к другому, и все макроскопические параметры тел остаются неизменными. Температура. Физический параметр, одинаковый для всех тел, находящихся в тепловом равновесии, мера средней тепловой энергии. k - постоянная Больцмана k = 1, 38· 10– 23 Дж/К
Температура газа Тепловое равновесие. Состояние системы тел, находящихся в тепловом контакте, при котором не происходит теплопередачи от одного тела к другому, и все макроскопические параметры тел остаются неизменными. Температура. Физический параметр, одинаковый для всех тел, находящихся в тепловом равновесии, мера средней тепловой энергии. k - постоянная Больцмана k = 1, 38· 10– 23 Дж/К
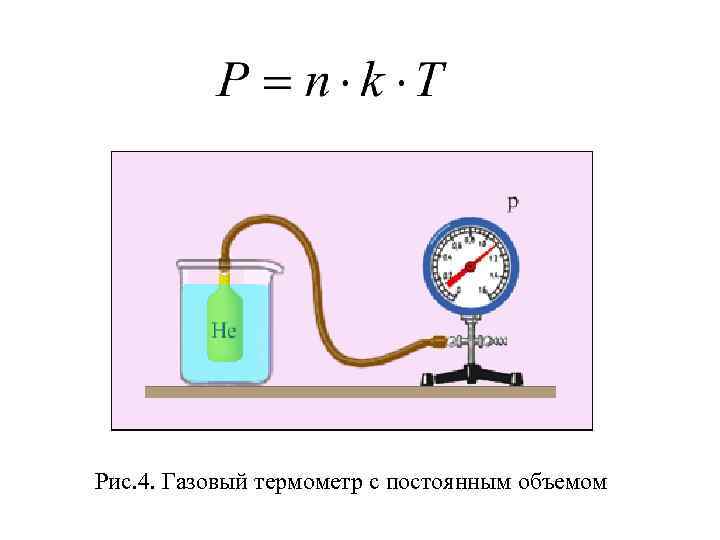 Рис. 4. Газовый термометр с постоянным объемом
Рис. 4. Газовый термометр с постоянным объемом
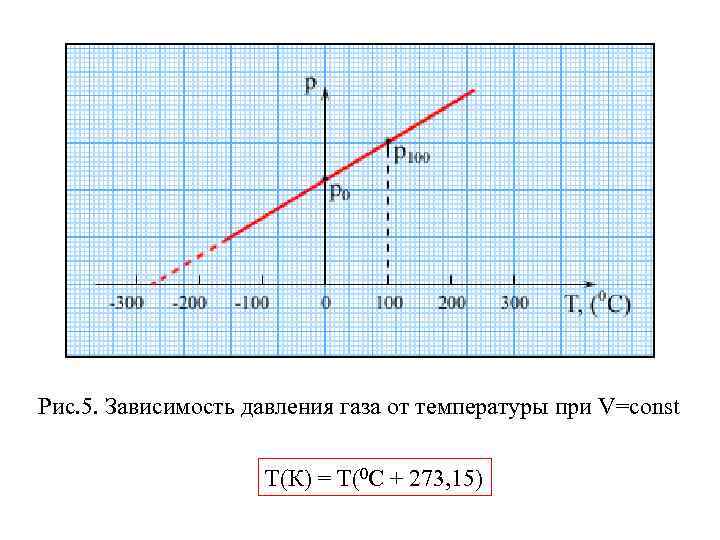 Рис. 5. Зависимость давления газа от температуры при V=const T(К) = T(0 С + 273, 15)
Рис. 5. Зависимость давления газа от температуры при V=const T(К) = T(0 С + 273, 15)
 Закон Дальтона Давление в смеси химически невзаимодействующих газов равно сумме их парциальных давлений P = Р 1 + Р 2 + Р 3 +…= (n 1 + n 2 + n 3 +…)k. T n 1, n 2, n 3, … – концентрации молекул различных газов в смеси
Закон Дальтона Давление в смеси химически невзаимодействующих газов равно сумме их парциальных давлений P = Р 1 + Р 2 + Р 3 +…= (n 1 + n 2 + n 3 +…)k. T n 1, n 2, n 3, … – концентрации молекул различных газов в смеси
 ВНУТРЕННЯЯ ЭНЕРГИЯ ГАЗА Внутренняя энергия одного моля идеального одноатомного газа (гелий, неон и др. ) Внутренняя энергия одного моля идеального многоатомного газа i – число степеней свободы частицы газа
ВНУТРЕННЯЯ ЭНЕРГИЯ ГАЗА Внутренняя энергия одного моля идеального одноатомного газа (гелий, неон и др. ) Внутренняя энергия одного моля идеального многоатомного газа i – число степеней свободы частицы газа
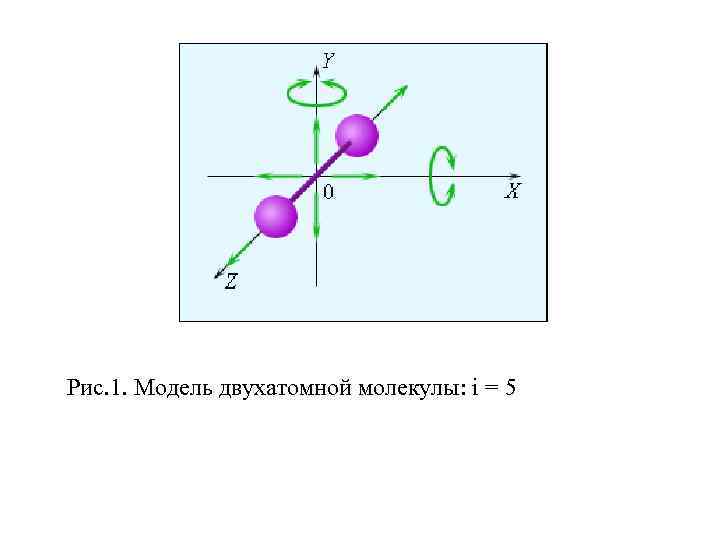 Рис. 1. Модель двухатомной молекулы: i = 5
Рис. 1. Модель двухатомной молекулы: i = 5