ГПХ MMR_1209.ppt
- Количество слайдов: 76
 Молекулярно-масові характеристики полімерів Лекція 2 l Взаємозвязок основних понять в хімії полімерів l Середні молекулярні маси l Молекулярно-масовий розподіл l Гель-проникаюча хроматографія
Молекулярно-масові характеристики полімерів Лекція 2 l Взаємозвязок основних понять в хімії полімерів l Середні молекулярні маси l Молекулярно-масовий розподіл l Гель-проникаюча хроматографія
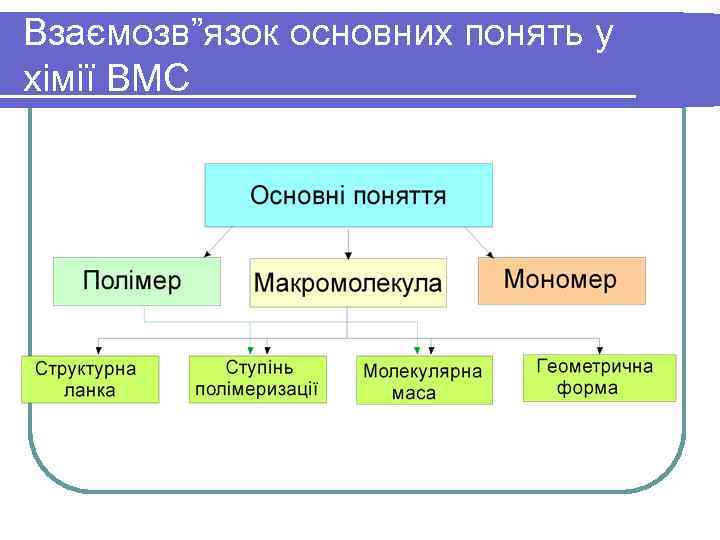 Взаємозв”язок основних понять у хімії ВМС
Взаємозв”язок основних понять у хімії ВМС
 Теорія Штаудінгера l l l ШТАУДИНГЕР, ГЕРМАН (Staudinger, Hermann) (1881– 1965), немецкий химик, удостоенный в 1953 Нобелевской премии по химии. В Цюрихе Штаудингер начал исследования природных и синтетических высокомолекулярных веществ. В 1921 показал, что молекулы каучука и других коллоидных соединений состоят из огромного числа атомов (от тысяч до миллионов), соединенных ковалентными связями, вопреки господствовавшим тогда представлениями, что они образуются из относительно низкомолекулярных соединений под действием неких «ассоциативных сил» . В 1922 Штаудингер предложил называть подобные молекулы «макромолекулами» .
Теорія Штаудінгера l l l ШТАУДИНГЕР, ГЕРМАН (Staudinger, Hermann) (1881– 1965), немецкий химик, удостоенный в 1953 Нобелевской премии по химии. В Цюрихе Штаудингер начал исследования природных и синтетических высокомолекулярных веществ. В 1921 показал, что молекулы каучука и других коллоидных соединений состоят из огромного числа атомов (от тысяч до миллионов), соединенных ковалентными связями, вопреки господствовавшим тогда представлениями, что они образуются из относительно низкомолекулярных соединений под действием неких «ассоциативных сил» . В 1922 Штаудингер предложил называть подобные молекулы «макромолекулами» .
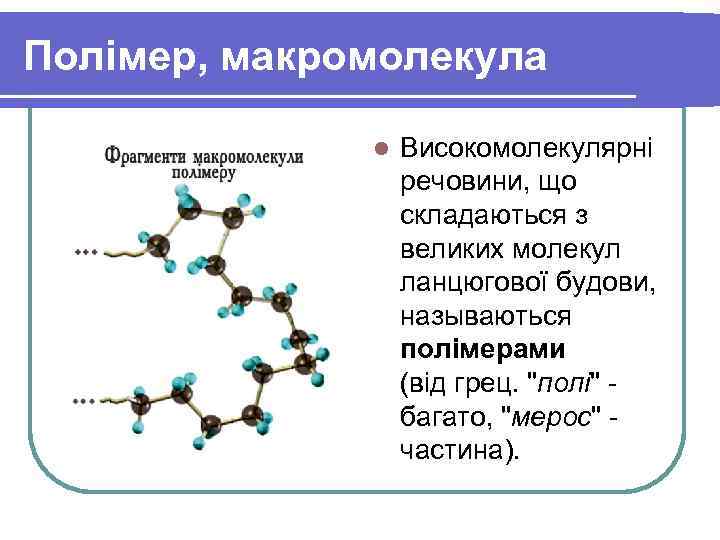 Полімер, макромолекула l Високомолекулярні речовини, що складаються з великих молекул ланцюгової будови, называються полімерами (від грец. "полі" багато, "мерос" частина).
Полімер, макромолекула l Високомолекулярні речовини, що складаються з великих молекул ланцюгової будови, называються полімерами (від грец. "полі" багато, "мерос" частина).
 Колоїдний розчин l розмір частинок якого складає од 10 -9 до 5 х10 -7 м (1 -500 нм).
Колоїдний розчин l розмір частинок якого складає од 10 -9 до 5 х10 -7 м (1 -500 нм).
 Колоїдні системи l Коллоидный раствор - размер частиц которого составляет от 10 -9 до 5 х10 -7 м (1 -500 нм). В частности, отличается от истинного раствора (размер частиц менее 10 -9 м) большей оптической активностью (как правило — непрозрачен). Выделяют коллоидные растворы газа в жидкости (пена), жидкости в жидкости (эмульсия), твердого тела в жидкости (суспензия) и др.
Колоїдні системи l Коллоидный раствор - размер частиц которого составляет от 10 -9 до 5 х10 -7 м (1 -500 нм). В частности, отличается от истинного раствора (размер частиц менее 10 -9 м) большей оптической активностью (как правило — непрозрачен). Выделяют коллоидные растворы газа в жидкости (пена), жидкости в жидкости (эмульсия), твердого тела в жидкости (суспензия) и др.
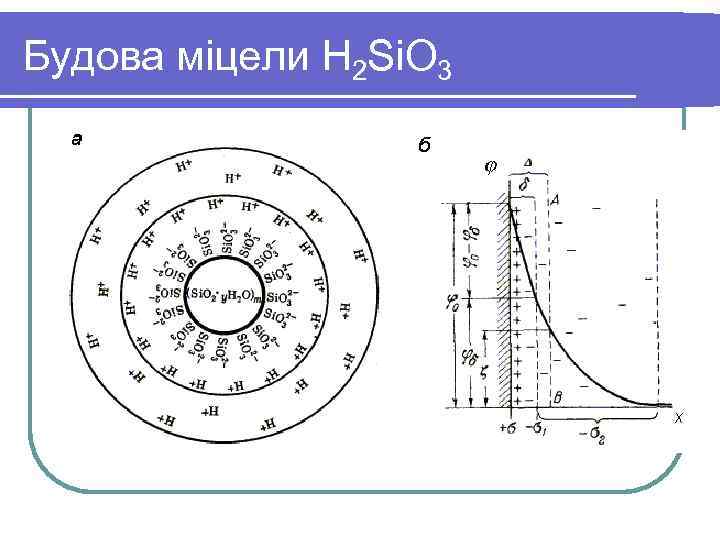 Будова міцели H 2 Si. O 3
Будова міцели H 2 Si. O 3
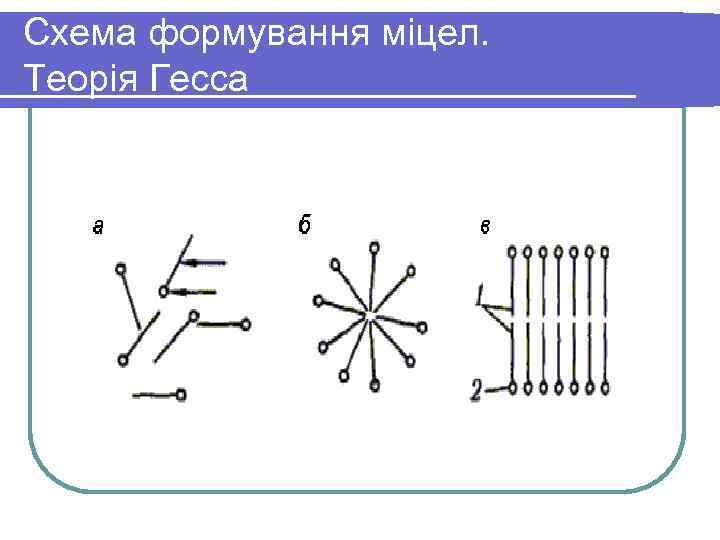 Схема формування міцел. Теорія Гесса
Схема формування міцел. Теорія Гесса
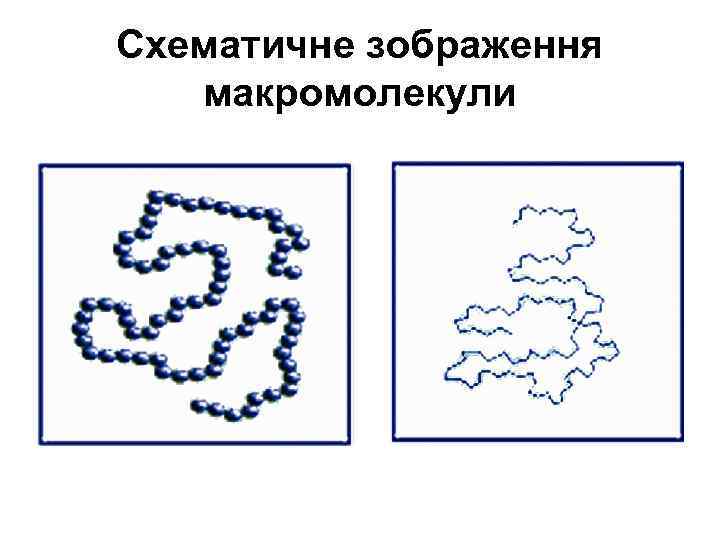 Схематичне зображення макромолекули
Схематичне зображення макромолекули
 Основні поняття і визначення в хімії ВМС • • • ПОНЯТТЯ : Мономер Макромолекула Полімер Олігомер Високомолекулярна сполука Мономерна ланка Ступінь полімеризації Усереднена молекулярна маса
Основні поняття і визначення в хімії ВМС • • • ПОНЯТТЯ : Мономер Макромолекула Полімер Олігомер Високомолекулярна сполука Мономерна ланка Ступінь полімеризації Усереднена молекулярна маса
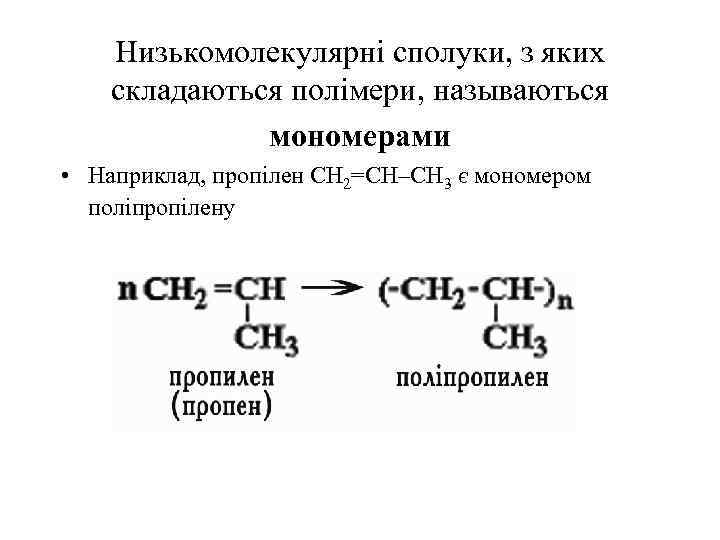 Низькомолекулярні сполуки, з яких складаються полімери, называються мономерами • Наприклад, пропілен СН 2=СH–CH 3 є мономером поліпропілену
Низькомолекулярні сполуки, з яких складаються полімери, называються мономерами • Наприклад, пропілен СН 2=СH–CH 3 є мономером поліпропілену
 ВМС, НМС, олігомер В залежності від значень Мм разрізняють високомолекулярні сполуки, олігомери и низкомолекулярні сполуки. При М>5000– 10000 високомолекулярні сполуки, М=500 – 5000 – олігомер, М<500 – низькомолекулярна сполука
ВМС, НМС, олігомер В залежності від значень Мм разрізняють високомолекулярні сполуки, олігомери и низкомолекулярні сполуки. При М>5000– 10000 високомолекулярні сполуки, М=500 – 5000 – олігомер, М<500 – низькомолекулярна сполука
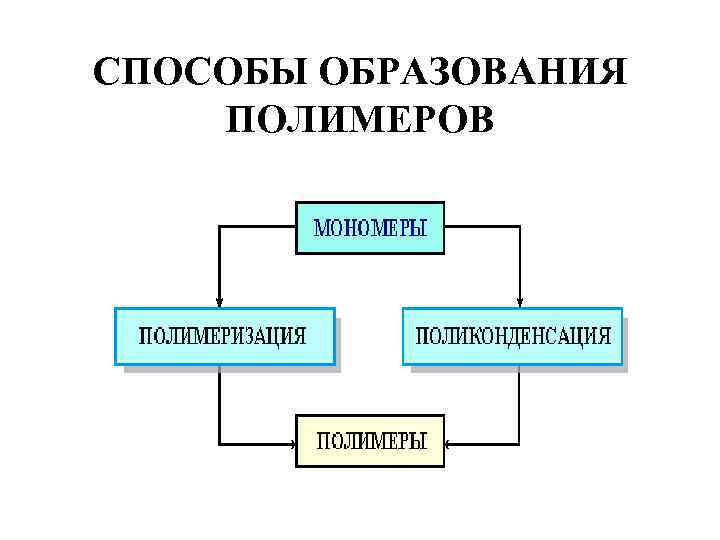 СПОСОБЫ ОБРАЗОВАНИЯ ПОЛИМЕРОВ
СПОСОБЫ ОБРАЗОВАНИЯ ПОЛИМЕРОВ
 Полімеризація • Ріст ланцюга
Полімеризація • Ріст ланцюга
 Мономери для полімеризації • Мономерами в полімеризації можуть бути речовини, здатні вступати в реакції приєднання. • Це ненасичені сполуки, що містять подвійні або потрійні зв'язки а також деякі речовини циклічної будови.
Мономери для полімеризації • Мономерами в полімеризації можуть бути речовини, здатні вступати в реакції приєднання. • Це ненасичені сполуки, що містять подвійні або потрійні зв'язки а також деякі речовини циклічної будови.
 Поліконденсація НO-R-OH + HOOC-R`-COOH → Поліефіри. H 2 N-R-NH 2 + HOOC-R`-COOH→ Поліаміди.
Поліконденсація НO-R-OH + HOOC-R`-COOH → Поліефіри. H 2 N-R-NH 2 + HOOC-R`-COOH→ Поліаміди.
 Група атомів, що багато разів повторюється в ланцюговій макромолекулі, називається її структурною ланкою. . -CH 2 -CHCl-CH 2 -CHCl-. . . полівінілхлорид У формулі макромолекули цю ланку зазвичай виділяють дужками: (-CH 2 -CHCl-)n
Група атомів, що багато разів повторюється в ланцюговій макромолекулі, називається її структурною ланкою. . -CH 2 -CHCl-CH 2 -CHCl-. . . полівінілхлорид У формулі макромолекули цю ланку зазвичай виділяють дужками: (-CH 2 -CHCl-)n
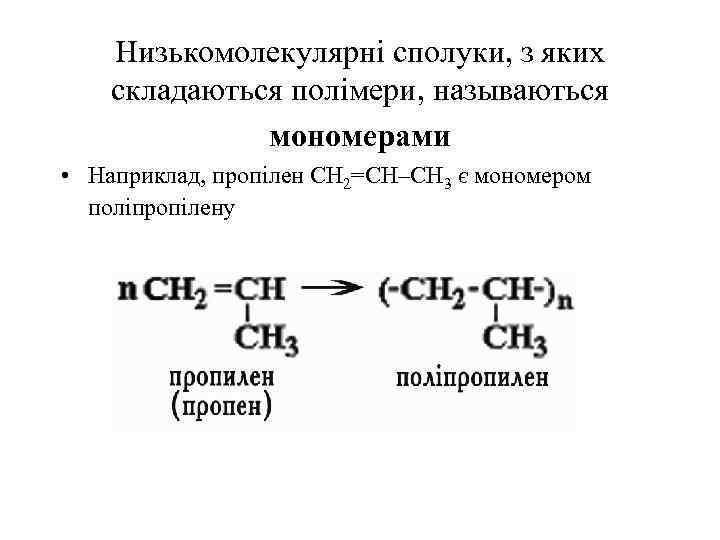 Низькомолекулярні сполуки, з яких складаються полімери, называються мономерами • Наприклад, пропілен СН 2=СH–CH 3 є мономером поліпропілену
Низькомолекулярні сполуки, з яких складаються полімери, называються мономерами • Наприклад, пропілен СН 2=СH–CH 3 є мономером поліпропілену
 Ступінь полімеризації - це число, що показує скільки молекул мономера з’єдналося в макромолекулу. В формулі макромолекули ступінь полімеризації звичайно позначується індексом "n" за лапками, що містять в собі структурну(мономерну) ланку: поліетилен полістирол n >> 1 поліізопрен
Ступінь полімеризації - це число, що показує скільки молекул мономера з’єдналося в макромолекулу. В формулі макромолекули ступінь полімеризації звичайно позначується індексом "n" за лапками, що містять в собі структурну(мономерну) ланку: поліетилен полістирол n >> 1 поліізопрен
 Пластомери –пластмаси і пластики Пластомери Поліолефіни Полівінілхлорид Полістирол Поліакрилати Полівінілацетат Поліаміди Фенопласти Амінопласти (- CH 2 – CH 2 -)n (-CH 2 -CHCl-)n (-CH 2 -CH(C 6 H 5)-)n (-CH 2 -C [COOCH 3] (CH 3)-)n (-CH 2 -C[OOCCH 3]H-)n (-NH-(CH 2)6 -NHCO-(CH 2)4 -CO-)n
Пластомери –пластмаси і пластики Пластомери Поліолефіни Полівінілхлорид Полістирол Поліакрилати Полівінілацетат Поліаміди Фенопласти Амінопласти (- CH 2 – CH 2 -)n (-CH 2 -CHCl-)n (-CH 2 -CH(C 6 H 5)-)n (-CH 2 -C [COOCH 3] (CH 3)-)n (-CH 2 -C[OOCCH 3]H-)n (-NH-(CH 2)6 -NHCO-(CH 2)4 -CO-)n
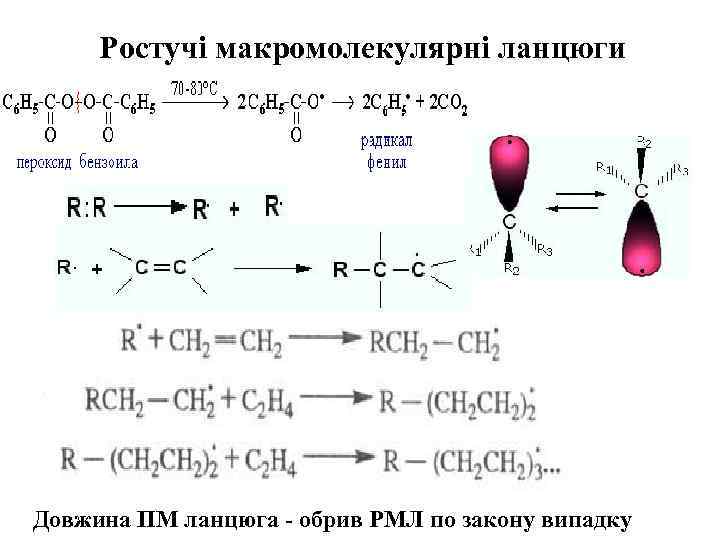 Ростучі макромолекулярні ланцюги Довжина ПМ ланцюга - обрив РМЛ по закону випадку
Ростучі макромолекулярні ланцюги Довжина ПМ ланцюга - обрив РМЛ по закону випадку
 Середньочислове значення Мм • Нехай, N молекул поліетилену (-CH 2 -)n мають молекулярну масу 28000 , а 3 N молекул 140000. Визначити середню молекулярну масу цього полімеру.
Середньочислове значення Мм • Нехай, N молекул поліетилену (-CH 2 -)n мають молекулярну масу 28000 , а 3 N молекул 140000. Визначити середню молекулярну масу цього полімеру.
 Молекулярна маса макромолекули і полімеру • Молекулярна маса макромолекули зв» язана із ступенем полімеризації співвідношенням • М(макромолекули) = M(ланки) × n • Mср(полімеру) = M(ланки) × nср
Молекулярна маса макромолекули і полімеру • Молекулярна маса макромолекули зв» язана із ступенем полімеризації співвідношенням • М(макромолекули) = M(ланки) × n • Mср(полімеру) = M(ланки) × nср

 Типи усереднених величин молекулярної маси l Молекулярна маса: l Середньо-числова, l Середньо-масова, l Середньов”язкісна l Z-середня l Полімер являє собою суміш молекул з різною молекулярною масою. Макромолекули, які складаються з однакових хімічних ланок і володіють різною довжиною, називаються полімернгомологами. Практично неможливо чітко розділити суміш ВМС на індивідуальні речовини з певною молекулярною масою. Визначення молекулярні маси тим чи іншим методом є усередненою величиною і числове значення її залежить від застосовуваного методу.
Типи усереднених величин молекулярної маси l Молекулярна маса: l Середньо-числова, l Середньо-масова, l Середньов”язкісна l Z-середня l Полімер являє собою суміш молекул з різною молекулярною масою. Макромолекули, які складаються з однакових хімічних ланок і володіють різною довжиною, називаються полімернгомологами. Практично неможливо чітко розділити суміш ВМС на індивідуальні речовини з певною молекулярною масою. Визначення молекулярні маси тим чи іншим методом є усередненою величиною і числове значення її залежить від застосовуваного методу.
 Поняття полімолекулярності полімерів l Всі синтетичні полімери, незалежно від хімічного способу отримання, відрізняються полидисперсністю. Зростання кожної окремої молекулы полимера при полімеризації або в якомунебудь іншому хімічному процесі отримання полімерів може припинитися у будь-який момент залежно від умов проведення даного процесу. Тому довжина кожної макромолекули полімера в кінцевому продукті хімичної реакції виявляється довільною, а зразок полімера є суміш макромолекул різної довжини. З цієї причини зазвичай говорять, що полимер володіє полімолекулярністю.
Поняття полімолекулярності полімерів l Всі синтетичні полімери, незалежно від хімічного способу отримання, відрізняються полидисперсністю. Зростання кожної окремої молекулы полимера при полімеризації або в якомунебудь іншому хімічному процесі отримання полімерів може припинитися у будь-який момент залежно від умов проведення даного процесу. Тому довжина кожної макромолекули полімера в кінцевому продукті хімичної реакції виявляється довільною, а зразок полімера є суміш макромолекул різної довжини. З цієї причини зазвичай говорять, що полимер володіє полімолекулярністю.
 Поняття полімолекулярності полімерів 2 Величину кожної молекули можна характеризувати ступенем полімеризації Р, числом елементарних ланок N в макромолекулі або молекулярною масою М. У разі, коли елементарна ланка є залишок одного мономера, N=Р. l У зв'язку з тим, що будь-яка властивість полимеров зазвичай визначається, усереднено для всіх молекул даного типу, і розраховане значення молекулярних характеристик також матиме деяку середню величину. Найчастіше для характеристики макромолекул використовують Мn. l
Поняття полімолекулярності полімерів 2 Величину кожної молекули можна характеризувати ступенем полімеризації Р, числом елементарних ланок N в макромолекулі або молекулярною масою М. У разі, коли елементарна ланка є залишок одного мономера, N=Р. l У зв'язку з тим, що будь-яка властивість полимеров зазвичай визначається, усереднено для всіх молекул даного типу, і розраховане значення молекулярних характеристик також матиме деяку середню величину. Найчастіше для характеристики макромолекул використовують Мn. l
 Поняття полімолекулярності полімерів 3 l Залежно від способу визначення середня молекулярна маса також може розрізнятися. Це пов'язано з тим, що зміряна інтенсивність тієї або іншої властивості полимеру залежить від довжини, їх маси або об'єму. Тому існує декілька груп методів, що дозволяють визначити різні значення молекулярної маси
Поняття полімолекулярності полімерів 3 l Залежно від способу визначення середня молекулярна маса також може розрізнятися. Це пов'язано з тим, що зміряна інтенсивність тієї або іншої властивості полимеру залежить від довжини, їх маси або об'єму. Тому існує декілька груп методів, що дозволяють визначити різні значення молекулярної маси

 Середньо- числова молекулярна маса полімеру l виражається відношенням маси полімера до числа молекул Ni, Xi, wi – число молекул, числова і масова частка молекул з молекулярною масою Мі відповідно
Середньо- числова молекулярна маса полімеру l виражається відношенням маси полімера до числа молекул Ni, Xi, wi – число молекул, числова і масова частка молекул з молекулярною масою Мі відповідно
 Методи визначення Середньочислової молекулярної маси 1 l Средньочислова молекулярна маса визначається експериментальними методами, заснованими на вимірюванні інтенсивності властивостей, пов'язаних з числом молекул. Ці методи засновані на визначенні активності розчиненї речовини і чутливі до присутності низькомолекулярних фракцій і сторонніх низькомолекулярних речовин
Методи визначення Середньочислової молекулярної маси 1 l Средньочислова молекулярна маса визначається експериментальними методами, заснованими на вимірюванні інтенсивності властивостей, пов'язаних з числом молекул. Ці методи засновані на визначенні активності розчиненї речовини і чутливі до присутності низькомолекулярних фракцій і сторонніх низькомолекулярних речовин
 Методи визначення Середньочислової молекулярної маси 2 l Термодинамічні методи: l - ебуліоскопічний метод; l - кріоскопічний метод; l - метод ізотермічної дистилляції; l - метод визначення тиску пари над розчинами; l - метод осмотичного тиску.
Методи визначення Середньочислової молекулярної маси 2 l Термодинамічні методи: l - ебуліоскопічний метод; l - кріоскопічний метод; l - метод ізотермічної дистилляції; l - метод визначення тиску пари над розчинами; l - метод осмотичного тиску.
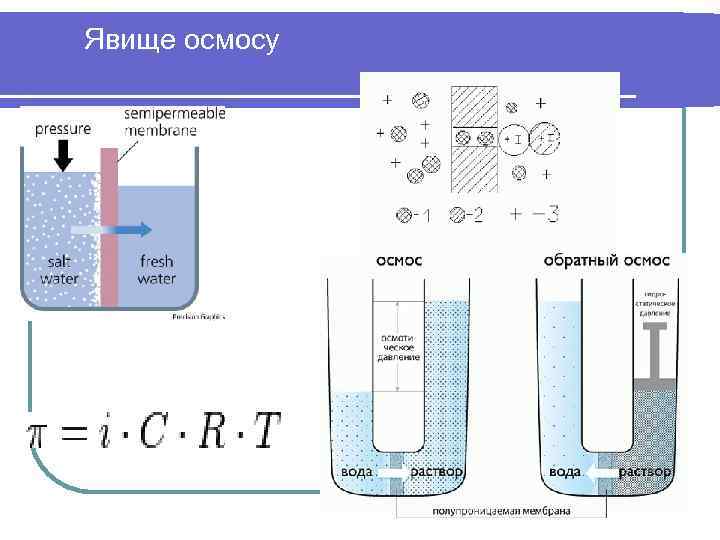 Явище осмосу
Явище осмосу
 Осмометрія- метод визначення Мм • Кількісна характеристика осмосу - осмотичний тиск, пропорційний числу молекул в одиниці об'єму розчину. Прагнення молекул розчинника до самовільного проникнення через мембрану визначається різницею хімічних потенціалів розчинника в частинах системи, розділених перегородкою
Осмометрія- метод визначення Мм • Кількісна характеристика осмосу - осмотичний тиск, пропорційний числу молекул в одиниці об'єму розчину. Прагнення молекул розчинника до самовільного проникнення через мембрану визначається різницею хімічних потенціалів розчинника в частинах системи, розділених перегородкою
 Приведений осмотичний тиск • Знайдена з вимірювань осмотичного тиску молекулярна маса характеризує
Приведений осмотичний тиск • Знайдена з вимірювань осмотичного тиску молекулярна маса характеризує
 Середньо- числова молекулярна маса полімеру • виражається відношенням маси полімера до числа молекул Ni, Xi, wi – число молекул, числова і масова частка молекул з молекулярною масою Мі відповідно
Середньо- числова молекулярна маса полімеру • виражається відношенням маси полімера до числа молекул Ni, Xi, wi – число молекул, числова і масова частка молекул з молекулярною масою Мі відповідно
 Додаткові методи визначення Мnчислової молекулярної маси 3 Методи кінцевих груп. 1). Хімічні методи, засновані на хімічній взаємодії спеціально підібраного реагента з хімічно активними кінцевими групами. l 2). Спектроскопічні методи використовуються в тих випадках, коли кінцеві групи мають оптичну активність. l 3). Радіаційні методи засновані на визначенні радиоактивности при введенні спеціальних міток – радіоактивних кінцевих груп. l l
Додаткові методи визначення Мnчислової молекулярної маси 3 Методи кінцевих груп. 1). Хімічні методи, засновані на хімічній взаємодії спеціально підібраного реагента з хімічно активними кінцевими групами. l 2). Спектроскопічні методи використовуються в тих випадках, коли кінцеві групи мають оптичну активність. l 3). Радіаційні методи засновані на визначенні радиоактивности при введенні спеціальних міток – радіоактивних кінцевих груп. l l

 Середньо-масова молекулярна маса Методи визначення
Середньо-масова молекулярна маса Методи визначення
 Середньо-масова молекулярна маса Средньомасова молекулярна маса сума мас окремих фракцій l wi - масова частка молекул з молекулярною масою Мі. l
Середньо-масова молекулярна маса Средньомасова молекулярна маса сума мас окремих фракцій l wi - масова частка молекул з молекулярною масою Мі. l
 Методи визначення Середньомасової молекулярної маси : l -метод разсіювання світла, l -метод дифузії, l - метод швидкісної седиментації (ультрацентрифугування). l молекулярна масса
Методи визначення Середньомасової молекулярної маси : l -метод разсіювання світла, l -метод дифузії, l - метод швидкісної седиментації (ультрацентрифугування). l молекулярна масса
 Метод світлорозсіювання l Теория рассеяния света на термодинамических флуктуациях в среде
Метод світлорозсіювання l Теория рассеяния света на термодинамических флуктуациях в среде
 Теорія Эйнштейна розсіювання світла • розсіювання світла відбувається на сферических частинках • Розсіююча здатність характеризується коефіц. розсіювання R • l– відстань, на якій спостерігають розсіяне світло від розсіюючого тіла; v – розсіюючий об/єм.
Теорія Эйнштейна розсіювання світла • розсіювання світла відбувається на сферических частинках • Розсіююча здатність характеризується коефіц. розсіювання R • l– відстань, на якій спостерігають розсіяне світло від розсіюючого тіла; v – розсіюючий об/єм.
 Метод розсіювання світла • Для розрахунку Мм використовують рівняння Дебая • для розрахунку Мм потрібно виміряти кутове розсіювання світла, коефіцієнт заломлення середовища • с – масова концентрація, г/см 3; K – оптична постійна, залежна від коефиіціента заломлення середовища (n 0), концентраційного інкремента коефіциєнта заломлення розчину (dn/dc) і довжини хвилі світла
Метод розсіювання світла • Для розрахунку Мм використовують рівняння Дебая • для розрахунку Мм потрібно виміряти кутове розсіювання світла, коефіцієнт заломлення середовища • с – масова концентрація, г/см 3; K – оптична постійна, залежна від коефиіціента заломлення середовища (n 0), концентраційного інкремента коефіциєнта заломлення розчину (dn/dc) і довжини хвилі світла
 Теорія методу розсіювання світла • где Н – оптическая постоянная, Н = 16 p K/3.
Теорія методу розсіювання світла • где Н – оптическая постоянная, Н = 16 p K/3.

 Mетод дифузії грунтується на: • Статистичній теорії броунівського руху • Допущення : рівняння Эйнштейна для дифузії полімерних молекул в розчині • Молекулярна маса сферичних макромолекул визначається як маса 1 моля полімера:
Mетод дифузії грунтується на: • Статистичній теорії броунівського руху • Допущення : рівняння Эйнштейна для дифузії полімерних молекул в розчині • Молекулярна маса сферичних макромолекул визначається як маса 1 моля полімера:

 Метод седиментації
Метод седиментації
 Метод седиментації • Сведберг в 1926 г. (ультрацентрифугування) • сила, діюча на молекулу в відцентровому полі • где F– сила, діюча на молекулу полимера; w 2 x – прискорення центробіжного поля, w – кутова швидкість обертання; x – відстань від молекули до центра обертання; mh – масса одної сольватованой молекулы; vh – объем одної молекули, r 0 - густина розчинника, vhr 0 – поправка на виштовхувальну силу.
Метод седиментації • Сведберг в 1926 г. (ультрацентрифугування) • сила, діюча на молекулу в відцентровому полі • где F– сила, діюча на молекулу полимера; w 2 x – прискорення центробіжного поля, w – кутова швидкість обертання; x – відстань від молекули до центра обертання; mh – масса одної сольватованой молекулы; vh – объем одної молекули, r 0 - густина розчинника, vhr 0 – поправка на виштовхувальну силу.
 Метод седиментації • Маса одної сольватованой молекули • Объем одної сольватованої макромолекули • де hs- число сольватаціїї макромолекул (г/г).
Метод седиментації • Маса одної сольватованой молекули • Объем одної сольватованої макромолекули • де hs- число сольватаціїї макромолекул (г/г).
 Метод седиментації Сила тертя, зрівноважує центробежну силу в стационарному режимі В умовах стационарности F= F' Сведберг пропонує поняття константи седиментациії S
Метод седиментації Сила тертя, зрівноважує центробежну силу в стационарному режимі В умовах стационарности F= F' Сведберг пропонує поняття константи седиментациії S

 Середньов’язкісна молекулярна маса l α, K – константи
Середньов’язкісна молекулярна маса l α, K – константи
 Віскозиметрія Вимірюємо в'язкість розчину полімеру l Полімери, коли ви розчиняєте їх в розчиннику, значно збільшують в'язкість розчину. Полімери використовуються як згущувачі в таких продуктах, як шампуні і навіть морозиво. Цей ефект збільшення в'язкості розчину може бути використаний для оцінки молекулярної маси полімерів. l Цей ефект загусання допомагає вам оцінити молекулярну масу завдяки простому факту: чим більше молекулярна маса, тим більше стає в'язкість розчину. l Беремо трубку, що зображена на малюнку, і вимірюємо скільки часу пройде, перш ніж через неї протече певний об'єм рідини l
Віскозиметрія Вимірюємо в'язкість розчину полімеру l Полімери, коли ви розчиняєте їх в розчиннику, значно збільшують в'язкість розчину. Полімери використовуються як згущувачі в таких продуктах, як шампуні і навіть морозиво. Цей ефект збільшення в'язкості розчину може бути використаний для оцінки молекулярної маси полімерів. l Цей ефект загусання допомагає вам оцінити молекулярну масу завдяки простому факту: чим більше молекулярна маса, тим більше стає в'язкість розчину. l Беремо трубку, що зображена на малюнку, і вимірюємо скільки часу пройде, перш ніж через неї протече певний об'єм рідини l
 Відносна в”язкість l Знаємо, як вимірювати час, який потрібний щоб рівень рідини впав на задану відстань. Цей час називається часом витіквння. l Вимірюємо часи витікання для різних концентрацій розчинів нашого полімеру. Також вимірюємо для порівняння час витікання чистого розчинника, в якому повністю відсутній розчинений полімер, назвемо час витікання для чистого розчинника t 0. Обчислимо відношення в'язкості розчинів полімерів до в'язкості чистого розчинника, поділивши час витікання розчину полімеру при даній концентрації (яке ми називаємо t) на t 0, час витікання для чистого розчинника. Це дасть відносну в'язкість. (буква h).
Відносна в”язкість l Знаємо, як вимірювати час, який потрібний щоб рівень рідини впав на задану відстань. Цей час називається часом витіквння. l Вимірюємо часи витікання для різних концентрацій розчинів нашого полімеру. Також вимірюємо для порівняння час витікання чистого розчинника, в якому повністю відсутній розчинений полімер, назвемо час витікання для чистого розчинника t 0. Обчислимо відношення в'язкості розчинів полімерів до в'язкості чистого розчинника, поділивши час витікання розчину полімеру при даній концентрації (яке ми називаємо t) на t 0, час витікання для чистого розчинника. Це дасть відносну в'язкість. (буква h).
 Питома і приведена в'язкість Віднімаємо час витікання чистого розчинника, t 0 з часу витікання розчину t. результат цього ділимо на t 0, називаємо цей результат питомою в'язкістю. l Поділимо її на відповідну концентрацію розчинника і отримаємо приведену в'язкість l
Питома і приведена в'язкість Віднімаємо час витікання чистого розчинника, t 0 з часу витікання розчину t. результат цього ділимо на t 0, називаємо цей результат питомою в'язкістю. l Поділимо її на відповідну концентрацію розчинника і отримаємо приведену в'язкість l
 Характеристична в'язкість Здобудемо різні значення приведеної в'язкості при різних концентраціях. Якщо ми відкладемо приведену в'язкість по осі у, а по осі x відкладемо концентрацію, ми отримаємо графік: l Визначаємо тангенс кута нахилу до Ох. Екстраполюємо цей графік до нульових значень концентрації і називаємо точку його перетину з віссю у характеристичною в'язкістю. (Характеристична в'язкість - це уявна величина. Оскільки в'язкість міняється з концентрацією, то характеристична в'язкість визначається як гіпотетична в'язкість при гіпотетичній "нульовій концентрації"), отримуємо рівняння прямої у формі "тангенс кута нахилу і зсув", у = mx + b, де m - це тангенс кута нахилу, а b - це точка перетину прямої з віссю у: l
Характеристична в'язкість Здобудемо різні значення приведеної в'язкості при різних концентраціях. Якщо ми відкладемо приведену в'язкість по осі у, а по осі x відкладемо концентрацію, ми отримаємо графік: l Визначаємо тангенс кута нахилу до Ох. Екстраполюємо цей графік до нульових значень концентрації і називаємо точку його перетину з віссю у характеристичною в'язкістю. (Характеристична в'язкість - це уявна величина. Оскільки в'язкість міняється з концентрацією, то характеристична в'язкість визначається як гіпотетична в'язкість при гіпотетичній "нульовій концентрації"), отримуємо рівняння прямої у формі "тангенс кута нахилу і зсув", у = mx + b, де m - це тангенс кута нахилу, а b - це точка перетину прямої з віссю у: l
 Рівняння Марка-Куна-Хаувінка l Візьмемо натуральний логарифм відносної в'язкості і поділимо її на величину концентрації розчину, для якого проводилося вимірювання. Це дає нам логарифмічну в'язкість. Як і у разі приведеної в'язкості, існує своє значення логарифмічної в'язкості для кожного зміряного значення концентрації. Побудуємо графік логарифмічної в'язкості по осі у, а по осі x відкладемо концентрацію розчину. Тоді ми отримаємо графік такого вигляду. Як і раніше, [h] - це точка перетину нашого графіка з віссю у, але кут нахилу цього разу у нас інший, він рівний k'' [h]2. Так, і цього разу наш графік задається тангенсом кута нахилу і зсувом по осі у. Ми зазвичай обчислюємо нашу характеристичну в'язкість, використовуючи обидва цих методу. Якщо їх результати співпадають, то ми знаємо, що ми всі зробили правильно. Ми зазвичай поміщаємо обидві прямі на один малюнок, отримуючи таким чином графік, на якому дві прямі зустрічаються в загальній точці перетину з віссю у:
Рівняння Марка-Куна-Хаувінка l Візьмемо натуральний логарифм відносної в'язкості і поділимо її на величину концентрації розчину, для якого проводилося вимірювання. Це дає нам логарифмічну в'язкість. Як і у разі приведеної в'язкості, існує своє значення логарифмічної в'язкості для кожного зміряного значення концентрації. Побудуємо графік логарифмічної в'язкості по осі у, а по осі x відкладемо концентрацію розчину. Тоді ми отримаємо графік такого вигляду. Як і раніше, [h] - це точка перетину нашого графіка з віссю у, але кут нахилу цього разу у нас інший, він рівний k'' [h]2. Так, і цього разу наш графік задається тангенсом кута нахилу і зсувом по осі у. Ми зазвичай обчислюємо нашу характеристичну в'язкість, використовуючи обидва цих методу. Якщо їх результати співпадають, то ми знаємо, що ми всі зробили правильно. Ми зазвичай поміщаємо обидві прямі на один малюнок, отримуючи таким чином графік, на якому дві прямі зустрічаються в загальній точці перетину з віссю у:
 Mz-середня молекулярна маса l Величина Mz визначається методом седиментації в ультрацентрифузі. Цим же методом можна одержати Mw.
Mz-середня молекулярна маса l Величина Mz визначається методом седиментації в ультрацентрифузі. Цим же методом можна одержати Mw.
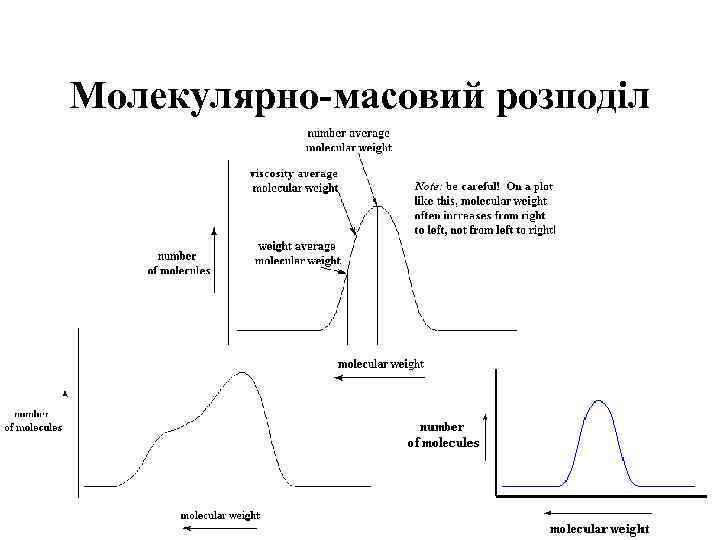 Молекулярно-масовий розподіл
Молекулярно-масовий розподіл
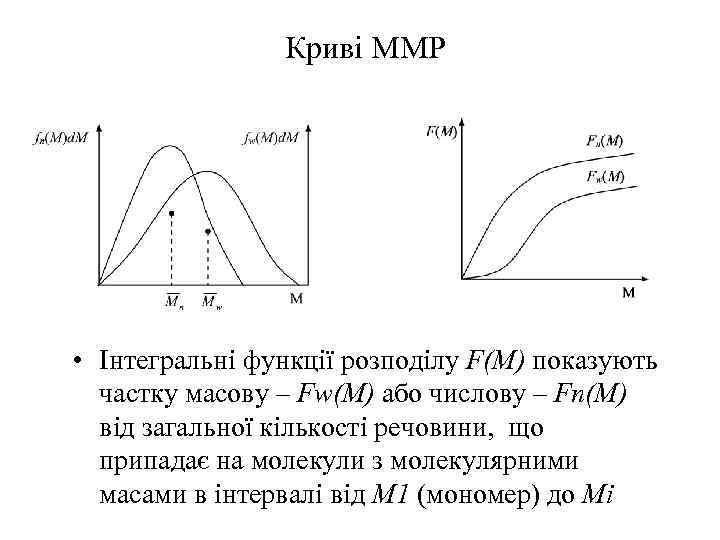 Криві ММР • Інтегральні функції розподілу F(M) показують частку масову – Fw(M) або числову – Fn(M) від загальної кількості речовини, що припадає на молекули з молекулярними масами в інтервалі від М 1 (мономер) до Мi
Криві ММР • Інтегральні функції розподілу F(M) показують частку масову – Fw(M) або числову – Fn(M) від загальної кількості речовини, що припадає на молекули з молекулярними масами в інтервалі від М 1 (мономер) до Мi
 Розподіл макромолекул за молекулярними масами • Функції молекулярно-масового розподілу (ММР)- для характеристики полімолекулярності полімерів. Масова диференціальна функція розподілу fw(M)d. M виражає масову частку макромолекул з молекулярними масами в інтервалі від Mi до (Mi+d. M) від загальної маси речовини, а числова диференціальна функція fn(M)d. M – числову частку макромолекул з молекулярними масами в інтервалі від Mi до (Mi+d. M) від загального числа макромолекул. .
Розподіл макромолекул за молекулярними масами • Функції молекулярно-масового розподілу (ММР)- для характеристики полімолекулярності полімерів. Масова диференціальна функція розподілу fw(M)d. M виражає масову частку макромолекул з молекулярними масами в інтервалі від Mi до (Mi+d. M) від загальної маси речовини, а числова диференціальна функція fn(M)d. M – числову частку макромолекул з молекулярними масами в інтервалі від Mi до (Mi+d. M) від загального числа макромолекул. .
 Розподіл макромолекул за молекулярними масами • Функції молекулярно-масового розподілу (ММР)- для характеристики полімолекулярності полімерів. • Абсциси центрів тяжіння площ, обмежених диференціальними кривими розподілу і віссю абсцис, дають відповідні середні молекулярні маси: для кривої fn(M)d. M і для кривої fw(M)d. M.
Розподіл макромолекул за молекулярними масами • Функції молекулярно-масового розподілу (ММР)- для характеристики полімолекулярності полімерів. • Абсциси центрів тяжіння площ, обмежених диференціальними кривими розподілу і віссю абсцис, дають відповідні середні молекулярні маси: для кривої fn(M)d. M і для кривої fw(M)d. M.
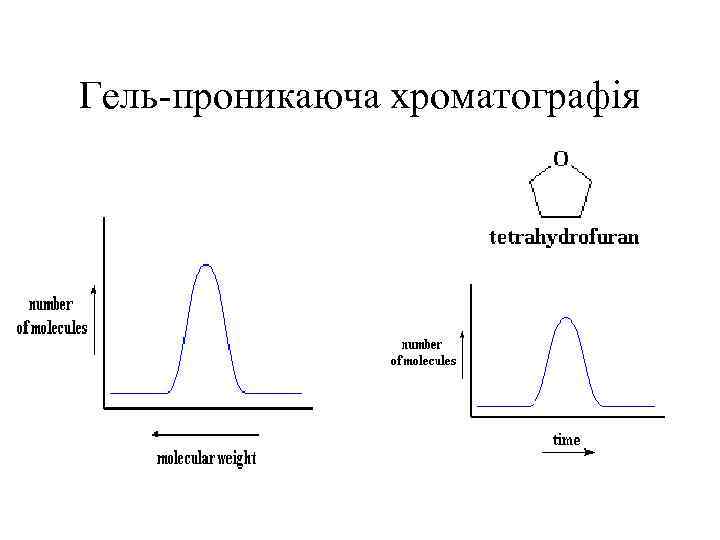 Гель-проникаюча хроматографія
Гель-проникаюча хроматографія
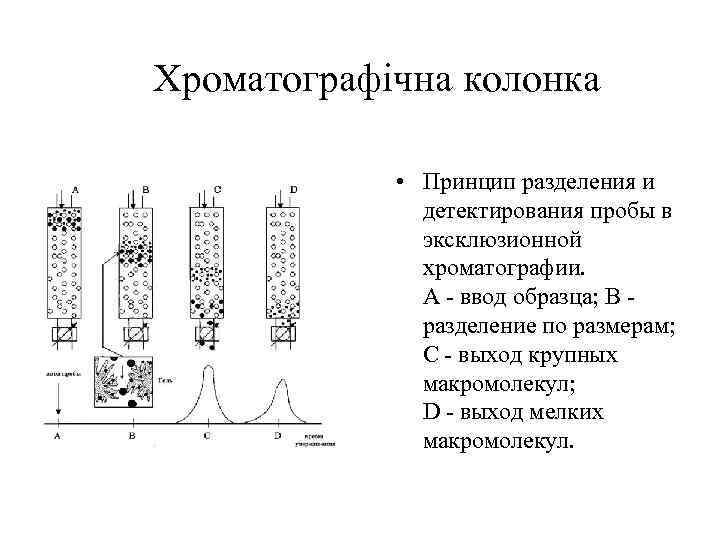 Хроматографічна колонка • Принцип разделения и детектирования пробы в эксклюзионной хроматографии. А - ввод образца; В разделение по размерам; С - выход крупных макромолекул; D - выход мелких макромолекул.
Хроматографічна колонка • Принцип разделения и детектирования пробы в эксклюзионной хроматографии. А - ввод образца; В разделение по размерам; С - выход крупных макромолекул; D - выход мелких макромолекул.
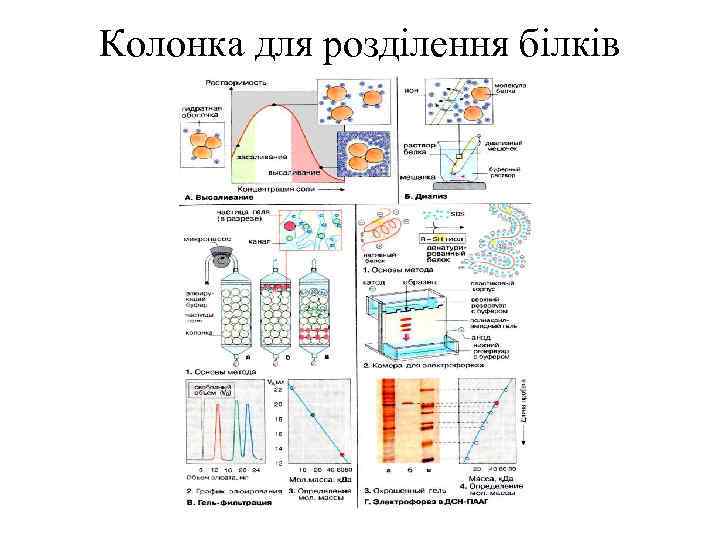 Колонка для розділення білків
Колонка для розділення білків
 Визначення полідисперсності полімеру • Синтетичний полімер в більшості випадків є сумішшю макромолекул з різною молекулярною масою (сумішшю полімергомологів). Для такої суміші величина молекулярної маси, знайдена тим або іншим способом, буде деякою середньою величиною; яка залежить від ступеня полідисперсності (молекулярної неоднорідності), від вигляду функції молекулярно-масового розподілу (ММР) і від способу експериментального визначення.
Визначення полідисперсності полімеру • Синтетичний полімер в більшості випадків є сумішшю макромолекул з різною молекулярною масою (сумішшю полімергомологів). Для такої суміші величина молекулярної маси, знайдена тим або іншим способом, буде деякою середньою величиною; яка залежить від ступеня полідисперсності (молекулярної неоднорідності), від вигляду функції молекулярно-масового розподілу (ММР) і від способу експериментального визначення.
 Визначення полідисперсності полімеру • Визначення молекулярної маси абсолютними (осмометрія, ебуліоскопія, кріоскопія, вимірювання теплових ефектів конденсації) або відносними (віскозиметрія) методами, або навіть знаходження відношення середньомасової молекулярної маси до середньочислової в багатьох випадках недостатньо для повної молекулярної характеристики полімерів. Для розуміння механізму утворення і хімічних перетворень полімерів, а також для виявлення залежності властивостей полімерів від їх молекулярних характеристик необхідно мати точну картину молекулярної неоднорідності полімеру, тобто визначити криву ММР.
Визначення полідисперсності полімеру • Визначення молекулярної маси абсолютними (осмометрія, ебуліоскопія, кріоскопія, вимірювання теплових ефектів конденсації) або відносними (віскозиметрія) методами, або навіть знаходження відношення середньомасової молекулярної маси до середньочислової в багатьох випадках недостатньо для повної молекулярної характеристики полімерів. Для розуміння механізму утворення і хімічних перетворень полімерів, а також для виявлення залежності властивостей полімерів від їх молекулярних характеристик необхідно мати точну картину молекулярної неоднорідності полімеру, тобто визначити криву ММР.
 Метод турбидиметрії • Для аналізу кінетики хімічних реакцій достатньо дістати картину ММР аналітичними методами (седиментація, гель-проникаюча хроматографія, турбідиметрія). • Суть методу турбідиметричного титрування полягає у вимірюванні мутності системи при повільному додаванні осадника до розведеного розчину полімеру, який знаходиться у кюветі. Осадник додається в кювету з постійною швидкістю і перемішується з розчином полімеру.
Метод турбидиметрії • Для аналізу кінетики хімічних реакцій достатньо дістати картину ММР аналітичними методами (седиментація, гель-проникаюча хроматографія, турбідиметрія). • Суть методу турбідиметричного титрування полягає у вимірюванні мутності системи при повільному додаванні осадника до розведеного розчину полімеру, який знаходиться у кюветі. Осадник додається в кювету з постійною швидкістю і перемішується з розчином полімеру.
 Мутність з’являється після деякої критичної концентрації осадника (порогу осадження), внаслідок виникнення нової фази осадженого полімеру з новим, вімінним від розчину, показником заломлення. Мутність при даній концентрації полімеру пов’язана з кількістю полімеру, який випав в осад. Будуючи залежність мутності τ (або оптичної густини D) при різних об’ємних долях осадника дістають криві турбідиметричного титрування. За такими кривими можна провести якісне порівняння полідисперсності різних зразків одного і того ж полімеру
Мутність з’являється після деякої критичної концентрації осадника (порогу осадження), внаслідок виникнення нової фази осадженого полімеру з новим, вімінним від розчину, показником заломлення. Мутність при даній концентрації полімеру пов’язана з кількістю полімеру, який випав в осад. Будуючи залежність мутності τ (або оптичної густини D) при різних об’ємних долях осадника дістають криві турбідиметричного титрування. За такими кривими можна провести якісне порівняння полідисперсності різних зразків одного і того ж полімеру
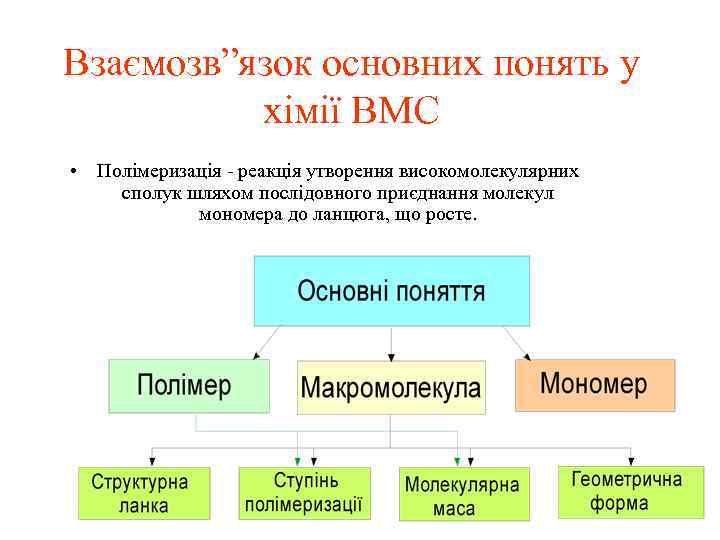 Взаємозв”язок основних понять у хімії ВМС • Полімеризація - реакція утворення високомолекулярних сполук шляхом послідовного приєднання молекул мономера до ланцюга, що росте.
Взаємозв”язок основних понять у хімії ВМС • Полімеризація - реакція утворення високомолекулярних сполук шляхом послідовного приєднання молекул мономера до ланцюга, що росте.



 Метод седиментації • 2
Метод седиментації • 2


