лек.11 молекулярно-кинетическая теория.ppt
- Количество слайдов: 64

Молекулярно кинетическая теория Курс общей физики Лекция № 11 Prof. N. A. Timchenko Tomsk polytechnic university

8. 2. УДАР АБСОЛЮТНО УПРУГИХ И НЕУПРУГИХ ТЕЛ Применим законы сохранения энергии и импульса к лобовому упругому и неупругому удару. Тела во время удара претерпевают деформацию. Сущность удара заключается в том, что кинетическая энергия относительного движения соударяющихся тел на короткое время преобразуется в энергию упругой деформации. Во время удара происходит перераспределение энергии между соударяющимися телами. Наблюдения показывают, что относительная скорость тел после удара не достигает своего прежнего значения. Это объясняется тем, что нет идеально упругих тел и идеально гладких поверхностей.

Отношение нормальных составляющих относительной скорости тел после и до удара называется коэффициентом восстановления k: Если для сталкивающихся тел k = 0, то такие тела называются абсолютно неупругими, если k = 1 – абсолютно упругими. На практике для тел 0<k<1 (например, для стальных шаров k ≈ 0, 56, для шаров из слоновой кости k ≈ 0, 89, для свинца k ≈ 0). Однако в некоторых случаях тела можно рассматривать с большой степенью точности как абсолютно упругие, либо как абсолютно неупругие.

Прямая, проходящая через точку соприкосновения тел и нормальная к поверхности их соприкосновения, называется линией удара. Удар называется центральным, если тела до удара движутся вдоль прямой, проходящей через их центр масс. Мы будем рассматривать только центральные абсолютно упругие и абсолютно неупругие удары.

8. 2. а). Абсолютно упругий удар – столкновение двух тел, в результате которого в обоих взаимодействующих телах не остается никаких деформаций и кинетическая энергия, которой обладали тела до удара, после удара снова превращается в кинетическую энергию (это идеальный случай). Для абсолютно упругого удара выполняется закон сохранения импульса и закон сохранения кинетической энергии.

Обозначим скорости частиц до удара через V 1 и V 2, а после удара и. При любом значении V > 0 частица движется вправо (координата х возрастает), в то время как при V<0 частица движется влево и координата х уменьшается. Напоминаю, мы рассматриваем центральный удар.
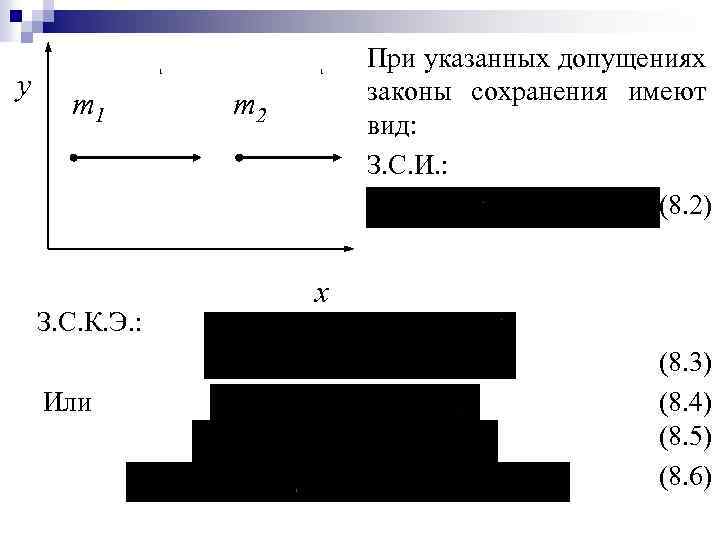
y 1 m 1 З. С. К. Э. : Или 1 m 2 При указанных допущениях законы сохранения имеют вид: З. С. И. : (8. 2) x (8. 3) (8. 4) (8. 5) (8. 6)

Разделив (8. 6) на (8. 5), получим или (8. 7) Итак, мы получили, что относительная скорость двух частиц после столкновения в точности равна их относительной скорости до столкновения; это верно для любого лобового удара, независимо от того, какие массы имеют частицы.

Разберем несколько примеров 1. Частицы с одинаковыми массами. Из закона сохранения импульса имеем: а). . Поскольку неизвестных величин две, необходимо еще одно уравнение. Можно использовать закон сохранения кинетической энергии, но проще применить уравнение (8. 7), согласно которому, относительные скорости до и после столкновения одинаковы.

б). . Сумма а) и б) дает , а разность а) и б) дает , таким образом, в результате столкновения частицы “обмениваются” скоростями; частица 2 приобретает скорость частицы 1, и наоборот. Если частица 2 первоначально покоилась (V 2=0), то мы имеем , . 2. Частица 2 первоначально покоилась (V 2=0). Объединяя уравнение сохранения импульсов с полученными выше соотношениями для и , получаем: , (8. 8)

Представляют интерес некоторые частные случаи: а) V 2=0, m 1=m 2. Здесь мы имеем и. Этот случай мы уже рассматривали. б) V 2=0, m 1>>m 2. Это случай, когда очень массивная частица налетает на легкую покоящуюся частицу. Используя (8. 8) имеем, , . Таким образом, скорость массивной частицы практически не меняется, а скорость легкой становится равной удвоенной скорости налетающей частицы. в) , . Движущееся легкое тело сталкивается с очень массивным покоящимся телом. Из (8. 8) имеем: , .

Массивное тело практически остается в покое, тогда как очень легкое тело отскакивает практически с той же по величине (но противоположно направленной) скоростью. г) V 2=0, m 1>m 2. Первый шар продолжает двигаться в том же направлении, как и до удара, но с меньшей скоростью. Скорость второго шара после удара больше, чем скорость первого после удара.

д) V 2=0, m 1<m 2. Направление удара первого шара изменяется – шар отскакивает обратно. Второй шар движется в ту же сторону, в которую двигался первый шар до удара, но с меньшей скоростью, т. е. .

8. 2. б). Абсолютно неупругий удар – столкновение двух тел, в результате которого тела объединяются, двигаясь дальше как единое целое. Продемонстрировать абсолютно неупругий удар можно с помощью шаров из пластилина (глины), движущихся навстречу другу. Если массы шаров m 1 и m 2, их скорости до удара и , то используя закон сохранения импульса, можно записать , где - скорость движения шаров после удара. Тогда: (8. 9)

Если шары двигались навстречу другу, то они вместе будут продолжать двигаться в ту сторону, в которую двигался шар, обладающий большим импульсом. В частном случае, если массы шаров равны (m 1=m 2), то. Выясним, как меняется кинетическая энергия шаров при центральном абсолютно неупругом ударе. Так как в процессе соударения шаров между ними действуют силы, зависящие не от самих деформаций, а от их скоростей, то мы имеем дело с силами, подобными силам трения, поэтому закон сохранения механической энергии не должен соблюдаться.

Вследствие деформации происходит “потеря” кинетической энергии , перешедшей в тепловую или другие формы энергии. Эту “потерю” можно определить по разности кинетических энергий до и после удара: Используя (8. 9), получаем Если ударяемое тело было первоначально неподвижно (V 2=0), то ,

Когда m 2>>m 1 (масса неподвижного тела очень большая), то V<<V 1 и почти вся кинетическая энергия при ударе переходит в другие формы энергии. Поэтому, например, для получения значительной деформации наковальня должна быть массивнее молотка. Когда m 1>>m 2, тогда V≈V 1 и практически вся энергия затрачивается на возможно большее перемещение, а не на остаточную деформацию (пример, молоток - гвоздь). Абсолютно неупругий удар – пример того, как происходит “потеря” механической энергии под действием диссипативных сил.

2. 3. Функция распределения Максвелла
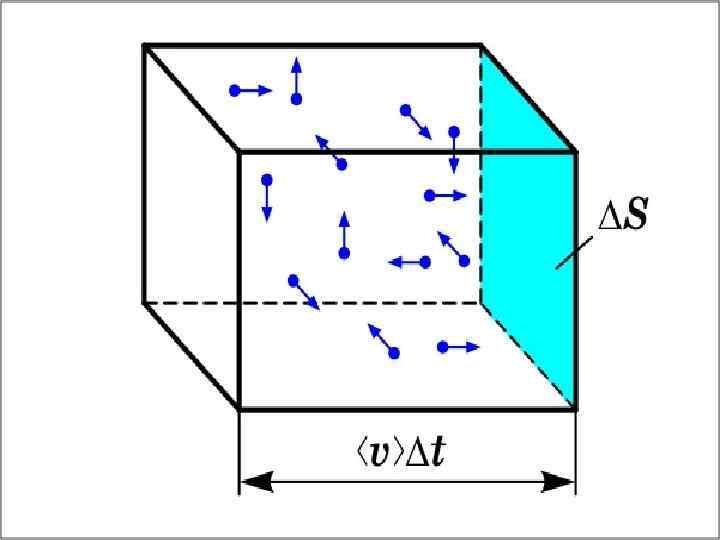

В результате каждого столкновения проекции скорости молекулы испытывают случайное изменение на vx, vy, vz, причем изменения каждой проекции скорости независимы друг от друга. Будем предполагать, что силовые поля на частицы не действуют. Найдем в этих условиях, каково число частиц dn из общего числа n имеет скорость в интервале от v до

Если скорость частицы попадает в интервал от до , то такая частица изобразится точкой между сферическими поверхностями радиусом и. Тогда число атомных частиц dn, из общего числа n, имеющих скорость в интервале пространства скоростей, равно плотности изображающих точек ρ(υ) [1/(м/с)3] между сферическими поверхностями с радиусами υ и , умноженной на объем области между этими сферами (рисунок 2. 2)
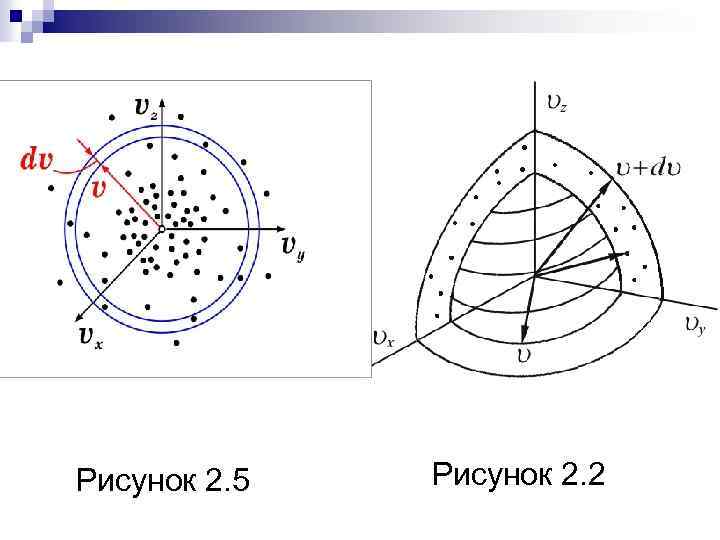
Рисунок 2. 5 Рисунок 2. 2

Вследствие изотропности пространства


Отсюда следует закон Максвелла – распределение молекул по абсолютным значениям скоростей: (2. 3. 3) где – доля всех частиц единичного объёма, скорости которых лежат в интервале от υ до

При получаем плотность вероятности, или функцию распределения молекул по скоростям: (2. 3. 4) Эта функция обозначает долю молекул единичного объёма газа, абсолютные скорости которых заключены в единичном интервале скоростей, включающем данную скорость.

Обозначим (2. 3. 4) получим: тогда, из (2. 3. 5) График этой функции показан на рис. 2. 6.
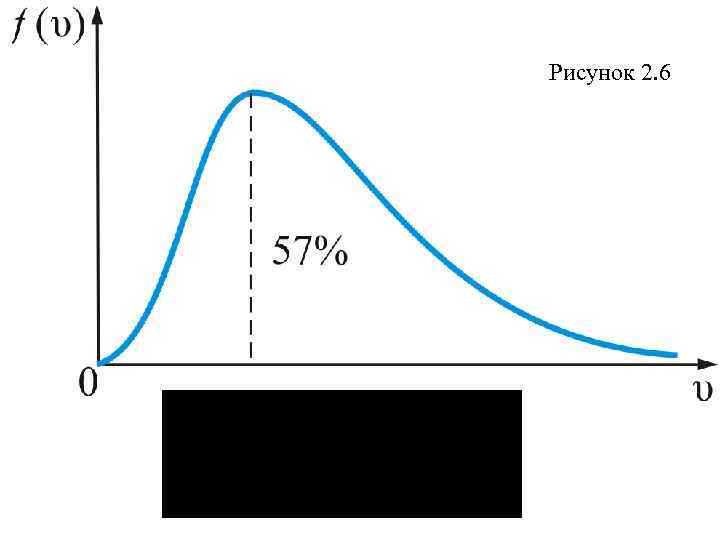
Рисунок 2. 6

Выводы: - Вид распределения молекул газа по скоростям, для каждого газа зависит от рода газа (m) и от параметра состояния (Т). Давление P и объём газа V на распределение молекул не влияют. - В показателе степени стоит отношение, кинетической энергии, соответствующей данной скорости υ к средней энергии теплового движения молекул при данной температуре:

Наиболее вероятная, среднеквадратичная и средняя арифметическая скорости молекул газа Рассмотрим, как изменяется с абсолютной величиной скорости число частиц, приходящихся на единичный интервал скоростей, при единичной концентрации частиц. График функции распр. Максвелла приведен на рис. 2. 7.
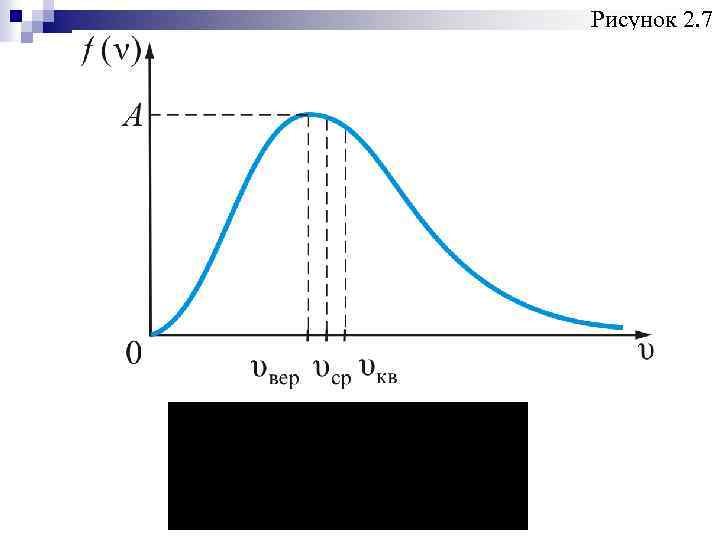
Рисунок 2. 7
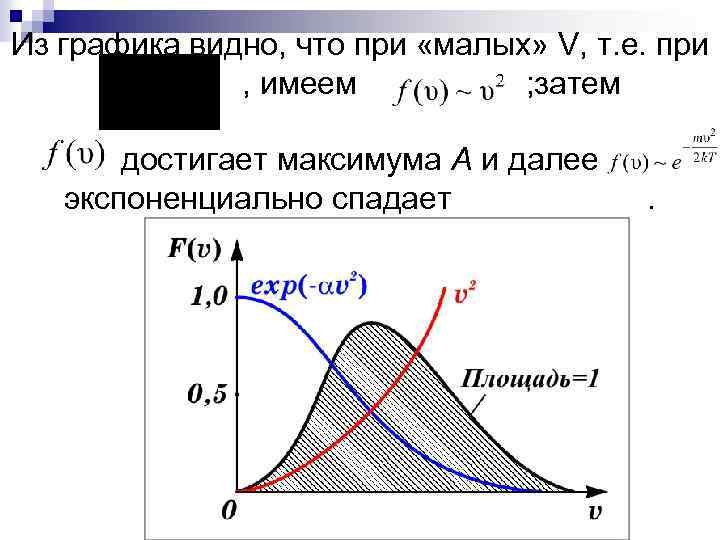
Из графика видно, что при «малых» V, т. е. при , имеем ; затем достигает максимума А и далее экспоненциально спадает .

Величина скорости, на которую приходится максимум зависимости называют наиболее вероятной скоростью. Величину этой скорости найдем из условия равенства нулю производной

Среднюю квадратичную скорость найдем используя соотношение : – для одной молекулы. (2. 3. 8) – газа. (2. 3. 9) для одного моля

Формула Максвелла для относительных скоростей Для решения многих задач удобно использовать формулу Максвелла, где скорость выражена в относительных единицах. Относительную скорость обозначим через u: (2. 3. 13) где

Формула Максвелла для относительных скоростей Это уравнение универсальное. В таком виде функция распределения не зависит ни от рода газа, ни от температуры (рис. 2. 8).
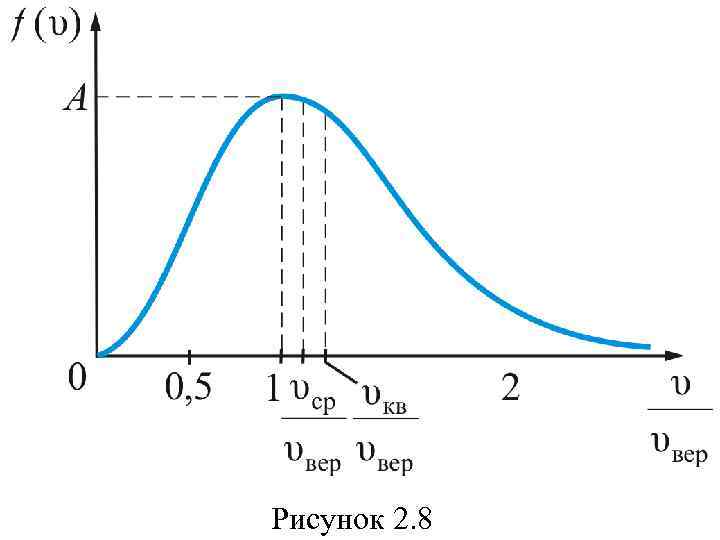
Рисунок 2. 8
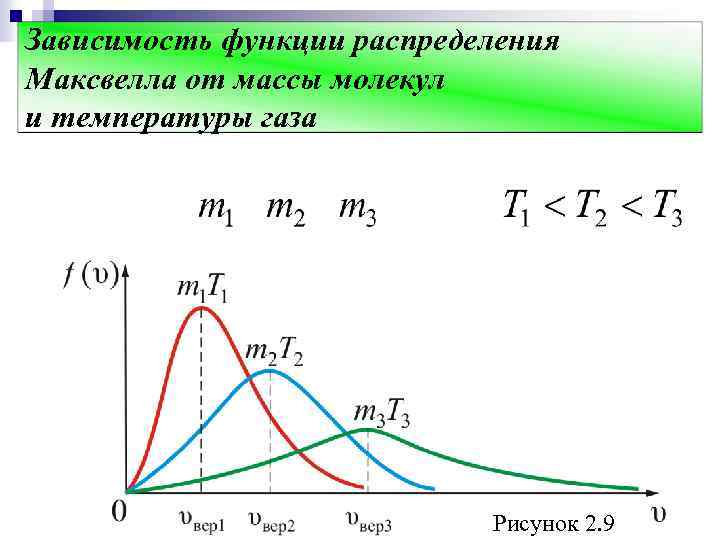
Зависимость функции распределения Максвелла от массы молекул и температуры газа Рисунок 2. 9

Экспериментально впервые скорости молекул были измерены в 1920 г. Штерном. За этот опыт и за большой вклад в развитие молекулярной физики в 1943 г. он был удостоен Нобелевской премии. В этом опыте были не только измерены скорости газовых молекул, но и показано, что они имеют большой разброс по скоростям. Причина, в хаотичности теплового движения молекул. Ещё в XIX веке Максвелл утверждал, что молекулы беспорядочно сталкиваясь друг с другом как-то «распределяются» по скоростям, причём вполне определённым образом. Cодержание
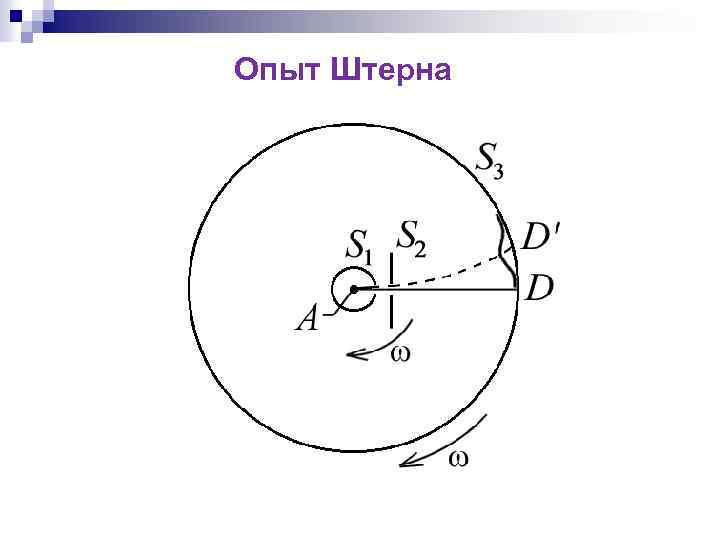
Опыт Штерна

Пусть l – расстояние между D и, измеренное вдоль поверхности цилиндра S 3, где – линейная скорость точек поверхности цилиндра S 3, радиусом R; время прохождения атомами серебра расстояния. Таким образом, имеем отсюда –скорость теплового движения атомов серебра:

Температура нити в опытах Штерна равнялась 1200 С, что соответствует среднеквадратичной скорости В эксперименте для этой величины получилось значение от 560 до 640 м/с. Кроме того, изображение щели D всегда оказывалось размытым, что указывало на то, что атомы Ag движутся с различными скоростями.

2. 4. Барометрическая формула Рассмотрим ещё один, очень важный закон.
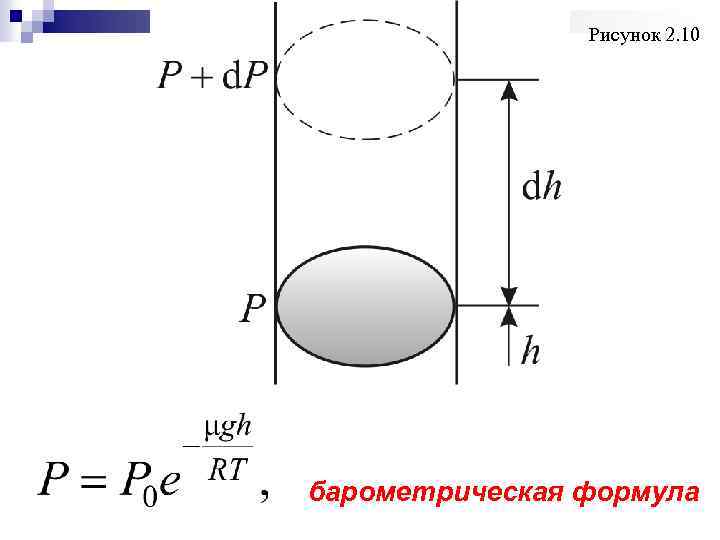
Рисунок 2. 10 барометрическая формула

Причём , d. Р < 0, так как на большей высоте давление меньше. Разность давления равна весу газа, заключённого в объёме цилиндра с площадью основания равного единице и высотой dh, ρ плотность газа на высоте h, медленно убывает с высотой. Отсюда где P 0 – давление на высоте барометрическая формула. (2. 4. 1). Это

2. 5. Распределение Больцмана

Пусть идеальный газ находится в поле консервативных сил, в условиях теплового равновесия. При этом, концентрация газа будет различной в точках с различной потенциальной энергией, что необходимо для соблюдения условий механического равновесия. Число молекул в единичном объеме n убывает с удалением от поверхности Земли, и давление, в силу соотношения тоже убывает.

Исходя из основного уравнения молекулярно-кинетической теории: , заменим P и P 0 в барометрической формуле (2. 4. 1) на n и n 0 и получим распределение Больцмана для молярной массы газа: (2. 5. 1) где n 0 и n число молекул в единичном объёме на высоте h = 0 и h, соответственно.
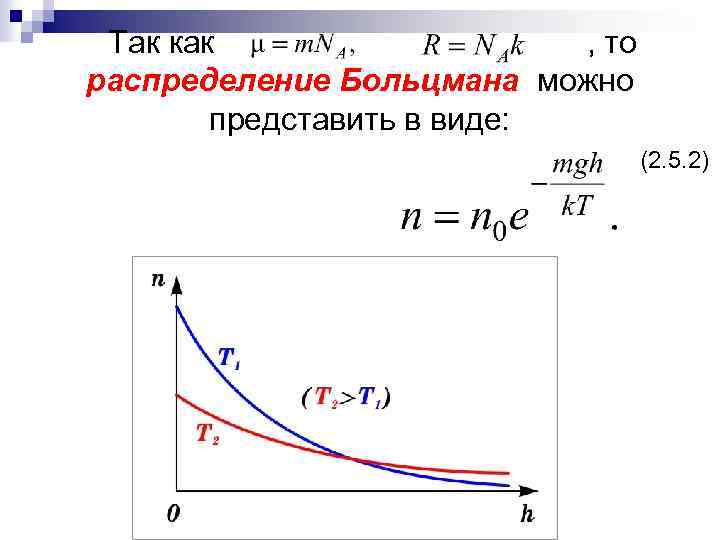
Так как , то распределение Больцмана можно представить в виде: (2. 5. 2)

С уменьшением температуры число молекул на высотах, отличных от нуля, убывает. При тепловое движение прекращается, все молекулы расположились бы на земной поверхности. При высоких температурах, наоборот, молекулы оказываются распределёнными по высоте почти равномерно, а плотность молекул медленно убывает с высотой.

Так как –потенциальная энергия, следовательно, распределение Больцмана характеризует распределение частиц по значениям потенциальной энергии: (2. 5. 3) – это закон распределения частиц по потенциальным энергиям – распределение Больцмана. Здесь n 0 – число молекул в единице объёма в там, где.
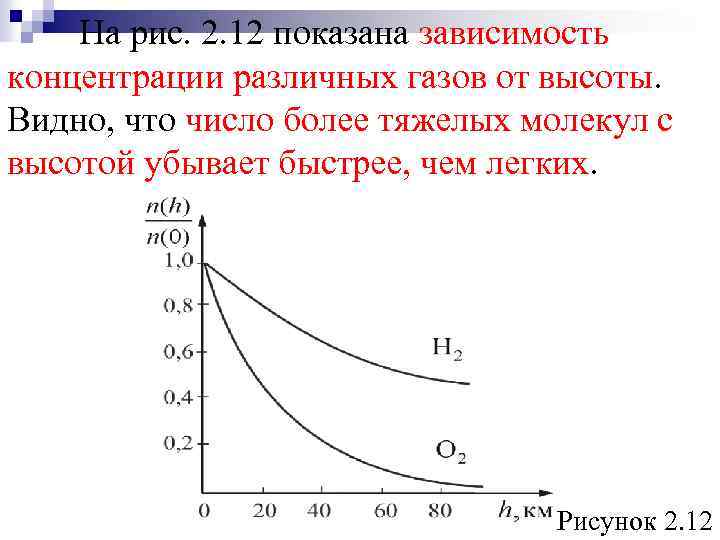
На рис. 2. 12 показана зависимость концентрации различных газов от высоты. Видно, что число более тяжелых молекул с высотой убывает быстрее, чем легких. Рисунок 2. 12

Из (2. 5. 3) можно получить, что отношение концентраций молекул в точках с U 1 и U 2 обладающих именно таким значением (2. 5. 4) Больцман доказал, что соотношение (2. 5. 3) справедливо не только в потенциальном поле сил гравитации, но и в любом потенциальном поле, для совокупности любых одинаковых частиц, находящихся в состоянии хаотического теплового движения.

2. 6. Закон распределения Максвелла -Больцмана В п. 2. 3 мы получили выражение для распределения молекул по скоростям (распределение Максвелла): (2. 6. 1)

Из этого выражения легко найти распределение молекул газа по значениям кинетической энергии K. Для этого перейдём от переменной υ к переменной : где dn(K) – число молекул, имеющих кинетическую энергию поступательного движения, заключённую в интервале от K до

Отсюда получим функцию распределения молекул по энергиям теплового движения: (2. 6. 2) Средняя кинетическая молекулы идеального газа: энергия то есть получили результат, совпадающий с прежним результатом, полученным в п. 1. 3.

Итак, закон Максвелла даёт распределение частиц по значениям кинетической энергии а закон Больцмана – распределение частиц по значениям потенциальной энергии. Оба распределения можно объединить в единый закон Максвелла-Больцмана, согласно которому, число молекул в единице объёма, скорости которых лежат в пределах от υ до равно: (2. 6. 3)

Обозначим Тогда – полная энергия. (2. 6. 4) Это и есть закон распределения Максвелла-Больцмана. Здесь n 0 – число молекул в единице объёма в той точке, где ; .

В последнем выражении, потенциальная и кинетическая энергии, а следовательно и полная энергия Е, могут принимать непрерывный ряд значений. Если же энергия частицы может принимать лишь дискретный ряд значений Е 1, Е 2. . . (как это имеет место, например, для внутренней энергии атома), то в этом случае распределение Больцмана имеет вид: , (2. 6. 5)

где Ni – число частиц, находящихся в состоянии с энергией Еi, а А – коэффициент пропорциональности, который должен удовлетворять условию: где N – полное число частиц в рассматриваемой системе.

1. Скорости газовых молекул. Опыт Штерна. Поставьте себя на место исследователей 60 -х годов позапрошлого столетия. Сформулирована молекулярно-кинетическая теория, но нет никаких доказательств существования самих молекул! А вся теория базируется на предположении о движении молекул. С какой они движутся скоростью? И как эту скорость измерить, если молекулы невидимы. Из уравнения молекулярно-кинетической теории газов известно, что (13. 1)
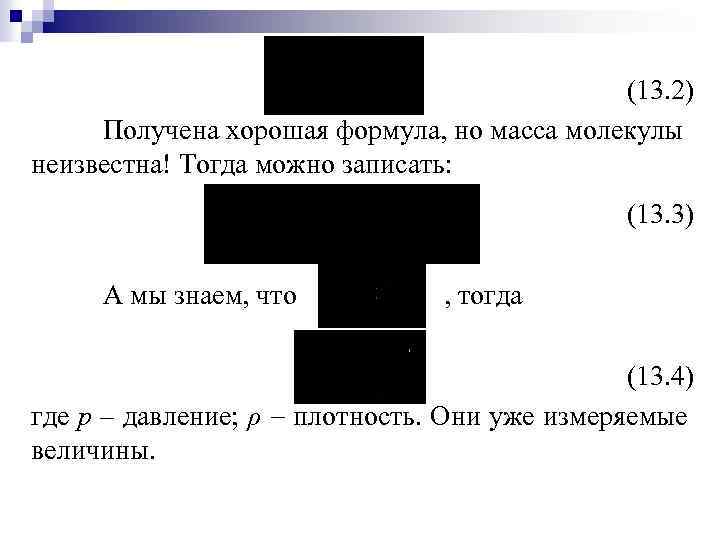
(13. 2) Получена хорошая формула, но масса молекулы неизвестна! Тогда можно записать: (13. 3) А мы знаем, что , тогда (13. 4) где р – давление; ρ плотность. Они уже измеряемые величины.


Thank you!
лек.11 молекулярно-кинетическая теория.ppt