Молекулярно-генетические аспекты канцерогенеза..ppt
- Количество слайдов: 12
 Молекулярно-генетические аспекты канцерогенеза Выполнил студент 324 группы Козлов В. Д.
Молекулярно-генетические аспекты канцерогенеза Выполнил студент 324 группы Козлов В. Д.
 ПРИРОДА РАКА. Когда мы говорим рак, то имеем ввиду более чем 100 различных разновидностей этой болезни. Она поражает почти все ткани организма, но при этом у всех видов рака есть общие черты. Сейчас мы постараемся представить себе именно эти общие черты. Во- первых отметим два принципиальных различия между раком и другими генетическими болезнями: Рак вызывается по большей части соматическими мутациями. Каждый индивидуальный случай рака происходит в результате накопления нескольких мутаций. Клетки нашего организма распределены по категориям, типам, которые определенно отличаются друг от друга. Таких категорий около 200. Это дифференцированные клетки.
ПРИРОДА РАКА. Когда мы говорим рак, то имеем ввиду более чем 100 различных разновидностей этой болезни. Она поражает почти все ткани организма, но при этом у всех видов рака есть общие черты. Сейчас мы постараемся представить себе именно эти общие черты. Во- первых отметим два принципиальных различия между раком и другими генетическими болезнями: Рак вызывается по большей части соматическими мутациями. Каждый индивидуальный случай рака происходит в результате накопления нескольких мутаций. Клетки нашего организма распределены по категориям, типам, которые определенно отличаются друг от друга. Таких категорий около 200. Это дифференцированные клетки.
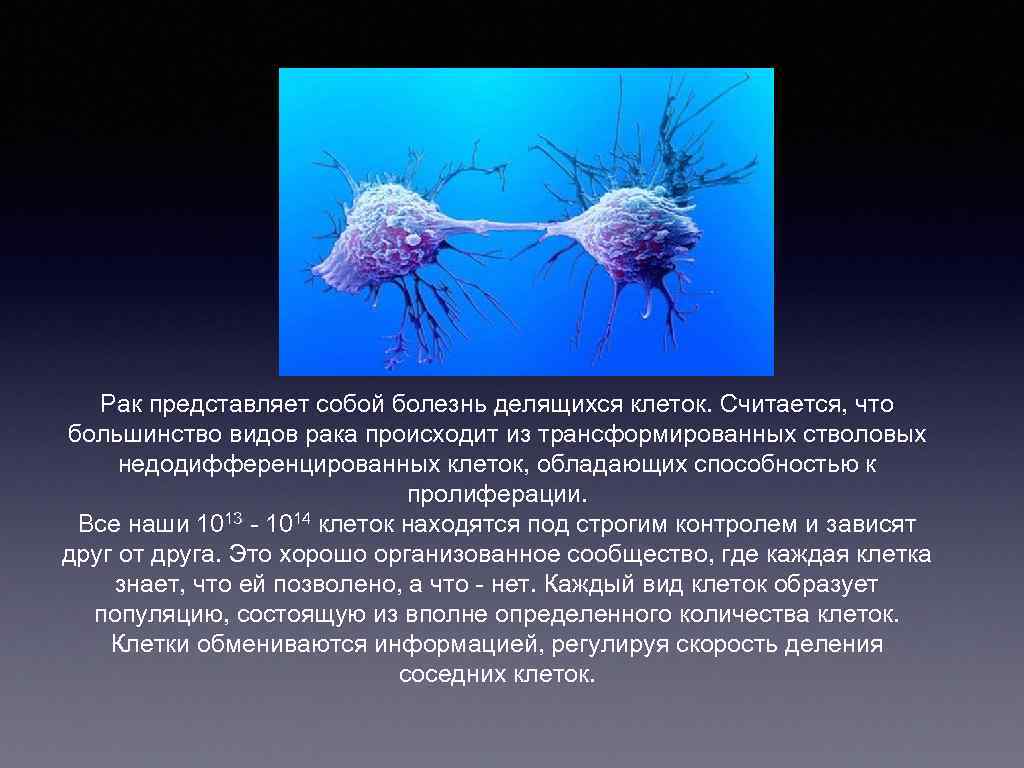 Рак представляет собой болезнь делящихся клеток. Считается, что большинство видов рака происходит из трансформированных стволовых недодифференцированных клеток, обладающих способностью к пролиферации. Все наши 1013 - 1014 клеток находятся под строгим контролем и зависят друг от друга. Это хорошо организованное сообщество, где каждая клетка знает, что ей позволено, а что - нет. Каждый вид клеток образует популяцию, состоящую из вполне определенного количества клеток. Клетки обмениваются информацией, регулируя скорость деления соседних клеток.
Рак представляет собой болезнь делящихся клеток. Считается, что большинство видов рака происходит из трансформированных стволовых недодифференцированных клеток, обладающих способностью к пролиферации. Все наши 1013 - 1014 клеток находятся под строгим контролем и зависят друг от друга. Это хорошо организованное сообщество, где каждая клетка знает, что ей позволено, а что - нет. Каждый вид клеток образует популяцию, состоящую из вполне определенного количества клеток. Клетки обмениваются информацией, регулируя скорость деления соседних клеток.
 Раковая клетка выходит из под этого контроля ( трансформация опухлевая ) и начинает жить по своей собственной программе, безудержно размножаясь и игнорируя сигналы из окружения. Она образует множество себе подобных клеток, которые приобретают способность отрываться от своего первоначального места, мигрировать в другие части тела и размножаться там, образуя метастазы. Чем дальше, тем агрессивнее становятся эти клетки, и в конце концов, когда они поражают жизненно важные системы организма, организм погибает. Канцерогенез - многоступенчатый процесс накопления мутаций и других генетических изменений, приводящих к нарушениям регуляции клеточного цикла , апоптоза , дифференцировки , морфогенетических реакций клетки , противоопухолевого иммунитета.
Раковая клетка выходит из под этого контроля ( трансформация опухлевая ) и начинает жить по своей собственной программе, безудержно размножаясь и игнорируя сигналы из окружения. Она образует множество себе подобных клеток, которые приобретают способность отрываться от своего первоначального места, мигрировать в другие части тела и размножаться там, образуя метастазы. Чем дальше, тем агрессивнее становятся эти клетки, и в конце концов, когда они поражают жизненно важные системы организма, организм погибает. Канцерогенез - многоступенчатый процесс накопления мутаций и других генетических изменений, приводящих к нарушениям регуляции клеточного цикла , апоптоза , дифференцировки , морфогенетических реакций клетки , противоопухолевого иммунитета.
 Ключевую роль в возникновении указанных свойств неопластической клетки играют нарушения функции опухолевых супрессоров и протоонкогенов. Исследования последних лет позволили идентифицировать сигнальные пути, контролируемые большинством этих генов. Выяснилось, что многие из них регулируют активность одних и тех же путей на разных этажах передачи сигналов. Оказалось, что некоторые из таких сигнальных путей одновременно вовлечены в регуляцию нескольких важнейших физиологических процессов. Продукты некоторых из опухолевых супрессоров и протоонкогенов являются местами пересечения различных сигнальных путей. Отсюда становится понятной частая встречаемость изменений генов р53 и RAS в самых разных новообразованиях - их мутации позволяют за один шаг преодолеть несколько важных этапов опухолевой прогрессии и придать неопластической клетке сразу несколько необходимых свойств.
Ключевую роль в возникновении указанных свойств неопластической клетки играют нарушения функции опухолевых супрессоров и протоонкогенов. Исследования последних лет позволили идентифицировать сигнальные пути, контролируемые большинством этих генов. Выяснилось, что многие из них регулируют активность одних и тех же путей на разных этажах передачи сигналов. Оказалось, что некоторые из таких сигнальных путей одновременно вовлечены в регуляцию нескольких важнейших физиологических процессов. Продукты некоторых из опухолевых супрессоров и протоонкогенов являются местами пересечения различных сигнальных путей. Отсюда становится понятной частая встречаемость изменений генов р53 и RAS в самых разных новообразованиях - их мутации позволяют за один шаг преодолеть несколько важных этапов опухолевой прогрессии и придать неопластической клетке сразу несколько необходимых свойств.
 В то же время для ряда новообразований, и в первую очередь для лейкозов, характерны генетические изменения, встречающиеся только при данном заболевании. К ним относятся прежде всего хромосомные транслокации, перемещающие протоонкогены и/или опухолевые супрессоры в другое место генома. Специфичность таких изменений объясняется, повидимому, тремя основными причинами.
В то же время для ряда новообразований, и в первую очередь для лейкозов, характерны генетические изменения, встречающиеся только при данном заболевании. К ним относятся прежде всего хромосомные транслокации, перемещающие протоонкогены и/или опухолевые супрессоры в другое место генома. Специфичность таких изменений объясняется, повидимому, тремя основными причинами.
 Во-первых, в определенных типах клеток может быть значительно повышена вероятность некоторых генетических перестроек. Так, в ходе дифференцировки В-лимфоцитов происходит запрограммированная перестройка генов иммуноглобулинов. Закономерной ошибкой таких перестроек являются хромосомные транслокации, соединяющие гены иммуноглобулинов с протоонкогеном MYC, содержащим в своем составе специфические сигнальные последовательности, которые распознаются рекомбиназами, осуществляющими перестройку генов иммуноглобулинов. Естественно предположить, что в предшественниках В-лимфоцитов такие транслокации, нарушающие нормальную регуляцию белка Myc, происходят чаще, чем другие мутации, приводящие к сходным биологическим последствиям. Во-вторых, тканеспецифичными могут быть экспрессия или действие определенных онкогенов/опухолевых супрессоров.
Во-первых, в определенных типах клеток может быть значительно повышена вероятность некоторых генетических перестроек. Так, в ходе дифференцировки В-лимфоцитов происходит запрограммированная перестройка генов иммуноглобулинов. Закономерной ошибкой таких перестроек являются хромосомные транслокации, соединяющие гены иммуноглобулинов с протоонкогеном MYC, содержащим в своем составе специфические сигнальные последовательности, которые распознаются рекомбиназами, осуществляющими перестройку генов иммуноглобулинов. Естественно предположить, что в предшественниках В-лимфоцитов такие транслокации, нарушающие нормальную регуляцию белка Myc, происходят чаще, чем другие мутации, приводящие к сходным биологическим последствиям. Во-вторых, тканеспецифичными могут быть экспрессия или действие определенных онкогенов/опухолевых супрессоров.
 В-третьих, для приобретения злокачественного фенотипа разные типы клеток могут нуждаться в неодинаковых наборах биологических свойств. Так, для гемопоэтических клеток по сравнению с клетками других тканей менее существенным представляется приобретение таких признаков, как потеря контактного торможения размножения и локомоторный фенотип. Определяющими для их злокачественной трансформации являются, по- видимому, стимуляция пролиферации, подавление апоптоза и блокирование специфической дифференцировки. Поэтому при развитии гемобластозов особой селективной ценностью обладают, очевидно, перестройки типа PML/RARa, способные сразу придавать клеткам некоторых типов эти три важнейших свойства. Несмотря на достигнутый в последние годы значительный прогресс в понимании базовых механизмов канцерогенеза, много вопросов остаются неясными. Среди них важное место занимают механизмы тканеспецифического действия онкогенов и опухолевых супрессоров. Можно думать, что исследование этой проблемы станет в ближайшее время одной из наиболее бурно развивающихся областей онкологии.
В-третьих, для приобретения злокачественного фенотипа разные типы клеток могут нуждаться в неодинаковых наборах биологических свойств. Так, для гемопоэтических клеток по сравнению с клетками других тканей менее существенным представляется приобретение таких признаков, как потеря контактного торможения размножения и локомоторный фенотип. Определяющими для их злокачественной трансформации являются, по- видимому, стимуляция пролиферации, подавление апоптоза и блокирование специфической дифференцировки. Поэтому при развитии гемобластозов особой селективной ценностью обладают, очевидно, перестройки типа PML/RARa, способные сразу придавать клеткам некоторых типов эти три важнейших свойства. Несмотря на достигнутый в последние годы значительный прогресс в понимании базовых механизмов канцерогенеза, много вопросов остаются неясными. Среди них важное место занимают механизмы тканеспецифического действия онкогенов и опухолевых супрессоров. Можно думать, что исследование этой проблемы станет в ближайшее время одной из наиболее бурно развивающихся областей онкологии.
 Известно примерно 50 наследственных форм рака ( Knudson A. G. , 1993 ). Эти же формы могут быть и ненаследственными, а спорадическими. Предрасположенность к раку наследуется как обычный Менделевский доминантный признак с той или иной степенью пенетрантности и возникновеннием в более раннем возрасте, чем спорадические формы. Среди наследственных раков известны самые разные формы - карциномы различной локализации, нейробластомы , нейрофиброматоз , множественные эндокринные неоплазии , детские раки ( ретинобластома , опухоль Вилмса ). В поисках генов супрессирующих злокачественное перерождение клеток изучаются генетические механизмы, определяющие различные формы наследственных и спорадических форм злокачественных опухолей. Однако наибольшее число исследований посвящено гену rb , контролирующему развитие ретинобластомы и гену, кодирующему белок р53.
Известно примерно 50 наследственных форм рака ( Knudson A. G. , 1993 ). Эти же формы могут быть и ненаследственными, а спорадическими. Предрасположенность к раку наследуется как обычный Менделевский доминантный признак с той или иной степенью пенетрантности и возникновеннием в более раннем возрасте, чем спорадические формы. Среди наследственных раков известны самые разные формы - карциномы различной локализации, нейробластомы , нейрофиброматоз , множественные эндокринные неоплазии , детские раки ( ретинобластома , опухоль Вилмса ). В поисках генов супрессирующих злокачественное перерождение клеток изучаются генетические механизмы, определяющие различные формы наследственных и спорадических форм злокачественных опухолей. Однако наибольшее число исследований посвящено гену rb , контролирующему развитие ретинобластомы и гену, кодирующему белок р53.
 Гены, участвующие в трансформации клеток: Генетика рака заставляет пересматривать простые догмы о причинноследственной связи в заболеваниях. Рак это пример сложной мультифакторной генетической болезни. В развитие опухолей вовлекается громадное разнообразие генов. Происходит разрегулирование множества клеточных функций, включая механизмы контроля клеточной пролиферации , репарации ДНК , стабильности хромосом , межклеточных взаимодействий , взаимодействий клеток с матриксом , ангиогенеза , клеточного старения , апоптоза и т. д. Гены, вовлеченые в опухолеобразование могут действовать на опухолевую прогрессию , либо меняя структуру кодируемого продукта вследствие мутациий, либо вследствие изменений в их экспрессии в ответ на какие-либо события в клетке. В результате может облегчаться инициация прогрессии опухоли, как происходит при активации протоонкогенов, или может сниматься ингибирование этой прогрессии, как происходит при инактивации супрессоров опухолей. То, что не только мутации, меняющие структуру продуктов протоонкогенов, но и изменение уровня их экспрессии может приводить к стимуляции опухоли, легко видеть на примере стимуляции опухолевой трансформации при внедрении рядом с протоонкогенами ретровирусов, не содержащих онкогенов. При этом ретровирус меняет экспрессию протоонкогенов, но не их структуру. При опухолеобразовании часто наблюдается амплификация области хромосом, содержащих протоонкогены. Это также приводит к увеличению количества синтезированных продуктов, а не к изменению их струтур.
Гены, участвующие в трансформации клеток: Генетика рака заставляет пересматривать простые догмы о причинноследственной связи в заболеваниях. Рак это пример сложной мультифакторной генетической болезни. В развитие опухолей вовлекается громадное разнообразие генов. Происходит разрегулирование множества клеточных функций, включая механизмы контроля клеточной пролиферации , репарации ДНК , стабильности хромосом , межклеточных взаимодействий , взаимодействий клеток с матриксом , ангиогенеза , клеточного старения , апоптоза и т. д. Гены, вовлеченые в опухолеобразование могут действовать на опухолевую прогрессию , либо меняя структуру кодируемого продукта вследствие мутациий, либо вследствие изменений в их экспрессии в ответ на какие-либо события в клетке. В результате может облегчаться инициация прогрессии опухоли, как происходит при активации протоонкогенов, или может сниматься ингибирование этой прогрессии, как происходит при инактивации супрессоров опухолей. То, что не только мутации, меняющие структуру продуктов протоонкогенов, но и изменение уровня их экспрессии может приводить к стимуляции опухоли, легко видеть на примере стимуляции опухолевой трансформации при внедрении рядом с протоонкогенами ретровирусов, не содержащих онкогенов. При этом ретровирус меняет экспрессию протоонкогенов, но не их структуру. При опухолеобразовании часто наблюдается амплификация области хромосом, содержащих протоонкогены. Это также приводит к увеличению количества синтезированных продуктов, а не к изменению их струтур.
 В развитие раковой опухоли вовлекается значительно большее число генов, чем количество генов, реально получивших мутации. Сегодня часто высказывается мнение, что на самом деле "раковым" геном следует считать любой ген, изменение структуры или экспрессии которого вовлекается в качестве необходимого элемента опухолеобразования. Например, повышенная экспрессия немутантного рецептора эпидермального ростового фактора или эстрогенового рецептора может оказаться онкогенным. Другой пример: раковые гены, такие как myc, p 53, WT 1 кодируют транскрипционные факторы, которые в свою очередь регулируют экспрессию множества других генов. Ясно, что изменение в уровне их экспрессии может вызывать целый каскад событий, среди которых могут оказываться и такие, которые приведут к опухолевому изменению фенотипа клетки. Среди таких событий могут оказаться и изменения, которые вызывают дестабилизацию генома клетки. Мы увидим позже, что возможно это необходимый пререквизит опухолевой трансформации. Ведь для быстрого прогресса опухоли нужно несколько мутационных событий. В нормальной клетке мутации возникают с незначительной скоростью. Чтобы эту скорость повысить и нужны изменения, которые приводят к дестабилизации генома. Пути для этого могут быть разными, но стадия дестабилизации генома является, возможно, универсальным событием на пути к опухоли.
В развитие раковой опухоли вовлекается значительно большее число генов, чем количество генов, реально получивших мутации. Сегодня часто высказывается мнение, что на самом деле "раковым" геном следует считать любой ген, изменение структуры или экспрессии которого вовлекается в качестве необходимого элемента опухолеобразования. Например, повышенная экспрессия немутантного рецептора эпидермального ростового фактора или эстрогенового рецептора может оказаться онкогенным. Другой пример: раковые гены, такие как myc, p 53, WT 1 кодируют транскрипционные факторы, которые в свою очередь регулируют экспрессию множества других генов. Ясно, что изменение в уровне их экспрессии может вызывать целый каскад событий, среди которых могут оказываться и такие, которые приведут к опухолевому изменению фенотипа клетки. Среди таких событий могут оказаться и изменения, которые вызывают дестабилизацию генома клетки. Мы увидим позже, что возможно это необходимый пререквизит опухолевой трансформации. Ведь для быстрого прогресса опухоли нужно несколько мутационных событий. В нормальной клетке мутации возникают с незначительной скоростью. Чтобы эту скорость повысить и нужны изменения, которые приводят к дестабилизации генома. Пути для этого могут быть разными, но стадия дестабилизации генома является, возможно, универсальным событием на пути к опухоли.
 Этапы понимания молекулярных механизмов канцерогенеза
Этапы понимания молекулярных механизмов канцерогенеза


