Наследственные заболевания 4-5л.ppt
- Количество слайдов: 96

Молекулярная природа наследственных заболеваний и современные подходы к их лечению С. Е. ДРОМАШКО Институт генетики и цитологии НАН Беларуси Беларусь, Минск 220072, ул. Академическая, 27, тел. : +375(17)284 -21 -90, e-mail: S. Dromashko@igc. bas-net. by

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Здоровье или предрасположенность к различным заболеваниям в значительной мере зависит от генетических особенностей человека. Расшифровка структуры его генома открыла недоступные ранее возможности для понимания молекулярных основ наследственных болезней, разработки новых стратегий диагностики и лечения. Всего известно 5 тыс. наследственных заболеваний, из них 2 тыс. - тяжелых расстройств, приводящих к инвалидности. До недавнего времени были изучены главным образом моногенные болезни, т. е. возникающие при нарушении работы одного гена. Их сегодня известно более тысячи - от них в общей сложности страдает около 5% новорожденных.

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Большинство наследственных болезней связаны с одновременным нарушением работы нескольких генов и определенными воздействиями внешней среды - их называют мультифакторными. В той или иной мере наследственные особенности определяют восприимчивость или устойчивость к большинству заболеваний, в том числе и к инфекционным. В конечном итоге здоровье или болезнь есть результат взаимодействия наследственных задатков и среды. Геномные исследования позволяют выявлять предрасположенность к ряду патологий на любой стадии развития организма, что безусловно расширяет объем пресимптоматической, дородовой и преимплантационной (предшествующей внедрению зародыша в матку) диагностики. Для этого проводится анализ ДНК, получаемой обычно из крови или других биологических образцов индивида.

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Термины «Наследственные болезни» и «Врожденные болезни» не являются синонимами, так как врожденные болезни (проявляющиеся с момента рождения) могут быть обусловлены как наследственными, так и средовыми тератогенными факторами(сифилис, краснуха). В то же время не все наследственные болезни являются врожденными (вероятность, их около 50%). Некоторые болезни проявляются в детском возрасте (миопатия Дюшенна, гемофилия), другие- в зрелом (миотоническая дистония, хорея Гентингтона) и даже в пожилом возрасте (болезнь Альцгеймера).

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Наследственные заболевания обусловлены хромосомными или генными мутациями. У человека различают наследственные заболевания с полным проявлением мутации (все хромосомные и некоторые генные) – синдром Дауна, гемофилия А, В, С, фенилкетонурия и др. ; с неполным (зависящим от условий среды) проявлением мутаций – некоторые формы диабета, подагра и др. ; возникающие из-за внешних факторов, но обусловленные генетической предрасположенностью к ним – аллергия, атеросклероз, рахит и др. Среди генных наследственных заболеваний выделяют моногенные и полигенные (мультифакторные), а среди моногенных различают формы с разным типом наследования (аутосомно-доминантные, аутосомно-рецессивные, доминантные и рецессивные сцепленные с полом). Доля наследственных заболеваний составляет около 10% всех заболеваний человека.
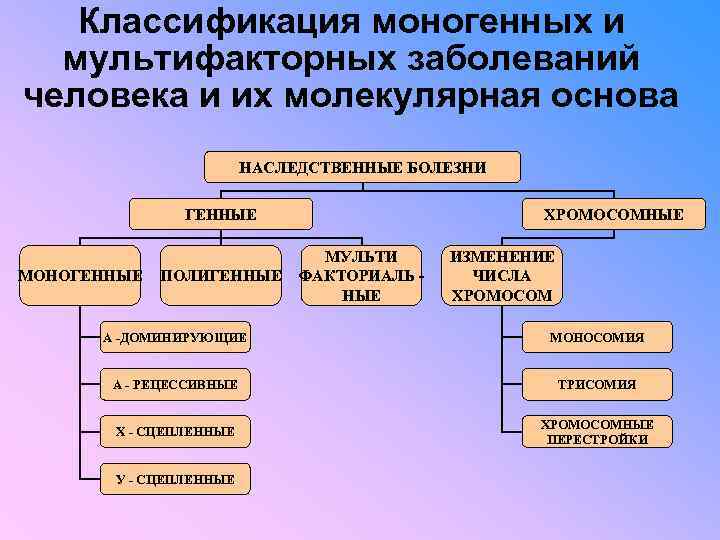
Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа НАСЛЕДСТВЕННЫЕ БОЛЕЗНИ ГЕННЫЕ МОНОГЕННЫЕ ПОЛИГЕННЫЕ ХРОМОСОМНЫЕ МУЛЬТИ ФАКТОРИАЛЬ НЫЕ ИЗМЕНЕНИЕ ЧИСЛА ХРОМОСОМ А -ДОМИНИРУЮЩИЕ МОНОСОМИЯ А - РЕЦЕССИВНЫЕ ТРИСОМИЯ Х - СЦЕПЛЕННЫЕ ХРОМОСОМНЫЕ ПЕРЕСТРОЙКИ У - СЦЕПЛЕННЫЕ

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа С достаточной уверенностью можно утверждать, что многие мутации генов и практически все аберрации хромосом неблагоприятны как для индивида, так и для популяции; большинство хромосомных аберраций губит зиготу в период эмбрионального развития, меньшая часть таких зигот доживает до рождения и продолжает существовать дальше, но пораженные пациенты страдают тяжелыми врожденными пороками. Генные мутации часто ведут к врожденным заболеваниям с простым типом наследования или к дефектам в мультифакториальных генетических системах. Доля благоприятных мутаций, в лучшем случае, очень незначительна.

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Частота численных аберраций хромосом увеличивается с возрастом матери, поэтому любой сдвиг в материнском возрасте приведет к соответствующему изменению в общей распространенности таких хромосомных мутаций. Во многих современных популяциях существует тенденция к уменьшению числа детей в семье и концентрация деторождения в возрастной группе с наименьшим риском (женщины в возрасте от 20 до 30 лет). Было подсчитано, что в западных странах и в Японии эта тенденция должна была уменьшить число детей с синдромом Дауна на 25– 40%. Однако ряд последних исследований показывает, что склонность многих современных женщин откладывать рождение ребенка на несколько более поздний возраст легко может привести к изменению этой тенденции на противоположную.

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Для многих генов частота мутаций увеличивается с возрастом отца, поэтому любой сдвиг в возрастной структуре отцов соответствующим образом повлияет на частоту мутаций. Для редких аутосомно-доминантных состояний изменения под действием возраста отца не будут столь крупными, как для численных хромосомных аберраций; влияние возраста отца на частоту мутаций в доминантных и сцепленных с Х-хромосомой генов меньше возраста матери на частоту численных аномалий хромосом. С медицинских позиций общее воздействие отцовского возраста представляется относительно небольшим и практически не принимается в расчет фактический риск поражения доминантной мутацией ребенка, имеющего пожилого отца.

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Хромосомные болезни - это группа болезней, в основе развития которых лежат нарушения числа или структуры хромосом, возникающие в гаметах родителей или на ранних стадиях дробления зиготы. История изучения Х. б. берет начало с клинических исследований, проводившихся задолго до описания хромосом человека и открытия хромосомных аномалий. Х. б. - болезнь Дауна (трисомия 21), синдромы: Тернера (трисомия 18), Клайнфелтера, Патау (трисомия 13), Эдвардса.

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа В настоящее время описано 2 варианта нарушений числа хромосомных наборов - тетраплоидия и триплодия. Другая группа синдромов обусловлена нарушениями числа отдельных хромосом – трисомиями (когда имеется добавочная хромосома в диплоидном наборе) или моносомия (одна из хромосом отсутствует). Моносомии аутосом несовместимы с жизнью. Трисомии – более часто встречающаяся паталогия у человека. Ряд хромосомных болезней связан с нарушением числа половых хромосом. Самая многочисленная группа Х. б. - это синдромы, обусловленные структурными перестройками хромосом. Выделяют хромосомные синдромы так называемых частичных моносомий (увеличение или уменьшение числа отдельных хромосом не на целую хромосому, а на ее часть).

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Моногенные заболевания При фенилкетонурии мутации нарушают работу гена, контролирующего превращение аминокислоты фенилаланина в тирозин. Болезнь развивается, когда ребенок получает поврежденный ген от обоих родителей. Если один из пары генов нормален, человек остается здоровым. Сегодня частота появления фенилкетонурии (т. е. мутаций в обеих копиях гена) составляет 1 на 10 -17 тыс. рождений, а частота скрытого носительства болезнетворного аллеля - 1 на 100. Поскольку эта патология встречается достаточно часто, всех новорожденных тестируют на фенилкетонурию. Вовремя назначенная специальная диета может предотвратить болезнь или значительно облегчить ее течение. У каждого народа свой спектр характерных мутаций. Например, в Волго. Уральском регионе России фенилкетонурия особенно часто встречается среди русских. Большинство случаев заболевания вызвано одной и той же мутацией, принесенной сюда переселенцами из Северной Европы. В семьях других национальностей фенилкетонурия вызывается несколькими различными мутациями.

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа При аутосомно-рецессивном заболевании - болезни Вильсона. Коновалова из-за мутаций в гене, связанном с обменом меди, в организме накапливается медь. В результате ее токсического действия поражаются печень и головной мозг. Заболевание долгое время протекает скрыто, ранние проявления весьма многообразны, что затрудняет его выявление. Болезнью Вильсона-Коновалова страдают во всем мире, причем некоторые народы особенно часто. Так, у евреев-ашкенази ее частота в 30 раз превышает среднемировую. В настоящее время известно более 70 различных мутаций, приводящих к этой патологии. Распространенность любой из них указывает на время появления: чем чаще встречается мутация, тем она древней (возникла на ранних этапах формирования человечества). Для русских наиболее характерна мутация, распространенная среди европейских народов. В некоторых этнических группах, наряду с широко известными, можно обнаружить “молодые” мутации, свойственные только им. Например, у представителей татарской национальности выявлена мутация, которая нигде больше не встречается. Молекулярно-генетический анализ позволил предположить ее тюркские корни.

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Этнические особенности обнаружены в спектре и частоте мутаций для такой тяжелой патологии, как муковисцидоз. У представителей белой расы - это одно из самых распространенных моногенных заболеваний. Изменения в гене белка, участвующего в переносе ионов хлора через клеточную мембрану, приводят к нарушению секреции эндокринных желез жизненно важных органов с поражением дыхательного и желудочно-кишечного трактов. В Башкортостане выявлено девять связанных с муковисцидозом мутаций, а всего в мире их описано более тысячи. В Волжско. Уральском регионе “европейская” мутация найдена у русских и татар, а “тюркская” - у татар и башкир.

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Большинство моногенных мутаций проявляется на ранних этапах развития - в детстве или даже во внутриутробном периоде. При болезнях плода чаще всего нарушается работа белков, регулирующих одновременно множество генов (факторов транскрипции). На первом году жизни наиболее часты нарушения, связанные с обменом веществ. Однако некоторые генетические дефекты могут не проявляться до глубокой старости. Например, в генах белков пресениллинов (PS) найдены мутации, приводящие к болезни Альцгеймера - одной из форм старческого слабоумия. А встраивание избыточных тринуклеотидных повторов в “гентингтон”-ген связано с другой болезнью, также проявляющейся в преклонном возрасте, - хореей Гентингтона.
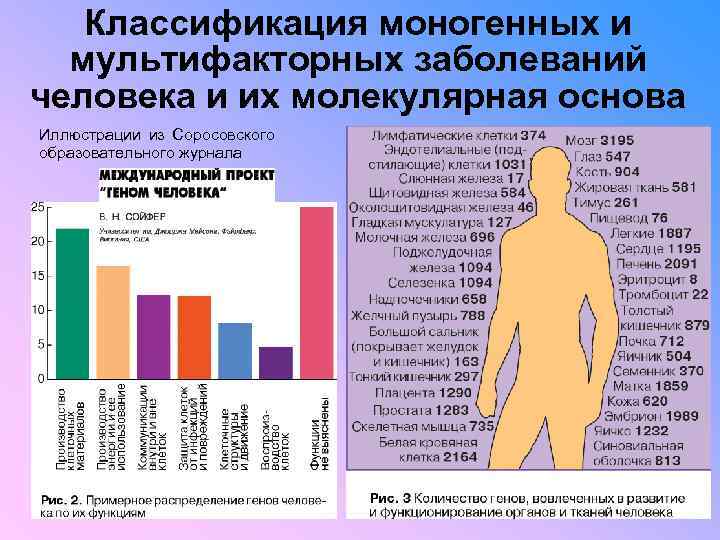
Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Иллюстрации из Соросовского образовательного журнала

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Мультифакторные заболевания К заболеваниям, развитие которых зависит от взаимодействия множества факторов, как наследственных, так и средовых, относят диабет, ишемическую болезнь сердца, эссенциальную гипертензию, бронхиальную астму, алкогольный психоз, наркоманию. Сегодня уже известны некоторые гены, обусловливающие предрасположенность к ним. Патогенные мутации в этих генах не обязательно приводят к заболеванию, но риск его развития повышен. Предрасположенность к таким мультифакторным болезням возникает, когда генетическими отклонениями нарушена регуляция нервных процессов, обмена веществ (например, липидов или углеводов) или работа систем обезвреживания чужеродных веществ (ксенобиотиков).
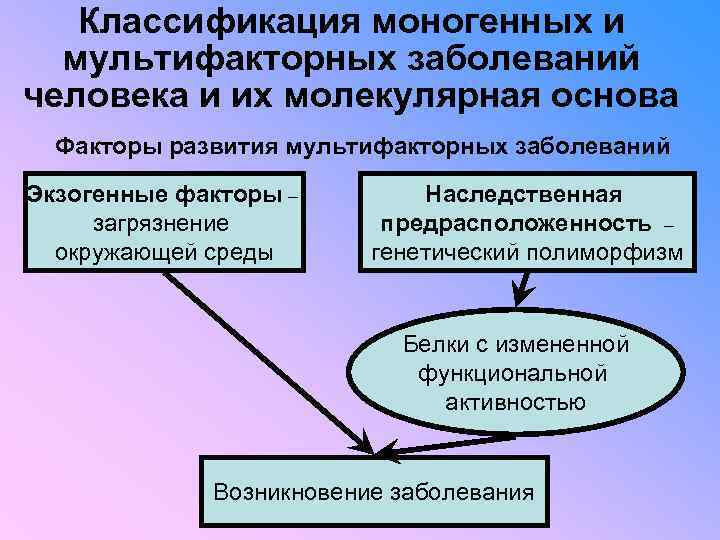
Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Факторы развития мультифакторных заболеваний Экзогенные факторы – загрязнение окружающей среды Наследственная предрасположенность – генетический полиморфизм Белки с измененной функциональной активностью Возникновение заболевания

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Попав в организм, ксенобиотики разлагаются в два этапа: сначала подвергаются ферментативной модификации, а лишь затем промежуточные метаболиты превращаются в растворимые безвредные соединения и выводятся. Различные варианты генов, кодирующих ферменты системы детоксикации, определяют скорость их работы. При сочетании высокой активности ферментов первого этапа и низкой на втором этапе в организме человека накапливаются промежуточные продукты, обладающие порой даже более высокой токсичностью, чем исходные вещества. Так, при сниженной активности детоксификационной функции плаценты (фермента плацентарной глютатионметионинтрансферазы, GSTM 1) возрастает риск ранних спонтанных абортов. Генетически детерминированная активность глютатионтрансфераз влияет и на развитие различных форм рака. Например, сочетание определенных мутаций увеличивает риск рака груди у женщин в 3 -10 раз, а у курильщиц - в 40 раз.

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Эффективность лечения различными препаратами также связана с состоянием генов. Так, лечение эндометриоза (заболевания, встречающегося почти у 10% женщин белой расы) широко используемым препаратом циклофероном у части больных безрезультатно по причинам генетического характера. Мультифакторные заболевания отличаются от моногенных тем, что связь между генетическими особенностями и вероятностью развития патологии для них гораздо сложнее. В разных популяциях болезнь может вызываться своеобразной комбинацией генетических и средовых факторов. Роль генетических факторов во многом зависит от условий среды и образа жизни человека.
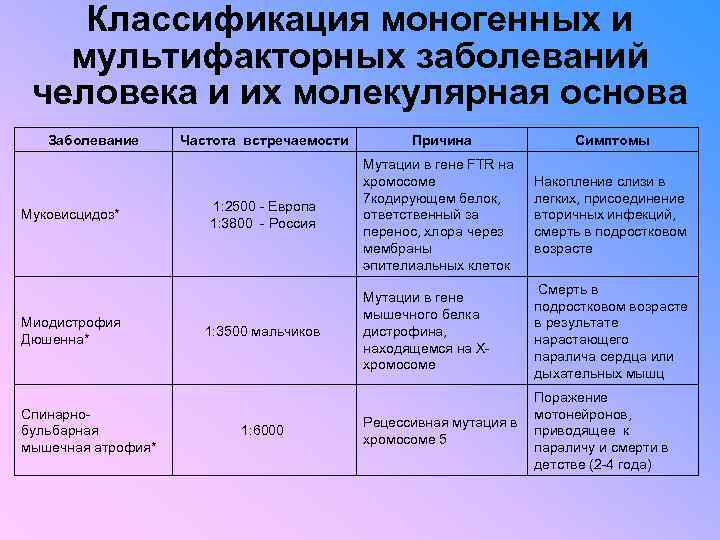
Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Заболевание Муковисцидоз* Миодистрофия Дюшенна* Спинарнобульбарная мышечная атрофия* Частота встречаемости Причина Симптомы 1: 2500 - Европа 1: 3800 - Россия Мутации в гене FTR на хромосоме 7 кодирующем белок, ответственный за перенос, хлора через мембраны эпителиальных клеток Накопление слизи в легких, присоединение вторичных инфекций, смерть в подростковом возрасте Мутации в гене мышечного белка дистрофина, находящемся на Ххромосоме Смерть в подростковом возрасте в результате нарастающего паралича сердца или дыхательных мышц 1: 3500 мальчиков 1: 6000 Поражение мотонейронов, Рецессивная мутация в приводящее к хромосоме 5 параличу и смерти в детстве (2 -4 года)
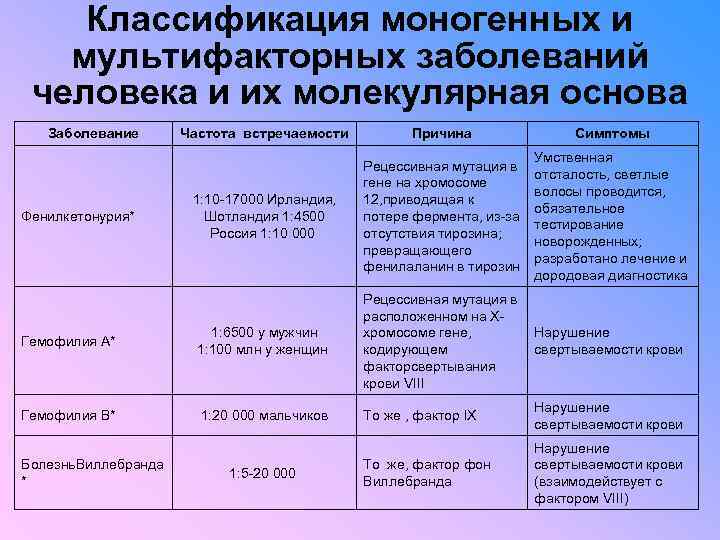
Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Заболевание Фенилкетонурия* Частота встречаемости Причина Симптомы 1: 10 -17000 Ирландия, Шотландия 1: 4500 Россия 1: 10 000 Рецессивная мутация в гене на хромосоме 12, приводящая к потере фермента, из-за отсутствия тирозина; превращающего фенилаланин в тирозин Умственная отсталость, светлые волосы проводится, обязательное тестирование новорожденных; разработано лечение и дородовая диагностика Гемофилия А* 1: 6500 у мужчин 1: 100 млн у женщин Рецессивная мутация в расположенном на Ххромосоме гене, Нарушение кодирующем свертываемости крови факторсвертывания крови VIII Гемофилия В* 1: 20 000 мальчиков То же , фактор IХ Нарушение свертываемости крови То же, фактор фон Виллебранда Нарушение свертываемости крови (взаимодействует с фактором VIII) Болезнь. Виллебранда * 1: 5 -20 000
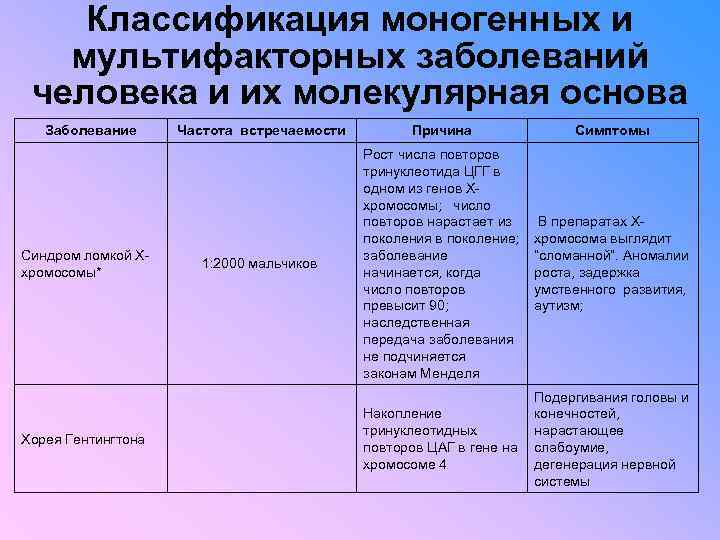
Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Заболевание Синдром ломкой Ххромосомы* Хорея Гентингтона Частота встречаемости Причина Симптомы 1: 2000 мальчиков Рост числа повторов тринуклеотида ЦГГ в одном из генов Ххромосомы; число повторов нарастает из поколения в поколение; заболевание начинается, когда число повторов превысит 90; наследственная передача заболевания не подчиняется законам Менделя В препаратах Ххромосома выглядит “сломанной”. Аномалии роста, задержка умственного развития, аутизм; Подергивания головы и конечностей, Накопление тринуклеотидных нарастающее повторов ЦАГ в гене на слабоумие, хромосоме 4 дегенерация нервной системы
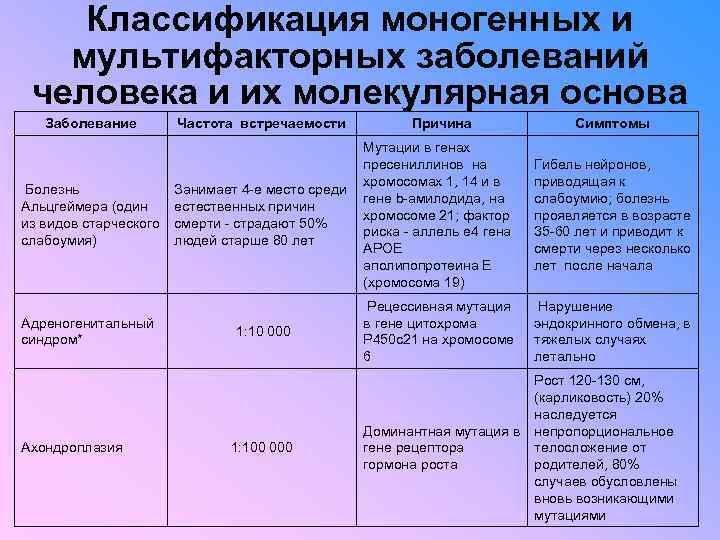
Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Заболевание Частота встречаемости Причина Симптомы Мутации в генах пресениллинов на хромосомах 1, 14 и в Болезнь Занимает 4 -е место среди гене b-амилодида, на Альцгеймера (один естественных причин хромосоме 21; фактор из видов старческого смерти - страдают 50% риска - аллель е 4 гена слабоумия) людей старше 80 лет APOE аполипопротеина Е (хромосома 19) Гибель нейронов, приводящая к слабоумию; болезнь проявляется в возрасте 35 -60 лет и приводит к смерти через несколько лет после начала Рецессивная мутация в гене цитохрома Р 450 с21 на хромосоме 6 Нарушение эндокринного обмена, в тяжелых случаях летально Адреногенитальный синдром* Ахондроплазия 1: 10 000 1: 100 000 Рост 120 -130 см, (карликовость) 20% наследуется Доминантная мутация в непропорциональное гене рецептора телосложение от гормона роста родителей, 80% случаев обусловлены вновь возникающими мутациями

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа К настоящему времени на хромосомах человека картировано около 800 генов, мутации которых приводят к различным наследственным заболеваниям. Количество моногенных заболеваний, для которых известна локализация контролирующего гена, еще больше и приближается к 950 за счет существования аллельных серий, то есть групп болезней, клинически сильно отличающихся друг от друга, но обусловленных мутациями в одном и том же гене. Среди них гены, орбусловливающие предрасположенность к остеопорозу (VDR-3), дефектам заращения нервной трубки (ДЗНТ), коронарной болезни сердца (КБС) и атеросклерозу (MTHFR), инфаркту миокарда (АСЕ), атеросклерозу (Аро. Е), аденоме и раку простаты (AR), диабету (IDDM-1 и -5), астме (СС 16) и др. Известны также онкогены (Ras, Miс) и антионкогены (p 53), мутации которых с большой вероятностью ведут к различным опухолям. Уже идентифицированы гены, мутации которых не только предрасполагают, но и с большой вероятностью вызывают серьезные заболевания (BRCA 1, BRCA 2 - рак молочной железы, PS-1, PS-2 - болезнь Альцгеймера и др. ). Быстро увеличивается и список наследственных болезней с поздней манифестацией, для которых вполне реальна ранняя досимптоматическая диагностика в любом возрасте (хорея Гентингтона, другие нейродегенеративные заболевания, рак толстой кишки, щитовидной железы и др. ).

Классификация моногенных и мультифакторных заболеваний человека и их молекулярная основа Наконец, уже сегодня можно выявлять гетерозиготное носительство наиболее частых смертельных наследственных болезней в семьях высокого риска (муковисцидоз, миодистрофия Дюшенна, фенилкетонурия, синдром Мартина-Белла, гемофилия, спинальная мышечная атрофия, адреногенитальный синдром). Очень важно, что эти и многие другие тяжелые наследственные недуги с успехом диагностируются еще пренатально, что позволяет предотвратить рождение больных детей.

Классификация наследственных заболеваний человека • В настоящее время описано 2 варианта нарушений числа хромосомных наборов - тетраплоидия и триплодия. Другая группа синдромов обусловлена нарушениями числа отдельных хромосом – трисомиями (когда имеется добавочная хромосома в диплоидном наборе) или моносомия (одна из хромосом отсутствует). Моносомии аутосом несовместимы с жизнью. Трисомии – более часто встречающаяся паталогия у человека. Ряд хромосомных болезней связан с нарушением числа половых хромосом. Самая многочисленная группа хромосомных болезней - это синдромы, обусловленные структурными перестройками хромосом. Выделяют хромосомные синдромы так называемых частичных моносомий (увеличение или уменьшение числа отдельных хромосом не на целую хромосому, а на ее часть).

Хромосомные заболевания человека • Механизмы, лежащие в основе геномных мутаций (аномалии числа хромосом). Аномалии числа хромосом могут быть вызваны разными причинами: 1. Наиболее важным механизмом является нерасхождение. Хромосомы, которые в норме должны разделиться во время клеточного деления, остаются соединенными вместе и в анафазе отходят к одному полюсу. Это может произойти в ходе митотического деления, но чаще наблюдается во время мейоза. У человека по неизвестным причинам именно акроцентрические хромосомы имеют тенденцию чаще вовлекаться в нерасхождение. Мейотическое нерасхождение было открыто Бриджесом (1916) у дрозофилы. На каждую гамету с одной добавочной хромосомой приходится другая, без одной хромосомы. После оплодотворения гаметой с нормальным набором хромосом зигота оказывается по одной из хромосом либо трисомной, либо моносомной. Соматическое нерасхождение в митотически делящихся клетках во время раннего развития может приводить к мозаицизму с наличием нормальных клеток, трисомиков и моносомиков.

Хромосомные заболевания человека 2. Вторым механизмом, обусловливающим геномные мутации, является утрата отдельной хромосомы вследствие «анафазного отставания» : во время анафазного движения одна хромосома может отстать от всех других. Утрата хромосом ведет к мозаицизму, при котором имеются одна эуплоидная и одна моносомная клеточная популяция У мыши стадия пронуклеусов (т. е. период между проникновением ядра спермия в ооцит и слиянием двух гаплоидных родительских ядер) особенно чувствительна к утрате отцовской Х-хромосомы. Этот период, как и первые стадии дробления, вероятно, весьма чувствителен и у человека, поскольку многие мозаики формируются именно на этой стадии. 3. Третьим механизмом является полиплоидизация. При этом в каждой клетке геном целиком представлен более чем дважды. У человека обнаружена только триплоидия, при которой число хромосом равно 3 n = 69.

Хромосомные заболевания человека • Аномальное число хромосом в клетке (анеуплоидия) увеличивает риск последующих нарушений, таких, как потеря хромосом вследствие анафазного отставания з последующих клеточных делениях. Для многих случаев мозаицизма с двумя клеточными популяциями, состоящими из равных пропорций трисомных и эуплоидных клеток, такое объяснение представляется наиболее удовлетворительным. Хромосома, лишенная партнера, в таких случаях, по-видимому, мешает нормальной конъюгации двух других гомологов.
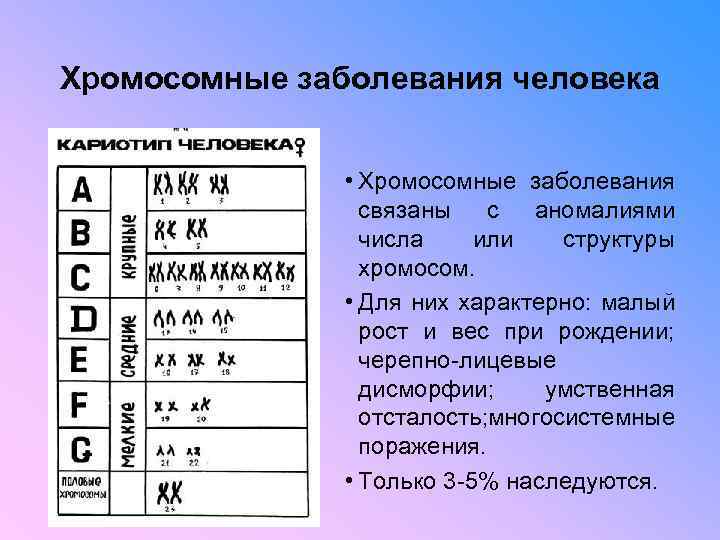
Хромосомные заболевания человека • Хромосомные заболевания связаны с аномалиями числа или структуры хромосом. • Для них характерно: малый рост и вес при рождении; черепно-лицевые дисморфии; умственная отсталость; ногосистемные м поражения. • Только 3 -5% наследуются.
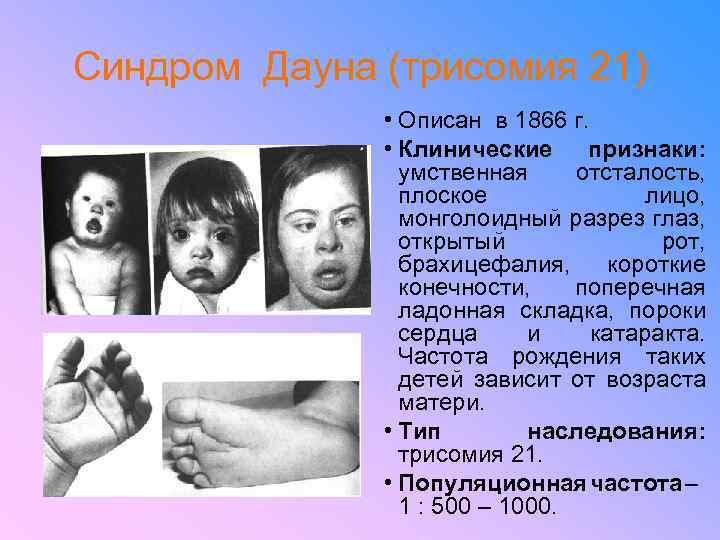
Синдром Дауна (трисомия 21) • Описан в 1866 г. • Клинические признаки: умственная отсталость, плоское лицо, монголоидный разрез глаз, открытый рот, брахицефалия, короткие конечности, поперечная ладонная складка, пороки сердца и катаракта. Частота рождения таких детей зависит от возраста матери. • Тип наследования: трисомия 21. • Популяционная частота – 1 : 500 – 1000.

Синдром Дауна (трисомия 21) • Наиболее важными характеристиками синдрома являются следующие: – это четко очерченное состояние. Несмотря на значительную изменчивость отдельных признаков, у опытного клинициста диагноз редко вызывает сомнение; – частота синдрома увеличивается с возрастом матери; – в большинстве случаев в семье регистрируется только один больной; в очень небольшом числе семей наблюдаются повторные случаи; – монозиготные (МЗ) близнецы обычно конкордантны, в то время как большинство дизиготных близнецов дискордантны. Из этого правила, однако, есть исключения - иногда встречаются дискордантные пары МЗ. Это связано, вероятно, с утерей лишней хромосомы той клеткой, из которой сформировался нормальный партнер; – мужчины с синдромом Дауна бесплодны, однако описано по крайней мере 17 женщин с этим синдромом, у которых были дети. Среди 19 таких детей (включая одну пару МЗ близнецов) у 7 имеется синдром Дауна, 9 - нормальные, 2 - умственно отсталые без синдрома Дауна и 2 мертворожденных МЗ близнеца - с нормальными кариотипами, которые учитывались как один индивид;

Синдром Дауна (трисомия 21) – продолжительность жизни больных сокращена. Согласно австралийским данным, опубликованным еще в 1963 г. , 31, 1% больных умирают в конце первого года жизни, 46% в конце третьего года. Продолжительность жизни укорочена и в поздних периодах жизни. В другой выборке 37 из 73 больных умерли от респираторных заболеваний (туберкулез не учитывался), что в 123 раза выше частоты смертельных случаев по тем же причинам в общей популяции того же возраста. 5 больных умерли от других инфекций. Эти данные дают основания предполагать наличие при болезни Дауна дефекта иммунной системы. Увеличена также частота врожденных пороков сердца; – степень выраженности отдельных фенотипических характеристик синдрома изменчивы. Например, врожденный порок сердца отмечает у некоторых, но не у всех больных, и это верно для многих других клинических признаков; – в 20 раз повышен риск смерти от острого лейкоза. Причины этого неизвестны. Существуют три гипотезы: высокий риск анеуплоидии, связанный с митотическими нарушениями в стволовых клетках крови, сниженная резистентность к инфекции лейкозогенными вирусами и, как показывают экспериментальные данные, низкая эффективность системы репарации.

Синдром Патау (трисомия 13) • Описан в 1961 г. • Клинические признаки: микроцефалия, расщепле –ние губы и неба, полидактилия, узкая глазная щель, эпикант, пороки внутренних органов, гипоплазия наружных половых органов; 95% умирают до 1 года. • Тип наследования: трисомия 13. • Популяционная частота - 1 : 7500.

Синдром Патау (трисомия 13) • Это открытие было результатом целенаправленного поиска на основе гипотезы, которая была сформулирована авторами следующим образом: – «С генетической точки зрения маловероятно, что добавление к нормальному набору какой-то аутосомы будет иметь такой же ограниченный эффект, как Хтрисомии. В настоящее время известен только один тип аутосомной трисомии, хотя лишняя хромосома является одной из двух самых маленьких аутосом, ее наличие в триплицированном состоянии приводит к монголизму. . . Следует ожидать, что другие аутосомные трисомии, если они совместимы с жизнью, должны также приводить к множественным врожденным порокам» .

Анеуплоидия по X-хромосоме у человека • Анеуплоидия по Х-хромосоме была первой из выявленных у человека хромосомных аномалий. Когда Джекобс и Стронг (1959) обследовали 42 -летнего мужчину с типичными признака синдрома Клайнфельтера (гинекомастия, маленькие тестикулы, линоз тестикулярной ткани), они обнаружили Ххроматин в клетках эпителия ротовой полости и «барабанные палочки» в нейтрофильных лейкоцитах. При исследовании хромосом в клетках костного мозга была выявлена добавочная субметацентрическая хромосома «в группе средних по размеру» . Авторы предположили, что кариотип больного - XXY.

Анеуплоидия по X-хромосоме у человека • Различие между Х-хромосомными и аутосомными анеуплоидиями: – умственное развитие в среднем хотя и ниже нормы, но аномалии развития мозга выражены не столь отчетливо, как при аномалиях аутосом. Многие пробанды имеют нормальное умственное развитие, а некоторые - даже выше среднего; – фенотипические нарушения в большей степени затрагивают развитие половых органов и гормонозависимый рост. Наблюдаются и другие пороки развития, особенно при синдроме Тернера, но встречаются они реже и по масштабам менее тяжелые.

Численные и структурные Xхромосомные анеуплоидии • В конечном счете Х-хромосомная анеуплоидия не нарушает эмбриональное развитие в такой степени, как аутосомные анеуплоидии. Объяснение, по-видимому, состоит в том, что в норме женщина имеет две, а мужчина только одну Х-хромосому, в связи с чем в эволюции сформировался специальный мощный механизм компенсации различий в дозе генов, сцепленных с Ххромосомой. Этот же механизм оказался фактором, благоприятствующим носителям Ххромосомных анеуплоидии.

Синдром Клайнфельтера (47, ХХY) • Описан в 1942 г. • Клинические признаки: высокий рост, хрупкое телосложение, гипоплазия яичек, импотенция и бесплодие, набухание молочных желез, широкий таз, поперечная ладонная складка, у взрослых наблюдается ожирение и склонность к алкоголизму, незначительное снижение умственного развития. • Тип наследования: ХХY-синдром. • Популяционная частота – 1 : 1000 мальчиков.

Синдром Клайнфельтера (47, ХХY) • Больные с классическим вариантом синдрома имеют кариотип 47, XXY. Возможны и другие кариотипы, а у 10% больных выявляется мозаицизм 46, XY/47, XXY, встречаются и более редкие кариотипы: 48, XXXY; 49, XXXXY; 48, XXYY 49, XXXYY. Синдром обычно проявляется в подростковом возрасте как задержка полового развития. • Примерно у 10% больных с синдромом Клайнфельтера наблюдается мозаицизм 46, XY/47, XXY. Поскольку в формировании фенотипа участвует клон клеток с нормальным кариотипом, больные с мозаицизмом 46, XY/47, XXY могут иметь нормально развитые половые железы и быть фертильными. Добавочная Ххромосома в 60% случаев наследуется от матери, особенно при поздней беременности. Риск наследования отцовской Х-хромосомы не зависит от возраста отца.

Синдром Шерешевского. Тернера (ХО-синдром) • Описан в 1925 г. Шерешевским и в 1938 г. Тернером. • Клинические признаки: низкий рост, первичная аменорея, бесплодие, стертые вторичные половые признаки, крыловидные кожные складки на шее, врожденные пороки сердца, гипоплазия ногтей, снижение остроты зрения и слуха, поперечная ладонная складка, незначительное снижение умственного развития. • Тип наследования: моносомия Ххромосомы. • Популяционная частота – 2 : 10000.

Синдром Шерешевского. Тернера (ХО-синдром) • Впервые эта болезнь как наследственная была описана в 1925 г. Шерешевским, который считал, что она обусловлена недоразвитием половых желез и передней доли гипофиза и сочетается с врожденными пороками внутреннего развития. В 1938 г. Тернер выделил характерную для этого симптомокомплекса триаду симптомов: половой инфантилизм, кожные крыловидные складки на боковых поверхностях шеи и деформацию локтевых суставов. В России этот синдром принято называть синдромом Шерешевского. Тернера. Этиология заболевания (моносомия по Ххромосоме) была раскрыта Фордом в 1959 г.
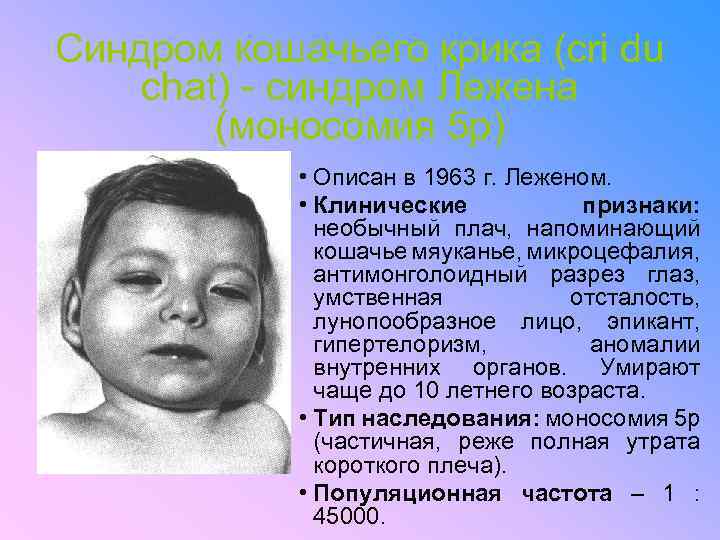
Синдром кошачьего крика (cri du chat) - синдром Лежена (моносомия 5 р) • Описан в 1963 г. Леженом. • Клинические признаки: необычный плач, напоминающий кошачье мяуканье, микроцефалия, антимонголоидный разрез глаз, умственная отсталость, лунопообразное лицо, эпикант, гипертелоризм, аномалии внутренних органов. Умирают чаще до 10 летнего возраста. • Тип наследования: моносомия 5 р (частичная, реже полная утрата короткого плеча). • Популяционная частота – 1 : 45000.

Синдром Свайера (дисгенезия гонад, ХY-тип) • Описан в 1955 г. • Клинические признаки: наружные половые органы сформированы по женскому типу, матка и маточные трубы недоразвиты, аменорея, бесплодие. Уровень эстрогенов и тестостерона снижен, а гонадотропинов повышен. • Тип наследования: Хрецессивный. • Популяционная частота – неизвестна.

Хромосомные болезни: триплоидия • К 1974 г. на основании изучения 275 триплоидных абортусов, полученных при сроках беременности менее чем 20 недель, была накоплена более или менее детальная информация. Двадцать два из исследованных плодов достигли возраста 28 недель; пять других погибли in utero; остальные прожили несколько часов или дней после рождения. Все живорожденные дети, прожившие дольше нескольких дней (к 1974 г. их было 8), оказались триплоиддиплоидными мозаиками. • Наиболее характерным. признаком триплоидии является пузырное перерождение плаценты (mole hydatidiforme). У некоторых эмбрионов обнаруживаются локальные пороки развития, но часть плодов имеет как будто бы нормальный фенотип.

Хромосомные болезни: триплоидия • Триплоиды, родившиеся живыми, имеют небольшой вес, широкий задний родничок с недоразвитыми затылочными и теменными костями черепа и другие неспецифические аномалии, которые характерны для многих аутосомных аберраций. • Триплоиды мужского пола с кариотипом 69, XXY характеризуются нарушением гениталий: у них маленький половой член в сочетании с гипоспадией, расщепленной мошонкой и неопустившимися яичками. Некоторые из мозаиков выживают. Клинические признаки не очень четкие, предварительный диагноз можно поставить на основании умственной отсталости в сочетании с аномалиями плаценты, синдактилией, аномалиями гениталий и асимметрией.

Хромосомные болезни: триплоидия • Триплоидия возникает вследствие ошибок при образовании половых клеток. Различия в причинах появления триплоидов определяют среди них соотношения индивидов с генотипами XXX, XXY и XYY. Существуют факты, свидетельствующие о том, что причиной триплоидии может быть двойное оплодотворение или отсутствие первого мейотического деления ооцита.
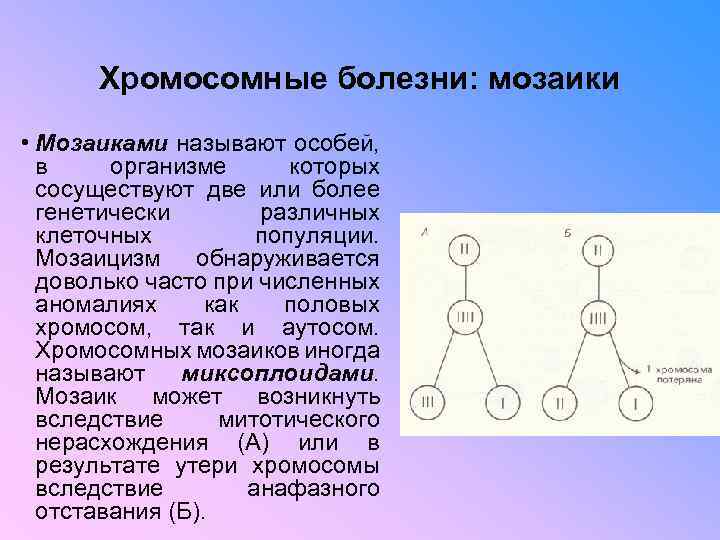
Хромосомные болезни: мозаики • Мозаиками называют особей, в организме которых сосуществуют две или более генетически различных клеточных популяции. Мозаицизм обнаруживается доволько часто при численных аномалиях как половых хромосом, так и аутосом. Хромосомных мозаиков иногда называют миксоплоидами. Мозаик может возникнуть вследствие митотического нерасхождения (А) или в результате утери хромосомы вследствие анафазного отставания (Б).

Хромосомные болезни: мозаики • Оценки частоты таких нарушений митоза получены в случае синдрома Дауна. Риск анафазного отставания в 400 раз выше в трисомной зиготе, чем в эуплоидной, а митотического нерасхождения - в 70 раз. Эти оценки основаны на сопоставле относительных частот различных типов мозаицизма и на анализе эффекта возраста матери. Частота мозаик возникающих вследствие мейотического нерасхождения с последующей утратой дополнительной хромосомы в анафазе теоретически должна увеличиваться с возрастом матери, так же, как и при обычных гаметических трисомиях.

Хромосомные аберрации и спонтанные аборты • Около 15% всех беременностей у человека прерываются диагностируемыми спонтанными абортами, если аборт определять как прекращение беременности до 22 -й недели (вес эмбриона 500 г и меньше). Однако доказано, что у человека, так же как и у других млекопитающих, теряется много больше зигот на самых ранних стадиях развития, и часто они имеют тяжелые пороки развития. Согласно некоторым оценкам, почти 50% всех зачатий не реализуется в пределах первых двух недель развития, до того, как беременность диагностируется. У человека эта ранняя утрата зигот обычно не распознается. Принимая 15% как частоту диагностируемых спонтанных абортов среди всех распознаваемых беременностей, антенатальная утрата зигот из-за хромосомных аберраций может быть оценена в 5 -6%. Это почти в 10 раз больше, чем частота хромосомных аберраций среди живорожденных (около 0, 5 -0, 6%).
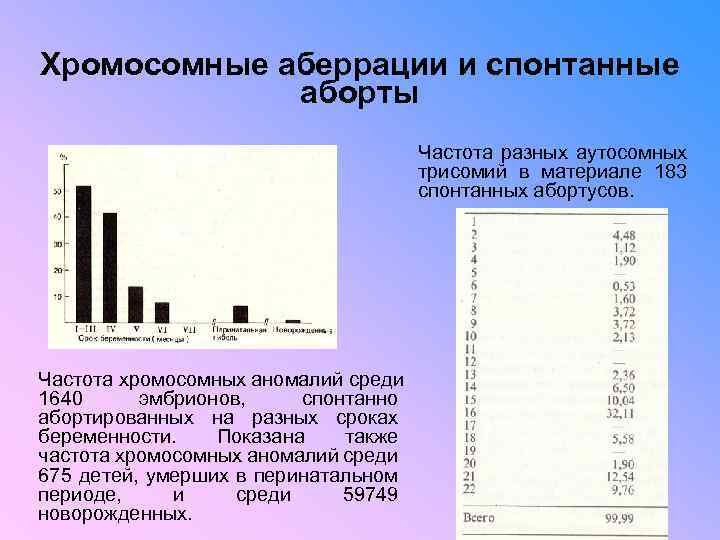
Хромосомные аберрации и спонтанные аборты Частота разных аутосомных трисомий в материале 183 спонтанных абортусов. Частота хромосомных аномалий среди 1640 эмбрионов, спонтанно абортированных нa разных сроках беременности. Показана также частота хромосомных аномалий среди 675 детей, умерших в перинатальном периоде, и среди 59749 новорожденных.

Предимплантационная генетическая диагностика • Предимплантационная генетическая диагностика (ПГД) представляет собой диагностику хромосомных и генетических нарушений эмбриона до его пересадки матери. • ПГД позволяет выявить эмбрионы, у которых отсутствуют хромосомные и генетические мутации. Ее целью является обеспечение здорового потомства и предупреждение передачи определенных патологий.
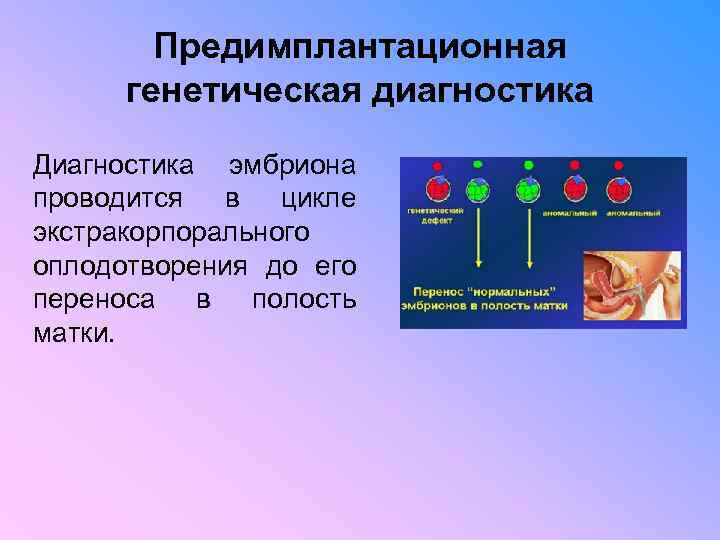
Предимплантационная генетическая диагностика Диагностика эмбриона проводится в цикле экстракорпорального оплодотворения до его переноса в полость матки.

Предимплантационная генетическая диагностика Метод экстракорпорального оплодотворения (ЭКО) был впервые применен в медицинской практике в 1978 году. • Суть процедуры сводится к получению из яичников женщины созревших яйцеклеток, оплодотворению их сперматозоидами мужа (донора), выращиванию получившихся эмбрионов в специальной среде вне организма женщины (инкубаторе) и переносу эмбрионов в матку. •
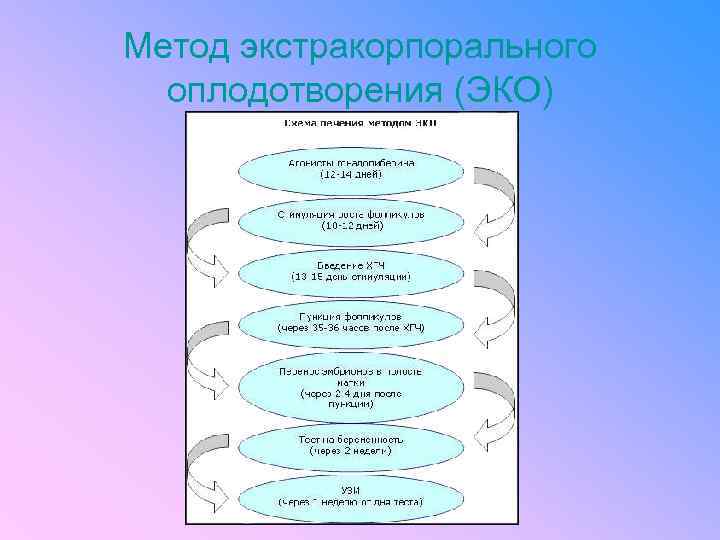
Метод экстракорпорального оплодотворения (ЭКО)

Показания для проведения предимплантационной диагностики • Возраст женщины старше 34 лет • Возраст мужчины старше 39 лет • Носительство хромосомных перестроек, транслокаций, инверсий и других хромосомных и генетических патологий • Привычное невынашивание беременности (более 2 выкидышей) • Неудачные попытки ЭКО в анамнезе (более двух) Биопсия бластомера эмбриона

Описание процедуры ПГД • Стандартная процедура ЭКО до этапа пункции яйцеклеток; • Стандартные эмбриологические процедуры по обработке яйцеклеток, спермы, проведению микроманипуляций; • Лабораторная процедура биопсии эмбриона на 3 день культивирования (с помощью механического, химического или лазерного метода), а затем фиксация бластомера; • Генетическая диагностика зафиксированных бластомеров и получение результатов диагностики к 5 дню культивирования эмбрионов; • Перенос в полость матки эмбрионов без генетических дефектов на 5 день культивирования на стадии бластоцисты; • Стандартные процедуры криоконсервации после переноса эмбрионов; • Стандартная процедура диагностики беременности примерно через две недели после переноса эмбрионов.

• ПГД проводится в ходе стандартного цикла экстракорпорального оплодотворения. • При ПГД из эмбриона извлекают одну или две клетки, а затем проводят их генетический анализ методом FISH (fluorescent in situ hybridization) на анеуплоидии, транслокации и другие структурные патологии. • Другой тип диагностики - полимеразная цепная реакция (ПЦР), которая применяется для диагностики моногенных заболеваний. ПЦР проходит в два этапа: 1) биопсия эмбриона и фиксация бластомера; 2) генетическая диагностика.

Преимущества предимплантационной диагностики • Выбор и перенос в матку только тех эмбрионов, которые не имеют хромосомных патологий • Снижение риска рождения ребенка с определенными генетическими дефектами • Снижение риска невынашивания (примерно в 2 раза) • Снижение риска многоплодия (примерно в 2 раза) • Увеличение шанса на успешную имплантацию (примерно на 10%) • Увеличение шансов на благополучное рождение ребенка (примерно на 15 -20%)

Основные генетические заболевания, диагностируемые методом ПГД • • • • • Хорея Гентингтона Синдром ломкой Х-хромосомы Миотоническая дистрофия Синдром Марфана Ретиношизис Гемофилия-А Фиброзно-кистозная дегенерация Бета-таласемия Гидроцефалия Мышечная дистрофия Эмери–Дрейфуса Недержание пигмента Острая интермиттирующая порфирия Адренолейкодистрофия Спинально-церебеллярная атаксия 3 Мышечная дистрофия Дюшенна Гипокальциемический паралич Ангионевротический отек Синдром Карнея Nistagmus

Риск при проведении предимплантационной диагностики • Риск случайного повреждения эмбриона (<1%) • Ошибочная диагностика (до 10%) • 3, 5% вероятности того, что эмбрион с патологией будет диагностирован как нормальный • 10% вероятности того, что здоровый эмбрион будет диагностирован как эмбрион с патологией • Отмена переноса эмбрионов из-за того, что по результатам ПГД во всех эмбрионах будет обнаружена патология (до 20%)
Митохондриальные заболевания человека http: //www. eyenews. ru/stati_terap_9. htm

Митохондриальные заболевания человека На сегодня известны более 100 точковых мутаций и несколько сот структурных перестроек митохондриальной ДНК (мт. ДНК), связанных с характерными нейромышечными и другими митохондриальными синдромами - от летальных в неонатальном периоде жизни до заболеваний с поздним началом. Непосредственная причина возникновения и развития митохондриальных расстройств кроется в дефектах системы окислительного фосфорилирования. Фенотипическая многоликость и феномен гетероплазмии, приравниваемый некоторыми авторами к мутационному грузу, - отличительная особенность митохондриальных болезней человека. Благодаря выявлению все большего количества пациентов и описанию сотен родословных, сведения о взаимоотношении между генотипом и фенотипом, структуре и частоте встречаемости патогенных и условнойпатогенных мутаций мт. ДНК в популяциях накапливаются ускоренными темпами.

Митохондриальные заболевания человека Патогенные мутации мт. ДНК, имеющие ключевое значение в патогенезе митохондриальных заболеваний, встречаются повсеместно. Так, в Англии они найдены с примерной частотой 1 на 8000 человек. Пенетрантность и экспрессивность таких мутаций варьируют в широких пределах от семьи к семье и между родственниками (по материнской линии) одной семьи и зависят от многих факторов, но главным образом от генотипа и уровня гетероплазмии (смесь мутантных и дикого типа молекул мт. ДНК). Уровень гетероплазмии колеблется в процессе клеточного деления, подчиняясь главным образом вероятностным механизмам, с наибольшей амплитудой действующим на ранних стадиях оогенеза и эмбриогенеза. Поэтому фиксация мутантной мт. ДНК на уровне 100% (гомоплазмия) иногда наступает уже в следующем поколении.

Митохондриальные заболевания человека Карта мт. ДНК с указанием положения генов и относительно часто встречающихся патогенных мутаций

Митохондриальные заболевания человека КЛАССИФИКАЦИЯ ПАТОГЕННЫХ МУТАЦИЙ МТДНК • Смысловые мутации в структурных генах • Мутации мт. ДНК, приводящие к нарушениям синтеза белка • Структурные перестройки мт. ДНК • Взаимодействие двух геномов

Митохондриальные заболевания человека КЛАССИФИКАЦИЯ ПАТОГЕННЫХ МУТАЦИЙ МТДНК • Взаимодействие двух геномов Хотя большинство генов, продукты которых ответственны за нормальное функционирование системы окислительного фосфорилирования, располагаются в хромосомах, на сегодня известно всего несколько локусов, мутации в которых могут рассматриваться в качестве этиологической причины митохондриальной болезни. В качестве примера можно сослаться на синдром нейрогастроинтестинальной энцефалопатии (MNGIE), обусловленной мутацией гена тимодинфосфорилазы. Гораздо чаще мутации в ядерных генах модифицируют экспрессию мутаций в митохондриальном геноме. Без вероятного влияния ядерного генома трудно объяснить, почему одна и та же точковая мутация (МТТЫ *MELAS 3243 G) ассоциируется с такими разными клиническими фенотипами, как сахарный диабет и энцефалопатия. Кроме того, в основе возникновения некоторых митохондриальных миопатий, таких как офтальмоплегия и птоз, может лежать дестабилизация молекулы мт. ДНК, инициируемая мутациями в ядерных генах.
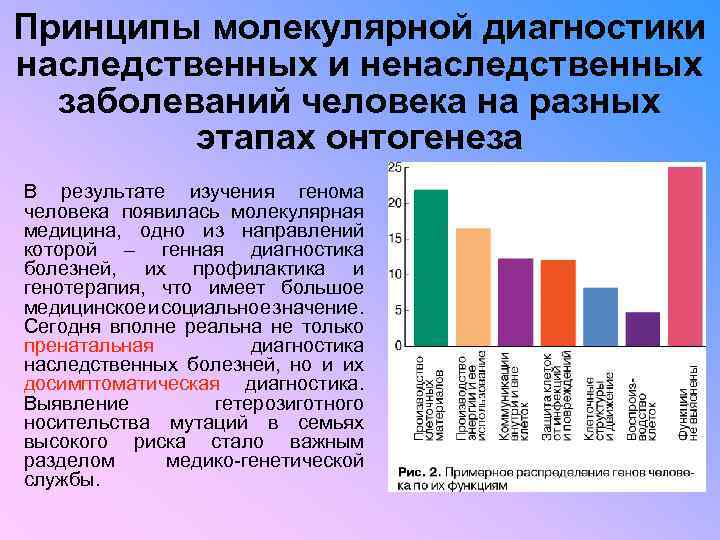
Принципы молекулярной диагностики наследственных и ненаследственных заболеваний человека на разных этапах онтогенеза В результате изучения генома человека появилась молекулярная медицина, одно из направлений которой – генная диагностика болезней, их профилактика и генотерапия, что имеет большое медицинское и социальное значение. Сегодня вполне реальна не только пренатальная диагностика наследственных болезней, но и их досимптоматическая диагностика. Выявление гетерозиготного носительства мутаций в семьях высокого риска стало важным разделом медико-генетической службы.

Принципы молекулярной диагностики наследственных и ненаследственных заболеваний человека на разных этапах онтогенеза Принципиально различают прямую и непрямую ДНКдиагностику моногенных наследственных болезней. В общем случае использование прямых методов диагностики возможно лишь для клонированных генов с известной нуклеотидной последовательностью полноразмерной к. ДНК, при этом необходимо предварительное генотипирование мутантных аллелей у родителей. В случае прямой диагностики объектом молекулярного анализа является сам ген, точнее, мутации этого гена. Такой подход особенно эффективен при наличии точной информации о природе, частоте и локализации наиболее распространенных (доминирующих по частоте) мутаций соответствующих генов, а также о наличии в них особенно легко мутирующих «горячих» точек.

Принципы молекулярной диагностики наследственных и ненаследственных заболеваний человека на разных этапах онтогенеза Главное преимущество прямого метода – это высокая, доходящая до 100%, точность диагностики и отсутствие необходимости анализа всей семьи на предмет ее информативности. Последнее обстоятельство особенно важно для проведения пренатальной диагностики тяжелых, зачастую летальных наследственных болезней (муковисцидоза, миодистрофии Дюшена, гемофилии А и др. ).

Принципы молекулярной диагностики наследственных и ненаследственных заболеваний человека на разных этапах онтогенеза Однако существует огромное количество наследственных болезней, для которых мутации не описаны либо не найдено мажорных ситуаций в исследуемых популяциях. Кроме того, всегда сохраняется возможность присутствия у пробанда неизвестных мутаций. Далеко не всегда возможно применение такого подхода и в силу очевидных финансовых и временных ограничений. Эти трудности успешно преодолеваются благодаря наличию непрямых (косвенных) методов молекулярной диагностики. Этот исторически более ранний подход основан на использовании сцепленных с геном полиморфных маркеров, с помощью которых проводится идентификация мутантных хромосом (точнее хромосом, несущих мутантный ген) в семьях высокого риска, т. е. у родителей больного и его ближайших родственников.

Принципы молекулярной диагностики наследственных и ненаследственных заболеваний человека на разных этапах онтогенеза В настоящее время косвенные методы молекулярной диагностики принципиально возможны практически для всех моногенных заболеваний с известной локализацией контролирующего гена, для каждого из которых уже разработана удобная система вне- и внутригенных полиморфных индексных маркеров. Косвенные методы молекулярной диагностики пригодны даже для тех болезней, гены которых еще не идентифицированы и мутации не известны. Единственным и непременным условием этого является наличие полиморфных сайтов рестрикции либо коротких тандемных повторов типа STR, находящихся в непосредственной близости от мутантного гена или, что еще лучше, внутри него (чаще всего в интронах). При помощи этих полиморфных сайтов удается маркировать мутантные аллели гена и проследить их передачу потомству.

Генная и клеточная терапия моногенных и мультифакторных заболеваний В мире каждый сотый ребенок рождается с серьезным наследственным дефектом, и количество таких дефектов неумолимо растет. Наследственные отклонения, как правило, приводят к физическим или умственным нарушениям и преждевременной смерти. Для большинства из известных в настоящее время наследственных заболеваний не найдено достаточно эффективных способов лечения. Спасением от таких заболеваний могло бы стать введение в организм больного неповрежденной копии мутантного участка ДНК. Первая успешная попытка применить генотерапию в клинической практике была предпринята в 1990 году в США. Ребенку, страдающему редким заболеванием – тяжелым комбинированным иммунодефицитом, – которое связано с дефектом гена, кодирующего фермент аденозиндезаминазу, была введена неповрежденная копия гена. И хотя использованный метод предполагал многократное введение гена на протяжении всей жизни пациента, то есть, строго говоря, не обеспечивал полного излечения, была открыта новая эра в медицине.

Генная и клеточная терапия моногенных и мультифакторных заболеваний Существуют несколько подходов к лечению генами. Гены можно вводить в половые клетки (сперматозоиды или яйцеклетки), в клетки эмбриона на ранних стадиях развития либо в соматические клетки (клетки тела, кроме половых или их предшественников). Введение генов в половые клетки означает, что приобретенное свойство будет передаваться из поколения в поколение. Именно этот метод широко используется при получении трансгенных животных, но он вряд ли применим к людям из этических соображений. Генотерапия соматических клеток в отличие от половых затрагивает организм только самого пациента и поэтому разрабатывается в качестве основного подхода. При этом большое значение имеет правильный выбор типа соматических клеток, которые должны обеспечить длительное сохранение и функционирование внесенного "лечебного" гена. Наследственные заболевания могут быть обусловлены дефектом одного или нескольких генов, а также крупными генетическими изменениями, например потерей целой хромосомы. Безусловно, на современном этапе можно пытаться лечить генами только заболевания первого типа, так называемые моногенные, при условии, если ответственный за дефект ген уже обнаружен и клонирован, то есть получен материал для введения больному.

Генная и клеточная терапия моногенных и мультифакторных заболеваний Существуют два пути передачи больному "лечебного" гена. Если болезнь связана с отсутствием или малыми количествами белкового продукта дефектного гена, то достаточно ввести в клетку неповрежденный ген и дать ему возможность работать; в результате появятся достаточные количества белка-продукта. Таким образом, внесенная копия гена заместит по функциям сохраняющийся в геноме больного дефектный ген, поэтому этот подход получил название заместительной терапии. Все используемые в настоящее время клинические методы переноса генов основаны на внесении в клетку дополнительных количеств ДНК, то есть на заместительной терапии. Другим, идеальным способом излечивать генетические заболевания могла бы быть корректирующая (или исправляющая) терапия, при помощи которой дефектный ген реально заменялся бы в геноме нормальной копией. Этого можно достичь основываясь на способности двух молекул ДНК к рекомбинации – обмену при помощи специальных ферментов фрагментами полинуклеотидных цепей. Однако из-за крайне низкой эффективности этого метода в условиях лаборатории до практического использования корректирующей терапии пока очень далеко.
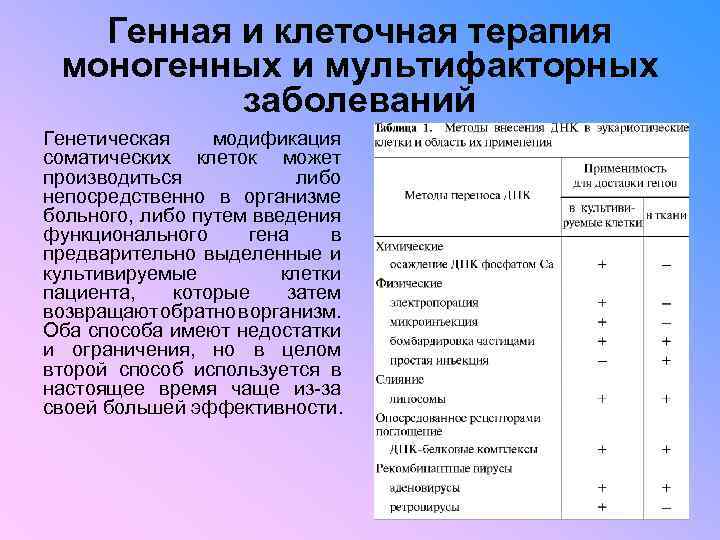
Генная и клеточная терапия моногенных и мультифакторных заболеваний Генетическая модификация соматических клеток может производиться либо непосредственно в организме больного, либо путем введения функционального гена в предварительно выделенные и культивируемые клетки пациента, которые затем возвращают братно рганизм. о во Оба способа имеют недостатки и ограничения, но в целом второй способ используется в настоящее время чаще из-за своей большей эффективности.

Генная и клеточная терапия моногенных и мультифакторных заболеваний Главное в методе переноса генов – включается (интегрирует) ли новый ген в хромосому клетки-мишени. Для активно делящихся клеток отсутствие интеграции внесенного гена в клеточную ДНК означает его неминуемую утрату в клетках-потомках. Одной из основных причин того, что в 80% случаев для внесения чужеродной ДНК при клинических испытаниях на людях использовали ретровирусные векторы, является его стабильная интеграция в клеточный геном. Кроме того, эти векторы обеспечивают высокую эффективность доставки генов и не приводят к ощутимым повреждениям в клеткемишени. В отличие от ретровирусных аденовирусные векторы в геном не интегрируются.
Генная и клеточная терапия моногенных и мультифакторных заболеваний
Молекулярная геномика Благодаря молекулярной медицине в будущем, вероятно, будут созданы новые лекарства, гораздо более избирательные и эффективные, чем ныне существующие. Поскольку они будут целенаправленно действовать на генные и белковые мишени, скоро можно будет прочитать и геном любого отдельно взятого человека. Это позволит установить, какие гены дефектны, какими заболеваниями это грозит. Уже сегодня в силах науки провести такой анализ и составить генетический паспорт человека.

Молекулярная геномика Исследования в этом направлении ведутся и в России: в Москве - в Научном центре медицинской генетики и Институте неврологии РАМН, в Санкт-Петербурге - в Институте биорегуляции и геронтологии РАМН и в лаборатории пренатальной диагностики НИИ акушерства и гинекологии РАМН, в Томске - в Институте медицинской генетики, в Медико-генетическом центре Новосибирска и в Институте биохимии и генетики Уфимского научного центра РАН Генетический анализ может выявить предрасположенность к гипертонии, диабету, некоторым формам рака, болезни Дауна, фенилкетонурии, к алкоголизму и наркомании, даже к гомосексуализму.

Молекулярная геномика Группа компаний с участием «Motorola Life Sciences» уже разрабатывает портативное устройство генной диагностики заболеваний на базе карманного компьютера. Оно будет определять болезнь, исследуя образец слюны пациента. Новая технология появится в лечебных учреждениях в течение ближайших пяти лет, а в быту – десяти лет. Генная диагностика позволит определить наиболее слабые участки человеческого организма, предрасположенность к тем или иным болезням. Соответственно человек сможет построить свою жизнь так, чтобы в дальнейшем избежать проблем со здоровьем. В случае, если генная диагностика выявит какое-то заболевание, лечить его будут с учетом индивидуальных особенностей организма конкретного человека. Сегодня для лечения используются массовые медицинские препараты, и на разных людей они действуют по-разному: из 100 человек у 60 могут произойти заметные улучшения в самочувствии, у 20 они будут незначительными, а еще 20 никак не почувствуют воздействие препарата.

Молекулярная геномика Геномный полиморфизм выражается в изменчивости отдельных участков (полиморфных) ДНК у разных индивидов. Функции многих полиморфных участков уже установлены, но у большинства они в настоящее время неизвестны. Экспериментально выявляются несколько основных вариантов геномного полиморфизма: количественные изменения в областях локализации повторяющихся последовательностей ДНК (мини- и микросателлитные повторы), качественные замены отдельных нуклеотидов (однонуклеотидный полиморфизм) или целых групп нуклеотидов и др. Однонуклеотидные полиморфизмы (single nucleotide polymorphisms, SNP’s) – это полиморфизмы, возникшие в результате замены или потери отдельных нуклеотидов в ДНК-последовательностях. В геноме человека выявлены также гипервариабельные участки ДНК (специфичные для индивидуума) представляющие собой короткие повторы нуклеотидов, функция которых не известна.

Понятие о генетическом паспорте человека Хотя определить все гены предрасположенности для каждого человека пока невозможно, сейчас уже технически доступен индивидуальный анализ по нескольким десяткам генов. Иными словами, желающие знать свои генетические характеристики могут получить генетический паспорт. В нем должна быть информация о наличии мутаций в генах наследственных болезней и в генах предрасположенности к мультифакторным заболеваниям. В некоторых западных странах генетическое тестирование проводят по медицинским показаниям или просто в качестве платной услуги. Сведения, записанные в генетическом паспорте, - такая же врачебная тайна, как и результаты любых других медицинских обследований.

Понятие о генетическом паспорте человека Зачем нужен такой паспорт и какие гены необходимо тестировать? Генетический паспорт обычно делается либо с целью ДНК -идентификации, либо для того, чтобы определить, какие опасные заболевания подстерегают вас в жизни. Это как бы штрих-код, описывающий человека, а точнее наличие тех или иных черт в его ДНК. В США, например, введено генетическое тестирование военнослужащих не для медицинских целей. Его результаты, хранящиеся в специальной базе данных, позволяют идентифицировать человека гораздо точнее, чем надетый на руку жетон. Очень важен генетический паспорт для криминалистики. В той же самой Америке решили пересмотреть дела, связанные с изнасилованием. Сравнили генетические паспорта осужденных и детей, которые родились у потерпевшей. И оказалось, что 30% сидящих по этой статье не являются отцами данных детей.

Понятие о генетическом паспорте человека Если генетический паспорт необходим для здорового молодого человека, желающего знать, какие болезни могут ожидать его в будущем и как предотвратить их развитие, прежде всего нужно составить его родословную и посмотреть, чем болели его родственники. Носительство мутаций, связанных с моногенными болезнями (фенилкетонурией, муковисцидозом), можно определять, если в семье имеются подобные больные или же заболевание встречается с высокой частотой в той этногеографической группе или того географического региона, где живет обследуемый. Если среди родственников обследуемого есть больше одного человека с одинаковой мультифакторной патологией, необходимо анализировать гены предрасположенности к ее развитию. При наличии факторов риска, связанных с профессией или с особыми условиями среды, нужно тестировать гены, имеющие отношение к болезням, провоцируемым именно этими факторами.

Понятие о генетическом паспорте человека Работы по генетической паспортизации уже начались. Они получили финансовую поддержку в Ирландии, Финляндии, в некоторых штатах США. Большие средства на генетическое тестирование детей с семилетнего возраста выделены правительством Эстонии. Такие работы сопровождаются публикациями в средствах массовой информации, обсуждениями этических и социальных проблем и правовых аспектов. Не случайно в материалах Всемирной организации здравоохранения за 1998 г. , посвященных этическим аспектам медицинской генетики, подчеркивается, что пресимптоматическое тестирование можно проводить только по желанию, только в случае возможной реальной пользы для пациента или его родственников, при условии максимально объективного информирования пациента о результатах тестирования.

Понятие о генетическом паспорте человека Большинство людей (около 70%) уже сейчас хотели бы получить генетический паспорт, 20% не хотят этого, 14% затруднились ответить. Большинство хотели бы получить медико-генетическую информацию о себе (60%) и своем супруге (50%). 92% респондентов считают, что такую информацию должны иметь родители о несовершеннолетних детях; 87% — взрослые дети о родителях. 50% считают, что о генетических рисках здоровья должен знать супруг. 73% доверились бы врачам медицинских учреждений с соблюдением врачебной тайны. Более 80% опрошенных против предоставления этой информации руководству предприятий.

Понятие о генетическом паспорте человека

Развитие молекулярной диагностики заболеваний человека в Беларуси
Развитие молекулярной диагностики заболеваний человека в Беларуси
Развитие молекулярной диагностики заболеваний человека в Беларуси

Развитие молекулярной диагностики заболеваний человека в Беларуси Рэспубліка. – 2009. – № 57. 28 сакавіка. – С. 8.
Развитие молекулярной диагностики заболеваний человека в Беларуси
Развитие молекулярной диагностики заболеваний человека в Беларуси

Развитие молекулярной диагностики заболеваний человека в Беларуси Институт генетики и цитологии НАН Беларуси • Лаборатория молекулярной генетики (акад. Н. А. Картель, к. б. н. Д. Г. Ярмолинский) • Лаборатория нехромосомной наследственности (чл. кор. О. Г. Давыденко, к. б. н. Н. Г. Даниленко) • Лаборатория генетической безопасности (д. б. н. Р. И. Гончарова, д. б. н. Т. Д. Кужир) • Лаборатория генетики человека (д. б. н. И. Б. Моссэ) • Лаборатория моделирования генетических процессов (д. б. н. С. Е. Дромашко, к. б. н. Н. Н. Чакова, к. б. н. Э. В. Крупнова)
Наследственные заболевания 4-5л.ppt