Лекция 4 мол организация ФСА.ppt
- Количество слайдов: 29

МОЛЕКУЛЯРНАЯ ОРГАНИЗАЦИЯ ФСА ФУНКЦИОНАЛЬНАЯ ОРГАНИЗАЦИЯ ТИЛАКОИДНЫХ МЕМБРАН ХЛОРОПЛАСТОВ 1. 2. 3. 4. ВОПРОСЫ: Липидный состав мембран тилакоидов. Белковые компоненты тилакоидных мембран Вода и неорганические ионы Физико-химические свойства тилакоидных мембра
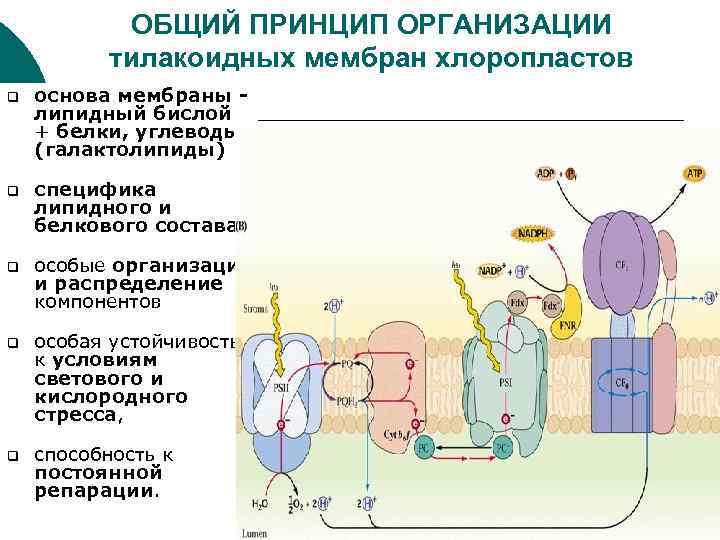
ОБЩИЙ ПРИНЦИП ОРГАНИЗАЦИИ тилакоидных мембран хлоропластов q основа мембраны липидный бислой + белки, углеводы (галактолипиды) q специфика липидного и белкового состава q особые организация и распределение компонентов q особая устойчивость к условиям светового и кислородного стресса, q способность к постоянной репарации.

1. ЛИПИДНЫЙ СОСТАВ МЕМБРАН ТИЛАКОИДОВ Липиды составляют около 50 % сухой массы мембран. ¡ Соотношение липидов и белков по весу = 1: 1. ¡ на 1 молекулу белка - 500 молекул липидов. ¡ В мембранах хлоропластов две группы липидов циклические нециклические (ацилсодержащие). ¡ ¡

ЦИКЛИЧЕСКИЕ ЛИПИДЫ 1. фотосинтетические пигменты (хлорофиллы и каротиноиды), 2. хиноны — Ø бензохиноны (пластохиноны) Ø нафтохиноны (филлохиноны). ¡ непосредственное участие в фотосинтезе. 3. α-токоферол, α-токоферилхинон ¡ ¡ структурированность мембран устойчивость к свободнорадикальным процессам

НЕЦИКЛИЧЕСКИЕ ЛИПИДЫ Галактолипиды 2. Фосфолипиды 3. Сульфолипиды. 1. ¡ Они формируют липидный матрикс мембран и участвуют в структурной организации мембран. ¡ Особенностью мембран хлоропластов является высокое содержание галактолипидов. (многие другие мембраны - преобладают фосфолипиды), в мембранах тилакоидов - до 75 % липидов - галактолипиды ¡
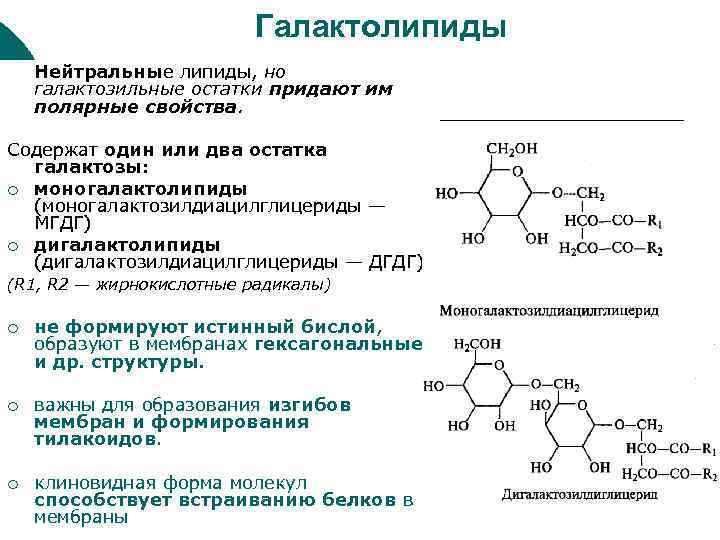
Галактолипиды Нейтральные липиды, но галактозильные остатки придают им полярные свойства. Содержат один или два остатка галактозы: ¡ моногалактолипиды (моногалактозилдиацилглицериды — МГДГ) ¡ дигалактолипиды (дигалактозилдиацилглицериды — ДГДГ). (R 1, R 2 — жирнокислотные радикалы) ¡ не формируют истинный бислой, образуют в мембранах гексагональные и др. структуры. ¡ важны для образования изгибов мембран и формирования тилакоидов. ¡ клиновидная форма молекул способствует встраиванию белков в мембраны
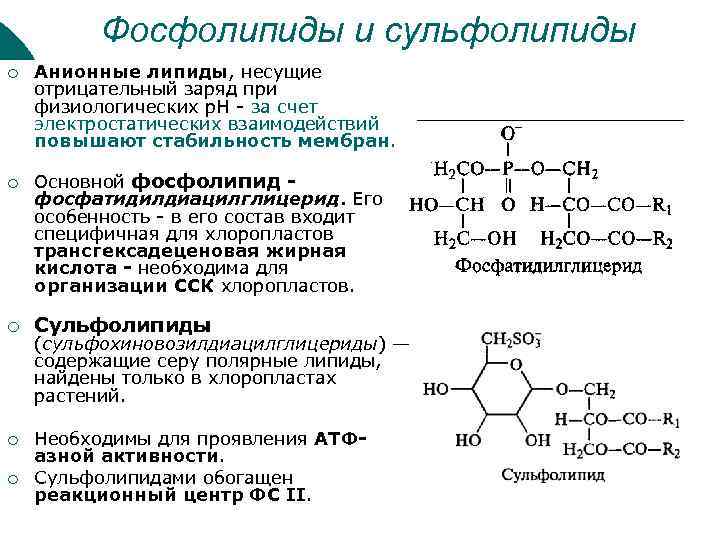
Фосфолипиды и сульфолипиды ¡ ¡ ¡ Анионные липиды, несущие отрицательный заряд при физиологических р. Н - за счет электростатических взаимодействий повышают стабильность мембран. Основной фосфолипид фосфатидилдиацилглицерид. Его особенность - в его состав входит специфичная для хлоропластов трансгексадеценовая жирная кислота - необходима для организации ССК хлоропластов. Сульфолипиды (сульфохиновозилдиацилглицериды) — содержащие серу полярные липиды, найдены только в хлоропластах растений. Необходимы для проявления АТФазной активности. Сульфолипидами обогащен реакционный центр ФС II.

ЖИРНОКИСЛОТНЫЙ СОСТАВ ЛИПИДОВ ВНУТРЕННИХ МЕМБРАН ¡ 1. 2. ¡ Высокое относительное содержание ненасыщенных жирных кислот: линолевой (С 18: 2) линоленовой (С 18: 3). Насыщенные жирные кислоты - главным образом пальмитиновая кислота (С 16: 0). Обогащенность НЕНАСЫЩЕННЫМИ ЖК → 1. Cдвиг температуры фазового перехода мембран тилакоидов в области более низких температур q определяет высокую текучесть внутренних мембран тилакоидов q способствует латеральной, ротационной и трансмембранной диффузии компонентов мембран, наблюдаемой в ходе световых реакций фотосинтеза → возможность молекулярного взаимодействия отдельных функциональных комплексов. 2. Ненасыщенные жирные кислоты подвержены перекисному окислению, что в условиях образования АФК в хлоропластах фактор риска повреждения мембран.

3. Организация ССК и контакт ССК с РЦ. . (А. Хорватч и др. (1987) : насыщение двойных связей жирных кислот мембранных липидов → нарушения ассоциации ССК II с РЦ II → отдаление ССК II → снижение активности транспорта е- от ФС II к пулу пластохинонов). ВЗАИМОДЕЙСТВИЕ ЛИПИДОВ С БЕЛКАМИ МЕМБРАН: 1. Стабилизация белковых комплексов 2. Взаимодействие липидов с каталитическими белками - определяют конформационную структуру белков, необходимую для их высокой активности (например, активация галактолипидами сопрягающего фактора СF 1 АТФ-синтазного комплекса). 3. Определенное функциональное значение для активности интегральных белков имеют обратимые фазовые переходы липидов, индуцируемые температурой.
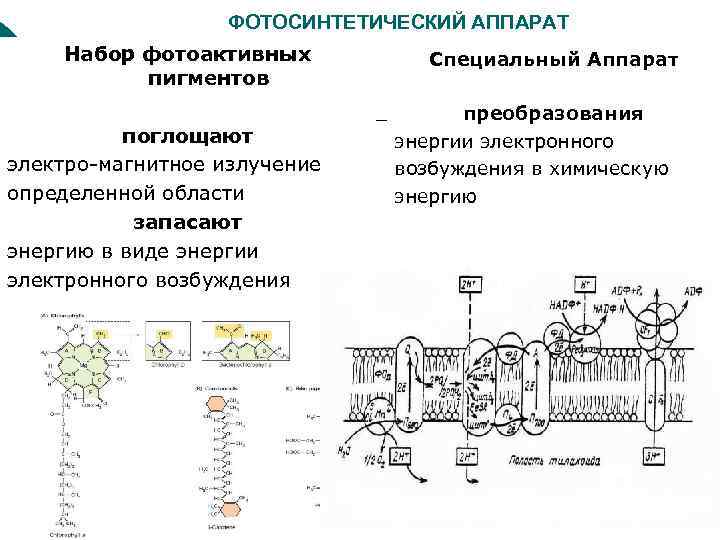
ФОТОСИНТЕТИЧЕСКИЙ АППАРАТ Набор фотоактивных пигментов поглощают электро-магнитное излучение определенной области запасают энергию в виде энергии электронного возбуждения Специальный Аппарат преобразования энергии электронного возбуждения в химическую энергию

2. БЕЛКОВЫЕ КОМПОНЕНТЫ ТИЛАКОИДНЫХ МЕМБРАН. ПБК В. Н. Любименко в 1921 г. - большая часть хлорофилла в листе связана с белком 1970 г. - систематическое изучение ПБК ¡ в лаборатории Дж. Торнбера выделено из живых листьев три окрашенных комплекса, различающихся по составу пигментов, белков и спектрам поглощения 1980 г. - Дж. Андерсон (Anderson, 1980) выделил 6 комплексов: l РЦ ФС I и ФС I I l ССК I и ССК II, l общий ССК l небольшую полосу свободного хлорофилла. ПИГМЕНТЫ образуют с белками стабильные комплексы связаны нековалентно ¡ ¡ ¡ МЕХАНИЗМ ОБРАЗОВАНИЯ ПБК электростатические взаимодействия АК белка с группой С=О хлорофилла, координационные взаимодействия с центральным атомом магния гидрофобные взаимодействия с фитолом.
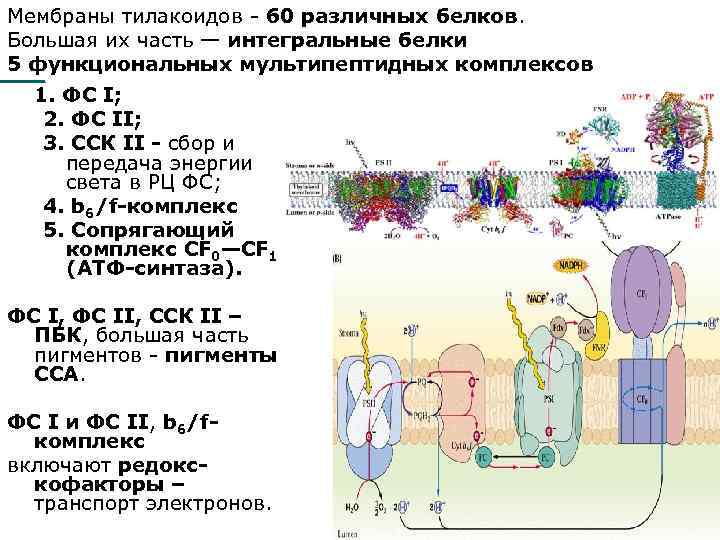
Мембраны тилакоидов - 60 различных белков. Большая их часть — интегральные белки 5 функциональных мультипептидных комплексов 1. ФС I; 2. ФС II; 3. ССК II - сбор и передача энергии света в РЦ ФС; 4. b 6/f-комплекс 5. Сопрягающий комплекс CF 0—CF 1 (АТФ-синтаза). ФС I, ФС II, ССК II – ПБК, большая часть пигментов - пигменты ССА. ФС I и ФС II, b 6/fкомплекс включают редокскофакторы – транспорт электронов.

ФОТОСИСТЕМЫ Определен полипептидный состав и субмолекулярная структура комплексов, установлена локализация в них редокс-кофакторов (P. R. Chitnis, 2001) ФС I и ФС II: 1. Центральная часть — структурное и функциональное ядро, способное осуществлять основные реакции, характерные для всего комплекса. ¡ белки, несущие компоненты РЦ и вторичные переносчики электронов, ¡ пигменты-светосборщики внутренних фокусирующих антенн. 2. Периферическая часть ü белки, связывающие пигменты-светосборщики внешней антенны комплекса, ü белки, либо играющие структурную роль, либо участвующие во взаимодействии с подвижными компонентами ЭТЦ.
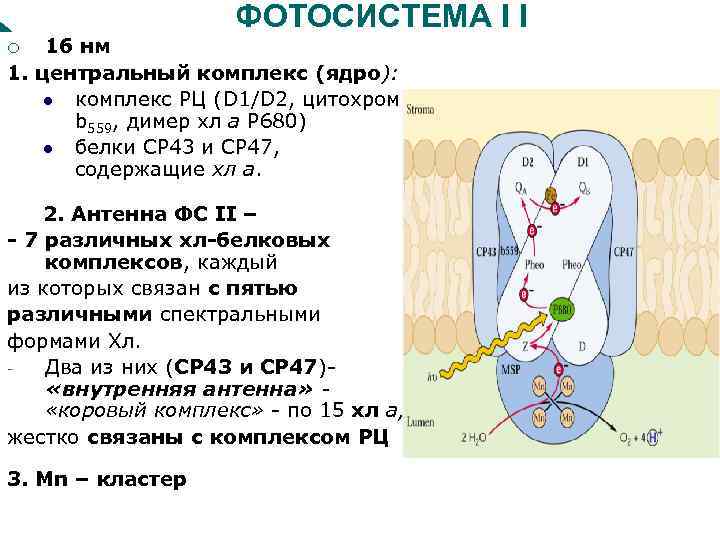
ФОТОСИСТЕМА I I 16 нм 1. центральный комплекс (ядро): l комплекс РЦ (D 1/D 2, цитохром b 559, димер хл а Р 680) l белки СР 43 и СР 47, содержащие хл а. ¡ 2. Антенна ФС II – - 7 различных хл-белковых комплексов, каждый из которых связан с пятью различными спектральными формами Хл. Два из них (СР 43 и СР 47) «внутренняя антенна» «коровый комплекс» - по 15 хл а, жестко связаны с комплексом РЦ 3. Mn – кластер
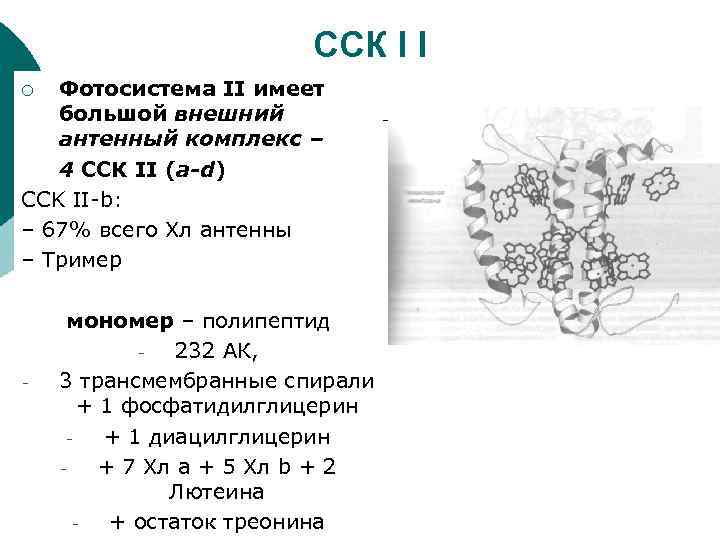
ССК I I Фотосистема II имеет большой внешний антенный комплекс – 4 ССК II (a-d) CCK II-b: – 67% всего Хл антенны – Тример ¡ - мономер – полипептид 232 АК, 3 трансмембранные спирали + 1 фосфатидилглицерин + 1 диацилглицерин + 7 Хл а + 5 Хл b + 2 Лютеина + остаток треонина
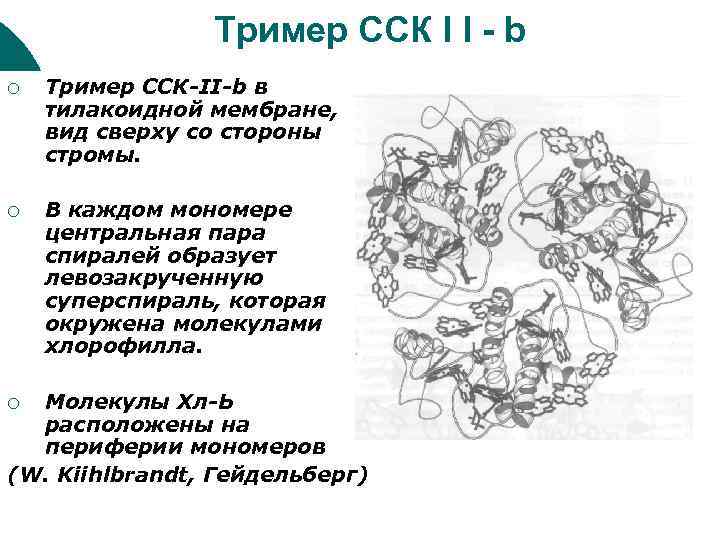
Тример ССК I I - b ¡ Тример ССК-II-b в тилакоидной мембране, вид сверху со стороны стромы. ¡ В каждом мономере центральная пара спиралей образует левозакрученную суперспираль, которая окружена молекулами хлорофилла. Молекулы Хл-Ь расположены на периферии мономеров (W. Kiihlbrandt, Гейдельберг) ¡
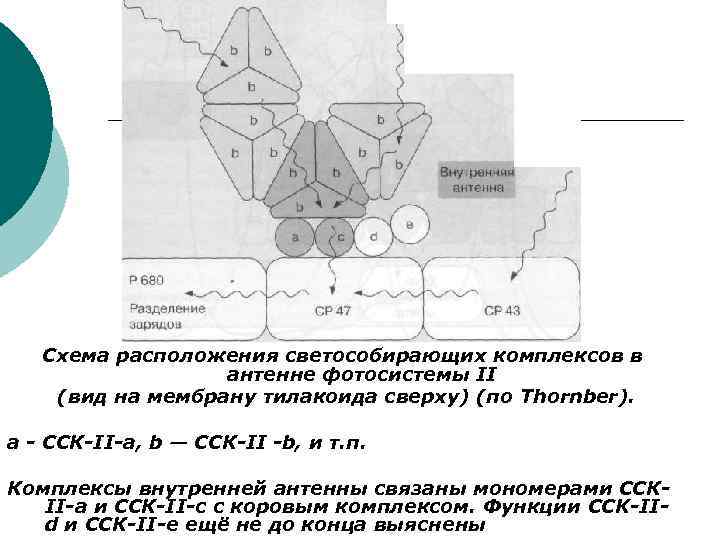
ССК I I Схема расположения светособирающих комплексов в антенне фотосистемы II (вид на мембрану тилакоида сверху) (по Thornber). а - ССК-II-а, b — ССК-II -b, и т. п. Комплексы внутренней антенны связаны мономерами ССКII-а и ССК-II-с с коровым комплексом. Функции CCK-IId и ССК-II-е ещё не до конца выяснены
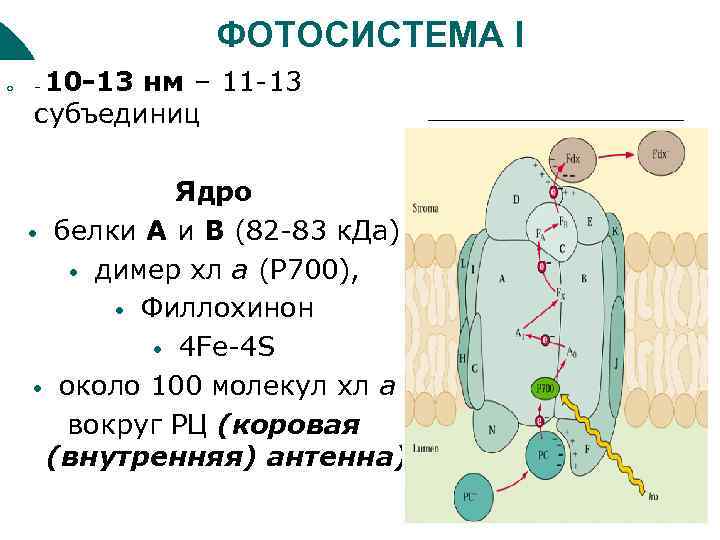
ФОТОСИСТЕМА I ¡ 10 -13 нм – 11 -13 субъединиц – Ядро • белки A и B (82 -83 к. Да) • димер хл а (Р 700), • Филлохинон • 4 Fe-4 S • около 100 молекул хл а вокруг РЦ (коровая (внутренняя) антенна).
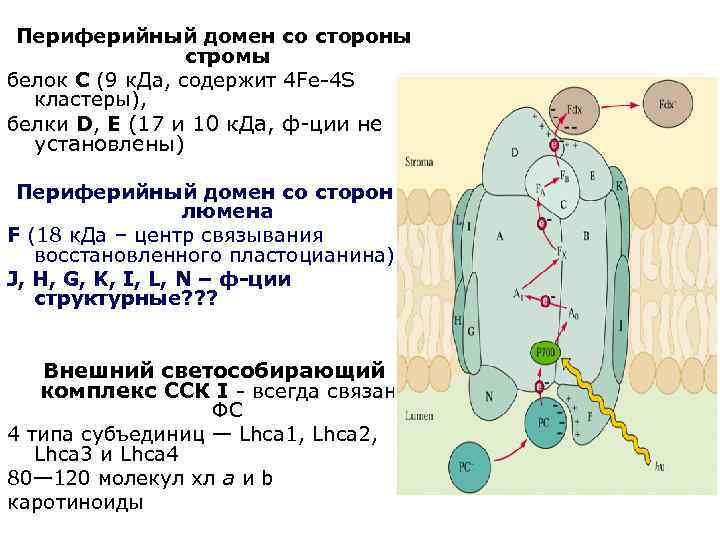
Периферийный домен со стороны стромы белок С (9 к. Да, содержит 4 Fe-4 S кластеры), белки D, E (17 и 10 к. Да, ф-ции не установлены) Периферийный домен со стороны люмена F (18 к. Да – центр связывания восстановленного пластоцианина) J, H, G, K, I, L, N – ф-ции структурные? ? ? Внешний светособирающий комплекс ССК I - всегда связан с ФС 4 типа субъединиц — Lhca 1, Lhca 2, Lhca 3 и Lhca 4 80— 120 молекул хл а и b каротиноиды

Комплекс цитохромов, b 6/f – комплекс, пластохинон-пластоцианин оксидоредуктаза 8 -9 нм (по структуре – аналог цитохромных комплексов бактерий и митохондрий ¡ Состоит из 5 -7 полипептидных субъединиц ¡ Цитохром f ¡ Цитохром b 6 ¡ Белок Риске - железосерный несут редокс-центры – транспорт электронов ¡ ¡ несколько субъединиц – организация функционального домена ¡ Окисляет пластохинон и восстанавливает пластоцианин
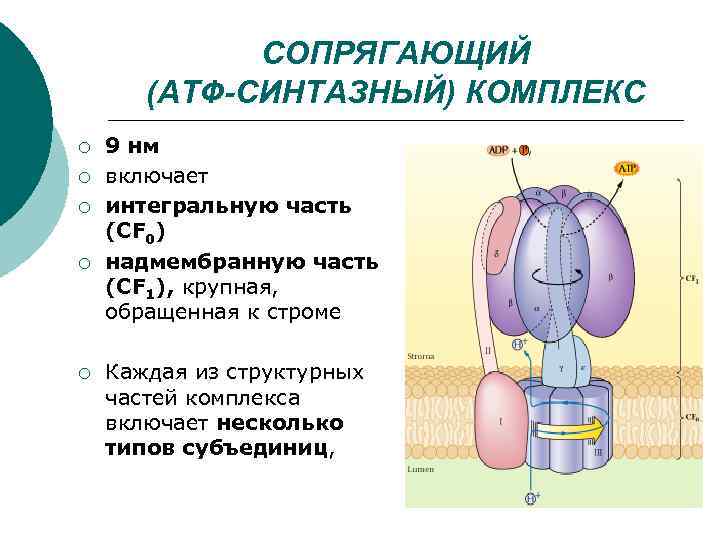
СОПРЯГАЮЩИЙ (АТФ-СИНТАЗНЫЙ) КОМПЛЕКС ¡ ¡ ¡ 9 нм включает интегральную часть (CF 0) надмембранную часть (CF 1), крупная, обращенная к строме Каждая из структурных частей комплекса включает несколько типов субъединиц,
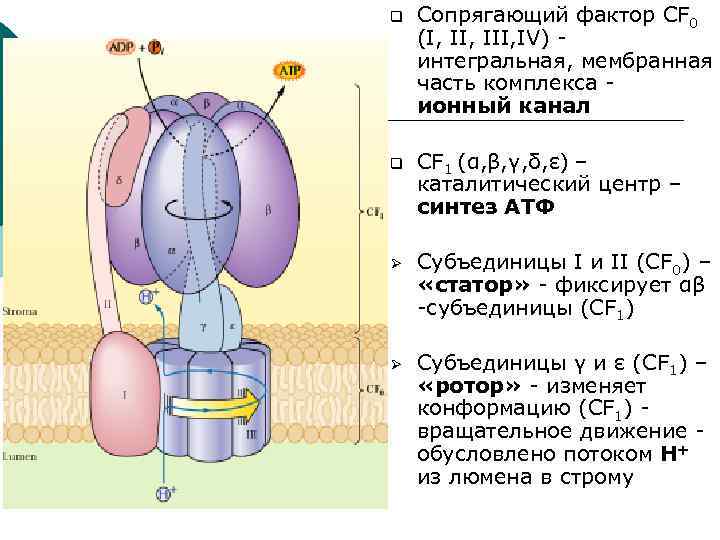
q Сопрягающий фактор CF 0 (I, III, IV) интегральная, мембранная часть комплекса ионный канал q CF 1 (α, β, γ, δ, ε) – каталитический центр – синтез АТФ Ø Субъединицы I и II (CF 0) – «статор» - фиксирует αβ -субъединицы (CF 1) Ø Субъединицы γ и ε (CF 1) – «ротор» - изменяет конформацию (CF 1) вращательное движение обусловлено потоком Н+ из люмена в строму
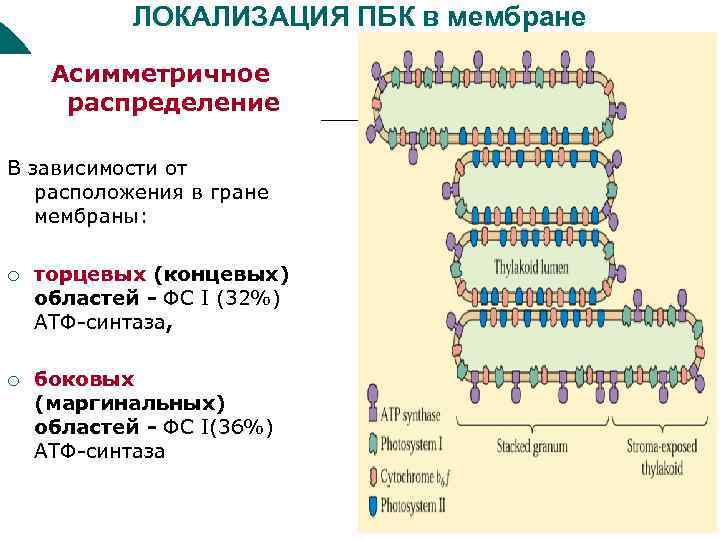
ЛОКАЛИЗАЦИЯ ПБК в мембране Асимметричное распределение В зависимости от расположения в гране мембраны: ¡ торцевых (концевых) областей - ФС I (32%) АТФ-синтаза, ¡ боковых (маргинальных) областей - ФС I(36%) АТФ-синтаза
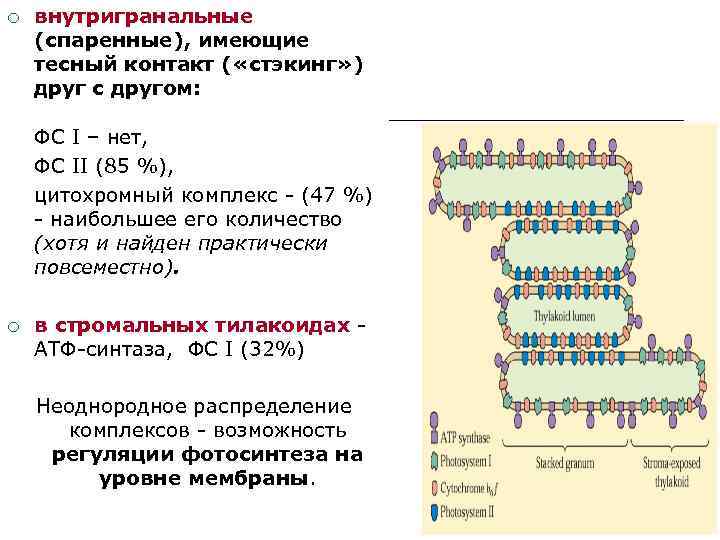
¡ внутригранальные (спаренные), имеющие тесный контакт ( «стэкинг» ) друг с другом: ФС I – нет, ФС II (85 %), цитохромный комплекс - (47 %) - наибольшее его количество (хотя и найден практически повсеместно). ¡ в стромальных тилакоидах АТФ-синтаза, ФС I (32%) Неоднородное распределение комплексов - возможность регуляции фотосинтеза на уровне мембраны.

МНОГООБРАЗИЕ ФУНКЦИЙ белков, входящих в комплексы 1. присоединяют органические и неорганические кофакторы и ориентируют комплексы в пространстве оптимальным для поглощения света и транспорта электронов образом. 2. влияют на свойства кофакторов, участвуя в лигандных взаимодействиях с металлами, образуя водородные связи или формируя гидрофобные окружения кофакторов. 3. участвуют в организации центров связывания белков и кофакторов, взаимодействующих с комплексом. 4. функции ряда белков комплексов могут быть связаны со стабилизацией всего комплекса. 5. пассивно защищают редоксагенты от внешних воздействий. ¡ Белки ядра комплексов кодируются хлоропластным геномом, белки периферической части - в ядерной ДНК.

ДРУГИЕ БЕЛКИ НЕБОЛЬШИЕ БЕЛКОВЫЕ КОМПОНЕНТЫ, расположенные на поверхности мембран ¡ Пластоцианин — со стороны люмена, на внутренней поверхности мембран тилакоидов, ¡ ферредоксин и ферредоксин. НАДФ-оксидоредуктаза — с наружной, стромальной стороны мембраны (НАД(Ф)Ндегидрогеназный комплекс) Участвуют в окислительновосстановительных реакциях, связанных с процессами преобразования энергии при фотосинтезе.

ВОДА И НЕОРГАНИЧЕСКИЕ ИОНЫ ВОДА ¡ ¡ ¡ играет структурную роль, участвуя в формировании функционально активной конформации белковых компонентов мембран, стабилизирует мембраны, непосредственно участвует в процессах фотосинтеза.

НЕОРГАНИЧЕСКИЕ ИОНЫ (К+, Na+, Mg 2+) 1. определяют общий поверхностный заряд мембран 2. возможность взаимодействия отдельных мембран друг с другом (контролируют образование гран в хлоропласте). 3. важны для сборки комплексов белков и создания определенной функционально активной конформации. 4. Катионы, экранируя отрицательные заряды на поверхности мембран, снижают силы их отталкивания, что ведет к слипанию мембран и образованию граны. l При снижении концентрации катионов в среде или полном их удалении - разделение тилакоидов в гране, грана рассыпается и остается система связанных тилакоидных везикул. При добавлении катионов - вновь возникает взаимное притяжение мембран тилакоидов и формируется грана.

ФИЗИКО-ХИМИЧЕСКИЕ СВОЙСТВА ТИЛАКОИДНЫХ МЕМБРАН 1. Отрицательный поверхностный заряд при физиологических p. Н и неоднородность его распределения на мембране (белки, липиды, катионы). 2. Асимметрия (неоднородность) мембран ¡ Трансмембранная – неоднородность хим. состава и структуры (расположение липидных и белковых компонентов) внешнего и внутр слоя мембраны ¡ Латеральная асимметрия - мембраны тилакоидов гран и стромы существенно различаются по химическому составу, структуре и функциям. 3. ¡ ¡ РАЗДЕЛЕНИЕ ЗАРЯДОВ НА МЕМБРАНЕ И ВЫСОКИЕ ЗНАЧЕНИЯ ЭЛЕКТРОХИМ ПОТЕНЦИАЛА в ходе трансформации энергии возможны благодаря : Высокой текучести мембран в широком диапазоне температур, обусловленной высоким содержанием полиненасыщенных ЖК Высокого электрического сопротивления липидного бислоя придающее мембране св-ва диэлектрика
Лекция 4 мол организация ФСА.ppt