05bioch-1711-2014-сигнализация.ppt
- Количество слайдов: 69

Молекулярная нейробиология Внутриклеточная сигнализация в нервной системе Лекция 5. И. А. Гривенников Институт молекулярной генетики РАН
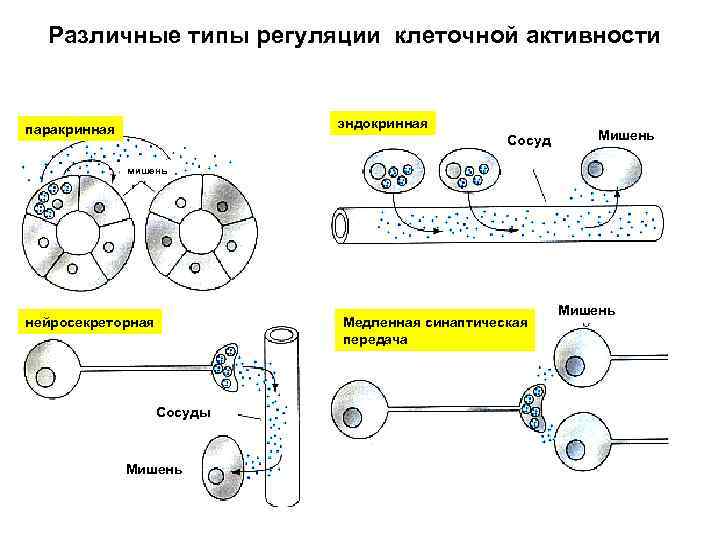
Различные типы регуляции клеточной активности эндокринная паракринная Сосуд Мишень мишень нейросекреторная Медленная синаптическая передача Сосуды Мишень
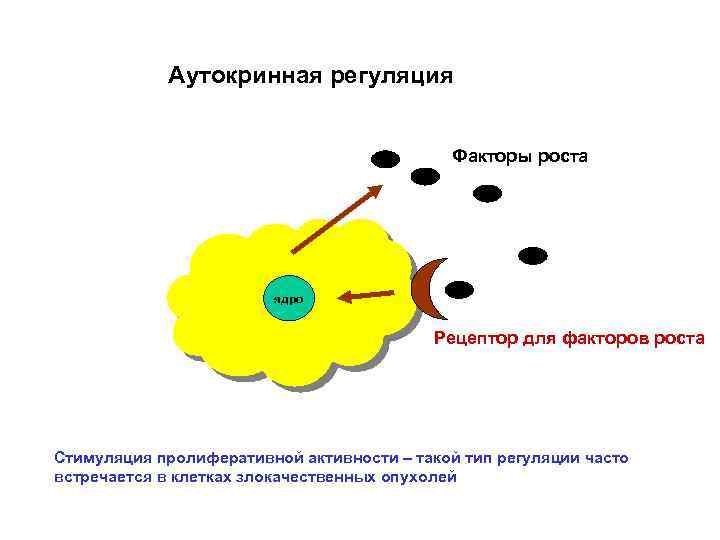
Аутокринная регуляция Факторы роста ядро Рецептор для факторов роста Стимуляция пролиферативной активности – такой тип регуляции часто встречается в клетках злокачественных опухолей
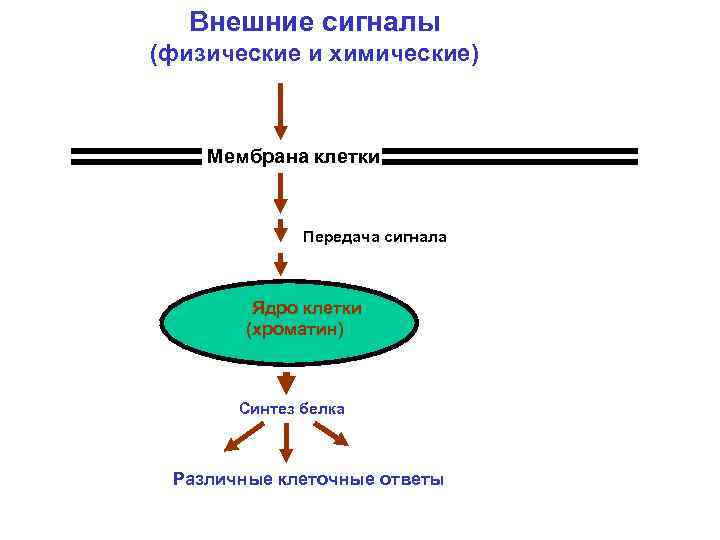
Внешние сигналы (физические и химические) Внеклеточное пространство Мембрана клетки Цитоплазма Передача сигнала Ядро клетки (хроматин) Синтез белка Различные клеточные ответы

Внешние сигналы 1. Гормоны (инсулин, глюкагон, адреналин) 2. Нейротрансмиттеры (глутамат, ацетилхолин) 3. Факторы роста и дифференцировки (ФРФ, ФНО, ФРН) 4. Регуляторные пептиды 5. Физические факторы (механическое воздействие, электрическое воздействие) 6. Стероидные гормоны, глюкокортикоиды. 7. Химические сигналы (вкус, обоняние)
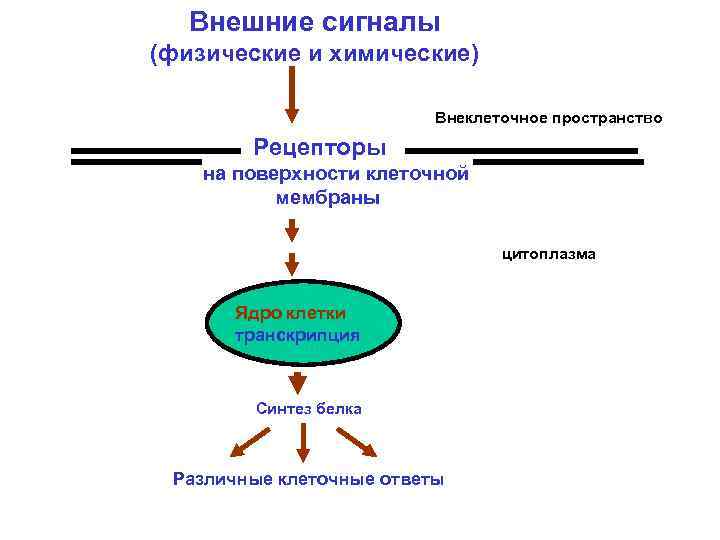
Внешние сигналы (физические и химические) Внеклеточное пространство Рецепторы на поверхности клеточной мембраны Цитоплазма цитоплазма Ядро клетки транскрипция Синтез белка Различные клеточные ответы
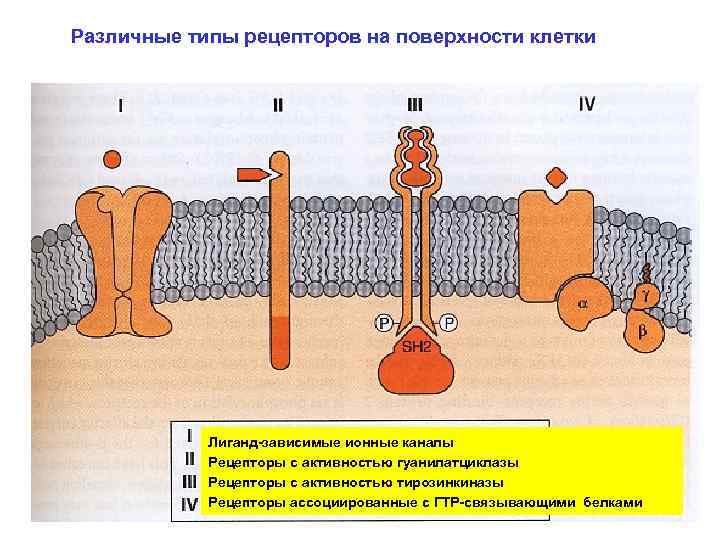
Различные типы рецепторов на поверхности клетки Лиганд-зависимые ионные каналы Рецепторы с активностью гуанилатциклазы Рецепторы с активностью тирозинкиназы Рецепторы ассоциированные с ГТР-связывающими белками

Сигналы от различных внешних воздействий передаются внутрь клетки на соответствующие ферменты через системы рецепторов и системы вторичных посредников или мессенджеров

Внешние сигналы (гормоны, регуляторные пептиды, факторы роста, нейротрансмиттеры и др. ) Внеклеточное пространство Рецепторы Цитоплазма Ферменты, производящие вторичные мессенджеры (аденилатциклаза, гуанилатциклаза, Фосфолипаза и др. ) с. АМР, с. GMP, ДА, ИТР, NO Ферменты, разрушающие вторичные мессенджеры Система протеинкиназ и протеинфосфатаз и их белковые субстраты Ядро клетки Экспрессия генов
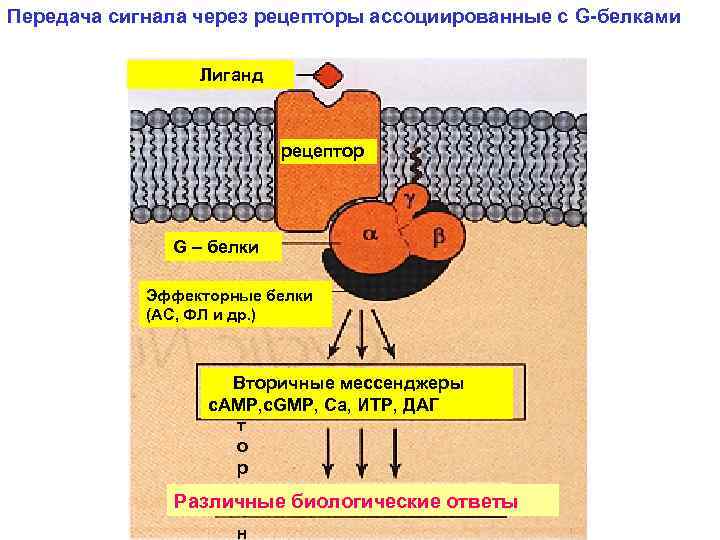
Передача сигнала через рецепторы ассоциированные с G-белками Лиганд рецептор G – белки Эффекторные белки (АС, ФЛ и др. ) В Вторичные мессенджеры В с. АМР, с. GМР, Са, ИТР, ДАГ т о р и Различные биологические ответы ч н
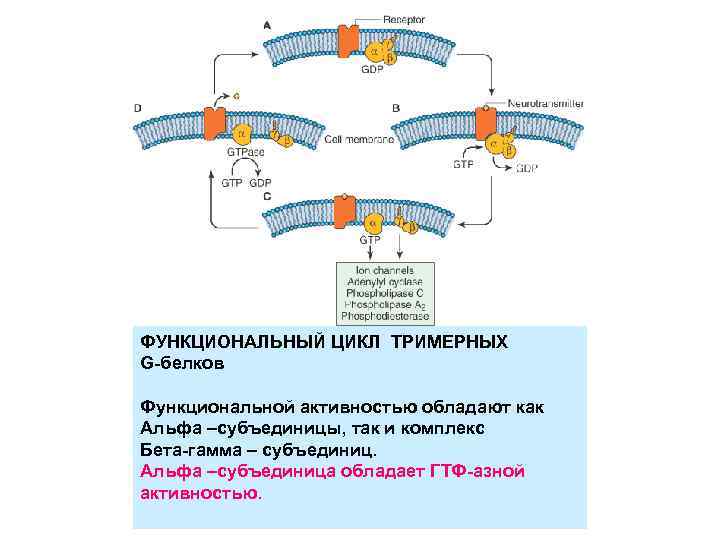
ФУНКЦИОНАЛЬНЫЙ ЦИКЛ ТРИМЕРНЫХ G-белков Функциональной активностью обладают как Альфа –субъединицы, так и комплекс Бета-гамма – субъединиц. Альфа –субъединица обладает ГТФ-азной активностью.

Альфа-субъединицы G-белков в мозге и некоторые их функции. (в ряде случаев эффекты на соответствующие белки-мишени могут осуществляться димером бета-гамма субъединиц)

c. АMP – пути образования в нервной системе
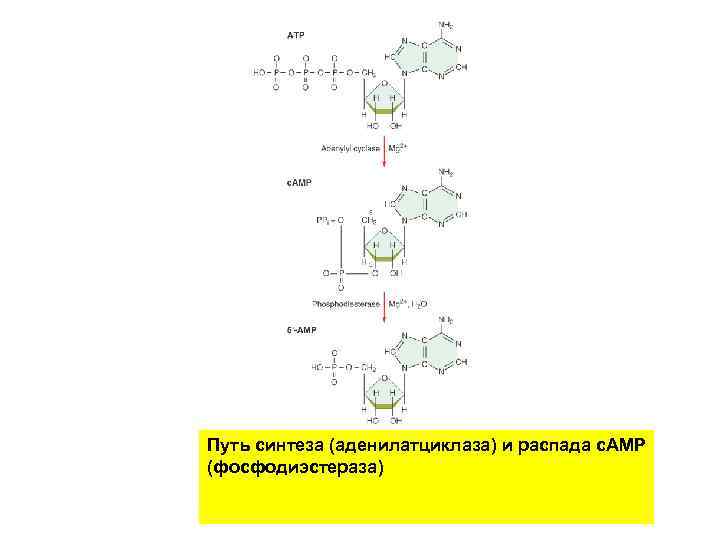
Путь синтеза (аденилатциклаза) и распада с. АМР (фосфодиэстераза)
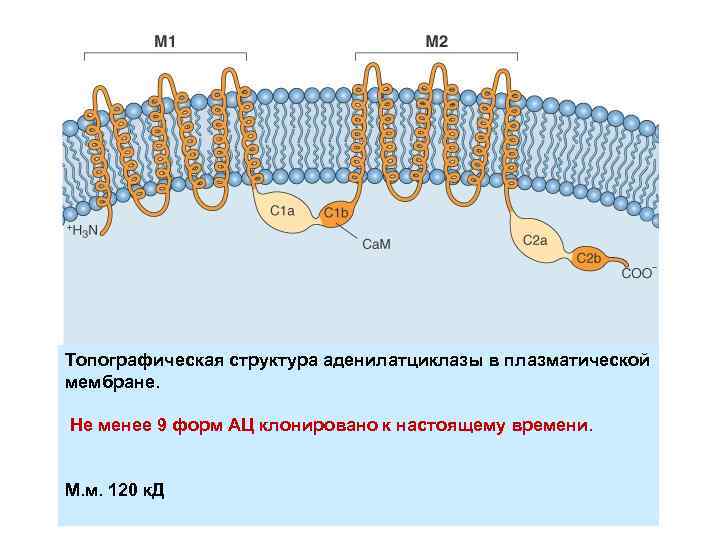
Топографическая структура аденилатциклазы в плазматической мембране. Не менее 9 форм АЦ клонировано к настоящему времени. М. м. 120 к. Д
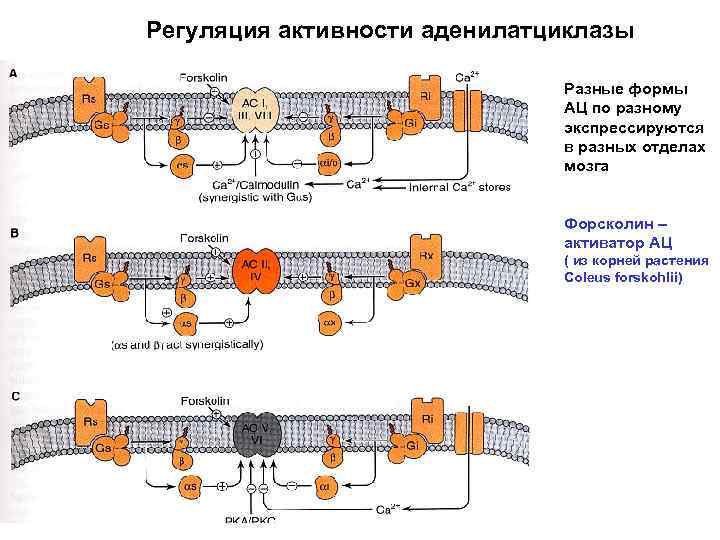
Регуляция активности аденилатциклазы Разные формы АЦ по разному экспрессируются в разных отделах мозга Форсколин – активатор АЦ ( из корней растения Coleus forskohlii)

В обонятельной системе существует специфическая форма альфа-субъединицы G-белков: альфа olf Запахи воспринимаются сотнями рецепторов находящихся в клетках нейроэпителия, которые активируют альфа olf и передают сигнал на аденилатциклазу III типа

Почему системы регулируемые G-белками устроены так сложно? Все трансмембранные сигнальные системы включают 2 основных элемента: - один (рецептор) узнает внеклеточный сигнал, - второй генерирует внутриклеточный сигнал (успешно реализуется в гуанилатциклазах и тирозинкиназах (мембранных) Системы регулируемые G-белками содержат продукты разных типов генов: Рецепторы - сотни генов Гетеротримерные G-белки - несколько генов Эффекторы - несколько генов Каждый компонент этой системы может регулироваться «независимо» на уровне транскрипции, посттрансляционной модификации и взаимодействия с другими молекулами Каждая клетка организма «выбирает» разный комплект таких молекул, что создает разнообразность ответов на сложные и, в частности, стрессорные воздействия внешней среды.
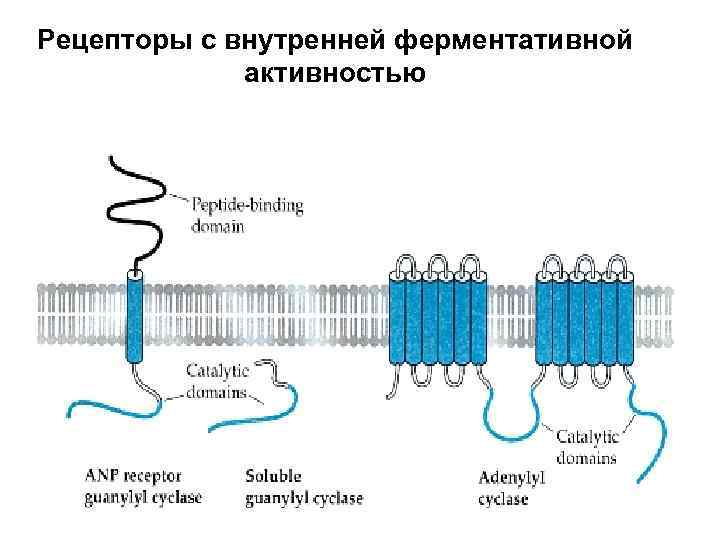
Рецепторы с внутренней ферментативной активностью

c. GMP – пути образования в нервной системе Образование c. GMP происходит из ГТР за счет фермента гуанилатциклазы Известны 2 основных класса этих ферментов: - мембранносвязанные - «растворимые» , цитоплазматические 3 основные мембранносвязанные формы гуанилатциклазы (м. м. 120 кд): А. связывает ANP ( натрийуретический пептид сердца), BNP (натрийуретический пептид мозга ). В. связывает CNP (натрийуретический пептид С-типа). Экспрессируется в мозге С. Связывает гуанилин. Экспрессируется в кишечнике.
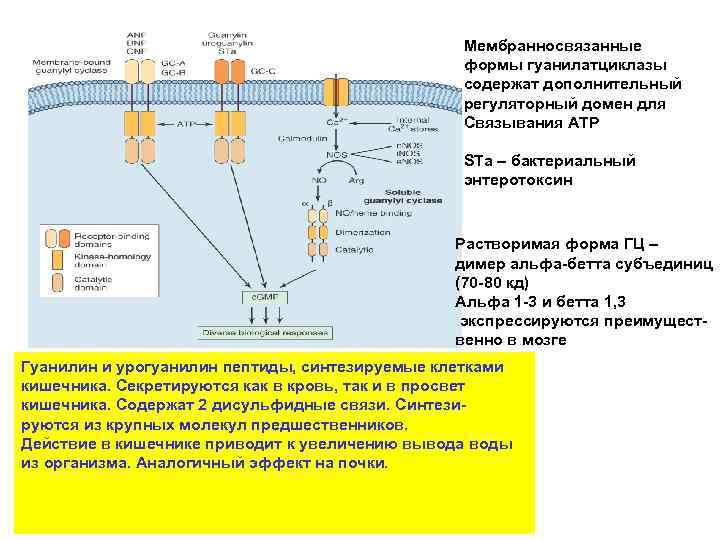
Мембранносвязанные формы гуанилатциклазы содержат дополнительный регуляторный домен для Связывания АТР STa – бактериальный энтеротоксин Растворимая форма ГЦ – димер альфа-бетта субъединиц (70 -80 кд) Альфа 1 -3 и бетта 1, 3 экспрессируются преимущественно в мозге Гуанилин и урогуанилин пептиды, синтезируемые клетками кишечника. Секретируются как в кровь, так и в просвет кишечника. Содержат 2 дисульфидные связи. Синтезируются из крупных молекул предшественников. Действие в кишечнике приводит к увеличению вывода воды из организма. Аналогичный эффект на почки.

Ферменты, расщепляющие вторичные посредники ( с. АМР, с. GМР)
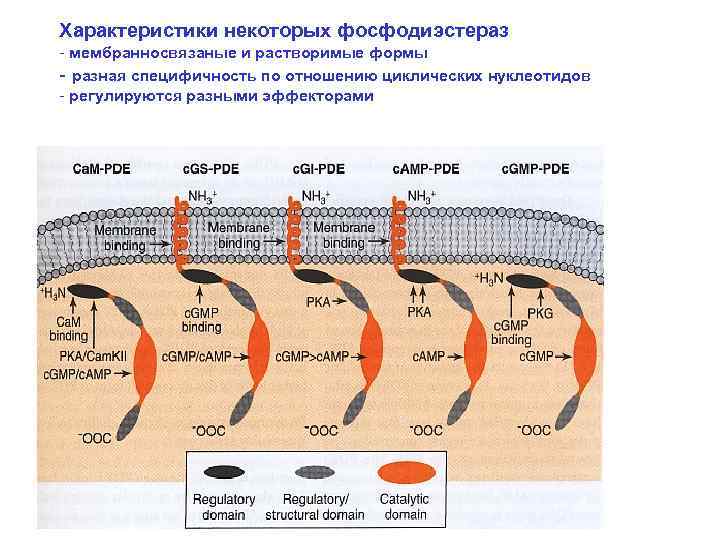
Характеристики некоторых фосфодиэстераз - мембранносвязаные и растворимые формы - разная специфичность по отношению циклических нуклеотидов - регулируются разными эффекторами
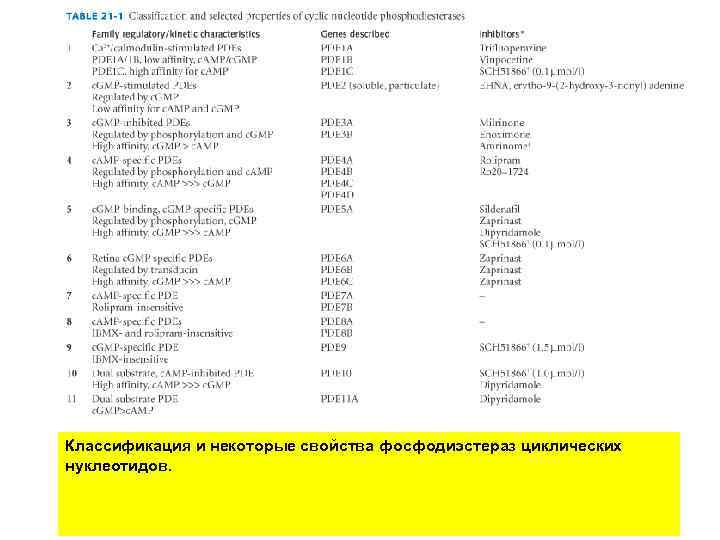
Классификация и некоторые свойства фосфодиэстераз циклических нуклеотидов.
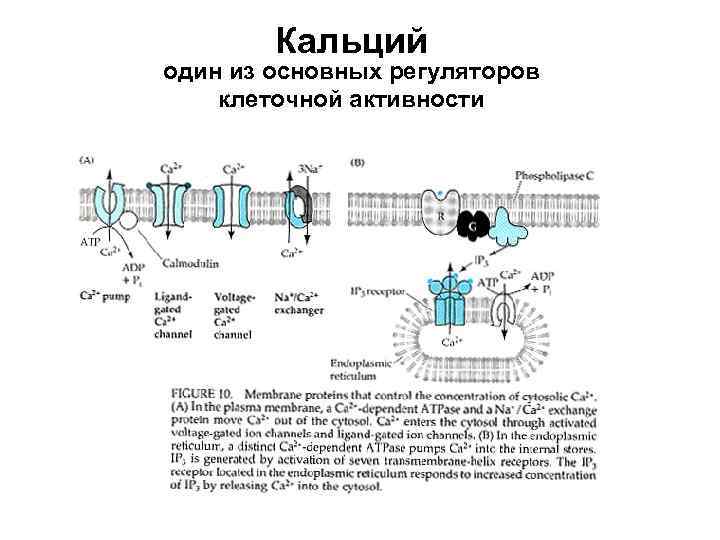
Кальций один из основных регуляторов клеточной активности
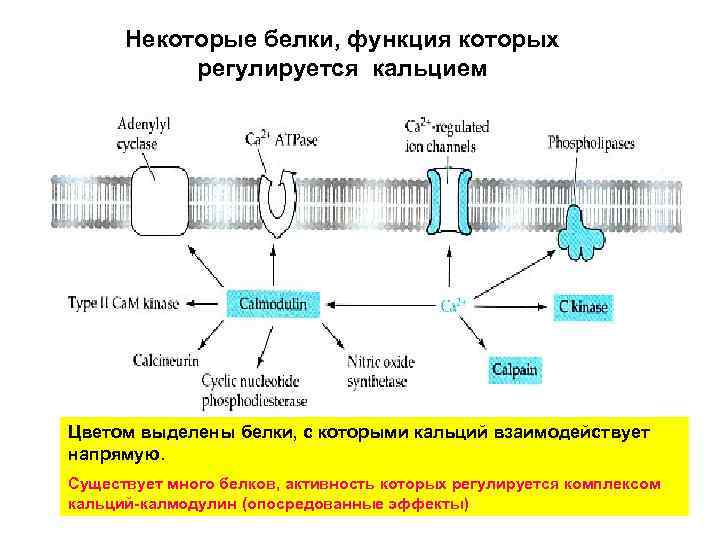
Некоторые белки, функция которых регулируется кальцием Цветом выделены белки, с которыми кальций взаимодействует напрямую. Существует много белков, активность которых регулируется комплексом кальций-калмодулин (опосредованные эффекты)
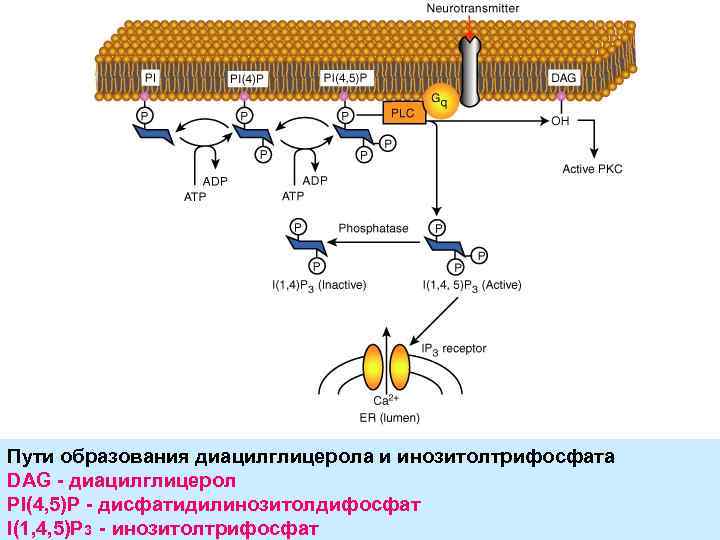
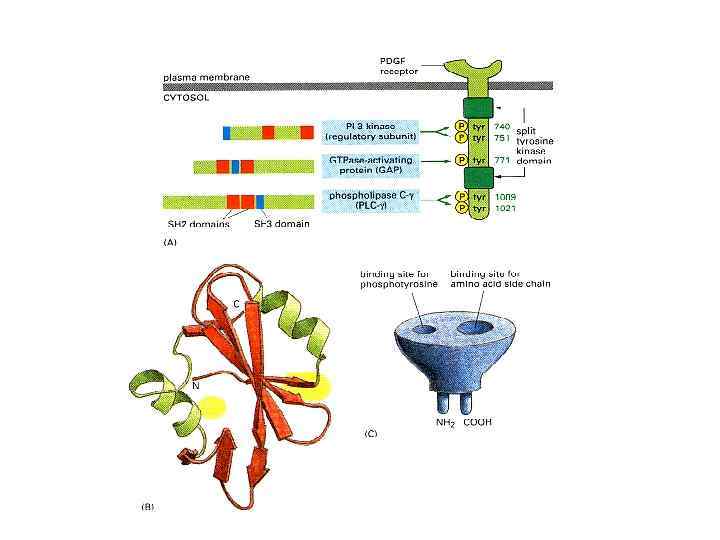
Пути образования диацилглицерола и инозитолтрифосфата DAG - диацилглицерол PI(4, 5)P - дисфатидилинозитолдифосфат I(1, 4, 5)P 3 - инозитолтрифосфат
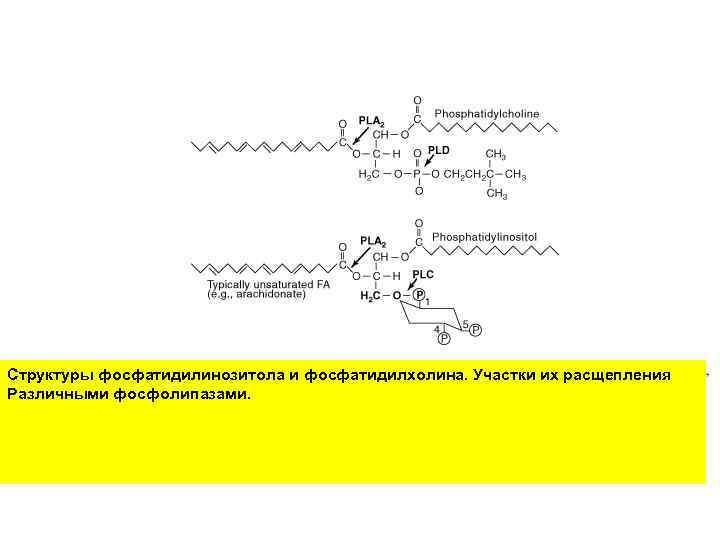
Структуры фосфатидилинозитола и фосфатидилхолина. Участки их расщепления Различными фосфолипазами.

Ковалентные модификации белков – способ регуляции их активности -Ацетилирование -Метилирование -Гликозилирование -Миристилирование -Фосфорилирование -и др.
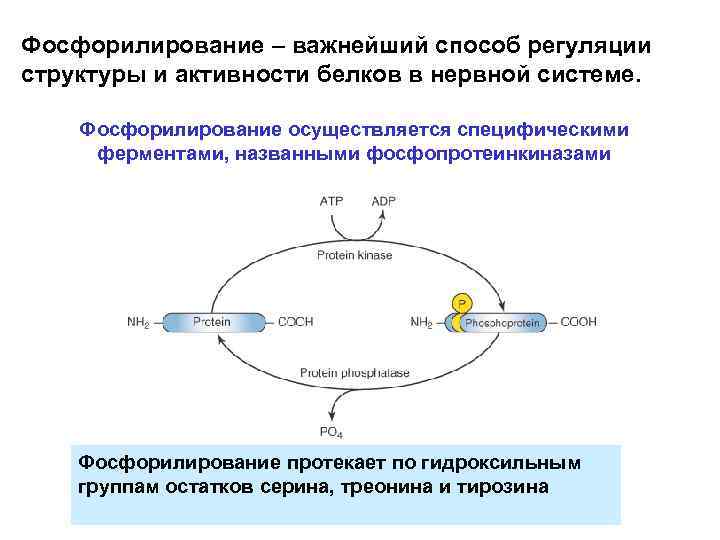
Фосфорилирование – важнейший способ регуляции структуры и активности белков в нервной системе. Фосфорилирование осуществляется специфическими ферментами, названными фосфопротеинкиназами Фосфорилирование протекает по гидроксильным группам остатков серина, треонина и тирозина

Генерация в клетке различных вторичных посредников приводит к стимуляции активности соответствующих протеинкиназ
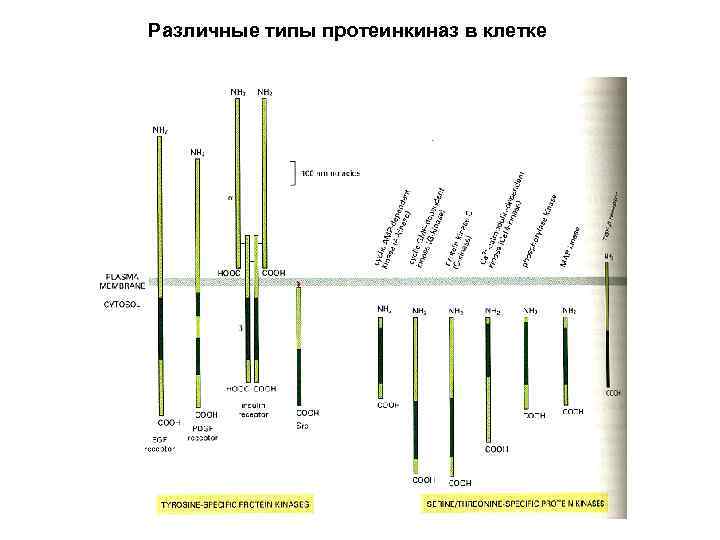
Различные типы протеинкиназ в клетке
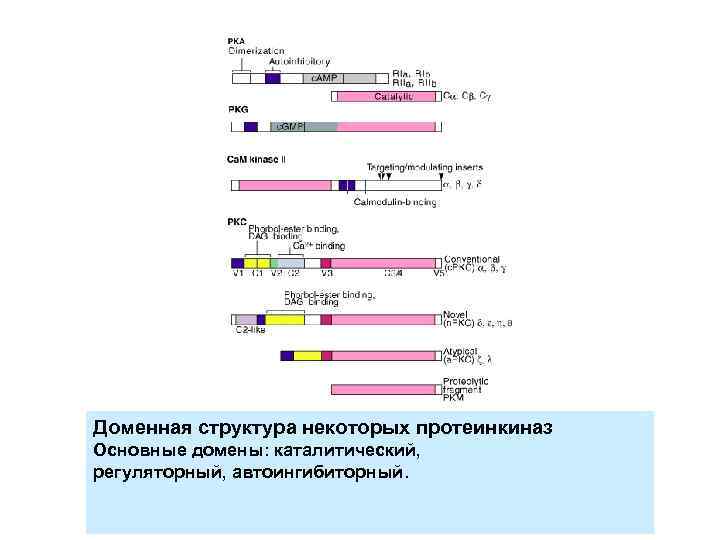
Доменная структура некоторых протеинкиназ Основные домены: каталитический, регуляторный, автоингибиторный.
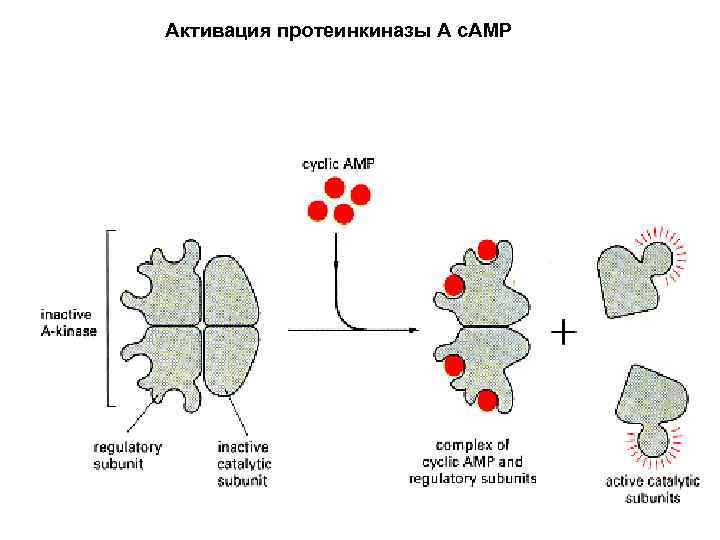
Активация протеинкиназы А с. АМР
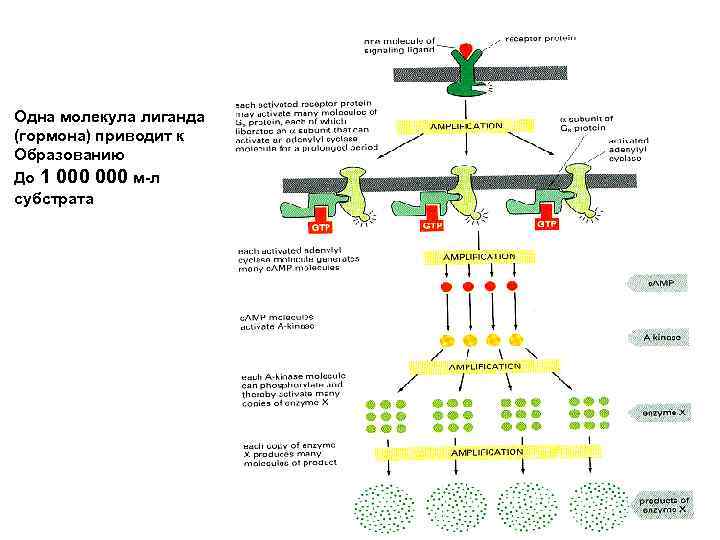
Усиление Сигнала !!! Одна молекула лиганда (гормона) приводит к Образованию До 1 000 м-л субстрата
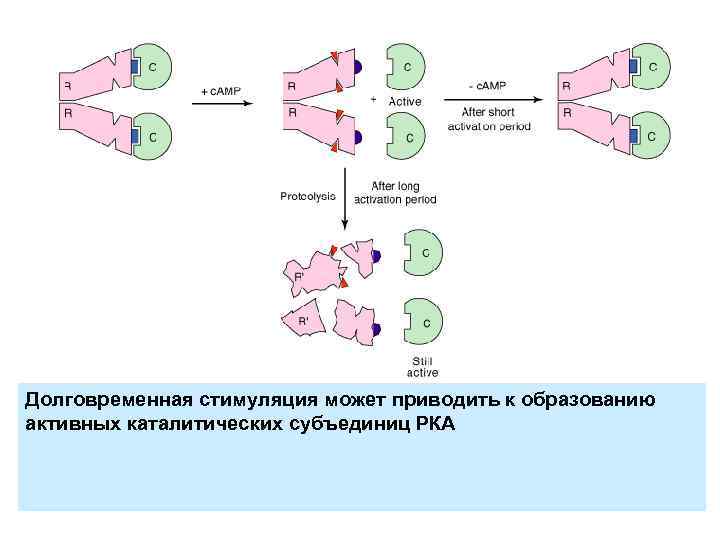
Долговременная стимуляция может приводить к образованию активных каталитических субъединиц РКА
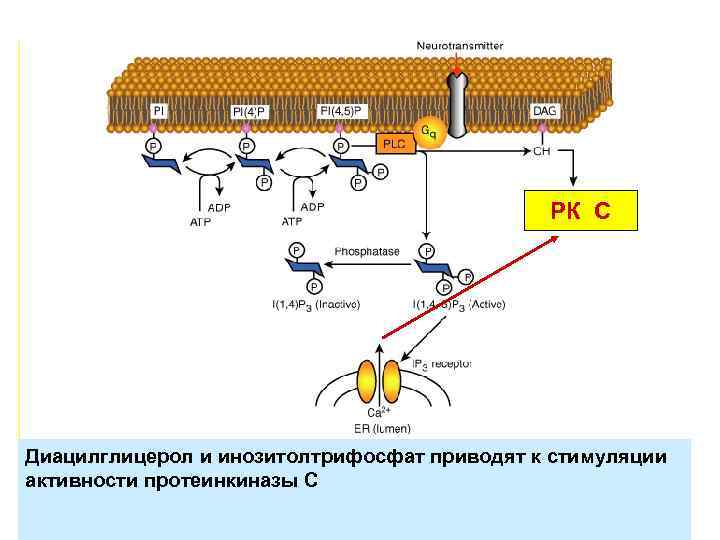
Путь активации протеинкиназы С РК С Диацилглицерол и инозитолтрифосфат приводят к стимуляции активности протеинкиназы С

Кальций Диацилглицерол Форболовые эфиры Протеинкиназа С (70 -90 к. Да) (Участие в экзо и эндоцитозе, регуляции роста и деления клеток, пластичности, ионных каналов и рецепторов) В отличие от РК-А протеинкиназа С мономер и содержит каталитический, Регуляторный и ингибиторный домены в одной полипептидной цепи. Много различных изоформ: - Обычные РКС (с. РКС) содержат все необходимые домены. - новые РКС (н. РКС) не содержат С 2 домена и не чувствительны к кальцию. - атипичные РКС (а. РКС) не содержат С 1 и С 2 домена и не чувствительны к кальцию, ДАГ и ФЭ.

Протеинкиназа С V 1 - ингибиторный домен V 3 – участок чувствительный к протеазам V 5 – участок ответственный за «заякоривание» РКС C 3 – каталитический домен При кальций-зависимом протеолизе неактивной РКС происходит образование РКМ – Киназы с постоянной активностью Доменная структура некоторых протеинкиназ Основные домены: каталитический, Регуляторный, автоингибиторный.

Участки фосфорилирования различными протеинкиназами имеют характерную последовательность
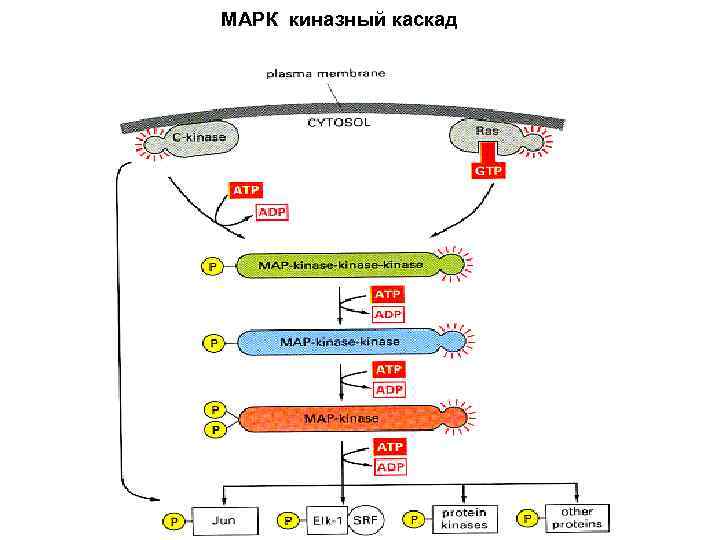
МАРК киназный каскад
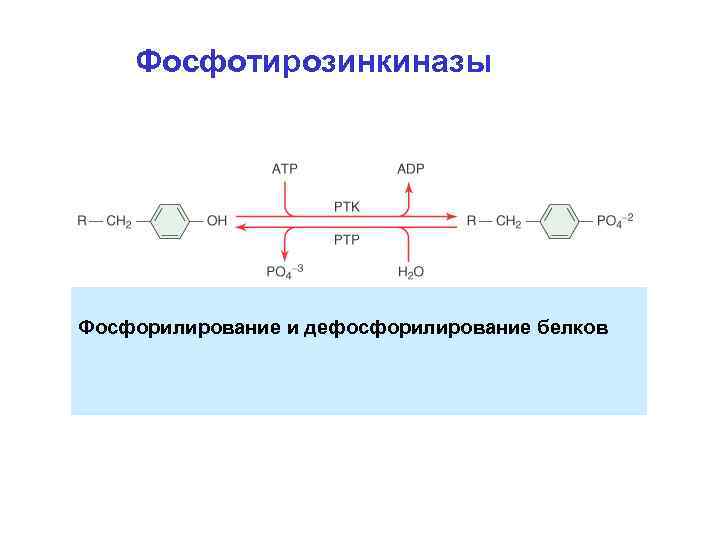
Фосфотирозинкиназы Фосфорилирование и дефосфорилирование белков

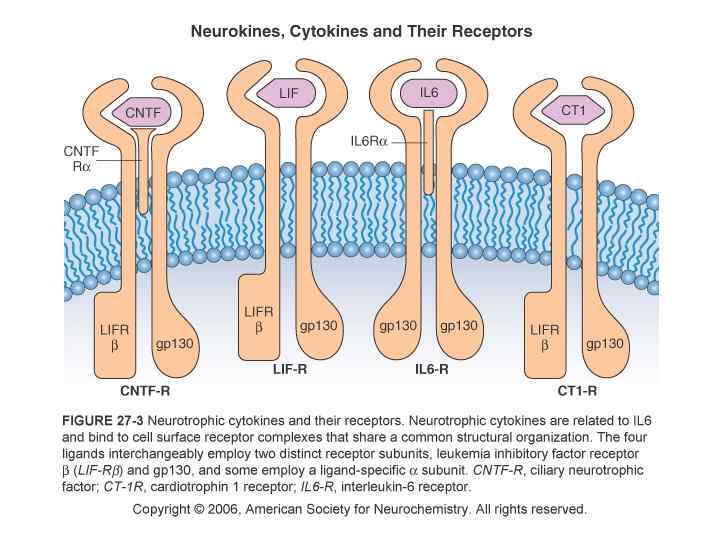
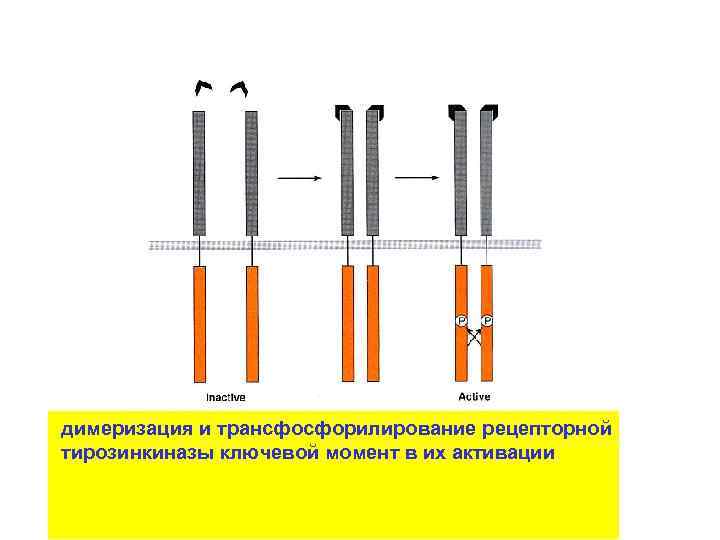
димеризация и трансфосфорилирование рецепторной тирозинкиназы ключевой момент в их активации
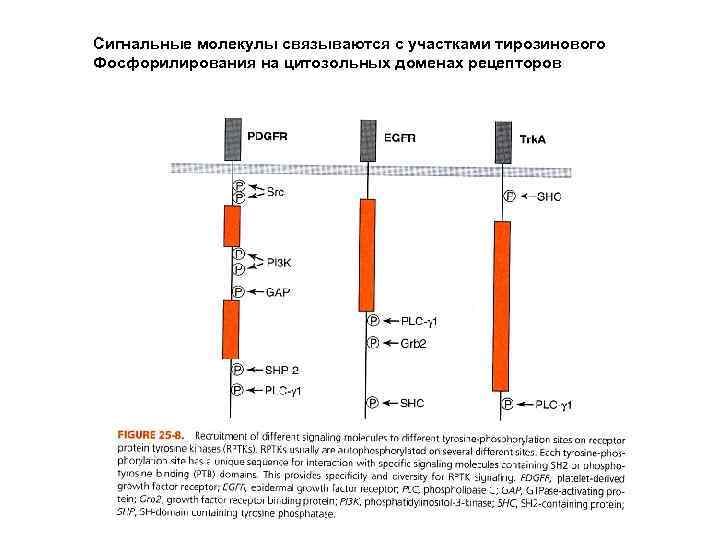
Сигнальные молекулы связываются с участками тирозинового Фосфорилирования на цитозольных доменах рецепторов


В нервной системе часто экспрессируются специфические формы протеинкиназ Некоторые примеры белков, подвергающихся фосфорилированию в нервной системе Нобелевская премия 2000 г. по физиологии/медицине Eric Kandel, Paul Greengard (фосфорилирование и дефосфорилирование белков в нервной системе)

Фосфорилированию подвергаются множество представителей различных классов белков: - ферменты, - белки ионных каналов, - рецепторы и траспортеры нейротрасмиттеров, - белки цитоскелета, - белки участвующие в генерации вторичных мессенджеров, - факторы траскрипции, - белки «синаптической передачи» - протеинкиназы и др.

Фосфорилирование тяжелых и средних нейрофиламентов приводит к их взаимному отталкиванию и увеличению толщины аксона и поддержанию его размеров и формы

Са. М киназа типа II (кальций-калмодулин зависимая Протеинкиназа II Много в нервной системе (в нейронах гиппокампа до 2% от общего белка клетки). Фосфорилирует многочисленные субстраты важные для активности нервных клеток: Тирозингидроксилазу, Синапсин I, МАР 2, Кальциевые каналы, Транскрипционные факторы В клетке обнаружена в цитозоле, ядре, в постсинаптических утолщениях, в комплексе с белками цитоскелета
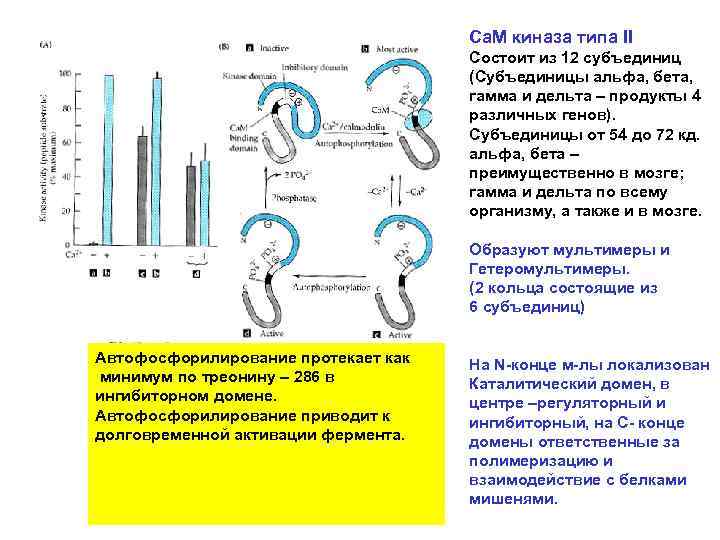
Са. М киназа типа II Состоит из 12 субъединиц (Субъединицы альфа, бета, гамма и дельта – продукты 4 различных генов). Субъединицы от 54 до 72 кд. альфа, бета – преимущественно в мозге; гамма и дельта по всему организму, а также и в мозге. Образуют мультимеры и Гетеромультимеры. (2 кольца состоящие из 6 субъединиц) Автофосфорилирование протекает как минимум по треонину – 286 в ингибиторном домене. Автофосфорилирование приводит к долговременной активации фермента. На N-конце м-лы локализован Каталитический домен, в центре –регуляторный и ингибиторный, на С- конце домены ответственные за полимеризацию и взаимодействие с белками мишенями.
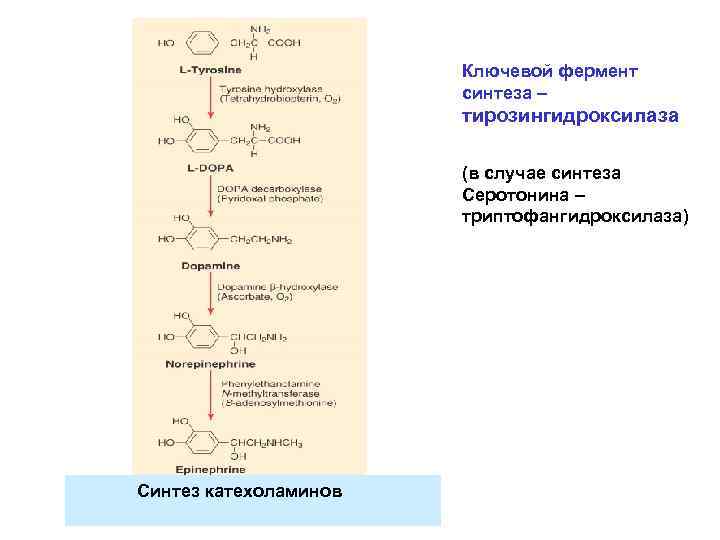
Ключевой фермент синтеза – тирозингидроксилаза (в случае синтеза Серотонина – триптофангидроксилаза) Синтез катехоламинов
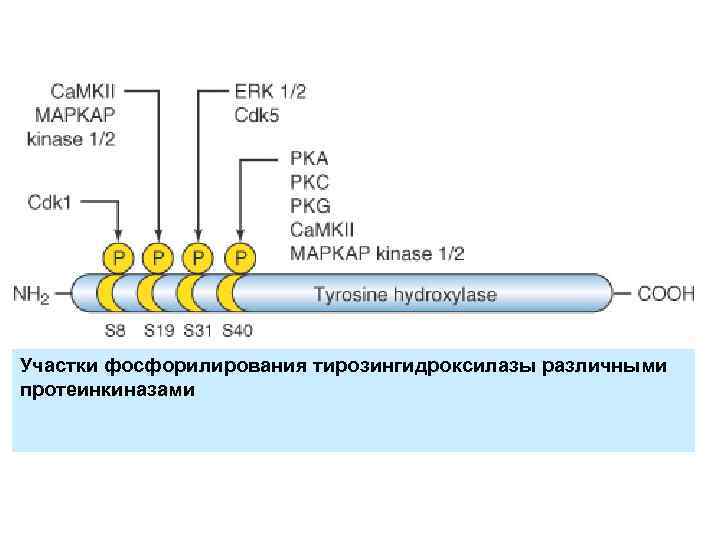
Участки фосфорилирования тирозингидроксилазы различными протеинкиназами
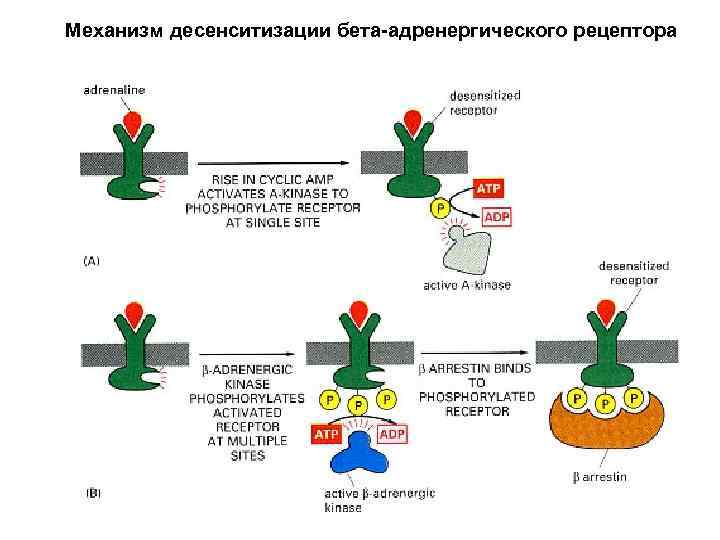
Механизм десенситизации бета-адренергического рецептора
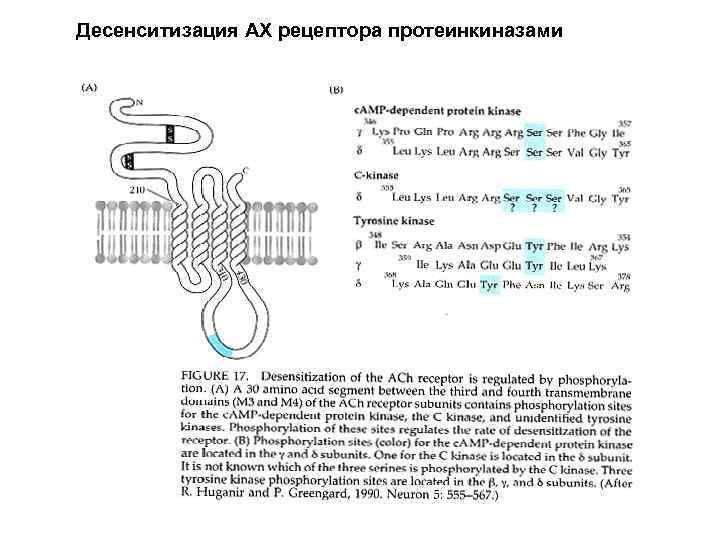
Десенситизация АХ рецептора протеинкиназами
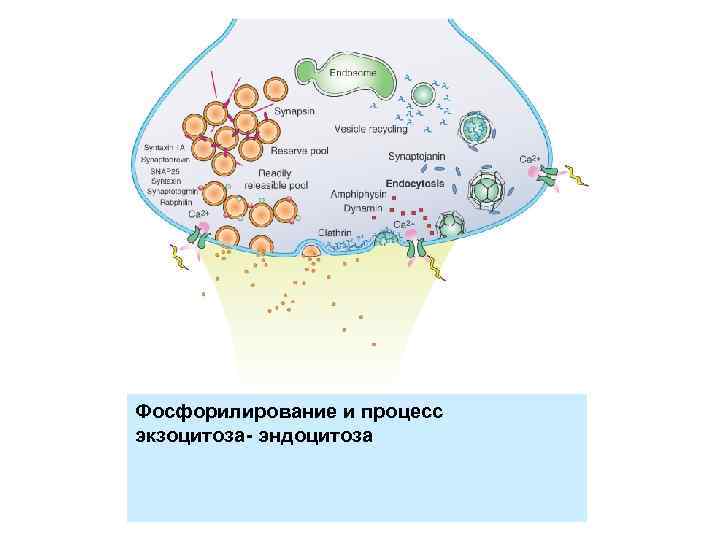
Фосфорилирование и процесс экзоцитоза- эндоцитоза
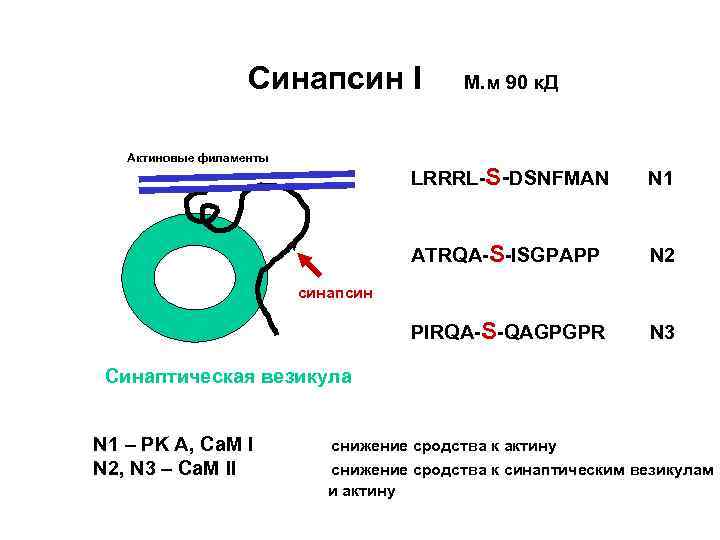
Синапсин I Актиновые филаменты М. м 90 к. Д LRRRL-S-DSNFMAN N 1 ATRQA-S-ISGPAPP N 2 PIRQA-S-QAGPGPR N 3 синапсин Синаптическая везикула N 1 – PK A, Ca. M I N 2, N 3 – Ca. M II снижение сродства к актину снижение сродства к синаптическим везикулам и актину
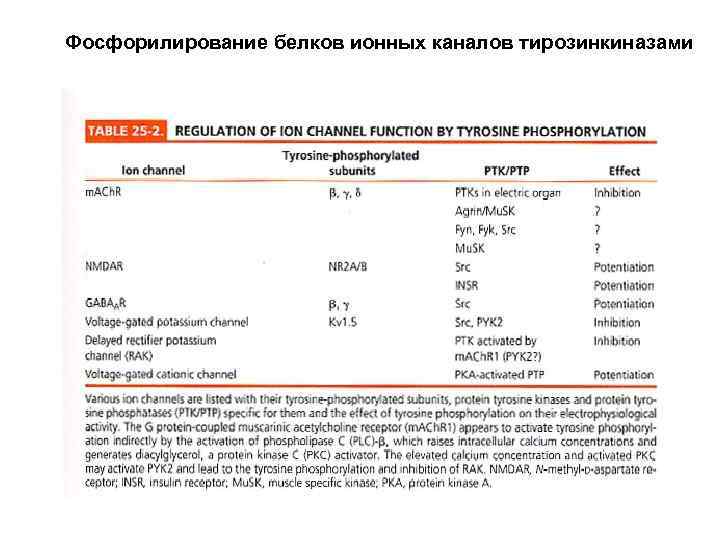
Фосфорилирование белков ионных каналов тирозинкиназами
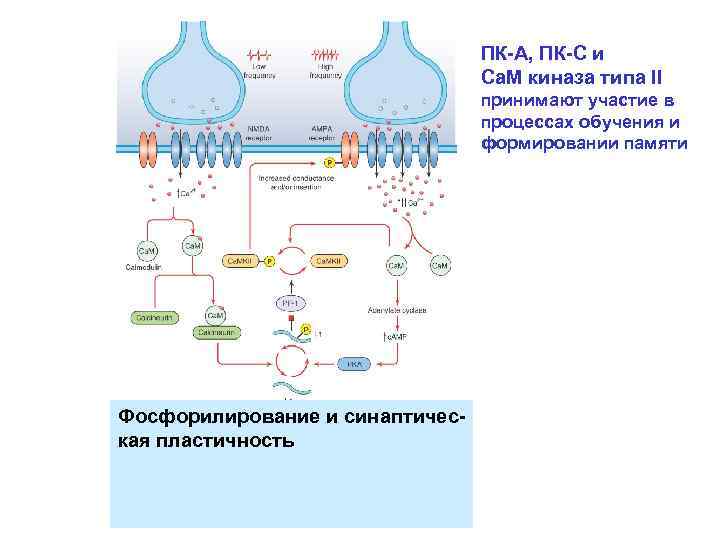
ПК-А, ПК-С и Са. М киназа типа II принимают участие в процессах обучения и формировании памяти Фосфорилирование и синаптическая пластичность
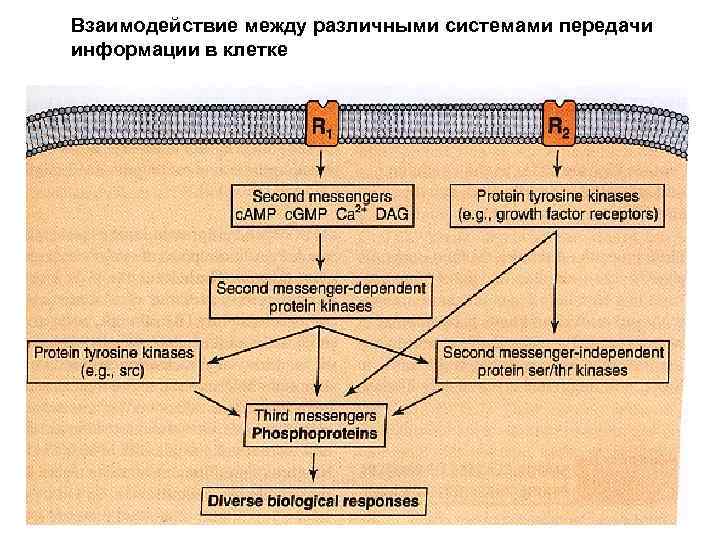
Взаимодействие между различными системами передачи информации в клетке
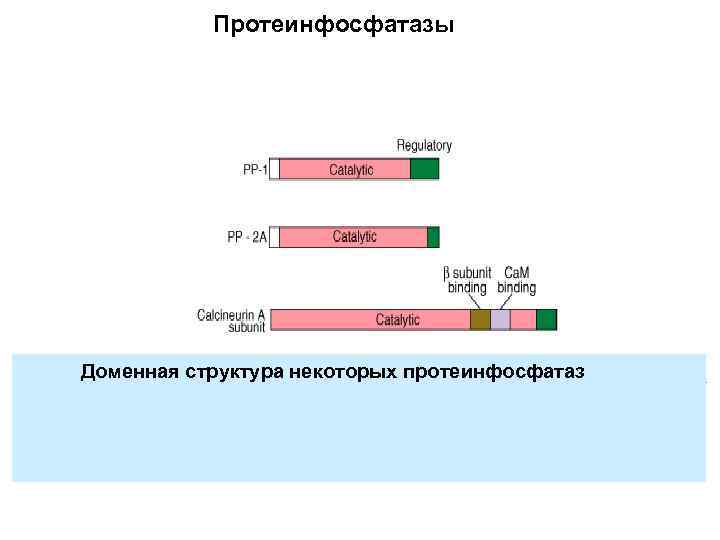
Протеинфосфатазы Доменная структура некоторых протеинфосфатаз
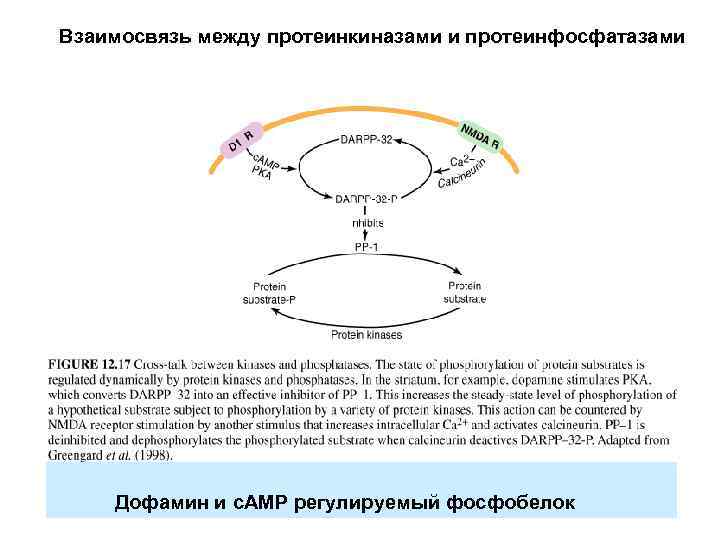
Взаимосвязь между протеинкиназами и протеинфосфатазами Дофамин и с. АМР регулируемый фосфобелок
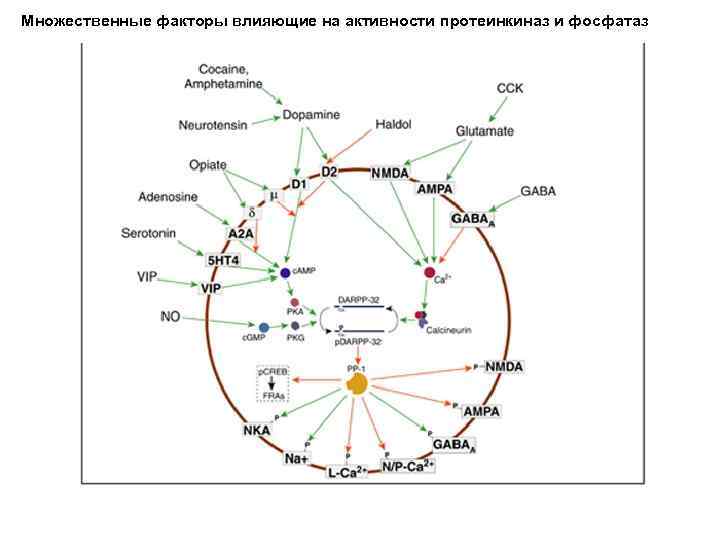
Множественные факторы влияющие на активности протеинкиназ и фосфатаз
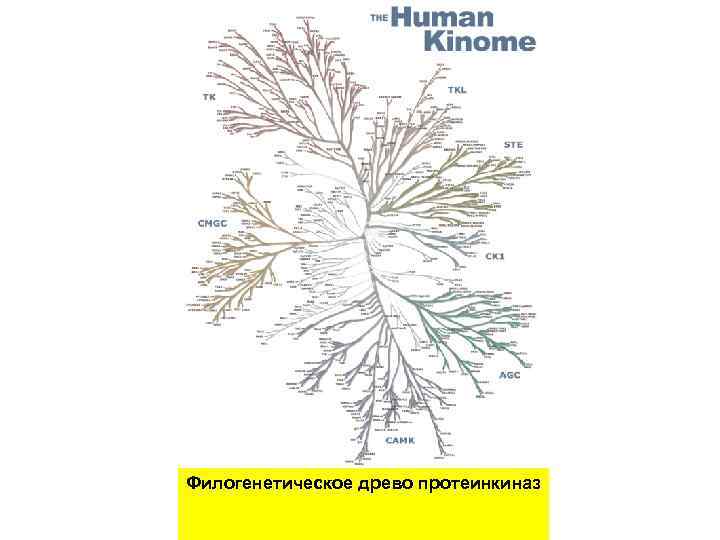
Филогенетическое древо протеинкиназ

От активации рецепторов, генерации вторичных мессенджеров и фосфорилирования белков к регуляции экспрессии генов
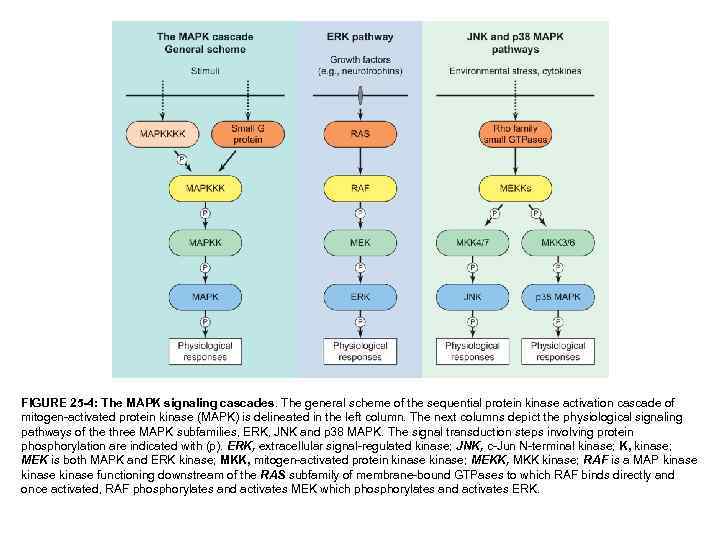
FIGURE 25 -4: The MAPK signaling cascades. The general scheme of the sequential protein kinase activation cascade of mitogen-activated protein kinase (MAPK) is delineated in the left column. The next columns depict the physiological signaling pathways of the three MAPK subfamilies, ERK, JNK and p 38 MAPK. The signal transduction steps involving protein phosphorylation are indicated with (p). ERK, extracellular signal-regulated kinase; JNK, c-Jun N-terminal kinase; K, kinase; MEK is both MAPK and ERK kinase; MKK, mitogen-activated protein kinase; MEKK, MKK kinase; RAF is a MAP kinase functioning downstream of the RAS subfamily of membrane-bound GTPases to which RAF binds directly and once activated, RAF phosphorylates and activates MEK which phosphorylates and activates ERK.

TABLE 25 -4: Hereditary Neuronal Disorders Caused by Mutations in Genes of Protein Kinases and Phosphatases Copyright © 2012, American Society for Neurochemistry. Published by Elsevier Inc. All rights reserved.
05bioch-1711-2014-сигнализация.ppt