12-1bioch-2212-2014-болезниЦНС.ppt
- Количество слайдов: 52

Молекулярная нейробиология Лекция 12. Болезни нервной системы. Нейродегенеративные болезни. Проблемы клеточной терапии. И. А. Гривенников Институт молекулярной генетики РАН

В нервной системе человека эспрессируется до 30000 генов. Это намного больше чем в других органах. Нарушения в работе этих генов, включая соответствующие мутации, приводят в итоге к развитию подавляющего количества заболеваний у человека. (причем развитие большинства заболеваний обусловлены нарушением в работе не одного, а нескольких генов).

Среди заболеваний нервной системы можно в качестве примеров отметить следующие: - Нейродегенеративные заболевания, - Нейропатии - Заболевания, связанные с миелином - Инсульты (ишемический, гемморагический) - Заболевания связанные с мышечной возбудимостью (миастения) - Энцефалопатии (связаны с недостатком кмслорода, глюкозы, витаминов и зависят от состояния работы других органов) - Заболевания связанные с обменом аминокислот (пример: фенилкетонурия) - Заболевания связанные с обменом углеводов, жиров, митохондриальными дисфункциями (мутации в генах обмена, либо доминантные, либо рецессивные) - Эпилепсия, - Шизофрения, - Алкоголизм, наркомании, табакокурение

Актуальность проблемы, связанной с нейродегенерацией в ЦНС 1. Нарастание в мировом масштабе количества заболеваний, связанных с гибелью нейронов в ЦНС (инсульты, нейродегенеративные заболевания). - Болезнь Альцгеймера (более 10 млн. больных) Инсульты (более 10 млн. случаев в год ) Болезнь Паркинсона (около 10 млн. больных) 2. Отсутствие эффективных лекарственных препаратов – нейропротекторов ( в частности, среди регуляторных пептидов), способных предотвращать гибель нервных клеток. Нейродегенеративные болезни могут быть врожденными (наследуемыми) и приобретенными (спорадическими)

Врожденные заболевания нервной системы связаны с нарушениями в работе определенных генов Нарушения в работе связаны с мутациями в генах 1. Точечные мутации (замена одного нуклеотида на другой) Например: «горячие точки» мутаций встречаются в последовательности Cp. G , где при метилировании или деаминировании нуклеотидов может происходить переход С в Т и G в А. Появление мутаций связано также с работой ряда ДНК- полимераз. 2. Инсерции, делеции, дупликации. Приводят к сдвигу рамки считывания и нарушению либо трансляции, либо к нарушению структуры и активности белковых молекул. 3. Экспансия (распространение) тринуклеотидных повторов в ряде генов. CAG - глутамин, CGG - аргинин GCC - аланин CUG - лейцин GAA – глутаминовая кислота
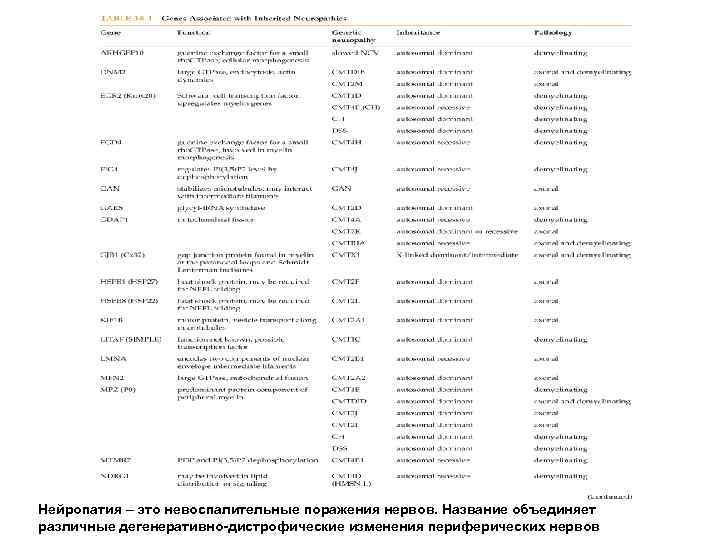
Нейропатия – это невоспалительные поражения нервов. Название объединяет различные дегенеративно-дистрофические изменения периферических нервов
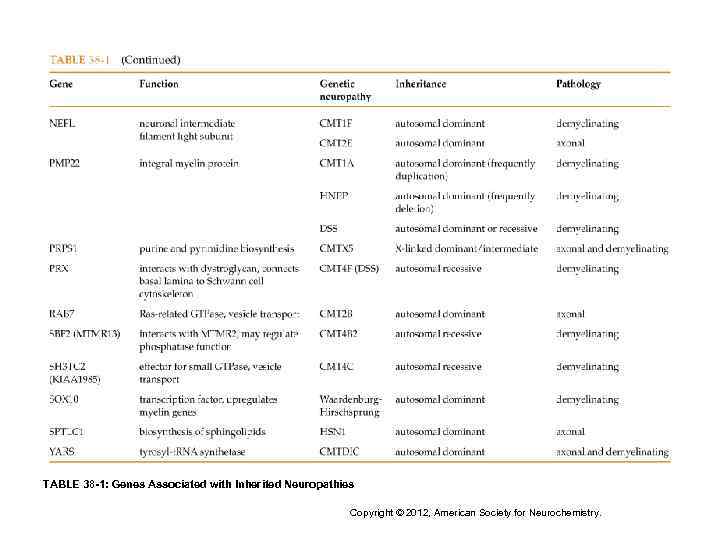
TABLE 38 -1: Genes Associated with Inherited Neuropathies Copyright © 2012, American Society for Neurochemistry.

Некоторые подходы к коррекции нейродегенеративных заболеваний 1. Клеточная трансплантация, в частности генетически модифицированных клеток, включая стволовые. 2. Введение экзогенных нейротрофинов и генетических векторов, их кодирующих в ЦНС. 3. Стимуляция уровня нейротрофинов в мозге с помощью коротких пептидов и их аналогов, а также других соединений. 4. Применение терапевтических препаратов, влияющих на метаболизм нервных клеток и предотвращающих их гибель.

Болезнь Паркинсона Гистопатология. Характеризуется прогрессивной гибелью дофаминергических нейронов в определенных отделах мозга (черная субстанция, хвостатое ядро, стриатум). В живых нейронах наблюдаются характерные включения (нерастворимые белковые агрегаты) – тельца Леви. Клиническая картина. Нарушение двигательной активности, координации. Ригидность, тремор. На поздних стадиях расстройства памяти. Две основные формы заболевания: Спорадическая Врожденная (наследственная) Распространенность 1, 8 : 1000 в общей популяции 1, 0 : 100 в популяции тех, кому за 70 1, 0 : 50 в популяции тех, кому за 80
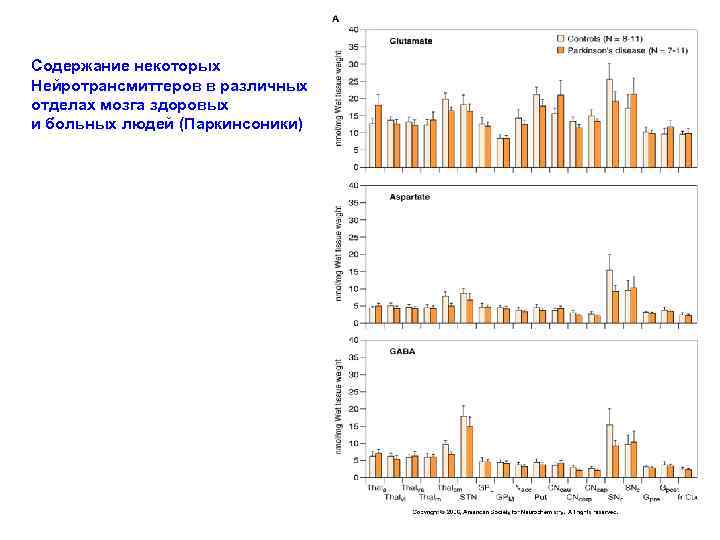
Содержание некоторых Нейротрансмиттеров в различных отделах мозга здоровых и больных людей (Паркинсоники)
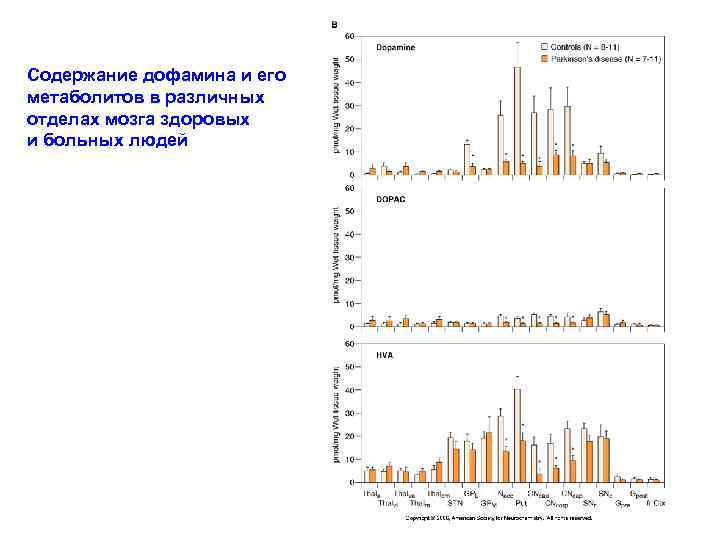
Содержание дофамина и его метаболитов в различных отделах мозга здоровых и больных людей

Copyright © 2012, American Society for Neurochemistry. Published by Elsevier Inc. All rights reserved.
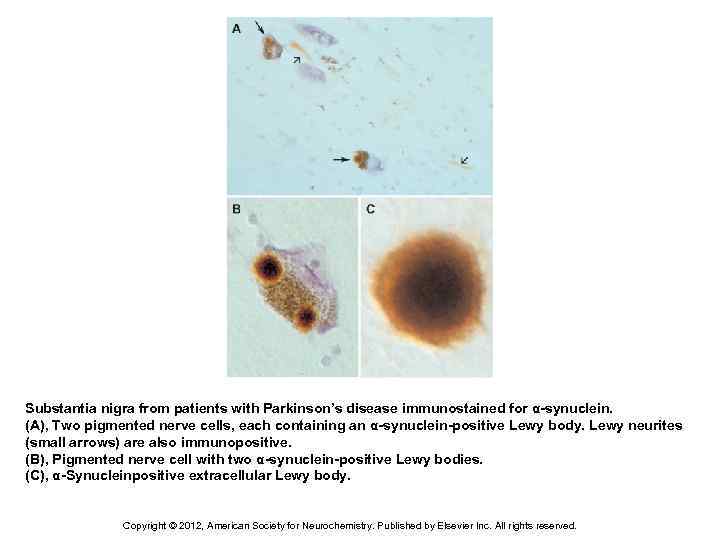
Substantia nigra from patients with Parkinson’s disease immunostained for α-synuclein. (A), Two pigmented nerve cells, each containing an α-synuclein-positive Lewy body. Lewy neurites (small arrows) are also immunopositive. (B), Pigmented nerve cell with two α-synuclein-positive Lewy bodies. (C), α-Synucleinpositive extracellular Lewy body. Copyright © 2012, American Society for Neurochemistry. Published by Elsevier Inc. All rights reserved.
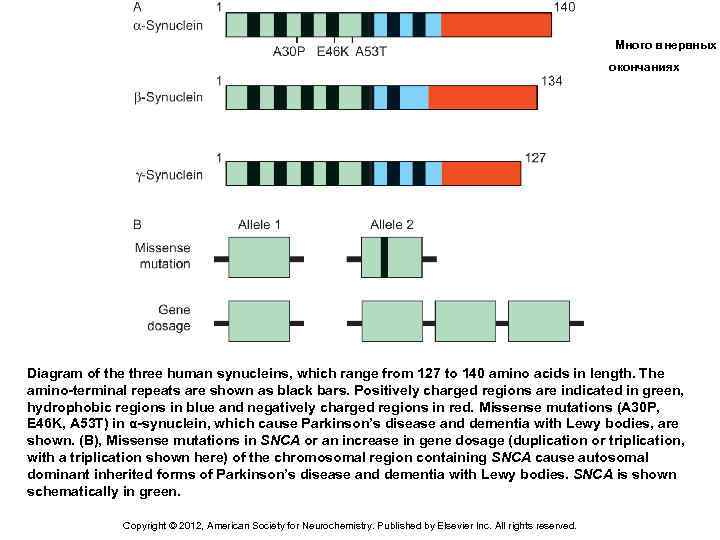
Много в нервных окончаниях Diagram of the three human synucleins, which range from 127 to 140 amino acids in length. The amino-terminal repeats are shown as black bars. Positively charged regions are indicated in green, hydrophobic regions in blue and negatively charged regions in red. Missense mutations (A 30 P, E 46 K, A 53 T) in α-synuclein, which cause Parkinson’s disease and dementia with Lewy bodies, are shown. (B), Missense mutations in SNCA or an increase in gene dosage (duplication or triplication, with a triplication shown here) of the chromosomal region containing SNCA cause autosomal dominant inherited forms of Parkinson’s disease and dementia with Lewy bodies. SNCA is shown schematically in green. Copyright © 2012, American Society for Neurochemistry. Published by Elsevier Inc. All rights reserved.
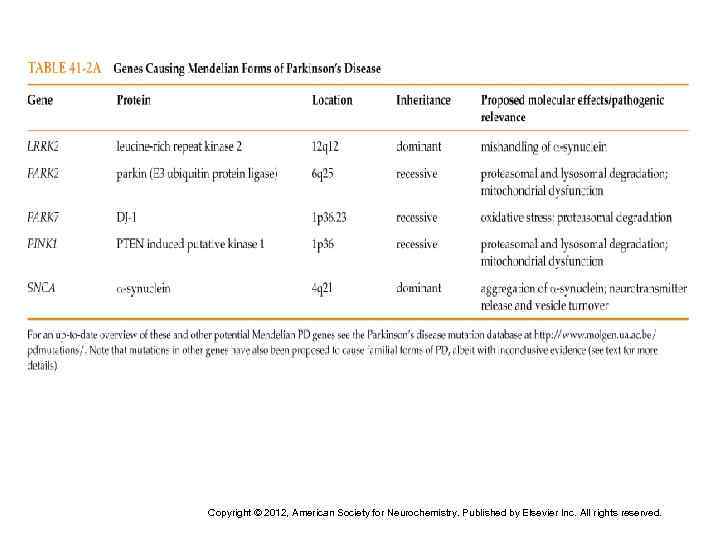
Copyright © 2012, American Society for Neurochemistry. Published by Elsevier Inc. All rights reserved.
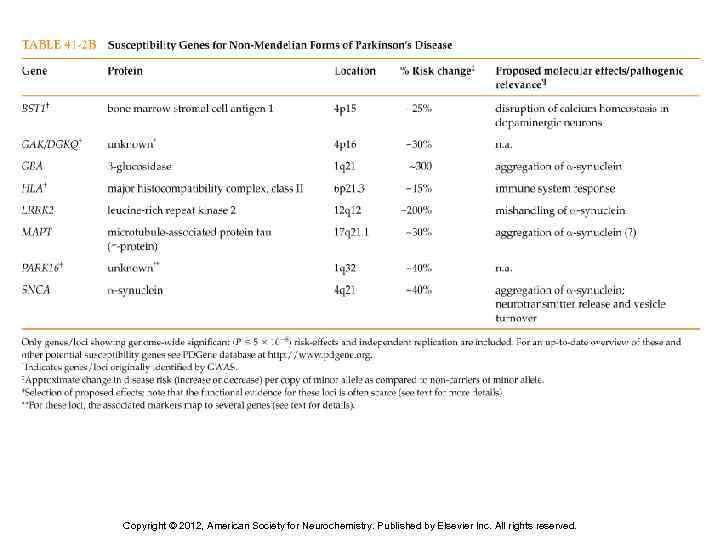
Copyright © 2012, American Society for Neurochemistry. Published by Elsevier Inc. All rights reserved.

Основная проблема возникающая при исследовании различных нейрологических заболеваний, включая нейродегенеративные невозможность проведения экспериментов на мозге человека (in vivo) Модели для исследования этого заболевания: - на животных можно создать с применением 6 -гидроксидофамина и МРТР (метилфенил-тетрагидропиридин) - на культурах нервных клеток из различных источников (мозг грызунов) можно создать с применением 6 -гидроксидофамина и МРТР (метилфенил-тетрагидропиридин) Подходы к лечению: Предшественники дофамина Нейротрофические факторы Генная терапия Клеточная терапия
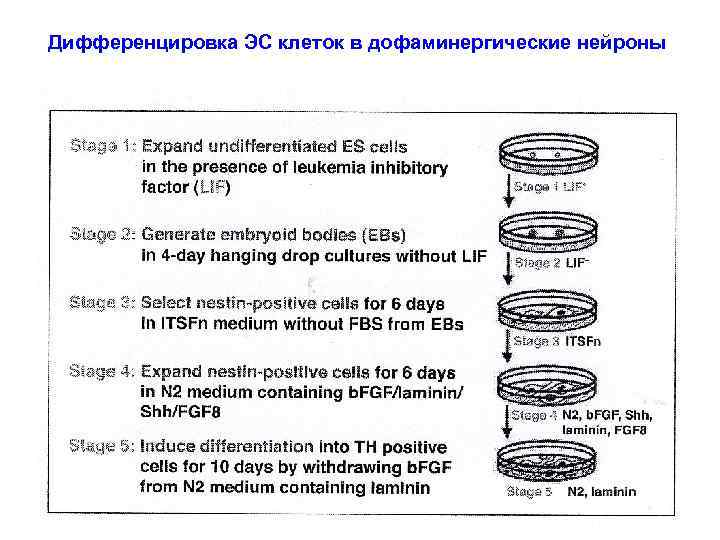
Дифференцировка ЭС клеток в дофаминергические нейроны
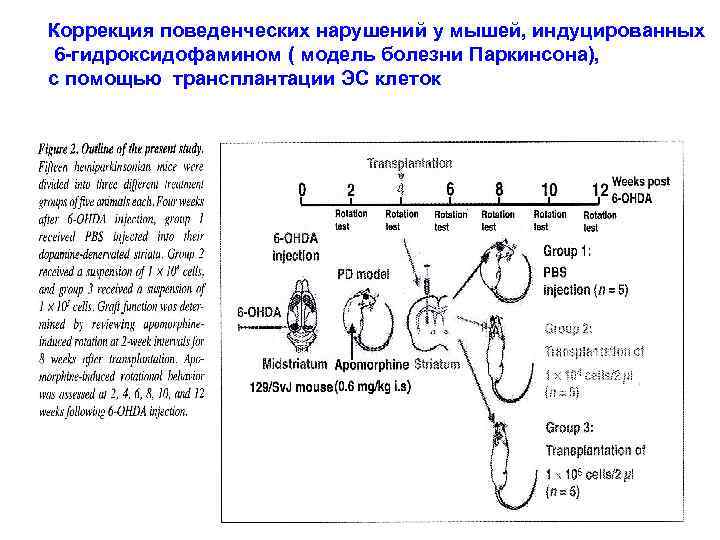
Коррекция поведенческих нарушений у мышей, индуцированных 6 -гидроксидофамином ( модель болезни Паркинсона), с помощью трансплантации ЭС клеток

Болезнь Альцгеймера (старческое слабоумие) Клиническая картина. Характеризуется расстройствами и полной потерей памяти. Гистопатология. Сопровождается гибелью в основном холинергических нейронов в различных отделах мозга (в основном в базальных ядрах переднего мозга и коре). Наблюдается отложение бляшек бета-амилоида и нейрофибриллярные клубки Распространенность 2 -4: 1000 в популяции
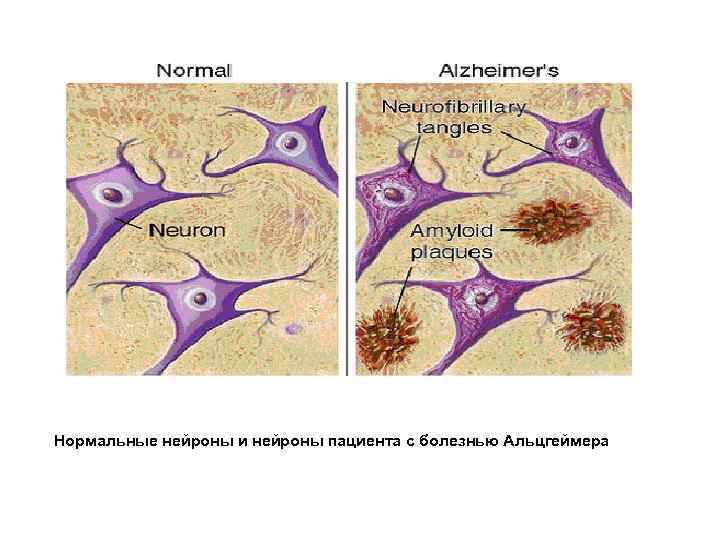
Нормальные нейроны и нейроны пациента с болезнью Альцгеймера
Развитие ранней формы болезни Альцгеймера (БА) (до 5% всех случаев БА) начинается в районе 40 лет и сопровождается мутациями в генах бета-амилоида с накоплением патогенной формы бета. А-42 и пресенилинов 1 и 2, которые представляют собой гамму-секретазу. Нормальная форма- бета. А-40. Основные мутации в гене бета-амилоида расположены около участка его процессинга (экзоны 16 и 17) Функция бета амилоида пока до конца не ясна, но Предполагается, что присутствие бета-амилоида является триггером повышения уровней одного из сигнальных белков, известного как centaurin-alpha 1 (Cent. A 1), который, по-видимому, и вызывает дисфункцию нейронов. Кроме того бета-амилиод участвует в процессах транспорта в нервных окончаниях.
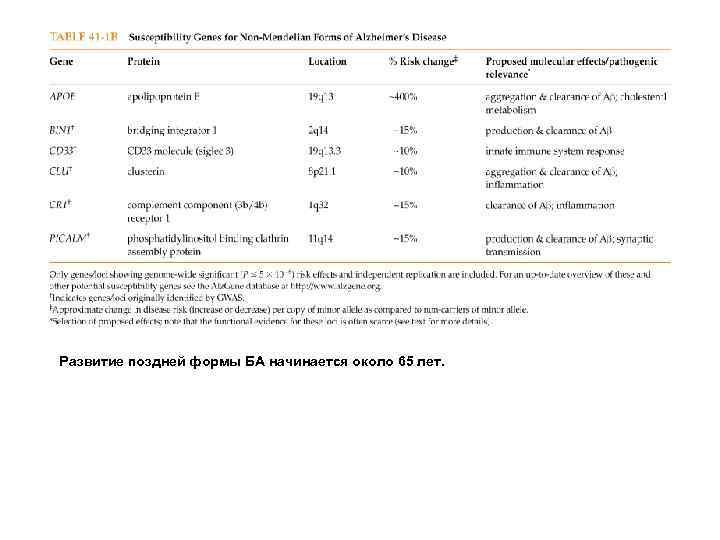
Развитие поздней формы БА начинается около 65 лет.

Две группы заболеваний, связанных с экспансией тринуклеотидных повторов: - Очень длинные повторы (сотни и тысячи). Такие м. РНК не способны транслироваться и давать белковые продукты. (миоклоническая дистрофия, атаксия Фрейдриха) - Среднее число повторов (40 -150). Происходит образование белковых продуктов с нарушенными функциями. (спинномозжечковая атрофия, болезнь Гентингтона). Важно отметить, что развитие ряда заболеваний (нейродегенеративных) происходит в среднем и старшем возрасте, зависит от типа клеток (ергичности нейронов) и их локализации

Хорея Гентингтона Нарушения в движениях и памяти Нарушение экспрессии гена гентингтина, связанная с экспансией триплетов CAG (глутамин) Болезнь (хорея) Гентингтона вызывается экспансией CAG триплетов в гене IT-15 (развитие заболевания начинается когда количество CAG триплетов в данном гене превышиет 35) Начало заболевания обычно после 35 -40 лет. Тяжесть протекания коррелирует с количеством глутаминовых повторов. Распространенность 1 -2 : 100000 в общей популяции

Клеточная терапия -Трансплантация клеток эмбрионального мозга человека -Трансплантация дифференцированных ЭС, ИПС и СТ клеток -Трансплантация генетически модифицированных клеток, синтезирующих нейротрофические факторы
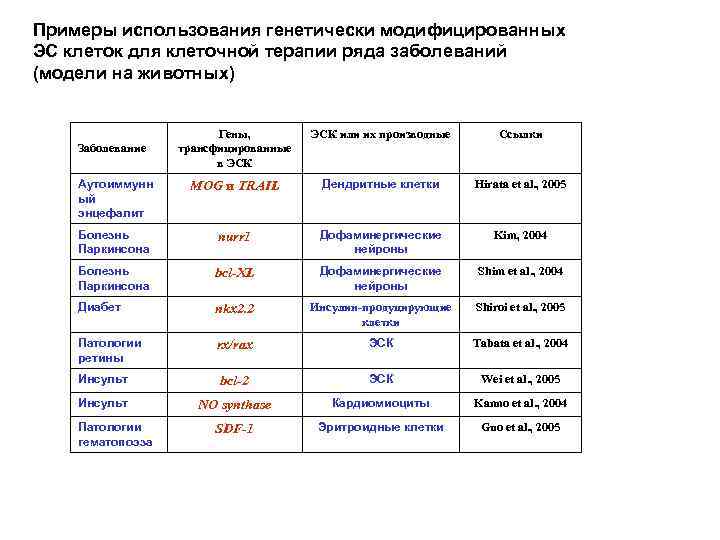
Примеры использования генетически модифицированных ЭС клеток для клеточной терапии ряда заболеваний (модели на животных) Гены, трансфицированные в ЭСК или их производные Ссылки Аутоиммунн ый энцефалит MOG и TRAIL Дендритные клетки Hirata et al. , 2005 Болезнь Паркинсона nurr 1 Дофаминергические нейроны Kim, 2004 Болезнь Паркинсона bcl-XL Дофаминергические нейроны Shim et al. , 2004 Диабет nkx 2. 2 Инсулин-продуцирующие клетки Shiroi et al. , 2005 Патологии ретины rx/rax ЭСК Tabata et al. , 2004 Инсульт bcl-2 ЭСК Wei et al. , 2005 Инсульт NO synthase Кардиомиоциты Kanno et al. , 2004 SDF-1 Эритроидные клетки Guo et al. , 2005 Заболевание Патологии гематопоэза

Возможные пути применения индуцированных плюрипотентных стволовых клеток человека в исследованиях патологий нервной системы 1. Создание клеточных моделей заболеваний человека 2. Тестирование потенциальных лекарственных препаратов 3. Индивидуальная клеточная терапия различных тяжелых заболеваний человека
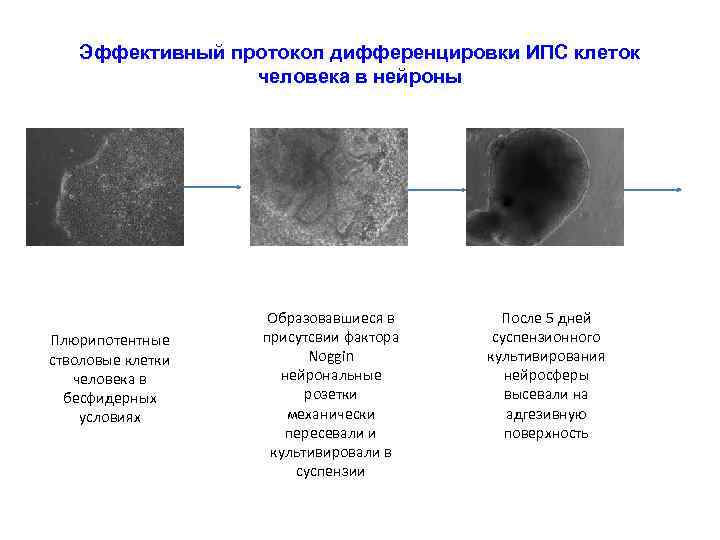
Эффективный протокол дифференцировки ИПС клеток человека в нейроны Плюрипотентные стволовые клетки человека в бесфидерных условиях Образовавшиеся в присутсвии фактора Noggin нейрональные розетки механически пересевали и культивировали в суспензии После 5 дней суспензионного культивирования нейросферы высевали на адгезивную поверхность
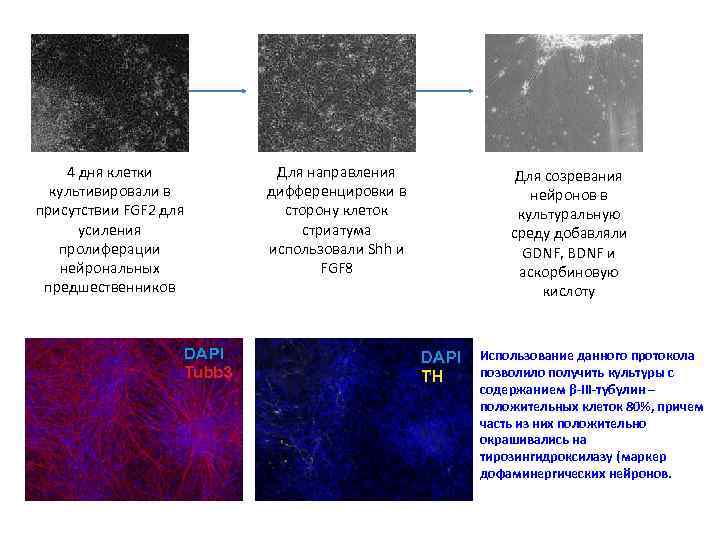
4 дня клетки культивировали в присутствии FGF 2 для усиления пролиферации нейрональных предшественников Для направления дифференцировки в сторону клеток стриатума использовали Shh и FGF 8 Для созревания нейронов в культуральную среду добавляли GDNF, BDNF и аскорбиновую кислоту Использование данного протокола позволило получить культуры с содержанием β-III-тубулин – положительных клеток 80%, причем часть из них положительно окрашивались на тирозингидроксилазу (маркер дофаминергических нейронов.

Примеры применения ИПС клеток человека в неврологии Получены ИПС клетки от больных Familian dysautonomia (нейропатия), из них получили разные нервные предшественники, и показали, что болезнь связана с тканеспецифичным неправильным сплайсингом гена IKBKAP. Studer et al. , (2009)

Некоторые примеры использования ИПС клеток в неврологии ИПС клетки при инъекции в поврежденную часть кортекса крыс c закупоркой центральной мозговой артерии (МСАО) уменьшают зону инфаркта, восстанавливают моторные функции после ишемического удара. (Li HY, Chiou SH. (2010) ИПС клетки при инъекции в поврежденную часть спинного мозга мышей восстанавливают двигательную активность (Okano (2009) ИПС клетки при инъекции в мозг животных с «болезнью Паркинсона» улучшали нарушенные функции (Wernig et al. (2008) ИПС клетки при лечении мозжечковых атаксий улучшают cостояние животных. (Erceg et al. (2011)

Моделирование болезни Паркинсона с использованием ИПС клеток Получены линии ИПС клеток несущих: - G 2019 S мутацию в гене leucine-rich repeat kinase 2 (LRRK 2) - Триплицикацию гена, кодирующего α-synuclein (синуклеин) - мутации в гене Паркина 2 (Е 3 -убиквитин лигаза) Полученные из таких клеток дофаминергические нейроны показывали более высокую чувствительность к окислительному стрессу (перекись водорода), к действию 6 -гидроксидофамина, а также к активации каспазы-3 по сравнению с контрольными (здоровыми) клетками. Полученные линии клетки являются эффективной моделью для диагностики заболеваний и тестирования фармакологических агентов. Blake Byers, (2012)
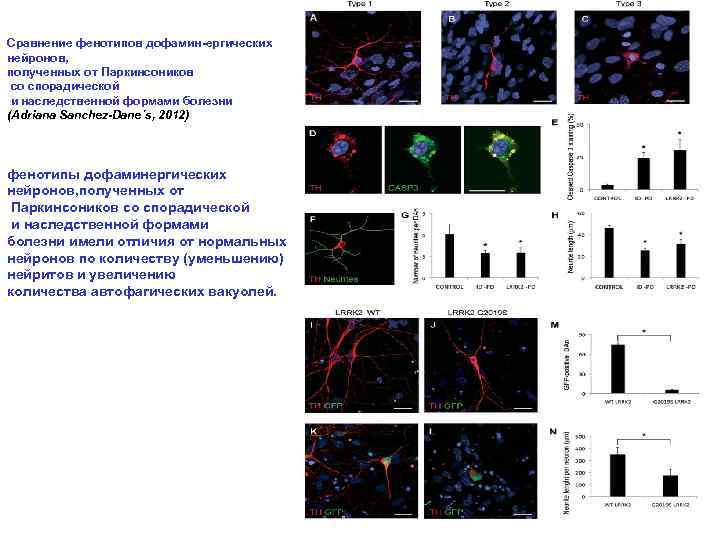
Сравнение фенотипов дофамин-ергических нейронов, полученных от Паркинсоников со спорадической и наследственной формами болезни (Adriana Sanchez-Dane´s, 2012) фенотипы дофаминергических нейронов, полученных от Паркинсоников со спорадической и наследственной формами болезни имели отличия от нормальных нейронов по количеству (уменьшению) нейритов и увеличению количества автофагических вакуолей.

Описание к предыдущей картинке Figure 4. Morphological alterations of PD-i. PSC-derived DA neurons after long-term culture. A-C. Immunofluorescence analyses of Ctrl-i. PSC (cell line SP 11. 1, A), ID-PD i. PSC (cell line SP 08. 1, B) and LRRK 2 -PD i. PSC (cell line SP 06. 2, C), differentiated towards DA neurons and cultured for 75 days on cortical astrocytes, stained for TH (red). Images are representative of the three morphologies of DA neurons found under these conditions. D. Immunofluorescence analysis of DA neurons differentiated from LRRK 2 -PD i. PSC (cell line SP 06. 2) for 75 days, co-stained for TH (red) and cleaved caspase-3 (green). In A–D nuclei are counterstained with DAPI, shown in blue. Scale bar, 12. 5 mm. E. Quantitative analyses of the percentage of DA neurons differentiated for 75 days showing cleaved caspase-3 staining. Data for CONTROL is the average of 4 i. PSC lines, for ID-PD from 7 i. PSC lines and LRRK 2 -PD from 4 i. PSC. Asterisks denote statistically significant differences between CONTROL and ID-PD ( pј 0. 004) or LRRK 2 -PD ( pј 0. 011) [F(2, 12)ј 5. 668; pј 0. 018]. F. Image of the same DA neuron shown in (A), with neurites outlined by green traces as processed by NIH Image. J software. G. Quantitative analyses of the number of neurites in DAn differentiated for 75 days. Data for CONTROL is the average of 87 DAn from 4 i. PSC lines, for ID-PD is from 119 DAn from 7 i. PSC lines and for LRRK 2 -PD is from 91 DAn from 4 i. PSC. Asterisks denote statistically significant differences between CONTROL and IDPD ( p<0. 001) or LRRK 2 -PD (p<0. 001) [F(2, 294)ј 21. 096; p<0. 001]. H. Quantitative analyses of the neurite length in DA neurons differentiated for 75 days. Data for CONTROL is the average of 540 neurites from 4 i. PSC lines, for ID-PD is from 409 neurites from 7 i. PSC lines and for LRRK 2 -PD is from 303 neurites from 4 i. PSC. Asterisks denote statistically significant differences between CONTROL and ID-PD ( p<0. 001) or LRRK 2 -PD (p<0. 001) [F(2, 1249)ј 42. 161; p<0. 001]. (E, G and H) bars represent average with SEM as error bars. I-L. DAn (TH positive, red) and GFP (green) from Ctrl-i. PSC (SP 11. 1) co-transfected with plasmids encoding WT LRRK 2 (WT, I and K) or mutant LRRK 2 G 2019 S (J and L) and GFP. (I and J) Images showing GFP negative DA neurons. (K and L) Co-transfected DA neurons being GFP positive. Nuclei are counterstained with DAPI, shown in blue. Scale bar, 12. 5 mm. M. Quantitative analysis of the number of GFP positive neurons present in co-transfected cells. N. Quantitative analyses of the neurite length per neuron in co-transfected DAn. For (M and N) data are average of two-independent experiments using two different Ctrl-i. PSC lines. Bars represent average with SEM as error bars. Statistically significant differences are indicated with asterisks ( pј 0. 003 in M; pј 0. 006 in N). ~

Induced Pluripotent Stem Cells from Patients with Huntington’s Disease Show CAG-Repeat-Expansion-Associated Phenotypes The HD i. PSC Consortium (Cell Stem Cell, 2012) SUMMARY Huntington’s disease (HD) is an inherited neurodegenerative disorder caused by an expanded stretch of CAG trinucleotide repeats that results in neuronal dysfunction and death. Here, The HD Consortium reports the generation and characterization of 14 induced pluripotent stem cell (i. PSC) lines from HDpatients and controls. Microarray profiling revealed CAG-repeat-expansion-associated gene expression patterns that distinguish patient lines from controls, and early onset versus late onset HD. Differentiated HD neural cells showed disease-associated changes in electrophysiology, metabolism, cell adhesion, and ultimately cell death for lines with both medium and longer CAG repeat expansions. The longer repeat lines were however the most vulnerable to cellular stressors and BDNF withdrawal, as assessed using а range of assays across consortium laboratories. The HD i. PSC collection represents a unique and well-characterized resource to elucidate disease mechanisms in HD and provides a human stem cell platform for screening new candidate therapeutics.
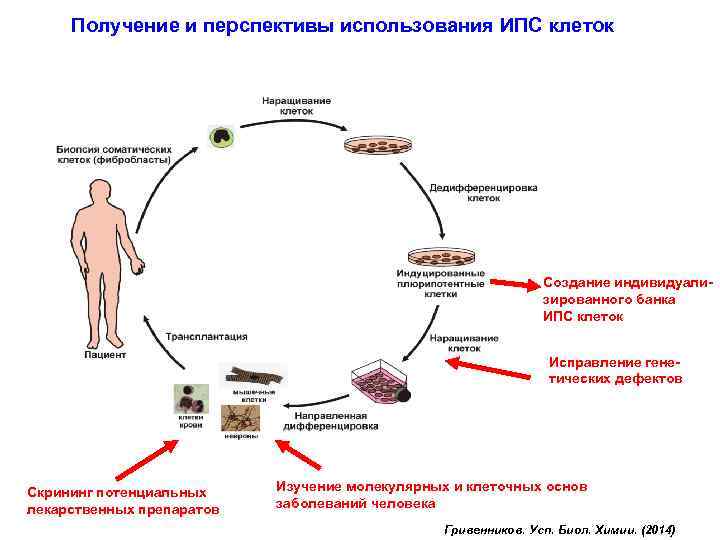
Получение и перспективы использования ИПС клеток Создание индивидуализированного банка ИПС клеток Исправление генетических дефектов Скрининг потенциальных лекарственных препаратов Изучение молекулярных и клеточных основ заболеваний человека Гривенников. Усп. Биол. Химии. (2014)

Проблемы возникающие при использовании ИПС клеток для клеточной терапии нейрологических заболеваний Злокачественное перерождение пересаженных клеток Жизнеспособность пересаженных клеток Правильное встраивание в определенных участках мозга Дифференцировка и установление правильных контактов Функциональная активность трансплантированных клеток
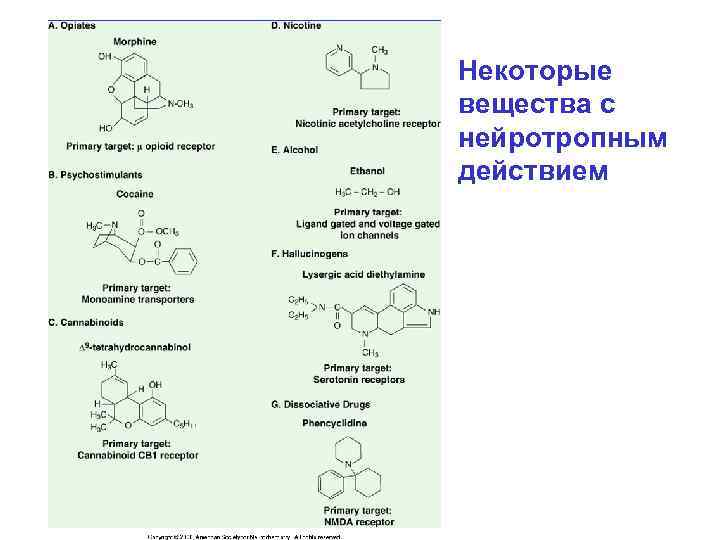
Некоторые вещества с нейротропным действием

Алкоголизм (от 8 до 10% населения в Российской и Американской популяциях) Алкоголь (этанол) – способен действовать на мембрану клеток, изменяя состояние ионных каналов в частности глутаматных рецепторов и др. мембранных белков В клетке этанол превращается в ацетальдегид ферментом алкогольдегидрогеназой и далее в ацетат ферментом ацетальдегидрогеназой

Ацетальдегид является основным источником «неприятных ощущений» при действии на мозгтак называемого «похмельного синдрома» Являясь, как и многие другие альдегиды, химически активной молекулой ацетальдегид способен реагировать с молекулами белков, аминокислот и др. соединений, в частности нейротрансмиттерами.

Pilot Study of i. PS-Derived Neural Cells to Examine Biologic Effects of Alcohol on Human Neurons In Vitro Richard Lieberman, Eric S. Levine, Henry R. Kranzler, Christine Abreu, and Jonathan Covault (2012) Background: Studies of the effects of alcohol on N-methyl-D-aspartate (NMDA) receptor function and gene expression have depended on rodent or postmortem human brain models. Ideally, the effects of alcohol might better be examined in living neural tissue derived from human subjects. In this study, we used new technologies to reprogram human subject-specific tissue into pluripotent cell colonies and generate human neural cultures as a model system to examine the molecular actions of alcohol. Methods: Induced pluripotent stem (i. PS) cells were generated from skin biopsies taken from 7 individuals, 4 alcohol-dependent subjects, and 3 social drinkers. We differentiated the i. PS cells into neural cultures and characterized them by immunocytochemistry using antibodies for the neuronal marker beta-III tubulin, glial marker s 100 b, and synaptic marker synpasin-1. Electrophysiology was performed to characterize the i. PS-derived neurons and to measure the effects of acute alcohol exposure on the NMDAreceptor response in chronically alcohol exposed and nonexposed neural cultures from 1 nonalcoholic. Finally, we examined changes in m. RNA expression of the NMDA receptor subunit genes GRIN 1, GRIN 2 A, GRIN 2 B, and GRIN 2 D after 7 days of alcohol exposure and after 24 -hour withdrawal from chronic alcohol exposure. Results: Immunocytochemistry revealed positive staining for neuronal, glial, and synaptic markers. i. PS-derived neurons displayed spontaneous electrical properties and functional ionotropic receptors. Acute alcohol exposure significantly attenuated the NMDA response, an effect that was not observed after 7 days of chronic alcohol exposure. After 7 days of chronic alcohol exposure, there were significant increases in m. RNA expression of GRIN 1, GRIN 2 A, and GRIN 2 D in cultures derived from alcoholic subjects but not in cultures derived from nonalcoholics. Conclusions: These findings support the potential utility of human i. PS-derived neural cultures as in vitro models to examine the molecular actions of alcohol on human neural cells.

Наркомании – получение удовлетворения за счет внешнего источника без достижения цели Достижение цели – получение удовлетворения (в ЦНС вещества внутреннего удовлетворения. Опиоиды и нейротензин)

Шизофрения (до 1% больных в человеческой популяции) Изменения (увеличение) в плотности Д 4 рецепторов для дофамина, Уменьшение количеств МАО (форма 3 отсутствует, форма 2 изменена). Ослабление глутаматергической передачи. Лечение: Хирургическое Терапевтическое (антагонисты дофаминовых рецепторов: галоперидол, трициклические нейролептики)
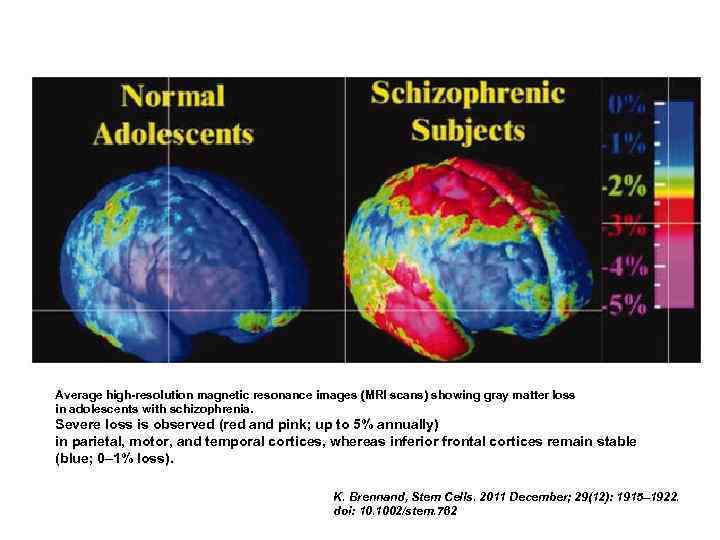
Average high-resolution magnetic resonance images (MRI scans) showing gray matter loss in adolescents with schizophrenia. Severe loss is observed (red and pink; up to 5% annually) in parietal, motor, and temporal cortices, whereas inferior frontal cortices remain stable (blue; 0– 1% loss). K. Brennand, Stem Cells. 2011 December; 29(12): 1915– 1922. doi: 10. 1002/stem. 762
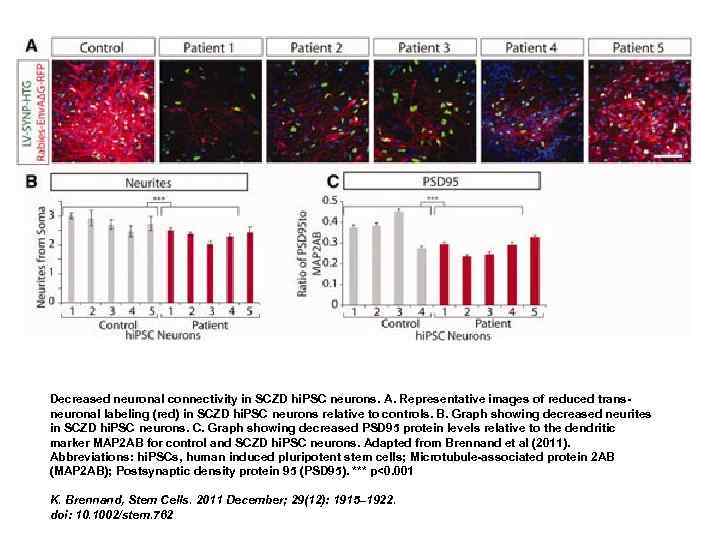
Decreased neuronal connectivity in SCZD hi. PSC neurons. A. Representative images of reduced transneuronal labeling (red) in SCZD hi. PSC neurons relative to controls. B. Graph showing decreased neurites in SCZD hi. PSC neurons. C. Graph showing decreased PSD 95 protein levels relative to the dendritic marker MAP 2 AB for control and SCZD hi. PSC neurons. Adapted from Brennand et al (2011). Abbreviations: hi. PSCs, human induced pluripotent stem cells; Microtubule-associated protein 2 AB (MAP 2 AB); Postsynaptic density protein 95 (PSD 95). *** p<0. 001 K. Brennand, Stem Cells. 2011 December; 29(12): 1915– 1922. doi: 10. 1002/stem. 762

Эпилепсия Важная роль в развитии данной патологии принадлежит глутаматергической системе, также значение имеет нарушение в ГАМКергической системе. Каинат и квискалат (агонисты) индуцируют судорожные состояния. В крови наблюдается повышенный уровень антител к глутаматным рецепторам? ? ? Бартитураты имеют участки связывания на глутаматных рецепторах и ослабляют развитие судорог

Депрессивные состояния Существенные изменения (снижение) в катехоламинергической и серотонинергической системах. В отличие от шизофрении изменения в большей степени касаются норадренергической передачи, а не дофаминергической Отмечается дисбаланс между ГАМК- и глутаматергическими системами мозга Лечение: препараты (имипрамин, прозак и др. ) ингибирующие обратный захват НА и СТ, либо их расщепление под действием МАО

Выводы. Заболевания нервной системы чрезвычайно распространены, В большинстве случаем мало изучены из-за сложности получения материала, Количество этих заболеваний продолжает увеличиваться во всем мире ИПС клетки представляют из себя уникальную модель для исследования различных патологий нервной системы и для поиска эффективных лекарственных препаратов


Программа лекций по молекулярной нейробиологии на осенний семестр 2014 г. для студентов кафедры Биохимии Общая характеристика клеток нервной системы и сигнализации в нейронах. Клетки нервной системы. Нейроны и глия, общая характеристика. Астроциты, олигодендроциты, микроглия. Особенности строения нейрона. Сигнализация в нейронах. Синапсы. Химические и электрические синапсы. Методы и уровни изучения нервной системы. Химические передатчики в синапсах. Непептидные и пептидные нейротрансмиттеры, общая характеристика. Локализация нейротрансмиттеров. Синаптические везикулы. Совместная локализация классических и пептидных нейротрансмиттеров. Тормозные и возбуждающие нейротрансмиттеры. Синтез и распад нейротрансмиттеров. Потенциал и лиганд-зависимые ионные каналы. Натриевые, калиевые и кальциевые каналы. Структура и принцип работы. Роль в передаче нервного импульса. Синаптическая передача. Ацетилхолиновый рецептор нервно-мышечного окончания. Структура и принцип работы. Сравнение ацетилхолинового рецептора нервно-мышечного окончания и мозга. Выброс нейротрансмиттеров в синаптической щели. Судьба нейротрансмиттеров в синаптической щели. Ионотропные и метаботропные рецепторы. Общая схема организации. Глутаматные рецепторы, дофаминовые и серотониновые рецепторы. ГАМК- рецепторы. Опиоидные рецепторы. Меланокортиновые рецепторы. Глициновые рецепторы. Подтипы разных рецепторов. Внутриклеточная сигнализация в нейронах и глиальных клетках. Передачи сигнала от рецепторов на мембране внутрь клетки. ГТФ- связывающие белки. Вторичные мессенджеры (с. АМР, с. ГМР). Синтез и распад вторичных мессенджеров: аденилатциклаза, гуанилатциклаза, фосфодиэстеразы циклических нуклеотидов. Инозитолтрифосфат, диацилглицерол. Оксид азота. Кальций, калмодулин. Система протеинкиназ. Усиление сигнала при передаче информации от рецептора на систему вторичных мессенджеров, протеинкиназ и их субстратов. Некоторые примеры регуляции активности нейроспецифических белков с помощью фосфорилирования (тирозингидроксилаза, рецепторы нейротрансмиттеров, белки, связанные с выбросом нейротрансмиттеров). Система протеинфосфатаз в нервной системе, примеры и характеристика отдельных представителей. Тирозинкиназы и тирозинфосфатазы в клетках нервной системы и их роль в передаче сигнала от факторов роста. Регуляция экспрессии генов в ЦНС. Иерархия регуляции. В нервной системе экспрессируется наибольшее количество генов по сравнению с другими тканями организма. Факторы транскрипции. Индуцибельные и конститутивные факторы транскрипции. Транскрипционный фактор CREB - структура и функции. CREB-зависимые гены. Протоонкогены и их роль в развитии нервной системы и ее функционировании. Рецепторы стероидных гормонов в качестве факторов транскрипции. Нейроспецифические гены.

Цитоскелет нервной клетки. Характеристика основных компонентов цитоскелета. Микротрубочки, промежуточные филаменты, актиновые микрофиламенты. Их сборка и время существования. Транспорт макромолекул в нервной клетке. Медленный и быстрый аксональный ток. Методы его изучения. Молекулярные моторы в быстром аксональном транспорте. Миелин и миелинизация. Происхождение миелина. Структура миелина. Миелин центральной и периферической нервной системы. Клетки, которые образуют миелин в нервной системе. Гены миелина и регуляция их экспрессии. Болезни, связанные с нарушениями в обмене миелина. Нейропептиды и регуляция функций нервной системы. Различные семейства нейропептидов. Их классификация. Образование. Специфичность Краткая характеристика функций различных представителей семейств. Гены нейропептидов, синтез и процессинг нейропептидов. Несколько копий нейропептида в молекуле предшественника (проопиомеланокортин). Опиоидные пептиды. Меланокортины и их рецепторы. Деградация нейропептидов. Лекарства на основе нейропептидов- лекарства нового поколения. Развитие и дифференцировка клеток нервной системы. Рост аксонов. Программируемая смерть клеток в нервной системе. Роль глии в прорастании аксонов. Молекулярный механизм нейронального развития. образования контактов. Развитие и функционирование нервно-мышечных окончаний. Молекулы клеточной адгезии и их характеристика. Нейротрофические факторы, их рецепторы и функции в нервной системе. Жизнь и смерть нейронов. Нейротрофические факторы и их характеристика. Семейство нейротрофинов. Фактор роста нервов, нейротрофический фактор мозга. Специфичность синтеза и действия нейротрофинов в нервной системе. Рецепторы нейротрофических факторов и механизм передачи сигнала в клетку. Регенерация клеток нервной системы, стволовые клетки. Регенерация клеток нервной системы. Возможна ли она? Стволовые клетки нервной системы. Стадии дифференцировки нейронов и клеток глии из клеток- предшественников. Локализация стволовых клеток в мозге млекопитающих. Методы и подходы к их идентификации. Память - основная функция нервной системы. Методы и подходы к ее изучению. Модели изучения памяти. Развитие представлений о формировании памяти. Роль нейротрансмиттеров и нейропептидов в процессах формирования памяти. Кратковременная и долговременная память. Биохимические механизмы формирования памяти. Некоторые патологии, связанные с нарушениями памяти. Примеры и краткая характеристика некоторых распространенных заболеваний нервной системы человека. Молекулярные подходы к изучению некоторых болезней нервной системы. Нейродегенеративные заболевания: Болезни Паркинсона, Альцгеймера, хорея Гентингтона. Эпилепсия и шизофрения. Возможные подходы к коррекции и лечению этих заболеваний. Генотерапия и клеточная терапия. Индуцированные плюрипотентные стволовые клетки и перспективы их использования в неврологии. Вещества с нейротропным действием. Алкоголь. Наркотики, галлюциногены. Возможные механизмы действия. Механизм развития наркотической и алкогольной зависимости.
12-1bioch-2212-2014-болезниЦНС.ppt