Ионные каналы.ppt
- Количество слайдов: 70
 Молекулярная физиология Лекция 2. Ионные каналы
Молекулярная физиология Лекция 2. Ионные каналы
 Содержание лекции • Функциональная классификация ионных каналов • Особенности молекулярной структуры и функционирования различных видов ионных каналов (Na+, Ca 2+, K+зависимых) • Транспорт через ионные каналы мебраны. • Регуляция состояния ионных каналов.
Содержание лекции • Функциональная классификация ионных каналов • Особенности молекулярной структуры и функционирования различных видов ионных каналов (Na+, Ca 2+, K+зависимых) • Транспорт через ионные каналы мебраны. • Регуляция состояния ионных каналов.
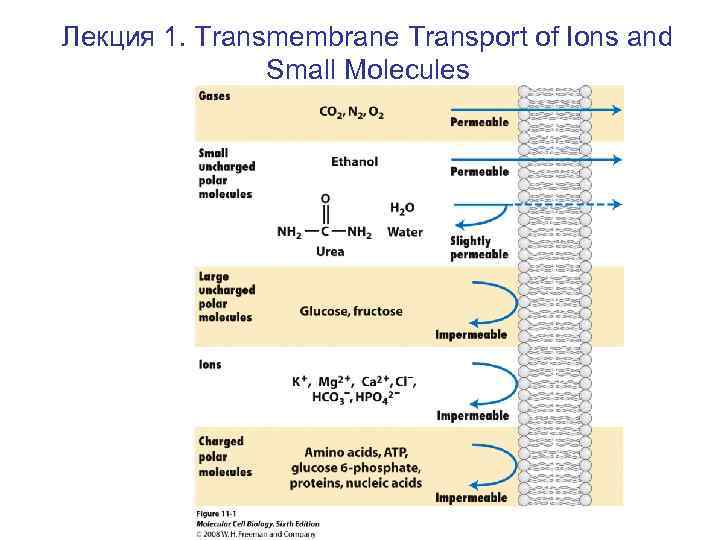 Лекция 1. Transmembrane Transport of Ions and Small Molecules
Лекция 1. Transmembrane Transport of Ions and Small Molecules
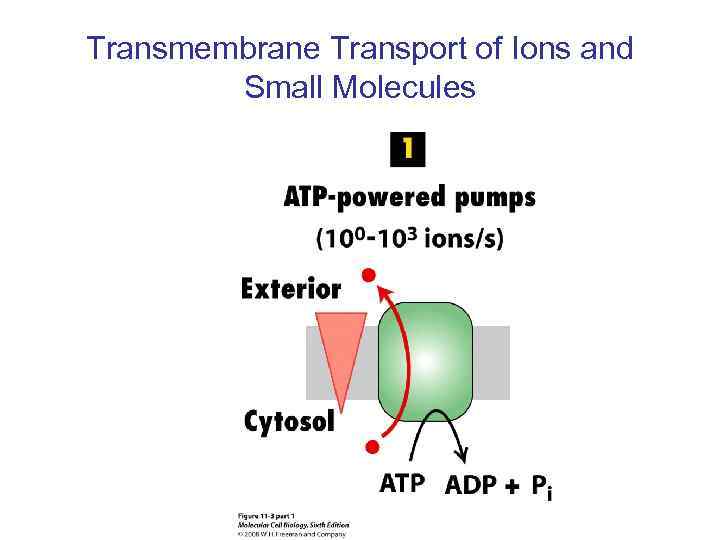 Transmembrane Transport of Ions and Small Molecules
Transmembrane Transport of Ions and Small Molecules
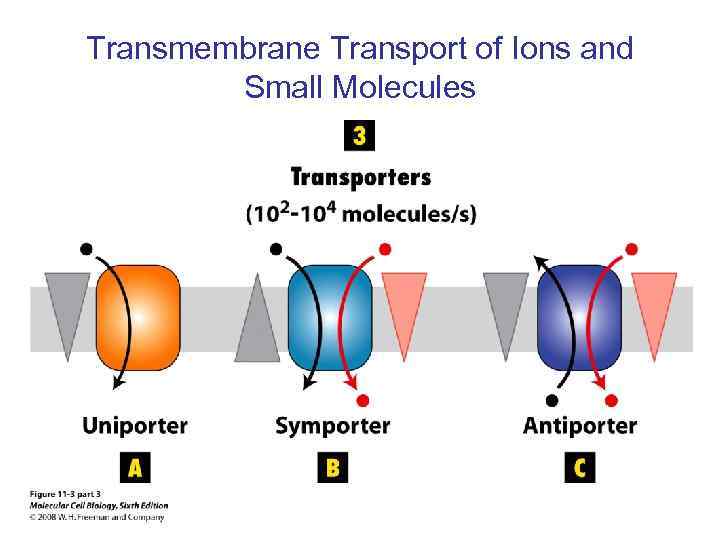 Transmembrane Transport of Ions and Small Molecules
Transmembrane Transport of Ions and Small Molecules
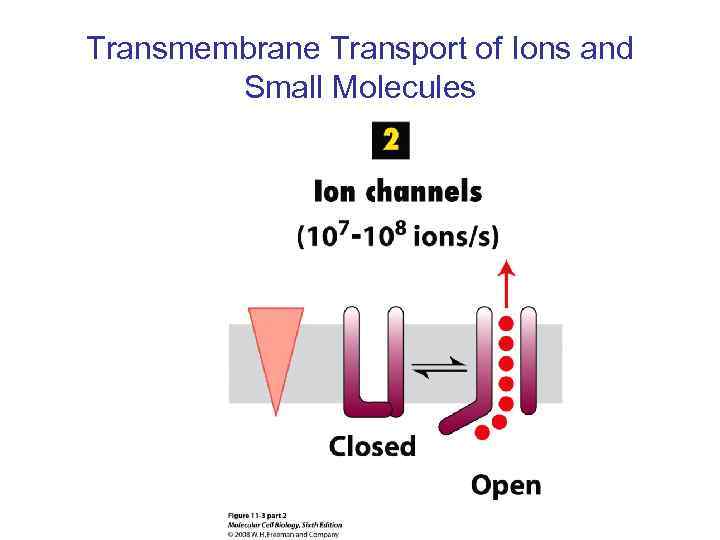 Transmembrane Transport of Ions and Small Molecules
Transmembrane Transport of Ions and Small Molecules
 Методы исследования ионных каналов
Методы исследования ионных каналов
 Методы исследования ионных каналов • • Электрофизиологические методы Регистрация интегральных токов и потенциалов. Внутриклеточная регистрация. Вышеописанные методы внутриклеточной регистрации не позволяют регистрировать ионные токи, текущие через мембрану возбудимой клетки. • Метод фиксации мембранного потенциала. • Измерение токов одиночного канала. пэтч-кламп (patchclamp).
Методы исследования ионных каналов • • Электрофизиологические методы Регистрация интегральных токов и потенциалов. Внутриклеточная регистрация. Вышеописанные методы внутриклеточной регистрации не позволяют регистрировать ионные токи, текущие через мембрану возбудимой клетки. • Метод фиксации мембранного потенциала. • Измерение токов одиночного канала. пэтч-кламп (patchclamp).
 Методы исследования ионных каналов • Биохимические и генетические методы исследования ионных каналов Исследования молекулярной структуры ионных каналов используются биохимические подходы, которые заключаются в выделении каналов из мембран и исследовании выделенных молекул с помощью физических и химических методов • Фармакологические методы связаны с использованием природных и синтетических соединений, модулирующих работу ионных каналов. например, некоторые токсины блокируют ионную проводимость Na-каналов. К ним относят тетродотоксин, содержащийся в яичниках и других органах рыбы фугу, и сакситоксин, синтезирующийся морским планктоном. Другая группа растительных токсинов, к которым относятся вератридин, аконитин и грайянотокин, вызывают постоянную активацию Na-каналов
Методы исследования ионных каналов • Биохимические и генетические методы исследования ионных каналов Исследования молекулярной структуры ионных каналов используются биохимические подходы, которые заключаются в выделении каналов из мембран и исследовании выделенных молекул с помощью физических и химических методов • Фармакологические методы связаны с использованием природных и синтетических соединений, модулирующих работу ионных каналов. например, некоторые токсины блокируют ионную проводимость Na-каналов. К ним относят тетродотоксин, содержащийся в яичниках и других органах рыбы фугу, и сакситоксин, синтезирующийся морским планктоном. Другая группа растительных токсинов, к которым относятся вератридин, аконитин и грайянотокин, вызывают постоянную активацию Na-каналов
 Методы исследования ионных каналов • Ультраструктурные методы. • Для определения локализации, плотности и распределения ионных каналов используются методы электронной микроскопии, иммуноцитохимии, методы флуоресцентной микроскопии, в том числе с использованием моноклональных антител. • Флуоресцентные методы широко применяются и для исследования изменений внутриклеточной концентрации кальция с использованием внутриклеточных кальциевых индикаторов (Van Der Kloot, Molgo, 1994).
Методы исследования ионных каналов • Ультраструктурные методы. • Для определения локализации, плотности и распределения ионных каналов используются методы электронной микроскопии, иммуноцитохимии, методы флуоресцентной микроскопии, в том числе с использованием моноклональных антител. • Флуоресцентные методы широко применяются и для исследования изменений внутриклеточной концентрации кальция с использованием внутриклеточных кальциевых индикаторов (Van Der Kloot, Molgo, 1994).
 Методы исследования ионных каналов • Исследования ионных каналов с помощью потенциалчувствительных красителей. Изменения МП и, следовательно, активность ионных каналов, можно регистрировать с помощью потенциал-чувствительных красителей, спектральные характеристики которых меняются в ответ на изменения потенциала. • Рентгенокристаллографический метод. Использование метода рентгенокристаллографии совместно с биохимическими, генетическими, электрофизиологическими методами позволило выявить принципы структуры и функционирования канальных белков. Рентгенокристаллографический метод позволяет оценить трехмерную структуру ионного канала.
Методы исследования ионных каналов • Исследования ионных каналов с помощью потенциалчувствительных красителей. Изменения МП и, следовательно, активность ионных каналов, можно регистрировать с помощью потенциал-чувствительных красителей, спектральные характеристики которых меняются в ответ на изменения потенциала. • Рентгенокристаллографический метод. Использование метода рентгенокристаллографии совместно с биохимическими, генетическими, электрофизиологическими методами позволило выявить принципы структуры и функционирования канальных белков. Рентгенокристаллографический метод позволяет оценить трехмерную структуру ионного канала.
 Структура калиевого канала, полученная с помощью рентгенокристаллического метода А - Вид на канал с внешней стороны мембраны. Область поры (Р) (показана белым) состоит из короткой спирали и петли, формирующей селективный фильтр канала. Б – Вид на канал сбоку, разными цветами показаны четыре субъединицы. В- Вид на канал сбоку, показаны две из четырех субъединиц, селективный фильтр Г – Схема канала в мембране,
Структура калиевого канала, полученная с помощью рентгенокристаллического метода А - Вид на канал с внешней стороны мембраны. Область поры (Р) (показана белым) состоит из короткой спирали и петли, формирующей селективный фильтр канала. Б – Вид на канал сбоку, разными цветами показаны четыре субъединицы. В- Вид на канал сбоку, показаны две из четырех субъединиц, селективный фильтр Г – Схема канала в мембране,
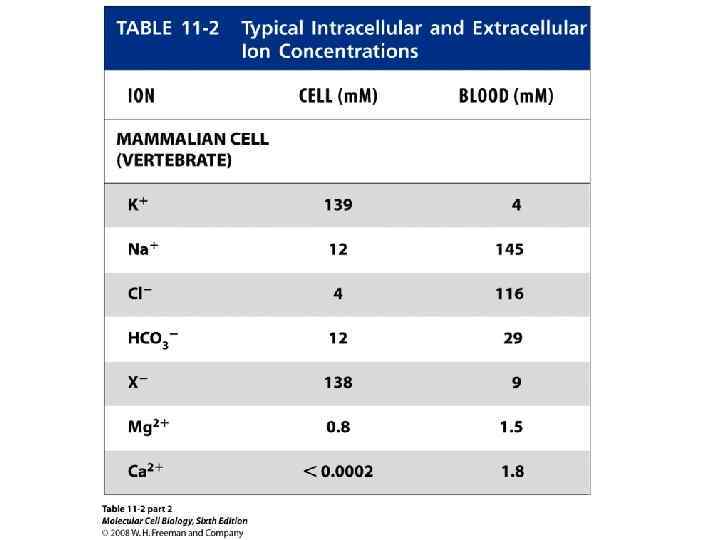
 Механизмы перемещения веществ через мембрану • Два механизма: посредством простой диффузии, т. е. без помощи специфического переносчика, и при помощи специфических переносчиков. В первом случае выделяют диффузию соединений непосредственно через липидный бислой мембраны и ионов через ионные каналы. • Во втором случае выделяют так называемую облегченную диффузию, первично активный транспорт и, наконец, вторично активный транспорт.
Механизмы перемещения веществ через мембрану • Два механизма: посредством простой диффузии, т. е. без помощи специфического переносчика, и при помощи специфических переносчиков. В первом случае выделяют диффузию соединений непосредственно через липидный бислой мембраны и ионов через ионные каналы. • Во втором случае выделяют так называемую облегченную диффузию, первично активный транспорт и, наконец, вторично активный транспорт.
 Строение и функциональные свойства различных типов ионных каналов
Строение и функциональные свойства различных типов ионных каналов
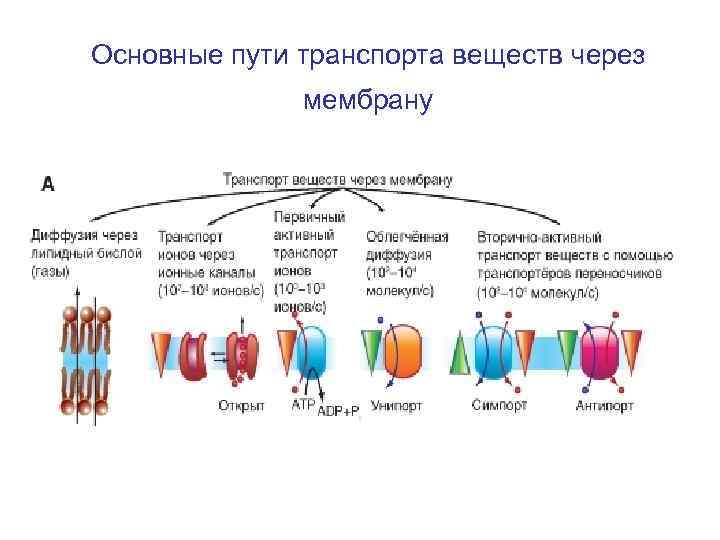 Основные пути транспорта веществ через мембрану
Основные пути транспорта веществ через мембрану
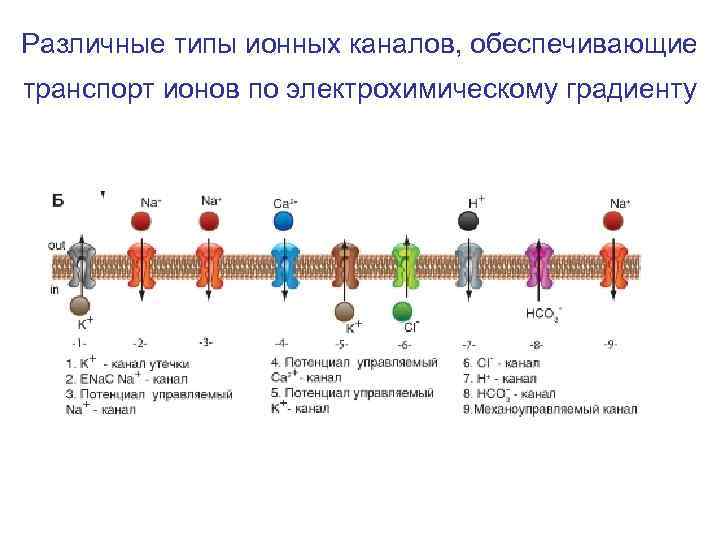 Различные типы ионных каналов, обеспечивающие транспорт ионов по электрохимическому градиенту
Различные типы ионных каналов, обеспечивающие транспорт ионов по электрохимическому градиенту
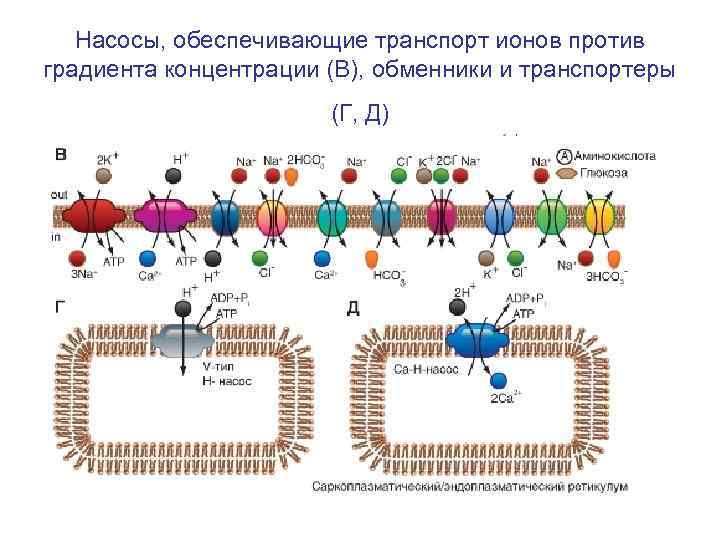 Насосы, обеспечивающие транспорт ионов против градиента концентрации (В), обменники и транспортеры (Г, Д)
Насосы, обеспечивающие транспорт ионов против градиента концентрации (В), обменники и транспортеры (Г, Д)
 Na+-канал. • Эти каналы обнаружены практически во всех возбудимых и многих невозбудимых клетках. В возбудимых клетках потенциал-активируемые Na-каналы участвуют в формировании ПД и обеспечивают достаточно высокую скорость распространения ПД по мембране (Зефиров, Гафуров, Шакирьянова, 1997). • Самая высокая плотность Na-каналов определяется в перехватах Ранвье миелинизированных нервных волокон, более низкая - в мембранах сомы нервной клетки, нервных окончаний, мышечных и эндокринных клеток. • В пресинаптических структурах Na-каналы, участвуя в формировании ПД, регулируют количество входящих ионов Са и, соответственно, количество освобождаемых квантов медиатора (Katz, 1971), а также синхронизируют секрецию медиатора во времени.
Na+-канал. • Эти каналы обнаружены практически во всех возбудимых и многих невозбудимых клетках. В возбудимых клетках потенциал-активируемые Na-каналы участвуют в формировании ПД и обеспечивают достаточно высокую скорость распространения ПД по мембране (Зефиров, Гафуров, Шакирьянова, 1997). • Самая высокая плотность Na-каналов определяется в перехватах Ранвье миелинизированных нервных волокон, более низкая - в мембранах сомы нервной клетки, нервных окончаний, мышечных и эндокринных клеток. • В пресинаптических структурах Na-каналы, участвуя в формировании ПД, регулируют количество входящих ионов Са и, соответственно, количество освобождаемых квантов медиатора (Katz, 1971), а также синхронизируют секрецию медиатора во времени.
 Na+-канал. Свойства • Детальный анализ функционирования потенциалактивируемых Na-каналов методами фиксации потенциала на гигантских аксонах беспозвоночных и миелинизированных нервных волокнах 39 позвоночных животных привел к созданию модели работы Na-канала • (Hille, 2001). • Воротный механизм Na-канала характеризуется 4 процессами: активация при деполяризации, инактивация при длительной деполяризации, деактивация после реполяризации и реактивация канала при его выходе из инактивированного состояния. • Na-каналы закрыты при нормальных значениях МП покоя и открываются на очень короткое время (1 мс и менее) при деполяризации.
Na+-канал. Свойства • Детальный анализ функционирования потенциалактивируемых Na-каналов методами фиксации потенциала на гигантских аксонах беспозвоночных и миелинизированных нервных волокнах 39 позвоночных животных привел к созданию модели работы Na-канала • (Hille, 2001). • Воротный механизм Na-канала характеризуется 4 процессами: активация при деполяризации, инактивация при длительной деполяризации, деактивация после реполяризации и реактивация канала при его выходе из инактивированного состояния. • Na-каналы закрыты при нормальных значениях МП покоя и открываются на очень короткое время (1 мс и менее) при деполяризации.
 Na+-канал. Свойства • Кроме основной роли в генерации и проведении ПД Na-каналы принимают участие в создании определенной внутриклеточной концентрации ионов Na, которая влияет на внутриклеточную концентрацию ионов Са через работу Na/Ca обменника. • Поэтому увеличение внутриклеточной концентрации ионов Na вызывает значительное усиление секреции медиатора.
Na+-канал. Свойства • Кроме основной роли в генерации и проведении ПД Na-каналы принимают участие в создании определенной внутриклеточной концентрации ионов Na, которая влияет на внутриклеточную концентрацию ионов Са через работу Na/Ca обменника. • Поэтому увеличение внутриклеточной концентрации ионов Na вызывает значительное усиление секреции медиатора.
 Na+-канал. Планометрическая организация • Структура канала, включает α-субъединицу и β 1 -, β 2 субъединицы. Внеклеточные участки β 1 -, β 2 субъединиц - участки вероятного гликозилирования; • P - места фосфорилирования протеинкиназой А (круги) и протеинкиназой C (ромбы); h инактивационная частица в петле инактивационных ворот. • α-Субъединица состоит из четырех доменов (DI-DIV), каждый из которых состоит из шести сегментов (S 1 S 6).
Na+-канал. Планометрическая организация • Структура канала, включает α-субъединицу и β 1 -, β 2 субъединицы. Внеклеточные участки β 1 -, β 2 субъединиц - участки вероятного гликозилирования; • P - места фосфорилирования протеинкиназой А (круги) и протеинкиназой C (ромбы); h инактивационная частица в петле инактивационных ворот. • α-Субъединица состоит из четырех доменов (DI-DIV), каждый из которых состоит из шести сегментов (S 1 S 6).
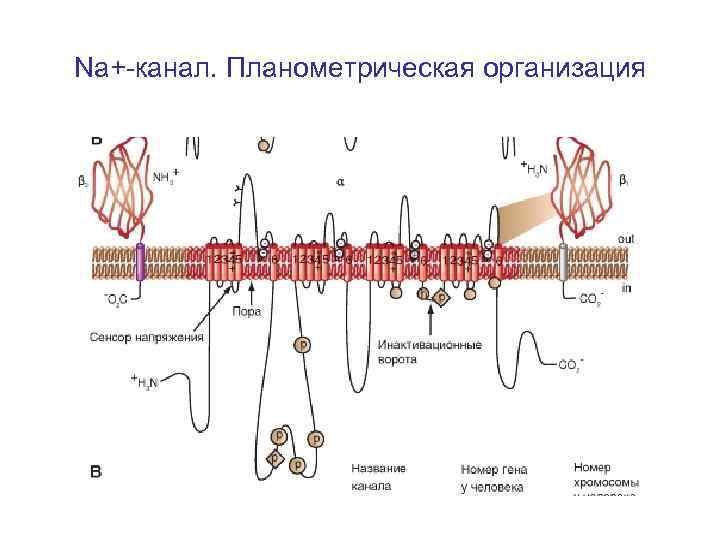 Na+-канал. Планометрическая организация
Na+-канал. Планометрическая организация
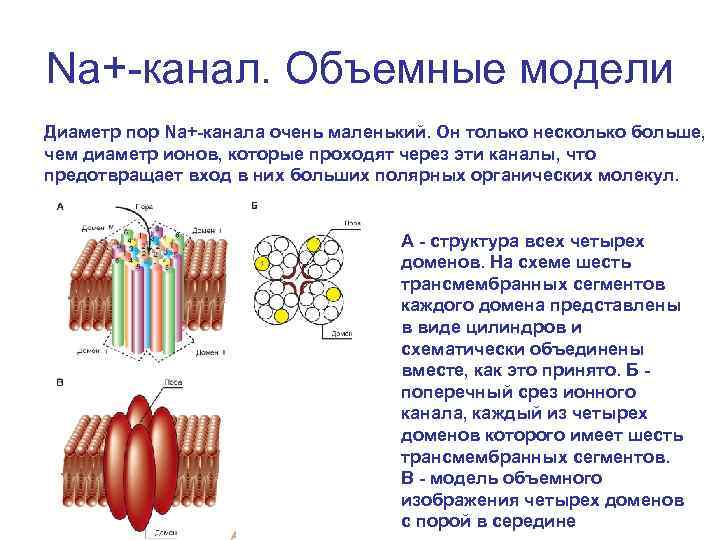 Na+-канал. Объемные модели Диаметр пор Na+-канала очень маленький. Он только несколько больше, чем диаметр ионов, которые проходят через эти каналы, что предотвращает вход в них больших полярных органических молекул. А - структура всех четырех доменов. На схеме шесть трансмембранных сегментов каждого домена представлены в виде цилиндров и схематически объединены вместе, как это принято. Б поперечный срез ионного канала, каждый из четырех доменов которого имеет шесть трансмембранных сегментов. В - модель объемного изображения четырех доменов с порой в середине
Na+-канал. Объемные модели Диаметр пор Na+-канала очень маленький. Он только несколько больше, чем диаметр ионов, которые проходят через эти каналы, что предотвращает вход в них больших полярных органических молекул. А - структура всех четырех доменов. На схеме шесть трансмембранных сегментов каждого домена представлены в виде цилиндров и схематически объединены вместе, как это принято. Б поперечный срез ионного канала, каждый из четырех доменов которого имеет шесть трансмембранных сегментов. В - модель объемного изображения четырех доменов с порой в середине
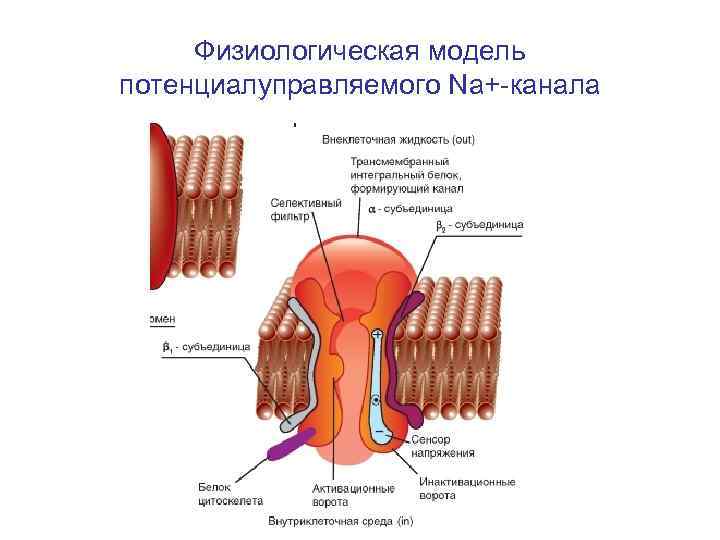 Физиологическая модель потенциалуправляемого Na+-канала
Физиологическая модель потенциалуправляемого Na+-канала
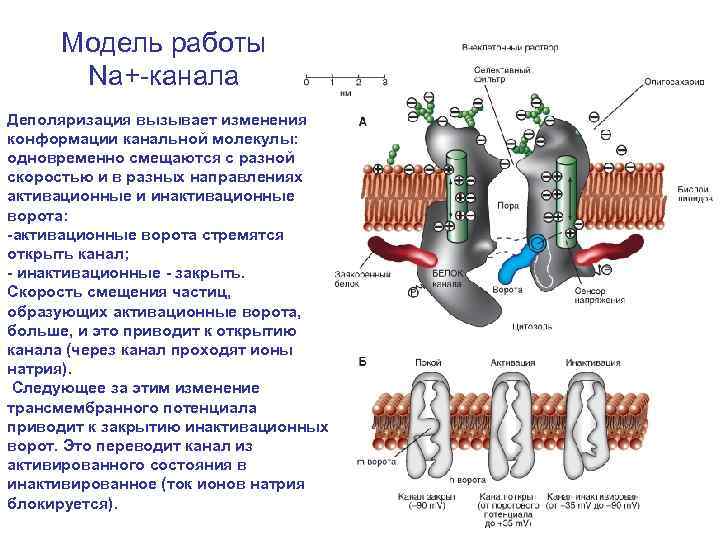 Модель работы Na+-канала Деполяризация вызывает изменения конформации канальной молекулы: одновременно смещаются с разной скоростью и в разных направлениях активационные и инактивационные ворота: -активационные ворота стремятся открыть канал; - инактивационные - закрыть. Скорость смещения частиц, образующих активационные ворота, больше, и это приводит к открытию канала (через канал проходят ионы натрия). Следующее за этим изменение трансмембранного потенциала приводит к закрытию инактивационных ворот. Это переводит канал из активированного состояния в инактивированное (ток ионов натрия блокируется).
Модель работы Na+-канала Деполяризация вызывает изменения конформации канальной молекулы: одновременно смещаются с разной скоростью и в разных направлениях активационные и инактивационные ворота: -активационные ворота стремятся открыть канал; - инактивационные - закрыть. Скорость смещения частиц, образующих активационные ворота, больше, и это приводит к открытию канала (через канал проходят ионы натрия). Следующее за этим изменение трансмембранного потенциала приводит к закрытию инактивационных ворот. Это переводит канал из активированного состояния в инактивированное (ток ионов натрия блокируется).
 Фармакология Na-каналов • Ряд биологических токсинов модифицируют свойства Naканалов. По участкам связывания и механизмам блокирующего действия все токсины можно разделить на несколько групп. • Первая группа. Токсины данной группы блокируют ионную проводимость Na-канала. К ним относится алкалоид тетродотоксин – 42 хорошо известный токсин, обнаруженный в рыбе фуга (Tetrodontidae). • Вторая группа. Эти токсины вызывают постоянную активацию Na-каналов. К ним относят липидорастворимые токсины вератридин, батрахотоксин, аконитин и грайянотоксин. Постоянная активация Na-каналов при действии данных вещества объясняется двумя эффектами: сдвигом потенциалзависимости активации к более отрицательным значениям МП и блокированием быстрой инактивации.
Фармакология Na-каналов • Ряд биологических токсинов модифицируют свойства Naканалов. По участкам связывания и механизмам блокирующего действия все токсины можно разделить на несколько групп. • Первая группа. Токсины данной группы блокируют ионную проводимость Na-канала. К ним относится алкалоид тетродотоксин – 42 хорошо известный токсин, обнаруженный в рыбе фуга (Tetrodontidae). • Вторая группа. Эти токсины вызывают постоянную активацию Na-каналов. К ним относят липидорастворимые токсины вератридин, батрахотоксин, аконитин и грайянотоксин. Постоянная активация Na-каналов при действии данных вещества объясняется двумя эффектами: сдвигом потенциалзависимости активации к более отрицательным значениям МП и блокированием быстрой инактивации.
 Фармакология Na-каналов • Третья группа. Токсины данной группы, связываясь с внеклеточной стороной канала, блокируют или замедляют инактивацию Na-каналов, предотвращая переход из открытого в инактивированное состояние. Это a-токсины скорпиона, выделенные из яда северо-африканских видов Androctonus, Buthus и Leiurus. • Четвертая группа. Данные токсины смещают потенциалзависимость активации Na-канала к более отрицательным значениям МП, не влияя на инактивацию. • Пятая группа. Токсины данной группы вызывают повторную нейрональную активность, изменяют потенциал-зависимость и блокируют инактивацию Na-каналов.
Фармакология Na-каналов • Третья группа. Токсины данной группы, связываясь с внеклеточной стороной канала, блокируют или замедляют инактивацию Na-каналов, предотвращая переход из открытого в инактивированное состояние. Это a-токсины скорпиона, выделенные из яда северо-африканских видов Androctonus, Buthus и Leiurus. • Четвертая группа. Данные токсины смещают потенциалзависимость активации Na-канала к более отрицательным значениям МП, не влияя на инактивацию. • Пятая группа. Токсины данной группы вызывают повторную нейрональную активность, изменяют потенциал-зависимость и блокируют инактивацию Na-каналов.
 Фармакология Na-каналов • Шестая группа. К токсинам, связывающимся с участком 6, относят пиретроидные инсектициды, которые являются сильными возбуждающими нейротоксинами. Они вызывают гипервозбуждение и паралич животных. Пиретроиды представляют особый интерес, так как проявляют высокую степень селективной токсичности между млекопитающими и беспозвоночными животными.
Фармакология Na-каналов • Шестая группа. К токсинам, связывающимся с участком 6, относят пиретроидные инсектициды, которые являются сильными возбуждающими нейротоксинами. Они вызывают гипервозбуждение и паралич животных. Пиретроиды представляют особый интерес, так как проявляют высокую степень селективной токсичности между млекопитающими и беспозвоночными животными.
 Са 2+-канал. • Са 2+-каналы были обнаружены практически во всех клетках. • Са 2+-каналы были классифицированы на основе двух принципов: • • химический символ главного иона, для которого они проницаемы (в данном случае ионы • Ca 2+); • • принцип физиологической регуляции работы канала, имея в виду, что эти каналы потенциалуправляемые (voltage gated calcium channels) Са 2+-каналы, • Са 2+-каналы представляют собой комплекс белков, образованный из четырех или пяти определенных субъединиц, кодирующихся большим семейством генов.
Са 2+-канал. • Са 2+-каналы были обнаружены практически во всех клетках. • Са 2+-каналы были классифицированы на основе двух принципов: • • химический символ главного иона, для которого они проницаемы (в данном случае ионы • Ca 2+); • • принцип физиологической регуляции работы канала, имея в виду, что эти каналы потенциалуправляемые (voltage gated calcium channels) Са 2+-каналы, • Са 2+-каналы представляют собой комплекс белков, образованный из четырех или пяти определенных субъединиц, кодирующихся большим семейством генов.
 Кальциевые токи • L-тип (от «long-lasting» - долго длящийся) Са 2+-токов требует сильной деполяризации для активации, он долго длящийся и блокируется органическими антагонистами L-типа Са 2+-каналов, включая дигидропиридины, фенилалкиламины и бензотиазепины. Са 2+-токи L-типа являются главными в мышцах и эндокринных клетках, где они инициируют сокращение и секрецию.
Кальциевые токи • L-тип (от «long-lasting» - долго длящийся) Са 2+-токов требует сильной деполяризации для активации, он долго длящийся и блокируется органическими антагонистами L-типа Са 2+-каналов, включая дигидропиридины, фенилалкиламины и бензотиазепины. Са 2+-токи L-типа являются главными в мышцах и эндокринных клетках, где они инициируют сокращение и секрецию.
 Кальциевые токи • N-тип (от «neither long nor transient» - ни L, ни T), P/Qтип и R-тип кальциевых токов также требуют сильной деполяризации для активации. Они относительно нечувствительны к антагонистами L-типа Са 2+каналов, но блокируются специфическими полипептидными токсинами из ядов улитки или паука. Эти токи в основном выражены в нейронах, где они инициируют нейротрансмиссию для большинства быстрых синапсов и также опосредуют вход Са 2+ в клеточные тела и дендриты.
Кальциевые токи • N-тип (от «neither long nor transient» - ни L, ни T), P/Qтип и R-тип кальциевых токов также требуют сильной деполяризации для активации. Они относительно нечувствительны к антагонистами L-типа Са 2+каналов, но блокируются специфическими полипептидными токсинами из ядов улитки или паука. Эти токи в основном выражены в нейронах, где они инициируют нейротрансмиссию для большинства быстрых синапсов и также опосредуют вход Са 2+ в клеточные тела и дендриты.
 Кальциевые токи • T-тип (от «transient» - преходящий) Са 2+токов активируется слабой деполяризацией, и эти токи мимолетные (преходящие). Они нечувствительны к органическим антагонистам и токсинам змей и пауков, которые используются для определения N- и P/Q Са 2+-токов. Са 2+-токи T-типа выражены в большом спектре клеточных типов, где они вовлечены в развитие потенциала действия и важны в клетках и тканях, обладающих ритмической активностью.
Кальциевые токи • T-тип (от «transient» - преходящий) Са 2+токов активируется слабой деполяризацией, и эти токи мимолетные (преходящие). Они нечувствительны к органическим антагонистам и токсинам змей и пауков, которые используются для определения N- и P/Q Са 2+-токов. Са 2+-токи T-типа выражены в большом спектре клеточных типов, где они вовлечены в развитие потенциала действия и важны в клетках и тканях, обладающих ритмической активностью.
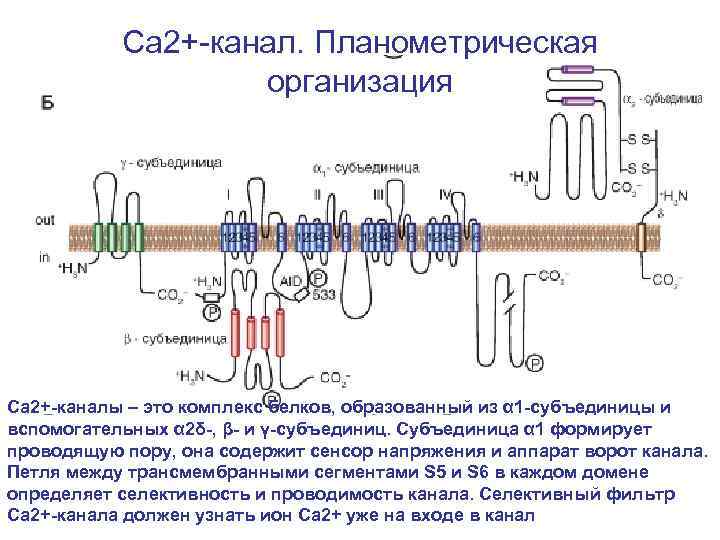 Са 2+-канал. Планометрическая организация Са 2+-каналы – это комплекс белков, образованный из α 1 -субъединицы и вспомогательных α 2δ-, β- и γ-субъединиц. Субъединица α 1 формирует проводящую пору, она содержит сенсор напряжения и аппарат ворот канала. Петля между трансмембранными сегментами S 5 и S 6 в каждом домене определяет селективность и проводимость канала. Селективный фильтр Са 2+-канала должен узнать ион Са 2+ уже на входе в канал
Са 2+-канал. Планометрическая организация Са 2+-каналы – это комплекс белков, образованный из α 1 -субъединицы и вспомогательных α 2δ-, β- и γ-субъединиц. Субъединица α 1 формирует проводящую пору, она содержит сенсор напряжения и аппарат ворот канала. Петля между трансмембранными сегментами S 5 и S 6 в каждом домене определяет селективность и проводимость канала. Селективный фильтр Са 2+-канала должен узнать ион Са 2+ уже на входе в канал
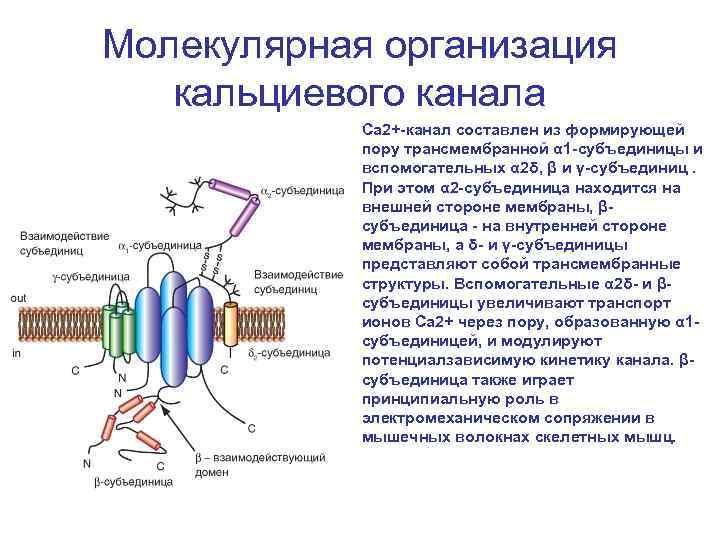 Молекулярная организация кальциевого канала Са 2+-канал составлен из формирующей пору трансмембранной α 1 -субъединицы и вспомогательных α 2δ, β и γ-субъединиц. При этом α 2 -субъединица находится на внешней стороне мембраны, βсубъединица - на внутренней стороне мембраны, а δ- и γ-субъединицы представляют собой трансмембранные структуры. Вспомогательные α 2δ- и βсубъединицы увеличивают транспорт ионов Са 2+ через пору, образованную α 1 субъединицей, и модулируют потенциалзависимую кинетику канала. βсубъединица также играет принципиальную роль в электромеханическом сопряжении в мышечных волокнах скелетных мышц.
Молекулярная организация кальциевого канала Са 2+-канал составлен из формирующей пору трансмембранной α 1 -субъединицы и вспомогательных α 2δ, β и γ-субъединиц. При этом α 2 -субъединица находится на внешней стороне мембраны, βсубъединица - на внутренней стороне мембраны, а δ- и γ-субъединицы представляют собой трансмембранные структуры. Вспомогательные α 2δ- и βсубъединицы увеличивают транспорт ионов Са 2+ через пору, образованную α 1 субъединицей, и модулируют потенциалзависимую кинетику канала. βсубъединица также играет принципиальную роль в электромеханическом сопряжении в мышечных волокнах скелетных мышц.
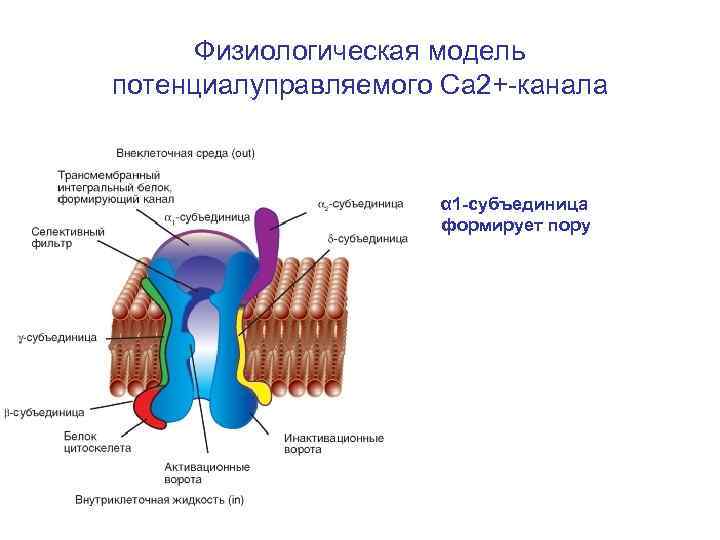 Физиологическая модель потенциалуправляемого Сa 2+-канала α 1 -субъединица формирует пору
Физиологическая модель потенциалуправляемого Сa 2+-канала α 1 -субъединица формирует пору
 Внутриклеточные Са-каналы • • • Цитоплазматическая концентрация свободных ионов Ca мала и значительное количество Ca находится во внутриклеточных структурах. Запасенный в них Ca может высвобождаться в ответ на адекватные стимулы через Са-каналы. В различных клетках описано большое количество структур, которые утилизируют внутриклеточный кальций (Балезина О. П. , 2002), главными из которых являются гладкий ЭПР На мембране гладкого ЭПР нервных клеток описаны, по крайней мере, два основных типа лиганд-активируемых Са-каналов: рианодиновые (Ри) и инозитолтрифосфатные (ИФ 3). В последние годы быстро растет число свидетельств существования и других разновидностей внутриклеточных Саканалов, избирательно активируемых внутриклеточными метаболитами (НАД+, НАДФ+, циклическая АДФ-рибоза и др. ),
Внутриклеточные Са-каналы • • • Цитоплазматическая концентрация свободных ионов Ca мала и значительное количество Ca находится во внутриклеточных структурах. Запасенный в них Ca может высвобождаться в ответ на адекватные стимулы через Са-каналы. В различных клетках описано большое количество структур, которые утилизируют внутриклеточный кальций (Балезина О. П. , 2002), главными из которых являются гладкий ЭПР На мембране гладкого ЭПР нервных клеток описаны, по крайней мере, два основных типа лиганд-активируемых Са-каналов: рианодиновые (Ри) и инозитолтрифосфатные (ИФ 3). В последние годы быстро растет число свидетельств существования и других разновидностей внутриклеточных Саканалов, избирательно активируемых внутриклеточными метаболитами (НАД+, НАДФ+, циклическая АДФ-рибоза и др. ),
 Са-каналы Ри-рецепторов. • Этот тип внутриклеточных Са-каналов активируется ионами Са и вызывает кальций-вызванное освобождение кальция из гладкого ЭПР и СПР в нервных клетках, скелетной, гладкой и сердечной мышцах. Внутриклеточные Ca-каналы обеспечивают длительное поддержание высокой внутриклеточной концентрации ионов Са, обеспечивают сокращение мышц и возникновение Са-волн.
Са-каналы Ри-рецепторов. • Этот тип внутриклеточных Са-каналов активируется ионами Са и вызывает кальций-вызванное освобождение кальция из гладкого ЭПР и СПР в нервных клетках, скелетной, гладкой и сердечной мышцах. Внутриклеточные Ca-каналы обеспечивают длительное поддержание высокой внутриклеточной концентрации ионов Са, обеспечивают сокращение мышц и возникновение Са-волн.
 Са-каналы Ри-рецепторов • В настоящее время охарактеризованы три разновидности молекул Ри-рецепторов (Балезина, 2002), все они имеются в нервной ткани, но наиболее распространенным в ЦНС является второй тип. • Первый и второй типы Ри-рецепторов активируются (помимо Са и АТФ) рианодином и кофеином, однако, различаются • чувствительностью к дантролену, который инактивирует лишь первый тип. • Третий тип Ри-рецепторов активируется ионами Са, ианодином • (в наномолярных концентрациях), не чувствителен к действию • кофеина и блокируется дантроленом.
Са-каналы Ри-рецепторов • В настоящее время охарактеризованы три разновидности молекул Ри-рецепторов (Балезина, 2002), все они имеются в нервной ткани, но наиболее распространенным в ЦНС является второй тип. • Первый и второй типы Ри-рецепторов активируются (помимо Са и АТФ) рианодином и кофеином, однако, различаются • чувствительностью к дантролену, который инактивирует лишь первый тип. • Третий тип Ри-рецепторов активируется ионами Са, ианодином • (в наномолярных концентрациях), не чувствителен к действию • кофеина и блокируется дантроленом.
 Са-каналы Ри-рецепторов • • Ри-рецепторы в симпатических нервных окончаниях морской свинки и в клетках Пуркинье мозжечка могут участвовать в освобождении медиатора. В нервно-мышечном соединении мыши рианодин усиливает кальций-зависимое освобождение медиатора. В сердце освобождение Са из внутриклеточных депо инициируется Са-входом через быстроактивируемые Са-каналы Т -типа и поддерживается Са-каналами L-типа во время фазы плато ПД. Кальций активирует Ри-рецепторы 2 -типа, экспрессируемые в сердечной и гладкой мышцах. В скелетной мышце освобождение кальция опосредуется Рирецепторами, которые локализованы в мембране СПР вблизи Ттрубочек и контактируют с потенциал-активируемыми Саканалами L-типа (ДГП-рецепторами) с помощью доменов, выступающих в цитозоль. Деполяризация тубулярной мембраны вызывает конформационные изменения рецептора, что ведет к активации Ри-рецепторов. Этот сигнал, передающийся между Ттубулярной системой и саркоплазматической мембраной, опосредует связь возбуждение-сокращение в мышце.
Са-каналы Ри-рецепторов • • Ри-рецепторы в симпатических нервных окончаниях морской свинки и в клетках Пуркинье мозжечка могут участвовать в освобождении медиатора. В нервно-мышечном соединении мыши рианодин усиливает кальций-зависимое освобождение медиатора. В сердце освобождение Са из внутриклеточных депо инициируется Са-входом через быстроактивируемые Са-каналы Т -типа и поддерживается Са-каналами L-типа во время фазы плато ПД. Кальций активирует Ри-рецепторы 2 -типа, экспрессируемые в сердечной и гладкой мышцах. В скелетной мышце освобождение кальция опосредуется Рирецепторами, которые локализованы в мембране СПР вблизи Ттрубочек и контактируют с потенциал-активируемыми Саканалами L-типа (ДГП-рецепторами) с помощью доменов, выступающих в цитозоль. Деполяризация тубулярной мембраны вызывает конформационные изменения рецептора, что ведет к активации Ри-рецепторов. Этот сигнал, передающийся между Ттубулярной системой и саркоплазматической мембраной, опосредует связь возбуждение-сокращение в мышце.
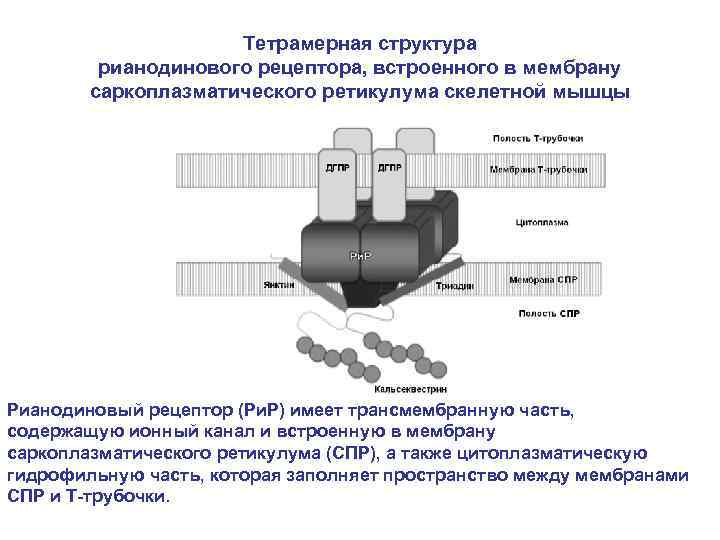 Тетрамерная структура рианодинового рецептора, встроенного в мембрану саркоплазматического ретикулума скелетной мышцы Рианодиновый рецептор (Ри. Р) имеет трансмембранную часть, содержащую ионный канал и встроенную в мембрану саркоплазматического ретикулума (СПР), а также цитоплазматическую гидрофильную часть, которая заполняет пространство между мембранами СПР и Т-трубочки.
Тетрамерная структура рианодинового рецептора, встроенного в мембрану саркоплазматического ретикулума скелетной мышцы Рианодиновый рецептор (Ри. Р) имеет трансмембранную часть, содержащую ионный канал и встроенную в мембрану саркоплазматического ретикулума (СПР), а также цитоплазматическую гидрофильную часть, которая заполняет пространство между мембранами СПР и Т-трубочки.
 Каналы рецептора инозитолтрифосфата (ИФ 3 -рецепторы). • ИФ 3 относится к вторичным посредникам, образующимся при активации фосфолипазы С гормонами и нейромедиаторами, расщепляющей фосфатидилинозитолдифосфат мембраны. ИФ 3 стимулирует высвобождение кальция из ЭПР путем активации ИФ 3 -рецепторов, что обеспечивает запуск целого ряда внутриклеточных Са-зависимых процессов: активацию Са-кальмодулин-зависимых
Каналы рецептора инозитолтрифосфата (ИФ 3 -рецепторы). • ИФ 3 относится к вторичным посредникам, образующимся при активации фосфолипазы С гормонами и нейромедиаторами, расщепляющей фосфатидилинозитолдифосфат мембраны. ИФ 3 стимулирует высвобождение кальция из ЭПР путем активации ИФ 3 -рецепторов, что обеспечивает запуск целого ряда внутриклеточных Са-зависимых процессов: активацию Са-кальмодулин-зависимых
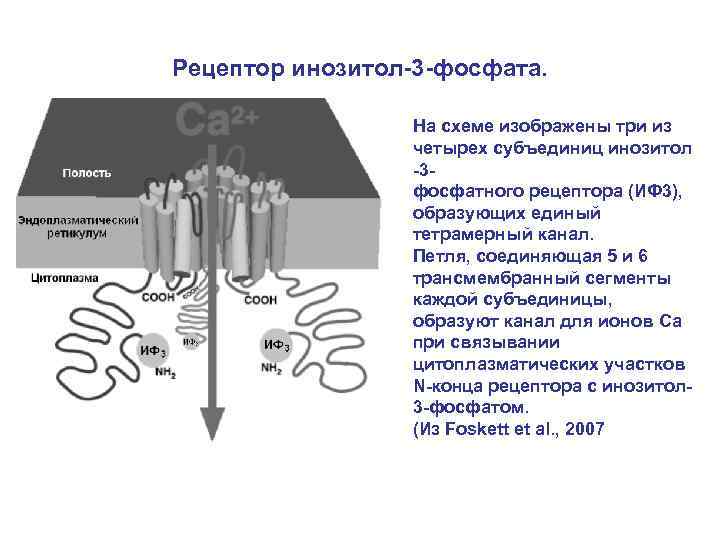 Рецептор инозитол-3 -фосфата. На схеме изображены три из четырех субъединиц инозитол -3 фосфатного рецептора (ИФ 3), образующих единый тетрамерный канал. Петля, соединяющая 5 и 6 трансмембранный сегменты каждой субъединицы, образуют канал для ионов Са при связывании цитоплазматических участков N-конца рецептора с инозитол 3 -фосфатом. (Из Foskett et al. , 2007
Рецептор инозитол-3 -фосфата. На схеме изображены три из четырех субъединиц инозитол -3 фосфатного рецептора (ИФ 3), образующих единый тетрамерный канал. Петля, соединяющая 5 и 6 трансмембранный сегменты каждой субъединицы, образуют канал для ионов Са при связывании цитоплазматических участков N-конца рецептора с инозитол 3 -фосфатом. (Из Foskett et al. , 2007
 K+-канал • Классификация К+-каналов: • потенциалуправляемые К+-каналы (KV); • Ca 2+- активируемые К+-каналы (KCa); • K+-каналы аномального выпрямления с током входящего направления (inward rectifier K+-channels) (Kir); • K+-каналы с двумя петлями в домене (two-P K+-channels) (К 2 Р). • АТФ-зависимый К-канал • К-канал утечки • К-каналы возбудимых клеток участвуют в образовании МП покоя, обеспечивают реполяризацию мембраны во время ПД, формируют следовую гиперполяризацию, модулируют повторную активность, имеют очень большое значение в регуляции секреции медиатора из нервных окончаний, принимают участие в механизмах обучения и памяти (Зефиров, Ситдикова, 2002, 2010).
K+-канал • Классификация К+-каналов: • потенциалуправляемые К+-каналы (KV); • Ca 2+- активируемые К+-каналы (KCa); • K+-каналы аномального выпрямления с током входящего направления (inward rectifier K+-channels) (Kir); • K+-каналы с двумя петлями в домене (two-P K+-channels) (К 2 Р). • АТФ-зависимый К-канал • К-канал утечки • К-каналы возбудимых клеток участвуют в образовании МП покоя, обеспечивают реполяризацию мембраны во время ПД, формируют следовую гиперполяризацию, модулируют повторную активность, имеют очень большое значение в регуляции секреции медиатора из нервных окончаний, принимают участие в механизмах обучения и памяти (Зефиров, Ситдикова, 2002, 2010).
 Потенциалуправляемые К+каналы (Kv) • KV каналы образованы белковыми субъединицами двух типов: α-субъединицами, формирующими пору, и вспомогательными βсубъединицами. Субъединицы α формируют тетрамер, чтобы образовать функциональный канал, проводящий ионы K+. • Одна субъединица ΚV-канала - белок с шестью трансмембранными сегментами (S) α-спирали (S 1 -S 6) и расположенными в цитоплазме N- и C-терминалями. • N- и С-концевым петлям. Они включают контроль за инактивацией каналов, белок-белковое взаимодействие (по типу тетрамеризации α-субъединиц, взаимодействие с цитоплазматическими β-субъединицами и сохранение последовательностей). • КV-каналы открыты при деполяризации трансмембранного потенциала, что способствует выходу ионов К+.
Потенциалуправляемые К+каналы (Kv) • KV каналы образованы белковыми субъединицами двух типов: α-субъединицами, формирующими пору, и вспомогательными βсубъединицами. Субъединицы α формируют тетрамер, чтобы образовать функциональный канал, проводящий ионы K+. • Одна субъединица ΚV-канала - белок с шестью трансмембранными сегментами (S) α-спирали (S 1 -S 6) и расположенными в цитоплазме N- и C-терминалями. • N- и С-концевым петлям. Они включают контроль за инактивацией каналов, белок-белковое взаимодействие (по типу тетрамеризации α-субъединиц, взаимодействие с цитоплазматическими β-субъединицами и сохранение последовательностей). • КV-каналы открыты при деполяризации трансмембранного потенциала, что способствует выходу ионов К+.
 Функции потенциалуправляемых К+-каналов (Kv) • Таким образом, КV-каналы чувствуют деполяризацию и, в свою очередь, действуют так, чтобы ее устранить. Одна из наиболее охарактеризованных ролей КV-каналов заключается в том, чтобы закончить сильную деполяризацию, вызванную активацией потенциалзависимого входа катионов (совместно образующих потенциал действия). Таким образом, можно постулировать, что любые увеличения КV-канальной активности будут приводить к более эффективному окончанию деполяризации (обычно укорачивая или убирая потенциал действия). Эта функциональная способность КV-каналов также лежит в основе формирования пачечной активности (взрывной). Таким образом, активность КV-каналов играет, например, роль в кодировании информации в нервной системе.
Функции потенциалуправляемых К+-каналов (Kv) • Таким образом, КV-каналы чувствуют деполяризацию и, в свою очередь, действуют так, чтобы ее устранить. Одна из наиболее охарактеризованных ролей КV-каналов заключается в том, чтобы закончить сильную деполяризацию, вызванную активацией потенциалзависимого входа катионов (совместно образующих потенциал действия). Таким образом, можно постулировать, что любые увеличения КV-канальной активности будут приводить к более эффективному окончанию деполяризации (обычно укорачивая или убирая потенциал действия). Эта функциональная способность КV-каналов также лежит в основе формирования пачечной активности (взрывной). Таким образом, активность КV-каналов играет, например, роль в кодировании информации в нервной системе.
 Планометрическая модель молекулярной организации потенциалуправляемого К+-канала (КV-канала). А - одна субъединица КV-канала представляет собой α-спираль с шестью трансмембранными сегментами (S 1 -S 6) и расположенными в цитоплазме Nи C-терминалями. Внеклеточная Pпетля между сегментами S 5 и S 6 формирует селективный фильтр для ионов К+ и пору канала, а положительно заряженный сегмент S 4 формирует сенсор напряжения белка. Длинные N- и C -терминальные петли контролируют инактивацию каналов и белок-белковое взаимодействие. Б - ассоциация четырех субъединиц в КV-канал
Планометрическая модель молекулярной организации потенциалуправляемого К+-канала (КV-канала). А - одна субъединица КV-канала представляет собой α-спираль с шестью трансмембранными сегментами (S 1 -S 6) и расположенными в цитоплазме Nи C-терминалями. Внеклеточная Pпетля между сегментами S 5 и S 6 формирует селективный фильтр для ионов К+ и пору канала, а положительно заряженный сегмент S 4 формирует сенсор напряжения белка. Длинные N- и C -терминальные петли контролируют инактивацию каналов и белок-белковое взаимодействие. Б - ассоциация четырех субъединиц в КV-канал
 Семейство KV • До настоящего времени в геноме человека описаны 38 генов, кодирующих различные каналы суперсемейства KV. • КV-каналы включают классические категории каналов: • К+-каналы задержанного выпрямления (delayed rectifier K+-channels) и быстрые транзиторные К+-каналы выходящего тока (fast transient K+-channels: fast transient K+current IA, или transient outward current Ito).
Семейство KV • До настоящего времени в геноме человека описаны 38 генов, кодирующих различные каналы суперсемейства KV. • КV-каналы включают классические категории каналов: • К+-каналы задержанного выпрямления (delayed rectifier K+-channels) и быстрые транзиторные К+-каналы выходящего тока (fast transient K+-channels: fast transient K+current IA, или transient outward current Ito).
 Семейство KV
Семейство KV
 К-каналы задержанного выпрямления (Кdr-каналы). «delayed rectifier K+-channels» • Название «delayed rectifier K+-channels» было первоначально дано потенциалуправляемым К+- каналам гигантского аксона кальмара из-за их отсроченной активации (по сравнению с быстро активизирующимися Na+-каналами). Члены всех KV подсемейств (включая KV 1 -4, EAG и KCNQ) могут формировать delayed rectifier K+-channels • К-каналы задержанного выпрямления (Кdr-каналы). Эти каналы преобладают в большинстве возбудимых клетках, активируются при деполяризации и не инактивируются, либо инактивируются очень медленно (от сотен миллисекунд до нескольких секунд).
К-каналы задержанного выпрямления (Кdr-каналы). «delayed rectifier K+-channels» • Название «delayed rectifier K+-channels» было первоначально дано потенциалуправляемым К+- каналам гигантского аксона кальмара из-за их отсроченной активации (по сравнению с быстро активизирующимися Na+-каналами). Члены всех KV подсемейств (включая KV 1 -4, EAG и KCNQ) могут формировать delayed rectifier K+-channels • К-каналы задержанного выпрямления (Кdr-каналы). Эти каналы преобладают в большинстве возбудимых клетках, активируются при деполяризации и не инактивируются, либо инактивируются очень медленно (от сотен миллисекунд до нескольких секунд).
 Быстрые К-каналы (КА-каналы). Fast transient K+-channels • Fast transient K+-channels (формирующие fast transient K+current: IA, или transient outward current Ito) - быстрые транзиторные ^-каналы выходящего тока представляют собой каналы, активируемые низким потенциалом (low voltageactivated). Они быстро инактивирующиеся (транзиторные, иначе - временные, мимолетные K+-каналы). Каналы этого типа обычно образованы из членов • Впервые КА-каналы были обнаружены в нейронах моллюсков. В различных нейронах функции КА-каналов включают регуляцию повторной активности, определение латентного периода первого спайка и, в некоторых случаях, участие в реполяризации ПД. • Поэтому КА- каналы способны регулировать повторную активность низкой частоты и преобладают в сенсорных нейронах, которые разряжаются с частотой, отражающей интенсивность стимула.
Быстрые К-каналы (КА-каналы). Fast transient K+-channels • Fast transient K+-channels (формирующие fast transient K+current: IA, или transient outward current Ito) - быстрые транзиторные ^-каналы выходящего тока представляют собой каналы, активируемые низким потенциалом (low voltageactivated). Они быстро инактивирующиеся (транзиторные, иначе - временные, мимолетные K+-каналы). Каналы этого типа обычно образованы из членов • Впервые КА-каналы были обнаружены в нейронах моллюсков. В различных нейронах функции КА-каналов включают регуляцию повторной активности, определение латентного периода первого спайка и, в некоторых случаях, участие в реполяризации ПД. • Поэтому КА- каналы способны регулировать повторную активность низкой частоты и преобладают в сенсорных нейронах, которые разряжаются с частотой, отражающей интенсивность стимула.
 Медленно активирующиеся К-каналы (КS-каналы). • Задержанные выпрямляющие К-токи с очень медленной кинетикой активации (slow) были впервые описаны в волокнах Пуркинье сердца. • Медленно активирующийся Ks-канал был обнаружен в изолированных нервных окончаниях гипофиза. Временная константа активации составляет 4 с при -50 м. В и уменьшается до 700 мс при -40 м. В
Медленно активирующиеся К-каналы (КS-каналы). • Задержанные выпрямляющие К-токи с очень медленной кинетикой активации (slow) были впервые описаны в волокнах Пуркинье сердца. • Медленно активирующийся Ks-канал был обнаружен в изолированных нервных окончаниях гипофиза. Временная константа активации составляет 4 с при -50 м. В и уменьшается до 700 мс при -40 м. В
 Группы Kir • Эти каналы преобладают в большинстве возбудимых клетках, активируются при деполяризации и не инактивируются, либо инактивируются очень медленно (от сотен миллисекунд до нескольких секунд). • Класс 2 S-белков включает три группы каналов inward rectifiers channels (Kir), которые можно назвать, хотя и очень длинно, как «К+-каналы аномального выпрямления с током входящего направления» . N- и С-терминали этих каналов также расположены в цитоплазме, P-петля между двумя трансмембранными доменами формирует пору, и функционирующий канал представляет собой тетрамер этих 2 S/1 P-субъединиц.
Группы Kir • Эти каналы преобладают в большинстве возбудимых клетках, активируются при деполяризации и не инактивируются, либо инактивируются очень медленно (от сотен миллисекунд до нескольких секунд). • Класс 2 S-белков включает три группы каналов inward rectifiers channels (Kir), которые можно назвать, хотя и очень длинно, как «К+-каналы аномального выпрямления с током входящего направления» . N- и С-терминали этих каналов также расположены в цитоплазме, P-петля между двумя трансмембранными доменами формирует пору, и функционирующий канал представляет собой тетрамер этих 2 S/1 P-субъединиц.
 Группы Kir • Эти каналы играют важную физиологическую роль в функции многих органов, включая мозг, сердце, почки, эндокринные клетки, слуховые клетки и клетки сетчатки.
Группы Kir • Эти каналы играют важную физиологическую роль в функции многих органов, включая мозг, сердце, почки, эндокринные клетки, слуховые клетки и клетки сетчатки.
 . Молекулярная организация inwardly rectifying potassium channels - K+-каналов аномального выпрямления с током входящего направления (Kir). • А - одна субъединица К 1 r-канала представляет собой α-спираль с двумя трансмембранными сегментами (S 5 и S 6), расположенными в цитоплазме Nи C-терминалями, и короткую Р-петлю, формирующую пору. Б - ассоциация четырех субъединиц в Кir-канал. В филогенетическое дерево для Кirканалов
. Молекулярная организация inwardly rectifying potassium channels - K+-каналов аномального выпрямления с током входящего направления (Kir). • А - одна субъединица К 1 r-канала представляет собой α-спираль с двумя трансмембранными сегментами (S 5 и S 6), расположенными в цитоплазме Nи C-терминалями, и короткую Р-петлю, формирующую пору. Б - ассоциация четырех субъединиц в Кir-канал. В филогенетическое дерево для Кirканалов
 K+-каналы с двумя петлями в домене (two-P potassium channels - К 2 Р) • Как ожидалось, для регуляторов возбудимости K 2 Рканалы находятся под сильным контролем множества химических и физических стимулов, включая напряжение кислорода, p. H, липиды, механические растяжения, нейротрансмиттеры и рецепторы, связанные с G-белком. • Каналы также служат молекулярными мишенями для некоторых летучих и местных анестетиков. • Регуляция K 2 Р-каналов связана с изменениями в их свойствах, например вероятности открытия каналов. • Тем не менее некоторые регуляторные изменения, например фосфорелирование K 2 P 2, обеспечивает появление выпрямляющих свойств с чувствительностью к потенциалу.
K+-каналы с двумя петлями в домене (two-P potassium channels - К 2 Р) • Как ожидалось, для регуляторов возбудимости K 2 Рканалы находятся под сильным контролем множества химических и физических стимулов, включая напряжение кислорода, p. H, липиды, механические растяжения, нейротрансмиттеры и рецепторы, связанные с G-белком. • Каналы также служат молекулярными мишенями для некоторых летучих и местных анестетиков. • Регуляция K 2 Р-каналов связана с изменениями в их свойствах, например вероятности открытия каналов. • Тем не менее некоторые регуляторные изменения, например фосфорелирование K 2 P 2, обеспечивает появление выпрямляющих свойств с чувствительностью к потенциалу.
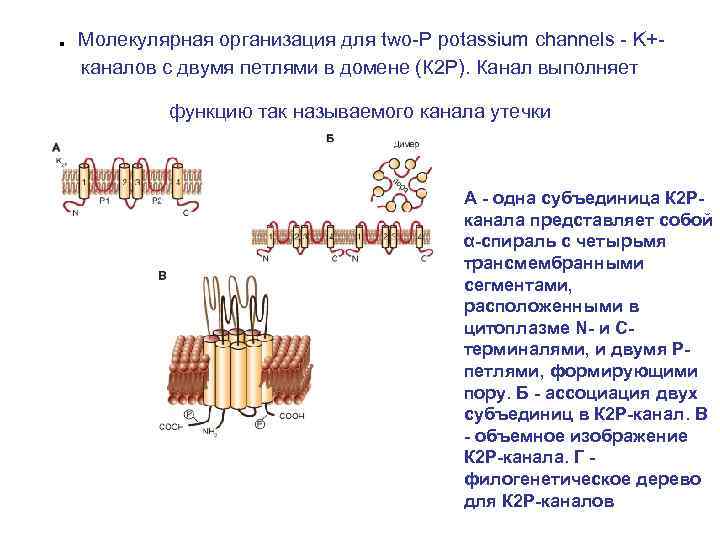 . Молекулярная организация для two-P potassium channels - K+каналов с двумя петлями в домене (К 2 Р). Канал выполняет функцию так называемого канала утечки А - одна субъединица К 2 Рканала представляет собой α-спираль с четырьмя трансмембранными сегментами, расположенными в цитоплазме N- и Cтерминалями, и двумя Рпетлями, формирующими пору. Б - ассоциация двух субъединиц в К 2 Р-канал. В - объемное изображение К 2 Р-канала. Г филогенетическое дерево для К 2 Р-каналов
. Молекулярная организация для two-P potassium channels - K+каналов с двумя петлями в домене (К 2 Р). Канал выполняет функцию так называемого канала утечки А - одна субъединица К 2 Рканала представляет собой α-спираль с четырьмя трансмембранными сегментами, расположенными в цитоплазме N- и Cтерминалями, и двумя Рпетлями, формирующими пору. Б - ассоциация двух субъединиц в К 2 Р-канал. В - объемное изображение К 2 Р-канала. Г филогенетическое дерево для К 2 Р-каналов
 G-белок управляемые К-каналы (GIRK-каналы). • Некоторые каналы входящего выпрямления управляются Gбелками (GIRK 1, 2, 4). • Нейрональные GIRK-каналы вовлекаются в регуляцию возбудимости нейрона и могут вносить вклад в создание МП покоя.
G-белок управляемые К-каналы (GIRK-каналы). • Некоторые каналы входящего выпрямления управляются Gбелками (GIRK 1, 2, 4). • Нейрональные GIRK-каналы вовлекаются в регуляцию возбудимости нейрона и могут вносить вклад в создание МП покоя.
 АТФ-зависимые К-каналы (КАТФ-каналы). • К-каналы, нечувствительные к МП и управляемые цитозольной АТФ, называются КАТФ-каналами. Они были обнаружены в b-клетках поджелудочной железы, где играют ключевую роль в секреции инсулина, в кардиомиоцитах, скелетных и гладкомышечных клетках и некоторых нейронах. КАТФ-каналы показаны в адренергических нервных окончаниях крысы, ГАМК-ергических нервных окончаниях субстанции нигра крысы и холинергических двигательных нервных окончаниях мыши.
АТФ-зависимые К-каналы (КАТФ-каналы). • К-каналы, нечувствительные к МП и управляемые цитозольной АТФ, называются КАТФ-каналами. Они были обнаружены в b-клетках поджелудочной железы, где играют ключевую роль в секреции инсулина, в кардиомиоцитах, скелетных и гладкомышечных клетках и некоторых нейронах. КАТФ-каналы показаны в адренергических нервных окончаниях крысы, ГАМК-ергических нервных окончаниях субстанции нигра крысы и холинергических двигательных нервных окончаниях мыши.
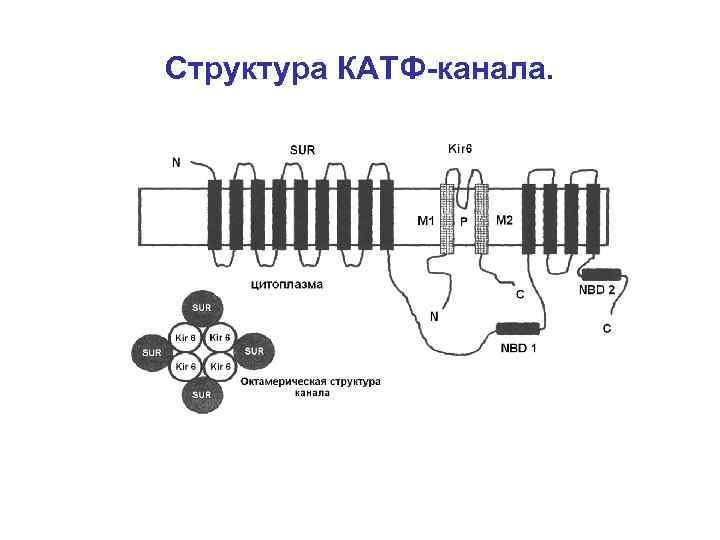 Структура КАТФ-канала.
Структура КАТФ-канала.
 Ca 2+-активируемые K+-каналы (KCa) • • КСа-каналы управляются не только потенциалом, но и внутриклеточной концентрацией ионов Са. КСа-токи обнаружены практически во всех нервных клетках (Зефиров, Халилов, Хамитов, 1987, Meir, Rahamimoff, 1999, Cowan, Sudhof, Stevens, 2000). Целый ряд токсинов эффективно влияют на функцию КСаканалов. К ним необходимо отнести токсины скорпиона харибдотоксин и ибериотоксин, апамин и бреветоксин-В. На основе биофизических и фармакологических свойств КСа-токи можно разделить на быстрые и медленные (Meir, Rahamimoff, 1999). Первые - активируются в течение миллисекунд, участвуют в реполяризации ПД. Медленные КСа-токи активируются с задержкой в несколько десятков миллисекунд, вносят вклад в следовую гиперполяризацию ПД По проводимости можно выделить КСа-каналы большой и малой проводимости. КСа-каналы большой проводимости (BK-каналы) имеют проводимость более 200 п. См, КСа-каналы малой проводимости (SK-каналы) имеют проводимость менее 100 п. См
Ca 2+-активируемые K+-каналы (KCa) • • КСа-каналы управляются не только потенциалом, но и внутриклеточной концентрацией ионов Са. КСа-токи обнаружены практически во всех нервных клетках (Зефиров, Халилов, Хамитов, 1987, Meir, Rahamimoff, 1999, Cowan, Sudhof, Stevens, 2000). Целый ряд токсинов эффективно влияют на функцию КСаканалов. К ним необходимо отнести токсины скорпиона харибдотоксин и ибериотоксин, апамин и бреветоксин-В. На основе биофизических и фармакологических свойств КСа-токи можно разделить на быстрые и медленные (Meir, Rahamimoff, 1999). Первые - активируются в течение миллисекунд, участвуют в реполяризации ПД. Медленные КСа-токи активируются с задержкой в несколько десятков миллисекунд, вносят вклад в следовую гиперполяризацию ПД По проводимости можно выделить КСа-каналы большой и малой проводимости. КСа-каналы большой проводимости (BK-каналы) имеют проводимость более 200 п. См, КСа-каналы малой проводимости (SK-каналы) имеют проводимость менее 100 п. См
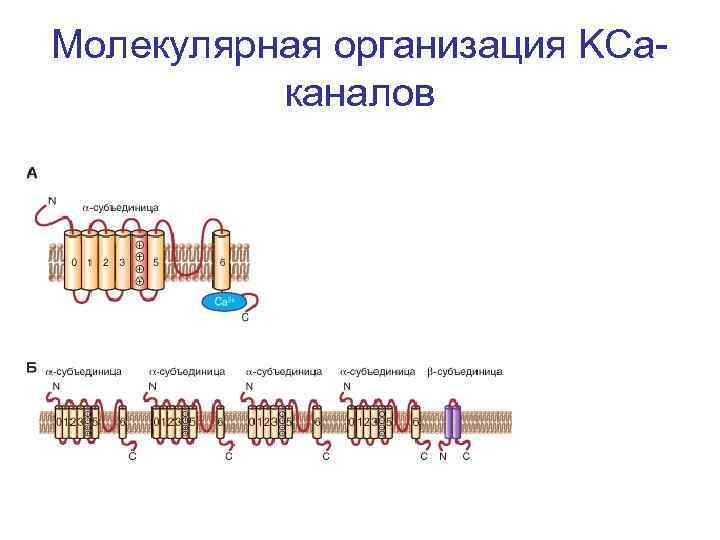 Молекулярная организация KCaканалов
Молекулярная организация KCaканалов
 Хлорные каналы • Ионы С 1 являются наиболее распространенными вне- и внутриклеточными анионами. С 1 -каналы присутствуют в плазматической мембране большинства клеток, играя важную роль в регуляции клеточного объема, трансэпителиального транспорта, секреции секреторных желез, стабилизации МП. В клетках животных концентрация Cl в цитоплазме ниже, чем во внеклеточной среде, а равновесный хлорный потенциал находится вблизи МП покоя. • • • Лиганд-активируемые Сl-каналы: ГАМК-активируемые Сl-каналы. Глицин-активируемые Сl-каналы. Кальций-активируемые Сl-каналы (Сl. Са-каналы). Потенциал-активируемые Cl-каналы (Cl. C).
Хлорные каналы • Ионы С 1 являются наиболее распространенными вне- и внутриклеточными анионами. С 1 -каналы присутствуют в плазматической мембране большинства клеток, играя важную роль в регуляции клеточного объема, трансэпителиального транспорта, секреции секреторных желез, стабилизации МП. В клетках животных концентрация Cl в цитоплазме ниже, чем во внеклеточной среде, а равновесный хлорный потенциал находится вблизи МП покоя. • • • Лиганд-активируемые Сl-каналы: ГАМК-активируемые Сl-каналы. Глицин-активируемые Сl-каналы. Кальций-активируемые Сl-каналы (Сl. Са-каналы). Потенциал-активируемые Cl-каналы (Cl. C).
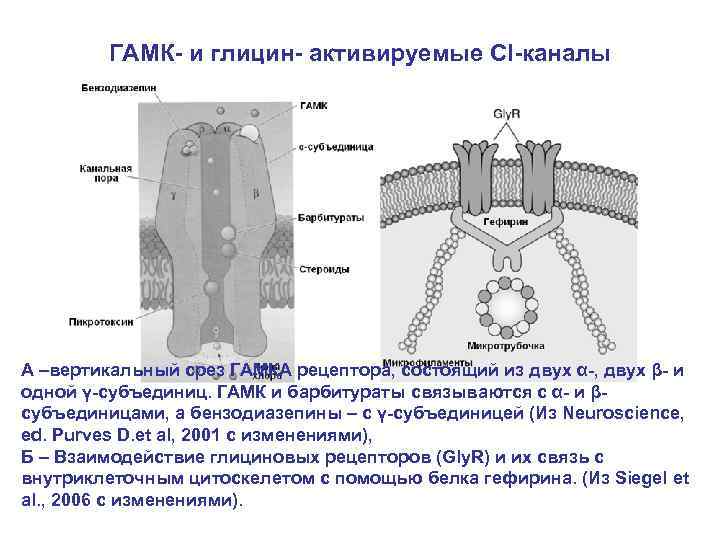 ГАМК- и глицин- активируемые Cl-каналы А –вертикальный срез ГАМКА рецептора, состоящий из двух α-, двух β- и одной γ-субъединиц. ГАМК и барбитураты связываются с α- и βсубъединицами, а бензодиазепины – с γ-субъединицей (Из Neuroscience, ed. Purves D. et al, 2001 с изменениями), Б – Взаимодействие глициновых рецепторов (Gly. R) и их связь с внутриклеточным цитоскелетом с помощью белка гефирина. (Из Siegel et al. , 2006 с изменениями).
ГАМК- и глицин- активируемые Cl-каналы А –вертикальный срез ГАМКА рецептора, состоящий из двух α-, двух β- и одной γ-субъединиц. ГАМК и барбитураты связываются с α- и βсубъединицами, а бензодиазепины – с γ-субъединицей (Из Neuroscience, ed. Purves D. et al, 2001 с изменениями), Б – Взаимодействие глициновых рецепторов (Gly. R) и их связь с внутриклеточным цитоскелетом с помощью белка гефирина. (Из Siegel et al. , 2006 с изменениями).
 ГАМК-активируемые Сl-каналы. • ГАМК является основным тормозным медиатором в ЦНС (Зефиров, Хазипов, Бен-Ари, 1998). Ее роль была впервые описана в нервной системе беспозвоночных. • Эффекты ГАМК реализуются через ГАМКА, ГАМКВ и ГАМКС –рецепторы, из которых ГАМКА и ГАМКС являются ионотропными, то есть формирующие ионный канал.
ГАМК-активируемые Сl-каналы. • ГАМК является основным тормозным медиатором в ЦНС (Зефиров, Хазипов, Бен-Ари, 1998). Ее роль была впервые описана в нервной системе беспозвоночных. • Эффекты ГАМК реализуются через ГАМКА, ГАМКВ и ГАМКС –рецепторы, из которых ГАМКА и ГАМКС являются ионотропными, то есть формирующие ионный канал.
 Глицин-активируемые Сl-каналы. • Известно, что глицин присутствует в ЦНС, являясь тормозным медиатором. Было показано, что глицин ингибирует освобождение медиатора в культуре гранулярных клеток мозжечка. Глицин-активируемые Сl-каналы были продемонстрированы в синаптонейросомах различных отделов мозга крысы, где аппликация глицина вызывает вход Cl, который блокируется стрихнином – ингибитором постсинаптических глицин-активируемых каналов.
Глицин-активируемые Сl-каналы. • Известно, что глицин присутствует в ЦНС, являясь тормозным медиатором. Было показано, что глицин ингибирует освобождение медиатора в культуре гранулярных клеток мозжечка. Глицин-активируемые Сl-каналы были продемонстрированы в синаптонейросомах различных отделов мозга крысы, где аппликация глицина вызывает вход Cl, который блокируется стрихнином – ингибитором постсинаптических глицин-активируемых каналов.
 Сl. Са-каналы • Сl-каналы, активируемые внутриклеточным кальцием, обнаружены во многих клеточных типах, включая эпителиальные, нервные, гладкомышечные, кардиальные (Jentsch, Thomas, 2002). • Сl. Са-каналы участвуют в регуляции клеточного объема многих клетках. В нейронах и мышечных клетках Сl. Са-каналы могут модулировать возбудимость, за счет генерации следовых потенциалов. В обонятельных нейронах Сl. Са-каналы участвуют в трансдукции, так как активируются ионами Са, входящими через ц. ГМФ-активируемые каналы.
Сl. Са-каналы • Сl-каналы, активируемые внутриклеточным кальцием, обнаружены во многих клеточных типах, включая эпителиальные, нервные, гладкомышечные, кардиальные (Jentsch, Thomas, 2002). • Сl. Са-каналы участвуют в регуляции клеточного объема многих клетках. В нейронах и мышечных клетках Сl. Са-каналы могут модулировать возбудимость, за счет генерации следовых потенциалов. В обонятельных нейронах Сl. Са-каналы участвуют в трансдукции, так как активируются ионами Са, входящими через ц. ГМФ-активируемые каналы.
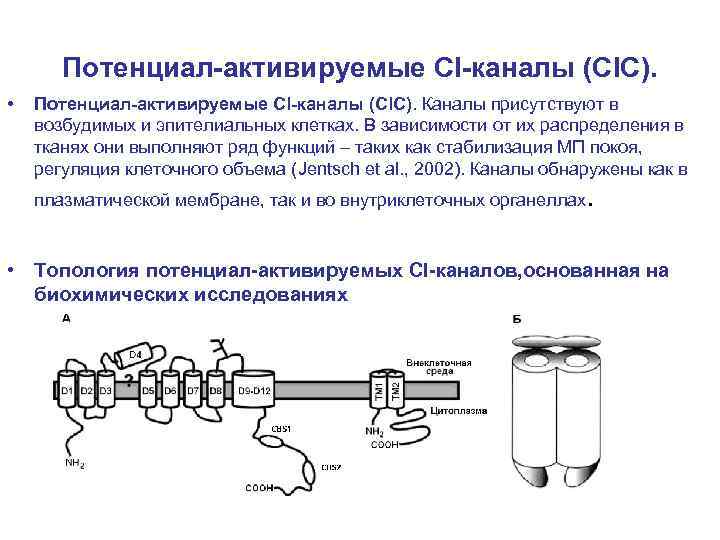 Потенциал-активируемые Cl-каналы (Cl. C). • Потенциал-активируемые Cl-каналы (Cl. C). Каналы присутствуют в возбудимых и эпителиальных клетках. В зависимости от их распределения в тканях они выполняют ряд функций – таких как стабилизация МП покоя, регуляция клеточного объема (Jentsch et al. , 2002). Каналы обнаружены как в плазматической мембране, так и во внутриклеточных органеллах. • Топология потенциал-активируемых Cl-каналов, основанная на биохимических исследованиях
Потенциал-активируемые Cl-каналы (Cl. C). • Потенциал-активируемые Cl-каналы (Cl. C). Каналы присутствуют в возбудимых и эпителиальных клетках. В зависимости от их распределения в тканях они выполняют ряд функций – таких как стабилизация МП покоя, регуляция клеточного объема (Jentsch et al. , 2002). Каналы обнаружены как в плазматической мембране, так и во внутриклеточных органеллах. • Топология потенциал-активируемых Cl-каналов, основанная на биохимических исследованиях
 Каналы синаптических везикул • В синаптических везикулах, изолированных из нервных окончаний электрического органа Torpedo и нейросекреторных терминалей гипофиза, были идентифицированы несколько типов ионных каналов. Большая часть каналов везикул неселективны. • Некоторые каналы являются потенциал-активируемыми или Саактивируемыми. В мембране синаптических везикул обнаружены Сl-каналы низкой проводимости и неселективные каналы, проводящие ионы К и С 1 и активирующиеся при изменении МП и повышении Са. • Материал лекции: Молекулярные основы синаптической передачи возбуждения.
Каналы синаптических везикул • В синаптических везикулах, изолированных из нервных окончаний электрического органа Torpedo и нейросекреторных терминалей гипофиза, были идентифицированы несколько типов ионных каналов. Большая часть каналов везикул неселективны. • Некоторые каналы являются потенциал-активируемыми или Саактивируемыми. В мембране синаптических везикул обнаружены Сl-каналы низкой проводимости и неселективные каналы, проводящие ионы К и С 1 и активирующиеся при изменении МП и повышении Са. • Материал лекции: Молекулярные основы синаптической передачи возбуждения.
 Спасибо за внимание!
Спасибо за внимание!


