Молекулярная физика (лекция).ppt
- Количество слайдов: 18
 Молекулярная физика (лекция) МКОУ СОШ № 1 Г. Н. Гудова
Молекулярная физика (лекция) МКОУ СОШ № 1 Г. Н. Гудова
 Содержание • • Основные понятия Основы МКТ Идеальный газ Газовые законы Законы термодинамики КПД Агрегатные состояния вещества Влажность воздуха
Содержание • • Основные понятия Основы МКТ Идеальный газ Газовые законы Законы термодинамики КПД Агрегатные состояния вещества Влажность воздуха
 Молекулярная физика. Основные понятия. Атом Молекула Идеальный газ Диффузия Броуновское движение • Макропараметры • Микропараметры • Температура • • • Основные положения МКТ • Масса молекулы • Относительная молекулярная масса • Молярная масса • Количество вещества • Число Авогадро • ИЗОпроцессы
Молекулярная физика. Основные понятия. Атом Молекула Идеальный газ Диффузия Броуновское движение • Макропараметры • Микропараметры • Температура • • • Основные положения МКТ • Масса молекулы • Относительная молекулярная масса • Молярная масса • Количество вещества • Число Авогадро • ИЗОпроцессы
 Три положения МКТ • • 1. Все вещества состоят из частиц - молекул, атомов и ионов. Молекула – мельчайшая частица вещества. Молекулы состоят из атомов. Атомы имеют сложную структуру, они состоят из элементарных частиц - протонов, нейтронов, входящих в состав ядра атома, электронов, а также других элементарных частиц. Атомы могут объединяться в молекулы, а могут быть вещества, состоящие только из атомов. Атомы в целом электронейтральны. Атомы, имеющие избыток или недостаток электронов называются ионами. Косвенным доказательством того, что вещества состоят из частиц является растворение краски в воде, изменение объема при нагревании и охлаждении
Три положения МКТ • • 1. Все вещества состоят из частиц - молекул, атомов и ионов. Молекула – мельчайшая частица вещества. Молекулы состоят из атомов. Атомы имеют сложную структуру, они состоят из элементарных частиц - протонов, нейтронов, входящих в состав ядра атома, электронов, а также других элементарных частиц. Атомы могут объединяться в молекулы, а могут быть вещества, состоящие только из атомов. Атомы в целом электронейтральны. Атомы, имеющие избыток или недостаток электронов называются ионами. Косвенным доказательством того, что вещества состоят из частиц является растворение краски в воде, изменение объема при нагревании и охлаждении
 Три положения МКТ 2. Частицы вещества беспрерывно и беспорядочно движутся • • Расстояние между атомами или молекулами газа во много раз больше размеров самих молекул. Молекулы в газе движутся хаотично с большими скоростями (сотни м/с). Сталкиваясь, они отскакивают друг от друга как абсолютно упругие шарики, изменяя величину и направление скоростей. Силы притяжения малы и не способны удержать молекулы газа друг возле друга. Газы легко сжимаются, Газы не сохраняют ни формы, ни объема. Они могут неограниченно расширяться и занимать весь предоставленный объем. Многочисленные удары молекул о стенки сосуда создают давление газа. Молекулы жидкости расположены почти вплотную друг к другу. Жидкости очень плохо сжимаются и сохраняют свой объем. Жидкости текучи, не сохраняют своей формы и принимают форму сосуда, в который налиты. Молекулы совершают колебания около положения равновесия но время от времени совершают переходы из одного оседлого состояния в другое, как правило, в направлении действия внешней силы. Атомы и молекулы твердых тел колеблются около определенных положений равновесия. Твердые тела сохраняют и объем, и форму. Если мысленно соединить центры положений равновесия атомов или ионов твердого тела, то получится кристаллическая решетка. Доказательством того, что частицы беспорядочно движутся является броуновское движение и диффузия.
Три положения МКТ 2. Частицы вещества беспрерывно и беспорядочно движутся • • Расстояние между атомами или молекулами газа во много раз больше размеров самих молекул. Молекулы в газе движутся хаотично с большими скоростями (сотни м/с). Сталкиваясь, они отскакивают друг от друга как абсолютно упругие шарики, изменяя величину и направление скоростей. Силы притяжения малы и не способны удержать молекулы газа друг возле друга. Газы легко сжимаются, Газы не сохраняют ни формы, ни объема. Они могут неограниченно расширяться и занимать весь предоставленный объем. Многочисленные удары молекул о стенки сосуда создают давление газа. Молекулы жидкости расположены почти вплотную друг к другу. Жидкости очень плохо сжимаются и сохраняют свой объем. Жидкости текучи, не сохраняют своей формы и принимают форму сосуда, в который налиты. Молекулы совершают колебания около положения равновесия но время от времени совершают переходы из одного оседлого состояния в другое, как правило, в направлении действия внешней силы. Атомы и молекулы твердых тел колеблются около определенных положений равновесия. Твердые тела сохраняют и объем, и форму. Если мысленно соединить центры положений равновесия атомов или ионов твердого тела, то получится кристаллическая решетка. Доказательством того, что частицы беспорядочно движутся является броуновское движение и диффузия.
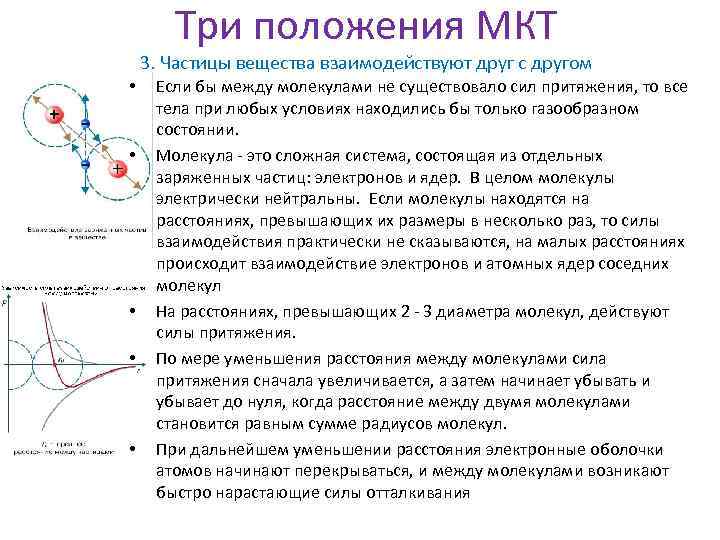 Три положения МКТ 3. Частицы вещества взаимодействуют друг с другом • • • Если бы между молекулами не существовало сил притяжения, то все тела при любых условиях находились бы только газообразном состоянии. Молекула - это сложная система, состоящая из отдельных заряженных частиц: электронов и ядер. В целом молекулы электрически нейтральны. Если молекулы находятся на расстояниях, превышающих их размеры в несколько раз, то силы взаимодействия практически не сказываются, на малых расстояниях происходит взаимодействие электронов и атомных ядер соседних молекул На расстояниях, превышающих 2 - 3 диаметра молекул, действуют силы притяжения. По мере уменьшения расстояния между молекулами сила притяжения сначала увеличивается, а затем начинает убывать и убывает до нуля, когда расстояние между двумя молекулами становится равным сумме радиусов молекул. При дальнейшем уменьшении расстояния электронные оболочки атомов начинают перекрываться, и между молекулами возникают быстро нарастающие силы отталкивания
Три положения МКТ 3. Частицы вещества взаимодействуют друг с другом • • • Если бы между молекулами не существовало сил притяжения, то все тела при любых условиях находились бы только газообразном состоянии. Молекула - это сложная система, состоящая из отдельных заряженных частиц: электронов и ядер. В целом молекулы электрически нейтральны. Если молекулы находятся на расстояниях, превышающих их размеры в несколько раз, то силы взаимодействия практически не сказываются, на малых расстояниях происходит взаимодействие электронов и атомных ядер соседних молекул На расстояниях, превышающих 2 - 3 диаметра молекул, действуют силы притяжения. По мере уменьшения расстояния между молекулами сила притяжения сначала увеличивается, а затем начинает убывать и убывает до нуля, когда расстояние между двумя молекулами становится равным сумме радиусов молекул. При дальнейшем уменьшении расстояния электронные оболочки атомов начинают перекрываться, и между молекулами возникают быстро нарастающие силы отталкивания
 Броуновское движение. • Броуновское движение - это тепловое движение мельчайших • • • частиц, взвешенных в жидкости или газе. Было открыто английским ботаником Броуном (1827 г. ) и явилось наглядным доказательством хаотичного молекулярного движения. Броуновские частицы движутся под влиянием нескомпенсированных ударов молекул. Из-за хаотичности теплового движения молекул частицы беспорядочно движутся меняется скорость по величине и направлению, а ее траектория представляет собой сложную зигзагообразную линию. Диффузия • Взаимное проникновение молекул одного вещества в • • промежутки между молекулами другого вещества при их взаимном соприкосновении Быстрее всего происходит в газах Скорость диффузии увеличивается при повышении температуры
Броуновское движение. • Броуновское движение - это тепловое движение мельчайших • • • частиц, взвешенных в жидкости или газе. Было открыто английским ботаником Броуном (1827 г. ) и явилось наглядным доказательством хаотичного молекулярного движения. Броуновские частицы движутся под влиянием нескомпенсированных ударов молекул. Из-за хаотичности теплового движения молекул частицы беспорядочно движутся меняется скорость по величине и направлению, а ее траектория представляет собой сложную зигзагообразную линию. Диффузия • Взаимное проникновение молекул одного вещества в • • промежутки между молекулами другого вещества при их взаимном соприкосновении Быстрее всего происходит в газах Скорость диффузии увеличивается при повышении температуры
 Масса молекулы • • В силу того, что массы частиц вещества крайне малы, удобно пользоваться не абсолютными, а относительными единицами массы. Для этого используется так называемая атомная единица массы (а. е. м. ), равная 1/12 массы атома углерода. Массу частицы, измеренную в а. е. м. принято называть относительной атомной (или молекулярной) массой (Mr). Значения относительных атомных масс приведены в периодической системе химических элементов Д. И. Менделеева. Относительная молекулярная масса молекулы вещества равна сумме относительных атомных масс атомов, составляющих данную молекулу. Экспериментально установлено, что 1 а. е. м. = 1, 66· 10 -27 кг. В Международной системе СИ для измерения количества вещества (v) введена специальная единица - моль. 1 моль - это количество вещества, в котором содержится столько же частиц, сколько атомов содержится в 12 граммах углерода. Постоянная Авогадро численно равна количеству частиц, содержащихся в 1 моле любого вещества: NA= 6 · 1023 моль -1 Масса 1 моля вещества называется молярной массой (М).
Масса молекулы • • В силу того, что массы частиц вещества крайне малы, удобно пользоваться не абсолютными, а относительными единицами массы. Для этого используется так называемая атомная единица массы (а. е. м. ), равная 1/12 массы атома углерода. Массу частицы, измеренную в а. е. м. принято называть относительной атомной (или молекулярной) массой (Mr). Значения относительных атомных масс приведены в периодической системе химических элементов Д. И. Менделеева. Относительная молекулярная масса молекулы вещества равна сумме относительных атомных масс атомов, составляющих данную молекулу. Экспериментально установлено, что 1 а. е. м. = 1, 66· 10 -27 кг. В Международной системе СИ для измерения количества вещества (v) введена специальная единица - моль. 1 моль - это количество вещества, в котором содержится столько же частиц, сколько атомов содержится в 12 граммах углерода. Постоянная Авогадро численно равна количеству частиц, содержащихся в 1 моле любого вещества: NA= 6 · 1023 моль -1 Масса 1 моля вещества называется молярной массой (М).
 Основные формулы
Основные формулы
 Идеальный газ. Основное уравнение МКТ. Для выяснения наиболее общих свойств, присущих всем газам, используют упрощенную модель реальных газов - идеальный газ. Основные отличия идеального газа от реального газа: 1. Частицы идеального газа - сферические тела очень малых размеров, практически материальные точки. 2. Между частицами отсутствуют силы межмолекулярного взаимодействия. 3. Соударения частиц являются абсолютно упругими. Реальные разреженные газы действительно ведут себя подобно идеальному газу.
Идеальный газ. Основное уравнение МКТ. Для выяснения наиболее общих свойств, присущих всем газам, используют упрощенную модель реальных газов - идеальный газ. Основные отличия идеального газа от реального газа: 1. Частицы идеального газа - сферические тела очень малых размеров, практически материальные точки. 2. Между частицами отсутствуют силы межмолекулярного взаимодействия. 3. Соударения частиц являются абсолютно упругими. Реальные разреженные газы действительно ведут себя подобно идеальному газу.
 Температура. Абсолютная шкала температур. • • Тепловым равновесием называют такое состояние, при котором все макроскопические параметры в системе сколь угодно долго остаются неизменными. Это означает, что в системе не меняются объем и давление, не изменяются агрегатные состояния вещества, концентрации веществ. Температура характеризует состояние теплового равновесия системы тел: все тела, находящиеся в тепловом равновесии имеют одну и ту же температуру. Давление газа прямо пропорционально температуре. Температура – мера средней кинетической энергии движения молекул Предельную температуру, при которой давление идеального газа обращается в нуль при фиксированном объеме или объем идеального газа стремится к нулю при неизменном давлении, называют абсолютным нулем температуры Ниже этой температуры быть уже не может Связь между абсолютной температурой и температурой по шкале Цельсия выражается зависимостью: T = t + 273 K 1 К по величине равен 10 С
Температура. Абсолютная шкала температур. • • Тепловым равновесием называют такое состояние, при котором все макроскопические параметры в системе сколь угодно долго остаются неизменными. Это означает, что в системе не меняются объем и давление, не изменяются агрегатные состояния вещества, концентрации веществ. Температура характеризует состояние теплового равновесия системы тел: все тела, находящиеся в тепловом равновесии имеют одну и ту же температуру. Давление газа прямо пропорционально температуре. Температура – мера средней кинетической энергии движения молекул Предельную температуру, при которой давление идеального газа обращается в нуль при фиксированном объеме или объем идеального газа стремится к нулю при неизменном давлении, называют абсолютным нулем температуры Ниже этой температуры быть уже не может Связь между абсолютной температурой и температурой по шкале Цельсия выражается зависимостью: T = t + 273 K 1 К по величине равен 10 С
 Основные формулы • Давление • Энергия • Скорость
Основные формулы • Давление • Энергия • Скорость
 Парциальное давление • • Если идеальный газ является смесью нескольких газов, то согласно закону Дальтона, давление смеси идеальных газов равно сумме парциальных давлений входящих в нее газов. Парциальное давление - это такое давление, которое производил бы газ, если бы он один занимал весь объем, равный объему смеси
Парциальное давление • • Если идеальный газ является смесью нескольких газов, то согласно закону Дальтона, давление смеси идеальных газов равно сумме парциальных давлений входящих в нее газов. Парциальное давление - это такое давление, которое производил бы газ, если бы он один занимал весь объем, равный объему смеси
 Уравнение Менделеева - Клапейрона • Изопроцессы – процессы, происходящий при какой-нибудь постоянной величине: P, V или Т.
Уравнение Менделеева - Клапейрона • Изопроцессы – процессы, происходящий при какой-нибудь постоянной величине: P, V или Т.
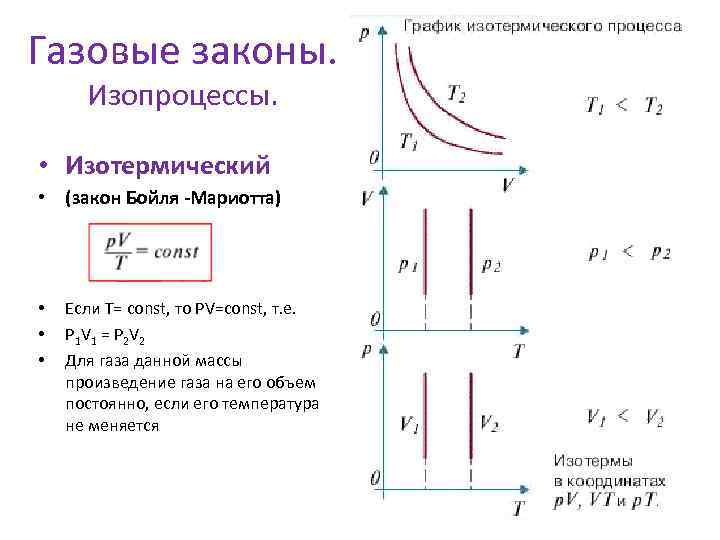 Газовые законы. Изопроцессы. • Изотермический • (закон Бойля -Мариотта) • • • Если Т= const, то PV=const, т. е. P 1 V 1 = P 2 V 2 Для газа данной массы произведение газа на его объем постоянно, если его температура не меняется
Газовые законы. Изопроцессы. • Изотермический • (закон Бойля -Мариотта) • • • Если Т= const, то PV=const, т. е. P 1 V 1 = P 2 V 2 Для газа данной массы произведение газа на его объем постоянно, если его температура не меняется
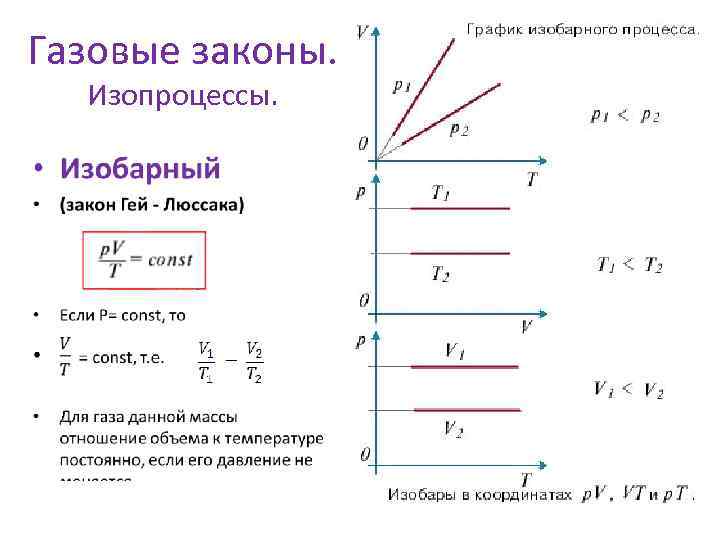 Газовые законы. Изопроцессы. •
Газовые законы. Изопроцессы. •
 Газовые законы. Изопроцессы. •
Газовые законы. Изопроцессы. •
 • Задачи
• Задачи


