Молекулярная физика и термодинамика.pptx
- Количество слайдов: 66
 Молекулярная физика и термодинамика
Молекулярная физика и термодинамика
 Молекулярная физика и термодинамика • – это по существу две разные по своим подходам, но тесно связанные науки, занимающиеся одним и тем же – изучением макроскопических свойств физических систем, но совершенно разными методами
Молекулярная физика и термодинамика • – это по существу две разные по своим подходам, но тесно связанные науки, занимающиеся одним и тем же – изучением макроскопических свойств физических систем, но совершенно разными методами
 Молекулярная физика • В основе молекулярной физики или молекулярнокинетической теории лежат определенные представления о строении вещества. – Для установления законов поведения макроскопических систем, состоящих из огромного числа частиц, в молекулярной физике используются различные модели вещества, например, модели идеального газа. • Молекулярная физика является статистической теорией, физика т. е. теорией, которая рассматривает поведение систем, состоящих из огромного числа частиц (атомов, молекул), на основе вероятностных моделей. Она стремится на основе статистического подхода установить связь между связь экспериментально измеренными макроскопическими величинами (давление, объем, температура и т. д. ) и величинами микроскопическими характеристиками частиц, входящих микроскопическими характеристиками в состав системы (масса, импульс, энергия и т. д. ).
Молекулярная физика • В основе молекулярной физики или молекулярнокинетической теории лежат определенные представления о строении вещества. – Для установления законов поведения макроскопических систем, состоящих из огромного числа частиц, в молекулярной физике используются различные модели вещества, например, модели идеального газа. • Молекулярная физика является статистической теорией, физика т. е. теорией, которая рассматривает поведение систем, состоящих из огромного числа частиц (атомов, молекул), на основе вероятностных моделей. Она стремится на основе статистического подхода установить связь между связь экспериментально измеренными макроскопическими величинами (давление, объем, температура и т. д. ) и величинами микроскопическими характеристиками частиц, входящих микроскопическими характеристиками в состав системы (масса, импульс, энергия и т. д. ).
 Термодинамика • В отличие от молекулярно-кинетической теории, термодинамика при изучении свойств термодинамика макроскопических систем не опирается ни на какие представления о молекулярной структуре вещества. Термодинамика является наукой феноменологической. – Она делает выводы о свойствах вещества на основе законов, установленных на опыте, таких, как закон сохранения энергии. Термодинамика оперирует только с макроскопическими величинами (давление, температура, объем и т. п. ), которые вводятся на основе физического эксперимента.
Термодинамика • В отличие от молекулярно-кинетической теории, термодинамика при изучении свойств термодинамика макроскопических систем не опирается ни на какие представления о молекулярной структуре вещества. Термодинамика является наукой феноменологической. – Она делает выводы о свойствах вещества на основе законов, установленных на опыте, таких, как закон сохранения энергии. Термодинамика оперирует только с макроскопическими величинами (давление, температура, объем и т. п. ), которые вводятся на основе физического эксперимента.
 • Оба подхода – термодинамический и статистический – не противоречат, а дополняют друга. • Только совместное использование термодинамики и молекулярнокинетической теории может дать наиболее полное представление о свойствах систем, состоящих из большого числа частиц
• Оба подхода – термодинамический и статистический – не противоречат, а дополняют друга. • Только совместное использование термодинамики и молекулярнокинетической теории может дать наиболее полное представление о свойствах систем, состоящих из большого числа частиц
 Молекулярная физика • Молекулярно-кинетическая теория –– учение о строении и свойствах вещества на основе представления о существовании атомов и молекул как наименьших частиц химических веществ.
Молекулярная физика • Молекулярно-кинетическая теория –– учение о строении и свойствах вещества на основе представления о существовании атомов и молекул как наименьших частиц химических веществ.
 Молекулярно-кинетическая теория Основные положения МКТ 1. Все вещества – жидкие, твердые и газообразные – образованы из мельчайших частиц – молекул, которые сами состоят из атомов ( «элементарных молекул» ). Молекулы химического вещества могут быть простыми и сложными, т. е. состоять из одного или нескольких атомов. Молекулы и атомы представляют собой электрически нейтральные частицы. При определенных условиях молекулы и атомы могут приобретать дополнительный электрический заряд и превращаться в положительные или отрицательные ионы. 2. Атомы и молекулы находятся в непрерывном хаотическом движении, которое называют тепловым движением 3. Частицы взаимодействуют друг с другом силами, имеющими электрическую природу. Гравитационное взаимодействие между частицами пренебрежимо мало.
Молекулярно-кинетическая теория Основные положения МКТ 1. Все вещества – жидкие, твердые и газообразные – образованы из мельчайших частиц – молекул, которые сами состоят из атомов ( «элементарных молекул» ). Молекулы химического вещества могут быть простыми и сложными, т. е. состоять из одного или нескольких атомов. Молекулы и атомы представляют собой электрически нейтральные частицы. При определенных условиях молекулы и атомы могут приобретать дополнительный электрический заряд и превращаться в положительные или отрицательные ионы. 2. Атомы и молекулы находятся в непрерывном хаотическом движении, которое называют тепловым движением 3. Частицы взаимодействуют друг с другом силами, имеющими электрическую природу. Гравитационное взаимодействие между частицами пренебрежимо мало.
 Молекулярно-кинетическая теория • Наиболее ярким экспериментальным подтверждением представлений молекулярно-кинетической теории о беспорядочном движении атомов и молекул является броуновское движение. • Броуновское движение –– это тепловое движение мельчайших микроскопических частиц, взвешенных в жидкости или газе. • Оно было открыто английским ботаником Р. Броуном в 1827 г. Броуновские частицы движутся под влиянием беспорядочных ударов молекул. Из-за хаотического теплового движения молекул эти удары никогда не уравновешивают друга. В результате скорость броуновской частицы беспорядочно меняется по модулю и направлению, а ее траектория представляет собой сложную зигзагообразную кривую (рис. ). Теория броуновского движения была создана А. Эйнштейном в 1905 г. Экспериментально теория Эйнштейна была подтверждена в опытах французского физика Ж. Перрена, проведенных в 1908– 1911 гг.
Молекулярно-кинетическая теория • Наиболее ярким экспериментальным подтверждением представлений молекулярно-кинетической теории о беспорядочном движении атомов и молекул является броуновское движение. • Броуновское движение –– это тепловое движение мельчайших микроскопических частиц, взвешенных в жидкости или газе. • Оно было открыто английским ботаником Р. Броуном в 1827 г. Броуновские частицы движутся под влиянием беспорядочных ударов молекул. Из-за хаотического теплового движения молекул эти удары никогда не уравновешивают друга. В результате скорость броуновской частицы беспорядочно меняется по модулю и направлению, а ее траектория представляет собой сложную зигзагообразную кривую (рис. ). Теория броуновского движения была создана А. Эйнштейном в 1905 г. Экспериментально теория Эйнштейна была подтверждена в опытах французского физика Ж. Перрена, проведенных в 1908– 1911 гг.
 Молекулярно-кинетическая теория • Постоянное хаотичное движение молекул вещества проявляется также в другом легко наблюдаемом явлении – диффузии. • Диффузией называется явление проникновения двух или нескольких соприкасающихся веществ друга. – Наиболее быстро процесс протекает в газе, если он газе неоднороден по составу. Диффузия приводит к образованию однородной смеси независимо от плотности компонентов. Так, если в двух частях сосуда, разделенных перегородкой, находятся кислород O 2 и водород H 2, то после удаления перегородки начинается процесс взаимопроникновения газов друга, приводящий к образованию взрывоопасной смеси – гремучего газа. Этот процесс идет и в том случае, когда легкий газ (водород) находится в верхней половине сосуда, а более тяжелый (кислород) – в нижней.
Молекулярно-кинетическая теория • Постоянное хаотичное движение молекул вещества проявляется также в другом легко наблюдаемом явлении – диффузии. • Диффузией называется явление проникновения двух или нескольких соприкасающихся веществ друга. – Наиболее быстро процесс протекает в газе, если он газе неоднороден по составу. Диффузия приводит к образованию однородной смеси независимо от плотности компонентов. Так, если в двух частях сосуда, разделенных перегородкой, находятся кислород O 2 и водород H 2, то после удаления перегородки начинается процесс взаимопроникновения газов друга, приводящий к образованию взрывоопасной смеси – гремучего газа. Этот процесс идет и в том случае, когда легкий газ (водород) находится в верхней половине сосуда, а более тяжелый (кислород) – в нижней.
 Молекулярно-кинетическая теория – Значительно медленнее протекают подобные процессы в жидкостях. Взаимопроникновение двух жидкостях разнородных жидкостей друг в друга, растворение твердых веществ в жидкостях (например, сахара в воде) и образование однородных растворов – примеры диффузионных процессов в жидкостях. В реальных условиях диффузия в жидкостях и газах маскируется более быстрыми процессами перемешивания, например, из-за возникновения конвекционных потоков.
Молекулярно-кинетическая теория – Значительно медленнее протекают подобные процессы в жидкостях. Взаимопроникновение двух жидкостях разнородных жидкостей друг в друга, растворение твердых веществ в жидкостях (например, сахара в воде) и образование однородных растворов – примеры диффузионных процессов в жидкостях. В реальных условиях диффузия в жидкостях и газах маскируется более быстрыми процессами перемешивания, например, из-за возникновения конвекционных потоков.
 Молекулярно-кинетическая теория – Наиболее медленно процесс диффузии протекает в твердых телах. Однако, опыты показывают, что при твердых телах контакте хорошо очищенных поверхностей двух металлов через длительное время в каждом из них обнаруживается атомы другого металла. • Диффузия и броуновское движение – Диффузия и броуновское движение родственные явления. Взаимопроникновение соприкасающихся веществ друга и беспорядочное движение мельчайших частиц, взвешенных в жидкости или газе, происходят вследствие хаотичного теплового движения молекул.
Молекулярно-кинетическая теория – Наиболее медленно процесс диффузии протекает в твердых телах. Однако, опыты показывают, что при твердых телах контакте хорошо очищенных поверхностей двух металлов через длительное время в каждом из них обнаруживается атомы другого металла. • Диффузия и броуновское движение – Диффузия и броуновское движение родственные явления. Взаимопроникновение соприкасающихся веществ друга и беспорядочное движение мельчайших частиц, взвешенных в жидкости или газе, происходят вследствие хаотичного теплового движения молекул.
 Молекулярно-кинетическая теория • Силы, действующие между двумя молекулами, Силы, действующие между двумя молекулами зависят от расстояния между ними. • Молекулы представляют собой сложные пространственные структуры, содержащие как положительные, так и отрицательные заряды. Если расстояние между молекулами достаточно велико, то преобладают силы межмолекулярного притяжения. На малых расстояниях преобладают силы отталкивания.
Молекулярно-кинетическая теория • Силы, действующие между двумя молекулами, Силы, действующие между двумя молекулами зависят от расстояния между ними. • Молекулы представляют собой сложные пространственные структуры, содержащие как положительные, так и отрицательные заряды. Если расстояние между молекулами достаточно велико, то преобладают силы межмолекулярного притяжения. На малых расстояниях преобладают силы отталкивания.
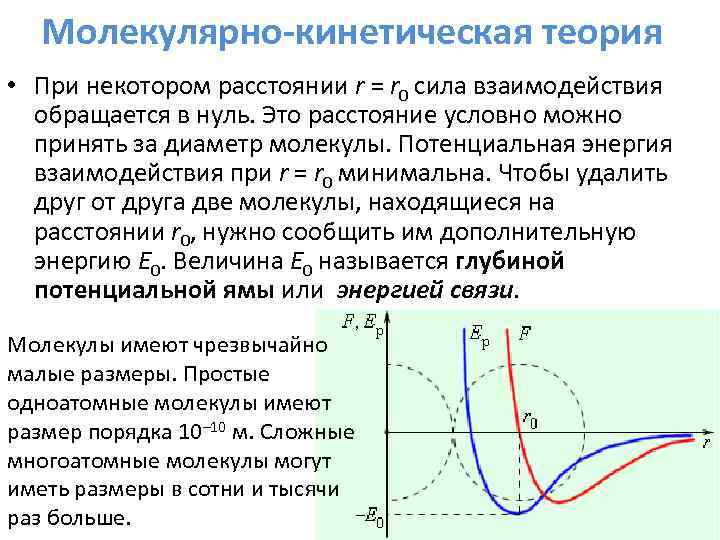 Молекулярно-кинетическая теория • При некотором расстоянии r = r 0 сила взаимодействия обращается в нуль. Это расстояние условно можно принять за диаметр молекулы. Потенциальная энергия взаимодействия при r = r 0 минимальна. Чтобы удалить друг от друга две молекулы, находящиеся на расстоянии r 0, нужно сообщить им дополнительную энергию E 0. Величина E 0 называется глубиной потенциальной ямы или энергией связи. Молекулы имеют чрезвычайно малые размеры. Простые одноатомные молекулы имеют размер порядка 10– 10 м. Сложные многоатомные молекулы могут иметь размеры в сотни и тысячи раз больше.
Молекулярно-кинетическая теория • При некотором расстоянии r = r 0 сила взаимодействия обращается в нуль. Это расстояние условно можно принять за диаметр молекулы. Потенциальная энергия взаимодействия при r = r 0 минимальна. Чтобы удалить друг от друга две молекулы, находящиеся на расстоянии r 0, нужно сообщить им дополнительную энергию E 0. Величина E 0 называется глубиной потенциальной ямы или энергией связи. Молекулы имеют чрезвычайно малые размеры. Простые одноатомные молекулы имеют размер порядка 10– 10 м. Сложные многоатомные молекулы могут иметь размеры в сотни и тысячи раз больше.
 Молекулярно-кинетическая теория • Кинетическая энергия теплового движения растет с возрастанием температуры • При низких температурах средняя кинетическая энергия молекулы может оказаться меньше глубины потенциальной ямы E 0. В этом случае молекулы конденсируются в жидкое или твердое вещество; при этом среднее расстояние между молекулами будет приблизительно равно r 0. • При повышении температуры средняя кинетическая энергия молекулы становится больше E 0, молекулы разлетаются, и образуется газообразное вещество
Молекулярно-кинетическая теория • Кинетическая энергия теплового движения растет с возрастанием температуры • При низких температурах средняя кинетическая энергия молекулы может оказаться меньше глубины потенциальной ямы E 0. В этом случае молекулы конденсируются в жидкое или твердое вещество; при этом среднее расстояние между молекулами будет приблизительно равно r 0. • При повышении температуры средняя кинетическая энергия молекулы становится больше E 0, молекулы разлетаются, и образуется газообразное вещество
 Молекулярно-кинетическая теория Агрегатные состояния вещества • В твердых телах молекулы совершают твердых телах беспорядочные колебания около фиксированных центров (положений равновесия). Эти центры могут быть расположены в пространстве нерегулярным образом (аморфные тела) или образовывать упорядоченные объемные структуры (кристаллические тела). • Поэтому твердые тела сохраняют и форму, и объем
Молекулярно-кинетическая теория Агрегатные состояния вещества • В твердых телах молекулы совершают твердых телах беспорядочные колебания около фиксированных центров (положений равновесия). Эти центры могут быть расположены в пространстве нерегулярным образом (аморфные тела) или образовывать упорядоченные объемные структуры (кристаллические тела). • Поэтому твердые тела сохраняют и форму, и объем
 Молекулярно-кинетическая теория Агрегатные состояния вещества • В жидкостях молекулы имеют значительно большую свободу для теплового движения. Они не привязаны к определенным центрам и могут перемещаться по всему объему. Этим объясняется текучесть жидкостей. Близко расположенные молекулы жидкости также могут образовывать упорядоченные структуры, содержащие несколько молекул. Это явление называется ближним порядком в отличие от дальнего порядка, характерного для кристаллических тел. • Поэтому жидкости • не сохраняют форму, • но сохраняют объем
Молекулярно-кинетическая теория Агрегатные состояния вещества • В жидкостях молекулы имеют значительно большую свободу для теплового движения. Они не привязаны к определенным центрам и могут перемещаться по всему объему. Этим объясняется текучесть жидкостей. Близко расположенные молекулы жидкости также могут образовывать упорядоченные структуры, содержащие несколько молекул. Это явление называется ближним порядком в отличие от дальнего порядка, характерного для кристаллических тел. • Поэтому жидкости • не сохраняют форму, • но сохраняют объем
 Молекулярно-кинетическая теория Агрегатные состояния вещества • В газах расстояния между молекулами обычно значительно больше их размеров. Силы взаимодействия между молекулами на таких больших расстояниях малы, и каждая молекула движется вдоль прямой линии до очередного столкновения с другой молекулой или со стенкой сосуда. – Среднее расстояние между молекулами воздуха при нормальных условиях порядка 10– 8 м, т. е. в десятки раз превышает размер молекул. Слабое взаимодействие между молекулами объясняет способность газов расширяться и заполнять весь объем сосуда. В пределе, когда взаимодействие стремится к нулю, мы приходим к представлению об идеальном газе. • Поэтому газы не сохраняют ни форму, ни объем
Молекулярно-кинетическая теория Агрегатные состояния вещества • В газах расстояния между молекулами обычно значительно больше их размеров. Силы взаимодействия между молекулами на таких больших расстояниях малы, и каждая молекула движется вдоль прямой линии до очередного столкновения с другой молекулой или со стенкой сосуда. – Среднее расстояние между молекулами воздуха при нормальных условиях порядка 10– 8 м, т. е. в десятки раз превышает размер молекул. Слабое взаимодействие между молекулами объясняет способность газов расширяться и заполнять весь объем сосуда. В пределе, когда взаимодействие стремится к нулю, мы приходим к представлению об идеальном газе. • Поэтому газы не сохраняют ни форму, ни объем
 Молекулярно-кинетическая теория Количество вещества • В молекулярно-кинетической теории количество вещества принято считать пропорциональным числу вещества частиц. Единица количества вещества называется молем (моль). • Моль – это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов 0, 012 кг углерода 12 C. • (Молекула углерода состоит из одного атома) • Таким образом, в одном моле любого вещества содержится одно и то же число частиц (молекул). • Это число называется постоянной Авогадро NА: NА = 6, 02· 1023 моль– 1. • Постоянная Авогадро – одна из важнейших постоянных в молекулярно-кинетической теории.
Молекулярно-кинетическая теория Количество вещества • В молекулярно-кинетической теории количество вещества принято считать пропорциональным числу вещества частиц. Единица количества вещества называется молем (моль). • Моль – это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов 0, 012 кг углерода 12 C. • (Молекула углерода состоит из одного атома) • Таким образом, в одном моле любого вещества содержится одно и то же число частиц (молекул). • Это число называется постоянной Авогадро NА: NА = 6, 02· 1023 моль– 1. • Постоянная Авогадро – одна из важнейших постоянных в молекулярно-кинетической теории.
 Молекулярно-кинетическая теория • Количество вещества ν определяется как отношение числа N частиц (молекул) вещества к постоянной Авогадро NА: • Массу одного моля вещества принято называть молярной массой M Молярная масса равна произведению массы m 0 одной молекулы данного вещества на постоянную Авогадро: M = NА · m 0 • Молярная масса выражается в килограммах на моль (кг/моль). Для веществ, молекулы которых состоят из одного атома, часто используется термин атомная масса. • За единицу массы атомов и молекул принимается 1/12 массы атома изотопа углерода 12 C (с массовым числом 12). • Эта единица называется атомной единицей массы(а. е. м. ): 1 а. е. м. = 1, 66· 10– 27 кг. • Эта величина почти совпадает с массой протона или нейтрона. Отношение массы атома или молекулы данного вещества к 1/12 массы атома углерода 12 C называется относительной массой.
Молекулярно-кинетическая теория • Количество вещества ν определяется как отношение числа N частиц (молекул) вещества к постоянной Авогадро NА: • Массу одного моля вещества принято называть молярной массой M Молярная масса равна произведению массы m 0 одной молекулы данного вещества на постоянную Авогадро: M = NА · m 0 • Молярная масса выражается в килограммах на моль (кг/моль). Для веществ, молекулы которых состоят из одного атома, часто используется термин атомная масса. • За единицу массы атомов и молекул принимается 1/12 массы атома изотопа углерода 12 C (с массовым числом 12). • Эта единица называется атомной единицей массы(а. е. м. ): 1 а. е. м. = 1, 66· 10– 27 кг. • Эта величина почти совпадает с массой протона или нейтрона. Отношение массы атома или молекулы данного вещества к 1/12 массы атома углерода 12 C называется относительной массой.
 Молекулярно-кинетическая теория • Простейшей моделью, рассматриваемой молекулярнокинетической теорией, является модель идеального газа: 1. В кинетической модели идеального газа молекулы 1. рассматриваются как идеально упругие шарики, взаимодействующие между собой и со стенками только во время упругих столкновений. 2. Суммарный объем всех молекул предполагается малым по 2. сравнению с объемом сосуда, в котором находится газ. • Модель идеального газа достаточно хорошо описывает поведение реальных газов в широком диапазоне давлений и температур. • Задача молекулярно-кинетической теории состоит в том, чтобы установить связь между микроскопическими (масса, микроскопическими скорость, кинетическая энергия молекул) и макроскопическими параметрами (давление, объем, макроскопическими параметрами температура).
Молекулярно-кинетическая теория • Простейшей моделью, рассматриваемой молекулярнокинетической теорией, является модель идеального газа: 1. В кинетической модели идеального газа молекулы 1. рассматриваются как идеально упругие шарики, взаимодействующие между собой и со стенками только во время упругих столкновений. 2. Суммарный объем всех молекул предполагается малым по 2. сравнению с объемом сосуда, в котором находится газ. • Модель идеального газа достаточно хорошо описывает поведение реальных газов в широком диапазоне давлений и температур. • Задача молекулярно-кинетической теории состоит в том, чтобы установить связь между микроскопическими (масса, микроскопическими скорость, кинетическая энергия молекул) и макроскопическими параметрами (давление, объем, макроскопическими параметрами температура).
 Молекулярно-кинетическая теория • В результате каждого столкновения между молекулами и молекул со стенками скорости молекул могут изменяться по модулю и по направлению; на интервалах времени между последовательными столкновениями молекулы движутся равномерно и прямолинейно. • В модели идеального газа предполагается, что все столкновения происходят по законам упругого удара, т. е. подчиняются законам механики Ньютона. • Используя модель идеального газа, вычислим давление газа на стенку сосуда. В процессе взаимодействия молекулы со стенкой сосуда между ними возникают силы, подчиняющиеся третьему закону Ньютона. В результате проекция υx скорости молекулы, перпендикулярная стенке, изменяет свой знак на противоположный, а проекция υy скорости, параллельная стенке, остается неизменной (рис. ).
Молекулярно-кинетическая теория • В результате каждого столкновения между молекулами и молекул со стенками скорости молекул могут изменяться по модулю и по направлению; на интервалах времени между последовательными столкновениями молекулы движутся равномерно и прямолинейно. • В модели идеального газа предполагается, что все столкновения происходят по законам упругого удара, т. е. подчиняются законам механики Ньютона. • Используя модель идеального газа, вычислим давление газа на стенку сосуда. В процессе взаимодействия молекулы со стенкой сосуда между ними возникают силы, подчиняющиеся третьему закону Ньютона. В результате проекция υx скорости молекулы, перпендикулярная стенке, изменяет свой знак на противоположный, а проекция υy скорости, параллельная стенке, остается неизменной (рис. ).
 Молекулярно-кинетическая теория • Формула для среднего давления газа на стенку сосуда запишется в виде • Это уравнение устанавливает связь между давлением p идеального газа, массой молекулы m 0, концентрацией молекул n, средним значением квадрата скорости и средней кинетической энергией поступательного движения молекул. • Это основное уравнение молекулярно-кинетической теории газов • Таким образом, давление газа равно двум третям средней кинетической энергии поступательного движения молекул, содержащихся в единице объема.
Молекулярно-кинетическая теория • Формула для среднего давления газа на стенку сосуда запишется в виде • Это уравнение устанавливает связь между давлением p идеального газа, массой молекулы m 0, концентрацией молекул n, средним значением квадрата скорости и средней кинетической энергией поступательного движения молекул. • Это основное уравнение молекулярно-кинетической теории газов • Таким образом, давление газа равно двум третям средней кинетической энергии поступательного движения молекул, содержащихся в единице объема.
 Молекулярно-кинетическая теория • В основное уравнение МКТ газов входит произведение концентрации молекул n на среднюю кинетическую энергию поступательного движения. • В этом случае давление пропорционально средней кинетической энергии. • Возникают вопросы: каким образом можно на опыте изменять среднюю кинетическую энергию движения молекул в сосуде неизменного объема? Какую физическую величину нужно изменить, чтобы изменилась средняя кинетическая энергия? Опыт показывает, что такой величиной является температура.
Молекулярно-кинетическая теория • В основное уравнение МКТ газов входит произведение концентрации молекул n на среднюю кинетическую энергию поступательного движения. • В этом случае давление пропорционально средней кинетической энергии. • Возникают вопросы: каким образом можно на опыте изменять среднюю кинетическую энергию движения молекул в сосуде неизменного объема? Какую физическую величину нужно изменить, чтобы изменилась средняя кинетическая энергия? Опыт показывает, что такой величиной является температура.
 • • Молекулярно-кинетическая теория Температура Понятие температуры тесно связано с понятием теплового равновесия. Тела, находящиеся в контакте друг с другом, могут обмениваться энергией. Энергия, передаваемая одним телом другому при тепловом контакте, называется количеством теплоты Q. Тепловое равновесие – это такое состояние системы тел, находящихся в тепловом контакте, при котором не происходит теплопередачи от одного тела к другому, и все макроскопические параметры тел остаются неизменными. Температура – это физический параметр, одинаковый для Температура всех тел, находящихся в тепловом равновесии. Возможность введения понятия температуры следует из опыта и носит название нулевого закона термодинамики.
• • Молекулярно-кинетическая теория Температура Понятие температуры тесно связано с понятием теплового равновесия. Тела, находящиеся в контакте друг с другом, могут обмениваться энергией. Энергия, передаваемая одним телом другому при тепловом контакте, называется количеством теплоты Q. Тепловое равновесие – это такое состояние системы тел, находящихся в тепловом контакте, при котором не происходит теплопередачи от одного тела к другому, и все макроскопические параметры тел остаются неизменными. Температура – это физический параметр, одинаковый для Температура всех тел, находящихся в тепловом равновесии. Возможность введения понятия температуры следует из опыта и носит название нулевого закона термодинамики.
 Молекулярно-кинетическая теория Температура • Для измерения температуры используются физические приборы – термометры, в которых о величине температуры судят по изменению какоголибо физического параметра. Для создания термометра необходимо выбрать термометрическое вещество (например, ртуть, спирт) и термометрическую величину, характеризующую свойство вещества (например, длина ртутного или спиртового столбика). В различных конструкциях термометров используются разнообразные физические свойства вещества (например, изменение линейных размеров твердых тел или изменение электрического сопротивления проводников при нагревании). • Термометры должны быть откалиброваны.
Молекулярно-кинетическая теория Температура • Для измерения температуры используются физические приборы – термометры, в которых о величине температуры судят по изменению какоголибо физического параметра. Для создания термометра необходимо выбрать термометрическое вещество (например, ртуть, спирт) и термометрическую величину, характеризующую свойство вещества (например, длина ртутного или спиртового столбика). В различных конструкциях термометров используются разнообразные физические свойства вещества (например, изменение линейных размеров твердых тел или изменение электрического сопротивления проводников при нагревании). • Термометры должны быть откалиброваны.
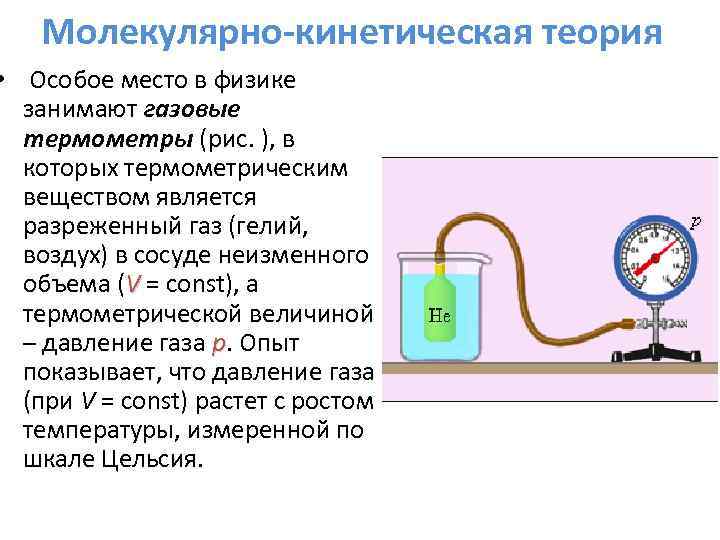 Молекулярно-кинетическая теория • Особое место в физике занимают газовые термометры (рис. ), в которых термометрическим веществом является разреженный газ (гелий, воздух) в сосуде неизменного объема (V = const), а термометрической величиной – давление газа p. Опыт показывает, что давление газа (при V = const) растет с ростом температуры, измеренной по шкале Цельсия.
Молекулярно-кинетическая теория • Особое место в физике занимают газовые термометры (рис. ), в которых термометрическим веществом является разреженный газ (гелий, воздух) в сосуде неизменного объема (V = const), а термометрической величиной – давление газа p. Опыт показывает, что давление газа (при V = const) растет с ростом температуры, измеренной по шкале Цельсия.
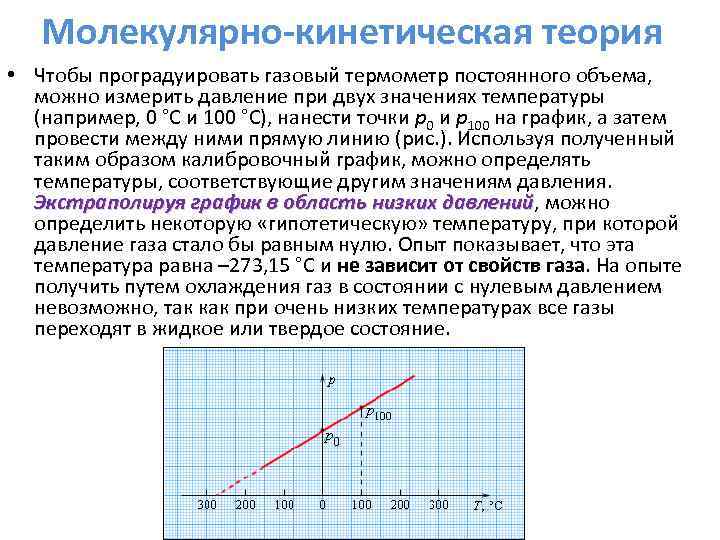 Молекулярно-кинетическая теория • Чтобы проградуировать газовый термометр постоянного объема, можно измерить давление при двух значениях температуры (например, 0 °C и 100 °C), нанести точки p 0 и p 100 на график, а затем провести между ними прямую линию (рис. ). Используя полученный таким образом калибровочный график, можно определять температуры, соответствующие другим значениям давления. Экстраполируя график в область низких давлений, можно Экстраполируя график в область низких давлений определить некоторую «гипотетическую» температуру, при которой давление газа стало бы равным нулю. Опыт показывает, что эта температура равна – 273, 15 °С и не зависит от свойств газа. На опыте получить путем охлаждения газ в состоянии с нулевым давлением невозможно, так как при очень низких температурах все газы переходят в жидкое или твердое состояние.
Молекулярно-кинетическая теория • Чтобы проградуировать газовый термометр постоянного объема, можно измерить давление при двух значениях температуры (например, 0 °C и 100 °C), нанести точки p 0 и p 100 на график, а затем провести между ними прямую линию (рис. ). Используя полученный таким образом калибровочный график, можно определять температуры, соответствующие другим значениям давления. Экстраполируя график в область низких давлений, можно Экстраполируя график в область низких давлений определить некоторую «гипотетическую» температуру, при которой давление газа стало бы равным нулю. Опыт показывает, что эта температура равна – 273, 15 °С и не зависит от свойств газа. На опыте получить путем охлаждения газ в состоянии с нулевым давлением невозможно, так как при очень низких температурах все газы переходят в жидкое или твердое состояние.
 Молекулярно-кинетическая теория • Английский физик У. Кельвин (Томсон) в 1848 г. предложил использовать точку нулевого давления газа для построения новой температурной шкалы (шкала Кельвина). В этой шкале единица измерения температуры такая же, как и в шкале Цельсия, но нулевая точка сдвинута: TК = TС + 273, 15. • В системе СИ принято единицу измерения температуры по шкале Кельвина называть кельвином и обозначать буквой K. Например, комнатная температура TС = 20 °С по шкале Кельвина равна TК = 293, 15 К.
Молекулярно-кинетическая теория • Английский физик У. Кельвин (Томсон) в 1848 г. предложил использовать точку нулевого давления газа для построения новой температурной шкалы (шкала Кельвина). В этой шкале единица измерения температуры такая же, как и в шкале Цельсия, но нулевая точка сдвинута: TК = TС + 273, 15. • В системе СИ принято единицу измерения температуры по шкале Кельвина называть кельвином и обозначать буквой K. Например, комнатная температура TС = 20 °С по шкале Кельвина равна TК = 293, 15 К.
 Молекулярно-кинетическая теория • Температурная шкала Кельвина называется абсолютной шкалой температур. Она оказывается наиболее шкалой температур удобной при построении физических теорий. • Нет необходимости привязывать шкалу Кельвина к двум фиксированным точкам – точке плавления льда и точке кипения воды при нормальном атмосферном давлении, как это принято в шкале Цельсия. • Кроме точки нулевого давления газа, которая называется абсолютным нулем температуры, абсолютным нулем температуры достаточно принять еще одну фиксированную опорную точку. В шкале Кельвина в качестве такой точки используется температура тройной точки воды (0, 01 °С), в которой в тепловом равновесии находятся все три фазы – лед, вода и пар. По шкале Кельвина температура тройной точки принимается равной 273, 16 К.
Молекулярно-кинетическая теория • Температурная шкала Кельвина называется абсолютной шкалой температур. Она оказывается наиболее шкалой температур удобной при построении физических теорий. • Нет необходимости привязывать шкалу Кельвина к двум фиксированным точкам – точке плавления льда и точке кипения воды при нормальном атмосферном давлении, как это принято в шкале Цельсия. • Кроме точки нулевого давления газа, которая называется абсолютным нулем температуры, абсолютным нулем температуры достаточно принять еще одну фиксированную опорную точку. В шкале Кельвина в качестве такой точки используется температура тройной точки воды (0, 01 °С), в которой в тепловом равновесии находятся все три фазы – лед, вода и пар. По шкале Кельвина температура тройной точки принимается равной 273, 16 К.
 Молекулярно-кинетическая теория • Таким образом, давление разреженного газа в сосуде постоянного объема V изменяется прямо пропорционально его абсолютной температуре: p ~ T. T • С другой стороны, опыт показывает, что при неизменных объеме V и температуре T давление газа изменяется прямо пропорционально отношению количества вещества ν в данном сосуде к объему V сосуда • где N – число молекул в сосуде, NА – постоянная Авогадро, n = N / V – концентрация молекул (т. е. число молекул в единице объема сосуда).
Молекулярно-кинетическая теория • Таким образом, давление разреженного газа в сосуде постоянного объема V изменяется прямо пропорционально его абсолютной температуре: p ~ T. T • С другой стороны, опыт показывает, что при неизменных объеме V и температуре T давление газа изменяется прямо пропорционально отношению количества вещества ν в данном сосуде к объему V сосуда • где N – число молекул в сосуде, NА – постоянная Авогадро, n = N / V – концентрация молекул (т. е. число молекул в единице объема сосуда).
 Молекулярно-кинетическая теория • Объединяя эти соотношения пропорциональности, можно записать: p = nk. T, • где k – некоторая универсальная для всех газов постоянная величина. Ее называют постоянной Больцмана, в честь австрийского физика Л. Больцмана, одного из создателей МКТ. Постоянная Больцмана – одна из фундаментальных физических констант. Ее численное значение в СИ: k = 1, 38· 10– 23 Дж/К.
Молекулярно-кинетическая теория • Объединяя эти соотношения пропорциональности, можно записать: p = nk. T, • где k – некоторая универсальная для всех газов постоянная величина. Ее называют постоянной Больцмана, в честь австрийского физика Л. Больцмана, одного из создателей МКТ. Постоянная Больцмана – одна из фундаментальных физических констант. Ее численное значение в СИ: k = 1, 38· 10– 23 Дж/К.
 Молекулярно-кинетическая теория • Сравнивая соотношения p = nk. T с основным уравнением МКТ газов, можно получить: • Средняя кинетическая энергия хаотического движения молекул газа прямо пропорциональна абсолютной температуре. • Таким образом, температура есть мера средней кинетической энергии поступательного движения молекул • Следует обратить внимание на то, что средняя кинетическая энергия поступательного движения молекулы не зависит от ее массы. Броуновская частица, взвешенная в жидкости или газе, обладает такой же средней кинетической энергией, как и отдельная молекула, масса которой на много порядков меньше массы броуновской частицы.
Молекулярно-кинетическая теория • Сравнивая соотношения p = nk. T с основным уравнением МКТ газов, можно получить: • Средняя кинетическая энергия хаотического движения молекул газа прямо пропорциональна абсолютной температуре. • Таким образом, температура есть мера средней кинетической энергии поступательного движения молекул • Следует обратить внимание на то, что средняя кинетическая энергия поступательного движения молекулы не зависит от ее массы. Броуновская частица, взвешенная в жидкости или газе, обладает такой же средней кинетической энергией, как и отдельная молекула, масса которой на много порядков меньше массы броуновской частицы.
 Молекулярно-кинетическая теория • Этот вывод распространяется и на случай, когда в сосуде находится смесь химически невзаимодействующих газов, молекулы которых имеют разные массы. В состоянии равновесия молекулы разных газов будут иметь одинаковые средние кинетические энергии теплового движения, определяемые только температурой смеси. Давление смеси газов на стенки сосуда будет складываться из парциальных давлений каждого газа: p = p 1 + p 2 + p 3 + … = (n 1 + n 2 + n 3 + …)k. T • В этом соотношении n 1, n 2, n 3, … – концентрации молекул различных газов в смеси. • Это соотношение выражает на языке молекулярнокинетической теории экспериментально установленный в начале XIX столетия закон Дальтона: давление в смеси закон Дальтона химически невзаимодействующих газов равно сумме их парциальных давлений.
Молекулярно-кинетическая теория • Этот вывод распространяется и на случай, когда в сосуде находится смесь химически невзаимодействующих газов, молекулы которых имеют разные массы. В состоянии равновесия молекулы разных газов будут иметь одинаковые средние кинетические энергии теплового движения, определяемые только температурой смеси. Давление смеси газов на стенки сосуда будет складываться из парциальных давлений каждого газа: p = p 1 + p 2 + p 3 + … = (n 1 + n 2 + n 3 + …)k. T • В этом соотношении n 1, n 2, n 3, … – концентрации молекул различных газов в смеси. • Это соотношение выражает на языке молекулярнокинетической теории экспериментально установленный в начале XIX столетия закон Дальтона: давление в смеси закон Дальтона химически невзаимодействующих газов равно сумме их парциальных давлений.
 Молекулярно-кинетическая теория Уравнение состояния идеального газа • Соотношение p = nk. T может быть записано в другой форме, устанавливающей связь между макроскопическими параметрами газа – объемом V, давлением p, температурой T и количеством вещества ν = m / M. M –– Это соотношение называется уравнением состояния идеального газа или уравнением состояния идеального газа Клапейрона–Менделеева – Произведение постоянной Авогадро NА на постоянную Больцмана k называется универсальной газовой постоянной и обозначается буквой R. Ее численное значение в СИ есть: R = k ∙NА = 8, 31 Дж/моль·К.
Молекулярно-кинетическая теория Уравнение состояния идеального газа • Соотношение p = nk. T может быть записано в другой форме, устанавливающей связь между макроскопическими параметрами газа – объемом V, давлением p, температурой T и количеством вещества ν = m / M. M –– Это соотношение называется уравнением состояния идеального газа или уравнением состояния идеального газа Клапейрона–Менделеева – Произведение постоянной Авогадро NА на постоянную Больцмана k называется универсальной газовой постоянной и обозначается буквой R. Ее численное значение в СИ есть: R = k ∙NА = 8, 31 Дж/моль·К.
 Молекулярно-кинетическая теория Уравнение состояния идеального газа – Если температура газа равна Tн = 273, 15 К (0 °С), а давление pн = 1 атм = 1, 013· 105 Па, то говорят, что газ находится при нормальных условиях. Как следует из уравнения состояния идеального газа, один моль любого газа при нормальных условиях занимает один и тот же объем V 0 = 0, 0224 м 3/моль = 22, 4 дм 3/моль. Это утверждение называется законом Авогадро.
Молекулярно-кинетическая теория Уравнение состояния идеального газа – Если температура газа равна Tн = 273, 15 К (0 °С), а давление pн = 1 атм = 1, 013· 105 Па, то говорят, что газ находится при нормальных условиях. Как следует из уравнения состояния идеального газа, один моль любого газа при нормальных условиях занимает один и тот же объем V 0 = 0, 0224 м 3/моль = 22, 4 дм 3/моль. Это утверждение называется законом Авогадро.
 Молекулярно-кинетическая теория Изопроцессы • Газ может участвовать в различных тепловых процессах, при которых могут изменяться все параметры, описывающие его состояние (p, V и T). Если процесс протекает достаточно медленно, то в любой момент система близка к своему равновесному состоянию. Такие процессы называются квазистатическими. В привычном квазистатическими для нас масштабе времени эти процессы могут протекать и не очень медленно. Например, разрежения и сжатия газа в звуковой волне, происходящие сотни раз в секунду, можно рассматривать как квазистатический процесс. Квазистатические процессы могут быть изображены на диаграмме состояний(например, в координатах p, V) в виде некоторой траектории, каждая точка которой представляет равновесное состояние. • Интерес представляют процессы, в которых один из параметров (p, V или T) остается неизменным. Такие процессы называются изопроцессами
Молекулярно-кинетическая теория Изопроцессы • Газ может участвовать в различных тепловых процессах, при которых могут изменяться все параметры, описывающие его состояние (p, V и T). Если процесс протекает достаточно медленно, то в любой момент система близка к своему равновесному состоянию. Такие процессы называются квазистатическими. В привычном квазистатическими для нас масштабе времени эти процессы могут протекать и не очень медленно. Например, разрежения и сжатия газа в звуковой волне, происходящие сотни раз в секунду, можно рассматривать как квазистатический процесс. Квазистатические процессы могут быть изображены на диаграмме состояний(например, в координатах p, V) в виде некоторой траектории, каждая точка которой представляет равновесное состояние. • Интерес представляют процессы, в которых один из параметров (p, V или T) остается неизменным. Такие процессы называются изопроцессами
 Изотермический процесс (T = const) • Изотермическим процессом называют квазистатический процесс, протекающий при постоянной температуре T. • Из уравнения состояния идеального газа следует, что при постоянной температуре T и T неизменном количестве вещества ν в сосуде произведение давления p газа на его p объем V должно оставаться постоянным: p. V = const
Изотермический процесс (T = const) • Изотермическим процессом называют квазистатический процесс, протекающий при постоянной температуре T. • Из уравнения состояния идеального газа следует, что при постоянной температуре T и T неизменном количестве вещества ν в сосуде произведение давления p газа на его p объем V должно оставаться постоянным: p. V = const
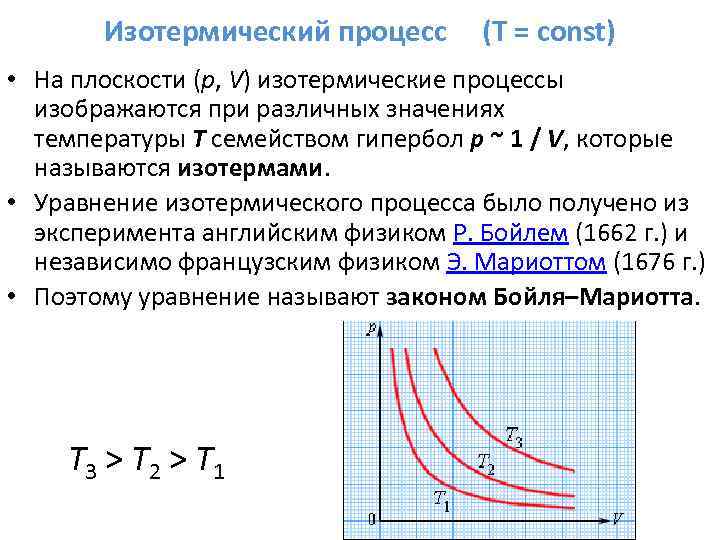 Изотермический процесс (T = const) • На плоскости (p, V) изотермические процессы изображаются при различных значениях температуры T семейством гипербол p ~ 1 / V, которые называются изотермами. • Уравнение изотермического процесса было получено из эксперимента английским физиком Р. Бойлем (1662 г. ) и независимо французским физиком Э. Мариоттом (1676 г. ) • Поэтому уравнение называют законом Бойля–Мариотта. T 3 > T 2 > T 1
Изотермический процесс (T = const) • На плоскости (p, V) изотермические процессы изображаются при различных значениях температуры T семейством гипербол p ~ 1 / V, которые называются изотермами. • Уравнение изотермического процесса было получено из эксперимента английским физиком Р. Бойлем (1662 г. ) и независимо французским физиком Э. Мариоттом (1676 г. ) • Поэтому уравнение называют законом Бойля–Мариотта. T 3 > T 2 > T 1
 Изохорный процесс (V = const) • Изохорный процесс – это процесс квазистатического нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным. • Как следует из уравнения состояния идеального газа, при этих условиях давление газа p изменяется прямо пропорционально его абсолютной температуре: p ~ T или • = const
Изохорный процесс (V = const) • Изохорный процесс – это процесс квазистатического нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным. • Как следует из уравнения состояния идеального газа, при этих условиях давление газа p изменяется прямо пропорционально его абсолютной температуре: p ~ T или • = const
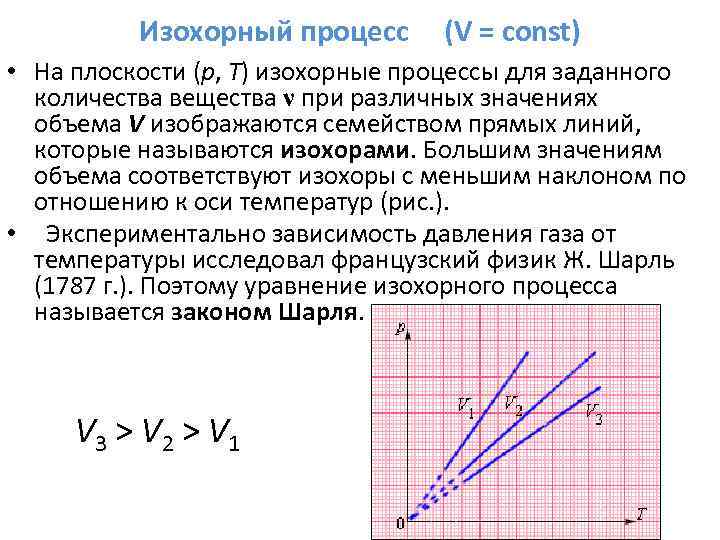 Изохорный процесс (V = const) • На плоскости (p, T) изохорные процессы для заданного количества вещества ν при различных значениях объема V изображаются семейством прямых линий, которые называются изохорами. Большим значениям объема соответствуют изохоры с меньшим наклоном по отношению к оси температур (рис. ). • Экспериментально зависимость давления газа от температуры исследовал французский физик Ж. Шарль (1787 г. ). Поэтому уравнение изохорного процесса называется законом Шарля. V 3 > V 2 > V 1
Изохорный процесс (V = const) • На плоскости (p, T) изохорные процессы для заданного количества вещества ν при различных значениях объема V изображаются семейством прямых линий, которые называются изохорами. Большим значениям объема соответствуют изохоры с меньшим наклоном по отношению к оси температур (рис. ). • Экспериментально зависимость давления газа от температуры исследовал французский физик Ж. Шарль (1787 г. ). Поэтому уравнение изохорного процесса называется законом Шарля. V 3 > V 2 > V 1
 Изобарный процесс (p = const) • Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. • Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид: • где V 0 – объем газа при температуре 0 °С. Коэффициент α равен (1/273, 15) К– 1. Его α называют температурным коэффициентом объемного расширения газов.
Изобарный процесс (p = const) • Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. • Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид: • где V 0 – объем газа при температуре 0 °С. Коэффициент α равен (1/273, 15) К– 1. Его α называют температурным коэффициентом объемного расширения газов.
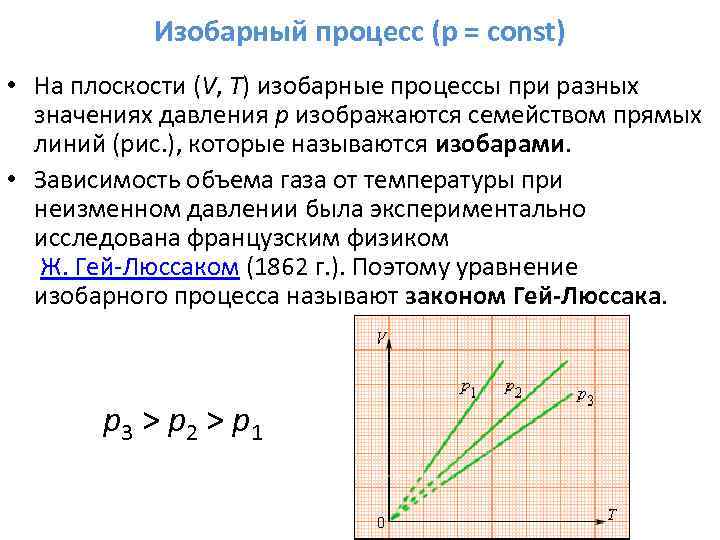 Изобарный процесс (p = const) • На плоскости (V, T) изобарные процессы при разных значениях давления p изображаются семейством прямых линий (рис. ), которые называются изобарами. • Зависимость объема газа от температуры при неизменном давлении была экспериментально исследована французским физиком Ж. Гей-Люссаком (1862 г. ). Поэтому уравнение изобарного процесса называют законом Гей-Люссака. p 3 > p 2 > p 1
Изобарный процесс (p = const) • На плоскости (V, T) изобарные процессы при разных значениях давления p изображаются семейством прямых линий (рис. ), которые называются изобарами. • Зависимость объема газа от температуры при неизменном давлении была экспериментально исследована французским физиком Ж. Гей-Люссаком (1862 г. ). Поэтому уравнение изобарного процесса называют законом Гей-Люссака. p 3 > p 2 > p 1
 Изопроцессы • Экспериментально установленные законы Бойля –Мариотта, Шарля и Гей-Люссака находят –Мариотта, Шарля и Гей-Люссака объяснение в молекулярно-кинетической теории газов. Они являются следствием уравнения состояния идеального газа.
Изопроцессы • Экспериментально установленные законы Бойля –Мариотта, Шарля и Гей-Люссака находят –Мариотта, Шарля и Гей-Люссака объяснение в молекулярно-кинетической теории газов. Они являются следствием уравнения состояния идеального газа.
 Термодинамика • Термодинамика – это наука о тепловых явлениях. В противоположность молекулярно-кинетической теории, которая делает выводы на основе представлений о молекулярном строении вещества, термодинамика исходит из наиболее общих закономерностей тепловых процессов и свойств макроскопических систем. • Выводы термодинамики опираются на совокупность опытных фактов и не зависят от наших знаний о внутреннем устройстве вещества, хотя в целом ряде случаев термодинамика использует молекулярнокинетические модели для иллюстрации своих выводов.
Термодинамика • Термодинамика – это наука о тепловых явлениях. В противоположность молекулярно-кинетической теории, которая делает выводы на основе представлений о молекулярном строении вещества, термодинамика исходит из наиболее общих закономерностей тепловых процессов и свойств макроскопических систем. • Выводы термодинамики опираются на совокупность опытных фактов и не зависят от наших знаний о внутреннем устройстве вещества, хотя в целом ряде случаев термодинамика использует молекулярнокинетические модели для иллюстрации своих выводов.
 Термодинамика • Термодинамика рассматривает изолированные системы тел, находящиеся в состоянии термодинамического равновесия. • Это означает, что в таких системах прекратились все наблюдаемые макроскопические процессы.
Термодинамика • Термодинамика рассматривает изолированные системы тел, находящиеся в состоянии термодинамического равновесия. • Это означает, что в таких системах прекратились все наблюдаемые макроскопические процессы.
 Термодинамика • Если термодинамическая система была подвержена внешнему воздействию, то в конечном итоге она перейдет в другое равновесное состояние. • Такой переход называется термодинамическим процессом. Если процесс протекает достаточно медленно (в пределе бесконечно медленно), то система в каждый момент времени оказывается близкой к равновесному состоянию. • Процессы, состоящие из последовательности равновесных состояний, называются квазистатическими.
Термодинамика • Если термодинамическая система была подвержена внешнему воздействию, то в конечном итоге она перейдет в другое равновесное состояние. • Такой переход называется термодинамическим процессом. Если процесс протекает достаточно медленно (в пределе бесконечно медленно), то система в каждый момент времени оказывается близкой к равновесному состоянию. • Процессы, состоящие из последовательности равновесных состояний, называются квазистатическими.
 Термодинамика. Внутренняя энергия • Одним из важнейших понятий термодинамики является внутренняя энергия тела. • Все макроскопические тела обладают энергией, заключенной внутри самих тел. С точки зрения МКТ внутренняя энергия вещества складывается из кинетической энергии всех атомов и молекул и потенциальной энергии их взаимодействия друг с другом. В частности, внутренняя энергия идеального газа равна сумме кинетических энергий всех частиц газа, находящихся в непрерывном и беспорядочном тепловом движении. Отсюда вытекает закон Джоуля, подтверждаемый многочисленными экспериментами: • Внутренняя энергия идеального газа зависит только от его температуры и не зависит от объема
Термодинамика. Внутренняя энергия • Одним из важнейших понятий термодинамики является внутренняя энергия тела. • Все макроскопические тела обладают энергией, заключенной внутри самих тел. С точки зрения МКТ внутренняя энергия вещества складывается из кинетической энергии всех атомов и молекул и потенциальной энергии их взаимодействия друг с другом. В частности, внутренняя энергия идеального газа равна сумме кинетических энергий всех частиц газа, находящихся в непрерывном и беспорядочном тепловом движении. Отсюда вытекает закон Джоуля, подтверждаемый многочисленными экспериментами: • Внутренняя энергия идеального газа зависит только от его температуры и не зависит от объема
 Термодинамика. Внутренняя энергия • МКТ приводит к следующему выражению для внутренней энергии одного моля идеального одноатомного газа (гелий, неон и др. ), молекулы которого совершают только поступательное движение: • • Поскольку потенциальная энергия взаимодействия молекул зависит от расстояния между ними, в общем случае внутренняя энергия U тела зависит наряду с температурой T также и от объема V: T U = U (T, V) • Таким образом, внутренняя энергия U тела однозначно определяется макроскопическими параметрами, характеризующими состояние тела. Она не зависит от того, каким путем было реализовано данное состояние. Принято говорить, что внутренняя энергия является функцией состояния.
Термодинамика. Внутренняя энергия • МКТ приводит к следующему выражению для внутренней энергии одного моля идеального одноатомного газа (гелий, неон и др. ), молекулы которого совершают только поступательное движение: • • Поскольку потенциальная энергия взаимодействия молекул зависит от расстояния между ними, в общем случае внутренняя энергия U тела зависит наряду с температурой T также и от объема V: T U = U (T, V) • Таким образом, внутренняя энергия U тела однозначно определяется макроскопическими параметрами, характеризующими состояние тела. Она не зависит от того, каким путем было реализовано данное состояние. Принято говорить, что внутренняя энергия является функцией состояния.
 Термодинамика. Способы изменения внутренней энергии • Внутренняя энергия тела может изменяться, если действующие на него внешние силы совершают работу (положительную или отрицательную). работу • Например, если газ подвергается сжатию в цилиндре под поршнем, то внешние силы совершают над газом некоторую положительную работу A'. В то же время силы давления, A' действующие со стороны газа на поршень, совершают работу A = –A'
Термодинамика. Способы изменения внутренней энергии • Внутренняя энергия тела может изменяться, если действующие на него внешние силы совершают работу (положительную или отрицательную). работу • Например, если газ подвергается сжатию в цилиндре под поршнем, то внешние силы совершают над газом некоторую положительную работу A'. В то же время силы давления, A' действующие со стороны газа на поршень, совершают работу A = –A'
 Термодинамика. Способы изменения внутренней энергии • Внутренняя энергия тела может изменяться не только в результате совершаемой работы, но и вследствие теплообмена. • При тепловом контакте тел внутренняя энергия одного из них может увеличиваться, а другого – уменьшаться. В этом случае говорят о тепловом потоке от одного тела к другому. • Количеством теплоты Q, полученным телом, Количеством теплоты Q называют изменение внутренней энергии тела в результате теплообмена.
Термодинамика. Способы изменения внутренней энергии • Внутренняя энергия тела может изменяться не только в результате совершаемой работы, но и вследствие теплообмена. • При тепловом контакте тел внутренняя энергия одного из них может увеличиваться, а другого – уменьшаться. В этом случае говорят о тепловом потоке от одного тела к другому. • Количеством теплоты Q, полученным телом, Количеством теплоты Q называют изменение внутренней энергии тела в результате теплообмена.
 Термодинамика. Способы изменения внутренней энергии • Передача энергии от одного тела другому в форме тепла может происходить только при наличии разности температур между ними. • Тепловой поток всегда направлен от горячего тела к холодному • Количество теплоты Q является энергетической величиной. В СИ количество теплоты измеряется в единицах механической работы – джоулях (Дж).
Термодинамика. Способы изменения внутренней энергии • Передача энергии от одного тела другому в форме тепла может происходить только при наличии разности температур между ними. • Тепловой поток всегда направлен от горячего тела к холодному • Количество теплоты Q является энергетической величиной. В СИ количество теплоты измеряется в единицах механической работы – джоулях (Дж).
 Термодинамика. Первый закон термодинамики • На рис. условно изображены энергетические потоки между выделенной термодинамической системой и окружающими телами. Величина Q > 0, если тепловой Q > 0 поток направлен в сторону термодинамической системы. Величина A > 0, если система совершает положительную A > 0 работу над окружающими телами. • Если система обменивается теплом с окружающими телами и совершает работу (положительную или отрицательную), то изменяется состояние системы, изменяется состояние системы т. е. изменяются ее макроскопические параметры (температура, давление, объем).
Термодинамика. Первый закон термодинамики • На рис. условно изображены энергетические потоки между выделенной термодинамической системой и окружающими телами. Величина Q > 0, если тепловой Q > 0 поток направлен в сторону термодинамической системы. Величина A > 0, если система совершает положительную A > 0 работу над окружающими телами. • Если система обменивается теплом с окружающими телами и совершает работу (положительную или отрицательную), то изменяется состояние системы, изменяется состояние системы т. е. изменяются ее макроскопические параметры (температура, давление, объем).
 Термодинамика. Первый закон термодинамики • Так как внутренняя энергия U однозначно определяется макроскопическими параметрами, характеризующими состояние системы, то отсюда следует, что процессы теплообмена и совершения работы сопровождаются изменением ΔU внутренней энергии системы.
Термодинамика. Первый закон термодинамики • Так как внутренняя энергия U однозначно определяется макроскопическими параметрами, характеризующими состояние системы, то отсюда следует, что процессы теплообмена и совершения работы сопровождаются изменением ΔU внутренней энергии системы.
 Термодинамика. Первый закон термодинамики • Первый закон термодинамики является обобщением закона сохранения и превращения энергии для термодинамической системы. Он формулируется следующим образом: • Изменение ΔU внутренней энергии неизолированной термодинамической системы равно разности между количеством теплоты Q, переданной системе, и работой A, совершенной системой над внешними телами. ΔU = Q – A • Соотношение, выражающее первый закон термодинамики, часто записывают в другой форме: Q = ΔU + A • Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы над внешними телами.
Термодинамика. Первый закон термодинамики • Первый закон термодинамики является обобщением закона сохранения и превращения энергии для термодинамической системы. Он формулируется следующим образом: • Изменение ΔU внутренней энергии неизолированной термодинамической системы равно разности между количеством теплоты Q, переданной системе, и работой A, совершенной системой над внешними телами. ΔU = Q – A • Соотношение, выражающее первый закон термодинамики, часто записывают в другой форме: Q = ΔU + A • Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы над внешними телами.
 Термодинамика. Первый закон термодинамики • • • Применим первый закон термодинамики к изопроцессам в газах. В изохорном процессе (V = const) газ работы не совершает, A = 0. Следовательно, Q = ΔU = U (T 2) – U (T 1). Здесь U (T 1) и U (T 2) – внутренние энергии газа в начальном и конечном состояниях. Внутренняя энергия идеального газа зависит только от температуры (закон Джоуля). При изохорном нагревании тепло поглощается газом (Q > 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q < 0). В изобарном процессе (p = const) работа, совершаемая газом, выражается соотношением A = p (V 2 – V 1) = p ΔV. Первый закон термодинамики для изобарного процесса дает: Q = U (T 2) – U (T 1) + p (V 2 – V 1) = ΔU + p ΔV. При изобарном расширении Q > 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном сжатии Q < 0 – тепло отдается внешним телам. В этом случае A < 0. Температура газа при изобарном сжатии уменьшается, T 2 < T 1; внутренняя энергия убывает, ΔU < 0. В изотермическом процессе температура газа не изменяется, следовательно, не изменяется и внутренняя энергия газа, ΔU = 0. Первый закон термодинамики для изотермического процесса выражается соотношением Q = A. Количество теплоты Q, полученной газом в процессе изотермического расширения, превращается в работу над внешними телами. При изотермическом сжатии работа внешних сил, произведенная над газом, превращается в тепло, которое передается окружающим телам. Наряду с изохорным, изобарным и изотермическим процессами в термодинамике часто рассматриваются процессы, протекающие в отсутствие теплообмена с окружающими телами. Сосуды с теплонепроницаемыми стенками называются адиабатическими оболочками, а процессы расширения или сжатия газа в таких сосудах называются адиабатическими. В адиабатическом процессе Q = 0; поэтому первый закон термодинамики принимает вид A = –ΔU, т. е. газ совершает работу за счет убыли его внутренней энергии.
Термодинамика. Первый закон термодинамики • • • Применим первый закон термодинамики к изопроцессам в газах. В изохорном процессе (V = const) газ работы не совершает, A = 0. Следовательно, Q = ΔU = U (T 2) – U (T 1). Здесь U (T 1) и U (T 2) – внутренние энергии газа в начальном и конечном состояниях. Внутренняя энергия идеального газа зависит только от температуры (закон Джоуля). При изохорном нагревании тепло поглощается газом (Q > 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q < 0). В изобарном процессе (p = const) работа, совершаемая газом, выражается соотношением A = p (V 2 – V 1) = p ΔV. Первый закон термодинамики для изобарного процесса дает: Q = U (T 2) – U (T 1) + p (V 2 – V 1) = ΔU + p ΔV. При изобарном расширении Q > 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном сжатии Q < 0 – тепло отдается внешним телам. В этом случае A < 0. Температура газа при изобарном сжатии уменьшается, T 2 < T 1; внутренняя энергия убывает, ΔU < 0. В изотермическом процессе температура газа не изменяется, следовательно, не изменяется и внутренняя энергия газа, ΔU = 0. Первый закон термодинамики для изотермического процесса выражается соотношением Q = A. Количество теплоты Q, полученной газом в процессе изотермического расширения, превращается в работу над внешними телами. При изотермическом сжатии работа внешних сил, произведенная над газом, превращается в тепло, которое передается окружающим телам. Наряду с изохорным, изобарным и изотермическим процессами в термодинамике часто рассматриваются процессы, протекающие в отсутствие теплообмена с окружающими телами. Сосуды с теплонепроницаемыми стенками называются адиабатическими оболочками, а процессы расширения или сжатия газа в таких сосудах называются адиабатическими. В адиабатическом процессе Q = 0; поэтому первый закон термодинамики принимает вид A = –ΔU, т. е. газ совершает работу за счет убыли его внутренней энергии.
 Тепловые двигатели. Термодинамические циклы. Цикл Карно • Тепловым двигателем называется устройство, способное превращать полученное количество теплоты в механическую работу. Механическая работа в тепловых двигателях производится в процессе расширения некоторого вещества, которое называется рабочим телом. В качестве рабочего тела обычно используются газообразные вещества (пары бензина, воздух, водяной пар). Рабочее тело получает (или отдает) тепловую энергию в процессе теплообмена с телами, имеющими большой запас внутренней энергии. Эти тела называются тепловыми резервуарами. • Реально существующие тепловые двигатели (паровые машины, двигатели внутреннего сгорания и т. д. ) работают циклически. Процесс теплопередачи и преобразования полученного количества теплоты в работу периодически повторяется. Для этого рабочее тело должно совершать круговой процесс или термодинамический цикл, при котором периодически восстанавливается исходное состояние.
Тепловые двигатели. Термодинамические циклы. Цикл Карно • Тепловым двигателем называется устройство, способное превращать полученное количество теплоты в механическую работу. Механическая работа в тепловых двигателях производится в процессе расширения некоторого вещества, которое называется рабочим телом. В качестве рабочего тела обычно используются газообразные вещества (пары бензина, воздух, водяной пар). Рабочее тело получает (или отдает) тепловую энергию в процессе теплообмена с телами, имеющими большой запас внутренней энергии. Эти тела называются тепловыми резервуарами. • Реально существующие тепловые двигатели (паровые машины, двигатели внутреннего сгорания и т. д. ) работают циклически. Процесс теплопередачи и преобразования полученного количества теплоты в работу периодически повторяется. Для этого рабочее тело должно совершать круговой процесс или термодинамический цикл, при котором периодически восстанавливается исходное состояние.
 Тепловые двигатели. Термодинамические циклы. Цикл Карно • Общее свойство всех круговых процессов состоит в том, что их невозможно провести, приводя рабочее тело в тепловой контакт только с одним тепловым резервуаром. Их нужно, по крайней мере, два. Тепловой резервуар с более высокой температурой называют нагревателем, а с более низкой – холодильником. • Совершая круговой процесс, рабочее тело получает от нагревателя некоторое количество теплоты Q 1 > 0 и отдает холодильнику количество теплоты Q 2 < 0. • Полное количество теплоты Q, полученное рабочим телом за цикл, равно Q = Q 1 + Q 2 = Q 1 – |Q 2| • При обходе цикла рабочее тело возвращается в первоначальное состояние, следовательно, изменение его внутренней энергии равно нулю (ΔU = 0) • Согласно первому закону термодинамики, ΔU = Q – A = 0 • Отсюда следует: A = Q 1 – |Q 2|
Тепловые двигатели. Термодинамические циклы. Цикл Карно • Общее свойство всех круговых процессов состоит в том, что их невозможно провести, приводя рабочее тело в тепловой контакт только с одним тепловым резервуаром. Их нужно, по крайней мере, два. Тепловой резервуар с более высокой температурой называют нагревателем, а с более низкой – холодильником. • Совершая круговой процесс, рабочее тело получает от нагревателя некоторое количество теплоты Q 1 > 0 и отдает холодильнику количество теплоты Q 2 < 0. • Полное количество теплоты Q, полученное рабочим телом за цикл, равно Q = Q 1 + Q 2 = Q 1 – |Q 2| • При обходе цикла рабочее тело возвращается в первоначальное состояние, следовательно, изменение его внутренней энергии равно нулю (ΔU = 0) • Согласно первому закону термодинамики, ΔU = Q – A = 0 • Отсюда следует: A = Q 1 – |Q 2|
 Тепловые двигатели. Термодинамические циклы. Цикл Карно • Работа A, совершаемая рабочим телом за цикл, равна полученному за цикл количеству теплоты Q. Отношение работы A к количеству теплоты Q 1, полученному рабочим телом за цикл от нагревателя, называется коэффициентом полезного действия η тепловой машины:
Тепловые двигатели. Термодинамические циклы. Цикл Карно • Работа A, совершаемая рабочим телом за цикл, равна полученному за цикл количеству теплоты Q. Отношение работы A к количеству теплоты Q 1, полученному рабочим телом за цикл от нагревателя, называется коэффициентом полезного действия η тепловой машины:
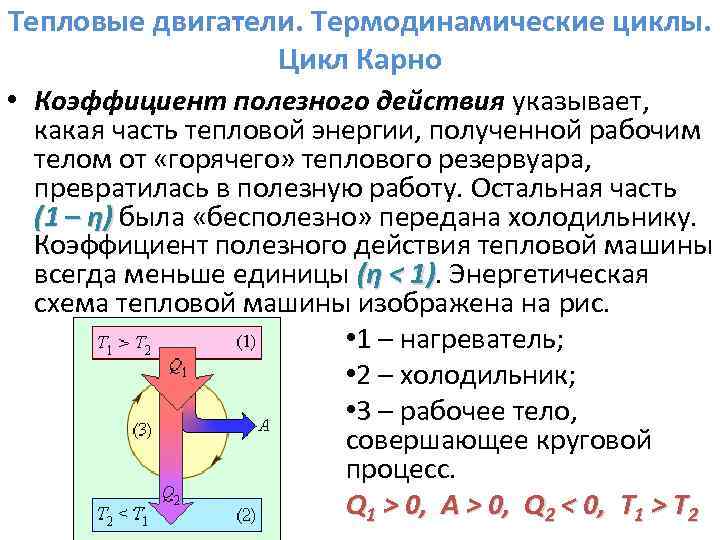 Тепловые двигатели. Термодинамические циклы. Цикл Карно • Коэффициент полезного действия указывает, какая часть тепловой энергии, полученной рабочим телом от «горячего» теплового резервуара, превратилась в полезную работу. Остальная часть (1 – η) была «бесполезно» передана холодильнику. (1 – η) Коэффициент полезного действия тепловой машины всегда меньше единицы (η < 1). Энергетическая (η < 1) схема тепловой машины изображена на рис. • 1 – нагреватель; • 2 – холодильник; • 3 – рабочее тело, совершающее круговой процесс. Q 1 > 0, A > 0, Q 2 < 0, T 1 > T 2
Тепловые двигатели. Термодинамические циклы. Цикл Карно • Коэффициент полезного действия указывает, какая часть тепловой энергии, полученной рабочим телом от «горячего» теплового резервуара, превратилась в полезную работу. Остальная часть (1 – η) была «бесполезно» передана холодильнику. (1 – η) Коэффициент полезного действия тепловой машины всегда меньше единицы (η < 1). Энергетическая (η < 1) схема тепловой машины изображена на рис. • 1 – нагреватель; • 2 – холодильник; • 3 – рабочее тело, совершающее круговой процесс. Q 1 > 0, A > 0, Q 2 < 0, T 1 > T 2
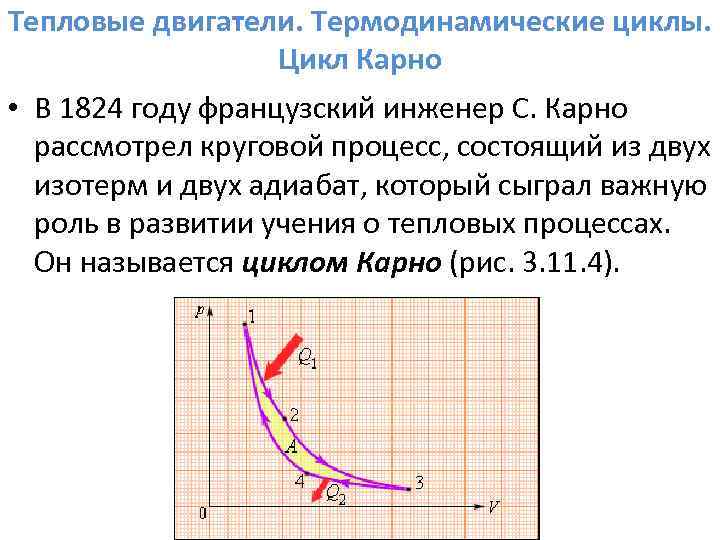 Тепловые двигатели. Термодинамические циклы. Цикл Карно • В 1824 году французский инженер С. Карно рассмотрел круговой процесс, состоящий из двух изотерм и двух адиабат, который сыграл важную роль в развитии учения о тепловых процессах. Он называется циклом Карно (рис. 3. 11. 4).
Тепловые двигатели. Термодинамические циклы. Цикл Карно • В 1824 году французский инженер С. Карно рассмотрел круговой процесс, состоящий из двух изотерм и двух адиабат, который сыграл важную роль в развитии учения о тепловых процессах. Он называется циклом Карно (рис. 3. 11. 4).
 Тепловые двигатели. Термодинамические циклы. Цикл Карно • Цикл Карно совершает газ, находящийся в цилиндре под поршнем. На изотермическом участке (1– 2) газ приводится в тепловой контакт с горячим тепловым резервуаром (нагревателем), имеющим температуру T 1. Газ изотермически расширяется, совершая работу A 12, при этом к газу подводится некоторое количество теплоты Q 1 = A 12. Далее на адиабатическом участке (2– 3) газ помещается в адиабатическую оболочку и продолжает расширяться в отсутствие теплообмена. На этом участке газ совершает работу A 23 > 0. Температура газа при адиабатическом расширении падает до значения T 2. На следующем изотермическом участке (3– 4) газ приводится в тепловой контакт с холодным тепловым резервуаром (холодильником) при температуре T 2 < T 1. Происходит процесс изотермического сжатия. Газ совершает работу A 34 < 0 и отдает тепло Q 2 < 0, равное произведенной работе A 34. Внутренняя энергия газа не изменяется. Наконец, на последнем участке адиабатического сжатия газ вновь помещается в адиабатическую оболочку. При сжатии температура газа повышается до значения T 1, газ совершает работу A 41 < 0. Полная работа A, совершаемая газом за цикл, равна сумме работ на отдельных участках: A = A 12 + A 23 + A 34 + A 41. • С. Карно выразил коэффициент полезного действия цикла через температуры нагревателя T 1 и холодильника T 2: • .
Тепловые двигатели. Термодинамические циклы. Цикл Карно • Цикл Карно совершает газ, находящийся в цилиндре под поршнем. На изотермическом участке (1– 2) газ приводится в тепловой контакт с горячим тепловым резервуаром (нагревателем), имеющим температуру T 1. Газ изотермически расширяется, совершая работу A 12, при этом к газу подводится некоторое количество теплоты Q 1 = A 12. Далее на адиабатическом участке (2– 3) газ помещается в адиабатическую оболочку и продолжает расширяться в отсутствие теплообмена. На этом участке газ совершает работу A 23 > 0. Температура газа при адиабатическом расширении падает до значения T 2. На следующем изотермическом участке (3– 4) газ приводится в тепловой контакт с холодным тепловым резервуаром (холодильником) при температуре T 2 < T 1. Происходит процесс изотермического сжатия. Газ совершает работу A 34 < 0 и отдает тепло Q 2 < 0, равное произведенной работе A 34. Внутренняя энергия газа не изменяется. Наконец, на последнем участке адиабатического сжатия газ вновь помещается в адиабатическую оболочку. При сжатии температура газа повышается до значения T 1, газ совершает работу A 41 < 0. Полная работа A, совершаемая газом за цикл, равна сумме работ на отдельных участках: A = A 12 + A 23 + A 34 + A 41. • С. Карно выразил коэффициент полезного действия цикла через температуры нагревателя T 1 и холодильника T 2: • .
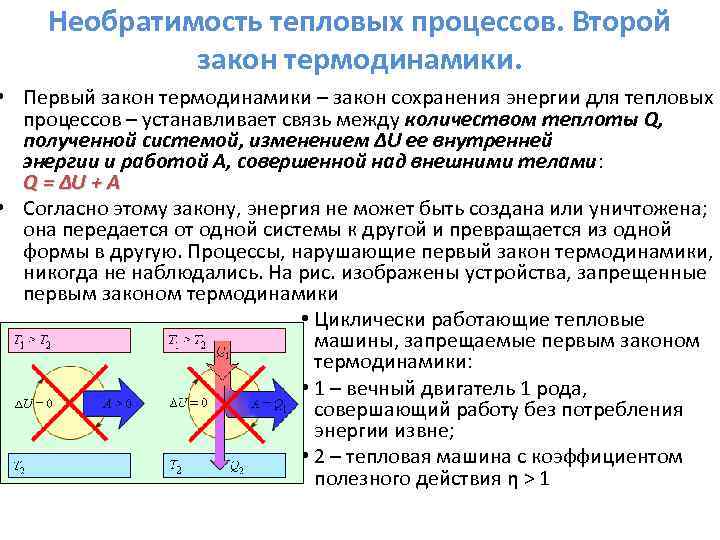 Необратимость тепловых процессов. Второй закон термодинамики. • Первый закон термодинамики – закон сохранения энергии для тепловых процессов – устанавливает связь между количеством теплоты Q, полученной системой, изменением ΔU ее внутренней энергии и работой A, совершенной над внешними телами: Q = ΔU + A • Согласно этому закону, энергия не может быть создана или уничтожена; она передается от одной системы к другой и превращается из одной формы в другую. Процессы, нарушающие первый закон термодинамики, никогда не наблюдались. На рис. изображены устройства, запрещенные первым законом термодинамики • Циклически работающие тепловые машины, запрещаемые первым законом термодинамики: • 1 – вечный двигатель 1 рода, совершающий работу без потребления энергии извне; • 2 – тепловая машина с коэффициентом полезного действия η > 1
Необратимость тепловых процессов. Второй закон термодинамики. • Первый закон термодинамики – закон сохранения энергии для тепловых процессов – устанавливает связь между количеством теплоты Q, полученной системой, изменением ΔU ее внутренней энергии и работой A, совершенной над внешними телами: Q = ΔU + A • Согласно этому закону, энергия не может быть создана или уничтожена; она передается от одной системы к другой и превращается из одной формы в другую. Процессы, нарушающие первый закон термодинамики, никогда не наблюдались. На рис. изображены устройства, запрещенные первым законом термодинамики • Циклически работающие тепловые машины, запрещаемые первым законом термодинамики: • 1 – вечный двигатель 1 рода, совершающий работу без потребления энергии извне; • 2 – тепловая машина с коэффициентом полезного действия η > 1
 Необратимость тепловых процессов. Второй закон термодинамики. • Первый закон термодинамики не устанавливает направления тепловых Первый закон термодинамики процессов. Однако, как показывает опыт, многие тепловые процессы могут протекать только в одном направлении. Такие процессы называются необратимыми. Например, при тепловом контакте двух тел с разными температурами тепловой поток всегда направлен от более теплого тела к более холодному. Никогда не наблюдается самопроизвольный процесс передачи тепла от тела с низкой температурой к телу с более высокой температурой. Следовательно, процесс теплообмена при конечной разности температур является необратимым. • Обратимыми процессами называют процессы перехода системы из одного равновесного состояния в другое, которые можно провести в обратном направлении через ту же последовательность промежуточных равновесных состояний. При этом сама система и окружающие тела возвращаются к исходному состоянию. • Процессы, в ходе которых система все время остается в состоянии равновесия, называются квазистатическими. Все квазистатические процессы обратимы. Все обратимые процессы являются квазистатическими.
Необратимость тепловых процессов. Второй закон термодинамики. • Первый закон термодинамики не устанавливает направления тепловых Первый закон термодинамики процессов. Однако, как показывает опыт, многие тепловые процессы могут протекать только в одном направлении. Такие процессы называются необратимыми. Например, при тепловом контакте двух тел с разными температурами тепловой поток всегда направлен от более теплого тела к более холодному. Никогда не наблюдается самопроизвольный процесс передачи тепла от тела с низкой температурой к телу с более высокой температурой. Следовательно, процесс теплообмена при конечной разности температур является необратимым. • Обратимыми процессами называют процессы перехода системы из одного равновесного состояния в другое, которые можно провести в обратном направлении через ту же последовательность промежуточных равновесных состояний. При этом сама система и окружающие тела возвращаются к исходному состоянию. • Процессы, в ходе которых система все время остается в состоянии равновесия, называются квазистатическими. Все квазистатические процессы обратимы. Все обратимые процессы являются квазистатическими.
 Необратимость тепловых процессов. Второй закон термодинамики. • Процессы превращения механической работы во внутреннюю энергию тела являются необратимыми из-за наличия трения, процессов диффузии в газах и жидкостях, процессы перемешивания газа при наличии начальной разности давлений и т. д. Все реальные процессы необратимы, но они могут сколь угодно близко приближаться к обратимым процессам. Обратимые процессы являются идеализацией реальных процессов. • Первый закон термодинамики не может отличить обратимые процессы от необратимых. Он просто требует от термодинамического процесса определенного энергетического баланса и ничего не говорит о том, возможен такой процесс или нет.
Необратимость тепловых процессов. Второй закон термодинамики. • Процессы превращения механической работы во внутреннюю энергию тела являются необратимыми из-за наличия трения, процессов диффузии в газах и жидкостях, процессы перемешивания газа при наличии начальной разности давлений и т. д. Все реальные процессы необратимы, но они могут сколь угодно близко приближаться к обратимым процессам. Обратимые процессы являются идеализацией реальных процессов. • Первый закон термодинамики не может отличить обратимые процессы от необратимых. Он просто требует от термодинамического процесса определенного энергетического баланса и ничего не говорит о том, возможен такой процесс или нет.
 Необратимость тепловых процессов. Второй закон термодинамики. • Направление самопроизвольно протекающих процессов устанавливает второй закон термодинамики. Он может быть сформулирован в термодинамики виде запрета на определенные виды термодинамических процессов. • Английский физик У. Кельвин дал в 1851 г. следующую формулировку второго закона: второго закона • В циклически действующей тепловой машине невозможен процесс, единственным результатом которого было бы преобразование в механическую работу всего количества теплоты, полученного от единственного теплового резервуара.
Необратимость тепловых процессов. Второй закон термодинамики. • Направление самопроизвольно протекающих процессов устанавливает второй закон термодинамики. Он может быть сформулирован в термодинамики виде запрета на определенные виды термодинамических процессов. • Английский физик У. Кельвин дал в 1851 г. следующую формулировку второго закона: второго закона • В циклически действующей тепловой машине невозможен процесс, единственным результатом которого было бы преобразование в механическую работу всего количества теплоты, полученного от единственного теплового резервуара.
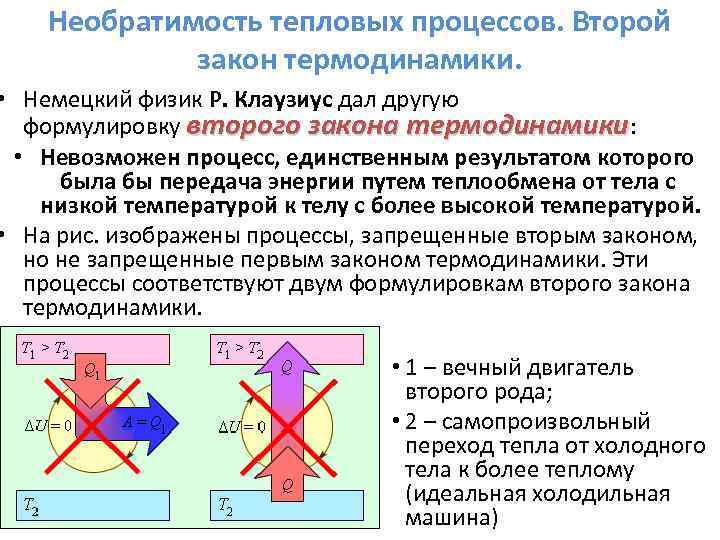 Необратимость тепловых процессов. Второй закон термодинамики. • Немецкий физик Р. Клаузиус дал другую формулировку второго закона термодинамики: • Невозможен процесс, единственным результатом которого была бы передача энергии путем теплообмена от тела с низкой температурой к телу с более высокой температурой. • На рис. изображены процессы, запрещенные вторым законом, но не запрещенные первым законом термодинамики. Эти процессы соответствуют двум формулировкам второго закона термодинамики. • 1 – вечный двигатель второго рода; • 2 – самопроизвольный переход тепла от холодного тела к более теплому (идеальная холодильная машина)
Необратимость тепловых процессов. Второй закон термодинамики. • Немецкий физик Р. Клаузиус дал другую формулировку второго закона термодинамики: • Невозможен процесс, единственным результатом которого была бы передача энергии путем теплообмена от тела с низкой температурой к телу с более высокой температурой. • На рис. изображены процессы, запрещенные вторым законом, но не запрещенные первым законом термодинамики. Эти процессы соответствуют двум формулировкам второго закона термодинамики. • 1 – вечный двигатель второго рода; • 2 – самопроизвольный переход тепла от холодного тела к более теплому (идеальная холодильная машина)


