молекулярная физика.ppt
- Количество слайдов: 54
 Молекулярная физика и основы термодинамики § 1. Основные положения МКТ Молекулярно-кинетической теорией называют учение о строении и свойствах вещества на основе представления о существовании атомов и молекул как наименьших частиц химического вещества
Молекулярная физика и основы термодинамики § 1. Основные положения МКТ Молекулярно-кинетической теорией называют учение о строении и свойствах вещества на основе представления о существовании атомов и молекул как наименьших частиц химического вещества
 Основные положения молекулярно - кинетической теории: 1. Все вещества состоят из мельчайших частиц - молекул. Молекула - наименьшая частица вещества, сохраняющая все его химические свойства. Все молекулы, образующие данное вещество, совершенно одинаковы. Молекулы состоят из атомов. Атом - мельчайшая частица химического элемента.
Основные положения молекулярно - кинетической теории: 1. Все вещества состоят из мельчайших частиц - молекул. Молекула - наименьшая частица вещества, сохраняющая все его химические свойства. Все молекулы, образующие данное вещество, совершенно одинаковы. Молекулы состоят из атомов. Атом - мельчайшая частица химического элемента.
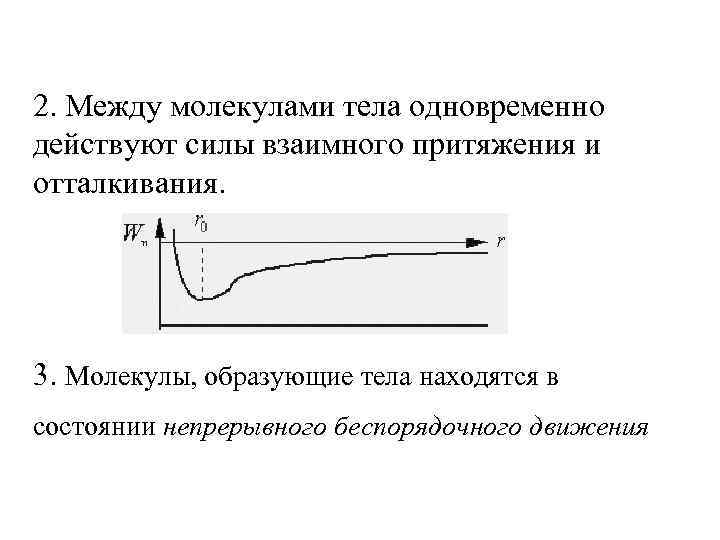 2. Между молекулами тела одновременно действуют силы взаимного притяжения и отталкивания. 3. Молекулы, образующие тела находятся в состоянии непрерывного беспорядочного движения
2. Между молекулами тела одновременно действуют силы взаимного притяжения и отталкивания. 3. Молекулы, образующие тела находятся в состоянии непрерывного беспорядочного движения
 Скорость движения молекул тем выше, чем выше температура тела. Температура - мера средней кинетической энергии молекул тела. Скорость движения молекул тела, определяющих кинетическую энергию, определяет тепловое состояние тела, величину его внутренней энергии. Хаотическое движение молекул называют тепловым.
Скорость движения молекул тем выше, чем выше температура тела. Температура - мера средней кинетической энергии молекул тела. Скорость движения молекул тела, определяющих кинетическую энергию, определяет тепловое состояние тела, величину его внутренней энергии. Хаотическое движение молекул называют тепловым.
 Внутренняя энергия газа, обусловленная кинетической энергией молекул, характеризуется макроскопической функцией - температурой, определяемой мерой нагретости тела. Температура характеризует состояние теплового равновесия тел: при тепловом равновесии температуры всех тел, входящих в данную систему, одинаковы. Теплота передается от более нагретого тела к менее нагретому телу. Температуру измеряют с помощью термометра - прибора, в котором отслеживается изменение какихлибо свойств термометрического вещества.
Внутренняя энергия газа, обусловленная кинетической энергией молекул, характеризуется макроскопической функцией - температурой, определяемой мерой нагретости тела. Температура характеризует состояние теплового равновесия тел: при тепловом равновесии температуры всех тел, входящих в данную систему, одинаковы. Теплота передается от более нагретого тела к менее нагретому телу. Температуру измеряют с помощью термометра - прибора, в котором отслеживается изменение какихлибо свойств термометрического вещества.
 В системе СИ принято единицу измерения температуры по шкале Кельвина называть кельвином и обозначать буквой К. Например, комнатная температура TС = 20 °С по шкале Кельвина равна TК = 293, 15 К. TК = TС + 273, 15. Температурная шкала Кельвина называется абсолютной шкалой температур. Она оказывается наиболее удобной при построении физических теорий.
В системе СИ принято единицу измерения температуры по шкале Кельвина называть кельвином и обозначать буквой К. Например, комнатная температура TС = 20 °С по шкале Кельвина равна TК = 293, 15 К. TК = TС + 273, 15. Температурная шкала Кельвина называется абсолютной шкалой температур. Она оказывается наиболее удобной при построении физических теорий.
 Средняя кинетическая энергия хаотического движения молекул газа прямо пропорциональна абсолютной температуре. Таким образом, температура есть мера средней кинетической энергии поступательного движения молекул.
Средняя кинетическая энергия хаотического движения молекул газа прямо пропорциональна абсолютной температуре. Таким образом, температура есть мера средней кинетической энергии поступательного движения молекул.
 В молекулярно-кинетической теории количество вещества принято считать пропорциональным числу частиц. Единица количества вещества называется молем (моль). Моль – это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов в 0, 012 кг углерода 12 C. Молекула углерода состоит из одного атома. Таким образом, в одном моле любого вещества содержится одно и то же число частиц (молекул). Это число называется постоянной Авогадро NА: NА = 6, 02· 1023 моль– 1
В молекулярно-кинетической теории количество вещества принято считать пропорциональным числу частиц. Единица количества вещества называется молем (моль). Моль – это количество вещества, содержащее столько же частиц (молекул), сколько содержится атомов в 0, 012 кг углерода 12 C. Молекула углерода состоит из одного атома. Таким образом, в одном моле любого вещества содержится одно и то же число частиц (молекул). Это число называется постоянной Авогадро NА: NА = 6, 02· 1023 моль– 1
 Количество вещества ν определяется как отношение числа N частиц (молекул) вещества к постоянной Авогадро NА: Массу одного моля вещества принято называть молярной массой M. Молярная масса равна произведению массы m 0 одной молекулы данного вещества на постоянную Авогадро: M = NA · m 0.
Количество вещества ν определяется как отношение числа N частиц (молекул) вещества к постоянной Авогадро NА: Массу одного моля вещества принято называть молярной массой M. Молярная масса равна произведению массы m 0 одной молекулы данного вещества на постоянную Авогадро: M = NA · m 0.
 Простейшей моделью молекулярно-кинетической теории является модель идеального газа. В кинетической модели идеального газа молекулы рассматриваются как идеально упругие шарики, взаимодействующие между собой и со стенками только во время упругих столкновений. Суммарный объем всех молекул предполагается малым по сравнению с объемом сосуда, в котором находится газ.
Простейшей моделью молекулярно-кинетической теории является модель идеального газа. В кинетической модели идеального газа молекулы рассматриваются как идеально упругие шарики, взаимодействующие между собой и со стенками только во время упругих столкновений. Суммарный объем всех молекул предполагается малым по сравнению с объемом сосуда, в котором находится газ.
 Модель идеального газа достаточно хорошо описывает поведение реальных газов в широком диапазоне давлений и температур. Задача молекулярно-кинетической теории состоит в том, чтобы установить связь между микроскопическими (масса, скорость, кинетическая энергия молекул) и макроскопическими параметрами (давление, газ, температура).
Модель идеального газа достаточно хорошо описывает поведение реальных газов в широком диапазоне давлений и температур. Задача молекулярно-кинетической теории состоит в том, чтобы установить связь между микроскопическими (масса, скорость, кинетическая энергия молекул) и макроскопическими параметрами (давление, газ, температура).
 § 2. Основное уравнение кинетической теории идеальных газов. Молекулы газа действуют на стенку сосуда. Стенки также действуют на газ с такой же силой, но направленной противоположно. Нормальная компонента силы, отнесенная к единице площади поверхности, называется давлением
§ 2. Основное уравнение кинетической теории идеальных газов. Молекулы газа действуют на стенку сосуда. Стенки также действуют на газ с такой же силой, но направленной противоположно. Нормальная компонента силы, отнесенная к единице площади поверхности, называется давлением
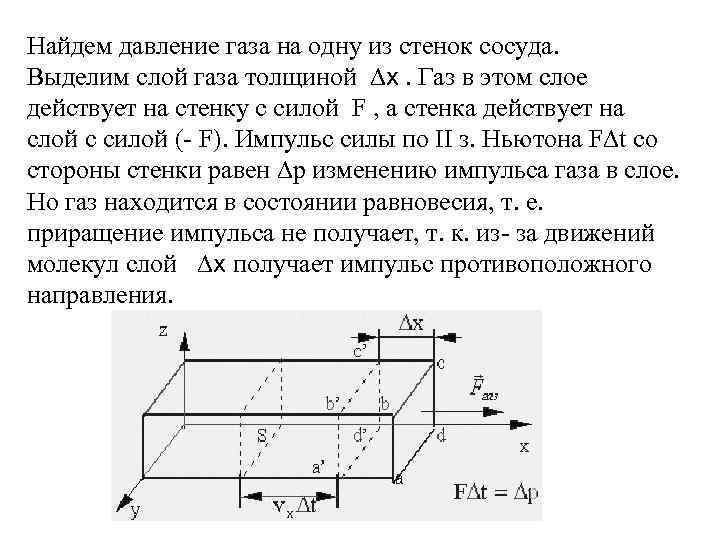 Найдем давление газа на одну из стенок сосуда. Выделим слой газа толщиной ∆х. Газ в этом слое действует на стенку с силой F , а стенка действует на слой с силой (- F). Импульс силы по II з. Ньютона F∆t со стороны стенки равен ∆p изменению импульса газа в слое. Но газ находится в состоянии равновесия, т. е. приращение импульса не получает, т. к. из- за движений молекул слой ∆х получает импульс противоположного направления.
Найдем давление газа на одну из стенок сосуда. Выделим слой газа толщиной ∆х. Газ в этом слое действует на стенку с силой F , а стенка действует на слой с силой (- F). Импульс силы по II з. Ньютона F∆t со стороны стенки равен ∆p изменению импульса газа в слое. Но газ находится в состоянии равновесия, т. е. приращение импульса не получает, т. к. из- за движений молекул слой ∆х получает импульс противоположного направления.
 За время ∆t в слой ∆х слева входит число молекул такое же, как и выходит справа. Если в единице объема газа содержится n 0 молекул, то слева направо входит половина N=1/2(n 0 SVx∆t) молекул, находящихся на расстоянии Vx∆t от границы a'b'c'd' слоя ∆x. Каждая из этих молекул обладает импульсом m. Vx , т. е. суммарный импульс слева направо равен За этот же промежуток времени слой покидает вторая половина молекул с импульсом обратного знака
За время ∆t в слой ∆х слева входит число молекул такое же, как и выходит справа. Если в единице объема газа содержится n 0 молекул, то слева направо входит половина N=1/2(n 0 SVx∆t) молекул, находящихся на расстоянии Vx∆t от границы a'b'c'd' слоя ∆x. Каждая из этих молекул обладает импульсом m. Vx , т. е. суммарный импульс слева направо равен За этот же промежуток времени слой покидает вторая половина молекул с импульсом обратного знака
 Изменение импульса слоя равно Это изменение импульса и компенсирует импульс упругой силы со стороны стенки сосуда
Изменение импульса слоя равно Это изменение импульса и компенсирует импульс упругой силы со стороны стенки сосуда
 Разделив на обе части равенства, получим Учтем, что проекции скоростей vx разных молекул различны и заменим средним значением
Разделив на обе части равенства, получим Учтем, что проекции скоростей vx разных молекул различны и заменим средним значением
 постоянная Больцмана
постоянная Больцмана
 В результате многочисленных соударений молекул газа между собой и со стенками в сосуде, содержащем большое число молекул, устанавливается некоторое статистическое распределение молекул по скоростям. При этом все направления векторов скоростей молекул оказываются равноправными (равновероятными), а модули скоростей и их проекции на координатные оси подчиняются определенным закономерностям. Распределение молекул газа по модулю скоростей называется распределением Максвелла (1860 г. ).
В результате многочисленных соударений молекул газа между собой и со стенками в сосуде, содержащем большое число молекул, устанавливается некоторое статистическое распределение молекул по скоростям. При этом все направления векторов скоростей молекул оказываются равноправными (равновероятными), а модули скоростей и их проекции на координатные оси подчиняются определенным закономерностям. Распределение молекул газа по модулю скоростей называется распределением Максвелла (1860 г. ).
 Дж. Максвелл вывел закон распределения молекул газа по скоростям, исходя из основных положений молекулярно-кинетической теории. На рис. представлены типичные кривые распределения молекул по скоростям. По оси абсцисс отложен модуль скорости, а по оси ординат – относительное число молекул, скорости которых лежат в интервале от υ до υ + Δυ. Это число равно площади выделенного на рис. столбика.
Дж. Максвелл вывел закон распределения молекул газа по скоростям, исходя из основных положений молекулярно-кинетической теории. На рис. представлены типичные кривые распределения молекул по скоростям. По оси абсцисс отложен модуль скорости, а по оси ординат – относительное число молекул, скорости которых лежат в интервале от υ до υ + Δυ. Это число равно площади выделенного на рис. столбика.
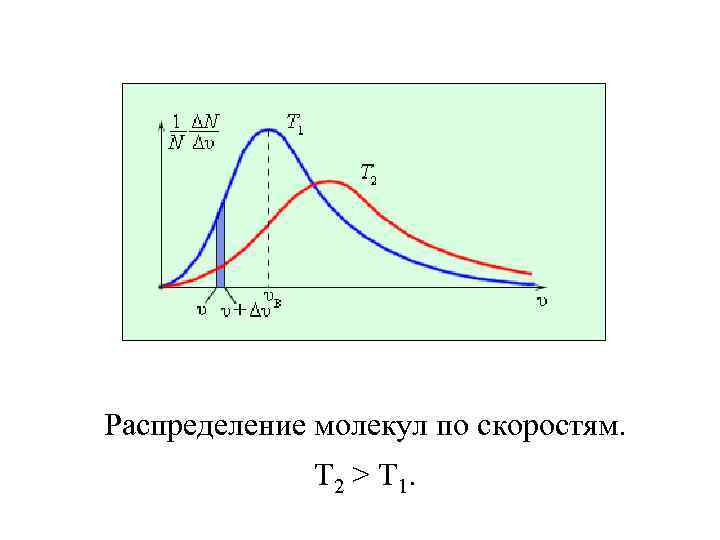 Распределение молекул по скоростям. T 2 > T 1.
Распределение молекул по скоростям. T 2 > T 1.
 Характерными параметрами распределения Максвелла являются наиболее вероятная скорость Vв, соответствующая максимуму кривой распределения, и среднеквадратичная скорость где Vкв – среднее значение квадрата скорости. С ростом температуры максимум кривой распределения смещается в сторону больших скоростей, при этом Vв и Vкв увеличиваются.
Характерными параметрами распределения Максвелла являются наиболее вероятная скорость Vв, соответствующая максимуму кривой распределения, и среднеквадратичная скорость где Vкв – среднее значение квадрата скорости. С ростом температуры максимум кривой распределения смещается в сторону больших скоростей, при этом Vв и Vкв увеличиваются.
 § 3. Уравнение состояния идеального газа. Изопроцессы. • Произведение постоянной Авогадро NА на постоянную Больцмана k называется универсальной газовой постоянной и обозначается буквой R. • Ее численное значение в СИ есть: R = 8, 31 Дж/моль·К.
§ 3. Уравнение состояния идеального газа. Изопроцессы. • Произведение постоянной Авогадро NА на постоянную Больцмана k называется универсальной газовой постоянной и обозначается буквой R. • Ее численное значение в СИ есть: R = 8, 31 Дж/моль·К.
 уравнение состояния идеального газа (уравнение Клапейрона–Менделеева)
уравнение состояния идеального газа (уравнение Клапейрона–Менделеева)
 Интерес представляют процессы, в которых один из параметров (p, V или T) остается неизменным. Такие процессы называются изопроцессами. Изотермический процесс (T = const) Изотермическим процессом называют процесс, протекающий при постоянной температуре T. p. V = const. закон Бойля–Мариотта
Интерес представляют процессы, в которых один из параметров (p, V или T) остается неизменным. Такие процессы называются изопроцессами. Изотермический процесс (T = const) Изотермическим процессом называют процесс, протекающий при постоянной температуре T. p. V = const. закон Бойля–Мариотта
 На плоскости (p, V) изотермические процессы изображаются при различных значениях температуры T семейством гипербол p ~ 1 / V, которые называются изотермами. Так коэффициент пропорциональности в этом соотношении увеличивается с ростом температуры, изотермы, соответствующие более высоким значениям температуры, располагаются на графике выше изотерм, соответствующих меньшим значениям температуры.
На плоскости (p, V) изотермические процессы изображаются при различных значениях температуры T семейством гипербол p ~ 1 / V, которые называются изотермами. Так коэффициент пропорциональности в этом соотношении увеличивается с ростом температуры, изотермы, соответствующие более высоким значениям температуры, располагаются на графике выше изотерм, соответствующих меньшим значениям температуры.
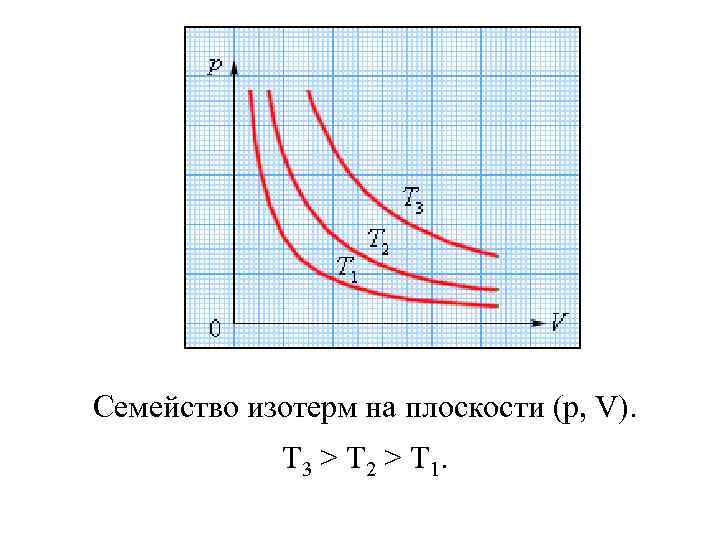 Семейство изотерм на плоскости (p, V). T 3 > T 2 > T 1.
Семейство изотерм на плоскости (p, V). T 3 > T 2 > T 1.
 Изохорный процесс (V = const) Изохорный процесс – это процесс нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным. закон Шарля На плоскости (p, T) изохорные процессы для заданного количества вещества ν при различных значениях объема V изображаются семейством прямых линий, которые называются изохорами. Большим значениям объема соответствуют изохоры с меньшим наклоном по отношению к оси температур.
Изохорный процесс (V = const) Изохорный процесс – это процесс нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным. закон Шарля На плоскости (p, T) изохорные процессы для заданного количества вещества ν при различных значениях объема V изображаются семейством прямых линий, которые называются изохорами. Большим значениям объема соответствуют изохоры с меньшим наклоном по отношению к оси температур.
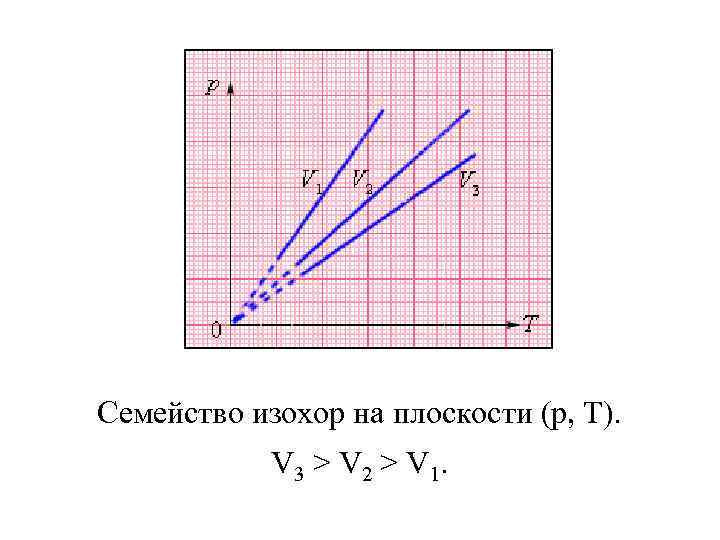 Семейство изохор на плоскости (p, T). V 3 > V 2 > V 1.
Семейство изохор на плоскости (p, T). V 3 > V 2 > V 1.
 Изобарный процесс (p = const) Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид: где V 0 – объем газа при температуре 0 °С. Коэффициент α равен 1/273, 15 К– 1. Его называют температурным коэффициентом объемного расширения газов. На плоскости (V, T) изобарные процессы при разных значениях давления p изображаются семейством прямых линий, которые называются изобарами.
Изобарный процесс (p = const) Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид: где V 0 – объем газа при температуре 0 °С. Коэффициент α равен 1/273, 15 К– 1. Его называют температурным коэффициентом объемного расширения газов. На плоскости (V, T) изобарные процессы при разных значениях давления p изображаются семейством прямых линий, которые называются изобарами.
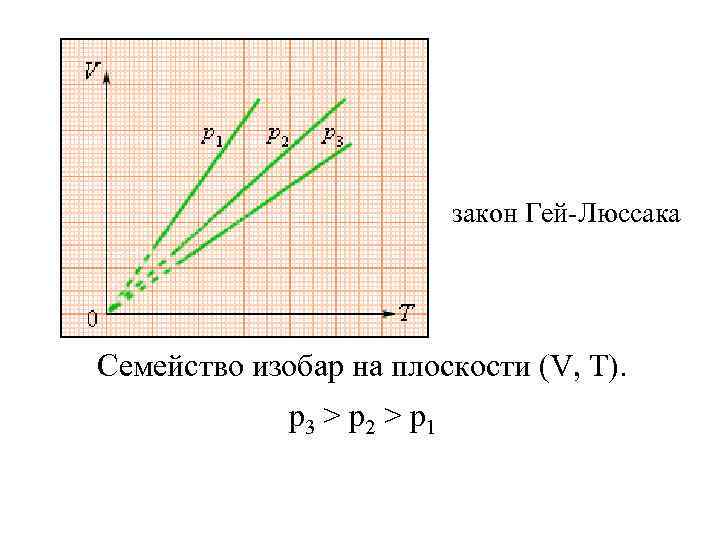 закон Гей-Люссака Семейство изобар на плоскости (V, T). p 3 > p 2 > p 1
закон Гей-Люссака Семейство изобар на плоскости (V, T). p 3 > p 2 > p 1
 § 4. Первый закон термодинамики • На рис. условно изображены энергетические потоки между выделенной термодинамической системой и окружающими телами. Величина Q > 0, если тепловой поток направлен в сторону термодинамической системы. Величина A > 0, если система совершает положительную работу над окружающими телами.
§ 4. Первый закон термодинамики • На рис. условно изображены энергетические потоки между выделенной термодинамической системой и окружающими телами. Величина Q > 0, если тепловой поток направлен в сторону термодинамической системы. Величина A > 0, если система совершает положительную работу над окружающими телами.
 Первый закон термодинамики является обобщением закона сохранения и превращения энергии для термодинамической системы. Он формулируется следующим образом: Изменение ΔU внутренней энергии неизолированной термодинамической системы равно разности между количеством теплоты Q, переданной системе, и работой A, совершенной системой над внешними телами. ΔU = Q – A
Первый закон термодинамики является обобщением закона сохранения и превращения энергии для термодинамической системы. Он формулируется следующим образом: Изменение ΔU внутренней энергии неизолированной термодинамической системы равно разности между количеством теплоты Q, переданной системе, и работой A, совершенной системой над внешними телами. ΔU = Q – A
 Соотношение, выражающее первый закон термодинамики, часто записывают в другой форме: Q = ΔU + A. Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы над внешними телами.
Соотношение, выражающее первый закон термодинамики, часто записывают в другой форме: Q = ΔU + A. Количество теплоты, полученное системой, идет на изменение ее внутренней энергии и совершение работы над внешними телами.
 Первый закон термодинамики является обобщением опытных фактов. Согласно этому закону, энергия не может быть создана или уничтожена; она передается от одной системы к другой и превращается из одной формы в другую. Важным следствием первого закона термодинамики является утверждение о невозможности создания машины, способной совершать полезную работу без потребления энергии извне и без каких-либо изменений внутри самой машины.
Первый закон термодинамики является обобщением опытных фактов. Согласно этому закону, энергия не может быть создана или уничтожена; она передается от одной системы к другой и превращается из одной формы в другую. Важным следствием первого закона термодинамики является утверждение о невозможности создания машины, способной совершать полезную работу без потребления энергии извне и без каких-либо изменений внутри самой машины.
 Применим первый закон термодинамики к изопроцессам в газах. В изохорном процессе (V = const) газ работы не совершает, A = 0. Следовательно, Q = ΔU = U(T 2) – U(T 1). Здесь U(T 1) и U(T 2) – внутренние энергии газа в начальном и конечном состояниях. Внутренняя энергия идеального газа зависит только от температуры (закон Джоуля). При изохорном нагревании тепло поглощается газом (Q > 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q < 0).
Применим первый закон термодинамики к изопроцессам в газах. В изохорном процессе (V = const) газ работы не совершает, A = 0. Следовательно, Q = ΔU = U(T 2) – U(T 1). Здесь U(T 1) и U(T 2) – внутренние энергии газа в начальном и конечном состояниях. Внутренняя энергия идеального газа зависит только от температуры (закон Джоуля). При изохорном нагревании тепло поглощается газом (Q > 0), и его внутренняя энергия увеличивается. При охлаждении тепло отдается внешним телам (Q < 0).
 В изобарном процессе (p = const) работа, совершаемая газом, выражается соотношением A = p(V 2 – V 1) = pΔV. Первый закон термодинамики для изобарного процесса дает: Q = U(T 2) – U(T 1) + p(V 2 – V 1) = ΔU + pΔV. При изобарном расширении Q > 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном сжатии Q < 0 – тепло отдается внешним телам. В этом случае A < 0. Температура газа при изобарном сжатии уменьшается, T 2 < T 1; внутренняя энергия убывает, ΔU < 0.
В изобарном процессе (p = const) работа, совершаемая газом, выражается соотношением A = p(V 2 – V 1) = pΔV. Первый закон термодинамики для изобарного процесса дает: Q = U(T 2) – U(T 1) + p(V 2 – V 1) = ΔU + pΔV. При изобарном расширении Q > 0 – тепло поглощается газом, и газ совершает положительную работу. При изобарном сжатии Q < 0 – тепло отдается внешним телам. В этом случае A < 0. Температура газа при изобарном сжатии уменьшается, T 2 < T 1; внутренняя энергия убывает, ΔU < 0.
 В изотермическом процессе температура газа не изменяется, следовательно, не изменяется и внутренняя энергия газа, ΔU = 0. Первый закон термодинамики для изотермического процесса выражается соотношением Q = A. Количество теплоты Q, полученной газом в процессе изотермического расширения, превращается в работу над внешними телами. При изотермическом сжатии работа внешних сил, произведенная над газом, превращается в тепло, которое передается окружающим телам.
В изотермическом процессе температура газа не изменяется, следовательно, не изменяется и внутренняя энергия газа, ΔU = 0. Первый закон термодинамики для изотермического процесса выражается соотношением Q = A. Количество теплоты Q, полученной газом в процессе изотермического расширения, превращается в работу над внешними телами. При изотермическом сжатии работа внешних сил, произведенная над газом, превращается в тепло, которое передается окружающим телам.
 Наряду с изохорным, изобарным и изотермическим процессами в термодинамике часто рассматриваются процессы, протекающие в отсутствие теплообмена с окружающими телами. Сосуды с теплонепроницаемыми стенками называются адиабатическими оболочками, а процессы расширения или сжатия газа в таких сосудах называются адиабатическими. В адиабатическом процессе Q = 0; поэтому первый закон термодинамики принимает вид A = –ΔU, то есть газ совершает работу за счет убыли его внутренней энергии.
Наряду с изохорным, изобарным и изотермическим процессами в термодинамике часто рассматриваются процессы, протекающие в отсутствие теплообмена с окружающими телами. Сосуды с теплонепроницаемыми стенками называются адиабатическими оболочками, а процессы расширения или сжатия газа в таких сосудах называются адиабатическими. В адиабатическом процессе Q = 0; поэтому первый закон термодинамики принимает вид A = –ΔU, то есть газ совершает работу за счет убыли его внутренней энергии.
 На плоскости (p, V) процесс адиабатического расширения (или сжатия) газа изображается кривой, которая называется адиабатой. При адиабатическом расширении газ совершает положительную работу (A > 0); поэтому его внутренняя энергия уменьшается (ΔU < 0). Это приводит к понижению температуры газа. Вследствие этого давление газа при адиабатическом расширении убывает быстрее, чем при изотермическом расширении.
На плоскости (p, V) процесс адиабатического расширения (или сжатия) газа изображается кривой, которая называется адиабатой. При адиабатическом расширении газ совершает положительную работу (A > 0); поэтому его внутренняя энергия уменьшается (ΔU < 0). Это приводит к понижению температуры газа. Вследствие этого давление газа при адиабатическом расширении убывает быстрее, чем при изотермическом расширении.
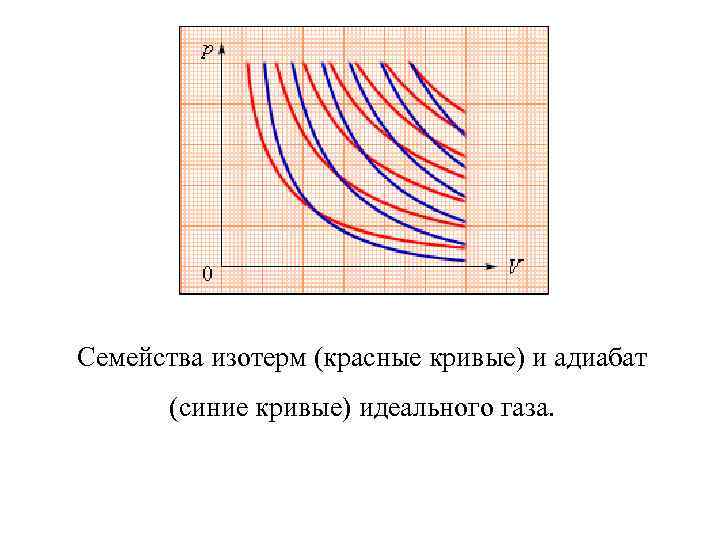 Семейства изотерм (красные кривые) и адиабат (синие кривые) идеального газа.
Семейства изотерм (красные кривые) и адиабат (синие кривые) идеального газа.
 Работа газа в адиабатическом процессе просто выражается через температуры T 1 и T 2 начального и конечного состояний: A = CV(T 2 – T 1). В термодинамике важную роль играет физическая величина, которая называется энтропией. Изменение энтропии в каком-либо квазистатическом процессе равно приведенному теплу ΔQ / T, полученному системой. Поскольку на любом участке адиабатического процесса ΔQ = 0, энтропия в этом процессе остается неизменной.
Работа газа в адиабатическом процессе просто выражается через температуры T 1 и T 2 начального и конечного состояний: A = CV(T 2 – T 1). В термодинамике важную роль играет физическая величина, которая называется энтропией. Изменение энтропии в каком-либо квазистатическом процессе равно приведенному теплу ΔQ / T, полученному системой. Поскольку на любом участке адиабатического процесса ΔQ = 0, энтропия в этом процессе остается неизменной.
 Процессы обратимые и необратимые. Обратимыми процессами называют процессы перехода системы из одного равновесного состояния в другое, которые можно провести в обратном направлении через ту же последовательность промежуточных равновесных состояний. При этом сама система и окружающие тела возвращаются к исходному состоянию. Необратимые процессы
Процессы обратимые и необратимые. Обратимыми процессами называют процессы перехода системы из одного равновесного состояния в другое, которые можно провести в обратном направлении через ту же последовательность промежуточных равновесных состояний. При этом сама система и окружающие тела возвращаются к исходному состоянию. Необратимые процессы
 § 5. Второй закон термодинамики • Первый закон термодинамики не устанавливает направление тепловых процессов. • Английский физик У. Кельвин дал в 1851 г. следующую формулировку второго закона: • В циклически действующей тепловой машине невозможен процесс, единственным результатом которого было бы преобразование в механическую работу всего количества теплоты, полученного от единственного теплового резервуара.
§ 5. Второй закон термодинамики • Первый закон термодинамики не устанавливает направление тепловых процессов. • Английский физик У. Кельвин дал в 1851 г. следующую формулировку второго закона: • В циклически действующей тепловой машине невозможен процесс, единственным результатом которого было бы преобразование в механическую работу всего количества теплоты, полученного от единственного теплового резервуара.
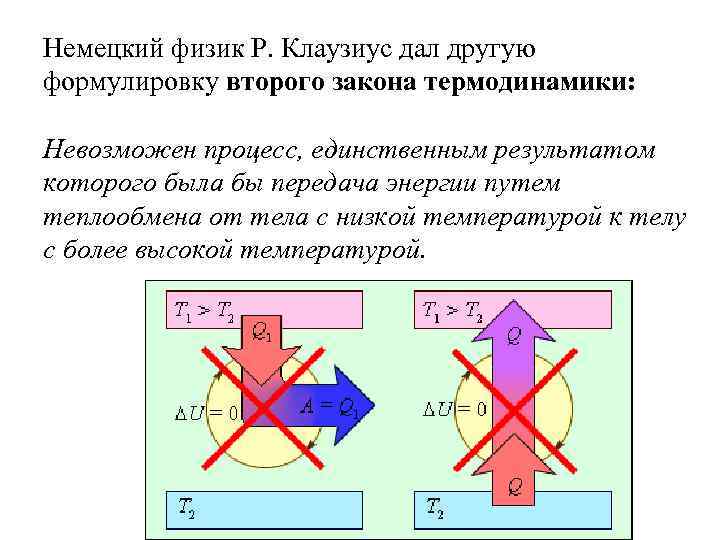 Немецкий физик Р. Клаузиус дал другую формулировку второго закона термодинамики: Невозможен процесс, единственным результатом которого была бы передача энергии путем теплообмена от тела с низкой температурой к телу с более высокой температурой.
Немецкий физик Р. Клаузиус дал другую формулировку второго закона термодинамики: Невозможен процесс, единственным результатом которого была бы передача энергии путем теплообмена от тела с низкой температурой к телу с более высокой температурой.
 § 6. Тепловые двигатели. Цикл Карно • Тепловым двигателем называется устройство, способное превращать полученное количество теплоты в механическую работу. • Механическая работа в тепловых двигателях производится в процессе расширения некоторого вещества, которое называется рабочим телом. • Полученное газом количество теплоты Q полностью превращается в работу A при изотермическом процессе, при котором внутренняя энергия остается неизменной (ΔU = 0): • A = Q.
§ 6. Тепловые двигатели. Цикл Карно • Тепловым двигателем называется устройство, способное превращать полученное количество теплоты в механическую работу. • Механическая работа в тепловых двигателях производится в процессе расширения некоторого вещества, которое называется рабочим телом. • Полученное газом количество теплоты Q полностью превращается в работу A при изотермическом процессе, при котором внутренняя энергия остается неизменной (ΔU = 0): • A = Q.
 Но такой однократный акт преобразования теплоты в работу не представляет интереса для техники. Реально существующие тепловые двигатели (паровые машины, двигатели внутреннего сгорания и т. д. ) работают циклически. Процесс теплопередачи и преобразования полученного количества теплоты в работу периодически повторяется. Для этого рабочее тело должно совершать круговой процесс или термодинамический цикл, при котором периодически восстанавливается исходное состояние.
Но такой однократный акт преобразования теплоты в работу не представляет интереса для техники. Реально существующие тепловые двигатели (паровые машины, двигатели внутреннего сгорания и т. д. ) работают циклически. Процесс теплопередачи и преобразования полученного количества теплоты в работу периодически повторяется. Для этого рабочее тело должно совершать круговой процесс или термодинамический цикл, при котором периодически восстанавливается исходное состояние.
 Круговые процессы изображаются на диаграмме (p, V) газообразного рабочего тела с помощью замкнутых кривых. При расширении газ совершает положительную работу A 1, равную площади под кривой abc, при сжатии газ совершает отрицательную работу A 2, равную по модулю площади под кривой cda. Полная работа за цикл A = A 1 + A 2 на диаграмме (p, V) равна площади цикла. Работа A положительна, если цикл обходится по часовой стрелке, и A отрицательна, если цикл обходится в противоположном направлении.
Круговые процессы изображаются на диаграмме (p, V) газообразного рабочего тела с помощью замкнутых кривых. При расширении газ совершает положительную работу A 1, равную площади под кривой abc, при сжатии газ совершает отрицательную работу A 2, равную по модулю площади под кривой cda. Полная работа за цикл A = A 1 + A 2 на диаграмме (p, V) равна площади цикла. Работа A положительна, если цикл обходится по часовой стрелке, и A отрицательна, если цикл обходится в противоположном направлении.
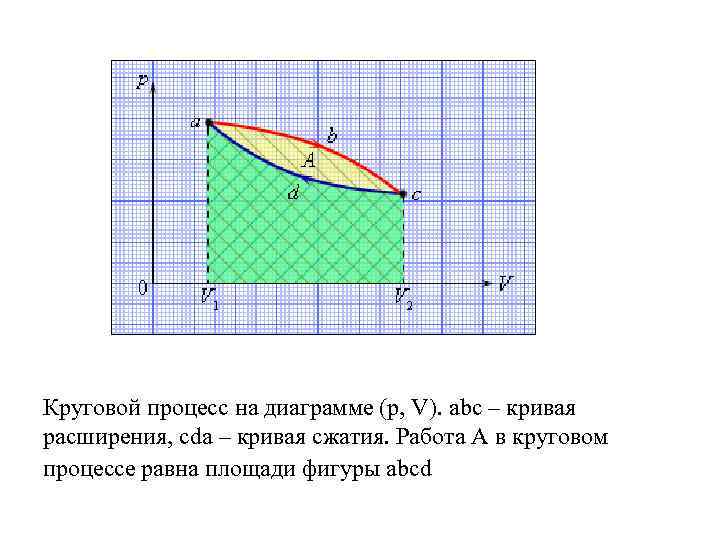 Круговой процесс на диаграмме (p, V). abc – кривая расширения, cda – кривая сжатия. Работа A в круговом процессе равна площади фигуры abcd
Круговой процесс на диаграмме (p, V). abc – кривая расширения, cda – кривая сжатия. Работа A в круговом процессе равна площади фигуры abcd
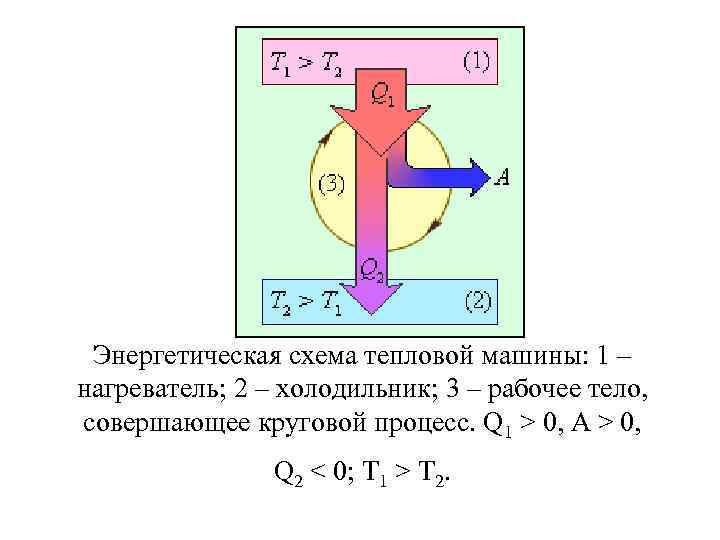 Энергетическая схема тепловой машины: 1 – нагреватель; 2 – холодильник; 3 – рабочее тело, совершающее круговой процесс. Q 1 > 0, A > 0, Q 2 < 0; T 1 > T 2.
Энергетическая схема тепловой машины: 1 – нагреватель; 2 – холодильник; 3 – рабочее тело, совершающее круговой процесс. Q 1 > 0, A > 0, Q 2 < 0; T 1 > T 2.
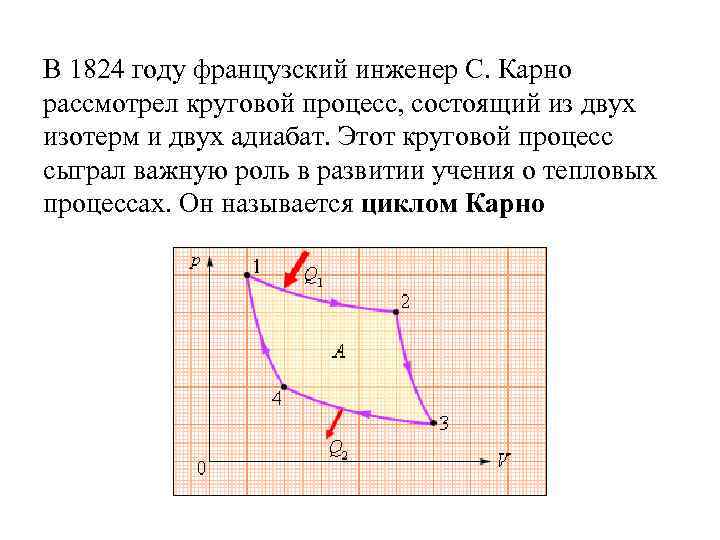 В 1824 году французский инженер С. Карно рассмотрел круговой процесс, состоящий из двух изотерм и двух адиабат. Этот круговой процесс сыграл важную роль в развитии учения о тепловых процессах. Он называется циклом Карно
В 1824 году французский инженер С. Карно рассмотрел круговой процесс, состоящий из двух изотерм и двух адиабат. Этот круговой процесс сыграл важную роль в развитии учения о тепловых процессах. Он называется циклом Карно
 Коэффициент полезного действия машины, работающей по циклу Карно: Q 1 количество теплоты, которое тепловая машина получает от нагревателя Q 2 количество теплоты, которое тепловая машина отдает холодильнику.
Коэффициент полезного действия машины, работающей по циклу Карно: Q 1 количество теплоты, которое тепловая машина получает от нагревателя Q 2 количество теплоты, которое тепловая машина отдает холодильнику.
 § 6. Испарение, конденсация, кипение. Насыщенные и ненасыщенные пары • Любое вещество при определенных условиях может находиться в различных агрегатных состояниях – твердом, жидком и газообразном. • Переход из одного состояния в другое называется фазовым переходом. • Испарение и конденсация являются примерами фазовых переходов. • Испарением называется фазовый переход из жидкого состояния в газообразное.
§ 6. Испарение, конденсация, кипение. Насыщенные и ненасыщенные пары • Любое вещество при определенных условиях может находиться в различных агрегатных состояниях – твердом, жидком и газообразном. • Переход из одного состояния в другое называется фазовым переходом. • Испарение и конденсация являются примерами фазовых переходов. • Испарением называется фазовый переход из жидкого состояния в газообразное.
 С точки зрения молекулярно-кинетической теории, испарение – это процесс, при котором с поверхности жидкости вылетают наиболее быстрые молекулы, кинетическая энергия которых превышает энергию их связи с остальными молекулами жидкости. Это приводит к уменьшению средней кинетической энергии оставшихся молекул, то есть к охлаждению жидкости (если нет подвода энергии от окружающих тел). Конденсация – это процесс, обратный процессу испарения. При конденсации молекулы пара возвращаются в жидкость.
С точки зрения молекулярно-кинетической теории, испарение – это процесс, при котором с поверхности жидкости вылетают наиболее быстрые молекулы, кинетическая энергия которых превышает энергию их связи с остальными молекулами жидкости. Это приводит к уменьшению средней кинетической энергии оставшихся молекул, то есть к охлаждению жидкости (если нет подвода энергии от окружающих тел). Конденсация – это процесс, обратный процессу испарения. При конденсации молекулы пара возвращаются в жидкость.
 В закрытом сосуде жидкость и ее пар могут находиться в состоянии динамического равновесия, когда число молекул, вылетающих из жидкости, равно числу молекул, возвращающихся в жидкость из пара, то есть когда скорости процессов испарения и конденсации одинаковы. Пар, находящийся в равновесии со своей жидкостью, называют насыщенным. Давление насыщенного пара p 0 данного вещества зависит только от его температуры и не зависит от объема
В закрытом сосуде жидкость и ее пар могут находиться в состоянии динамического равновесия, когда число молекул, вылетающих из жидкости, равно числу молекул, возвращающихся в жидкость из пара, то есть когда скорости процессов испарения и конденсации одинаковы. Пар, находящийся в равновесии со своей жидкостью, называют насыщенным. Давление насыщенного пара p 0 данного вещества зависит только от его температуры и не зависит от объема


