7-Закон Максвелла.ppt
- Количество слайдов: 38
 Молекулярная физика 7
Молекулярная физика 7
 Функция распределения • Это значит, что равна доле частиц, скорости которых заключены в единичном интервале скоростей вблизи скорости. • Переходя к пределу, можно формулу переписать в виде:
Функция распределения • Это значит, что равна доле частиц, скорости которых заключены в единичном интервале скоростей вблизи скорости. • Переходя к пределу, можно формулу переписать в виде:
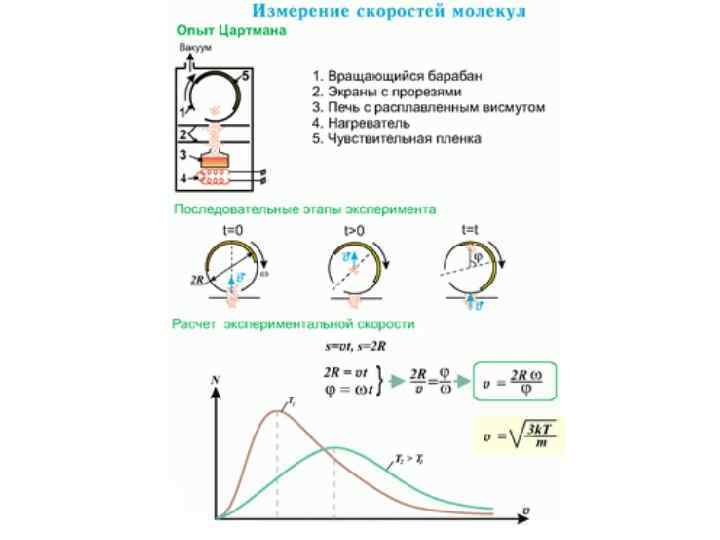
 Закон распределения скоростей Максвелла 1. Закон распределения скоростей Максвелла. 2. Средняя, средняя квадратичная и наиболее вероятная скорости молекул газа.
Закон распределения скоростей Максвелла 1. Закон распределения скоростей Максвелла. 2. Средняя, средняя квадратичная и наиболее вероятная скорости молекул газа.
 Распределение молекул по компонентам скорости Представим себе сосуд с газом, помещенный в пустое пространство в поле тяжести. Газ внутри сосуда находится в равновесии и его молекулы каким-то образом распределены по скоростям. Это распределение нам и требуется найти. Если в какой-то момент времени сосуд разбить, то молекулы газа станут двигаться по всем направлениям, в частности и вверх — против направления силы тяжести. Наличие силы тяжести и поможет нам найти то распределение, которое существовало в газе до того, как сосуд был разбит. Направим одну из координатных осей, например ось Z, по вертикали с началом отсчета в том месте, где находится сосуд. Ясно, что сила тяжести влияет только на zкомпоненту скорости молекул, так что будем искать распределение молекул не по скоростям, а по значениям составляющей скорости.
Распределение молекул по компонентам скорости Представим себе сосуд с газом, помещенный в пустое пространство в поле тяжести. Газ внутри сосуда находится в равновесии и его молекулы каким-то образом распределены по скоростям. Это распределение нам и требуется найти. Если в какой-то момент времени сосуд разбить, то молекулы газа станут двигаться по всем направлениям, в частности и вверх — против направления силы тяжести. Наличие силы тяжести и поможет нам найти то распределение, которое существовало в газе до того, как сосуд был разбит. Направим одну из координатных осей, например ось Z, по вертикали с началом отсчета в том месте, где находится сосуд. Ясно, что сила тяжести влияет только на zкомпоненту скорости молекул, так что будем искать распределение молекул не по скоростям, а по значениям составляющей скорости.
 Движение молекул вверх вдоль оси Z сопровождается уменьшением z-компоненты их скорости. Если, например, у некоторой молекулы на некоторой начальной высоте z 0 эта компонента была , то на высоте z справедливо соотношение закона сохранения энергии: (1) где — значение z-компоненты скорости на высоте z. Ясно, что те молекулы, у которых кинетическая энергия , не могут подняться до высоты, большей чем z. Для них наивысшая точка подъема z определяется равенством На этой высоте у таких молекул становится равной нулю, после чего они падают, ускоряясь, как всякое тело, брошенное вертикально вверх.
Движение молекул вверх вдоль оси Z сопровождается уменьшением z-компоненты их скорости. Если, например, у некоторой молекулы на некоторой начальной высоте z 0 эта компонента была , то на высоте z справедливо соотношение закона сохранения энергии: (1) где — значение z-компоненты скорости на высоте z. Ясно, что те молекулы, у которых кинетическая энергия , не могут подняться до высоты, большей чем z. Для них наивысшая точка подъема z определяется равенством На этой высоте у таких молекул становится равной нулю, после чего они падают, ускоряясь, как всякое тело, брошенное вертикально вверх.
 Выделим на некоторой произвольной высоте z слой газа высотой dz с площадью основания, равной единице (рис. ) Газ в этом слое состоит из движущихся молекул. Это молекулы, проходящие через него снизу вверх и сверху вниз (напомним, что нас интересуют только составляющие скоростей молекул по оси Z). Разница между молекулами, приходящими снизу и сверху, в том, что молекулы, приходящие снизу, имеют z-компоненты скоростей, которые по модулю непременно превышают значение , в то время как молекулы, приходящие сверху, могут иметь, zкомпоненты скорости любых значений, от 0 до ∞. В условиях равновесия, когда число молекул в слое должно быть постоянным, число молекул, проходящих сверху вниз, должно быть равно числу молекул, проходящих снизу вверх.
Выделим на некоторой произвольной высоте z слой газа высотой dz с площадью основания, равной единице (рис. ) Газ в этом слое состоит из движущихся молекул. Это молекулы, проходящие через него снизу вверх и сверху вниз (напомним, что нас интересуют только составляющие скоростей молекул по оси Z). Разница между молекулами, приходящими снизу и сверху, в том, что молекулы, приходящие снизу, имеют z-компоненты скоростей, которые по модулю непременно превышают значение , в то время как молекулы, приходящие сверху, могут иметь, zкомпоненты скорости любых значений, от 0 до ∞. В условиях равновесия, когда число молекул в слое должно быть постоянным, число молекул, проходящих сверху вниз, должно быть равно числу молекул, проходящих снизу вверх.
 На высоте z 0 число молекул в единице объема с zкомпонентами скорости, лежащими в интервале от определяется равенством до В единицу времени наш слой на высоте z пересекают таких молекул. Общее же число молекул, пересекающих слой снизу вверх (обозначим это число через N↑), равно Таким же образом мы получим, что число молекул, пересекающих слой сверху вниз (N↓), равно
На высоте z 0 число молекул в единице объема с zкомпонентами скорости, лежащими в интервале от определяется равенством до В единицу времени наш слой на высоте z пересекают таких молекул. Общее же число молекул, пересекающих слой снизу вверх (обозначим это число через N↑), равно Таким же образом мы получим, что число молекул, пересекающих слой сверху вниз (N↓), равно
 При равновесии, как указывалось, N↑ и N↓ должны быть равны другу, Разделив обе части этого равенства на согласно барометрической формуле и имея в виду, что , получаем: (2) Из закона сохранения энергии (1) дифференцированием получаем (имея в виду, что значение z фиксировано):
При равновесии, как указывалось, N↑ и N↓ должны быть равны другу, Разделив обе части этого равенства на согласно барометрической формуле и имея в виду, что , получаем: (2) Из закона сохранения энергии (1) дифференцированием получаем (имея в виду, что значение z фиксировано):
 Заменим под интегралом в левой части равенства (2) значение на равное ему значение. При этом нижний предел интегрирования нужно заменить нулем, так что Отсюда следует, что , или (3) Имея в виду формулу закона сохранения энергии (1), нетрудно видеть, что равенство (3) может быть справедливым, если только и
Заменим под интегралом в левой части равенства (2) значение на равное ему значение. При этом нижний предел интегрирования нужно заменить нулем, так что Отсюда следует, что , или (3) Имея в виду формулу закона сохранения энергии (1), нетрудно видеть, что равенство (3) может быть справедливым, если только и
 где А — некоторая постоянная. Чтобы в этом убедиться, достаточно подставить эти функции в формулу (3), принимая во внимание (1). При любом другом виде функции распределения уравнение (3) не будет совместимо с законом сохранения энергии. Итак, функция распределения молекул по составляющим скорости по оси Z имеет вид (4) Число молекул в единице объема, z-компоненты которых лежат в интервале от до , выражается теперь формулой , или
где А — некоторая постоянная. Чтобы в этом убедиться, достаточно подставить эти функции в формулу (3), принимая во внимание (1). При любом другом виде функции распределения уравнение (3) не будет совместимо с законом сохранения энергии. Итак, функция распределения молекул по составляющим скорости по оси Z имеет вид (4) Число молекул в единице объема, z-компоненты которых лежат в интервале от до , выражается теперь формулой , или
 Как уже указывалось, представляет собой вероятность того, что z-компонента скорости любой молекулы газа равна с точностью до. Нам остается еще определить постоянную А, входящую в функцию распределения. Для этого достаточно проинтегрировать по всем возможным значениям от - ∞ до + ∞. Тогда мы получим вероятность того, что молекула газа обладает скоростью с каким-то значением z-компоненты. А такая вероятность равна единице, так как о любой молекуле можно с достоверностью утверждать, что она обладает какой-то z-компонентой скорости (значение = 0 ничем не хуже всякого другого!). Таким образом,
Как уже указывалось, представляет собой вероятность того, что z-компонента скорости любой молекулы газа равна с точностью до. Нам остается еще определить постоянную А, входящую в функцию распределения. Для этого достаточно проинтегрировать по всем возможным значениям от - ∞ до + ∞. Тогда мы получим вероятность того, что молекула газа обладает скоростью с каким-то значением z-компоненты. А такая вероятность равна единице, так как о любой молекуле можно с достоверностью утверждать, что она обладает какой-то z-компонентой скорости (значение = 0 ничем не хуже всякого другого!). Таким образом,
 Для вычисления этого интеграла введем новую переменную. Тогда и Поэтому
Для вычисления этого интеграла введем новую переменную. Тогда и Поэтому
 Известно, что . Следовательно А интересующая нас постоянная А в уравнении (4) равна
Известно, что . Следовательно А интересующая нас постоянная А в уравнении (4) равна
 Выражение же для функции распределения принимает вид: (5) Графически эта функция имеет вид, изображенный на рис. Из графика видно, что функция стремится к нулю при. Но доля молекул с z-компонентой скорости, равной нулю, не равна нулю. Как видно из формулы (5) и из кривой рис. , доля молекул, z-компоненты скоростей которых близки к нулю, равна А (в этом и состоит физический смысл этой постоянной). С повышением температуры доля таких молекул уменьшается.
Выражение же для функции распределения принимает вид: (5) Графически эта функция имеет вид, изображенный на рис. Из графика видно, что функция стремится к нулю при. Но доля молекул с z-компонентой скорости, равной нулю, не равна нулю. Как видно из формулы (5) и из кривой рис. , доля молекул, z-компоненты скоростей которых близки к нулю, равна А (в этом и состоит физический смысл этой постоянной). С повышением температуры доля таких молекул уменьшается.
 Функцию распределения молекул по составляющим скорости мы получили, рассматривая газ в поле силы тяжести. Напомним, что это не значит, что вид распределения молекул по составляющим скорости как-то связан с действием силы тяжести или что именно сила тяжести и создает это распределение. Как уже указывалось, барометрическая формула, которой мы воспользовались при выводе, сама является следствием распределения молекул по скоростям. Роль силы тяжести в нашем выводе состояла только в том, что она «проявила» существовавшее в газе распределение. То, что сила тяжести не играет роли в установлении распределения, видно уже из того, что в функцию распределения не входит величина g, характеризующая силу тяжести.
Функцию распределения молекул по составляющим скорости мы получили, рассматривая газ в поле силы тяжести. Напомним, что это не значит, что вид распределения молекул по составляющим скорости как-то связан с действием силы тяжести или что именно сила тяжести и создает это распределение. Как уже указывалось, барометрическая формула, которой мы воспользовались при выводе, сама является следствием распределения молекул по скоростям. Роль силы тяжести в нашем выводе состояла только в том, что она «проявила» существовавшее в газе распределение. То, что сила тяжести не играет роли в установлении распределения, видно уже из того, что в функцию распределения не входит величина g, характеризующая силу тяжести.
 Распределение молекул по скоростям Полученное только что выражение для функции распределения молекул газа по z-компонентам скоростей не может быть «привилегией» именно z-компоненты скорости. Очевидно, что совершенно такие же выражения должны определять и распределения молекул по другим компонентам скоростей, так что ,
Распределение молекул по скоростям Полученное только что выражение для функции распределения молекул газа по z-компонентам скоростей не может быть «привилегией» именно z-компоненты скорости. Очевидно, что совершенно такие же выражения должны определять и распределения молекул по другим компонентам скоростей, так что ,
 Теперь мы можем найти и вероятность того, что скорость молекулы удовлетворяет одновременно трем условиям: 1. ее составляющая по оси X лежит в пределах 2. составляющая по оси У лежит в пределах от 3. составляющая по оси Z лежит в пределах от Значения составляющих скорости по каждой из осей координат не зависят от значений составляющих по другим осям. Поэтому вероятность того, что скорость молекулы одновременно удовлетворяет трем указанным условиям, есть вероятность сложного «события» . А она, как мы знаем, равна произведению вероятностей каждого из событий в отдельности. Если мы обозначим через число молекул в единице объема газа, составляющие которых по осям координат лежат в пределах, указанных выше, то мы можем написать:
Теперь мы можем найти и вероятность того, что скорость молекулы удовлетворяет одновременно трем условиям: 1. ее составляющая по оси X лежит в пределах 2. составляющая по оси У лежит в пределах от 3. составляющая по оси Z лежит в пределах от Значения составляющих скорости по каждой из осей координат не зависят от значений составляющих по другим осям. Поэтому вероятность того, что скорость молекулы одновременно удовлетворяет трем указанным условиям, есть вероятность сложного «события» . А она, как мы знаем, равна произведению вероятностей каждого из событий в отдельности. Если мы обозначим через число молекул в единице объема газа, составляющие которых по осям координат лежат в пределах, указанных выше, то мы можем написать:
 где . Отсюда или (6) Эта формула показывает, сколько молекул из числа находящихся в единице объема газа обладают скоростями, составляющие которых по осям координат лежат в интервалах между и , и , т. е. обладают скоростью, лежащей в интервале, заданном и по величине, и по направлению. Этой формуле можно дать наглядное геометрическое толкование.
где . Отсюда или (6) Эта формула показывает, сколько молекул из числа находящихся в единице объема газа обладают скоростями, составляющие которых по осям координат лежат в интервалах между и , и , т. е. обладают скоростью, лежащей в интервале, заданном и по величине, и по направлению. Этой формуле можно дать наглядное геометрическое толкование.
 Представим себе, что мы собрали все молекулы единицы объема газа, компоненты скорости которых заключены в указанных выше интервалах , и выпустили их. Через 1 секунду все они окажутся на расстоянии от начального положения в параллелепипеде со сторонами т. е. в объеме Это показано на рис. , на котором наш мысленный опыт представлен в своеобразной системе координат, по осям которой отложены составляющие. Число молекул, отнесенное к единице объема этого параллелепипеда (не путать с числом молекул в единице объема газа; здесь идет речь о единице объема в «пространстве» скоростей), равно
Представим себе, что мы собрали все молекулы единицы объема газа, компоненты скорости которых заключены в указанных выше интервалах , и выпустили их. Через 1 секунду все они окажутся на расстоянии от начального положения в параллелепипеде со сторонами т. е. в объеме Это показано на рис. , на котором наш мысленный опыт представлен в своеобразной системе координат, по осям которой отложены составляющие. Число молекул, отнесенное к единице объема этого параллелепипеда (не путать с числом молекул в единице объема газа; здесь идет речь о единице объема в «пространстве» скоростей), равно
 Величина эта не может, конечно, зависеть от направления вектора скорости. Поэтому нетрудно теперь найти и функцию распределения молекул по скоростям независимо от их направления. Действительно, если собрать вместе все молекулы единицы объема газа, скорости которых заключены в интервале от до по всем направлениям и выпустить их, то они, разлетаясь по всем направлениям, через 1 секунду окажутся равномерно распределенными в шаровом слое толщиной и радиусом (рис. ). Этот шаровой слой складывается из тех «параллелепипедов» , о которых говорилось выше. Число молекул в единице объема этого слоя (его, опять-таки, нельзя путать с числом молекул в единице объема газа) такое же, как и в каждом параллелепипеде, т. е. определяется формулой (6).
Величина эта не может, конечно, зависеть от направления вектора скорости. Поэтому нетрудно теперь найти и функцию распределения молекул по скоростям независимо от их направления. Действительно, если собрать вместе все молекулы единицы объема газа, скорости которых заключены в интервале от до по всем направлениям и выпустить их, то они, разлетаясь по всем направлениям, через 1 секунду окажутся равномерно распределенными в шаровом слое толщиной и радиусом (рис. ). Этот шаровой слой складывается из тех «параллелепипедов» , о которых говорилось выше. Число молекул в единице объема этого слоя (его, опять-таки, нельзя путать с числом молекул в единице объема газа) такое же, как и в каждом параллелепипеде, т. е. определяется формулой (6).
![• • d. V = [π(r + dr)2 - π r 2] ·b • • d. V = [π(r + dr)2 - π r 2] ·b](https://present5.com/presentation/3/136217509_155155259.pdf-img/136217509_155155259.pdf-24.jpg) • • d. V = [π(r + dr)2 - π r 2] ·b d. V = [πr 2 +2πrdr+ dr 2 - π r 2] ·b dr 2 << r d. V = 2πr·b·dr b
• • d. V = [π(r + dr)2 - π r 2] ·b d. V = [πr 2 +2πrdr+ dr 2 - π r 2] ·b dr 2 << r d. V = 2πr·b·dr b
 • • dΩ = 4/3 π(v + dv)3 – 4/3π v 3 dΩ = 4/3π(v 3 +3 v 2 dv+3 vdv 2 – v 3) dv 2 << v dΩ = 4/3π∙ 3 v 2 dv= 4πv 2 dv
• • dΩ = 4/3 π(v + dv)3 – 4/3π v 3 dΩ = 4/3π(v 3 +3 v 2 dv+3 vdv 2 – v 3) dv 2 << v dΩ = 4/3π∙ 3 v 2 dv= 4πv 2 dv
 Число же молекул во всем слое — это и есть число молекул в единице объема газа, скорости которых лежат в интервале от до. Число это, очевидно, равно где — объем шарового слоя, равный образом, . Таким или (7) Эта формула выражает закон Максвелла распределения молекул по скоростям.
Число же молекул во всем слое — это и есть число молекул в единице объема газа, скорости которых лежат в интервале от до. Число это, очевидно, равно где — объем шарового слоя, равный образом, . Таким или (7) Эта формула выражает закон Максвелла распределения молекул по скоростям.
 Величина — это вероятность того, что у произвольно выбранной молекулы газа скорость окажется лежащей в интервале между и . Иными словами, — это доля всех молекул единицы объема, скорости которых лежат в интервале от до. Величина (8) представляет собой функцию распределения молекул по скоростям. Она определяет долю молекул единицы объема газа, скорости которых заключены в интервале скоростей, равном единице, включающем данную скорость.
Величина — это вероятность того, что у произвольно выбранной молекулы газа скорость окажется лежащей в интервале между и . Иными словами, — это доля всех молекул единицы объема, скорости которых лежат в интервале от до. Величина (8) представляет собой функцию распределения молекул по скоростям. Она определяет долю молекул единицы объема газа, скорости которых заключены в интервале скоростей, равном единице, включающем данную скорость.
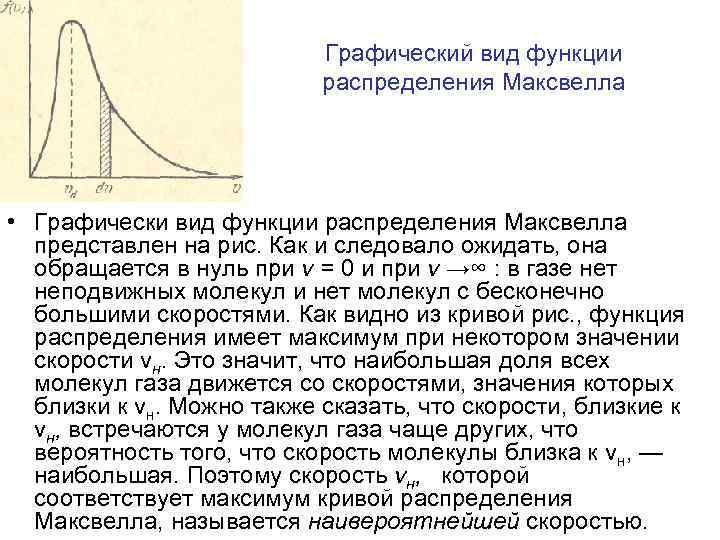 Графический вид функции распределения Максвелла • Графически вид функции распределения Максвелла представлен на рис. Как и следовало ожидать, она обращается в нуль при v = 0 и при v →∞ : в газе нет неподвижных молекул и нет молекул с бесконечно большими скоростями. Как видно из кривой рис. , функция распределения имеет максимум при некотором значении скорости vн. Это значит, что наибольшая доля всех молекул газа движется со скоростями, значения которых близки к vн. Можно также сказать, что скорости, близкие к vн, встречаются у молекул газа чаще других, что вероятность того, что скорость молекулы близка к vн, — наибольшая. Поэтому скорость vн, которой соответствует максимум кривой распределения Максвелла, называется наивероятнейшей скоростью.
Графический вид функции распределения Максвелла • Графически вид функции распределения Максвелла представлен на рис. Как и следовало ожидать, она обращается в нуль при v = 0 и при v →∞ : в газе нет неподвижных молекул и нет молекул с бесконечно большими скоростями. Как видно из кривой рис. , функция распределения имеет максимум при некотором значении скорости vн. Это значит, что наибольшая доля всех молекул газа движется со скоростями, значения которых близки к vн. Можно также сказать, что скорости, близкие к vн, встречаются у молекул газа чаще других, что вероятность того, что скорость молекулы близка к vн, — наибольшая. Поэтому скорость vн, которой соответствует максимум кривой распределения Максвелла, называется наивероятнейшей скоростью.
 • Чтобы лучше понять различие между распределением по скоростям и распределением по компонентам скоростей, рассмотрим аналогию с другим процессом, в котором, так же как в случае с установлением распределения молекул, главную роль играют законы случайности. • Представим себе, что производится стрельба в мишень, на которой целью служит точка в ее центре. Как бы ни был искусен стрелок и совершенно оружие, пули отнюдь не будут попадать точно в цель, а будут ложиться вблизи от нее на различных расстояниях от цели (рис. ). Это объясняется различными факторами, которые нельзя учесть: не вполне одинаковые заряды в патроне, влияние ветра и др.
• Чтобы лучше понять различие между распределением по скоростям и распределением по компонентам скоростей, рассмотрим аналогию с другим процессом, в котором, так же как в случае с установлением распределения молекул, главную роль играют законы случайности. • Представим себе, что производится стрельба в мишень, на которой целью служит точка в ее центре. Как бы ни был искусен стрелок и совершенно оружие, пули отнюдь не будут попадать точно в цель, а будут ложиться вблизи от нее на различных расстояниях от цели (рис. ). Это объясняется различными факторами, которые нельзя учесть: не вполне одинаковые заряды в патроне, влияние ветра и др.
 • В случае газа роль таких случайных факторов играют столкновения между молекулами. При достаточно большом числе выстрелов распределение пуль вокруг цели, т. е. распределение по расстояниям от нее, подчиняется, как оказывается, вполне определенному закону. Нетрудно выяснить характер этого закона. На рис. изображено распределение попаданий вокруг цели. Можно оценить это распределение двояким образом. • Можно разделить всю площадь мишени на кольцевые полосы , как это делается при соревнованиях по стрельбе, проведя ряд окружностей на равных расстояниях Δr друг от друга, и определять число попаданий Δn в каждой полосе, т. е. число попаданий, приходящихся на данное расстояние r от цели в интервале от r до r +Δr. В этом случае в центральном кружке, если он достаточно мал, число попаданий будет близко к нулю, потому что в достаточно малый кружок нельзя попасть. С увеличением расстояния кольцевой полосы от центра число попаданий в нее будет сначала расти, достигнет некоторого максимума, после чего оно будет убывать и на достаточном удалении от цели станет равным нулю (см. кривую на рис. ).
• В случае газа роль таких случайных факторов играют столкновения между молекулами. При достаточно большом числе выстрелов распределение пуль вокруг цели, т. е. распределение по расстояниям от нее, подчиняется, как оказывается, вполне определенному закону. Нетрудно выяснить характер этого закона. На рис. изображено распределение попаданий вокруг цели. Можно оценить это распределение двояким образом. • Можно разделить всю площадь мишени на кольцевые полосы , как это делается при соревнованиях по стрельбе, проведя ряд окружностей на равных расстояниях Δr друг от друга, и определять число попаданий Δn в каждой полосе, т. е. число попаданий, приходящихся на данное расстояние r от цели в интервале от r до r +Δr. В этом случае в центральном кружке, если он достаточно мал, число попаданий будет близко к нулю, потому что в достаточно малый кружок нельзя попасть. С увеличением расстояния кольцевой полосы от центра число попаданий в нее будет сначала расти, достигнет некоторого максимума, после чего оно будет убывать и на достаточном удалении от цели станет равным нулю (см. кривую на рис. ).
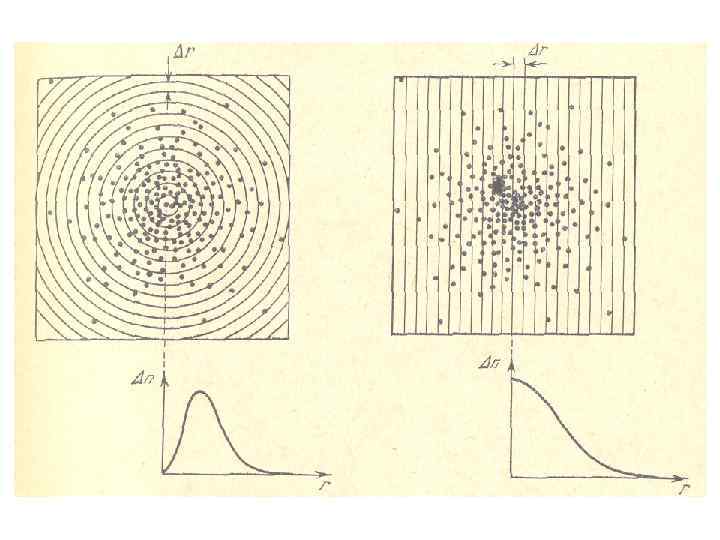
 • Можно поступить и другим путем. Разобьем площадь мишени на полосы, проведя ряд параллельных прямых, отстоящих друг от друга на таком же расстоянии Δr (рис. ). Если теперь определять число попаданий Δn , приходящихся на каждую полосу, то окажется, как это легко видеть из рисунка, что оно монотонно убывает по мере удаления от центральной полосы, стремясь к нулю на достаточно большом расстоянии от цели; это видно на кривой рис. • Первый из изложенных способов описания распределения соответствует определению функции f(v), второй — определению распределения f (vz) по компонентам скоростей.
• Можно поступить и другим путем. Разобьем площадь мишени на полосы, проведя ряд параллельных прямых, отстоящих друг от друга на таком же расстоянии Δr (рис. ). Если теперь определять число попаданий Δn , приходящихся на каждую полосу, то окажется, как это легко видеть из рисунка, что оно монотонно убывает по мере удаления от центральной полосы, стремясь к нулю на достаточно большом расстоянии от цели; это видно на кривой рис. • Первый из изложенных способов описания распределения соответствует определению функции f(v), второй — определению распределения f (vz) по компонентам скоростей.
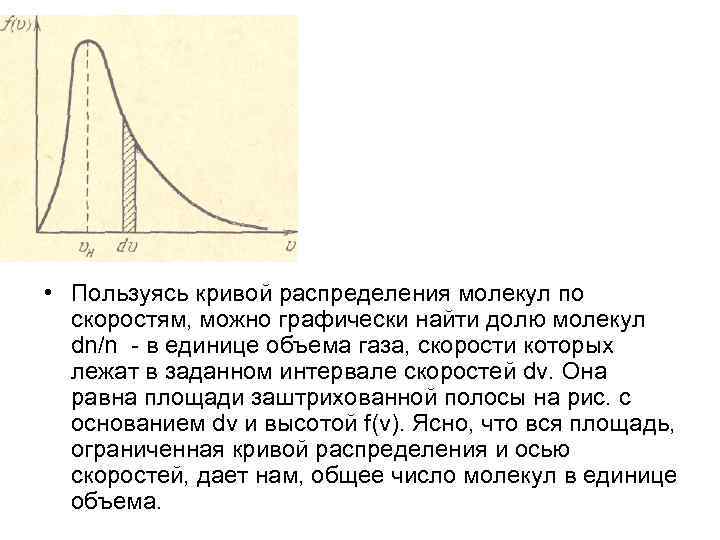 • Пользуясь кривой распределения молекул по скоростям, можно графически найти долю молекул dn/n - в единице объема газа, скорости которых лежат в заданном интервале скоростей dv. Она равна площади заштрихованной полосы на рис. с основанием dv и высотой f(v). Ясно, что вся площадь, ограниченная кривой распределения и осью скоростей, дает нам, общее число молекул в единице объема.
• Пользуясь кривой распределения молекул по скоростям, можно графически найти долю молекул dn/n - в единице объема газа, скорости которых лежат в заданном интервале скоростей dv. Она равна площади заштрихованной полосы на рис. с основанием dv и высотой f(v). Ясно, что вся площадь, ограниченная кривой распределения и осью скоростей, дает нам, общее число молекул в единице объема.
 • Как видно из формулы (8), вид кривой распределения зависит от природы газа (в формулу входит масса молекулы m) и от температуры. На рис. приведены кривые распределения молекул азота по скоростям при различных температурах. Из них видно, что при повышении температуры скорости молекул возрастают, так что вся кривая смещается в сторону больших скоростей. Но площади, ограниченные кривыми и осью скоростей, остаются, конечно, неизменными. Вследствие этого максимум кривой, при повышении температуры уменьшается.
• Как видно из формулы (8), вид кривой распределения зависит от природы газа (в формулу входит масса молекулы m) и от температуры. На рис. приведены кривые распределения молекул азота по скоростям при различных температурах. Из них видно, что при повышении температуры скорости молекул возрастают, так что вся кривая смещается в сторону больших скоростей. Но площади, ограниченные кривыми и осью скоростей, остаются, конечно, неизменными. Вследствие этого максимум кривой, при повышении температуры уменьшается.