5-Броуновское движение.ppt
- Количество слайдов: 55

Молекулярная физика 5

Броуновское движение 1. Равномерное распределение кинетической энергии по степеням свободы. 2. Теория Эйнштейна-Смолуховского.

X m 1 n 1 v 1 P 2 m 2 n 2 v 2 M • На предыдущей лекции мы доказали, что • при некоторых ограничениях. • Одно из ограничений состояло в том, что поршень, мог свободно перемещаться только в одном направлении - вдоль оси цилиндра или оси ОХ. • О такой ситуации кратко говорят, что поршень имеет одну степень свободы.
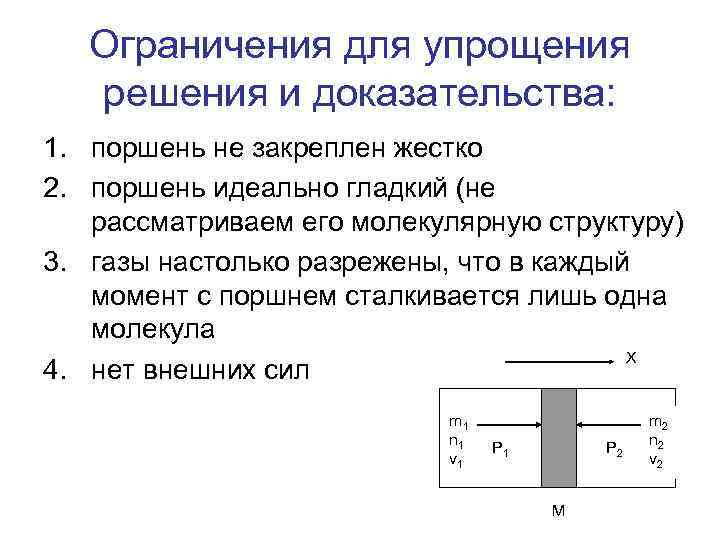
Ограничения для упрощения решения и доказательства: 1. поршень не закреплен жестко 2. поршень идеально гладкий (не рассматриваем его молекулярную структуру) 3. газы настолько разрежены, что в каждый момент с поршнем сталкивается лишь одна молекула X 4. нет внешних сил m 1 n 1 v 1 P 2 M m 2 n 2 v 2

• Для одной частицы идеального газа число степеней свободы равно 3, т. к. она могла перемещаться вдоль трех осей X, Y, Z. • Благодаря равновероятному характеру движения вдоль этих осей • Учтем далее, что

• Полученное нами соотношение • Отражает содержание известной теоремы о «Равномерном распределении кинетической энергии по степеням свободы» . • Но понятие о степенях свободы у нас было интуитивное.

• Число степеней свободы — число независимых переменных, которые определяют состояние системы. • В механике для тела их 6: • (3 координаты и 3 компоненты скорости) • • Е-функция Еп -координаты=3 степени состояния Ек - скорости=3 степени Но для идеального газа Еп=0 → только Ек≠ 0 и всего 3 степени свободы.

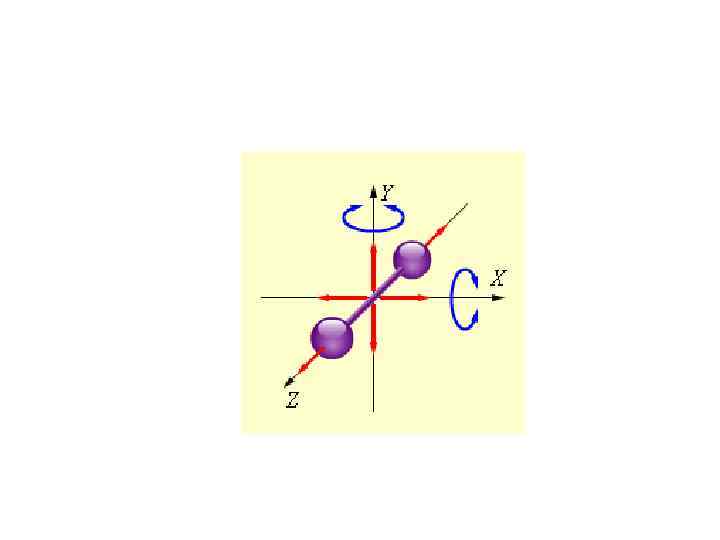
Число степеней свободы молекулы. Закон равномерного распределения энергии по степеням свободы молекул • Число степеней свободы — число независимых переменных (координат), полностью определяющих положение системы в пространстве. В ряде задач молекулу одноатомного газа (рис. , а) рассматривают как материальную точку, которой приписывают три степени свободы поступательного движения. При этом энергию вращательного движения можно не учитывать (r→ 0, I=mr 2→ 0, Tвр=Iω2/2→ 0)

Число степеней свободы молекулы. Закон равномерного распределения энергии по степеням свободы молекул • В классической механике молекула двухатомного газа в первом приближении рассматривается как совокупность двух материальных точек, жестко связанных недеформируемой связью (рис. , б). Эта система кроме трех степеней свободы поступательного движения имеет еще две степени свободы вращательного движения. Вращение вокруг третьей оси (оси, проходящей через оба атома) лишено смысла. Таким образом, двухатомный газ обладает пятью степенями свободы (i = 5). Трехатомная (рис. , в) и многоатомная нелинейные молекулы имеют шесть степеней свободы: три поступательных и три вращательных. Естественно, что жесткой связи между атомами не существует. Поэтому для реальных молекул необходимо учитывать также степени свободы колебательного движения.

Закон равномерного распределения энергии по степеням свободы молекул • Независимо от общего числа степеней свободы молекул три степени свободы всегда поступательные. Ни одна из поступательных степеней свободы не имеет преимущества перед другими, поэтому на каждую из них приходится в среднем одинаковая энергия, равная 1/3 значении <ε 0> :

Закон равномерного распределения энергии по степеням свободы молекул • В классической статистической физике выводится закон Больцмана о равномерном распределении энергии по степеням свободы молекул: • для статистической системы, находящейся в состоянии термодинамического равновесия, на каждую поступательную и вращательную степени свободы приходится в среднем кинетическая энергия, равная k. T/2, а на каждую колебательную степень свободы — в среднем энергия, равная k. T. Колебательная степень «обладает» вдвое большей энергией потому, что на нее приходится не только кинетическая энергия (как в случае поступательного и вращательного движений), но и потенциальная, причем средние значения кинетической и потенциальной энергий одинаковы. Таким образом, средняя энергия молекулы • где i — сумма числа поступательных, числа вращательных и удвоенного числа колебательных степеней свободы молекулы i = iпост + iвращ + 2 iколеб В классической теории рассматривают молекулы с жесткой связью между атомами; для них i совпадает с числом степеней свободы молекулы.



Учет ограничений • Разберемся, что будет с нашими результатами, а именно, смыслом температуры и теоремой о равномерном распределении энергии по степеням свободы при учете ограничений: 1. 2. поршень не закреплен жестко поршень идеально гладкий (не рассматриваем его молекулярную структуру) газы настолько разрежены, что в каждый момент с поршнем сталкивается лишь одна молекула нет внешних сил 3. 4.

Поршень не закреплен жестко • Пусть теперь он не свободен и удерживается в положении равновесия, например, пружиной с жесткостью κ. Если масса поршня М, то период его колебаний • удара молекулы. • Т. е. колебания поршня не почувствуют удары отдельных молекул. Поэтому наличие пружины (закрепление поршня) не влияет на результат.

Тепловые колебания поршня на пружине • • • Согласно классической теореме о равномерном распределении кинетической энергии по степеням свободы средняя кинетическая энергия, приходящаяся при тепловом равновесии на одну степень свободы любой атомно-молекулярной структуры, равна k. T/2, где k - постоянная Больцмана, T- температура. Рассмотрим поршень на пружине, помещённый в газ. Такая механическая система, если отвлечься от её молекулярного строения, обладает одной степенью свободы, т. к. положение поршня определяется единственной координатой x. Под действием нескомпенсированных ударов молекул поршень будет совершать хаотические движения относительно положения равновесия. Если состояние всей системы установилось, т. е. макроскопический процесс теплообмена закончился, то средняя кинетическая энергия движения поршня вдоль оси цилиндра равна средней кинетической энергии движения молекулы газа в том же направлении k. T/2. При хаотических колебаниях поршня на пружине его кинетическая энергия будет переходить в потенциальную энергию деформации пружины и наоборот. Нетрудно показать, что среднее значение кинетической и потенциальной энергий одинаковы. Таким образом, приравняв среднюю потенциальную энергию колебаний поршня на пружине к средней энергии k. T/2 мы находим среднеквадратическую амплитуду тепловых колебаний поршня на пружине. Средняя потенциальная энергия равна α<x 2>/2, где α - жёсткость пружины, x - отклонение пружины от положения равновесия, < > означает усреднение за большой промежуток времени. Поэтому <x 2>1/2 = (k. T/α)1/2 Для реальных механических систем амплитуда тепловых колебаний <x 2>1/2 очень мала. Однако в высокоточных измерительных системах, основанных на механических резонаторах, тепловые колебания являются фундаментальной причиной ограничивающей их максимальную чувствительность.

Поршень идеально гладкий • Учтем молекулярную структуру поршня. Для этого определим <εк> поступательного движения его молекул. • Если u скорость центра масс поршня, то • Возводя в квадрат и умножив на ½ М • Усредним теперь искомый результат по времени. При i≠j <uixujx>=0. Поэтому имеем

Поршень идеально гладкий • Пусть все mi одинаковы и их число во всем поршне равно N. Тогда имеем • Но мы уже получали соотношения такого типа при выводе смысла температуры • что позволяет нам записать • Полученное соотношение показывает, что и для молекул поршня на 1 степень свободы приходится ½k. T. Этот результат следовательно справедлив не только для разреженных газов.

M Газы разрежены, и в каждый момент времени с поршнем сталкивается лишь одна молекула • Это ограничение теперь можем убрать, т. к. и для сколь угодно плотного газа (поршень) имеем тот же результат. • Что будет если поршень убрать вовсе или вместо него поместить в газ какое-либо тело так, что оно охвачено газом мо всех сторон? • Ответ на первую часть вопроса очевиден – тоже ½k. T • Рассмотрим вторую часть. Пусть произвольное тело помещено в газообразную среду и может свободно двигаться в любом направлении. За счет ударов молекул о тело его центр масс будет совершать беспорядочное движение. Тогда <εк> для тела • Т. е. на поступательное движение центра масс тела приходится та же энергия, что и на поступательное движение одной молекулы. • Тело ведет себя как гигантская молекула!!! • Но М очень велика и <v> очень мала.

• Все рассмотренное выше является вескими аргументами в пользу теоремы о «Равномерном распределении кинетической энергии по степеням свободы» . • Строгое доказательство дается в статистической физике и базируется на двух положениях: 1. Применимости законов классической механики к атомно-молекулярным системам 2. Эргодической гипотезе, необходимой для согласования статистических и ТД методов описания.



Броуновское движение • Впервые наблюдал Броун в 1827 г. • Теория - Эйнштейн, Смолуховский (1905 г) • Сущность – частица в газе (жидкости) ведет себя подобно гигантской молекуле, т. е. дрожит (хаотически двигается) • Рассмотрим элементарную теорию эффекта • Идея – рассчитать <x 2> или - средний квадрат проекции на ось Х смещения частицы • -уравнение движения частицы (2 -й закон Ньютона) • r-радиус-вектор, F-равнодействующая сил

Броуновское движение • В проекции на ось Х • (1) • Среднее значение проекции смещения <x> будет равно нулю, т. к. смещение равновероятно как в положительном, так и в отрицательном направлении. Однако не будет равно рулю среднее значение квадрата смещения, т. е. <x 2> , т. к. x 2 не меняет знак, при изменении знака х. • Умножим обе части (1) на х: • (2)

Броуновское движение • Используем тождества • С учетом этих тождеств (2) можно переписать: • (3)

Броуновское движение • Выражение (3) справедливо для любой частицы и поэтому оно справедливо и для средних значений входящих в него величин, если усреднение вести по большому числу частиц. Усредняя имеем (4) <x. Fx>=0 т. к. x и Fx могут быть как положительными (+) так и отрицательными (-)

Величина в этом уравнении представляет собой среднее значение квадрата проекции скорости на ось X. Так как движения частиц вполне хаотичны, то средние значения квадратов проекций скорости по всем трем координатным осям должны быть равны другу, т. е.

Очевидно также, что сумма этих величин должна быть равна среднему значению квадрата скорости частиц : Следовательно, Таким образом, интересующее нас выражение, входящее в (4), равно:

Величина есть средняя кинетическая энергия броуновской частицы. Сталкиваясь с молекулами жидкости или газа, броуновские частицы обмениваются с ними энергией и находятся в тепловом равновесии со средой, в которой они движутся. Поэтому средняя кинетическая энергия поступательного движения броуновской частицы должна быть равна средней кинетической энергии молекул жидкости (или газа), которая, как мы знаем, равна : и следовательно (5)

То обстоятельство, что средняя кинетическая энергия броуновской частицы равна (как и для газовой молекулы!), имеет принципиальное значение. Действительно, выведенное нами ранее основное уравнение справедливо для любых не взаимодействующих друг с другом частиц, совершающих хаотические движения. Будут ли это невидимые глазом молекулы или значительно более крупные броуновские частицы, содержащие миллиарды молекул, — безразлично. С молекулярно-кинетической точки зрения броуновскую частицу можно трактовать как гигантскую молекулу. Поэтому выражение для средней кинетической энергии такой частицы должно быть таким же, как и для молекулы. Скорости же броуновских частиц, конечно, несравненно меньше, соответственно их большей массе. Вернемся теперь к уравнению (4) и, учтя (5), перепишем его в виде:

Это уравнение легко интегрируется. Обозначив получаем: , и после разделения переменных наше уравнение преобразуется в виде: Интегрируя левую часть этого уравнения в пределах от 0 до Z, а правую от 0 до t, получаем:

или Отсюда , потенцируя Величина , как легко убедиться, в обычных условиях опыта ничтожно мала за большое время. Для конечных промежутков времени Δt и соответствующих перемещений Δ<x 2> :

Обычно, частицы моделируются в виде шарика в жидкости. Тогда b=6πηα, где η – коэффициент вязкости жидкости, α – радиус частицы. Тогда - формула Стокса Отсюда (8) Среднее значение квадрата смещения броуновской частицы за промежуток времени Δt вдоль оси X, или любой другой оси, пропорционально этому промежутку времени.

Формула (8) позволяет вычислять среднее значение квадрата перемещений, причем среднее берется по всем частицам, участвующим в явлении. Но эта формула справедлива и для среднего значения квадрата многих последовательных перемещений одной-единственной частицы за равные промежутки времени. С экспериментальной точки зрения удобнее наблюдать именно перемещения одной частицы. Такие наблюдения и были проведены Перреном в 1909 г. Движение частиц Перрен наблюдал через микроскоп, окуляр которого был снабжен сеткой взаимно перпендикулярных линий, служивших координатной системой. Пользуясь этой сеткой, Перрен отмечал на ней последовательные положения одной облюбованной им частицы через определенные промежутки времени (например, 30 с). Соединив затем точки, отмечающие положения частицы на сетке, он получил картину, подобную той, которая изображена на рис. . На этом рисунке показаны как смещения частицы, так и их проекции на ось X.
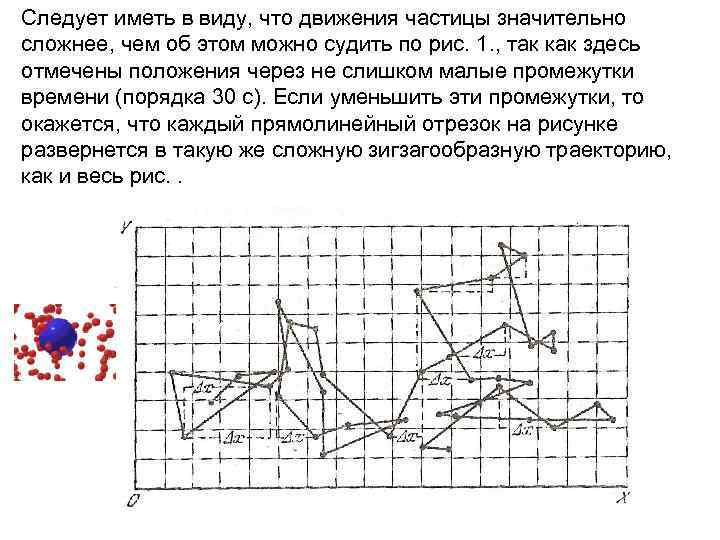
Следует иметь в виду, что движения частицы значительно сложнее, чем об этом можно судить по рис. 1. , так как здесь отмечены положения через не слишком малые промежутки времени (порядка 30 с). Если уменьшить эти промежутки, то окажется, что каждый прямолинейный отрезок на рисунке развернется в такую же сложную зигзагообразную траекторию, как и весь рис. .

Из своих наблюдений Перрен мог измерить смещения и вычислить среднее значение их квадратов. Данные этих измерений находились в хорошем согласии с формулой (8); тем самым была подтверждена правильность молекулярнокинетического объяснения явления броуновского движения и самой молекулярно-кинетической теории. Формула (8) может быть использована для определения постоянной Больцмана k, если известны значения вязкости η жидкости, ее температура Т и радиус частицы а. Значения этой постоянной, полученные Перреном и другими исследователями из подобных измерений, близки к приведенному выше значению эрг/град. Отметим здесь, что сам Перрен использовал полученные им данные для определения числа Авогадро по формуле , так как постоянная R может быть определена из уравнения состояния. Опыты Перрена имели большое значение для окончательного обоснования молекулярно-кинетической теории.

Броуновское движение (вариант) Выразив сразу силу трения f формулой Стокса

Для простоты предположим, что частица имеет форму сферы радиуса a. Тогда сила трения f может быть выражена формулой Стокса: где — коэффициент внутреннего трения жидкости (или газа), а - скорость движения частицы. Уравнение движения частицы (второй закон Ньютона) имеет поэтому вид: (1. 3. 1) Здесь т — масса частицы, r — ее радиус-вектор относительно произвольной системы координат, — скорость частицы и F - равнодействующая сил, вызванных ударами молекул. Рассмотрим проекцию радиуса-вектора на одну из координатных осей, например на ось X. Для этой составляющей уравнение (1. 3. 1) перепишется в виде: (1. 3. 2)

где Fх — составляющая результирующей силы F по оси X. Наша задача состоит в том, чтобы найти смещение x броуновской частицы, которое она получает под действием ударов молекул. Каждая из частиц все время подвергается соударениям с молекулами, после чего она меняет направление своего движения. Различные частицы получают смещения, отличающиеся как по величине, так и по направлению. Вероятное значение суммы смещений всех частиц равно нулю, так как смещения с равной вероятностью могут иметь и положительный, и отрицательный знак. Среднее значение проекции смещения частиц будет поэтому равно нулю. Не будет, однако, равно нулю среднее значение квадрата смещения, т. е. величина , так как х2 не изменяет своего знака при изменении знака x. Преобразуем поэтому уравнение (1. 3. 2) так, чтобы в него входила величина . Для этого умножим обе части этого уравнения на х: (1. 3. 3)

Используем очевидные тождества: , . Подставив эти выражения в (1. 3. 3), получим: Это равенство справедливо для любой частицы, и поэтому оно справедливо также и для средних значений входящих в него величин, если усреднение вести по достаточно большому числу частиц. Поэтому можно написать:

где - среднее значение квадрата перемещения частицы, а - среднее значение квадрата ее скорости. Что касается среднего значения величины , входящей в равенство, то оно равно нулю, так как для большого числа частиц x и Fx одинаково часто принимают как положительные, так и отрицательные значения. Уравнение (1. 3. 2) принимает поэтому вид: (1. 3. 4) Величина в этом уравнении представляет собой среднее значение квадрата проекций скорости на ось X. Так как движения частиц вполне хаотичны, то средние значения квадратов проекций скорости по всем трем координатным осям должны быть равны другу, т. е.

Очевидно также, что сумма этих величин должна быть равна среднему значению квадрата скорости частиц : Следовательно, Таким образом, интересующее нас выражение, входящее в (1. 3. 4), равно:

Величина есть средняя кинетическая энергия броуновской частицы. Сталкиваясь с молекулами жидкости или газа, броуновские частицы обмениваются с ними энергией и находятся в тепловом равновесии со средой, в которой они движутся. Поэтому средняя кинетическая энергия поступательного движения броуновской частицы должна быть равна средней кинетической энергии молекул жидкости (или газа), которая, как мы знаем, равна : и следовательно (1. 3. 5)

То обстоятельство, что средняя кинетическая энергия броуновской частицы равна (как и для газовой молекулы!), имеет принципиальное значение. Действительно, выведенное нами ранее основное уравнение справедливо для любых не взаимодействующих друг с другом частиц, совершающих хаотические движения. Будут ли это невидимые глазом молекулы или значительно более крупные броуновские частицы, содержащие миллиарды молекул, — безразлично. С молекулярно-кинетической точки зрения броуновскую частицу можно трактовать как гигантскую молекулу. Поэтому выражение для средней кинетической энергии такой частицы должно быть таким же, как и для молекулы. Скорости же броуновских частиц, конечно, несравненно меньше, соответственно их большей массе. Вернемся теперь к уравнению (1. 3. 4) и, учтя (1. 3. 5), перепишем его в виде:

Это уравнение легко интегрируется. Обозначив получаем: , и после разделения переменных наше уравнение преобразуется в виде: Интегрируя левую часть этого уравнения в пределах от 0 до Z, а правую от 0 до t, получаем:

или Отсюда Величина , как легко убедиться, в обычных условиях опыта ничтожно мала. Действительно, размеры броуновских частиц не превышают 10 -4 см, вязкость жидкости обычно близка к вязкости воды, т. е. приблизительно равна 10 -2 (в системе единиц СГС), плотность вещества частиц порядка единицы.

Имея в виду, что масса частицы т равна получим, что показатель степени что величиной , мы , при t > 10 -5 с, таков, можно пренебречь. Следовательно, если отрезок времени между последовательными наблюдениями за броуновской частицей превышает 10 -5 с, что, конечно, всегда имеет место, то (1. 3. 6)

Для конечных промежутков времени и соответствующих перемещений уравнение (1. 3. 6) можно переписать в виде: (1. 3. 6 а) Отсюда (1. 3. 7) Среднее значение квадрата смещения броуновской частицы за промежуток времени вдоль оси X, или любой другой оси, пропорционально этому промежутку времени.

Формула (1. 3. 7) позволяет вычислять среднее значение квадрата перемещений, причем среднее берется по всем частицам, участвующим в явлении. Но эта формула справедлива и для среднего значения квадрата многих последовательных перемещений одной-единственной частицы за равные промежутки времени. С экспериментальной точки зрения удобнее наблюдать именно перемещения одной частицы. Такие наблюдения и были проведены Перреном в 1909 г. Движение частиц Перрен наблюдал через микроскоп, окуляр которого был снабжен сеткой взаимно перпендикулярных линий, служивших координатной системой. Пользуясь этой сеткой, Перрен отмечал на ней последовательные положения одной облюбованной им частицы через определенные промежутки времени (например, 30 с). Соединив затем точки, отмечающие положения частицы на сетке, он получил картину, подобную той, которая изображена на рис. 1. 11. На этом рисунке показаны как смещения частицы, так и их проекции на ось X.
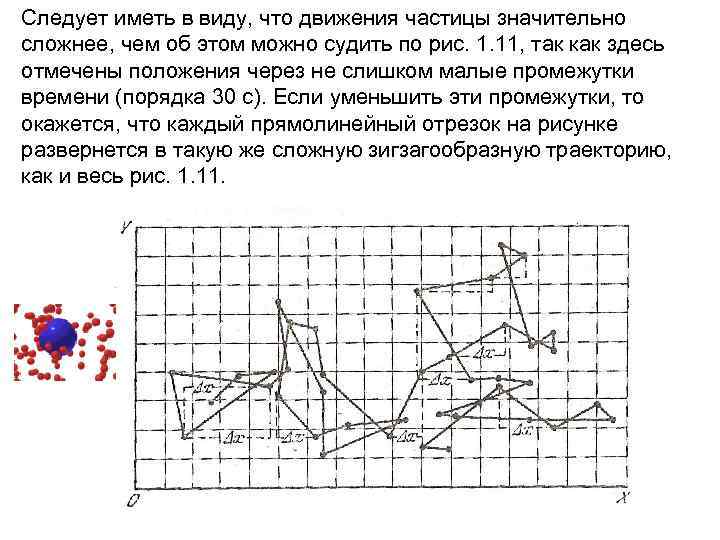
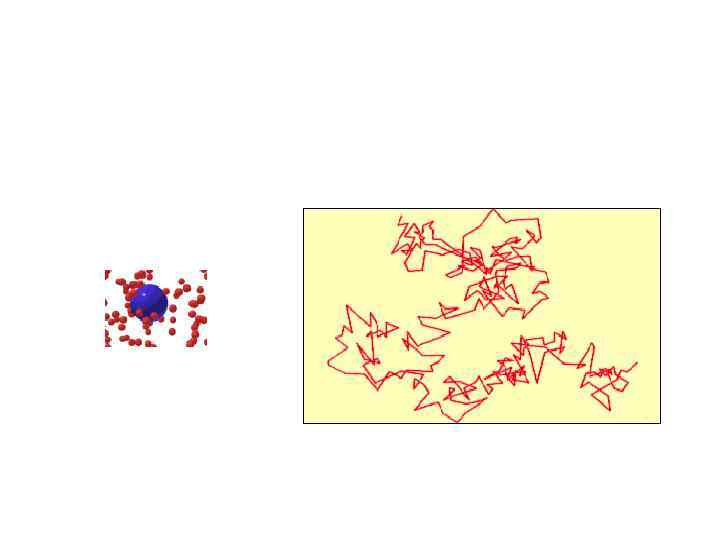
Следует иметь в виду, что движения частицы значительно сложнее, чем об этом можно судить по рис. 1. 11, так как здесь отмечены положения через не слишком малые промежутки времени (порядка 30 с). Если уменьшить эти промежутки, то окажется, что каждый прямолинейный отрезок на рисунке развернется в такую же сложную зигзагообразную траекторию, как и весь рис. 1. 11.

Из своих наблюдений Перрен мог измерить смещения и вычислить среднее значение их квадратов. Данные этих измерений находились в хорошем согласии с формулой (1. 3. 7); тем самым была подтверждена правильность молекулярнокинетического объяснения явления броуновского движения и самой молекулярно-кинетической теории. Формула (1. 3. 7) может быть использована для определения постоянной Больцмана k, если известны значения вязкости η жидкости, ее температура Т и радиус частицы а. Значения этой постоянной, полученные Перреном и другими исследователями из подобных измерений, близки к приведенному выше значению эрг/град. Отметим здесь, что сам Перрен использовал полученные им данные для определения числа Авогадро по формуле , так как постоянная R может быть определена из уравнения состояния. Опыты Перрена имели большое значение для окончательного обоснования молекулярно-кинетической теории.

• • • Все мельчайшие частицы, взвешенные в жидкости (или газе), находятся в непрерывном хаотическом движении. Это явление было открыто в 1827 году английским ботаником Броуном (1773 -1858). Это движение тем оживлённее, чем выше температура и чем меньше вязкость среды. Его едва удаётся обнаружить в глицерине, а в газах оно, напротив, чрезвычайно интенсивно. Броуновское движение вызывается толчками, испытываемыми взвешенными частицами со стороны окружающих молекул, совершающих тепловое движение. Толчки никогда в точности не уравновешивают друга. Поэтому, под влиянием ударов молекул окружающей среды скорость броуновской частицы непрерывно и беспорядочно меняется по величине и направлению. Это и есть броуновское движение. Основной физический принцип лежащий в основе броуновского движения состоит в том, что средняя кинетическая энергия движения молекул жидкости (или газа) равна средней кинетической энергии любой частицы, подвешенной в этой среде. Поэтому средняя кинетическая энергия < E > поступательного движения броуновской частицы равна: < E > = m<v 2>/ 2 = 3 k. T/2, где m - масса броуновской частицы, v - её скорость, k - постоянная Больцмана, T - температура. Мы можем видеть из этой формулы, что средняя кинетическая энергия броуновской частицы, а значит и интенсивность её движения растёт с увеличением температуры.

• Броуновская частица будет двигаться по зигзагообразному пути, удаляясь постепенно от начальной точки. Вычисления показывают, что значение среднего квадрата смещения броуновской частицы r 2 = x 2 + y 2 + z 2 описывается формулой: • < r 2 > = 6 k. TBt • где B - подвижность частицы, которая обратно пропорциональна вязкости среды и размеру частицы. Эта формула, называемая формулой Эйнштейна, была со всей возможной тщательностью подтверждена экспериментально французским физиком Жаном Перреном (1870 -1942). На основе измерения параметров движения броуновской частицы Перрен получил значения постоянной Больцмана и число Авогадро, хорошо согласующиеся в пределах ошибок измерений со значениям, полученными другими методами.
5-Броуновское движение.ppt