4-Уравнение состояния идеального газа.ppt
- Количество слайдов: 36
 Молекулярная физика 4
Молекулярная физика 4
 1. Уравнение состояния и законы идеального газа 2. Закон Бойля — Мариотта 3. Закон Гей-Люссака 4. Закон Авогадро 5. Закон Дальтона
1. Уравнение состояния и законы идеального газа 2. Закон Бойля — Мариотта 3. Закон Гей-Люссака 4. Закон Авогадро 5. Закон Дальтона
 1. Уравнение состояния идеального газа. 2. Изопроцессы
1. Уравнение состояния идеального газа. 2. Изопроцессы
 Уравнение состояния идеального газа • Соотношение p = nk. T, связывающее давление газа с его температурой и концентрацией молекул, получено для модели идеального газа, молекулы которого взаимодействуют между собой и со стенками сосуда только во время упругих столкновений. Это соотношение может быть записано в другой форме, устанавливающей связь между макроскопическими параметрами газа – объемом V, давлением p, температурой T и количеством вещества ν. Для этого нужно использовать равенства
Уравнение состояния идеального газа • Соотношение p = nk. T, связывающее давление газа с его температурой и концентрацией молекул, получено для модели идеального газа, молекулы которого взаимодействуют между собой и со стенками сосуда только во время упругих столкновений. Это соотношение может быть записано в другой форме, устанавливающей связь между макроскопическими параметрами газа – объемом V, давлением p, температурой T и количеством вещества ν. Для этого нужно использовать равенства
 Уравнение состояния идеального газа • Здесь N – число молекул в сосуде, NA – постоянная Авогадро, m – масса газа в сосуде, M – молярная масса газа. В итоге получим:
Уравнение состояния идеального газа • Здесь N – число молекул в сосуде, NA – постоянная Авогадро, m – масса газа в сосуде, M – молярная масса газа. В итоге получим:
 Уравнение состояния идеального газа • Произведение постоянной Авогадро NA на постоянную Больцмана k называется универсальной газовой постоянной и обозначается буквой R. • Ее численное значение в СИ есть: • R = 8, 31 Дж/моль·К • Соотношение • называется уравнением состояния идеального газа.
Уравнение состояния идеального газа • Произведение постоянной Авогадро NA на постоянную Больцмана k называется универсальной газовой постоянной и обозначается буквой R. • Ее численное значение в СИ есть: • R = 8, 31 Дж/моль·К • Соотношение • называется уравнением состояния идеального газа.
 Закон Авогадро • Для одного моля любого газа это соотношение принимает вид: p. V=RT • Если температура газа равна Tн = 273, 15 К (0 °С), а давление pн = 1 атм = 1, 013· 105 Па, то говорят, что газ находится при нормальных условиях. Как следует из уравнения состояния идеального газа, один моль любого газа при нормальных условиях занимает один и тот же объем V 0, равный • V 0 = 0, 0224 м 3/моль = 22, 4 дм 3/моль • Это утверждение называется законом Авогадро.
Закон Авогадро • Для одного моля любого газа это соотношение принимает вид: p. V=RT • Если температура газа равна Tн = 273, 15 К (0 °С), а давление pн = 1 атм = 1, 013· 105 Па, то говорят, что газ находится при нормальных условиях. Как следует из уравнения состояния идеального газа, один моль любого газа при нормальных условиях занимает один и тот же объем V 0, равный • V 0 = 0, 0224 м 3/моль = 22, 4 дм 3/моль • Это утверждение называется законом Авогадро.
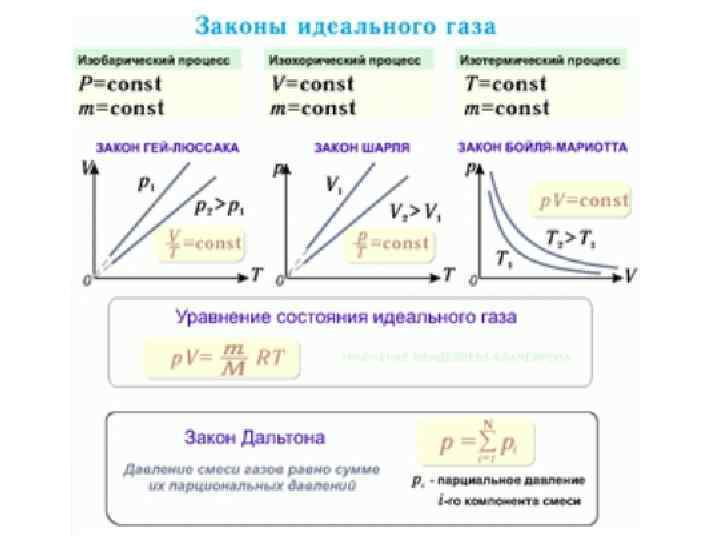
 Уравнение Клапейрона–Менделеева • Для смеси невзаимодействующих газов уравнение состояния принимает вид p. V = (ν 1 + ν 2 + ν 3 +. . . )RT, • где ν 1, ν 2, ν 3 и т. д. – количество вещества каждого из газов в смеси. • Уравнение, устанавливающее связь между давлением, объемом и температурой газа было получено в середине XIX века французским физиком Б. Клапейроном, в форме (p. V=m/M RT) оно было впервые записано Д. И. Менделеевым. Поэтому уравнение состояния газа называется уравнением Клапейрона–Менделеева. •
Уравнение Клапейрона–Менделеева • Для смеси невзаимодействующих газов уравнение состояния принимает вид p. V = (ν 1 + ν 2 + ν 3 +. . . )RT, • где ν 1, ν 2, ν 3 и т. д. – количество вещества каждого из газов в смеси. • Уравнение, устанавливающее связь между давлением, объемом и температурой газа было получено в середине XIX века французским физиком Б. Клапейроном, в форме (p. V=m/M RT) оно было впервые записано Д. И. Менделеевым. Поэтому уравнение состояния газа называется уравнением Клапейрона–Менделеева. •
 Уравнение Клапейрона–Менделеева • Следует отметить, что задолго до того, как уравнение состояния идеального газа было теоретически получено на основе молекулярно-кинетической модели, закономерности поведения газов в различных условиях были хорошо изучены экспериментально. Поэтому уравнение (Клапейрона–Менделеева p. V=m/M RT) можно рассматривать как обобщение опытных фактов, которые находят объяснение в молекулярно-кинетической теории.
Уравнение Клапейрона–Менделеева • Следует отметить, что задолго до того, как уравнение состояния идеального газа было теоретически получено на основе молекулярно-кинетической модели, закономерности поведения газов в различных условиях были хорошо изучены экспериментально. Поэтому уравнение (Клапейрона–Менделеева p. V=m/M RT) можно рассматривать как обобщение опытных фактов, которые находят объяснение в молекулярно-кинетической теории.
 Квазистатические процессы • Газ может участвовать в различных тепловых процессах, при которых могут изменяться все параметры, описывающие его состояние (p, V и T). Если процесс протекает достаточно медленно, то в любой момент система близка к своему равновесному состоянию. Такие процессы называются квазистатическими. В привычном для нас масштабе времени эти процессы могут протекать и не очень медленно. Например, разрежения и сжатия газа в звуковой волне, происходящие сотни раз в секунду, можно рассматривать как квазистатический процесс. Квазистатические процессы могут быть изображены на диаграмме состояний (например, в координатах p, V) в виде некоторой траектории, каждая точка которой представляет равновесное состояние.
Квазистатические процессы • Газ может участвовать в различных тепловых процессах, при которых могут изменяться все параметры, описывающие его состояние (p, V и T). Если процесс протекает достаточно медленно, то в любой момент система близка к своему равновесному состоянию. Такие процессы называются квазистатическими. В привычном для нас масштабе времени эти процессы могут протекать и не очень медленно. Например, разрежения и сжатия газа в звуковой волне, происходящие сотни раз в секунду, можно рассматривать как квазистатический процесс. Квазистатические процессы могут быть изображены на диаграмме состояний (например, в координатах p, V) в виде некоторой траектории, каждая точка которой представляет равновесное состояние.
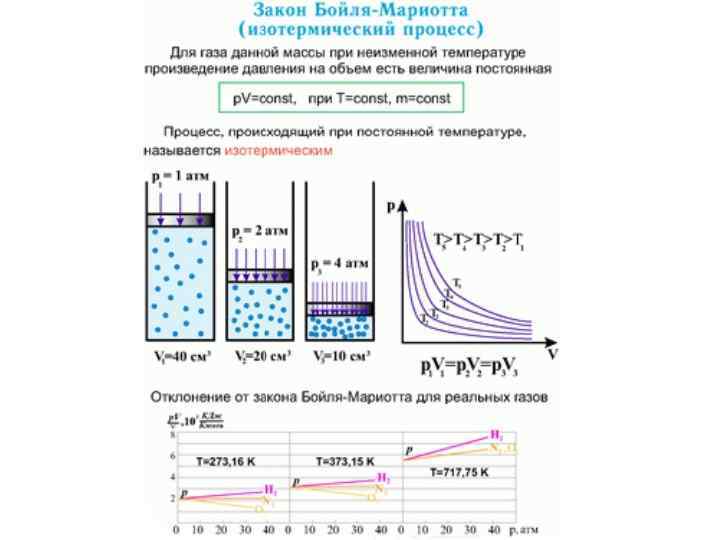
 Изотермический процесс • Интерес представляют процессы, в которых один из параметров (p, V или T) остается неизменным. Такие процессы называются изопроцессами. • Изотермический процесс (T = const) • Изотермическим процессом называют квазистатический процесс, протекающий при постоянной температуре T. Из уравнения состояния идеального газа (p. V= ν RT) следует, что при постоянной температуре T и неизменном количестве вещества ν в сосуде произведение давления p газа на его объем V должно оставаться постоянным: p. V = const
Изотермический процесс • Интерес представляют процессы, в которых один из параметров (p, V или T) остается неизменным. Такие процессы называются изопроцессами. • Изотермический процесс (T = const) • Изотермическим процессом называют квазистатический процесс, протекающий при постоянной температуре T. Из уравнения состояния идеального газа (p. V= ν RT) следует, что при постоянной температуре T и неизменном количестве вещества ν в сосуде произведение давления p газа на его объем V должно оставаться постоянным: p. V = const
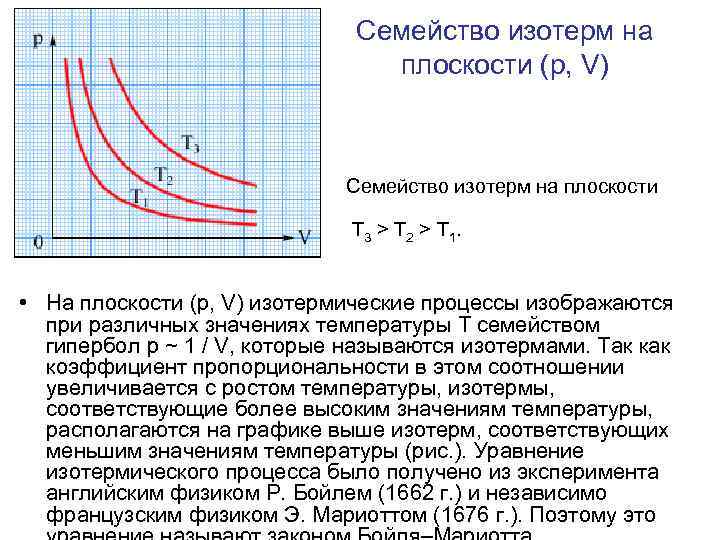 Семейство изотерм на плоскости (p, V) • Семейство изотерм на плоскости (p, V). • T 3 > T 2 > T 1. • На плоскости (p, V) изотермические процессы изображаются при различных значениях температуры T семейством гипербол p ~ 1 / V, которые называются изотермами. Так коэффициент пропорциональности в этом соотношении увеличивается с ростом температуры, изотермы, соответствующие более высоким значениям температуры, располагаются на графике выше изотерм, соответствующих меньшим значениям температуры (рис. ). Уравнение изотермического процесса было получено из эксперимента английским физиком Р. Бойлем (1662 г. ) и независимо французским физиком Э. Мариоттом (1676 г. ). Поэтому это
Семейство изотерм на плоскости (p, V) • Семейство изотерм на плоскости (p, V). • T 3 > T 2 > T 1. • На плоскости (p, V) изотермические процессы изображаются при различных значениях температуры T семейством гипербол p ~ 1 / V, которые называются изотермами. Так коэффициент пропорциональности в этом соотношении увеличивается с ростом температуры, изотермы, соответствующие более высоким значениям температуры, располагаются на графике выше изотерм, соответствующих меньшим значениям температуры (рис. ). Уравнение изотермического процесса было получено из эксперимента английским физиком Р. Бойлем (1662 г. ) и независимо французским физиком Э. Мариоттом (1676 г. ). Поэтому это
 Сжимаемость идеального газа. Изотермический коэффициент сжимаемости. • Свойство газа, как и всякого другого тела, изменять давление при изменении объема называется сжимаемостью. Если изменение объема происходит так, что температура газа при этом не меняется, то сжимаемость характеризуется изотермическим коэффициентом сжимаемости χ , который определяется как отноcительное изменение объема, вызывающее изменение давления на единицу. Очевидно, что
Сжимаемость идеального газа. Изотермический коэффициент сжимаемости. • Свойство газа, как и всякого другого тела, изменять давление при изменении объема называется сжимаемостью. Если изменение объема происходит так, что температура газа при этом не меняется, то сжимаемость характеризуется изотермическим коэффициентом сжимаемости χ , который определяется как отноcительное изменение объема, вызывающее изменение давления на единицу. Очевидно, что
 Изотермический коэффициент сжимаемости • Здесь d. V - изменение объема газа, вызывающее изменение давления на величину dр; V - первоначальный объем (относительным изменением какой-либо величины и называется отношение изменения этой величины к ее первоначальному значению). Индекс Т у производной показывает, что она берется при Т = соnst. • Для идеального газа легко вычислить значение χ. Из уравнения состояния (p. V= ν RT) получаем: • Отсюда • Знак минус указывает на то, что увеличение объема приводит к уменьшению давления.
Изотермический коэффициент сжимаемости • Здесь d. V - изменение объема газа, вызывающее изменение давления на величину dр; V - первоначальный объем (относительным изменением какой-либо величины и называется отношение изменения этой величины к ее первоначальному значению). Индекс Т у производной показывает, что она берется при Т = соnst. • Для идеального газа легко вычислить значение χ. Из уравнения состояния (p. V= ν RT) получаем: • Отсюда • Знак минус указывает на то, что увеличение объема приводит к уменьшению давления.
 Изотермический коэффициент сжимаемости • Изотермический коэффициент сжимаемости идеального газа равен, таким образом, обратной величине его давления и измеряется в системе СИ в единицах м 2/Н, а в системе СГС -в единицах см 2/дин. • С ростом давления величина χ , конечно, уменьшается, так как чем больше давление, тем меньше у газа возможностей для того, чтобы еще больше сжиматься.
Изотермический коэффициент сжимаемости • Изотермический коэффициент сжимаемости идеального газа равен, таким образом, обратной величине его давления и измеряется в системе СИ в единицах м 2/Н, а в системе СГС -в единицах см 2/дин. • С ростом давления величина χ , конечно, уменьшается, так как чем больше давление, тем меньше у газа возможностей для того, чтобы еще больше сжиматься.
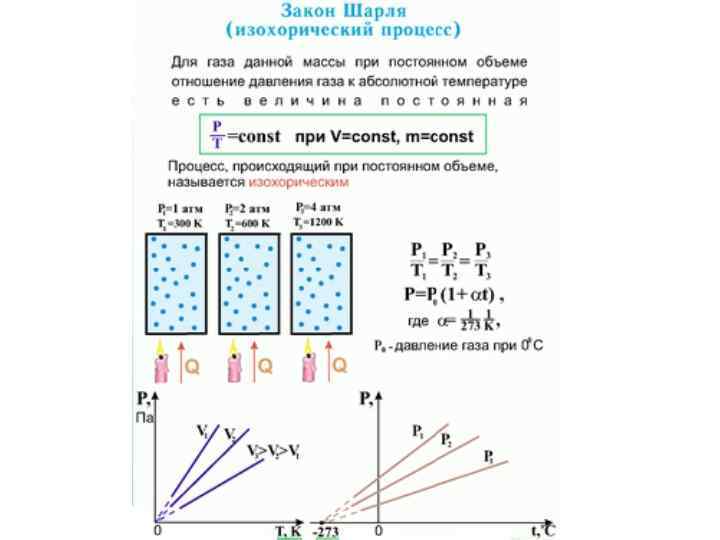
 Изохорный процесс • Изохорный процесс (V = const) • Изохорный процесс – это процесс квазистатического нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным.
Изохорный процесс • Изохорный процесс (V = const) • Изохорный процесс – это процесс квазистатического нагревания или охлаждения газа при постоянном объеме V и при условии, что количество вещества ν в сосуде остается неизменным.
 Изохорный процесс • Как следует из уравнения (p. V= ν RT) состояния идеального газа, при этих условиях давление газа p изменяется прямо пропорционально его абсолютной температуре: p ~ T или
Изохорный процесс • Как следует из уравнения (p. V= ν RT) состояния идеального газа, при этих условиях давление газа p изменяется прямо пропорционально его абсолютной температуре: p ~ T или
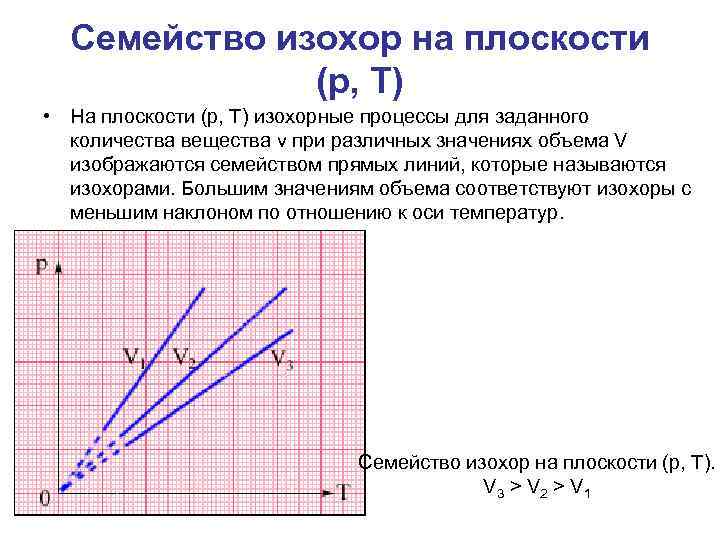 Семейство изохор на плоскости (p, T) • На плоскости (p, T) изохорные процессы для заданного количества вещества ν при различных значениях объема V изображаются семейством прямых линий, которые называются изохорами. Большим значениям объема соответствуют изохоры с меньшим наклоном по отношению к оси температур. • Семейство изохор на плоскости (p, T). V 3 > V 2 > V 1
Семейство изохор на плоскости (p, T) • На плоскости (p, T) изохорные процессы для заданного количества вещества ν при различных значениях объема V изображаются семейством прямых линий, которые называются изохорами. Большим значениям объема соответствуют изохоры с меньшим наклоном по отношению к оси температур. • Семейство изохор на плоскости (p, T). V 3 > V 2 > V 1
 Уравнение изохорного процесса • Экспериментально зависимость давления газа от температуры исследовал французский физик Ж. Шарль (1787 г. ). Поэтому уравнение изохорного процесса называется законом Шарля. • Уравнение изохорного процесса может быть записано в виде: • где p 0 – давление газа при T = T 0 = 273, 15 К (т. е. при температуре 0 °С). Коэффициент α, равный (1/273, 15) К– 1, называют температурным коэффициентом давления.
Уравнение изохорного процесса • Экспериментально зависимость давления газа от температуры исследовал французский физик Ж. Шарль (1787 г. ). Поэтому уравнение изохорного процесса называется законом Шарля. • Уравнение изохорного процесса может быть записано в виде: • где p 0 – давление газа при T = T 0 = 273, 15 К (т. е. при температуре 0 °С). Коэффициент α, равный (1/273, 15) К– 1, называют температурным коэффициентом давления.
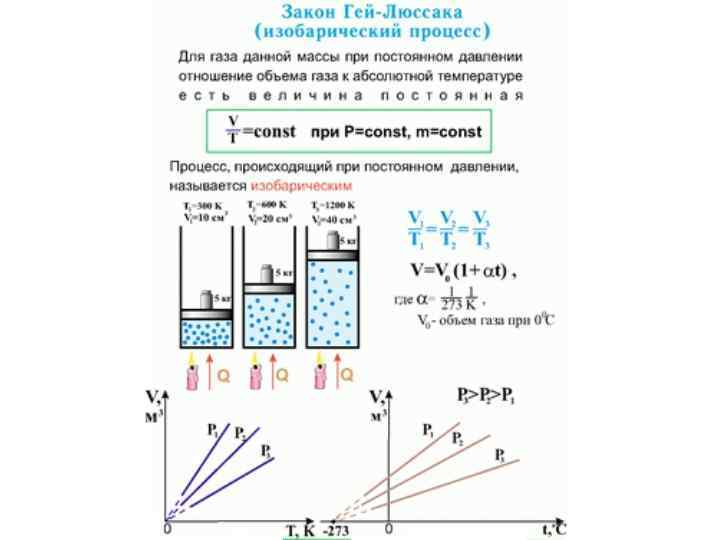
 Изобарный процесс • Изобарный процесс (p = const) • Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. • Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид: • или • где V 0 – объем газа при температуре 0 °С. Коэффициент α равен (1/273, 15) К– 1. Его называют температурным коэффициентом объемного расширения газов.
Изобарный процесс • Изобарный процесс (p = const) • Изобарным процессом называют квазистатический процесс, протекающий при неизменным давлении p. • Уравнение изобарного процесса для некоторого неизменного количества вещества ν имеет вид: • или • где V 0 – объем газа при температуре 0 °С. Коэффициент α равен (1/273, 15) К– 1. Его называют температурным коэффициентом объемного расширения газов.
 Коэффициент объемного расширения газа при постоянном давлении • Коэффициент объемного расширения α может быть представлен в виде, аналогичном коэффициенту сжимаемости: • Из уравнения состояния следует, что • Откуда • Т. е. коэффициент объемного расширения идеального газа равен обратной величине абсолютной температуры. При 0°С он равен 1/273, 15 К-1
Коэффициент объемного расширения газа при постоянном давлении • Коэффициент объемного расширения α может быть представлен в виде, аналогичном коэффициенту сжимаемости: • Из уравнения состояния следует, что • Откуда • Т. е. коэффициент объемного расширения идеального газа равен обратной величине абсолютной температуры. При 0°С он равен 1/273, 15 К-1
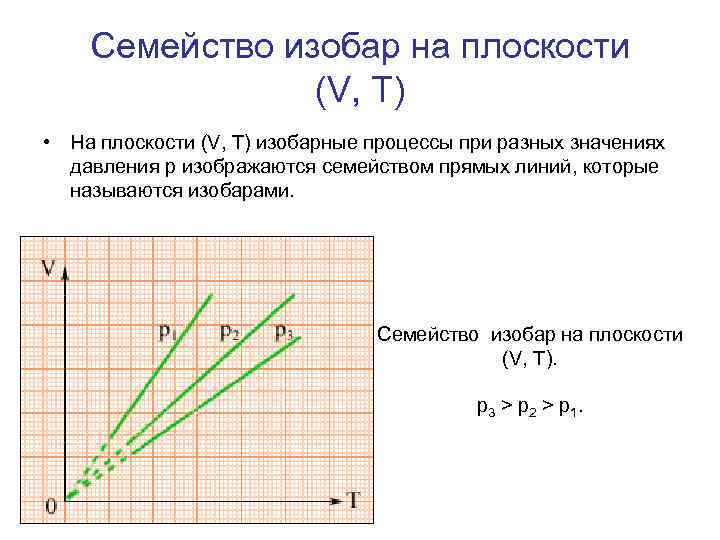 Семейство изобар на плоскости (V, T) • На плоскости (V, T) изобарные процессы при разных значениях давления p изображаются семейством прямых линий, которые называются изобарами. • Семейство изобар на плоскости (V, T). p 3 > p 2 > p 1.
Семейство изобар на плоскости (V, T) • На плоскости (V, T) изобарные процессы при разных значениях давления p изображаются семейством прямых линий, которые называются изобарами. • Семейство изобар на плоскости (V, T). p 3 > p 2 > p 1.
 Изобарный процесс • Зависимость объема газа от температуры при неизменном давлении была экспериментально исследована французским физиком Ж. Гей-Люссаком (1862 г. ). Поэтому уравнение изобарного процесса называют законом Гей-Люссака. • Экспериментально установленные законы Бойля–Мариотта, Шарля и Гей-Люссака находят объяснение в молекулярнокинетической теории газов. Они являются следствием уравнения состояния идеального газа.
Изобарный процесс • Зависимость объема газа от температуры при неизменном давлении была экспериментально исследована французским физиком Ж. Гей-Люссаком (1862 г. ). Поэтому уравнение изобарного процесса называют законом Гей-Люссака. • Экспериментально установленные законы Бойля–Мариотта, Шарля и Гей-Люссака находят объяснение в молекулярнокинетической теории газов. Они являются следствием уравнения состояния идеального газа.
 Давление смеси газов • Следует обратить внимание на то, что средняя кинетическая энергия поступательного движения молекулы не зависит от ее массы. Броуновская частица, взвешенная в жидкости или газе, обладает такой же средней кинетической энергией, как и отдельная молекула, масса которой на много порядков меньше массы броуновской частицы. Этот вывод распространяется и на случай, когда в сосуде находится смесь химически невзаимодействующих газов, молекулы которых имеют разные массы. В состоянии равновесия молекулы разных газов будут иметь одинаковые средние кинетические энергии теплового движения, определяемые только температурой смеси. Давление смеси газов на стенки сосуда будет складываться из парциальных давлений каждого газа: p = p 1 + p 2 + p 3 + … = (n 1 + n 2 + n 3 + …)k. T. • В этом соотношении n 1, n 2, n 3, … – концентрации молекул различных газов в смеси. Это соотношение выражает на языке молекулярнокинетической теории экспериментально установленный в начале XIX столетия закон Дальтона: давление в смеси химически невзаимодействующих газов равно сумме их парциальных давлений.
Давление смеси газов • Следует обратить внимание на то, что средняя кинетическая энергия поступательного движения молекулы не зависит от ее массы. Броуновская частица, взвешенная в жидкости или газе, обладает такой же средней кинетической энергией, как и отдельная молекула, масса которой на много порядков меньше массы броуновской частицы. Этот вывод распространяется и на случай, когда в сосуде находится смесь химически невзаимодействующих газов, молекулы которых имеют разные массы. В состоянии равновесия молекулы разных газов будут иметь одинаковые средние кинетические энергии теплового движения, определяемые только температурой смеси. Давление смеси газов на стенки сосуда будет складываться из парциальных давлений каждого газа: p = p 1 + p 2 + p 3 + … = (n 1 + n 2 + n 3 + …)k. T. • В этом соотношении n 1, n 2, n 3, … – концентрации молекул различных газов в смеси. Это соотношение выражает на языке молекулярнокинетической теории экспериментально установленный в начале XIX столетия закон Дальтона: давление в смеси химически невзаимодействующих газов равно сумме их парциальных давлений.