Молекулярная физика..ppt
- Количество слайдов: 45
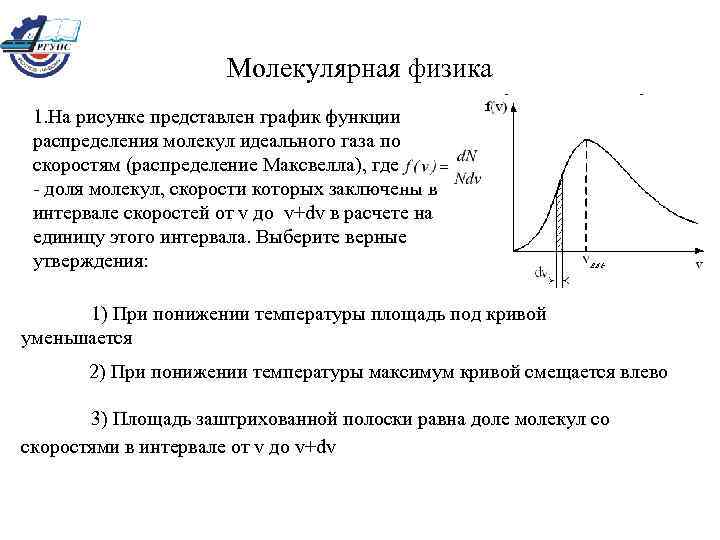 Молекулярная физика 1. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Выберите верные утверждения: 1) При понижении температуры площадь под кривой уменьшается 2) При понижении температуры максимум кривой смещается влево 3) Площадь заштрихованной полоски равна доле молекул со скоростями в интервале от v до v+dv
Молекулярная физика 1. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Выберите верные утверждения: 1) При понижении температуры площадь под кривой уменьшается 2) При понижении температуры максимум кривой смещается влево 3) Площадь заштрихованной полоски равна доле молекул со скоростями в интервале от v до v+dv
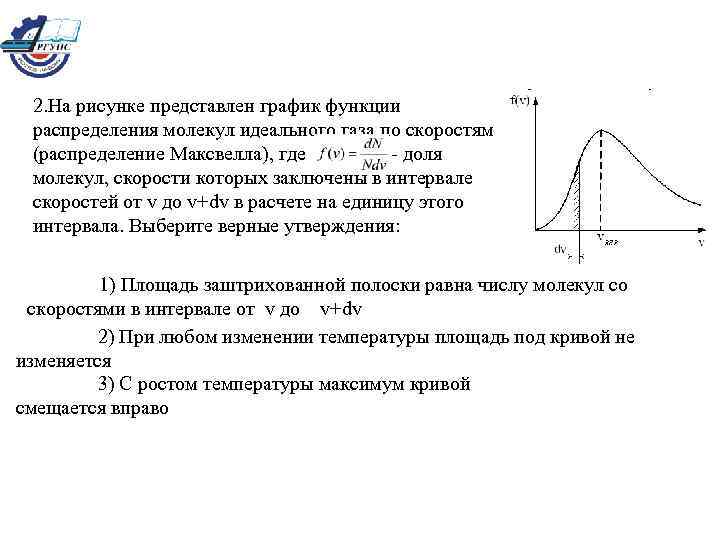 2. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Выберите верные утверждения: 1) Площадь заштрихованной полоски равна числу молекул со скоростями в интервале от v до v+dv 2) При любом изменении температуры площадь под кривой не изменяется 3) С ростом температуры максимум кривой смещается вправо
2. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Выберите верные утверждения: 1) Площадь заштрихованной полоски равна числу молекул со скоростями в интервале от v до v+dv 2) При любом изменении температуры площадь под кривой не изменяется 3) С ростом температуры максимум кривой смещается вправо
 3. На рисунке представлен график функции молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Выберите верные утверждения: 1) При любом изменении температуры площадь под кривой не изменяется 2) При понижении температуры максимум кривой смещается влево 3) Площадь заштрихованной полоски равная числу молекул со скоростями в интервале v до v+dv
3. На рисунке представлен график функции молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Выберите верные утверждения: 1) При любом изменении температуры площадь под кривой не изменяется 2) При понижении температуры максимум кривой смещается влево 3) Площадь заштрихованной полоски равная числу молекул со скоростями в интервале v до v+dv
 4. На рисунке представлен график функции молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Выберите верные утверждения … 1) При понижении температуры площадь под кривой уменьшается 2) При понижении температуры величина максимума уменьшается 3) Положение максимума кривой зависит как от температуры, так и от природы газа
4. На рисунке представлен график функции молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Выберите верные утверждения … 1) При понижении температуры площадь под кривой уменьшается 2) При понижении температуры величина максимума уменьшается 3) Положение максимума кривой зависит как от температуры, так и от природы газа
 5. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Для этой функции верным утверждением является. . . 1) При понижении температуры максимум кривой смещается влево 2) При понижении температуры величина максимума уменьшается 3) При понижении температуры площадь под кривой уменьшается
5. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Для этой функции верным утверждением является. . . 1) При понижении температуры максимум кривой смещается влево 2) При понижении температуры величина максимума уменьшается 3) При понижении температуры площадь под кривой уменьшается
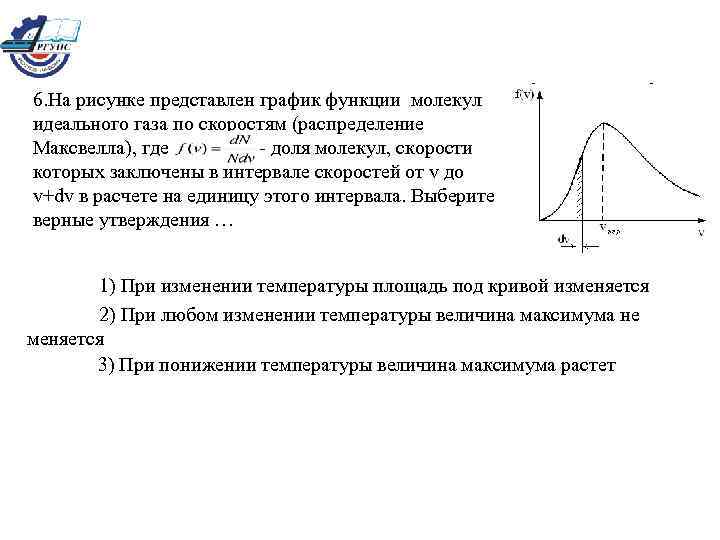 6. На рисунке представлен график функции молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Выберите верные утверждения … 1) При изменении температуры площадь под кривой изменяется 2) При любом изменении температуры величина максимума не меняется 3) При понижении температуры величина максимума растет
6. На рисунке представлен график функции молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Выберите верные утверждения … 1) При изменении температуры площадь под кривой изменяется 2) При любом изменении температуры величина максимума не меняется 3) При понижении температуры величина максимума растет
 7. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Выберите верные утверждения: 1) С ростом температуры максимум кривой смещается вправо 2) Вид функции распределения не зависит от природы газа (от массы молекул) 3) С ростом температуры площадь кривой не изменяется
7. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Выберите верные утверждения: 1) С ростом температуры максимум кривой смещается вправо 2) Вид функции распределения не зависит от природы газа (от массы молекул) 3) С ростом температуры площадь кривой не изменяется
 8. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Если, не меняя температуры и числа молекул, взять другой газ с меньшей молярной массой, то. . . 1) максимум кривой сместится влево в сторону меньших скоростей 2) максимум кривой сместится вправо в сторону больших скоростей 3) площадь под кривой уменьшится
8. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Если, не меняя температуры и числа молекул, взять другой газ с меньшей молярной массой, то. . . 1) максимум кривой сместится влево в сторону меньших скоростей 2) максимум кривой сместится вправо в сторону больших скоростей 3) площадь под кривой уменьшится
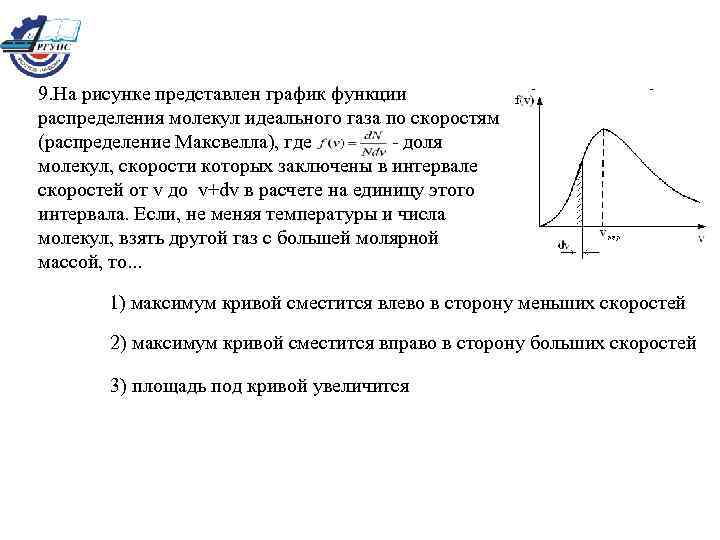 9. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Если, не меняя температуры и числа молекул, взять другой газ с большей молярной массой, то. . . 1) максимум кривой сместится влево в сторону меньших скоростей 2) максимум кривой сместится вправо в сторону больших скоростей 3) площадь под кривой увеличится
9. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Если, не меняя температуры и числа молекул, взять другой газ с большей молярной массой, то. . . 1) максимум кривой сместится влево в сторону меньших скоростей 2) максимум кривой сместится вправо в сторону больших скоростей 3) площадь под кривой увеличится
 10. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Если, не меняя температуры взять другой газ с меньшей молярной массой и таким же числом молекул, то … 1) величина максимума увеличится 2) максимум кривой сместится в сторону больших скоростей 3) площадь под кривой уменьшится
10. На рисунке представлен график функции распределения молекул идеального газа по скоростям (распределение Максвелла), где - доля молекул, скорости которых заключены в интервале скоростей от v до v+dv в расчете на единицу этого интервала. Если, не меняя температуры взять другой газ с меньшей молярной массой и таким же числом молекул, то … 1) величина максимума увеличится 2) максимум кривой сместится в сторону больших скоростей 3) площадь под кривой уменьшится
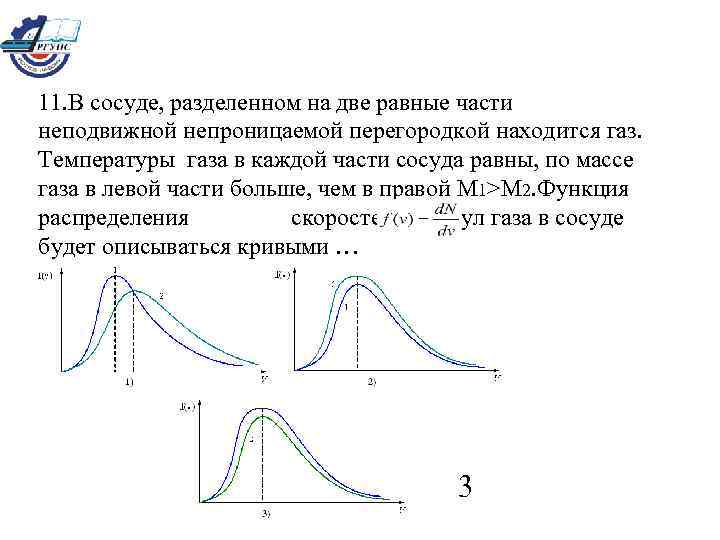 11. В сосуде, разделенном на две равные части неподвижной непроницаемой перегородкой находится газ. Температуры газа в каждой части сосуда равны, по массе газа в левой части больше, чем в правой М 1>М 2. Функция распределения скоростей молекул газа в сосуде будет описываться кривыми … 3
11. В сосуде, разделенном на две равные части неподвижной непроницаемой перегородкой находится газ. Температуры газа в каждой части сосуда равны, по массе газа в левой части больше, чем в правой М 1>М 2. Функция распределения скоростей молекул газа в сосуде будет описываться кривыми … 3
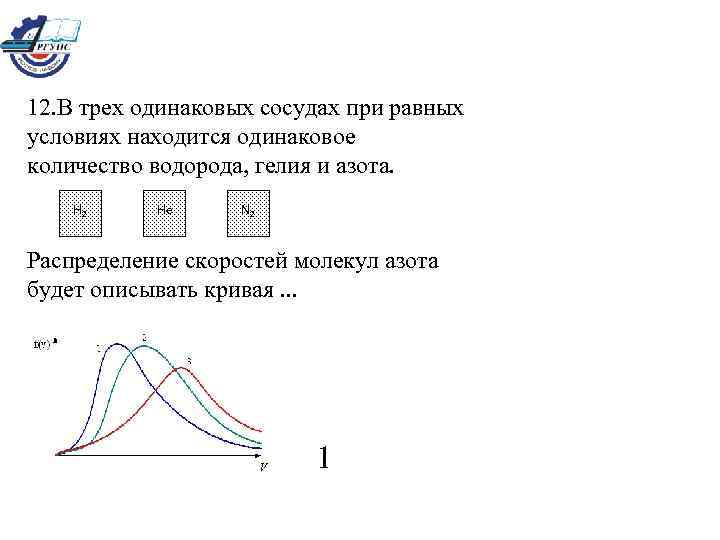 12. В трех одинаковых сосудах при равных условиях находится одинаковое количество водорода, гелия и азота. H 2 He N 2 Распределение скоростей молекул азота будет описывать кривая. . . 1
12. В трех одинаковых сосудах при равных условиях находится одинаковое количество водорода, гелия и азота. H 2 He N 2 Распределение скоростей молекул азота будет описывать кривая. . . 1
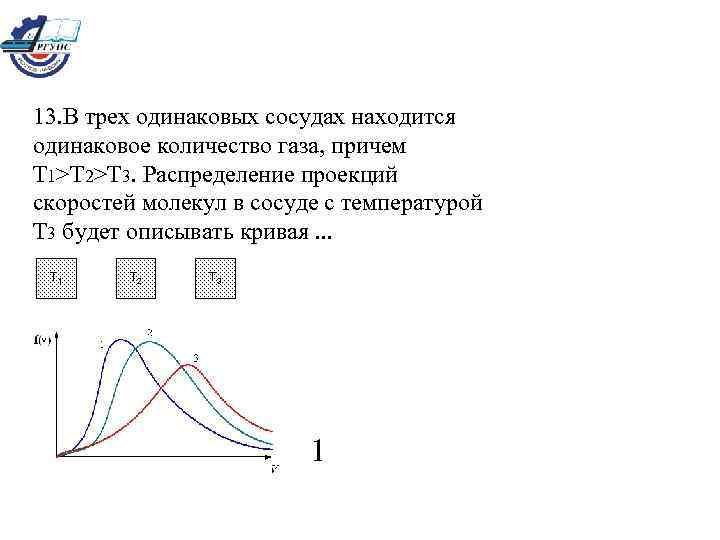 13. В трех одинаковых сосудах находится одинаковое количество газа, причем T 1>T 2>T 3. Распределение проекций скоростей молекул в сосуде с температурой T 3 будет описывать кривая. . . T 1 T 2 T 3 1
13. В трех одинаковых сосудах находится одинаковое количество газа, причем T 1>T 2>T 3. Распределение проекций скоростей молекул в сосуде с температурой T 3 будет описывать кривая. . . T 1 T 2 T 3 1
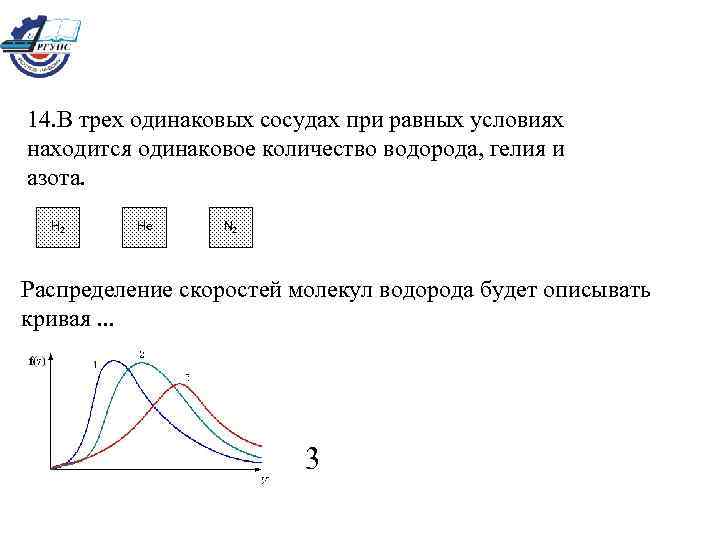 14. В трех одинаковых сосудах при равных условиях находится одинаковое количество водорода, гелия и азота. H 2 He N 2 Распределение скоростей молекул водорода будет описывать кривая. . . 3
14. В трех одинаковых сосудах при равных условиях находится одинаковое количество водорода, гелия и азота. H 2 He N 2 Распределение скоростей молекул водорода будет описывать кривая. . . 3
 15. В трех одинаковых сосудах при равных условиях находится одинаковое количество водорода, гелия и азота. Распределение проекций скоростей молекул водорода на произвольное направление Х будет описывать кривая … 1) 1 2) 2 3) 3
15. В трех одинаковых сосудах при равных условиях находится одинаковое количество водорода, гелия и азота. Распределение проекций скоростей молекул водорода на произвольное направление Х будет описывать кривая … 1) 1 2) 2 3) 3
 16. В трех одинаковых сосудах при равных условиях находится одинаковое количество водорода, гелия и азота. Распределение проекций скоростей молекул гелия на произвольное направление Х будет описывать кривая. . . 1) 1 2) 2 3) 3
16. В трех одинаковых сосудах при равных условиях находится одинаковое количество водорода, гелия и азота. Распределение проекций скоростей молекул гелия на произвольное направление Х будет описывать кривая. . . 1) 1 2) 2 3) 3
 17. В трех одинаковых сосудах при равных условиях находится одинаковое количество водорода, гелия и азота. Распределение проекций скоростей молекул азота на произвольное направление Х будет описывать кривая. . . 1) 1 2) 2 3) 3
17. В трех одинаковых сосудах при равных условиях находится одинаковое количество водорода, гелия и азота. Распределение проекций скоростей молекул азота на произвольное направление Х будет описывать кривая. . . 1) 1 2) 2 3) 3
 18. В трех одинаковых сосудах находится одинаковое количество газа, причем Т 1 > Т 2 > Т 3. f(vx) Т 1 Т 2 Т 3 Распределение проекций скоростей молекул водорода на произвольное направление Х для молекул в сосуде с температурой Т 1 будет описывать кривая. . . 1) 1 2) 2 3) 3 1 2 3 vx
18. В трех одинаковых сосудах находится одинаковое количество газа, причем Т 1 > Т 2 > Т 3. f(vx) Т 1 Т 2 Т 3 Распределение проекций скоростей молекул водорода на произвольное направление Х для молекул в сосуде с температурой Т 1 будет описывать кривая. . . 1) 1 2) 2 3) 3 1 2 3 vx
 19. В трех одинаковых сосудах находится одинаковое количество газа, причем T 1>T 2>T 3. T 1 T 2 T 3 Распределение проекций скоростей молекул на произвольное направление X в сосуде с температурой T 3 будет описывать кривая. . . 1) 1 2) 2 3) 3 f(vx) 1 2 3 vx
19. В трех одинаковых сосудах находится одинаковое количество газа, причем T 1>T 2>T 3. T 1 T 2 T 3 Распределение проекций скоростей молекул на произвольное направление X в сосуде с температурой T 3 будет описывать кривая. . . 1) 1 2) 2 3) 3 f(vx) 1 2 3 vx
 20. Средняя кинетическая энергия молекулы идеального газа при температуре Т равна. Здесь , где nп, nвр и nк – число степеней свободы поступательного, вращательного и колебательного движений молекулы. Для атомарного водорода число i равно. . . 1) 3 2) 5 3) 1 4) 7
20. Средняя кинетическая энергия молекулы идеального газа при температуре Т равна. Здесь , где nп, nвр и nк – число степеней свободы поступательного, вращательного и колебательного движений молекулы. Для атомарного водорода число i равно. . . 1) 3 2) 5 3) 1 4) 7
 21. Средняя кинетическая энергия молекулы идеального газа при температуре Т равна. Здесь , где nп, nвр и nк – число степеней свободы поступательного, вращательного и колебательного движений молекулы. При условии, что имеют место только поступательное и вращательное движение, для водяного пара (H 2 O) число i равно … 1) 5 2) 6 3) 3 4) 8
21. Средняя кинетическая энергия молекулы идеального газа при температуре Т равна. Здесь , где nп, nвр и nк – число степеней свободы поступательного, вращательного и колебательного движений молекулы. При условии, что имеют место только поступательное и вращательное движение, для водяного пара (H 2 O) число i равно … 1) 5 2) 6 3) 3 4) 8
 22. Средняя кинетическая энергия молекулы идеального газа при температуре Т равна. Здесь , где nп, nвр и nк – число степеней свободы поступательного, вращательного и колебательного движений молекулы. При условии, что имеют место только поступательное и вращательное движение, для водорода (H 2) число i равно. . . 1) 5 2) 7 3) 2 4) 8
22. Средняя кинетическая энергия молекулы идеального газа при температуре Т равна. Здесь , где nп, nвр и nк – число степеней свободы поступательного, вращательного и колебательного движений молекулы. При условии, что имеют место только поступательное и вращательное движение, для водорода (H 2) число i равно. . . 1) 5 2) 7 3) 2 4) 8
 23. Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. При условии, что имеют место только поступательное и вращательное движения, средняя энергия молекул углекислого газа (СО 2) равна …(Учесть, что молекула СО 2 – линейная) 1) 2) 3) 4)
23. Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. При условии, что имеют место только поступательное и вращательное движения, средняя энергия молекул углекислого газа (СО 2) равна …(Учесть, что молекула СО 2 – линейная) 1) 2) 3) 4)
 24. Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. При условии, что имеют место только поступательное и вращательное движения, средняя энергия молекул азота (N 2) равна … 1) 2) 3) 4)
24. Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. При условии, что имеют место только поступательное и вращательное движения, средняя энергия молекул азота (N 2) равна … 1) 2) 3) 4)
 25. Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. При условии, что имеют место только поступательное и вращательное движения, средняя энергия молекул метана (СH 4) равна … 1) 2) 3) 4)
25. Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. При условии, что имеют место только поступательное и вращательное движения, средняя энергия молекул метана (СH 4) равна … 1) 2) 3) 4)
 26. Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. При условии, что имеют место все виды движения, средняя энергия молекул азота (N 2) равна … 1) 2) 3) 4)
26. Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. При условии, что имеют место все виды движения, средняя энергия молекул азота (N 2) равна … 1) 2) 3) 4)
 27. Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. При условии, что имеют место только поступательное и вращательное движения, средняя энергия молекул водяного пара (H 2 O) равна … 1) 2) 3) 4)
27. Средняя кинетическая энергия молекул газа при температуре Т зависит от их структуры, что связано с возможностью различных видов движения атомов в молекуле. При условии, что имеют место только поступательное и вращательное движения, средняя энергия молекул водяного пара (H 2 O) равна … 1) 2) 3) 4)
 28. На каждую степень свободы движения молекулы приходится одинаковая энергия, равная ½ k. T (k постоянная Больцмана, Т - температура по шкале Кельвина). При условии, что имеют место все виды движения, средняя кинетическая энергия молекулы водорода (Н 2) равна. . . 1) 2) 3)
28. На каждую степень свободы движения молекулы приходится одинаковая энергия, равная ½ k. T (k постоянная Больцмана, Т - температура по шкале Кельвина). При условии, что имеют место все виды движения, средняя кинетическая энергия молекулы водорода (Н 2) равна. . . 1) 2) 3)
 29. На каждую степень свободы движения молекулы приходится одинаковая энергия, равная 1/2 k. T (k постоянная Больцмана, Т - температура по шкале Кельвина). Средняя кинетическая энергия атомарного водорода равна. . . 1) 2) 3) 4) 5)
29. На каждую степень свободы движения молекулы приходится одинаковая энергия, равная 1/2 k. T (k постоянная Больцмана, Т - температура по шкале Кельвина). Средняя кинетическая энергия атомарного водорода равна. . . 1) 2) 3) 4) 5)
 30. Максимальное число вращательных степеней свободы для молекулы N 2. . . 1) 1 2) 5 3) 2 4) 3 5) 4
30. Максимальное число вращательных степеней свободы для молекулы N 2. . . 1) 1 2) 5 3) 2 4) 3 5) 4
 31. Отношение энергии поступательного движения молекулы кислорода О 2 к ее полной внутренней энергии равно. . . 1) 2) 3) 4) 1 5)
31. Отношение энергии поступательного движения молекулы кислорода О 2 к ее полной внутренней энергии равно. . . 1) 2) 3) 4) 1 5)
 32. В баллоне емкостью V находится некоторый газ массы m под давлением p. Средняя квадратичная скорость молекул газа v равна. . . 1) 2) 3) 4)
32. В баллоне емкостью V находится некоторый газ массы m под давлением p. Средняя квадратичная скорость молекул газа v равна. . . 1) 2) 3) 4)
 33. Средний импульс молекулы идеального газа при уменьшении абсолютной температуры газа в 4 раза. . . 1) увеличится в 2 раза 2) увеличится в 4 раза 3) уменьшится в 2 раза 4) уменьшится в 4 раза
33. Средний импульс молекулы идеального газа при уменьшении абсолютной температуры газа в 4 раза. . . 1) увеличится в 2 раза 2) увеличится в 4 раза 3) уменьшится в 2 раза 4) уменьшится в 4 раза
 34. При увеличении абсолютной температуры идеального газа в 2 раза и концентрации молекул в 4 раза его давление. . . 1) увеличилось в 8 раз 2) увеличилось в 4 раза 3) увеличилось в 2 раза 4) уменьшилось в 2 раза
34. При увеличении абсолютной температуры идеального газа в 2 раза и концентрации молекул в 4 раза его давление. . . 1) увеличилось в 8 раз 2) увеличилось в 4 раза 3) увеличилось в 2 раза 4) уменьшилось в 2 раза
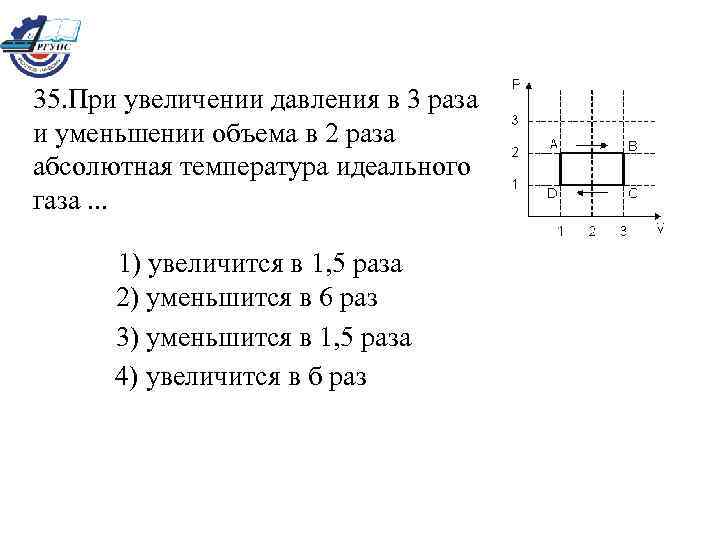 35. При увеличении давления в 3 раза и уменьшении объема в 2 раза абсолютная температура идеального газа. . . 1) увеличится в 1, 5 раза 2) уменьшится в 6 раз 3) уменьшится в 1, 5 раза 4) увеличится в б раз
35. При увеличении давления в 3 раза и уменьшении объема в 2 раза абсолютная температура идеального газа. . . 1) увеличится в 1, 5 раза 2) уменьшится в 6 раз 3) уменьшится в 1, 5 раза 4) увеличится в б раз
 36. При увеличении температуры и объема идеального газа в 2 раза, его давление. . . 1) увеличится в 4 раза 2) увеличится в 2 раза 3) уменьшится в 4 раза 4) не изменится 5) уменьшится в 2 раза
36. При увеличении температуры и объема идеального газа в 2 раза, его давление. . . 1) увеличится в 4 раза 2) увеличится в 2 раза 3) уменьшится в 4 раза 4) не изменится 5) уменьшится в 2 раза
 37. В баллоне емкостью 20 л находится метан (CH 4). Если в результате утечки газа давление снизилось в 4 раза при постоянной температуре, то масса метана уменьшилась. . . 1) в 2 раза 2) в 4 раза 3) в 16 раз 4) в 5 раз
37. В баллоне емкостью 20 л находится метан (CH 4). Если в результате утечки газа давление снизилось в 4 раза при постоянной температуре, то масса метана уменьшилась. . . 1) в 2 раза 2) в 4 раза 3) в 16 раз 4) в 5 раз
 38. При увеличении плотности водяных паров в воздухе в 2 раза при неизменной температуре их парциальное давление. . . 1) увеличится в 4 раза 2) не изменится 3) увеличится в 2 раза 4) уменьшится в 2 раза
38. При увеличении плотности водяных паров в воздухе в 2 раза при неизменной температуре их парциальное давление. . . 1) увеличится в 4 раза 2) не изменится 3) увеличится в 2 раза 4) уменьшится в 2 раза
 39. В цилиндре при сжатии постоянной массы воздуха давление возрастает в 3 раза. Если температура газа увеличилась в 2 раза, то отношение объемов до и после сжатия V 1/V 2 равно. . . 1) 6 2) 3/2 3) 2/3 4) 1/6
39. В цилиндре при сжатии постоянной массы воздуха давление возрастает в 3 раза. Если температура газа увеличилась в 2 раза, то отношение объемов до и после сжатия V 1/V 2 равно. . . 1) 6 2) 3/2 3) 2/3 4) 1/6
 40. На рисунке изображен цикл для постоянной массы газа в координатах V объем, p - давление. Из указанных на графике четырёх точек наибольшей температуре соответствует точка. . . 1) 2 2) 3 3) 1 4) 4
40. На рисунке изображен цикл для постоянной массы газа в координатах V объем, p - давление. Из указанных на графике четырёх точек наибольшей температуре соответствует точка. . . 1) 2 2) 3 3) 1 4) 4
 41. На (Р, V) – диаграмме изображен циклический процесс. На участках ВС-СD температура … 1) на ВС – повышается, на СD – понижается 2) понижается 3) повышается 4) на ВС – понижается, на СD – повышается
41. На (Р, V) – диаграмме изображен циклический процесс. На участках ВС-СD температура … 1) на ВС – повышается, на СD – понижается 2) понижается 3) повышается 4) на ВС – понижается, на СD – повышается
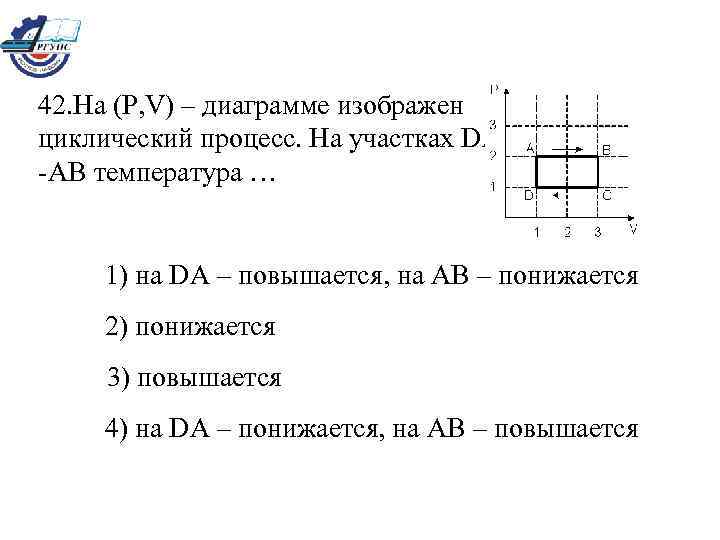 42. На (Р, V) – диаграмме изображен циклический процесс. На участках DА -АВ температура … 1) на DA – повышается, на AB – понижается 2) понижается 3) повышается 4) на DA – понижается, на AB – повышается
42. На (Р, V) – диаграмме изображен циклический процесс. На участках DА -АВ температура … 1) на DA – повышается, на AB – понижается 2) понижается 3) повышается 4) на DA – понижается, на AB – повышается
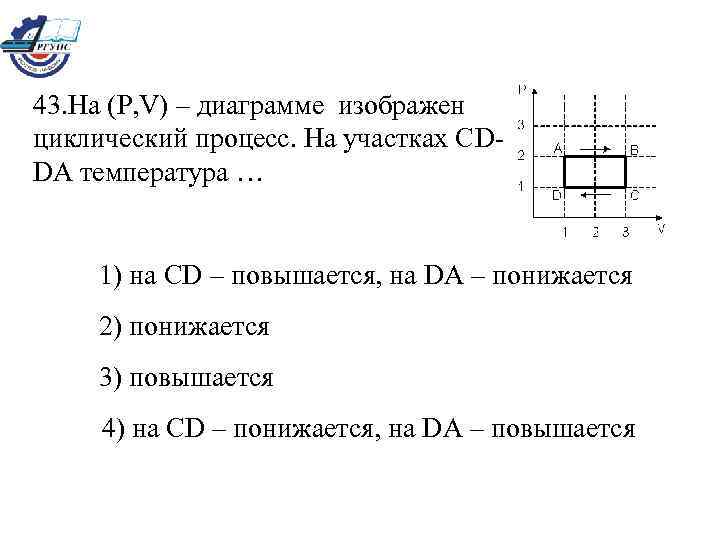 43. На (Р, V) – диаграмме изображен циклический процесс. На участках СDDА температура … 1) на CD – повышается, на DA – понижается 2) понижается 3) повышается 4) на СD – понижается, на DA – повышается
43. На (Р, V) – диаграмме изображен циклический процесс. На участках СDDА температура … 1) на CD – повышается, на DA – понижается 2) понижается 3) повышается 4) на СD – понижается, на DA – повышается
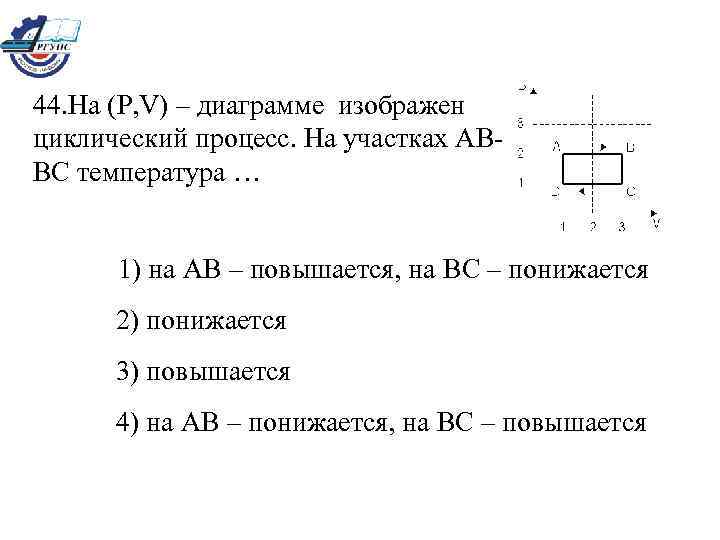 44. На (Р, V) – диаграмме изображен циклический процесс. На участках АВВС температура … 1) на АВ – повышается, на BС – понижается 2) понижается 3) повышается 4) на AВ – понижается, на BС – повышается
44. На (Р, V) – диаграмме изображен циклический процесс. На участках АВВС температура … 1) на АВ – повышается, на BС – понижается 2) понижается 3) повышается 4) на AВ – понижается, на BС – повышается
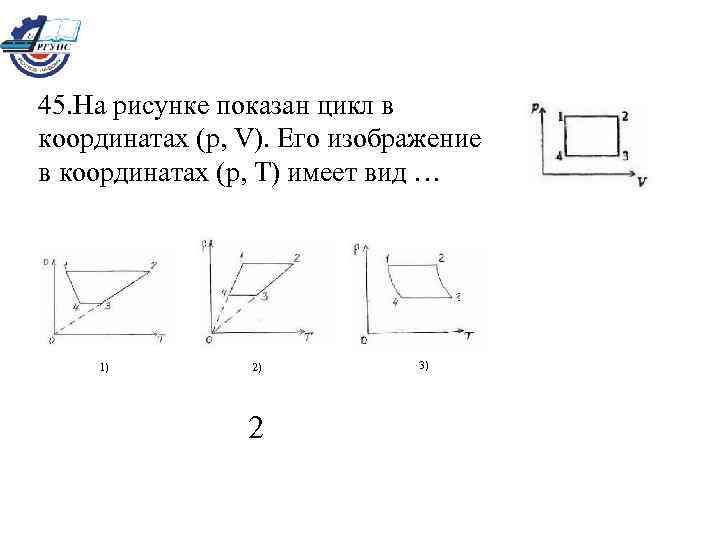 45. На рисунке показан цикл в координатах (p, V). Его изображение в координатах (р, Т) имеет вид … 1) 2) 2 3)
45. На рисунке показан цикл в координатах (p, V). Его изображение в координатах (р, Т) имеет вид … 1) 2) 2 3)


