98ff55227536d150aa54c31fd3de7224.ppt
- Количество слайдов: 47
 Molekulární hematologie nemaligní onemocnění Jozef Madžo Júlia Starková
Molekulární hematologie nemaligní onemocnění Jozef Madžo Júlia Starková
 Geneticky podmíněné hematologické onemocnění Thalasemie molekulární patogeneze Srpkovitá anemie / sickle cell anaemia léčba ovlivněním exprese genů Hemofilie genová terapie
Geneticky podmíněné hematologické onemocnění Thalasemie molekulární patogeneze Srpkovitá anemie / sickle cell anaemia léčba ovlivněním exprese genů Hemofilie genová terapie
 Hemoglobinopatie Poruchy v syntéze hemoglobinu
Hemoglobinopatie Poruchy v syntéze hemoglobinu
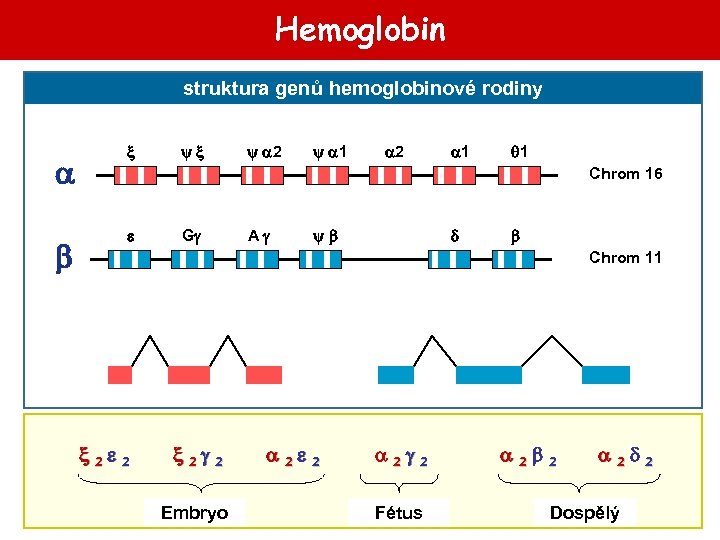 Hemoglobin struktura genů hemoglobinové rodiny 2 1 2 1 1 Chrom 16 G A Chrom 11 2 2 Embryo 2 2 Fétus 2 2 Dospělý
Hemoglobin struktura genů hemoglobinové rodiny 2 1 2 1 1 Chrom 16 G A Chrom 11 2 2 Embryo 2 2 Fétus 2 2 Dospělý
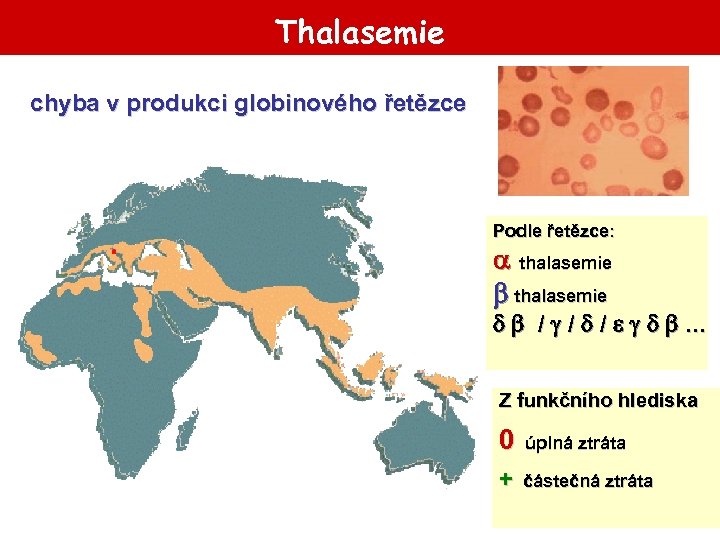 Thalasemie chyba v produkci globinového řetězce Podle řetězce: thalasemie / / / . . . Z funkčního hlediska 0 úplná ztráta + částečná ztráta
Thalasemie chyba v produkci globinového řetězce Podle řetězce: thalasemie / / / . . . Z funkčního hlediska 0 úplná ztráta + částečná ztráta
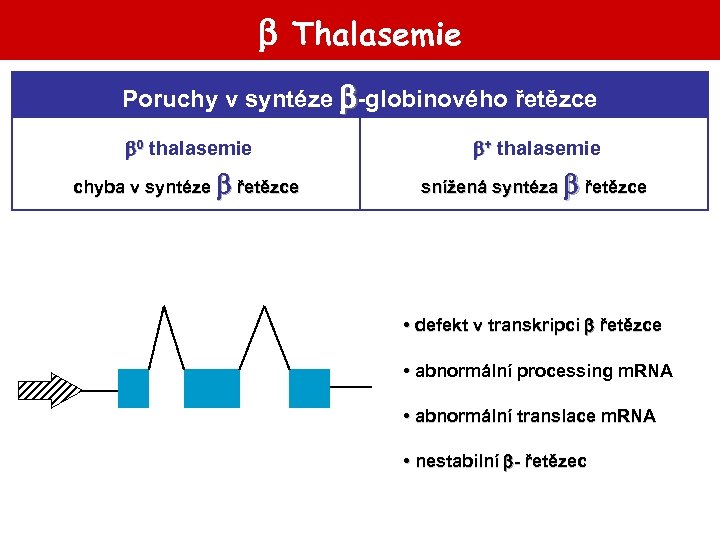 Thalasemie Poruchy v syntéze -globinového řetězce 0 thalasemie + thalasemie chyba v syntéze řetězce snížená syntéza řetězce • defekt v transkripci řetězce • abnormální processing m. RNA • abnormální translace m. RNA • nestabilní - řetězec
Thalasemie Poruchy v syntéze -globinového řetězce 0 thalasemie + thalasemie chyba v syntéze řetězce snížená syntéza řetězce • defekt v transkripci řetězce • abnormální processing m. RNA • abnormální translace m. RNA • nestabilní - řetězec
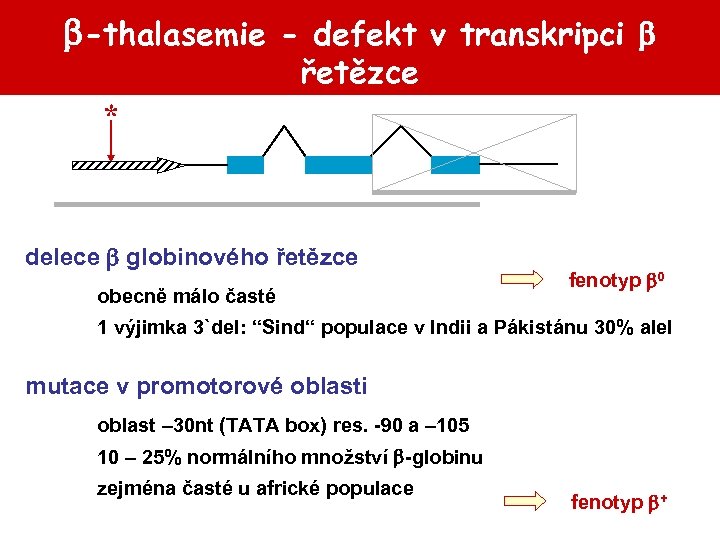 -thalasemie - defekt v transkripci řetězce * delece globinového řetězce obecně málo časté fenotyp 0 1 výjimka 3`del: “Sind“ populace v Indii a Pákistánu 30% alel mutace v promotorové oblasti oblast – 30 nt (TATA box) res. -90 a – 105 10 – 25% normálního množství -globinu zejména časté u africké populace fenotyp +
-thalasemie - defekt v transkripci řetězce * delece globinového řetězce obecně málo časté fenotyp 0 1 výjimka 3`del: “Sind“ populace v Indii a Pákistánu 30% alel mutace v promotorové oblasti oblast – 30 nt (TATA box) res. -90 a – 105 10 – 25% normálního množství -globinu zejména časté u africké populace fenotyp +
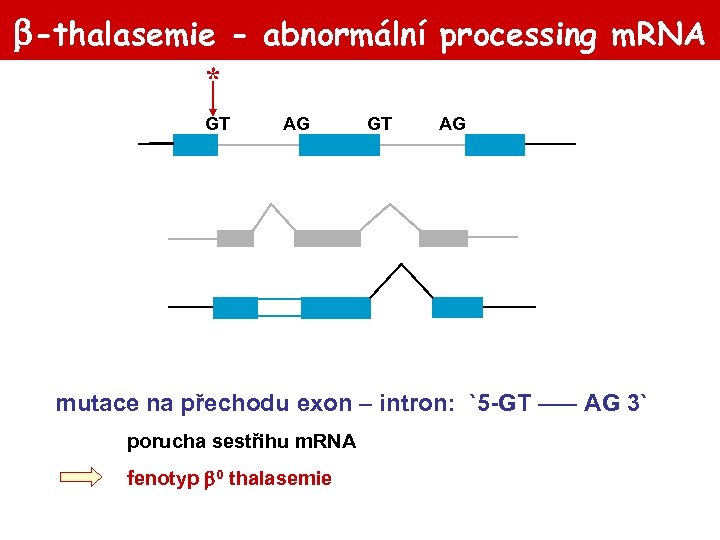 -thalasemie - abnormální processing m. RNA * GT AG mutace na přechodu exon – intron: `5 -GT ––– AG 3` porucha sestřihu m. RNA fenotyp 0 thalasemie
-thalasemie - abnormální processing m. RNA * GT AG mutace na přechodu exon – intron: `5 -GT ––– AG 3` porucha sestřihu m. RNA fenotyp 0 thalasemie
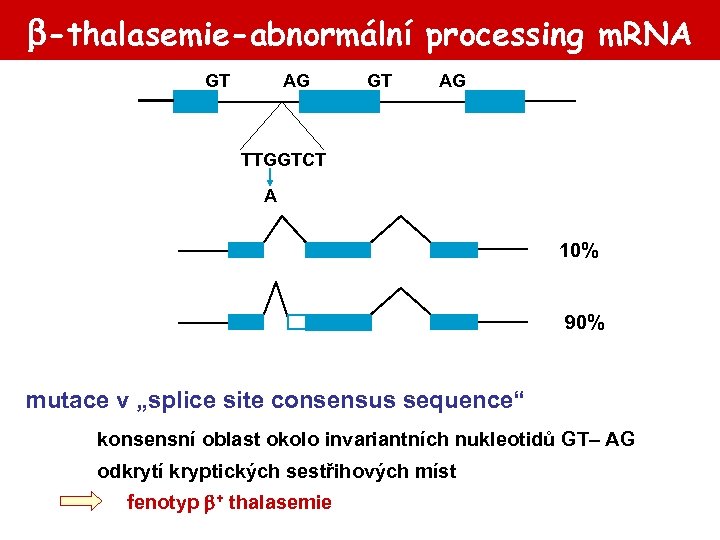 -thalasemie-abnormální processing m. RNA GT AG TTGGTCT A 10% 90% mutace v „splice site consensus sequence“ konsensní oblast okolo invariantních nukleotidů GT– AG odkrytí kryptických sestřihových míst fenotyp + thalasemie
-thalasemie-abnormální processing m. RNA GT AG TTGGTCT A 10% 90% mutace v „splice site consensus sequence“ konsensní oblast okolo invariantních nukleotidů GT– AG odkrytí kryptických sestřihových míst fenotyp + thalasemie
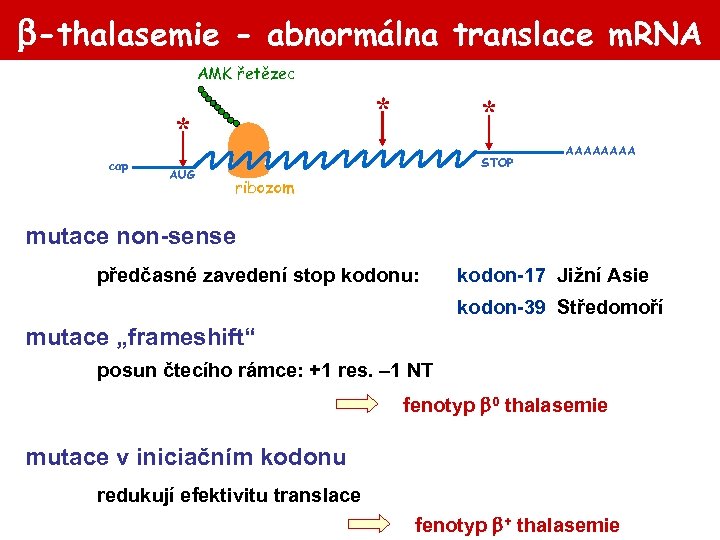 -thalasemie - abnormálna translace m. RNA AMK řetězec * * cap AUG * STOP AAAA ribozom mutace non-sense předčasné zavedení stop kodonu: kodon-17 Jižní Asie kodon-39 Středomoří mutace „frameshift“ posun čtecího rámce: +1 res. – 1 NT fenotyp 0 thalasemie mutace v iniciačním kodonu redukují efektivitu translace fenotyp + thalasemie
-thalasemie - abnormálna translace m. RNA AMK řetězec * * cap AUG * STOP AAAA ribozom mutace non-sense předčasné zavedení stop kodonu: kodon-17 Jižní Asie kodon-39 Středomoří mutace „frameshift“ posun čtecího rámce: +1 res. – 1 NT fenotyp 0 thalasemie mutace v iniciačním kodonu redukují efektivitu translace fenotyp + thalasemie
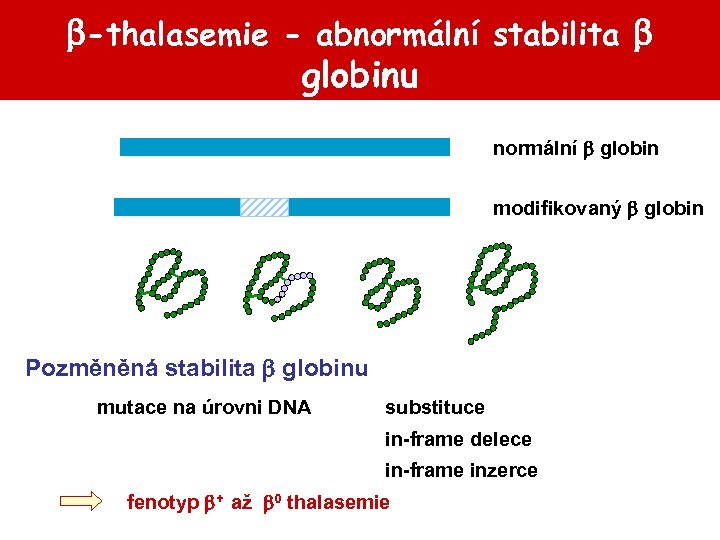 -thalasemie - abnormální stabilita globinu normální globin modifikovaný globin Pozměněná stabilita globinu mutace na úrovni DNA substituce in-frame delece in-frame inzerce fenotyp + až 0 thalasemie
-thalasemie - abnormální stabilita globinu normální globin modifikovaný globin Pozměněná stabilita globinu mutace na úrovni DNA substituce in-frame delece in-frame inzerce fenotyp + až 0 thalasemie
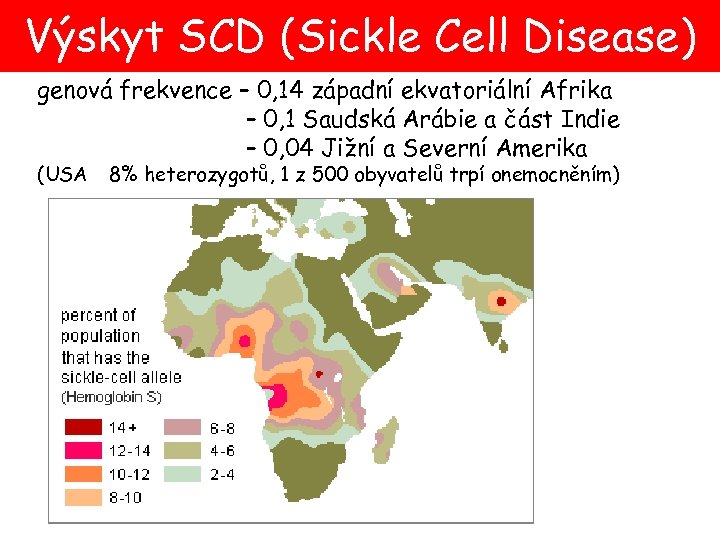 Výskyt SCD (Sickle Cell Disease) genová frekvence – 0, 14 západní ekvatoriální Afrika – 0, 1 Saudská Arábie a část Indie – 0, 04 Jižní a Severní Amerika (USA 8% heterozygotů, 1 z 500 obyvatelů trpí onemocněním)
Výskyt SCD (Sickle Cell Disease) genová frekvence – 0, 14 západní ekvatoriální Afrika – 0, 1 Saudská Arábie a část Indie – 0, 04 Jižní a Severní Amerika (USA 8% heterozygotů, 1 z 500 obyvatelů trpí onemocněním)
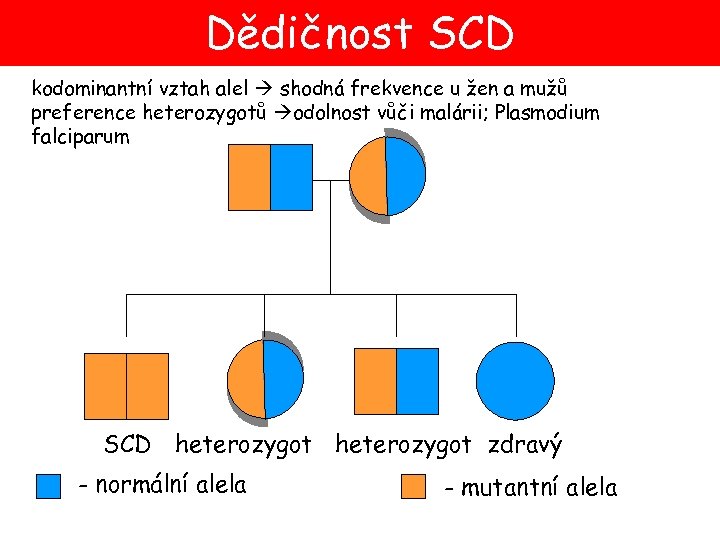 Dědičnost SCD kodominantní vztah alel shodná frekvence u žen a mužů preference heterozygotů odolnost vůči malárii; Plasmodium falciparum SCD heterozygot zdravý - normální alela - mutantní alela
Dědičnost SCD kodominantní vztah alel shodná frekvence u žen a mužů preference heterozygotů odolnost vůči malárii; Plasmodium falciparum SCD heterozygot zdravý - normální alela - mutantní alela
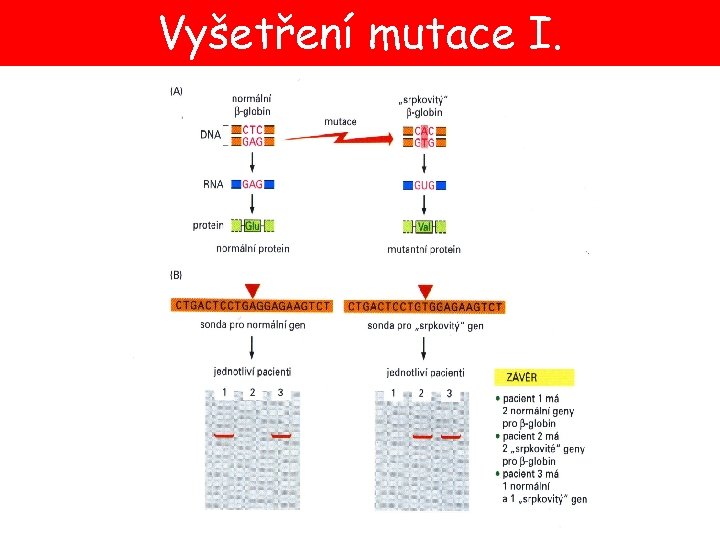 Vyšetření mutace I.
Vyšetření mutace I.
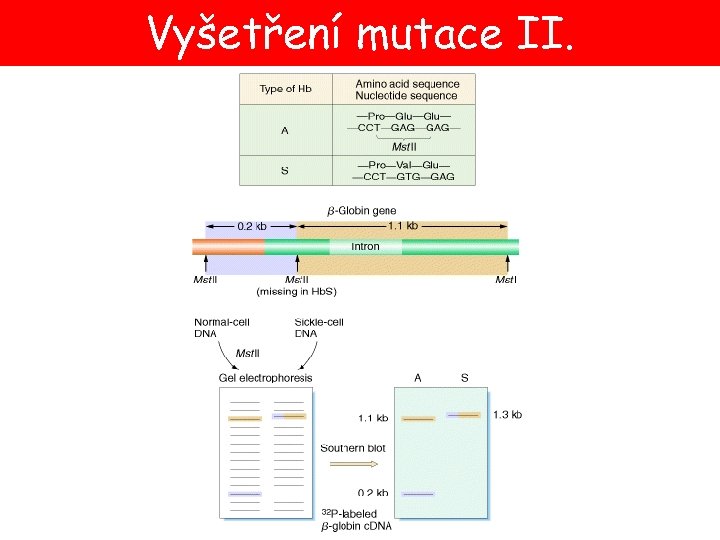 Vyšetření mutace II.
Vyšetření mutace II.
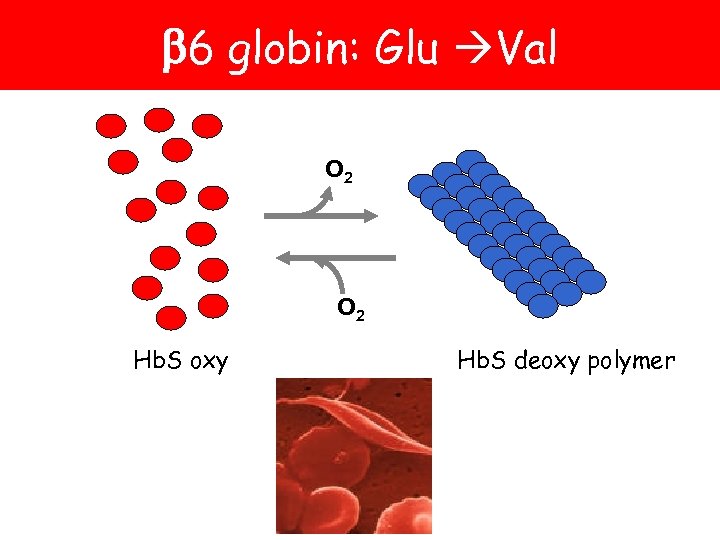 6 globin: Glu Val O 2 Hb. S oxy Hb. S deoxy polymer
6 globin: Glu Val O 2 Hb. S oxy Hb. S deoxy polymer
 Patofyziologie SCD • vytvoření polymerů Hb. S u deoxygenních erytrocytů formování srpkovitých buněk • zvýšená adheze erytrocytů k endotelu • abnormální kationtová homeostáza buněčná dehydrace • vasokonstrikce (via NO, endothelin-1) prodloužení mikrovaskulárního tranzitu erytrocytů
Patofyziologie SCD • vytvoření polymerů Hb. S u deoxygenních erytrocytů formování srpkovitých buněk • zvýšená adheze erytrocytů k endotelu • abnormální kationtová homeostáza buněčná dehydrace • vasokonstrikce (via NO, endothelin-1) prodloužení mikrovaskulárního tranzitu erytrocytů
 Klinické projevy • nedostatečné proudění krve v krevních cévách • nedostatečné zásobování kyslíku v kostech, svalech, plících, mozku, srdci • splenomegalie - infekční choroby • bolesti končetín, acute chest syndrome, mozkové příhody
Klinické projevy • nedostatečné proudění krve v krevních cévách • nedostatečné zásobování kyslíku v kostech, svalech, plících, mozku, srdci • splenomegalie - infekční choroby • bolesti končetín, acute chest syndrome, mozkové příhody
 Terapie I. • • tranfúzní program transplantace kostní dřeně (~ 5% mortalita) blokátory iontových kanálů anti-adhezivní a protizánětlivá léčba (anti-P-selectin, inhibitor NFκB) • inhalace NO • genová terapie lentivirový konstrukt s βA-T 87 Q globinovým genem transdukován do HSC a transplantován dvěma myším inhibice dehydratace a deformace erytrocytů, ústup splenomegalie a hypostenurie
Terapie I. • • tranfúzní program transplantace kostní dřeně (~ 5% mortalita) blokátory iontových kanálů anti-adhezivní a protizánětlivá léčba (anti-P-selectin, inhibitor NFκB) • inhalace NO • genová terapie lentivirový konstrukt s βA-T 87 Q globinovým genem transdukován do HSC a transplantován dvěma myším inhibice dehydratace a deformace erytrocytů, ústup splenomegalie a hypostenurie
 Terapie II. • Hydroxyurea – cytotoxická látka; zvyšuje koncentraci Hb. F – zvýšení množství Hb. F a F buněk – inhibice kationtové deplece, adhezivity s endotelem – nevýhody – velký počet non-respondentů, karcinogenní a leukemogenní efekt při dlouhodobé léčbě – teratogenní účinek byl pozorován u zvířat
Terapie II. • Hydroxyurea – cytotoxická látka; zvyšuje koncentraci Hb. F – zvýšení množství Hb. F a F buněk – inhibice kationtové deplece, adhezivity s endotelem – nevýhody – velký počet non-respondentů, karcinogenní a leukemogenní efekt při dlouhodobé léčbě – teratogenní účinek byl pozorován u zvířat
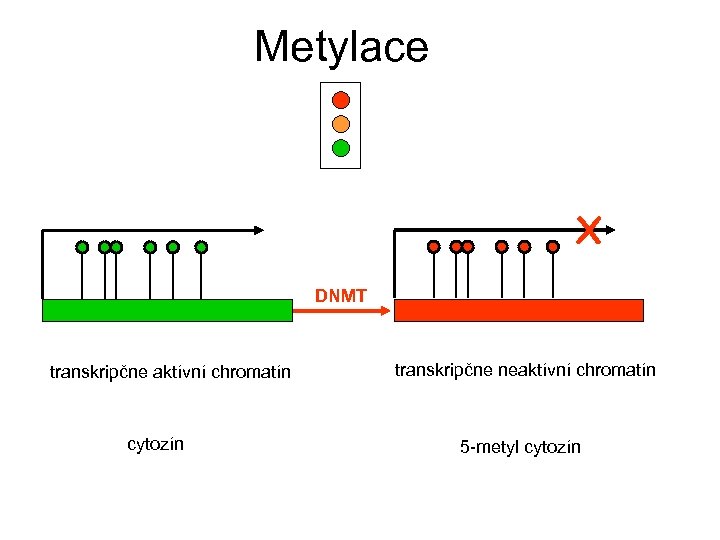 Metylace X DNMT transkripčne aktívní chromatín cytozín transkripčne neaktívní chromatín 5 -metyl cytozín
Metylace X DNMT transkripčne aktívní chromatín cytozín transkripčne neaktívní chromatín 5 -metyl cytozín
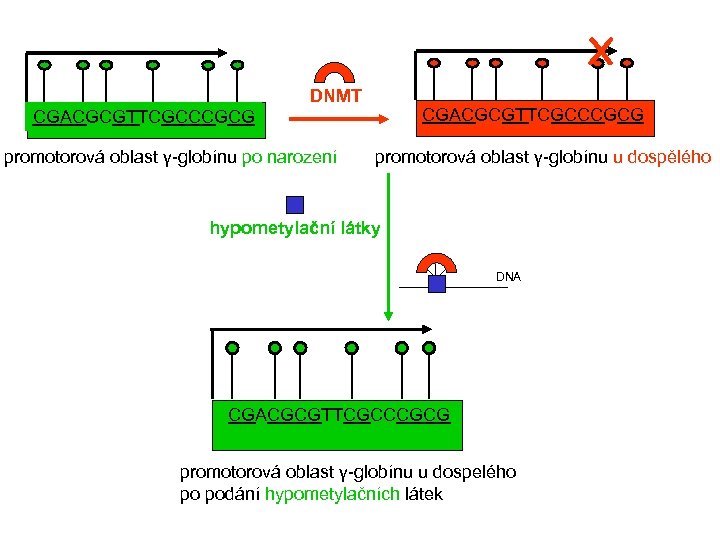 X DNMT CGACGCGTTCGCCCGCG promotorová oblast γ-globínu po narození promotorová oblast γ-globínu u dospělého hypometylační látky DNA CGACGCGTTCGCCCGCG promotorová oblast γ-globínu u dospelého po podání hypometylačních látek
X DNMT CGACGCGTTCGCCCGCG promotorová oblast γ-globínu po narození promotorová oblast γ-globínu u dospělého hypometylační látky DNA CGACGCGTTCGCCCGCG promotorová oblast γ-globínu u dospelého po podání hypometylačních látek
 Terapie III. Hypometylační látky 5 -azacytidine inkorporace do DNA a RNA, kovalentní vazba s DNA metyltransferasou (DNMT; udržuje metylační pattern během replikace) účinek: u paviánů 40 -70 násobné zvýšení exprese γ-globinového genu; metylace γ-globinového promotoru snižuje koncentraci Hb. F (10 -25%), F buňky (30 -40%) 5 -aza-2’-deoxycytidine(decitabine) inkorporace do DNA, účinnější než 5 -azacytidin hypometylace γ-globinu; zvýšení acetylovaného H 3 a H 4 asociovaného s γ-globinovým promotorem
Terapie III. Hypometylační látky 5 -azacytidine inkorporace do DNA a RNA, kovalentní vazba s DNA metyltransferasou (DNMT; udržuje metylační pattern během replikace) účinek: u paviánů 40 -70 násobné zvýšení exprese γ-globinového genu; metylace γ-globinového promotoru snižuje koncentraci Hb. F (10 -25%), F buňky (30 -40%) 5 -aza-2’-deoxycytidine(decitabine) inkorporace do DNA, účinnější než 5 -azacytidin hypometylace γ-globinu; zvýšení acetylovaného H 3 a H 4 asociovaného s γ-globinovým promotorem
 První studie na pacientech 8 pacientů léčených intravenózně decitabinem 2 týdny (5 pacientů nezvyšovalo hladiny Hb. F, 2 pacienti neodpovídali na léčbu HU a 1 nebyl léčený HU) 3, 5% 13, 5%Hb. F 21% 55% F buňky sledování toxicity 63 týdnů – bez toxických příznaků, výskyt neutropenie 8 pacientů léčených subkutánně decitabinem 6 týdnů (pacienti neodpovídali na léčbu HU) 6, 5% 20, 4% Hb. F 38% 71% F buňky
První studie na pacientech 8 pacientů léčených intravenózně decitabinem 2 týdny (5 pacientů nezvyšovalo hladiny Hb. F, 2 pacienti neodpovídali na léčbu HU a 1 nebyl léčený HU) 3, 5% 13, 5%Hb. F 21% 55% F buňky sledování toxicity 63 týdnů – bez toxických příznaků, výskyt neutropenie 8 pacientů léčených subkutánně decitabinem 6 týdnů (pacienti neodpovídali na léčbu HU) 6, 5% 20, 4% Hb. F 38% 71% F buňky
 Koagulopatie Poruchy v syntéze proteinů koagulační kaskády
Koagulopatie Poruchy v syntéze proteinů koagulační kaskády
 Hemofilie: genetický podklad Hemofilie (dědičná porucha v produkci koagulačního faktoru) Podtypy A: F – VIII. B: F- IX. Hemofilie A chromozóm X vázána porucha Xq 28 => častější výskyt u mužského pohlaví Xh. Y => ženy přenašečky Xh. X F VIII produkován hlavně v játrech deficient F VIII- hemofilie A za přítomnosti všech ostatních faktorů
Hemofilie: genetický podklad Hemofilie (dědičná porucha v produkci koagulačního faktoru) Podtypy A: F – VIII. B: F- IX. Hemofilie A chromozóm X vázána porucha Xq 28 => častější výskyt u mužského pohlaví Xh. Y => ženy přenašečky Xh. X F VIII produkován hlavně v játrech deficient F VIII- hemofilie A za přítomnosti všech ostatních faktorů
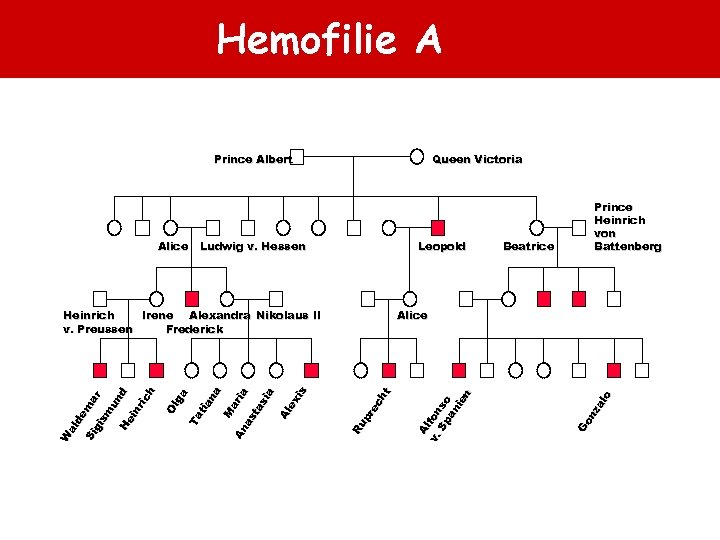 Hemofilie A Prince Albert Ludwig v. Hessen Leopold Beatrice Prince Heinrich von Battenberg Go nz al o Alice Ru pr ec ht Ol ga Ta tia na M ar An ia as ta si a Al ex is W al de m Si ar gi sm un d He in ric h Irene Alexandra Nikolaus II Heinrich v. Preussen Frederick Al v. fon Sp so an ie n Alice Queen Victoria
Hemofilie A Prince Albert Ludwig v. Hessen Leopold Beatrice Prince Heinrich von Battenberg Go nz al o Alice Ru pr ec ht Ol ga Ta tia na M ar An ia as ta si a Al ex is W al de m Si ar gi sm un d He in ric h Irene Alexandra Nikolaus II Heinrich v. Preussen Frederick Al v. fon Sp so an ie n Alice Queen Victoria
 Hemofilie A
Hemofilie A
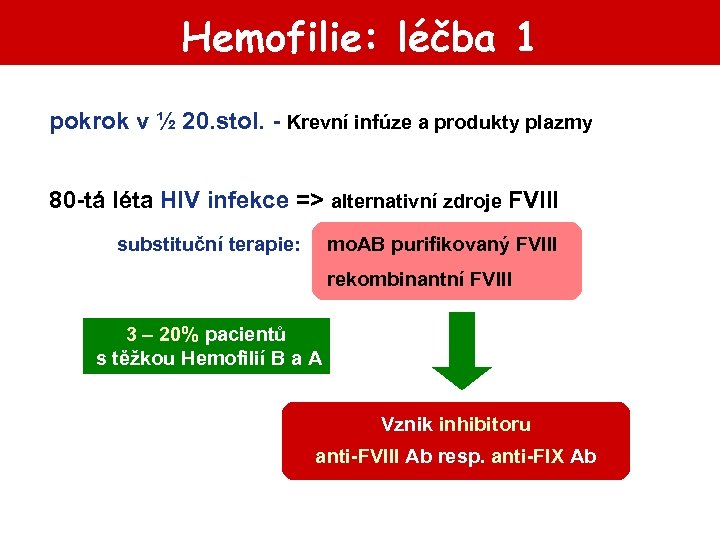 Hemofilie: léčba 1 pokrok v ½ 20. stol. - Krevní infúze a produkty plazmy 80 -tá léta HIV infekce => alternativní zdroje FVIII substituční terapie: mo. AB purifikovaný FVIII rekombinantní FVIII 3 – 20% pacientů s těžkou Hemofilií B a A Vznik inhibitoru anti-FVIII Ab resp. anti-FIX Ab
Hemofilie: léčba 1 pokrok v ½ 20. stol. - Krevní infúze a produkty plazmy 80 -tá léta HIV infekce => alternativní zdroje FVIII substituční terapie: mo. AB purifikovaný FVIII rekombinantní FVIII 3 – 20% pacientů s těžkou Hemofilií B a A Vznik inhibitoru anti-FVIII Ab resp. anti-FIX Ab
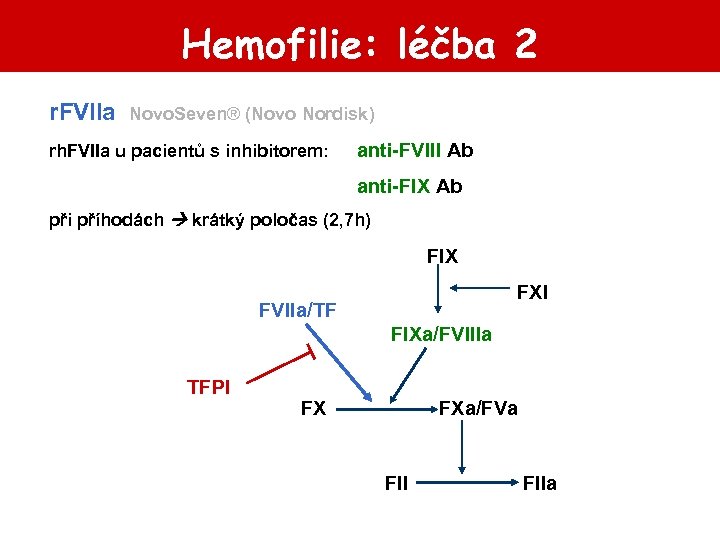 Hemofilie: léčba 2 r. FVIIa Novo. Seven® (Novo Nordisk) rh. FVIIa u pacientů s inhibitorem: anti-FVIII Ab anti-FIX Ab při příhodách krátký poločas (2, 7 h) FIX FXI FVIIa/TF FIXa/FVIIIa TFPI FX FXa/FVa FIIa
Hemofilie: léčba 2 r. FVIIa Novo. Seven® (Novo Nordisk) rh. FVIIa u pacientů s inhibitorem: anti-FVIII Ab anti-FIX Ab při příhodách krátký poločas (2, 7 h) FIX FXI FVIIa/TF FIXa/FVIIIa TFPI FX FXa/FVa FIIa
 Genová Terapie 1 • • ADA deficient SCID X-linked SCID Gaucher´s disease chronic granulomatous disease Fanconi´s anaemia HIV haemoglobinopathies haemophilia
Genová Terapie 1 • • ADA deficient SCID X-linked SCID Gaucher´s disease chronic granulomatous disease Fanconi´s anaemia HIV haemoglobinopathies haemophilia
 Proč je hemofilie vhodná pro genovou terapii? • Zvýšení hladiny faktoru >1% odstraní nejtěžší příznaky a vede ke snížení mortality • faktor může být produkován širokým spektrem buněk • široké „terapeutické okno“: 1. 5% až 100% normálních hladin faktoru • zvířecí modely (psi a myši) a myší a psí geny pro faktory VIII a IX k disposici • jednoduché sledování výsledků léčby - laboratorní i klinické
Proč je hemofilie vhodná pro genovou terapii? • Zvýšení hladiny faktoru >1% odstraní nejtěžší příznaky a vede ke snížení mortality • faktor může být produkován širokým spektrem buněk • široké „terapeutické okno“: 1. 5% až 100% normálních hladin faktoru • zvířecí modely (psi a myši) a myší a psí geny pro faktory VIII a IX k disposici • jednoduché sledování výsledků léčby - laboratorní i klinické
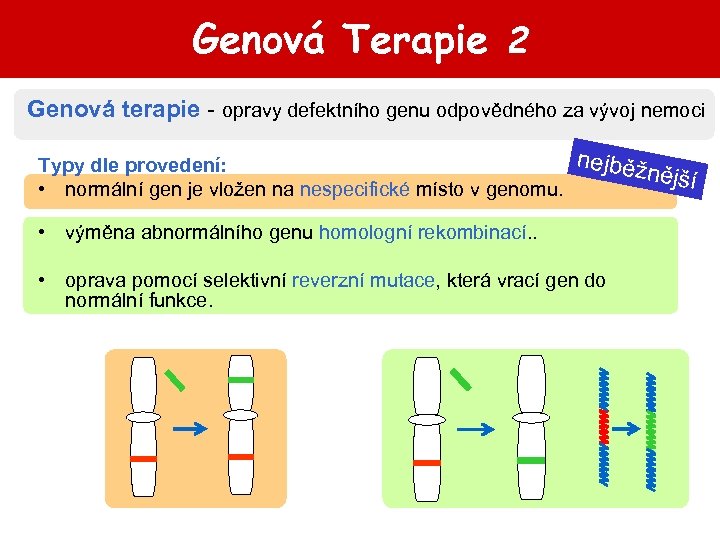 Genová Terapie 2 Genová terapie - opravy defektního genu odpovědného za vývoj nemoci nejběž Typy dle provedení: nější • normální gen je vložen na nespecifické místo v genomu. . • výměna abnormálního genu homologní rekombinací. . • oprava pomocí selektivní reverzní mutace, která vrací gen do normální funkce.
Genová Terapie 2 Genová terapie - opravy defektního genu odpovědného za vývoj nemoci nejběž Typy dle provedení: nější • normální gen je vložen na nespecifické místo v genomu. . • výměna abnormálního genu homologní rekombinací. . • oprava pomocí selektivní reverzní mutace, která vrací gen do normální funkce.
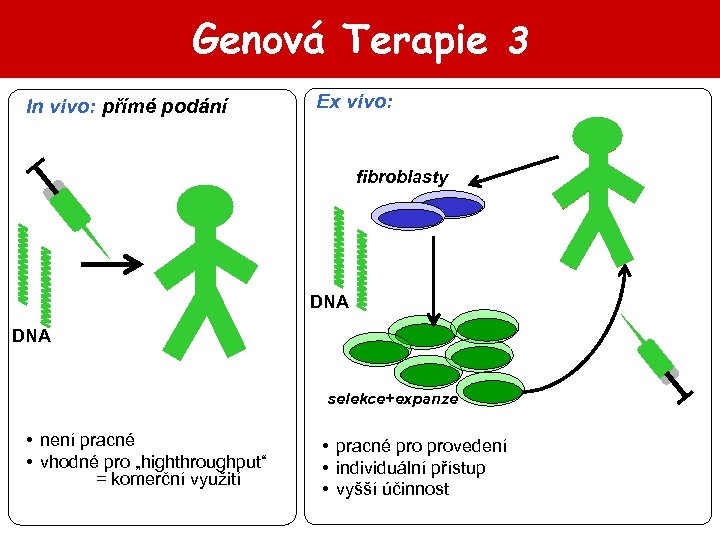 Genová Terapie 3 In vivo: přímé podání Ex vivo: fibroblasty DNA selekce+expanze • není pracné • vhodné pro „highthroughput“ = komerční využití • pracné provedení • individuální přístup • vyšší účinnost
Genová Terapie 3 In vivo: přímé podání Ex vivo: fibroblasty DNA selekce+expanze • není pracné • vhodné pro „highthroughput“ = komerční využití • pracné provedení • individuální přístup • vyšší účinnost
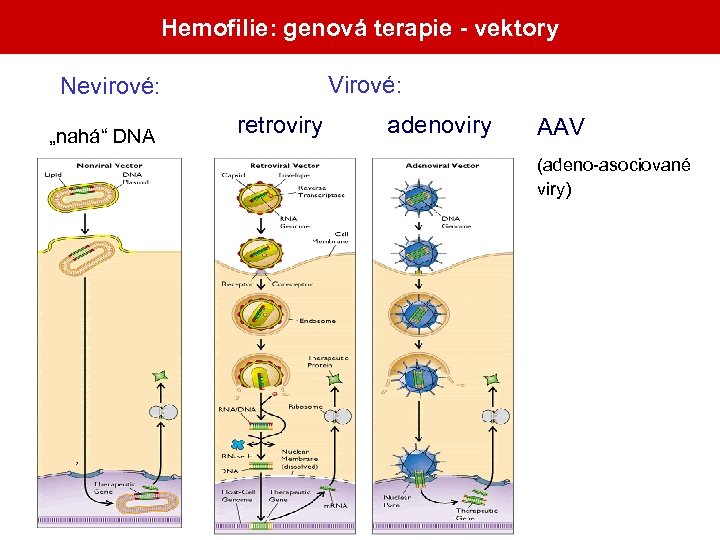 Hemofilie: genová terapie - vektory Virové: Nevirové: „nahá“ DNA retroviry adenoviry AAV (adeno-asociované viry)
Hemofilie: genová terapie - vektory Virové: Nevirové: „nahá“ DNA retroviry adenoviry AAV (adeno-asociované viry)
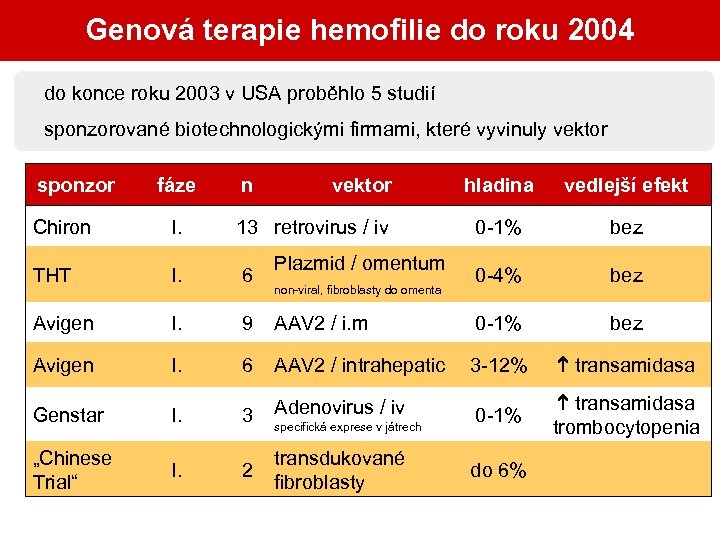 Genová terapie hemofilie do roku 2004 do konce roku 2003 v USA proběhlo 5 studií sponzorované biotechnologickými firmami, které vyvinuly vektor sponzor fáze n vektor hladina vedlejší efekt 0 -1% bez 0 -4% bez Chiron I. 13 retrovirus / iv THT I. 6 Avigen I. 9 AAV 2 / i. m 0 -1% bez Avigen I. 6 AAV 2 / intrahepatic 3 -12% transamidasa Genstar I. 3 Adenovirus / iv 0 -1% transamidasa trombocytopenia „Chinese Trial“ I. 2 transdukované fibroblasty Plazmid / omentum non-viral, fibroblasty do omenta specifická exprese v játrech do 6%
Genová terapie hemofilie do roku 2004 do konce roku 2003 v USA proběhlo 5 studií sponzorované biotechnologickými firmami, které vyvinuly vektor sponzor fáze n vektor hladina vedlejší efekt 0 -1% bez 0 -4% bez Chiron I. 13 retrovirus / iv THT I. 6 Avigen I. 9 AAV 2 / i. m 0 -1% bez Avigen I. 6 AAV 2 / intrahepatic 3 -12% transamidasa Genstar I. 3 Adenovirus / iv 0 -1% transamidasa trombocytopenia „Chinese Trial“ I. 2 transdukované fibroblasty Plazmid / omentum non-viral, fibroblasty do omenta specifická exprese v játrech do 6%
 studie 1: Chiron • studie: fáze I. „dose escalation study“ • pacientů: 13 s těžkou hemofilií A (HIV a HCV pozitivní) • vektor: retrovirální (deletováná B doména h. FVIII) • podání: intravenózní infuze • dávka: 3 x 107 - 9 x 108 vp/kg • efekt: u žádného hladina FVIII ne z : <1% • komentář: limitována kapacita retrovirálné integrace do nedělicích se buněk jater a nepřítomnost pro játra specifického promotoru ve vektoru
studie 1: Chiron • studie: fáze I. „dose escalation study“ • pacientů: 13 s těžkou hemofilií A (HIV a HCV pozitivní) • vektor: retrovirální (deletováná B doména h. FVIII) • podání: intravenózní infuze • dávka: 3 x 107 - 9 x 108 vp/kg • efekt: u žádného hladina FVIII ne z : <1% • komentář: limitována kapacita retrovirálné integrace do nedělicích se buněk jater a nepřítomnost pro játra specifického promotoru ve vektoru
 studie 2: THT • studie: fáze I. • pacientů: 6 s hemofilií A • vektor: plazmid elektroporovaný do autologních fibroblastů • podání: injekce do omenta • dávka: 100 M – 400 M buněk • efekt: u 4 / 6 hladina FVIII z oproti původní až na 4% • komentář: redukce užívaní rekomb. /purif. faktoru a spontánního krvácení u všech pacientů po dobu 12 měsíců • pokles: ? gene silencing, imunologický dozor „clerance“, zestárnutí „senescence“ reimplantovaných fibroblastů
studie 2: THT • studie: fáze I. • pacientů: 6 s hemofilií A • vektor: plazmid elektroporovaný do autologních fibroblastů • podání: injekce do omenta • dávka: 100 M – 400 M buněk • efekt: u 4 / 6 hladina FVIII z oproti původní až na 4% • komentář: redukce užívaní rekomb. /purif. faktoru a spontánního krvácení u všech pacientů po dobu 12 měsíců • pokles: ? gene silencing, imunologický dozor „clerance“, zestárnutí „senescence“ reimplantovaných fibroblastů
 studie 3: Avigen I. • studie: fáze I. „dose escalation study“ • pacientů: 9 s hemofilií B • vektor: AAV 2 s h. FIX c. DNA • podání: intramuskulární injekce • dávka: nejnižší - 2 x 1011 vp/kg • efekt: hladina z na 1 -2% (neměnila se při dávkách 10 -90 injekcí) • komentář: 50% redukce užívaní faktoru a spontánního krvácení po dobu 40 měsíců virus detekován ve všech tělesních tekutinách kromně spermatu neutralizační anti-AAV 2 protilátky v závislosti na dávce viru
studie 3: Avigen I. • studie: fáze I. „dose escalation study“ • pacientů: 9 s hemofilií B • vektor: AAV 2 s h. FIX c. DNA • podání: intramuskulární injekce • dávka: nejnižší - 2 x 1011 vp/kg • efekt: hladina z na 1 -2% (neměnila se při dávkách 10 -90 injekcí) • komentář: 50% redukce užívaní faktoru a spontánního krvácení po dobu 40 měsíců virus detekován ve všech tělesních tekutinách kromně spermatu neutralizační anti-AAV 2 protilátky v závislosti na dávce viru
 studie 4: Avigen II. • studie: fáze I. „dose escalation study“ • pacientů: 6 s „těžkou“ hemofilií B (HCV pozitivní) • vektor: AAV 2 s h. FIX c. DNA • podání: injekce do hepatální arterie • dávka: 8 x 1010 – 2 x 1012 vp/kg • efekt: hladina z do 2% (4 pacienti - nízká a středních dávka) hladina z 3 -12% (2 pacienti - nízká a středních dávka) • komentář: trvání 2 -3 týdny dále po 6 týdnech pokles <1% dočasně pozastaveno virus detekován ve spermatu, nepotvrzen ve spermiích pokles FIX koreloval se vzestupem (9 x) jaterní transaminasy
studie 4: Avigen II. • studie: fáze I. „dose escalation study“ • pacientů: 6 s „těžkou“ hemofilií B (HCV pozitivní) • vektor: AAV 2 s h. FIX c. DNA • podání: injekce do hepatální arterie • dávka: 8 x 1010 – 2 x 1012 vp/kg • efekt: hladina z do 2% (4 pacienti - nízká a středních dávka) hladina z 3 -12% (2 pacienti - nízká a středních dávka) • komentář: trvání 2 -3 týdny dále po 6 týdnech pokles <1% dočasně pozastaveno virus detekován ve spermatu, nepotvrzen ve spermiích pokles FIX koreloval se vzestupem (9 x) jaterní transaminasy
 studie 5: Genstar • studie: fáze I. „dose escalation study“ • pacientů: 3 s „těžkou“ hemofilií A • vektor: oslabený („gutless“) adenovisus s h. FVIII c. DNA • podání: intravenózní injekce • dávka: nízké - vysoké • efekt: bez signifikantního z hladiny (bez ohledu na dávku) • komentář: u vysoké dávky vzestupem jaterní transaminasy a trombocytopenie
studie 5: Genstar • studie: fáze I. „dose escalation study“ • pacientů: 3 s „těžkou“ hemofilií A • vektor: oslabený („gutless“) adenovisus s h. FVIII c. DNA • podání: intravenózní injekce • dávka: nízké - vysoké • efekt: bez signifikantního z hladiny (bez ohledu na dávku) • komentář: u vysoké dávky vzestupem jaterní transaminasy a trombocytopenie
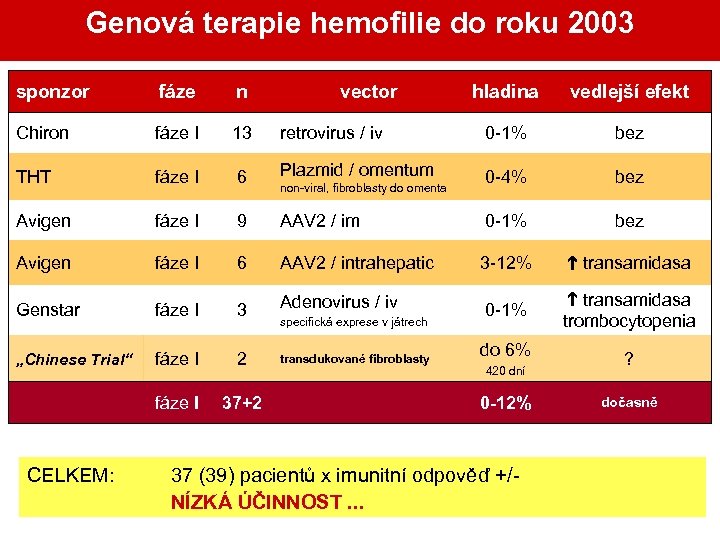 Genová terapie hemofilie do roku 2003 sponzor fáze n Chiron fáze I 13 THT fáze I Avigen hladina vedlejší efekt retrovirus / iv 0 -1% bez 6 Plazmid / omentum 0 -4% bez fáze I 9 AAV 2 / im 0 -1% bez Avigen fáze I 6 AAV 2 / intrahepatic 3 -12% transamidasa Genstar fáze I 3 Adenovirus / iv 0 -1% transamidasa trombocytopenia „Chinese Trial“ fáze I 2 do 6% ? fáze I 37+2 CELKEM: vector non-viral, fibroblasty do omenta specifická exprese v játrech transdukované fibroblasty 420 dní 0 -12% 37 (39) pacientů x imunitní odpověď +/NÍZKÁ ÚČINNOST. . . dočasně
Genová terapie hemofilie do roku 2003 sponzor fáze n Chiron fáze I 13 THT fáze I Avigen hladina vedlejší efekt retrovirus / iv 0 -1% bez 6 Plazmid / omentum 0 -4% bez fáze I 9 AAV 2 / im 0 -1% bez Avigen fáze I 6 AAV 2 / intrahepatic 3 -12% transamidasa Genstar fáze I 3 Adenovirus / iv 0 -1% transamidasa trombocytopenia „Chinese Trial“ fáze I 2 do 6% ? fáze I 37+2 CELKEM: vector non-viral, fibroblasty do omenta specifická exprese v játrech transdukované fibroblasty 420 dní 0 -12% 37 (39) pacientů x imunitní odpověď +/NÍZKÁ ÚČINNOST. . . dočasně
 Hemofilie: genová terapie Ano? – phase I/II klinické studie • nebyla přerušena u žádného pacienta • bez vzniku inhibitoru • zvýšení hladin FVIII/FIX (nižší než u zvířecích modelů) - klinicky nesignifikantní Ekonomické kriterium • Finančně dostupné pro rozvojové země • Jen 20% pacientu má přístup k „high-tech“ terapii z ekonomicky rozvinutých zemí Možnost opravy porušených genů • náhrada mutovaného úseku DNA za nemutovanú DNA • nové nevirové vektory: DNA-RNA oligont. Zvířecí modely Zavedené modely Ne? vektory (i oslabené) vyvolávají zánětlivou reakci 1 úmrtí po podání Adenovirálního vektoru do hepatální artérie (zánětlivá reakce, horečka, respirační potíže multiorgánové selhání Studie s „gutted“ Adenovir. V. zastavena po objevení: horeček, trombocytopenie (obnovena s nižšími dávkami) riziko vzniku malignity Náhodné chromozomální integrace: aktivace protoonkogenů / inaktivace tumor supresorů 2/10 případy leukémie „Phase I“klinické studie SCID retrovirální vektor integrován v blízkosti protoonkogenu LMO 2 leden 2003 FDA pozastavilo všechny studie s retrovir. v. u krevních kmenových buněk „Primum non nocere“
Hemofilie: genová terapie Ano? – phase I/II klinické studie • nebyla přerušena u žádného pacienta • bez vzniku inhibitoru • zvýšení hladin FVIII/FIX (nižší než u zvířecích modelů) - klinicky nesignifikantní Ekonomické kriterium • Finančně dostupné pro rozvojové země • Jen 20% pacientu má přístup k „high-tech“ terapii z ekonomicky rozvinutých zemí Možnost opravy porušených genů • náhrada mutovaného úseku DNA za nemutovanú DNA • nové nevirové vektory: DNA-RNA oligont. Zvířecí modely Zavedené modely Ne? vektory (i oslabené) vyvolávají zánětlivou reakci 1 úmrtí po podání Adenovirálního vektoru do hepatální artérie (zánětlivá reakce, horečka, respirační potíže multiorgánové selhání Studie s „gutted“ Adenovir. V. zastavena po objevení: horeček, trombocytopenie (obnovena s nižšími dávkami) riziko vzniku malignity Náhodné chromozomální integrace: aktivace protoonkogenů / inaktivace tumor supresorů 2/10 případy leukémie „Phase I“klinické studie SCID retrovirální vektor integrován v blízkosti protoonkogenu LMO 2 leden 2003 FDA pozastavilo všechny studie s retrovir. v. u krevních kmenových buněk „Primum non nocere“
 Molekulární hematologie nemaligní onemocnění www. lf 2. cuni. cz/clip Publikace prezentace > Výukové presentace
Molekulární hematologie nemaligní onemocnění www. lf 2. cuni. cz/clip Publikace prezentace > Výukové presentace
 Trombofilní stavy
Trombofilní stavy
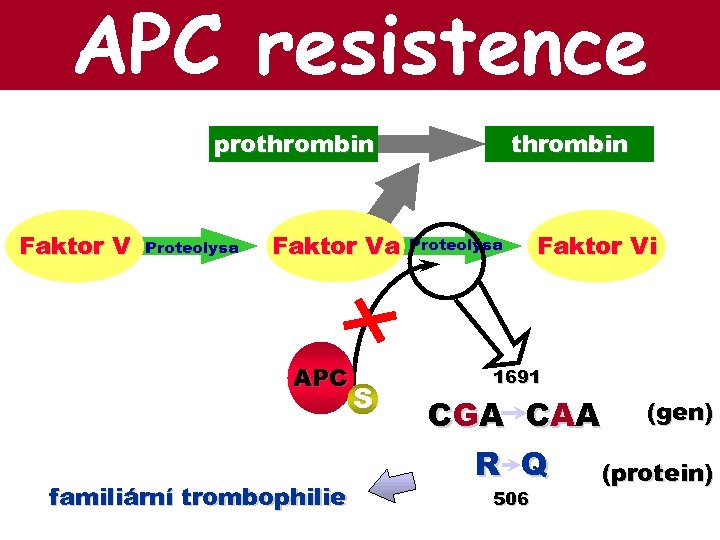 APC resistence prothrombin Faktor V Proteolysa Faktor Va APC familiární trombophilie S thrombin Proteolysa Faktor Vi 1691 CGA CAA (gen) R Q (protein) 506
APC resistence prothrombin Faktor V Proteolysa Faktor Va APC familiární trombophilie S thrombin Proteolysa Faktor Vi 1691 CGA CAA (gen) R Q (protein) 506
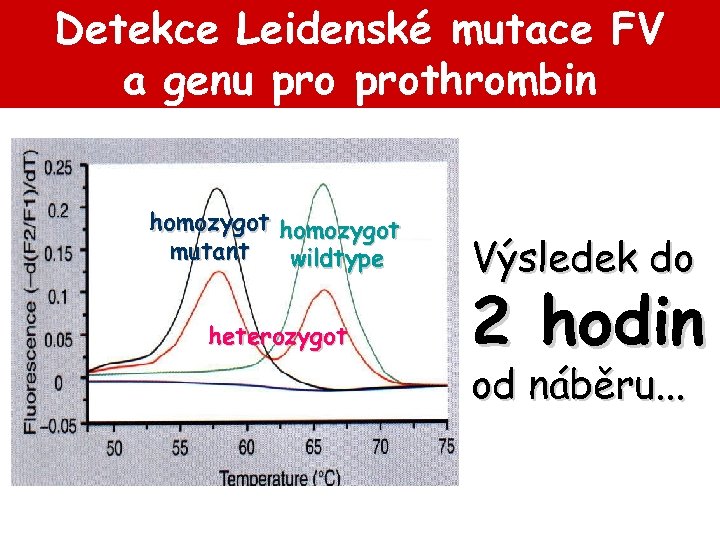 Detekce Leidenské mutace FV a genu prothrombin homozygot mutant wildtype heterozygot Výsledek do 2 hodin od náběru. . .
Detekce Leidenské mutace FV a genu prothrombin homozygot mutant wildtype heterozygot Výsledek do 2 hodin od náběru. . .


