Квантовая и ядерная физика.ppt
- Количество слайдов: 110
 МОДУЛЬ 3. КВАНТОВАЯ И ЯДЕРНАЯ ФИЗИКА
МОДУЛЬ 3. КВАНТОВАЯ И ЯДЕРНАЯ ФИЗИКА
 х Глава 7. Квантовые свойства электромагнитного излучения. Теория атома водорода по Бору 1. Тепловое излучение 2. Фотоэффект 3. Эффект Комптона 4. Формула. Бальмера 5. Модель атома Томсона 6. Ядерная модель атома Резерфорда 7. Атом водорода по Бору
х Глава 7. Квантовые свойства электромагнитного излучения. Теория атома водорода по Бору 1. Тепловое излучение 2. Фотоэффект 3. Эффект Комптона 4. Формула. Бальмера 5. Модель атома Томсона 6. Ядерная модель атома Резерфорда 7. Атом водорода по Бору
 х 1. Тепловое излучение – электромагнитное излучение, испускаемое веществом возникающее за счет его внутренней энергии. Все другие виды свечения (излучения света), возбуждаемые за счет любого другого вида энергии, кроме теплового, называются хемилюминесценция люминесценцией: электролюминесценция фотолюминесценция Опыт показывает, что единственным видом излучения, которое может находиться в равновесии с излучающими телами, является тепловое излучение.
х 1. Тепловое излучение – электромагнитное излучение, испускаемое веществом возникающее за счет его внутренней энергии. Все другие виды свечения (излучения света), возбуждаемые за счет любого другого вида энергии, кроме теплового, называются хемилюминесценция люминесценцией: электролюминесценция фотолюминесценция Опыт показывает, что единственным видом излучения, которое может находиться в равновесии с излучающими телами, является тепловое излучение.
 х Закон Кирхгофа Поток энергии, испускаемый единицей поверхности излучающего тела в единицу времени во всех направлениях называется энергетической светимостью тела (R) [R] = Вт/м 2. . , Т -спектральная плотность энергетической светимости или лучеиспускательная способность тела. Таким образом, - есть функция ω и T соответственно и ;
х Закон Кирхгофа Поток энергии, испускаемый единицей поверхности излучающего тела в единицу времени во всех направлениях называется энергетической светимостью тела (R) [R] = Вт/м 2. . , Т -спектральная плотность энергетической светимости или лучеиспускательная способность тела. Таким образом, - есть функция ω и T соответственно и ;
 х Энергетическая светимость: или поглощательная способность тела. Для тела, полностью поглощающего излучения всех частот - абсолютно черное тело. и меньше единицы - серое тело. Реальное тело всегда отражает часть энергии падающего на него излучения
х Энергетическая светимость: или поглощательная способность тела. Для тела, полностью поглощающего излучения всех частот - абсолютно черное тело. и меньше единицы - серое тело. Реальное тело всегда отражает часть энергии падающего на него излучения
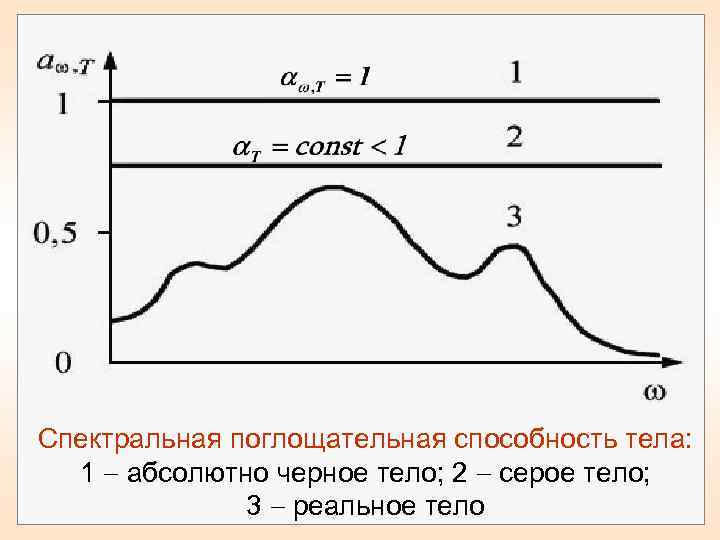 Спектральная поглощательная способность тела: 1 абсолютно черное тело; 2 серое тело; 3 реальное тело
Спектральная поглощательная способность тела: 1 абсолютно черное тело; 2 серое тело; 3 реальное тело
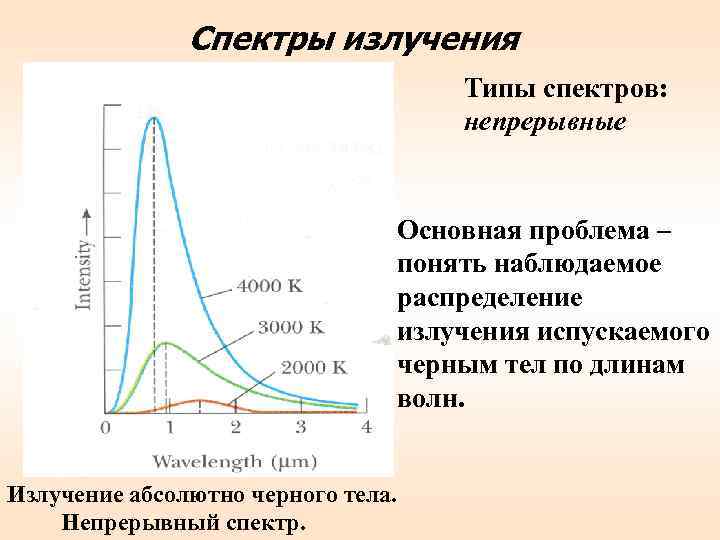 Спектры излучения Типы спектров: непрерывные Основная проблема – понять наблюдаемое распределение излучения испускаемого черным тел по длинам волн. Излучение абсолютно черного тела. Непрерывный спектр.
Спектры излучения Типы спектров: непрерывные Основная проблема – понять наблюдаемое распределение излучения испускаемого черным тел по длинам волн. Излучение абсолютно черного тела. Непрерывный спектр.
 х Кирхгоф Густав Роберт (1824 – 1887) – немецкий физик. Работы посвящены электричеству, механике, гидродинамике, математической физике, оптике, гидродинамике. Построил общую теорию движению тока в проводниках. Развил строгую теорию дифракции. Установил один из основных законов теплового излучения, согласно которому отношение испускательной способности тела к поглощательной не зависит от природы излучающего тела (закон Кирхгофа). Густав Кирхгоф в 1856 году сформулировал закон (он же в 1862 году предложил модель абсолютно черного тела).
х Кирхгоф Густав Роберт (1824 – 1887) – немецкий физик. Работы посвящены электричеству, механике, гидродинамике, математической физике, оптике, гидродинамике. Построил общую теорию движению тока в проводниках. Развил строгую теорию дифракции. Установил один из основных законов теплового излучения, согласно которому отношение испускательной способности тела к поглощательной не зависит от природы излучающего тела (закон Кирхгофа). Густав Кирхгоф в 1856 году сформулировал закон (он же в 1862 году предложил модель абсолютно черного тела).
 х
х
 х – универсальная функция Кирхгофа Сажа или платиновая чернь имеют поглощающую способность
х – универсальная функция Кирхгофа Сажа или платиновая чернь имеют поглощающую способность
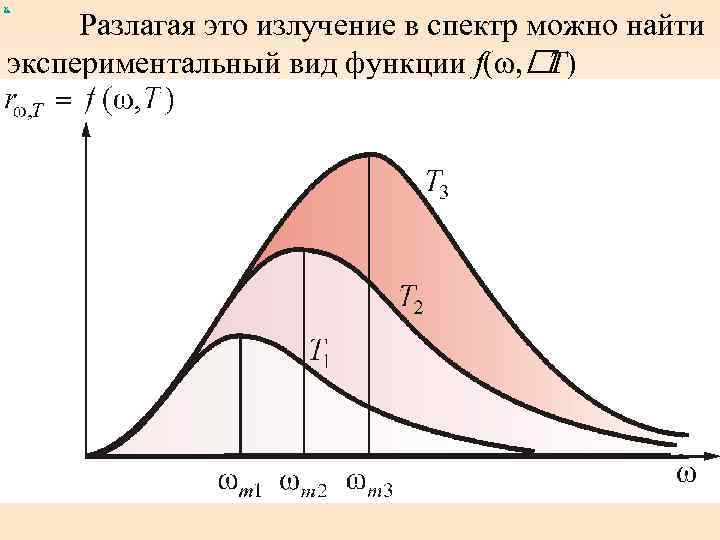 х Разлагая это излучение в спектр можно найти экспериментальный вид функции f(ω, T)
х Разлагая это излучение в спектр можно найти экспериментальный вид функции f(ω, T)
 По определению a , T не может быть больше единицы. Тело, у которого a , T меньше единицы и одинакова по всему диапазону частот, называют серым телом. Тело, у которого a , T равно единицы- абсолютно черное тело Реальное тело всегда отражает часть энергии падающего на него излучения (рис. ).
По определению a , T не может быть больше единицы. Тело, у которого a , T меньше единицы и одинакова по всему диапазону частот, называют серым телом. Тело, у которого a , T равно единицы- абсолютно черное тело Реальное тело всегда отражает часть энергии падающего на него излучения (рис. ).
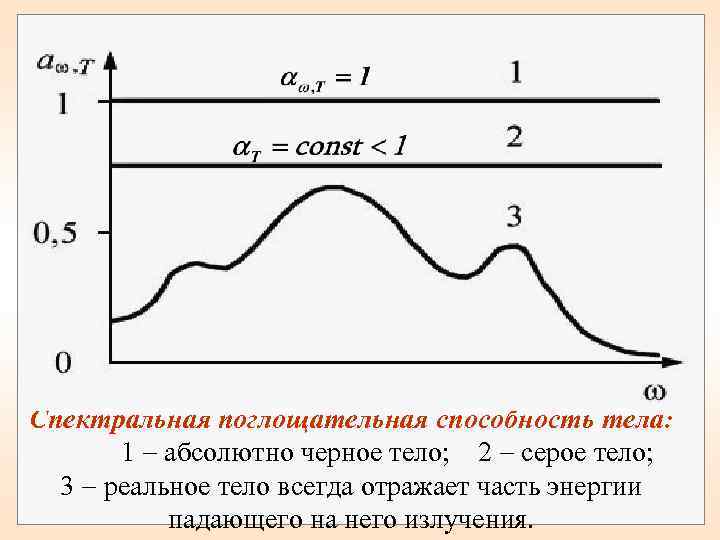 Спектральная поглощательная способность тела: 1 абсолютно черное тело; 2 серое тело; 3 реальное тело всегда отражает часть энергии падающего на него излучения.
Спектральная поглощательная способность тела: 1 абсолютно черное тело; 2 серое тело; 3 реальное тело всегда отражает часть энергии падающего на него излучения.
 х Закон Стефана-Больцмана Австрийский физик Стефан в 1879 году анализируя экспериментальные данные, пришел к выводу, что энергетическая светимость любого тела пропорциональна Т 4. Больцман Людвиг (1844 – 1906) – австрийский физик-теоретик, один из основоположников классической статической физик. Основные работы в области кинетической газов, теории л термодинамики и ное кинетическое уравнение газов, являющееся основой физической кинематики. Впервые применил к излучению принципы термодинамики. Позднее Больцман, применив термодинамический метод к исследованию черного излучения, показал, что это
х Закон Стефана-Больцмана Австрийский физик Стефан в 1879 году анализируя экспериментальные данные, пришел к выводу, что энергетическая светимость любого тела пропорциональна Т 4. Больцман Людвиг (1844 – 1906) – австрийский физик-теоретик, один из основоположников классической статической физик. Основные работы в области кинетической газов, теории л термодинамики и ное кинетическое уравнение газов, являющееся основой физической кинематики. Впервые применил к излучению принципы термодинамики. Позднее Больцман, применив термодинамический метод к исследованию черного излучения, показал, что это
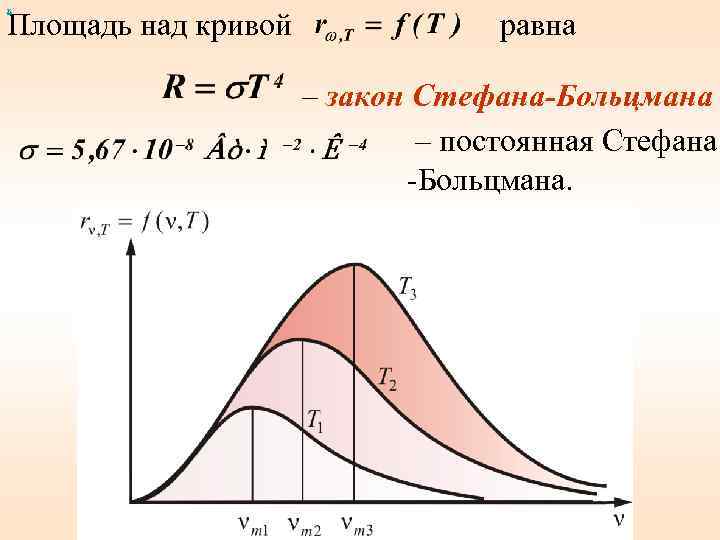 х Площадь над кривой равна – закон Стефана-Больцмана – постоянная Стефана -Больцмана.
х Площадь над кривой равна – закон Стефана-Больцмана – постоянная Стефана -Больцмана.
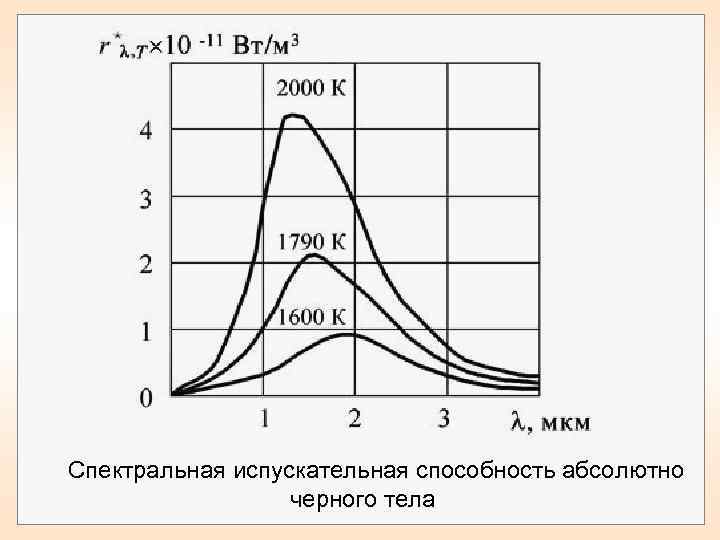 Спектральная испускательная способность абсолютно черного тела
Спектральная испускательная способность абсолютно черного тела
 х Законы смещения Вина В 1893 году немецкий ученый Вильгельм Вин рассмотрел задачу об адиабатическом сжатии черного излучения цилиндрическом сосуде. При вдвижении поршня энергия излучения единицы объема (плотность энергии) будет возрастать по двум причинам: • за счёт уменьшения объема (общая величина энергии постоянна); • за счёт работы совершаемой поршнем против давления излучения.
х Законы смещения Вина В 1893 году немецкий ученый Вильгельм Вин рассмотрел задачу об адиабатическом сжатии черного излучения цилиндрическом сосуде. При вдвижении поршня энергия излучения единицы объема (плотность энергии) будет возрастать по двум причинам: • за счёт уменьшения объема (общая величина энергии постоянна); • за счёт работы совершаемой поршнем против давления излучения.
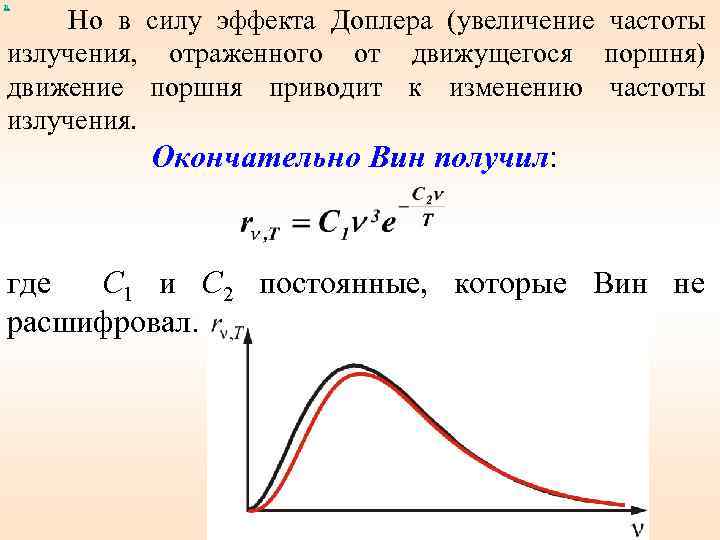 х Но в силу эффекта Доплера (увеличение частоты излучения, отраженного от движущегося поршня) движение поршня приводит к изменению частоты излучения. Окончательно Вин получил: где С 1 и С 2 постоянные, которые Вин не расшифровал. .
х Но в силу эффекта Доплера (увеличение частоты излучения, отраженного от движущегося поршня) движение поршня приводит к изменению частоты излучения. Окончательно Вин получил: где С 1 и С 2 постоянные, которые Вин не расшифровал. .
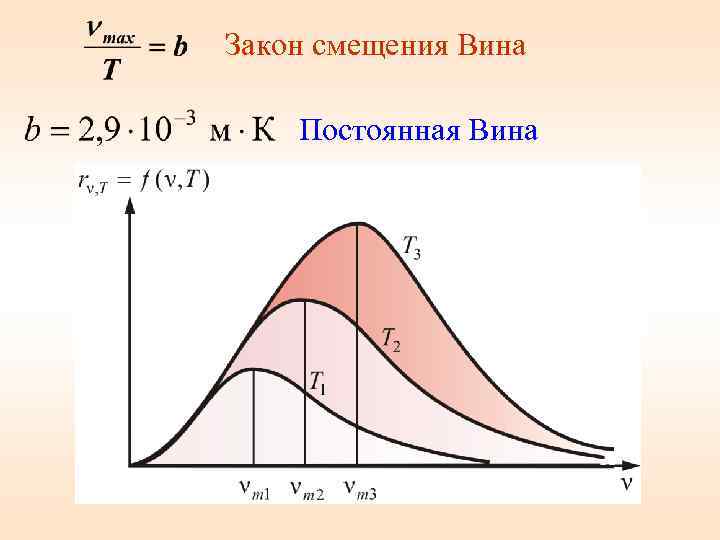 Закон смещения Вина Постоянная Вина
Закон смещения Вина Постоянная Вина
 х Формула Рэлея-Джинса Рэлей (Стретт) Джон Уильям (1842 – 1919) английский физик. Работы посвящены теории колебаний, одним из основоположников которой он является, акустике, теории теплового излучения, молекулярной физике, гидродинамике, электромагнетизму, оптике. Исследовал колебания упругих тел, первый обратил внимание на автоколебания. Заложил основы теории молекулярного рассеяния света, объяснил голубой цвет неба. Сконструировал рефрактометр (рефрактометр Рэлея). Рассмотрел равновесное излучение в замкнутой полости с зеркальными стенками как совокупность стоячих электромагнитных волн (осцилляторов).
х Формула Рэлея-Джинса Рэлей (Стретт) Джон Уильям (1842 – 1919) английский физик. Работы посвящены теории колебаний, одним из основоположников которой он является, акустике, теории теплового излучения, молекулярной физике, гидродинамике, электромагнетизму, оптике. Исследовал колебания упругих тел, первый обратил внимание на автоколебания. Заложил основы теории молекулярного рассеяния света, объяснил голубой цвет неба. Сконструировал рефрактометр (рефрактометр Рэлея). Рассмотрел равновесное излучение в замкнутой полости с зеркальными стенками как совокупность стоячих электромагнитных волн (осцилляторов).
 х Джинс Джеймс Хопвуд (1877 – 1946) – английский физик и астрофизик. Основные физические исследование посвящены кинетической теории газов и теории теплового излучения. Вывел в 1905 формулу плотности энергии (закон Релея-Джинса). Работы Джинса посвящены также квантовой теории, математической теории электричества и магнетизма, теоретической механике, теории относительности.
х Джинс Джеймс Хопвуд (1877 – 1946) – английский физик и астрофизик. Основные физические исследование посвящены кинетической теории газов и теории теплового излучения. Вывел в 1905 формулу плотности энергии (закон Релея-Джинса). Работы Джинса посвящены также квантовой теории, математической теории электричества и магнетизма, теоретической механике, теории относительности.
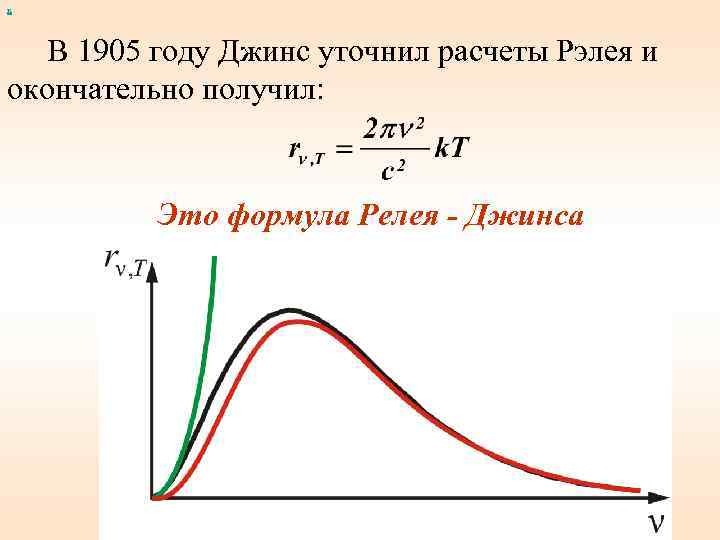 х В 1905 году Джинс уточнил расчеты Рэлея и окончательно получил: Это формула Релея - Джинса
х В 1905 году Джинс уточнил расчеты Рэлея и окончательно получил: Это формула Релея - Джинса
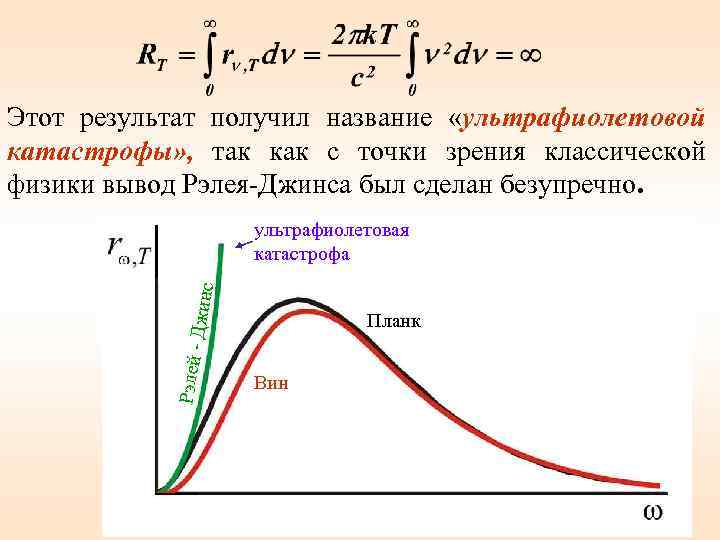 Этот результат получил название «ультрафиолетовой катастрофы» , так как с точки зрения классической физики вывод Рэлея-Джинса был сделан безупречно. Рэлей - Джинс ультрафиолетовая катастрофа. Планк Вин 23
Этот результат получил название «ультрафиолетовой катастрофы» , так как с точки зрения классической физики вывод Рэлея-Джинса был сделан безупречно. Рэлей - Джинс ультрафиолетовая катастрофа. Планк Вин 23
 х Формула Планк Макс Карл Эрнст Людвиг (1858 – 1947) – немецкий физик-теоретик, основоположник квантовой теории. Работы относятся к термодинамике, теории теплового излучения, теории относительности, квантовой теории, истории и методологии физики, философии науки. Вывел закон распределения энергии в спектре абсолютно черного тела. Ввел фундаментальную постоянную с размерностью действия. Формула закона Планка сразу же получила экспериментальное подтверждение.
х Формула Планк Макс Карл Эрнст Людвиг (1858 – 1947) – немецкий физик-теоретик, основоположник квантовой теории. Работы относятся к термодинамике, теории теплового излучения, теории относительности, квантовой теории, истории и методологии физики, философии науки. Вывел закон распределения энергии в спектре абсолютно черного тела. Ввел фундаментальную постоянную с размерностью действия. Формула закона Планка сразу же получила экспериментальное подтверждение.
 х Термодинамическая вероятность – число возможных микроскопических комбинаций, совместимое с данным состоянием в целом. Энергия осциллятора должна быть целым кратным некоторой единицы энергии, пропорциональной его частоте: Минимальная порция энергии:
х Термодинамическая вероятность – число возможных микроскопических комбинаций, совместимое с данным состоянием в целом. Энергия осциллятора должна быть целым кратным некоторой единицы энергии, пропорциональной его частоте: Минимальная порция энергии:
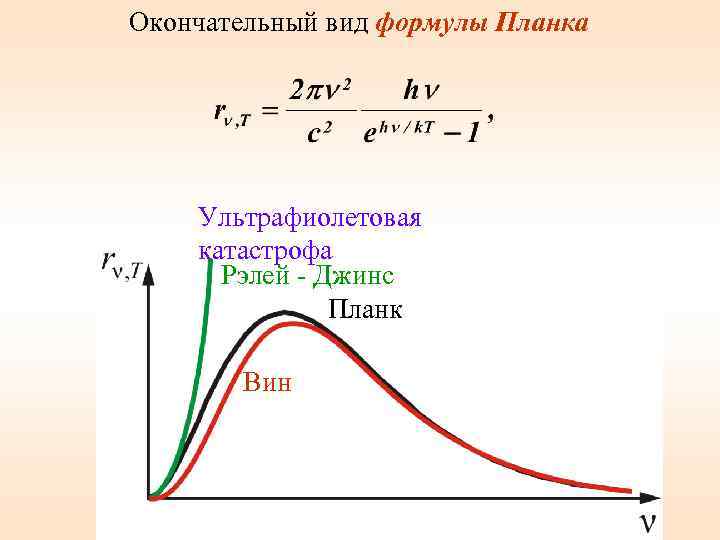 Окончательный вид формулы Планка Ультрафиолетовая катастрофа Рэлей - Джинс Планк Вин
Окончательный вид формулы Планка Ультрафиолетовая катастрофа Рэлей - Джинс Планк Вин
 х Из формулы Планка 1) В области малых частот, т. е. при Получаем формулу Рэлея-Джинса
х Из формулы Планка 1) В области малых частот, т. е. при Получаем формулу Рэлея-Джинса
 2) В области больших частот, при из формулы Планка получаем формулу Вина 3) Также из формулы Планка можно получить закон Стефана-Больцмана: . Отсюда можно вывести закон Стефана-Больцмана:
2) В области больших частот, при из формулы Планка получаем формулу Вина 3) Также из формулы Планка можно получить закон Стефана-Больцмана: . Отсюда можно вывести закон Стефана-Больцмана:
 х Другая форма записи формулы Планка
х Другая форма записи формулы Планка
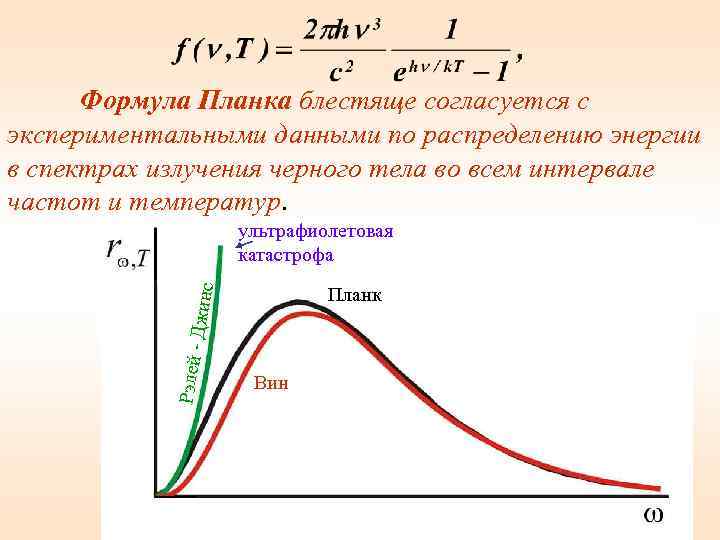 Формула Планка блестяще согласуется с экспериментальными данными по распределению энергии в спектрах излучения черного тела во всем интервале частот и температур. Рэлей - Джинс ультрафиолетовая катастрофа Планк . Вин 30
Формула Планка блестяще согласуется с экспериментальными данными по распределению энергии в спектрах излучения черного тела во всем интервале частот и температур. Рэлей - Джинс ультрафиолетовая катастрофа Планк . Вин 30
 Из формулы Планка, зная универсальные постоянные h, k и c, можно вычислить постоянную Стефана-Больцмана σ и Вина b. С другой стороны, зная экспериментальные значения σ и b, можно вычислить h и k (именно так и было впервые найдено числовое значение постоянной Планка).
Из формулы Планка, зная универсальные постоянные h, k и c, можно вычислить постоянную Стефана-Больцмана σ и Вина b. С другой стороны, зная экспериментальные значения σ и b, можно вычислить h и k (именно так и было впервые найдено числовое значение постоянной Планка).
 Теоретически вывод этой формулы М. Планк изложил 14 декабря 1900 г. на заседании Немецкого физического общества. Этот день стал датой рождения квантовой физики.
Теоретически вывод этой формулы М. Планк изложил 14 декабря 1900 г. на заседании Немецкого физического общества. Этот день стал датой рождения квантовой физики.
 х 2. Фотоэффект Различают фотоэффект внешний, внутренний, вентильный и многофотонный. Внешним фотоэффектом называется испускание электронов веществом под действием электромагнитного излучения. Внутренний фотоэффект – это вызванные электромагнитным излучением переходы электронов внутри полупроводника или диэлектрика из связанных состояний в свободные без вылета наружу. Вентильный фотоэффект, – возникновение эдс (фото-эдс) при освещении контакта двух разных полупроводников или полупроводника и металла (при отсутствии внешнего электрического поля).
х 2. Фотоэффект Различают фотоэффект внешний, внутренний, вентильный и многофотонный. Внешним фотоэффектом называется испускание электронов веществом под действием электромагнитного излучения. Внутренний фотоэффект – это вызванные электромагнитным излучением переходы электронов внутри полупроводника или диэлектрика из связанных состояний в свободные без вылета наружу. Вентильный фотоэффект, – возникновение эдс (фото-эдс) при освещении контакта двух разных полупроводников или полупроводника и металла (при отсутствии внешнего электрического поля).
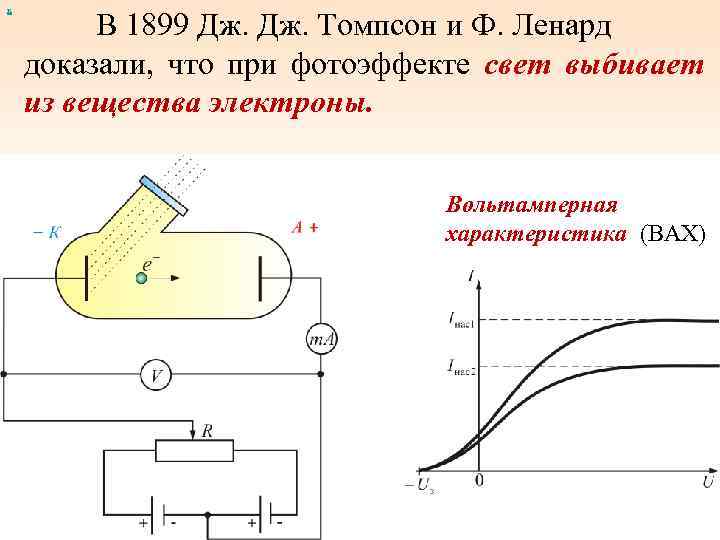 х В 1899 Дж. Томпсон и Ф. Ленард доказали, что при фотоэффекте свет выбивает из вещества электроны. Вольтамперная характеристика (ВАХ)
х В 1899 Дж. Томпсон и Ф. Ленард доказали, что при фотоэффекте свет выбивает из вещества электроны. Вольтамперная характеристика (ВАХ)
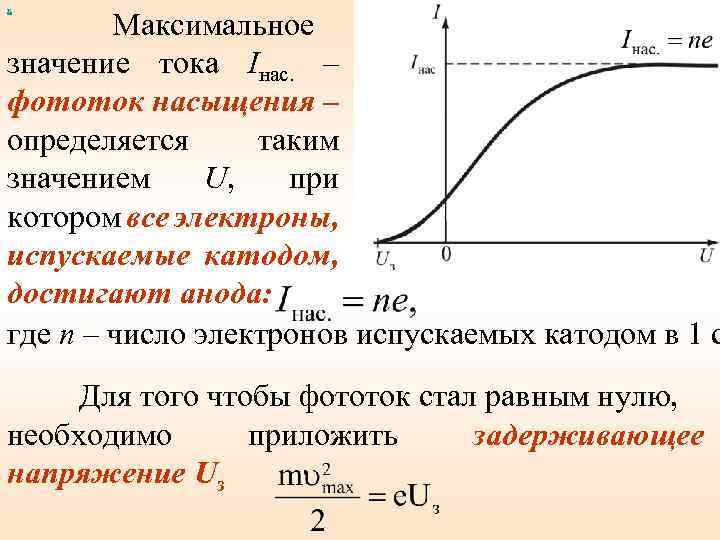 х Максимальное значение тока Iнас. – фототок насыщения – определяется таким значением U, при котором все электроны, испускаемые катодом, достигают анода: где n – число электронов испускаемых катодом в 1 с Для того чтобы фототок стал равным нулю, необходимо приложить задерживающее напряжение Uз
х Максимальное значение тока Iнас. – фототок насыщения – определяется таким значением U, при котором все электроны, испускаемые катодом, достигают анода: где n – число электронов испускаемых катодом в 1 с Для того чтобы фототок стал равным нулю, необходимо приложить задерживающее напряжение Uз
 Законы фотоэффекта: 1. Закон Столетова: при фиксированной частоте падающего света число фотоэлектронов, вырываемых из катода в единицу времени, пропорционально интенсивности света. 2. Максимальная скорость фотоэлектронов не зависит от интенсивности падающего света, а определяется только его частотой ν. 3. Для каждого вещества существует красная граница фотоэффекта, т. е. минимальная частота ν 0 света (зависящая от химической природы вещества и состояния его поверхности), ниже которой фотоэффект невозможен:
Законы фотоэффекта: 1. Закон Столетова: при фиксированной частоте падающего света число фотоэлектронов, вырываемых из катода в единицу времени, пропорционально интенсивности света. 2. Максимальная скорость фотоэлектронов не зависит от интенсивности падающего света, а определяется только его частотой ν. 3. Для каждого вещества существует красная граница фотоэффекта, т. е. минимальная частота ν 0 света (зависящая от химической природы вещества и состояния его поверхности), ниже которой фотоэффект невозможен:
 Объяснение наблюдаемых экспериментально закономерностей было дано Эйнштейном: Свет не только испускается (Планк), но и распространяется, и поглощается веществом отдельными порциями (квантами), энергия которых : ε = hν. Уравнение Эйнштейна для фотоэффекта: А – работа выхода электронов.
Объяснение наблюдаемых экспериментально закономерностей было дано Эйнштейном: Свет не только испускается (Планк), но и распространяется, и поглощается веществом отдельными порциями (квантами), энергия которых : ε = hν. Уравнение Эйнштейна для фотоэффекта: А – работа выхода электронов.
 х Из теории Эйнштейна для фотоэффекта следует: 1. Увеличение интенсивности света означает увеличение числа налетающих фотонов, которые выбивают с поверхности металла больше электронов. Но так как энергия фотонов одна и та же, максимальная кинетическая энергия электрона не изменится (подтверждение I закона фотоэффекта). 2. При увеличении частоты падающего света максимальная кинетическая энергия электронов возрастает линейно по формуле Эйнштейна (т. е. II закон фотоэффекта).
х Из теории Эйнштейна для фотоэффекта следует: 1. Увеличение интенсивности света означает увеличение числа налетающих фотонов, которые выбивают с поверхности металла больше электронов. Но так как энергия фотонов одна и та же, максимальная кинетическая энергия электрона не изменится (подтверждение I закона фотоэффекта). 2. При увеличении частоты падающего света максимальная кинетическая энергия электронов возрастает линейно по формуле Эйнштейна (т. е. II закон фотоэффекта).
 х 3. Если частота ν меньше частоты ν 0, при которой hν 0 = A, то выбивание электронов с поверхности не происходит. (III закон). Уравнение Эйнштейна было подтверждено опытами Милликена, выполненными в 1913 – 1914 гг.
х 3. Если частота ν меньше частоты ν 0, при которой hν 0 = A, то выбивание электронов с поверхности не происходит. (III закон). Уравнение Эйнштейна было подтверждено опытами Милликена, выполненными в 1913 – 1914 гг.

 Альберт Эйнштейн (Albert Einstein) Родился 14 марта 1879 Ульм (Ulm) Германия Умер 18 апреля 1955 Принцетон (Princeton ) США (New Jersey) величайший ученый 20 века важнейшие работы теория относительности и статистическая механика квантовая космология Нобелевская премия по физике 1921
Альберт Эйнштейн (Albert Einstein) Родился 14 марта 1879 Ульм (Ulm) Германия Умер 18 апреля 1955 Принцетон (Princeton ) США (New Jersey) величайший ученый 20 века важнейшие работы теория относительности и статистическая механика квантовая космология Нобелевская премия по физике 1921
 х В 1905 г. Эйнштейн выдвинул смелую идею, обобщавшую гипотезу квантов, и положил ее в основу новой теории света (квантовой теории фотоэффекта). Согласно Эйнштейну свет частотой ν не только испускается, как это предполагал Планк, но и распространяется и поглощается веществом отдельными порциями (квантами), энергия которых ε 0 = hν. Таким образом, распространение света нужно рассматривать не как непрерывный волновой процесс, а как поток локализованных в пространстве дискретных световых квантов, движущихся со скоростью c распространения света в вакууме Кванты электромагнитного излучения получили название фотонов.
х В 1905 г. Эйнштейн выдвинул смелую идею, обобщавшую гипотезу квантов, и положил ее в основу новой теории света (квантовой теории фотоэффекта). Согласно Эйнштейну свет частотой ν не только испускается, как это предполагал Планк, но и распространяется и поглощается веществом отдельными порциями (квантами), энергия которых ε 0 = hν. Таким образом, распространение света нужно рассматривать не как непрерывный волновой процесс, а как поток локализованных в пространстве дискретных световых квантов, движущихся со скоростью c распространения света в вакууме Кванты электромагнитного излучения получили название фотонов.
 х Масса, энергия и импульс фотона Фотон обладает энергией W = hν = h(c/λ). Для видимого света λ = 500 Ǻ и W = 2, 2 э. В, для рентгеновских лучей λ = 10– 4 Ǻ и W = 0, 5 э. В. Фотон обладает инертной массой: W = mc 2 mф = W/c 2 = hc/λc 2 = h/cλ; Фотон движется со скоростью света c = 3· 108 м/с. Подставим это значение скорости в выражение: Фотон – частица, не обладающая массой покоя потому, что она может существовать только двигаясь со скоростью света c.
х Масса, энергия и импульс фотона Фотон обладает энергией W = hν = h(c/λ). Для видимого света λ = 500 Ǻ и W = 2, 2 э. В, для рентгеновских лучей λ = 10– 4 Ǻ и W = 0, 5 э. В. Фотон обладает инертной массой: W = mc 2 mф = W/c 2 = hc/λc 2 = h/cλ; Фотон движется со скоростью света c = 3· 108 м/с. Подставим это значение скорости в выражение: Фотон – частица, не обладающая массой покоя потому, что она может существовать только двигаясь со скоростью света c.
 х : Релятивистское выражение для импульса: И для энергии: Отсюда связь : – волновое число – волновой вектор фотона.
х : Релятивистское выражение для импульса: И для энергии: Отсюда связь : – волновое число – волновой вектор фотона.
 х 3. Эффект Комптона А. Г. Комптон занимался изучением рассеяния рентгеновского излучения различными веществами и обнаружил, что частота рассеянного света меньше частоты падающего света.
х 3. Эффект Комптона А. Г. Комптон занимался изучением рассеяния рентгеновского излучения различными веществами и обнаружил, что частота рассеянного света меньше частоты падающего света.
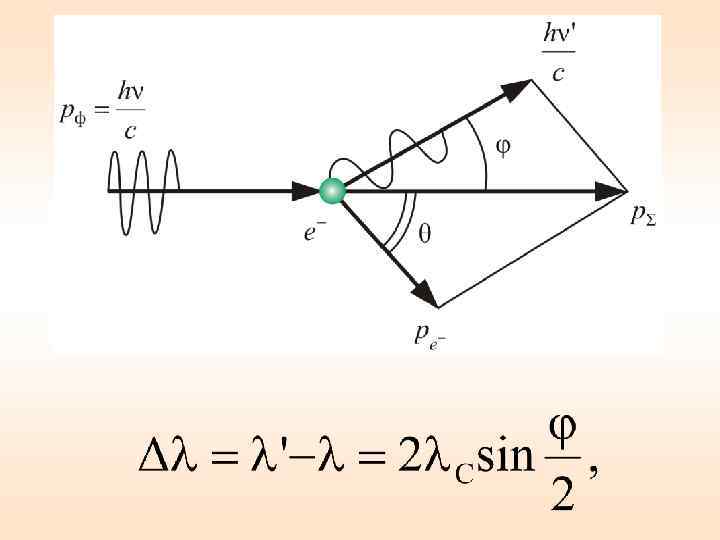
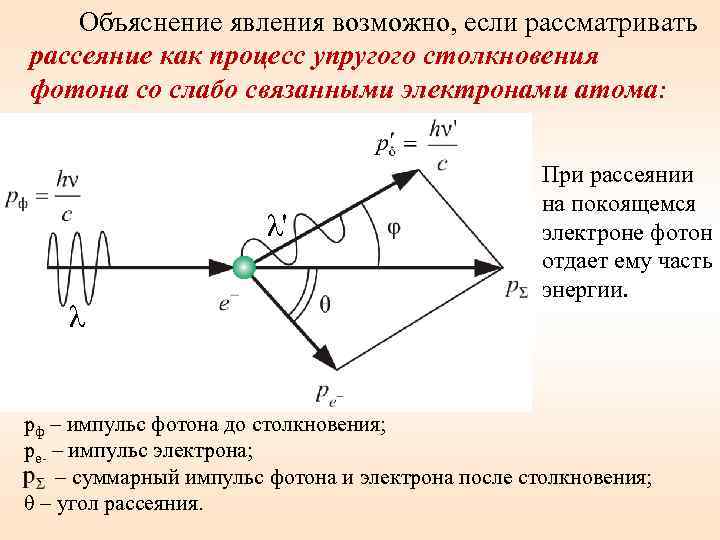 Объяснение явления возможно, если рассматривать рассеяние как процесс упругого столкновения фотона со слабо связанными электронами атома: λ' λ При рассеянии на покоящемся электроне фотон отдает ему часть энергии. рф – импульс фотона до столкновения; ре- – импульс электрона; – суммарный импульс фотона и электрона после столкновения; θ – угол рассеяния.
Объяснение явления возможно, если рассматривать рассеяние как процесс упругого столкновения фотона со слабо связанными электронами атома: λ' λ При рассеянии на покоящемся электроне фотон отдает ему часть энергии. рф – импульс фотона до столкновения; ре- – импульс электрона; – суммарный импульс фотона и электрона после столкновения; θ – угол рассеяния.
 х Опыты показали, что разность Δλ = λ – λ'' не зависит от длины волны λ падающего излучения и природы рассеивающего вещества, а определяется только углом рассеяния φ λ' – длина волны рассеянного излучения, λe – комптоновская длина волны (при рассеянии фотона на электроне λe =2, 426 пм).
х Опыты показали, что разность Δλ = λ – λ'' не зависит от длины волны λ падающего излучения и природы рассеивающего вещества, а определяется только углом рассеяния φ λ' – длина волны рассеянного излучения, λe – комптоновская длина волны (при рассеянии фотона на электроне λe =2, 426 пм).
 Опытным путем Комптон установил, что разность длин волн рассеянного и падающего излучения не зависит от материала рассеивателя, а определяется только величиной угла рассеяния θ: = с (1 – cos ). формула Комптона. Значение постоянной с = 2, 426 10 12 м Комптон определил экспериментально.
Опытным путем Комптон установил, что разность длин волн рассеянного и падающего излучения не зависит от материала рассеивателя, а определяется только величиной угла рассеяния θ: = с (1 – cos ). формула Комптона. Значение постоянной с = 2, 426 10 12 м Комптон определил экспериментально.
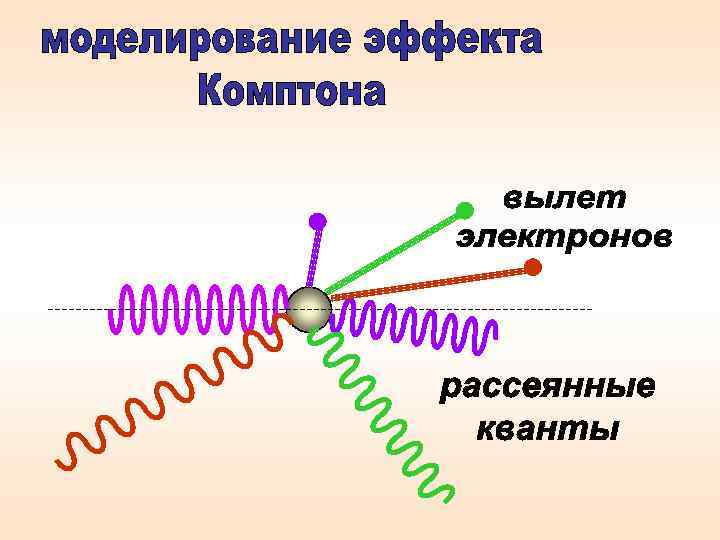
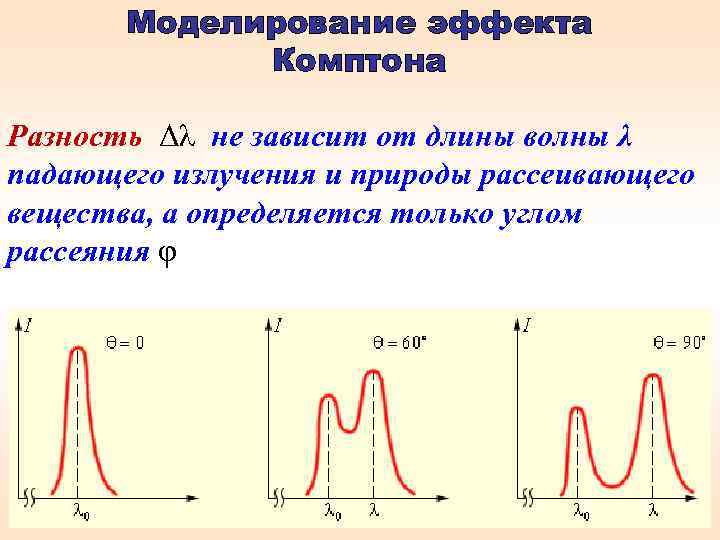 Моделирование эффекта Комптона Разность Δλ не зависит от длины волны λ падающего излучения и природы рассеивающего вещества, а определяется только углом рассеяния φ
Моделирование эффекта Комптона Разность Δλ не зависит от длины волны λ падающего излучения и природы рассеивающего вещества, а определяется только углом рассеяния φ

 х 4. Формула. Бальмера Изолированные атомы в виде разреженного газа или паров металлов испускают спектр, состоящий из отдельных спектральных линий (линейчатый спектр). Изучение атомных спектров послужило ключом к познанию строения атомов. Прежде всего было замечено, что линии в спектрах расположены не беспорядочно, а сериями. Расстояние между линиями в серии закономерно уменьшается по мере перехода от длинных волн к коротким.
х 4. Формула. Бальмера Изолированные атомы в виде разреженного газа или паров металлов испускают спектр, состоящий из отдельных спектральных линий (линейчатый спектр). Изучение атомных спектров послужило ключом к познанию строения атомов. Прежде всего было замечено, что линии в спектрах расположены не беспорядочно, а сериями. Расстояние между линиями в серии закономерно уменьшается по мере перехода от длинных волн к коротким.
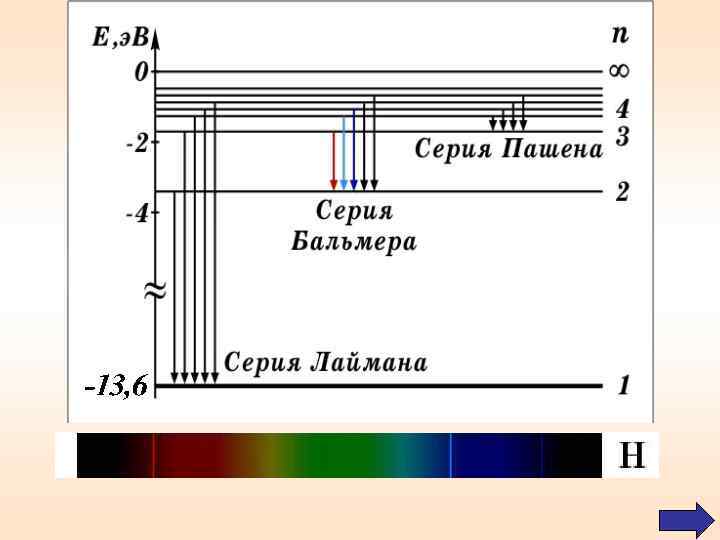
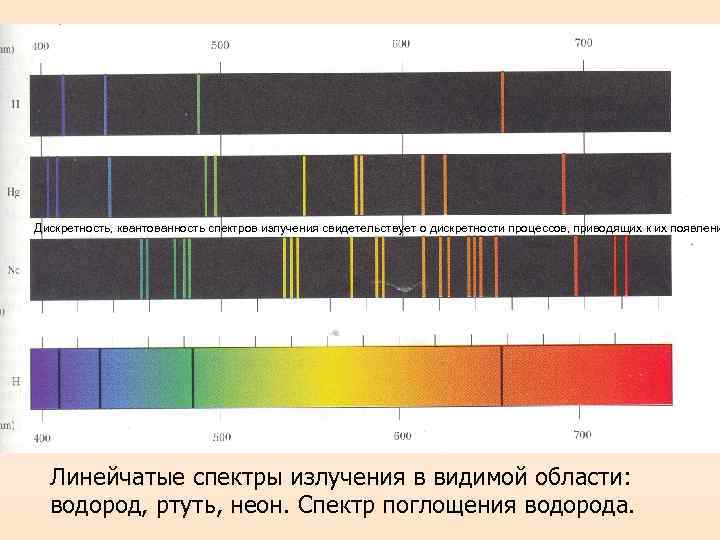 Дискретность, квантованность спектров излучения свидетельствует о дискретности процессов, приводящих к их появлени Линейчатые спектры излучения в видимой области: водород, ртуть, неон. Спектр поглощения водорода.
Дискретность, квантованность спектров излучения свидетельствует о дискретности процессов, приводящих к их появлени Линейчатые спектры излучения в видимой области: водород, ртуть, неон. Спектр поглощения водорода.
 х Швейцарский физик Й. Бальмер в 1885 году установил, что длины волн серии в видимой части спектра водорода могут быть представлены формулой (формула Бальмера): 0 = const, n = 3, 4, 5, … или R = 1, 09· 107 м-1 – постоянная Ридберга, n = 3, 4, 5, … В физике постоянной Ридберга называют и другую величину равную R = R ·с. R = 3, 29· 1015 c-1
х Швейцарский физик Й. Бальмер в 1885 году установил, что длины волн серии в видимой части спектра водорода могут быть представлены формулой (формула Бальмера): 0 = const, n = 3, 4, 5, … или R = 1, 09· 107 м-1 – постоянная Ридберга, n = 3, 4, 5, … В физике постоянной Ридберга называют и другую величину равную R = R ·с. R = 3, 29· 1015 c-1
 х Дальнейшие исследования показали, что в спектре водорода имеется еще несколько серий: Серия Лаймона n = 2, 3, 4, … Серия Пашена n = 4, 5, 6, … Серия Брэкета n = 5, 6, 7, … Серия Пфунда n = 6, 7, 8, …
х Дальнейшие исследования показали, что в спектре водорода имеется еще несколько серий: Серия Лаймона n = 2, 3, 4, … Серия Пашена n = 4, 5, 6, … Серия Брэкета n = 5, 6, 7, … Серия Пфунда n = 6, 7, 8, …
 Обобщенная формула Й. Бальмера или где k = 1, 2, 3, …, n = k + 1, k + 2, ….
Обобщенная формула Й. Бальмера или где k = 1, 2, 3, …, n = k + 1, k + 2, ….
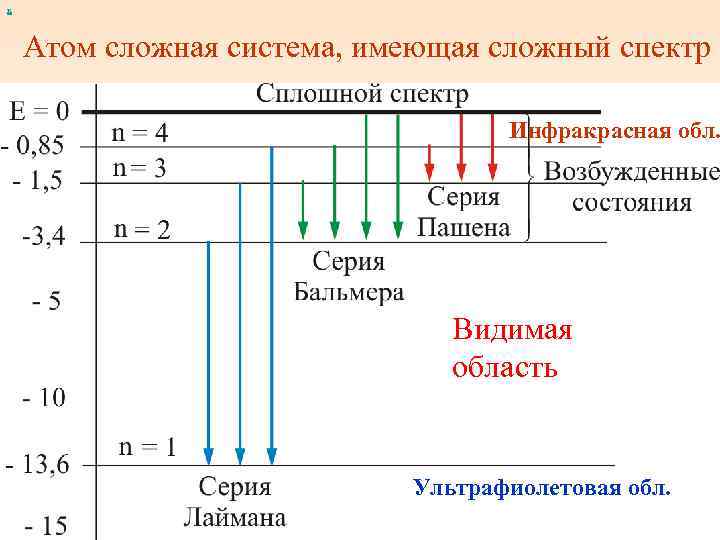 х Атом сложная система, имеющая сложный спектр Инфракрасная обл. Видимая область Ультрафиолетовая обл.
х Атом сложная система, имеющая сложный спектр Инфракрасная обл. Видимая область Ультрафиолетовая обл.
 5. Модель атома Томсона
5. Модель атома Томсона






 1895 - открытие Хлучей Рентгеном 1896 - открытие радиоактивности Беккерелем
1895 - открытие Хлучей Рентгеном 1896 - открытие радиоактивности Беккерелем
 1897 - открытие электрона
1897 - открытие электрона
 Физики «отобрали» атом у химиков
Физики «отобрали» атом у химиков
 Были предложены различные модели строения атома. 1 2 3
Были предложены различные модели строения атома. 1 2 3
 Модель Ж. Перрена (1901)
Модель Ж. Перрена (1901)
 Модель Х. Нагаока (1904)
Модель Х. Нагаока (1904)
 х В 1904 году Дж. Томсон, предложил модель атома: сфера, равномерно заполненная положительным электричеством, внутри которой находятся электроны. Суммарный заряд сферы равен заряду электронов. Атом в целом нейтрален. Теория такого атома давала, что спектр должен быть сложным, но никоим образом не линейчатым, что противоречило экспериментам.
х В 1904 году Дж. Томсон, предложил модель атома: сфера, равномерно заполненная положительным электричеством, внутри которой находятся электроны. Суммарный заряд сферы равен заряду электронов. Атом в целом нейтрален. Теория такого атома давала, что спектр должен быть сложным, но никоим образом не линейчатым, что противоречило экспериментам.
 Какая из моделей верна?
Какая из моделей верна?
 Резерфорд Эрнест (1871– 1937) – английский физик, основоположник ядерной физики. Исследования посвящены атомной и ядерной физике, радиоактивности. Своими фундаментальными открытиями в этих областях заложил основы современного учения о радиоактивности и теории строения атома. В 1899 г. открыл альфа - и бета-лучи. Вместе с Ф. Содди в 1903 г. разработал теорию радиоактивного распада и установил закон радиоактивных превращений. В 1903 году доказал, что альфа-лучи состоят из положительно заряженных частиц. Предсказал существование трансурановых элементов. В 1908 г. ему была присуждена Нобелевская премия.
Резерфорд Эрнест (1871– 1937) – английский физик, основоположник ядерной физики. Исследования посвящены атомной и ядерной физике, радиоактивности. Своими фундаментальными открытиями в этих областях заложил основы современного учения о радиоактивности и теории строения атома. В 1899 г. открыл альфа - и бета-лучи. Вместе с Ф. Содди в 1903 г. разработал теорию радиоактивного распада и установил закон радиоактивных превращений. В 1903 году доказал, что альфа-лучи состоят из положительно заряженных частиц. Предсказал существование трансурановых элементов. В 1908 г. ему была присуждена Нобелевская премия.
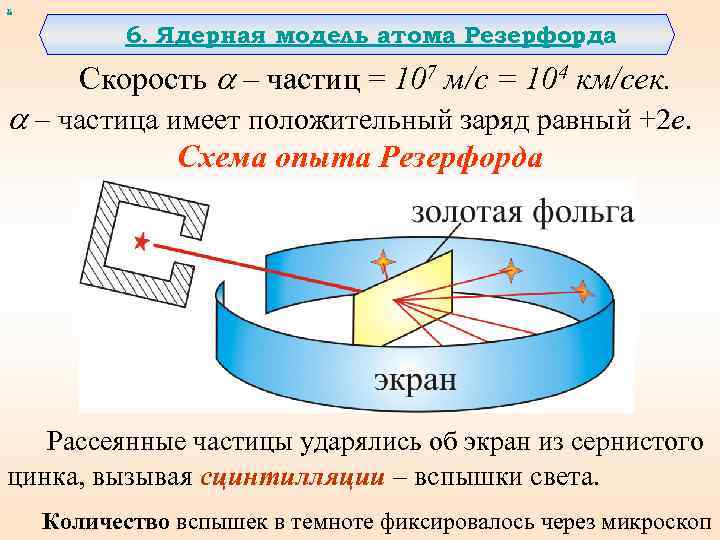 х 6. Ядерная модель атома Резерфорда Скорость – частиц = 107 м/с = 104 км/сек. – частица имеет положительный заряд равный +2 е. Схема опыта Резерфорда Рассеянные частицы ударялись об экран из сернистого цинка, вызывая сцинтилляции – вспышки света. Количество вспышек в темноте фиксировалось через микроскоп
х 6. Ядерная модель атома Резерфорда Скорость – частиц = 107 м/с = 104 км/сек. – частица имеет положительный заряд равный +2 е. Схема опыта Резерфорда Рассеянные частицы ударялись об экран из сернистого цинка, вызывая сцинтилляции – вспышки света. Количество вспышек в темноте фиксировалось через микроскоп
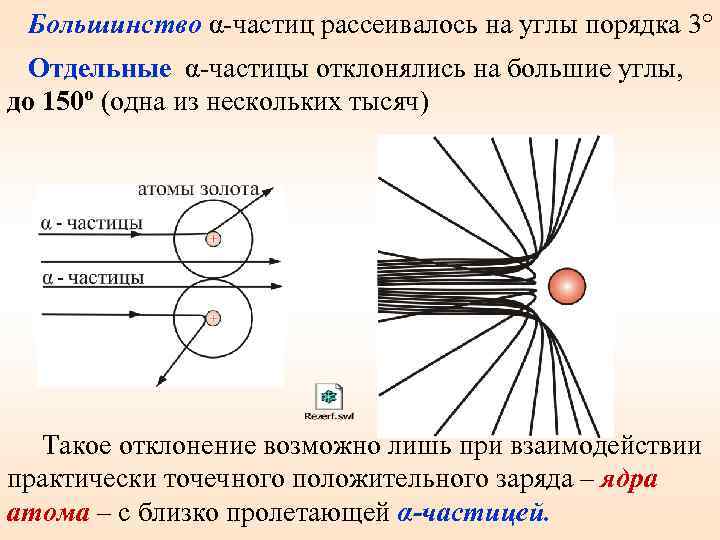 Большинство α-частиц рассеивалось на углы порядка 3° Отдельные α-частицы отклонялись на большие углы, до 150º (одна из нескольких тысяч) Такое отклонение возможно лишь при взаимодействии практически точечного положительного заряда – ядра атома – с близко пролетающей α-частицей.
Большинство α-частиц рассеивалось на углы порядка 3° Отдельные α-частицы отклонялись на большие углы, до 150º (одна из нескольких тысяч) Такое отклонение возможно лишь при взаимодействии практически точечного положительного заряда – ядра атома – с близко пролетающей α-частицей.
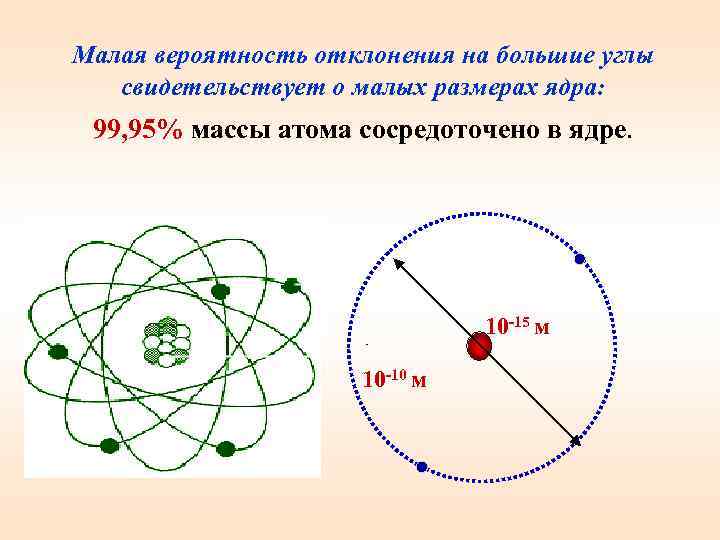 Малая вероятность отклонения на большие углы свидетельствует о малых размерах ядра: 99, 95% массы атома сосредоточено в ядре. 10 -15 м 10 -10 м
Малая вероятность отклонения на большие углы свидетельствует о малых размерах ядра: 99, 95% массы атома сосредоточено в ядре. 10 -15 м 10 -10 м
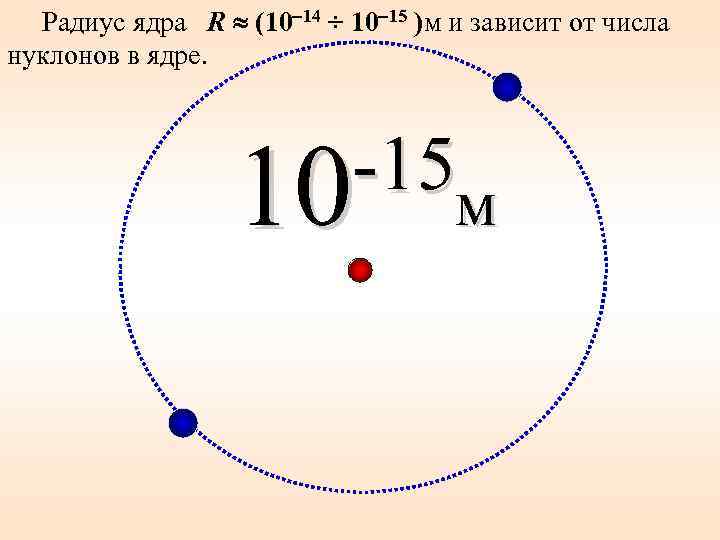 Радиус ядра R (10 14 ÷ 10 15 )м и зависит от числа нуклонов в ядре. -15 м 10
Радиус ядра R (10 14 ÷ 10 15 )м и зависит от числа нуклонов в ядре. -15 м 10
 Планетарная модель атома Однако, планетарная модель была в явном противоречии с классической электродинамикой: электрон, двигаясь по окружности, т. е. с нормальным ускорением, должен был излучать энергию, следовательно, замедлять скорость и упасть на ядро. Т. о. модель Резерфорда не могла объяснить, почему атом устойчив
Планетарная модель атома Однако, планетарная модель была в явном противоречии с классической электродинамикой: электрон, двигаясь по окружности, т. е. с нормальным ускорением, должен был излучать энергию, следовательно, замедлять скорость и упасть на ядро. Т. о. модель Резерфорда не могла объяснить, почему атом устойчив
 Планетарная модель атома противоречит электродинамике Максвелла!!!
Планетарная модель атома противоречит электродинамике Максвелла!!!
 Согласно теории Максвелла, ускоренно движущийся заряд излучает электромагнитные волны.
Согласно теории Максвелла, ускоренно движущийся заряд излучает электромагнитные волны.
 При движении по окружности имеется центростремительное ускорение. Поэтому электрон должен терять энергию на электромагнитное излучение и падать на ядро.
При движении по окружности имеется центростремительное ускорение. Поэтому электрон должен терять энергию на электромагнитное излучение и падать на ядро.
 … излучать и падать. . .
… излучать и падать. . .
 Падать на ядро! Нестабильный атом? !
Падать на ядро! Нестабильный атом? !
 Попыткой спасения планетарной модели атома стали постулаты Н. Бора
Попыткой спасения планетарной модели атома стали постулаты Н. Бора
 х 7. Атом водорода по Бору БОР Нильс Хендрик Давид (1885– 1962) – Выдающийся датский физиктеоретик, один из создателей современной физики. Сформулировал идею о дискретности энергетических состояний атомов, в свете новых идей построил атомную модель, открыв условия устойчивости атомов, и объяснил большой круг явлений. Создал первую квантовую модель атома, основанную на двух постулатах, которые прямо противоречили классическим представлениям и законам. Бор много сделал для развития ядерной физики. Он – автор теории составного ядра, один из создателей капельной модели ядра и теории деления атомного ядра.
х 7. Атом водорода по Бору БОР Нильс Хендрик Давид (1885– 1962) – Выдающийся датский физиктеоретик, один из создателей современной физики. Сформулировал идею о дискретности энергетических состояний атомов, в свете новых идей построил атомную модель, открыв условия устойчивости атомов, и объяснил большой круг явлений. Создал первую квантовую модель атома, основанную на двух постулатах, которые прямо противоречили классическим представлениям и законам. Бор много сделал для развития ядерной физики. Он – автор теории составного ядра, один из создателей капельной модели ядра и теории деления атомного ядра.

 1. Атом следует описывать как «пирамиду» стационарных энергетических состояний. Пребывая в одном из стационарных состояний, атом не излучает энергию.
1. Атом следует описывать как «пирамиду» стационарных энергетических состояний. Пребывая в одном из стационарных состояний, атом не излучает энергию.

 2. При переходах между стационарными состояниями атом поглощает или излучает квант энергии. При поглощении энергии атом переходит в более энергетическое состояние.
2. При переходах между стационарными состояниями атом поглощает или излучает квант энергии. При поглощении энергии атом переходит в более энергетическое состояние.
 Постулаты Бора 1. Электроны движутся только по определенным (стационарным) орбитам. При этом не происходит излучения энергии. Условие для стационарных орбит: из всех орбит электрона возможны только те, для которых момент импульса электрона, равен целому кратному постоянной Планка: me vr = nħ n = 1, 2, 3, … главное квантовое число.
Постулаты Бора 1. Электроны движутся только по определенным (стационарным) орбитам. При этом не происходит излучения энергии. Условие для стационарных орбит: из всех орбит электрона возможны только те, для которых момент импульса электрона, равен целому кратному постоянной Планка: me vr = nħ n = 1, 2, 3, … главное квантовое число.
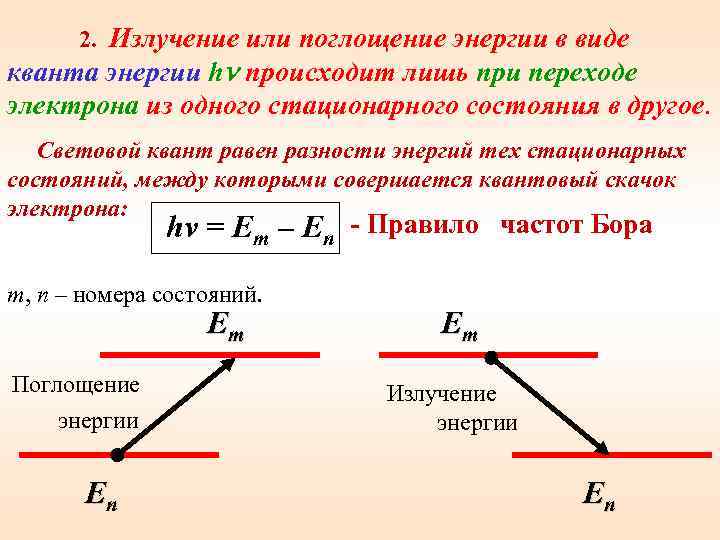 2. Излучение или поглощение энергии в виде кванта энергии h происходит лишь при переходе электрона из одного стационарного состояния в другое. Световой квант равен разности энергий тех стационарных состояний, между которыми совершается квантовый скачок электрона: hv = Em – En - Правило частот Бора m, n – номера состояний. Em Поглощение энергии Еn Em Излучение энергии Еn
2. Излучение или поглощение энергии в виде кванта энергии h происходит лишь при переходе электрона из одного стационарного состояния в другое. Световой квант равен разности энергий тех стационарных состояний, между которыми совершается квантовый скачок электрона: hv = Em – En - Правило частот Бора m, n – номера состояний. Em Поглощение энергии Еn Em Излучение энергии Еn
 х Уравнение движения электрона получим из равенства центробежной силе кулоновской силе: meυr = nħ Отсюда найдем радиус стационарных орбит: =>
х Уравнение движения электрона получим из равенства центробежной силе кулоновской силе: meυr = nħ Отсюда найдем радиус стационарных орбит: =>
 х Радиус первой орбиты водородного атома называют Боровским радиусом: При n =1, Z = 1 для водорода имеем: Å= 0, 529· 10– 10 м.
х Радиус первой орбиты водородного атома называют Боровским радиусом: При n =1, Z = 1 для водорода имеем: Å= 0, 529· 10– 10 м.
 х Внутренняя энергия слагается атома из кинетической энергии электрона и потенциальной энергией взаимодействия электрона с ядром: Отсюда видно, что: энергия электрона может принимать только дискретные значения, т. к. n = 1, 2, 3, …
х Внутренняя энергия слагается атома из кинетической энергии электрона и потенциальной энергией взаимодействия электрона с ядром: Отсюда видно, что: энергия электрона может принимать только дискретные значения, т. к. n = 1, 2, 3, …
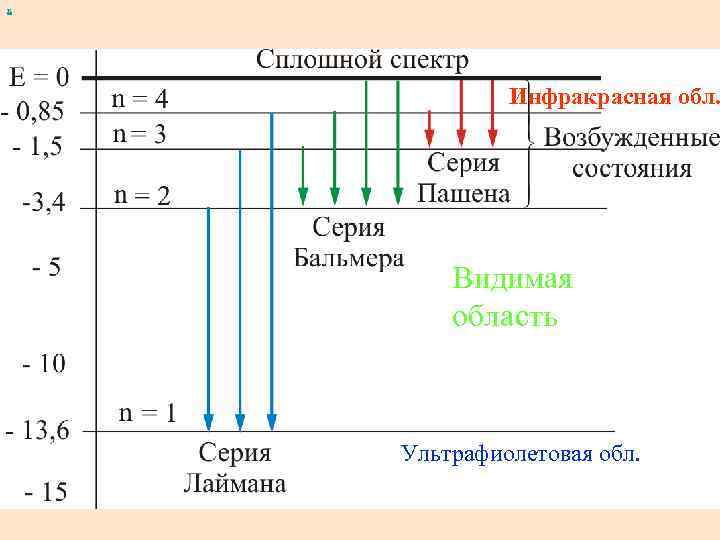 х Инфракрасная обл. Видимая область Ультрафиолетовая обл.
х Инфракрасная обл. Видимая область Ультрафиолетовая обл.
 При переходе электрона в атоме водорода из состояния n в состояние k излучается фотон с энергией : х и частота излучения, Мы получили обобщенную формулу Бальмера, которая хорошо согласуется с экспериментом, где постоянная Ридберга
При переходе электрона в атоме водорода из состояния n в состояние k излучается фотон с энергией : х и частота излучения, Мы получили обобщенную формулу Бальмера, которая хорошо согласуется с экспериментом, где постоянная Ридберга
 Серьезным успехом теории Бора явилось: • вычисление постоянной Ридберга для водородоподобных систем и • объяснение структуры их линейчатых спектров. Бору удалось объяснить линии спектра ионизованного гелия.
Серьезным успехом теории Бора явилось: • вычисление постоянной Ридберга для водородоподобных систем и • объяснение структуры их линейчатых спектров. Бору удалось объяснить линии спектра ионизованного гелия.
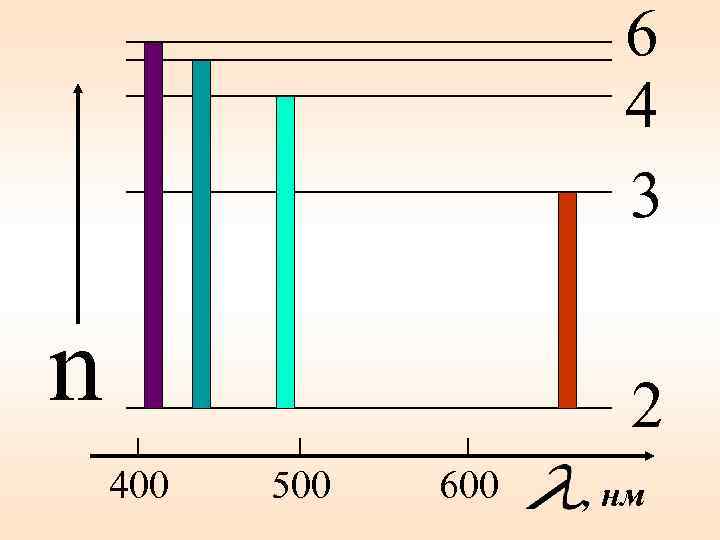 6 4 3 n 2 400 500 600 , нм
6 4 3 n 2 400 500 600 , нм
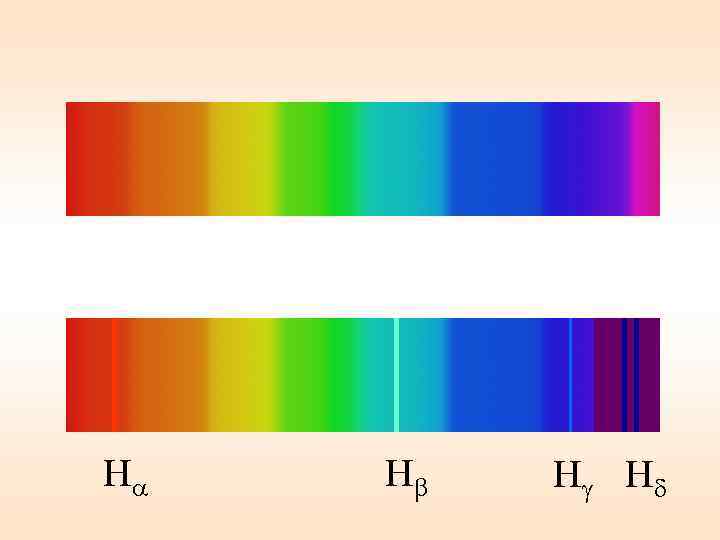 H H H H
H H H H
 х Бор теоретически вычислил отношение массы протона к массе электрона mp/me = 1847, это находится в соответствии с экспериментом. Все это было важным подтверждением основных идей, содержащихся в теории Бора. Теория Бора сыграла огромную роль в создании атомной физики. В период ее развития (1913 – 1925 г. г. ) были сделаны важные открытия, навсегда вошедшие в сокровищницу мировой науки.
х Бор теоретически вычислил отношение массы протона к массе электрона mp/me = 1847, это находится в соответствии с экспериментом. Все это было важным подтверждением основных идей, содержащихся в теории Бора. Теория Бора сыграла огромную роль в создании атомной физики. В период ее развития (1913 – 1925 г. г. ) были сделаны важные открытия, навсегда вошедшие в сокровищницу мировой науки.
 «Портрет» атома радия ( Н. Бор, 1925 )
«Портрет» атома радия ( Н. Бор, 1925 )
 х Однако наряду с успехами в теории Бора с самого начала обнаружились существенные недостатки. • Главнейшее – внутренняя противоречивость теории: механическое соединение классической физики с квантовыми постулатами. • Теория не могла объяснить вопрос об интенсивностях спектральных линий. • Серьезной неудачей являлась абсолютная невозможность применить теорию для объяснения спектров гелия (He) (два электрона на орбите, и уже теория Бора не справляется).
х Однако наряду с успехами в теории Бора с самого начала обнаружились существенные недостатки. • Главнейшее – внутренняя противоречивость теории: механическое соединение классической физики с квантовыми постулатами. • Теория не могла объяснить вопрос об интенсивностях спектральных линий. • Серьезной неудачей являлась абсолютная невозможность применить теорию для объяснения спектров гелия (He) (два электрона на орбите, и уже теория Бора не справляется).
 х Стало ясно, что теория Бора является лишь переходным этапом на пути создания более общей и правильной теории. Такой теорией и являлась квантовая (волновая) механика.
х Стало ясно, что теория Бора является лишь переходным этапом на пути создания более общей и правильной теории. Такой теорией и являлась квантовая (волновая) механика.
 Дальнейшее развитие квантовой механики привело к отказу от механической картины движения электрона в поле ядра.
Дальнейшее развитие квантовой механики привело к отказу от механической картины движения электрона в поле ядра.


