Модуль 3 МГУ.ppt
- Количество слайдов: 138
 Модуль 3 Атомная структура и строение твердых тел • Условия образования конденсированного вещества • Порядок и беспорядок. Энтропия. Свободная энергия Гиббса • Кристаллическая решетка. 14 решеток Браве • Кристаллографические символы • Симметрия, несовершенства структуры и физические свойства кристаллов • Специфика атомного строения наночастиц
Модуль 3 Атомная структура и строение твердых тел • Условия образования конденсированного вещества • Порядок и беспорядок. Энтропия. Свободная энергия Гиббса • Кристаллическая решетка. 14 решеток Браве • Кристаллографические символы • Симметрия, несовершенства структуры и физические свойства кристаллов • Специфика атомного строения наночастиц
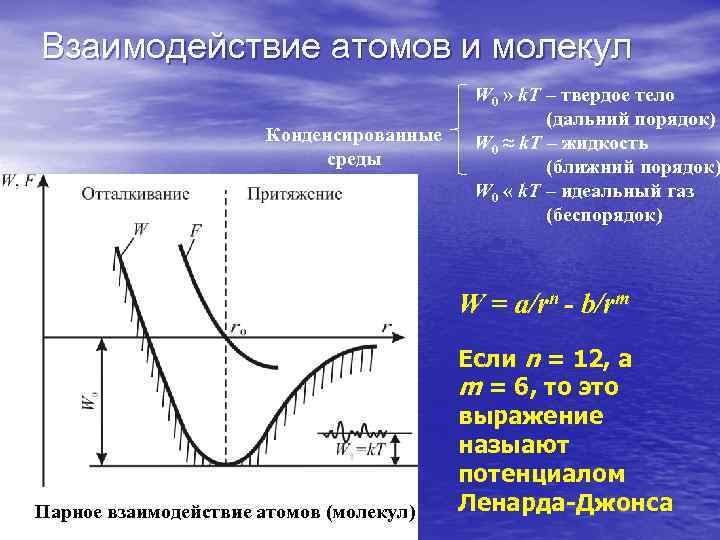 Взаимодействие атомов и молекул Конденсированные среды W 0 » k. T – твердое тело (дальний порядок) W 0 ≈ k. T – жидкость (ближний порядок) W 0 « k. T – идеальный газ (беспорядок) W = a/rn - b/rm Парное взаимодействие атомов (молекул) Если n = 12, а m = 6, то это выражение назыают потенциалом Ленарда-Джонса
Взаимодействие атомов и молекул Конденсированные среды W 0 » k. T – твердое тело (дальний порядок) W 0 ≈ k. T – жидкость (ближний порядок) W 0 « k. T – идеальный газ (беспорядок) W = a/rn - b/rm Парное взаимодействие атомов (молекул) Если n = 12, а m = 6, то это выражение назыают потенциалом Ленарда-Джонса
 Качественно зависимость потенциала взаимодействия двух атомов или молекул (далее частиц) от расстояния r между ними выглядит так, как показано на слайде и может быть описана соотношением: W = a/rn – b/rm, где a, b, n, m – константы для данной пары взаимодействующих частиц. При r
Качественно зависимость потенциала взаимодействия двух атомов или молекул (далее частиц) от расстояния r между ними выглядит так, как показано на слайде и может быть описана соотношением: W = a/rn – b/rm, где a, b, n, m – константы для данной пары взаимодействующих частиц. При r
 Зависимость энергии взаимодействия от межатомного расстояния для некоторых инертных газов Пиментел Г. , Спратли Р. Как квантовая механика объясняет химическую связь. М. : Издательство «Мир» , 1973. 332 с.
Зависимость энергии взаимодействия от межатомного расстояния для некоторых инертных газов Пиментел Г. , Спратли Р. Как квантовая механика объясняет химическую связь. М. : Издательство «Мир» , 1973. 332 с.
 Связь между Ккал/моль и э. В • 1 э. В – это энергия, которую приобретает электрон или однозарядный ион, свободно переместившись между точками с разностью потенциалов 1 В. • 1 э. В = 1. 6 10 19 Кл В = 1. 6 10 19 Дж • 1 ккал = 4. 18 к. Дж • 1 Моль содержит 6. 02 10 23 частиц Отсюда: 1 ккал/моль = (4180/ 6 10 23 )/ 1. 6 10 19 = 0. 0433 э. В 1 э. В = 96. 5 к. Дж/ моль = 23 ккал/моль
Связь между Ккал/моль и э. В • 1 э. В – это энергия, которую приобретает электрон или однозарядный ион, свободно переместившись между точками с разностью потенциалов 1 В. • 1 э. В = 1. 6 10 19 Кл В = 1. 6 10 19 Дж • 1 ккал = 4. 18 к. Дж • 1 Моль содержит 6. 02 10 23 частиц Отсюда: 1 ккал/моль = (4180/ 6 10 23 )/ 1. 6 10 19 = 0. 0433 э. В 1 э. В = 96. 5 к. Дж/ моль = 23 ккал/моль
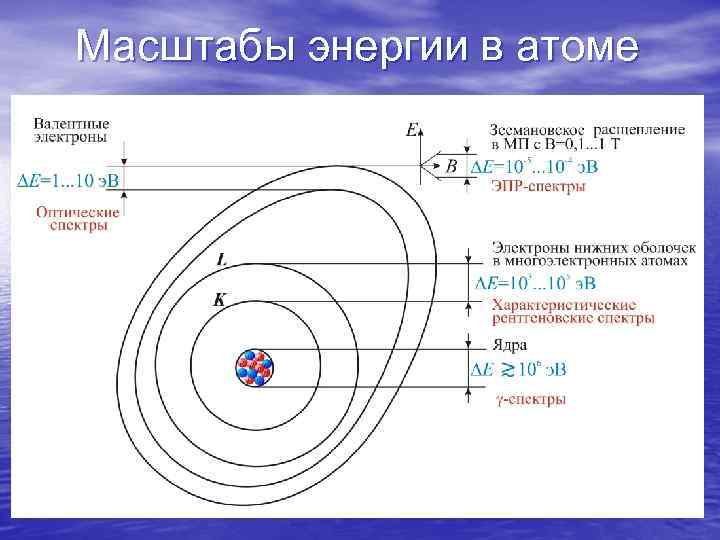 Масштабы энергии в атоме
Масштабы энергии в атоме
 Типичные значения энергии связи в твердых телах в зависимости от типа связи между атомами • Ккал/моль э. В Ван дер ваальсова До ~ 2 До ~ 0, 1 • Водородная 4… 10 0, 2… 0, 5 • Ионная до 185 до 8 • Металлическая до 200 до 8, 5 • Ковалентная до 165 до 6 • Характерная тепловая энергия WT = k. BT при Т = 300 К 0, 6 0, 026 Энергия фотонов видимого света 1. 5 – 3
Типичные значения энергии связи в твердых телах в зависимости от типа связи между атомами • Ккал/моль э. В Ван дер ваальсова До ~ 2 До ~ 0, 1 • Водородная 4… 10 0, 2… 0, 5 • Ионная до 185 до 8 • Металлическая до 200 до 8, 5 • Ковалентная до 165 до 6 • Характерная тепловая энергия WT = k. BT при Т = 300 К 0, 6 0, 026 Энергия фотонов видимого света 1. 5 – 3
 Конденсированные среды Конденсированная среда – это состояние вещества, в котором энергия взаимодействия атомов/молекул сопоставима или превышает среднюю энергию тепловых колебаний. • • • жидкости переохлажденные жидкости (стекла) кристаллические твердые тела жидкие кристаллы квазикристаллы
Конденсированные среды Конденсированная среда – это состояние вещества, в котором энергия взаимодействия атомов/молекул сопоставима или превышает среднюю энергию тепловых колебаний. • • • жидкости переохлажденные жидкости (стекла) кристаллические твердые тела жидкие кристаллы квазикристаллы
 Деление конденсированных сред на твердые и жидкие (по агрегатному состоянию) характеризует лишь свойство сохранять свою форму или принимать форму вмещающего их сосуда (или капель). С точки зрения физики гораздо важнее их внутренняя структура, порядок расположения атомов (молекул), характер их взаимодействия. В классических жидкостях наблюдается ближний порядок в нескольких координационных сферах от избранной частицы. Если жидкость быстро переохладить, то возникнет аморфное твердое тело (синоним – стекло, не обязательно прозрачное, как, например, в случае с металлами и сплавами). Вещества, состоящие из атомов одного сорта или простых молекул (H 2 O, CO 2, Al 2 O 3, Si. O 2, N 2, Li. F, Ga. As и т. п. ) при медленном охлаждении образуют кристаллы – хорошо упорядоченные среды с дальним порядком (т. е. повторением основного мотива структуры на протяжении многих тысяч периодов). Ряд органических веществ образует жидкие кристаллы – среды, характеризующиеся упорядоченностью молекул подобно обычным кристаллам, но не сохраняющими внешней формы, а текучими как вязкие жидкости. Квазикристаллы – твердые тела, состоящие из атомов, не образующих кристаллической решетки с трансляционной симметрией, но, тем не менее, обладающие дальним координационным порядком и способностью когерентно рассеивать падающее излучение.
Деление конденсированных сред на твердые и жидкие (по агрегатному состоянию) характеризует лишь свойство сохранять свою форму или принимать форму вмещающего их сосуда (или капель). С точки зрения физики гораздо важнее их внутренняя структура, порядок расположения атомов (молекул), характер их взаимодействия. В классических жидкостях наблюдается ближний порядок в нескольких координационных сферах от избранной частицы. Если жидкость быстро переохладить, то возникнет аморфное твердое тело (синоним – стекло, не обязательно прозрачное, как, например, в случае с металлами и сплавами). Вещества, состоящие из атомов одного сорта или простых молекул (H 2 O, CO 2, Al 2 O 3, Si. O 2, N 2, Li. F, Ga. As и т. п. ) при медленном охлаждении образуют кристаллы – хорошо упорядоченные среды с дальним порядком (т. е. повторением основного мотива структуры на протяжении многих тысяч периодов). Ряд органических веществ образует жидкие кристаллы – среды, характеризующиеся упорядоченностью молекул подобно обычным кристаллам, но не сохраняющими внешней формы, а текучими как вязкие жидкости. Квазикристаллы – твердые тела, состоящие из атомов, не образующих кристаллической решетки с трансляционной симметрией, но, тем не менее, обладающие дальним координационным порядком и способностью когерентно рассеивать падающее излучение.
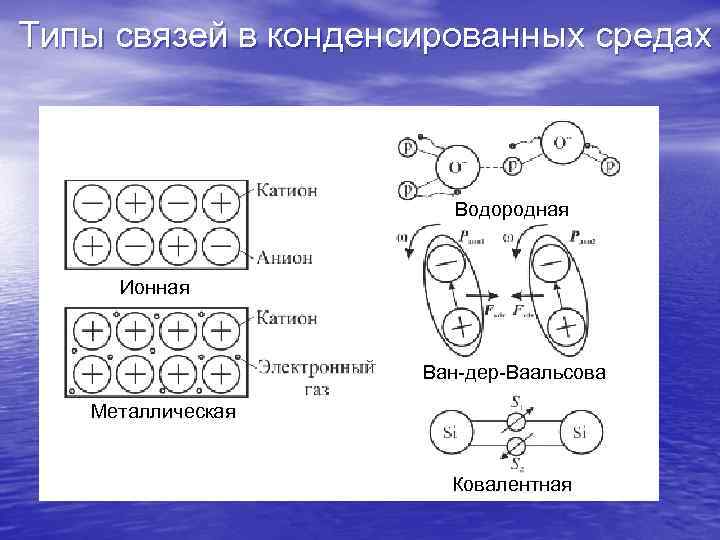 Типы связей в конденсированных средах Водородная Ионная Ван-дер-Ваальсова Металлическая Ковалентная
Типы связей в конденсированных средах Водородная Ионная Ван-дер-Ваальсова Металлическая Ковалентная
 По характеру (природе) межатомных сил принято выделять несколько типов связи в конденсированных средах: ионная, металлическая, ковалентная, Ван-дер-Ваальсова (молекулярная), водородная. В чистом виде они встречаются редко. В реальном веществе связи имеют, как правило, смешанный характер с преобладанием того или иного типа. Различают направленные (ковалентная) и ненаправленные связи (металлическая), физические и химические связи (под последними обычно подразумевают ковалентные). Несмотря на различия, с фундаментальной точки зрения все типы связей определяются строением валентных оболочек взаимодействующих атомов (по большей части силами их кулоновского взаимодействия и квантовомеханическими законами). В твердых телах мерой связи атомных частиц служит теплота возгонки, а в жидкости – теплота испарения.
По характеру (природе) межатомных сил принято выделять несколько типов связи в конденсированных средах: ионная, металлическая, ковалентная, Ван-дер-Ваальсова (молекулярная), водородная. В чистом виде они встречаются редко. В реальном веществе связи имеют, как правило, смешанный характер с преобладанием того или иного типа. Различают направленные (ковалентная) и ненаправленные связи (металлическая), физические и химические связи (под последними обычно подразумевают ковалентные). Несмотря на различия, с фундаментальной точки зрения все типы связей определяются строением валентных оболочек взаимодействующих атомов (по большей части силами их кулоновского взаимодействия и квантовомеханическими законами). В твердых телах мерой связи атомных частиц служит теплота возгонки, а в жидкости – теплота испарения.
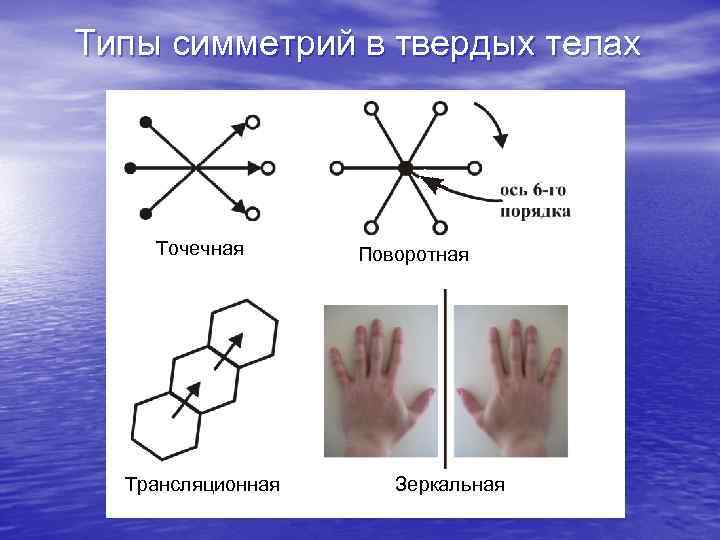 Типы симметрий в твердых телах Точечная Трансляционная Поворотная Зеркальная
Типы симметрий в твердых телах Точечная Трансляционная Поворотная Зеркальная
 В общем случае симметрией в физике называют свойство системы (или описывающих её уравнений) сохранять (не менять) своего состояния (гамильтониана) в результате какоголибо преобразования. Тогда считается, что она обладает симметрией относительно данного преобразования. Из соображений симметрии можно вывести многие свойства вещества и законы физики. Так, из пространственно-временной симметрии вакуума вытекают фундаментальные законы сохранения энергии, импульса, момента импульса. В описании строения и свойств молекул, конденсированных сред, кристаллов симметрийные подходы имеют очень важное значение. Различают точечные, поворотные, трансляционные и зеркальные группы симметрии, примеры которых показаны на слайде. Наличие пространственной симметрии в системе проявляется в анизотропии свойств, внешней огранке (габитусе) кристаллов, энергетическом спектре электронов, дифракции электронов, нейтронов и рентгеновских лучей.
В общем случае симметрией в физике называют свойство системы (или описывающих её уравнений) сохранять (не менять) своего состояния (гамильтониана) в результате какоголибо преобразования. Тогда считается, что она обладает симметрией относительно данного преобразования. Из соображений симметрии можно вывести многие свойства вещества и законы физики. Так, из пространственно-временной симметрии вакуума вытекают фундаментальные законы сохранения энергии, импульса, момента импульса. В описании строения и свойств молекул, конденсированных сред, кристаллов симметрийные подходы имеют очень важное значение. Различают точечные, поворотные, трансляционные и зеркальные группы симметрии, примеры которых показаны на слайде. Наличие пространственной симметрии в системе проявляется в анизотропии свойств, внешней огранке (габитусе) кристаллов, энергетическом спектре электронов, дифракции электронов, нейтронов и рентгеновских лучей.
 Энтропия и свободная энергия при кристаллизации G = SW 0–TS – свободная энергия Гиббса S = Q/T; S = klnw – энтропия – мера беспорядка в системе При P = const, T = const DG = SW 0–TDS
Энтропия и свободная энергия при кристаллизации G = SW 0–TS – свободная энергия Гиббса S = Q/T; S = klnw – энтропия – мера беспорядка в системе При P = const, T = const DG = SW 0–TDS
 В описании процессов образования твердого тела большую роль играют термодинамические подходы и такие понятия (величины), как свободная энергия G, локальный и глобальный минимумы свободной энергии (Gl и Gg соответственно). Переход газообразного состояния в жидкое или из жидкого (газообразного) в твердое возможен только при температуре ниже точки равновесия между этими фазами, когда возникает определенный термодинамический выигрыш G для такого перехода. Причем, он не может быть бесконечно малым, поскольку для фазового превращения необходимо преодолеть некоторый энергетический барьер (природа которого зависит от типа превращения, свойств фаз, их состава, строения и др. ). В общих чертах этот подход сохраняется и для полиморфных превращений (фазовых превращений в твердом теле).
В описании процессов образования твердого тела большую роль играют термодинамические подходы и такие понятия (величины), как свободная энергия G, локальный и глобальный минимумы свободной энергии (Gl и Gg соответственно). Переход газообразного состояния в жидкое или из жидкого (газообразного) в твердое возможен только при температуре ниже точки равновесия между этими фазами, когда возникает определенный термодинамический выигрыш G для такого перехода. Причем, он не может быть бесконечно малым, поскольку для фазового превращения необходимо преодолеть некоторый энергетический барьер (природа которого зависит от типа превращения, свойств фаз, их состава, строения и др. ). В общих чертах этот подход сохраняется и для полиморфных превращений (фазовых превращений в твердом теле).
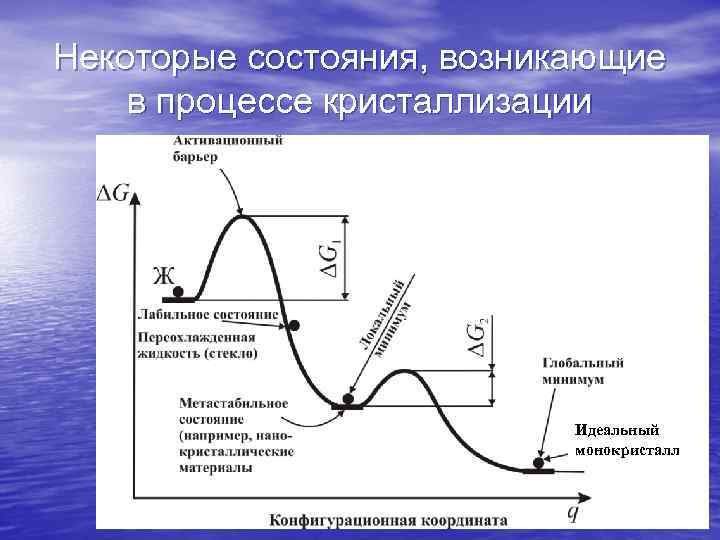 Некоторые состояния, возникающие в процессе кристаллизации Идеальный монокристалл
Некоторые состояния, возникающие в процессе кристаллизации Идеальный монокристалл
 В процессе перехода из жидкого в кристаллическое состояние могут возникнуть некоторые промежуточные состояния. Если они характеризуются локальными минимумами свободной энергии, то называются метастабильными, а если «застревают» на склоне потенциального профиля благодаря кинетическому затормаживанию релаксационных процессов ( «замораживанию» структуры, препятствующему термодинамически выгодным превращениям) – называют лабильными. Примерами первых являются реальные кристаллы, содержащие собственные структурные дефекты (см. ниже), а примерами вторых – аморфные сплавы (металлические стекла).
В процессе перехода из жидкого в кристаллическое состояние могут возникнуть некоторые промежуточные состояния. Если они характеризуются локальными минимумами свободной энергии, то называются метастабильными, а если «застревают» на склоне потенциального профиля благодаря кинетическому затормаживанию релаксационных процессов ( «замораживанию» структуры, препятствующему термодинамически выгодным превращениям) – называют лабильными. Примерами первых являются реальные кристаллы, содержащие собственные структурные дефекты (см. ниже), а примерами вторых – аморфные сплавы (металлические стекла).
 Гомогенное и гетерогенное зарождение новой фазы В процессах кристаллизации из жидкой и газообразной фазы, эпитаксиального роста, полиморфных и других фазовых превращениях в твердых телах большую роль играет образование зародышей новой фазы и их последующий рост. Различают гомогенное и гетерогенное зарождение. Гетерогенным называют процесс с участием уже существующих неоднородностей в материнской фазе или на контактирующих с ней поверхностях. Это могут быть пылинки, пузырьки газа в жидкости, электрически заряженные объекты, микрошероховатости стенок сосуда, наночастички катализатора и т. п. В отсутствие этих возмущений зародышеобразование называют гомогенным. Оно требует, как правило, гораздо больших переохлаждений системы (иногда достигающих многих десятков градусов). Микроскопические атомные механизмы гомогенного образования кристаллических зародышей в переохлажденной жидкости или паре до сих пор в деталях не известны, а термодинамические причины рассмотрены ниже.
Гомогенное и гетерогенное зарождение новой фазы В процессах кристаллизации из жидкой и газообразной фазы, эпитаксиального роста, полиморфных и других фазовых превращениях в твердых телах большую роль играет образование зародышей новой фазы и их последующий рост. Различают гомогенное и гетерогенное зарождение. Гетерогенным называют процесс с участием уже существующих неоднородностей в материнской фазе или на контактирующих с ней поверхностях. Это могут быть пылинки, пузырьки газа в жидкости, электрически заряженные объекты, микрошероховатости стенок сосуда, наночастички катализатора и т. п. В отсутствие этих возмущений зародышеобразование называют гомогенным. Оно требует, как правило, гораздо больших переохлаждений системы (иногда достигающих многих десятков градусов). Микроскопические атомные механизмы гомогенного образования кристаллических зародышей в переохлажденной жидкости или паре до сих пор в деталях не известны, а термодинамические причины рассмотрены ниже.
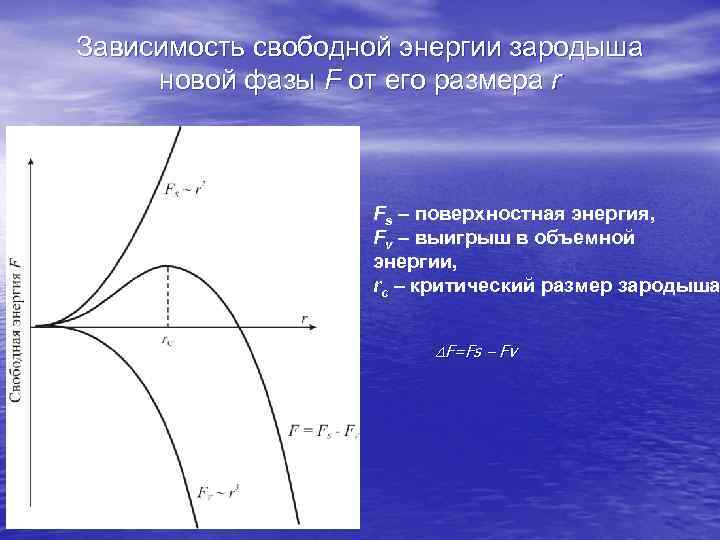 Зависимость свободной энергии зародыша новой фазы F от его размера r Fs – поверхностная энергия, Fv – выигрыш в объемной энергии, rc – критический размер зародыша F=Fs – Fv
Зависимость свободной энергии зародыша новой фазы F от его размера r Fs – поверхностная энергия, Fv – выигрыш в объемной энергии, rc – критический размер зародыша F=Fs – Fv
 В простейшей модели гомогенного зародышеобразования учитывается два обстоятельства: образование новой фазы приводит к созданию новой поверхности S с избыточной энергией Fs = S~ r 2 (здесь - удельная поверхностная энергия); переход атомов/молекул через межфазную границу сопровождается изменением их химического потенциала и понижением свободной энергии в системе Fv ~ N ~ r 3 (здесь N – число атомов/молекул в зародыше). Изменение свободной энергии F=Fs – Fv при росте r сначала растет, а после достижения критического размера зародыша rc начинает падать. Это означает, что при r< rc образующиеся зародыши неустойчивы, т. к. термодинамически невыгодны. Их стабильный рост может происходить лишь при r> rc. Такая элементарная модель призвана лишь пояснить принципы рассмотрения гомогенного зародышеобразования. Учет анизотропии, различия поверхностной энергии на разных кристаллографических гранях, внутренних перестроек при росте зародыша, его несферичности, внутренних напряжений (если он растет в твердой матрице) и др. способен уточнить величину rc, параметры кинетики роста и др. , но не отменяет общих термодинамических подходов.
В простейшей модели гомогенного зародышеобразования учитывается два обстоятельства: образование новой фазы приводит к созданию новой поверхности S с избыточной энергией Fs = S~ r 2 (здесь - удельная поверхностная энергия); переход атомов/молекул через межфазную границу сопровождается изменением их химического потенциала и понижением свободной энергии в системе Fv ~ N ~ r 3 (здесь N – число атомов/молекул в зародыше). Изменение свободной энергии F=Fs – Fv при росте r сначала растет, а после достижения критического размера зародыша rc начинает падать. Это означает, что при r< rc образующиеся зародыши неустойчивы, т. к. термодинамически невыгодны. Их стабильный рост может происходить лишь при r> rc. Такая элементарная модель призвана лишь пояснить принципы рассмотрения гомогенного зародышеобразования. Учет анизотропии, различия поверхностной энергии на разных кристаллографических гранях, внутренних перестроек при росте зародыша, его несферичности, внутренних напряжений (если он растет в твердой матрице) и др. способен уточнить величину rc, параметры кинетики роста и др. , но не отменяет общих термодинамических подходов.
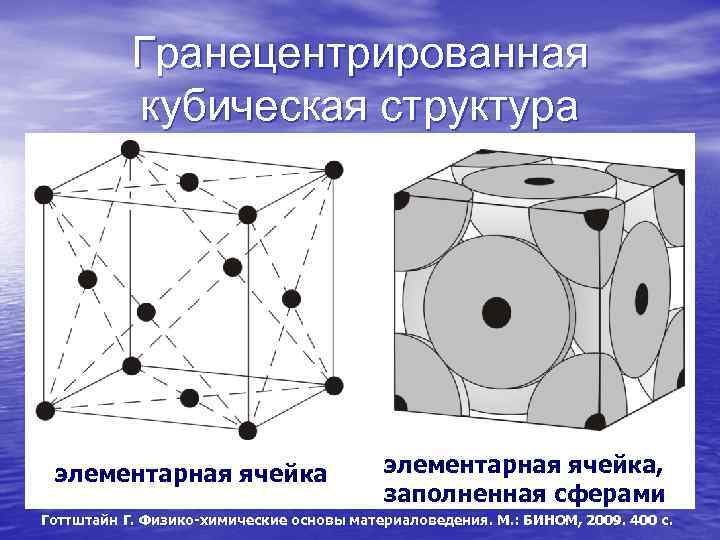 Гранецентрированная кубическая структура элементарная ячейка, заполненная сферами Готтштайн Г. Физико-химические основы материаловедения. М. : БИНОМ, 2009. 400 с.
Гранецентрированная кубическая структура элементарная ячейка, заполненная сферами Готтштайн Г. Физико-химические основы материаловедения. М. : БИНОМ, 2009. 400 с.
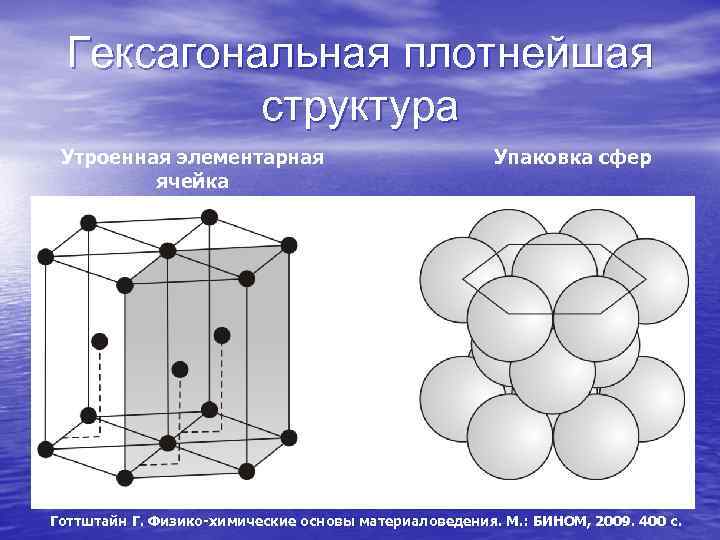 Гексагональная плотнейшая структура Утроенная элементарная ячейка Упаковка сфер Готтштайн Г. Физико-химические основы материаловедения. М. : БИНОМ, 2009. 400 с.
Гексагональная плотнейшая структура Утроенная элементарная ячейка Упаковка сфер Готтштайн Г. Физико-химические основы материаловедения. М. : БИНОМ, 2009. 400 с.
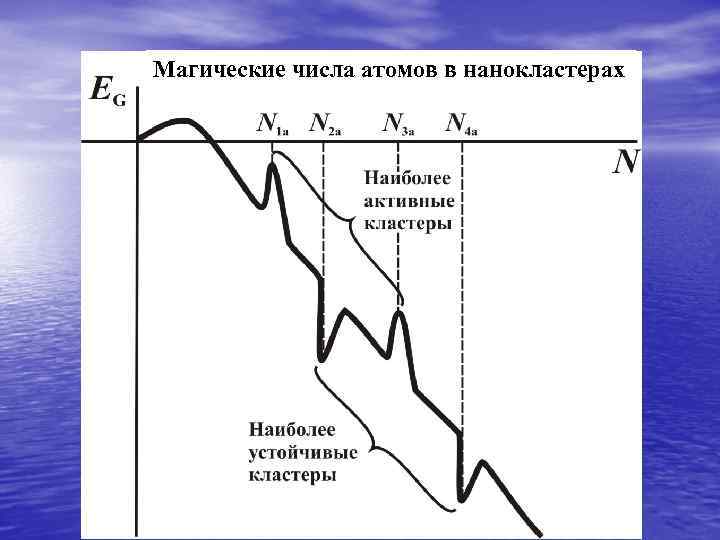 Магические числа атомов в нанокластерах
Магические числа атомов в нанокластерах
 В процессе роста зародыша новой фазы могут происходить перестройки его внутренней структуры (например, от икосаэдрической на начальной стадии, к гранецентрованной кубической (ГЦК) на более поздних), изменение внешней огранки, достраивание внешних граней до заполнения, конденсация первых атомов нового слоя на грани и т. п. Все эти события приводят к немонотонному падению свободной энергии кластера, чему отвечают более или менее устойчивые конфигурации атомов. В первом случае вероятность встретить такие кластеры в ансамбле повышается, а во втором понижается.
В процессе роста зародыша новой фазы могут происходить перестройки его внутренней структуры (например, от икосаэдрической на начальной стадии, к гранецентрованной кубической (ГЦК) на более поздних), изменение внешней огранки, достраивание внешних граней до заполнения, конденсация первых атомов нового слоя на грани и т. п. Все эти события приводят к немонотонному падению свободной энергии кластера, чему отвечают более или менее устойчивые конфигурации атомов. В первом случае вероятность встретить такие кластеры в ансамбле повышается, а во втором понижается.
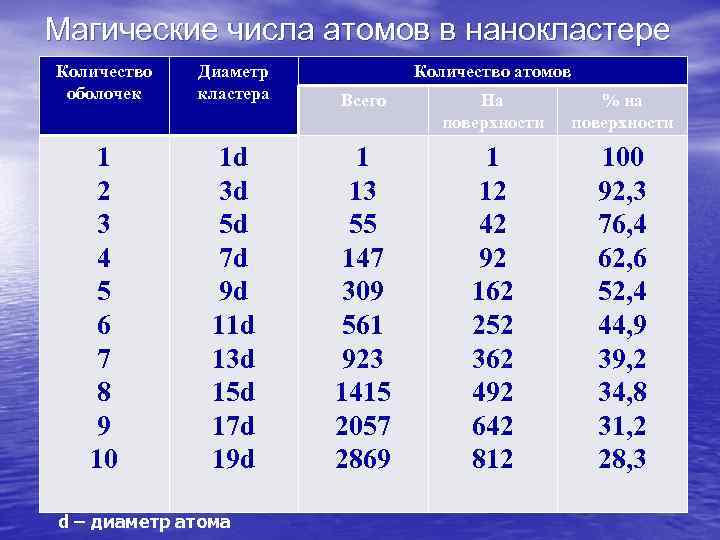 Магические числа атомов в нанокластере Количество оболочек Диаметр кластера Всего На поверхности % на поверхности 1 2 3 4 5 6 7 8 9 10 1 d 3 d 5 d 7 d 9 d 11 d 13 d 15 d 17 d 19 d 1 13 55 147 309 561 923 1415 2057 2869 1 12 42 92 162 252 362 492 642 812 100 92, 3 76, 4 62, 6 52, 4 44, 9 39, 2 34, 8 31, 2 28, 3 d – диаметр атома Количество атомов
Магические числа атомов в нанокластере Количество оболочек Диаметр кластера Всего На поверхности % на поверхности 1 2 3 4 5 6 7 8 9 10 1 d 3 d 5 d 7 d 9 d 11 d 13 d 15 d 17 d 19 d 1 13 55 147 309 561 923 1415 2057 2869 1 12 42 92 162 252 362 492 642 812 100 92, 3 76, 4 62, 6 52, 4 44, 9 39, 2 34, 8 31, 2 28, 3 d – диаметр атома Количество атомов
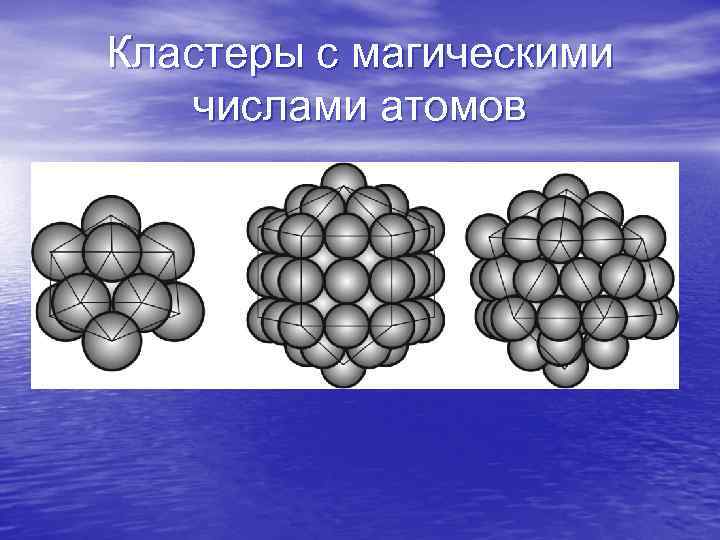 Кластеры с магическими числами атомов
Кластеры с магическими числами атомов
 Числа атомов в кластерах с локальным минимумом энергии называется «магическими» . Как правило, они соответствуют кластерам с полностью достроенными гранями. Так, в ГЦК- нанокластерах образуется ряд магических чисел, приведенных в таблице. Здесь имеется косвенная аналогия с заполнением электронных оболочек в атоме: атомы с заполненными оболочками более устойчивы, чем с незаполненными.
Числа атомов в кластерах с локальным минимумом энергии называется «магическими» . Как правило, они соответствуют кластерам с полностью достроенными гранями. Так, в ГЦК- нанокластерах образуется ряд магических чисел, приведенных в таблице. Здесь имеется косвенная аналогия с заполнением электронных оболочек в атоме: атомы с заполненными оболочками более устойчивы, чем с незаполненными.
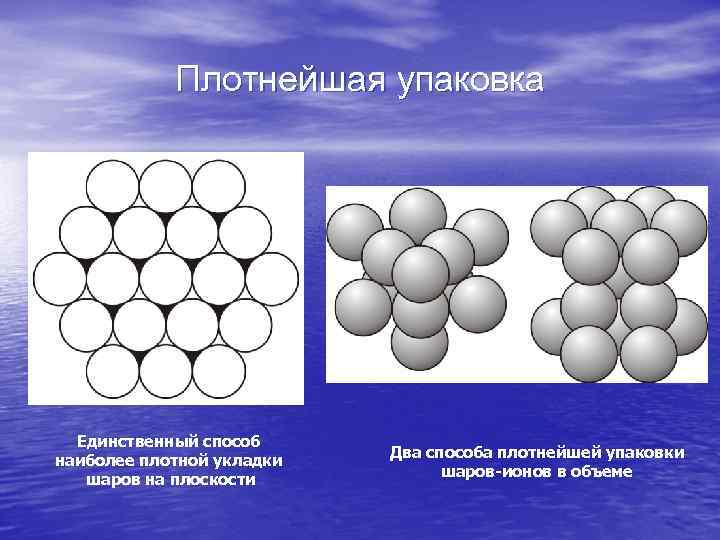 Плотнейшая упаковка Единственный способ наиболее плотной укладки шаров на плоскости Два способа плотнейшей упаковки шаров-ионов в объеме
Плотнейшая упаковка Единственный способ наиболее плотной укладки шаров на плоскости Два способа плотнейшей упаковки шаров-ионов в объеме
 Сферические частицы с радиально-симметричным потенциалом взаимодействия (например, атомы или ионы металлов, инертных газов) могут образовать плотноупакованные структуры. Это обеспечивает минимум занимаемого объема и поверхностной энергии. На плоскости существует единственный способ такой упаковки. В трехмерном случае – их два. Они соответствуют гранецентрированной кубической (ГЦК) и гексагональной плотноупакованной (ГПУ) кристаллическим решеткам, которые часто реализуются в реальных кристаллах.
Сферические частицы с радиально-симметричным потенциалом взаимодействия (например, атомы или ионы металлов, инертных газов) могут образовать плотноупакованные структуры. Это обеспечивает минимум занимаемого объема и поверхностной энергии. На плоскости существует единственный способ такой упаковки. В трехмерном случае – их два. Они соответствуют гранецентрированной кубической (ГЦК) и гексагональной плотноупакованной (ГПУ) кристаллическим решеткам, которые часто реализуются в реальных кристаллах.
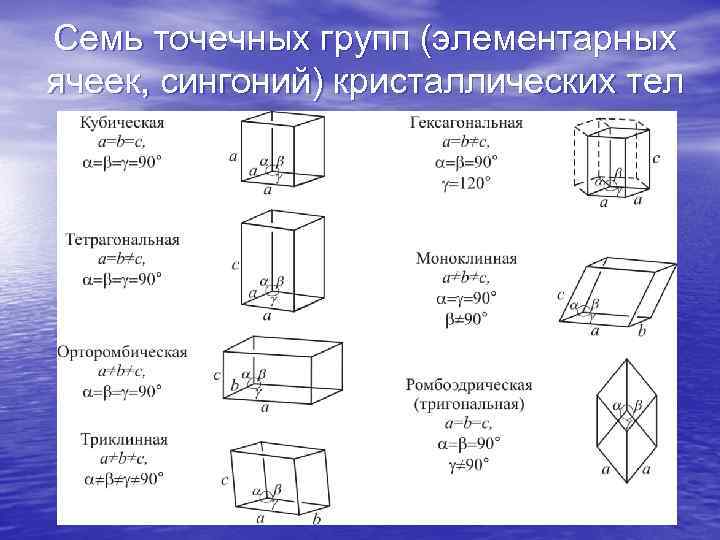 Семь точечных групп (элементарных ячеек, сингоний) кристаллических тел
Семь точечных групп (элементарных ячеек, сингоний) кристаллических тел
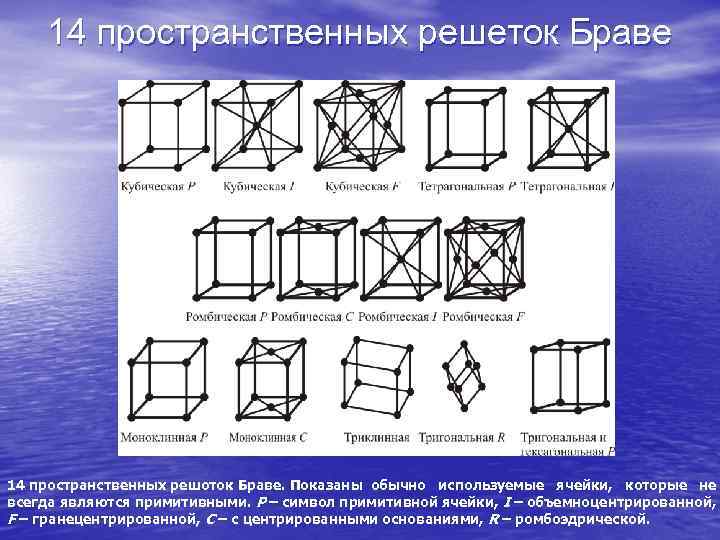 14 пространственных решеток Браве 14 пространственных решоток Браве. Показаны обычно используемые ячейки, которые не всегда являются примитивными. P – символ примитивной ячейки, I – объемноцентрированной, F – гранецентрированной, C – с центрированными основаниями, R – ромбоэдрической.
14 пространственных решеток Браве 14 пространственных решоток Браве. Показаны обычно используемые ячейки, которые не всегда являются примитивными. P – символ примитивной ячейки, I – объемноцентрированной, F – гранецентрированной, C – с центрированными основаниями, R – ромбоэдрической.
 В связи с тем, что не все атомы обладают сферическим потенциалом и создают ненаправленные связи (например, атомы кремния в нормальных условиях имеют четыре направленных ковалентных связи, которые образуют в пространстве тетраэдр) в природе возникают и другие кристаллические структуры. Из соображений симметрии можно вывести 14 пространственных решеток (это сделал в середине 19 века французский физик Огюст Браве).
В связи с тем, что не все атомы обладают сферическим потенциалом и создают ненаправленные связи (например, атомы кремния в нормальных условиях имеют четыре направленных ковалентных связи, которые образуют в пространстве тетраэдр) в природе возникают и другие кристаллические структуры. Из соображений симметрии можно вывести 14 пространственных решеток (это сделал в середине 19 века французский физик Огюст Браве).
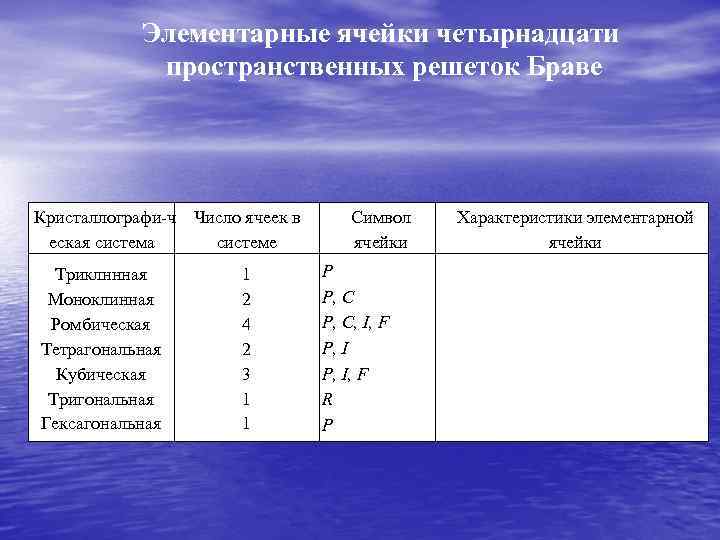 Элементарные ячейки четырнадцати пространственных решеток Браве Кристаллографи ч Число ячеек в еская система системе Триклннная Моноклинная Ромбическая Тетрагональная Кубическая Тригональная Гексагональная 1 2 4 2 3 1 1 Символ ячейки Р Р, С, I, F Р, I, F R Р Характеристики элементарной ячейки a≠b≠c; ≠b≠ a≠b≠c; = =90 ≠b a≠b≠c; =b= =90 a=b=c; =b= <120 , ≠ 90 a=b≠c; =b=90 , =120
Элементарные ячейки четырнадцати пространственных решеток Браве Кристаллографи ч Число ячеек в еская система системе Триклннная Моноклинная Ромбическая Тетрагональная Кубическая Тригональная Гексагональная 1 2 4 2 3 1 1 Символ ячейки Р Р, С, I, F Р, I, F R Р Характеристики элементарной ячейки a≠b≠c; ≠b≠ a≠b≠c; = =90 ≠b a≠b≠c; =b= =90 a=b=c; =b= <120 , ≠ 90 a=b≠c; =b=90 , =120
 Не все решетки Браве являются элементарными, т. е. состоящими из минимально необходимого для однозначного описания структуры числа атомов. Элементарных ячеек всего семь видов. Их характеристики приведены в таблице.
Не все решетки Браве являются элементарными, т. е. состоящими из минимально необходимого для однозначного описания структуры числа атомов. Элементарных ячеек всего семь видов. Их характеристики приведены в таблице.
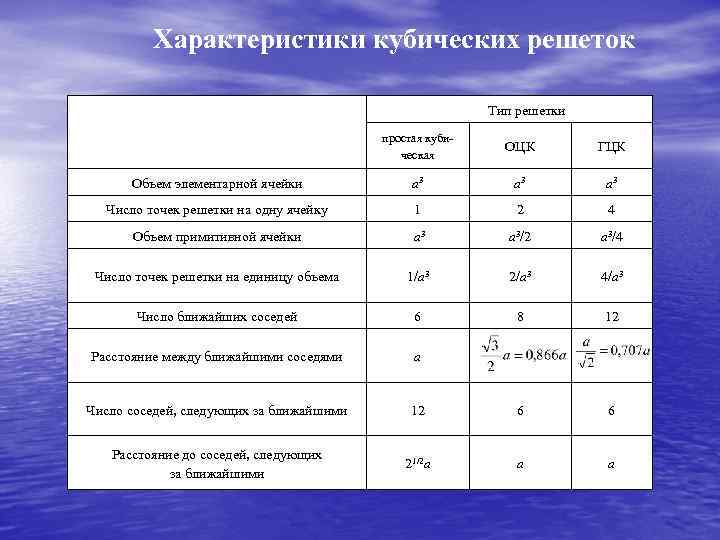 Характеристики кубических решеток Тип решетки простая куби ческая OЦК ГЦК Объем элементарной ячейки а 3 а 3 Число точек решетки на одну ячейку 1 2 4 Объем примитивной ячейки а 3/2 а 3/4 Число точек решетки на единицу объема 1/а 3 2/а 3 4/а 3 Число ближайших соседей 6 8 12 Расстояние между ближайшими соседями а Число соседей, следующих за ближайшими 12 6 6 Расстояние до соседей, следующих за ближайшими 21/2 a а а
Характеристики кубических решеток Тип решетки простая куби ческая OЦК ГЦК Объем элементарной ячейки а 3 а 3 Число точек решетки на одну ячейку 1 2 4 Объем примитивной ячейки а 3/2 а 3/4 Число точек решетки на единицу объема 1/а 3 2/а 3 4/а 3 Число ближайших соседей 6 8 12 Расстояние между ближайшими соседями а Число соседей, следующих за ближайшими 12 6 6 Расстояние до соседей, следующих за ближайшими 21/2 a а а
 В таблице приведены характеристики часто встречающихся кубических решеток. Органические, искусственные полимерные молекулы в определенных условиях также склонны образовывать упорядоченные структуры. Например, глобулярные белки образуют при замораживании ГЦК или ГПУ кристаллы, стержнеобразные и дискообразные молекулы – нематические, смектические и холестерические жидкие кристаллы, отдельные звенья искусственных полимеров – упорядоченные кристаллические ламели, сферолиты и др.
В таблице приведены характеристики часто встречающихся кубических решеток. Органические, искусственные полимерные молекулы в определенных условиях также склонны образовывать упорядоченные структуры. Например, глобулярные белки образуют при замораживании ГЦК или ГПУ кристаллы, стержнеобразные и дискообразные молекулы – нематические, смектические и холестерические жидкие кристаллы, отдельные звенья искусственных полимеров – упорядоченные кристаллические ламели, сферолиты и др.
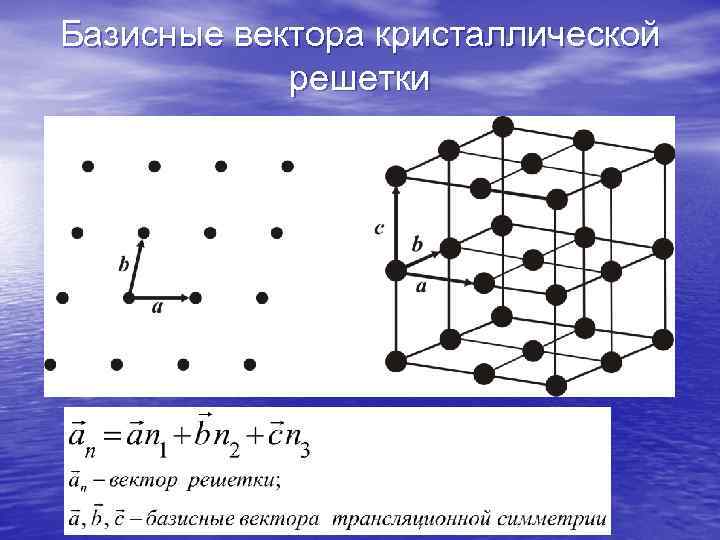 Базисные вектора кристаллической решетки
Базисные вектора кристаллической решетки
 Для описания периодических кристаллических структур имеется математический аппарат, оперирующий понятиями базисных векторов, направлений, плоскостей прямой и обратной кристаллической решетки. Все узлы идеальной решетки могут быть найдены путем трансляции базисных векторов в трех (не обязательно взаимно перпендикулярных направлениях).
Для описания периодических кристаллических структур имеется математический аппарат, оперирующий понятиями базисных векторов, направлений, плоскостей прямой и обратной кристаллической решетки. Все узлы идеальной решетки могут быть найдены путем трансляции базисных векторов в трех (не обязательно взаимно перпендикулярных направлениях).
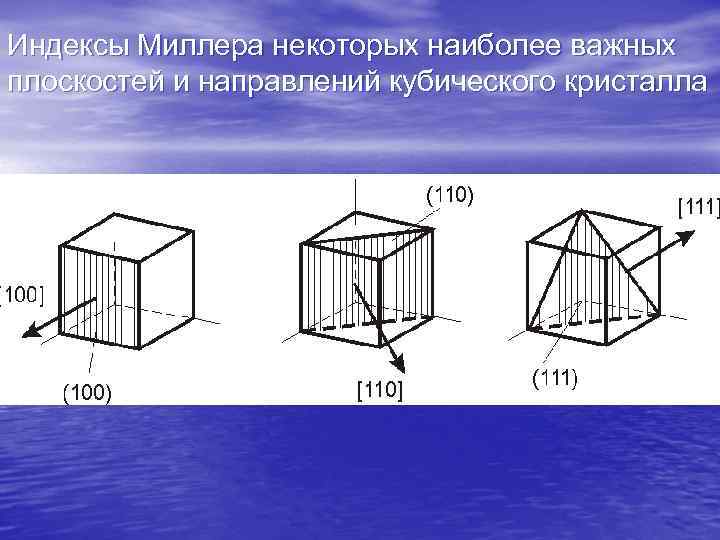 Индексы Миллера некоторых наиболее важных плоскостей и направлений кубического кристалла
Индексы Миллера некоторых наиболее важных плоскостей и направлений кубического кристалла
 Для задания направлений (в квадратных скобках) и плоскостей (в круглых скобках) в кристаллических решетках широко используются индексы Миллера. Для плоскостей в кубической структуре цифры означают отрезки, отсекаемые созданной плоскостью на декартовых осях и выраженные в наименьших из возможных целых числах. Перпендикулярный этой плоскости вектор задает направление с теми же индексами Миллера. Плоскости (100), (200), (300) и т. д. физически эквивалентны (как и 111) и (222), (333) и т. д. Плоскости с малыми индексами Миллера содержат наибольшее число атомов.
Для задания направлений (в квадратных скобках) и плоскостей (в круглых скобках) в кристаллических решетках широко используются индексы Миллера. Для плоскостей в кубической структуре цифры означают отрезки, отсекаемые созданной плоскостью на декартовых осях и выраженные в наименьших из возможных целых числах. Перпендикулярный этой плоскости вектор задает направление с теми же индексами Миллера. Плоскости (100), (200), (300) и т. д. физически эквивалентны (как и 111) и (222), (333) и т. д. Плоскости с малыми индексами Миллера содержат наибольшее число атомов.
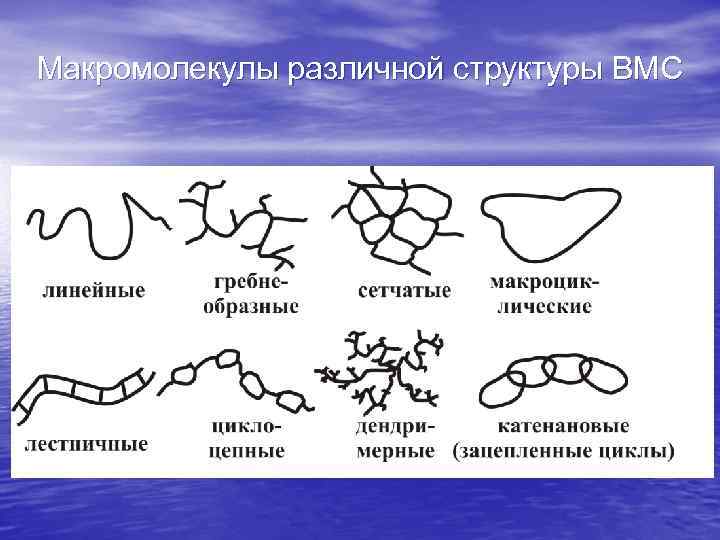 Макромолекулы различной структуры ВМС
Макромолекулы различной структуры ВМС
 Полимеры (естественные и искусственные) имеют более сложную структуру, чем простые низкомолекулярные вещества. Различают первичную молекулярную структуру (топологию самих молекул, включающую архитектуру хребтовой цепи, боковых групп и ответвлений), и надмолекулярные структуры второго, третьего и четвертого уровней иерархической организации. Возможные варианты первичной структуры показаны на слайде.
Полимеры (естественные и искусственные) имеют более сложную структуру, чем простые низкомолекулярные вещества. Различают первичную молекулярную структуру (топологию самих молекул, включающую архитектуру хребтовой цепи, боковых групп и ответвлений), и надмолекулярные структуры второго, третьего и четвертого уровней иерархической организации. Возможные варианты первичной структуры показаны на слайде.
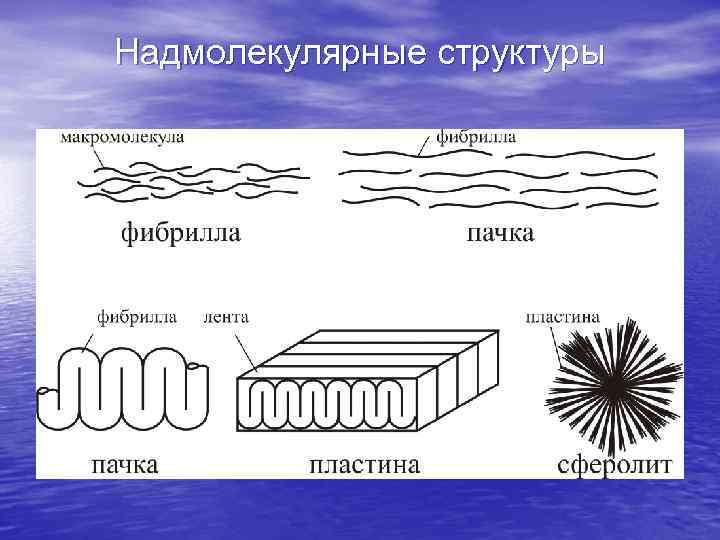 Надмолекулярные структуры
Надмолекулярные структуры
 На схеме показаны некоторые типы упорядочения надмолекулярных структур в полимерах. Фибриллы, пачки, ленты, пластины, сферолиты представляют собой различные этажи иерархии надмолекулярных структур линейных полимеров.
На схеме показаны некоторые типы упорядочения надмолекулярных структур в полимерах. Фибриллы, пачки, ленты, пластины, сферолиты представляют собой различные этажи иерархии надмолекулярных структур линейных полимеров.
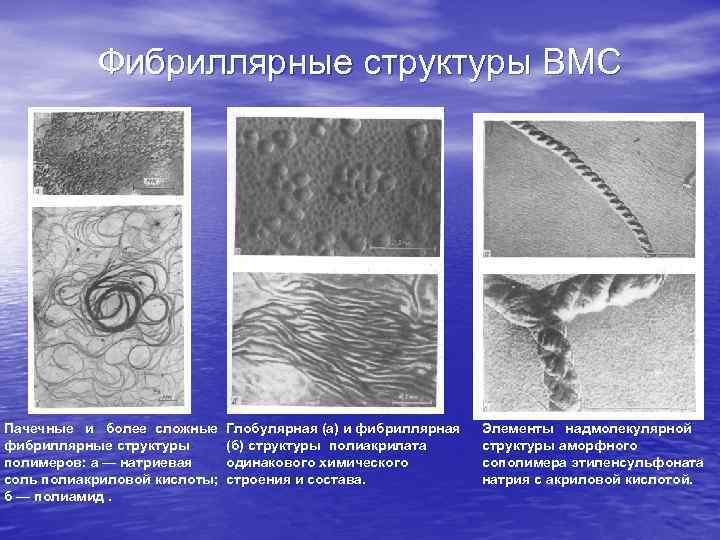 Фибриллярные структуры ВМС Пачечные и более сложные фибриллярные структуры полимеров: а — натриевая соль полиакриловой кислоты; б — полиамид. Глобулярная (а) и фибриллярная (б) структуры полиакрилата одинакового химического строения и состава. Элементы надмолекулярной структуры аморфного сополимера этиленсульфоната натрия с акриловой кислотой.
Фибриллярные структуры ВМС Пачечные и более сложные фибриллярные структуры полимеров: а — натриевая соль полиакриловой кислоты; б — полиамид. Глобулярная (а) и фибриллярная (б) структуры полиакрилата одинакового химического строения и состава. Элементы надмолекулярной структуры аморфного сополимера этиленсульфоната натрия с акриловой кислотой.
 Даны реальные примеры надмолекулярных фибриллярных структур высокомолекулярных соединений.
Даны реальные примеры надмолекулярных фибриллярных структур высокомолекулярных соединений.
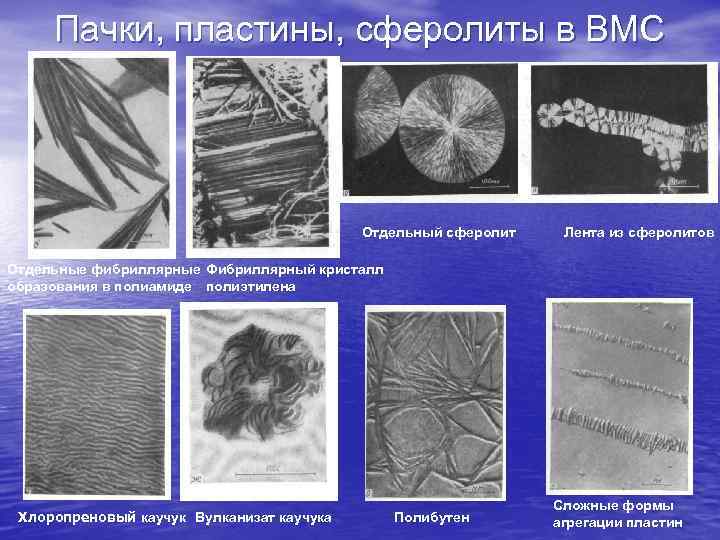 Пачки, пластины, сферолиты в ВМС Отдельный сферолит Лента из сферолитов Отдельные фибриллярные Фибриллярный кристалл образования в полиамиде полиэтилена Хлоропреновый каучук Вулканизат каучука Полибутен Сложные формы агрегации пластин
Пачки, пластины, сферолиты в ВМС Отдельный сферолит Лента из сферолитов Отдельные фибриллярные Фибриллярный кристалл образования в полиамиде полиэтилена Хлоропреновый каучук Вулканизат каучука Полибутен Сложные формы агрегации пластин
 Даны примеры реальных вторичных, третичных, четвертичных надмолекулярных структур.
Даны примеры реальных вторичных, третичных, четвертичных надмолекулярных структур.
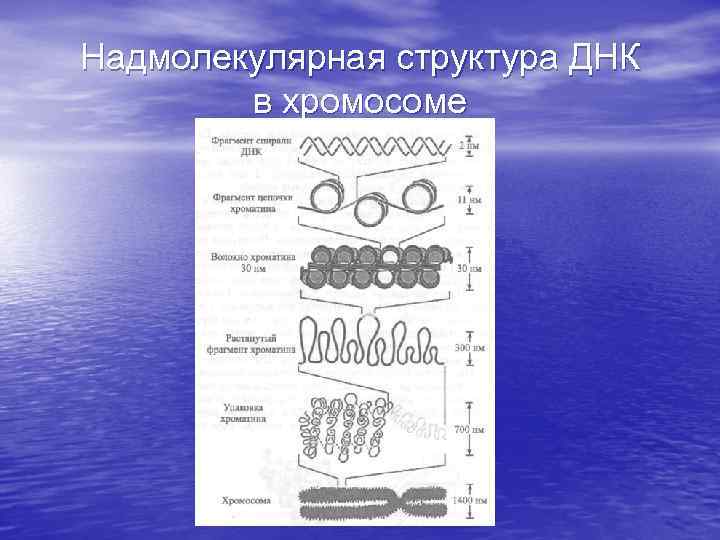 Надмолекулярная структура ДНК в хромосоме
Надмолекулярная структура ДНК в хромосоме
 Схематически изображены надмолекулярные структуры, отвечающие различным уровням упаковки ДНК в хромосоме.
Схематически изображены надмолекулярные структуры, отвечающие различным уровням упаковки ДНК в хромосоме.
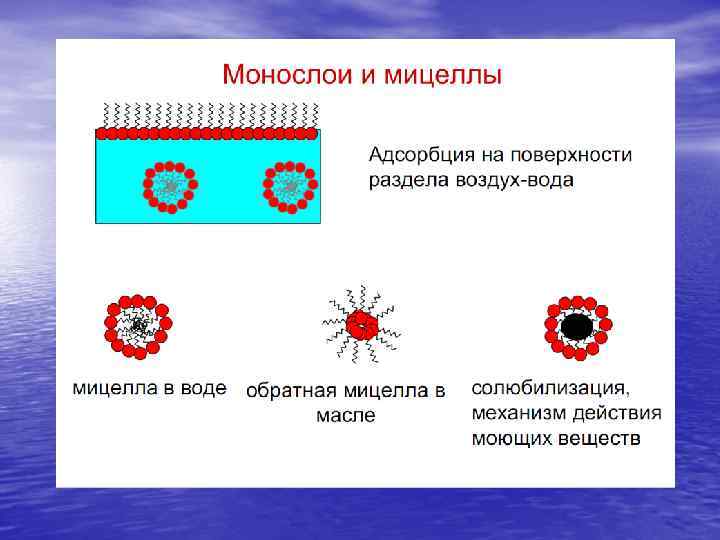


 Дифракционные методы исследования атомного порядка Для этих методов используют рентгеновские кванты, нейтроны и электроны с эквивалентной длиной волны де Бройля порядка межатомного расстояния
Дифракционные методы исследования атомного порядка Для этих методов используют рентгеновские кванты, нейтроны и электроны с эквивалентной длиной волны де Бройля порядка межатомного расстояния
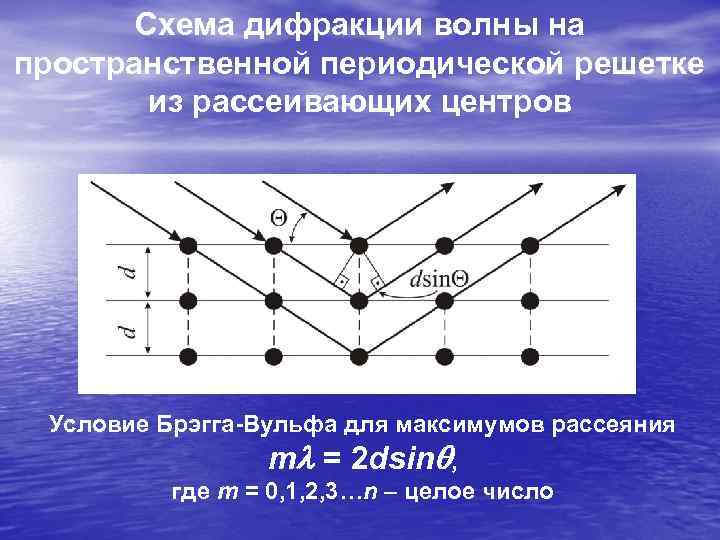 Схема дифракции волны на пространственной периодической решетке из рассеивающих центров Условие Брэгга-Вульфа для максимумов рассеяния ml = 2 dsinq, где m = 0, 1, 2, 3…n – целое число
Схема дифракции волны на пространственной периодической решетке из рассеивающих центров Условие Брэгга-Вульфа для максимумов рассеяния ml = 2 dsinq, где m = 0, 1, 2, 3…n – целое число
 Дифракция волны любой природы на упорядоченной структуре рассеивающих центров подчиняется соотношению Брегга-Вульфа, представленному на слайде. Его смысл заключается в том, что оно определяет набор направлений (углов) рассеяния, вдоль которых интенсивность рассеянной волны будет иметь локальный максимум. Он возникнет тогда, когда разность хода 2 sin между двумя волнами, рассеянными соседними атомными плоскостями , становится равной или кратной длине волны . Это означает, что рассеянные волны находятся «в фазе» и усиливают друга. Этим направлениям соответствуют максимумы сигналов с соответствующих детекторов, а на фотопленке – максимумы засветки (рефлексы). Решая обратную задачу (иногда весьма сложную), по совокупности этих максимумов (рефлексов) можно расшифровать атомную структуру вещества. В первой половине прошлого века расшифровка неизвестной структуры могла занимать месяцы непрерывных расчетов. В настоящее время имеющиеся базы данных различных структур и соответствующие компьютерные программы позволяют проводить расшифровку в течение секунд или минут.
Дифракция волны любой природы на упорядоченной структуре рассеивающих центров подчиняется соотношению Брегга-Вульфа, представленному на слайде. Его смысл заключается в том, что оно определяет набор направлений (углов) рассеяния, вдоль которых интенсивность рассеянной волны будет иметь локальный максимум. Он возникнет тогда, когда разность хода 2 sin между двумя волнами, рассеянными соседними атомными плоскостями , становится равной или кратной длине волны . Это означает, что рассеянные волны находятся «в фазе» и усиливают друга. Этим направлениям соответствуют максимумы сигналов с соответствующих детекторов, а на фотопленке – максимумы засветки (рефлексы). Решая обратную задачу (иногда весьма сложную), по совокупности этих максимумов (рефлексов) можно расшифровать атомную структуру вещества. В первой половине прошлого века расшифровка неизвестной структуры могла занимать месяцы непрерывных расчетов. В настоящее время имеющиеся базы данных различных структур и соответствующие компьютерные программы позволяют проводить расшифровку в течение секунд или минут.
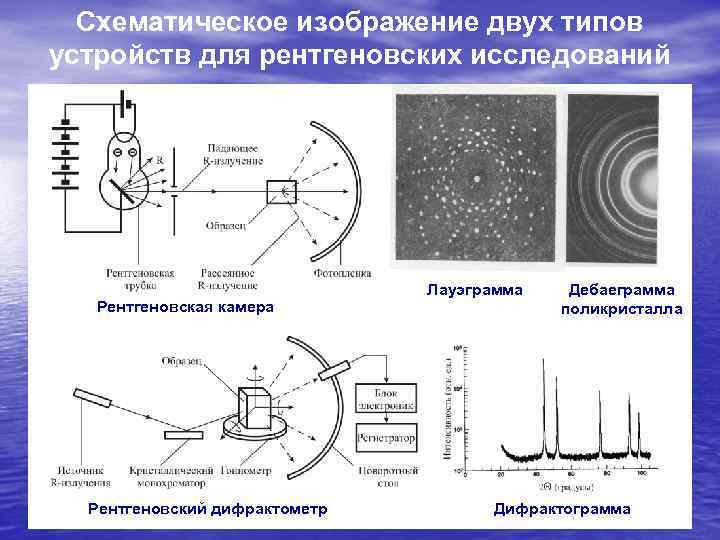 Схематическое изображение двух типов устройств для рентгеновских исследований Рентгеновская камера Рентгеновский дифрактометр Лауэграмма монокристалла Дебаеграмма поликристалла Дифрактограмма
Схематическое изображение двух типов устройств для рентгеновских исследований Рентгеновская камера Рентгеновский дифрактометр Лауэграмма монокристалла Дебаеграмма поликристалла Дифрактограмма
 Все приборы для рентгеноструктурного анализа можно разбить на два класса: рентгеновские камеры, регистрирующие дифракционную картину на фотопленку, и дифрактометры, в которых регистрация рассеянного рентгеновского излучения осуществляется специальными детекторами, регистрирующими падающее на них излучение и преобразующими его в электрический сигнал. Он обрабатывается электроникой и записывается компьютером. На слайде справа показаны примеры типичных дифракционных картин от монокристалла (лауэграмма) и поликристалла (дебаеграмма). Ниже представлена запись дифрактограммы порошка Ni. Она получается обычно движением детектора рентгеновского излучения по дуговой направляющей, поэтому в качестве аргумента на оси абсцисс в дифрактограмме откладывают двойной угол падения 2. По величине углов 2 , на которые приходятся максимумы дифракции, можно рассчитать межплоскостные расстояния в кристаллической структуре, а в аморфной – можно выявить функцию распределения плотности около некоторого атома (в последнем случае на дебаеграмме наблюдаются размытые кольцевые галло, а на дифрактограмме – сильно размытые максимумы.
Все приборы для рентгеноструктурного анализа можно разбить на два класса: рентгеновские камеры, регистрирующие дифракционную картину на фотопленку, и дифрактометры, в которых регистрация рассеянного рентгеновского излучения осуществляется специальными детекторами, регистрирующими падающее на них излучение и преобразующими его в электрический сигнал. Он обрабатывается электроникой и записывается компьютером. На слайде справа показаны примеры типичных дифракционных картин от монокристалла (лауэграмма) и поликристалла (дебаеграмма). Ниже представлена запись дифрактограммы порошка Ni. Она получается обычно движением детектора рентгеновского излучения по дуговой направляющей, поэтому в качестве аргумента на оси абсцисс в дифрактограмме откладывают двойной угол падения 2. По величине углов 2 , на которые приходятся максимумы дифракции, можно рассчитать межплоскостные расстояния в кристаллической структуре, а в аморфной – можно выявить функцию распределения плотности около некоторого атома (в последнем случае на дебаеграмме наблюдаются размытые кольцевые галло, а на дифрактограмме – сильно размытые максимумы.
 От типа атомного порядка или кристаллической решетки зависят все важнейшие свойства вещества • • анизотропия термодинамические характеристики кинетические коэффициенты химические свойства электронно-оптические свойства магнитные свойства механические свойства
От типа атомного порядка или кристаллической решетки зависят все важнейшие свойства вещества • • анизотропия термодинамические характеристики кинетические коэффициенты химические свойства электронно-оптические свойства магнитные свойства механические свойства
 • • Тип кристаллической решетки определяет многие характеристики и свойства веществ, перечисленных на слайде. Следует иметь в виду следующее: Анизотропия может проявляться только в монокристаллах. В поликристаллах хаотическая разориентация отдельных зерен нивелирует её. Многие элементарные, бинарные и другие простые вещества могут иметь несколько кристаллических фаз (хрестоматийный пример – углерод в алмазной, графитовой, аморфной фазе или в виде фуллеренов, нанотрубок и др. ) в зависимости от условий синтеза, термодинамических условий существования, предыстории могут реализоваться условия для существования или сосуществования различных твердых фаз. Они могут иметь резко различающиеся физические свойства. Например, алмаз – прозрачен, тверд, хороший диэлектрик, а графит непрозрачен, мягок, хороший проводник. -железо (равновесно до t = 723 ºС) с ОЦК решеткой – сильный ферромагнетик, а -железо (равновесно при t выше 723 ºС) имеет ГЦК – решетку и является парамагнетиком.
• • Тип кристаллической решетки определяет многие характеристики и свойства веществ, перечисленных на слайде. Следует иметь в виду следующее: Анизотропия может проявляться только в монокристаллах. В поликристаллах хаотическая разориентация отдельных зерен нивелирует её. Многие элементарные, бинарные и другие простые вещества могут иметь несколько кристаллических фаз (хрестоматийный пример – углерод в алмазной, графитовой, аморфной фазе или в виде фуллеренов, нанотрубок и др. ) в зависимости от условий синтеза, термодинамических условий существования, предыстории могут реализоваться условия для существования или сосуществования различных твердых фаз. Они могут иметь резко различающиеся физические свойства. Например, алмаз – прозрачен, тверд, хороший диэлектрик, а графит непрозрачен, мягок, хороший проводник. -железо (равновесно до t = 723 ºС) с ОЦК решеткой – сильный ферромагнетик, а -железо (равновесно при t выше 723 ºС) имеет ГЦК – решетку и является парамагнетиком.
 Особенности атомного строения наночастиц
Особенности атомного строения наночастиц
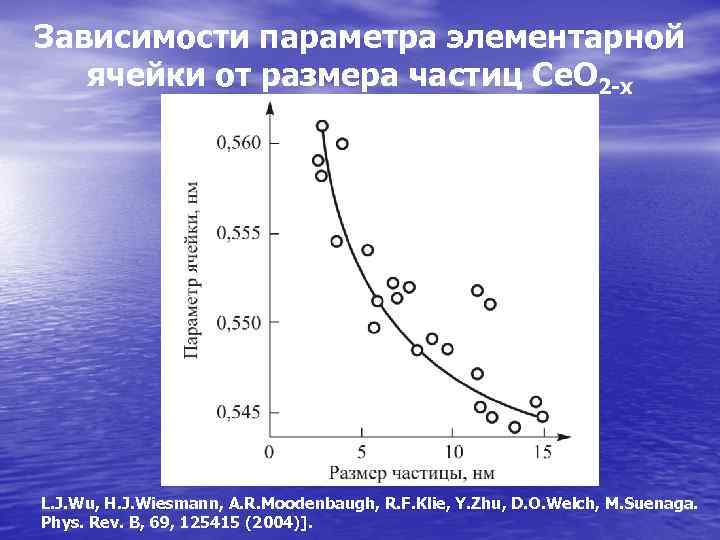 Зависимости параметра элементарной ячейки от размера частиц Се. О 2 -х L. J. Wu, H. J. Wiesmann, A. R. Moodenbaugh, R. F. Klie, Y. Zhu, D. O. Welch, M. Suenaga. Phys. Rev. B, 69, 125415 (2004)].
Зависимости параметра элементарной ячейки от размера частиц Се. О 2 -х L. J. Wu, H. J. Wiesmann, A. R. Moodenbaugh, R. F. Klie, Y. Zhu, D. O. Welch, M. Suenaga. Phys. Rev. B, 69, 125415 (2004)].
 • Как правило, параметры кристаллической решетки (а следовательно, и все связанные с ней свойства кристалла) плавно меняются, при уменьшении размеров частицы в наноразмерную область. В качестве примера на слайде показана размерная зависимость для Се. О 2 -х
• Как правило, параметры кристаллической решетки (а следовательно, и все связанные с ней свойства кристалла) плавно меняются, при уменьшении размеров частицы в наноразмерную область. В качестве примера на слайде показана размерная зависимость для Се. О 2 -х
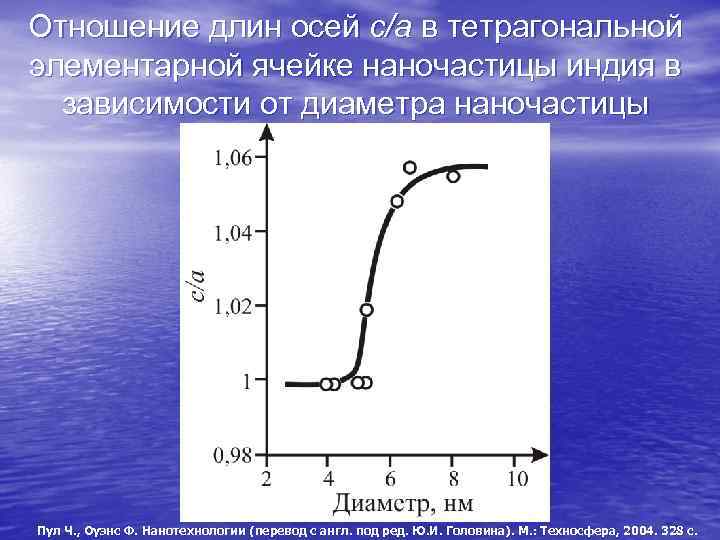 Отношение длин осей с/а в тетрагональной элементарной ячейке наночастицы индия в зависимости от диаметра наночастицы Пул Ч. , Оуэнс Ф. Нанотехнологии (перевод с англ. под ред. Ю. И. Головина). М. : Техносфера, 2004. 328 с.
Отношение длин осей с/а в тетрагональной элементарной ячейке наночастицы индия в зависимости от диаметра наночастицы Пул Ч. , Оуэнс Ф. Нанотехнологии (перевод с англ. под ред. Ю. И. Головина). М. : Техносфера, 2004. 328 с.
 Особенности атомного строения наночастиц (НЧ) • Атомный порядок (симметрия), • • • межатомные расстояния в НЧ могут сильно отличаться от объемных 3 5 приповерхностных атомных слоя могут иметь структуру, отличную от объемной Спектр атомных дефектов в НЧ может отличаться от объемного Механические, термодинамические, кинетические свойства НЧ отличаются от объемных
Особенности атомного строения наночастиц (НЧ) • Атомный порядок (симметрия), • • • межатомные расстояния в НЧ могут сильно отличаться от объемных 3 5 приповерхностных атомных слоя могут иметь структуру, отличную от объемной Спектр атомных дефектов в НЧ может отличаться от объемного Механические, термодинамические, кинетические свойства НЧ отличаются от объемных
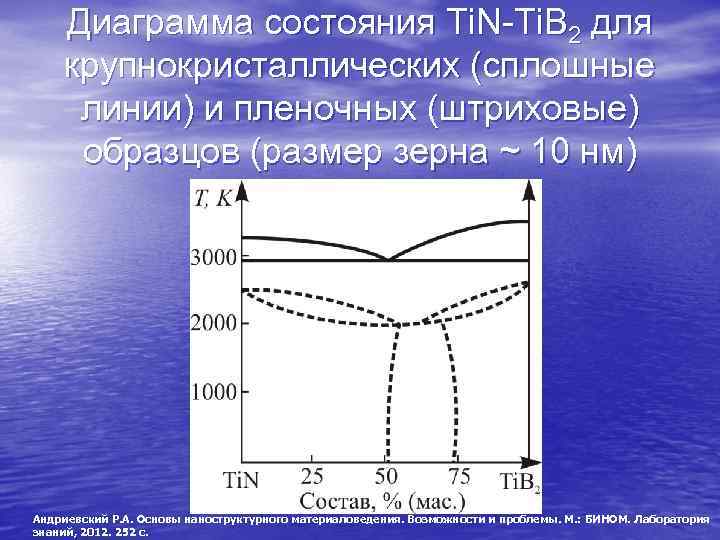 Диаграмма состояния Ti. N-Ti. B 2 для крупнокристаллических (сплошные линии) и пленочных (штриховые) образцов (размер зерна ~ 10 нм) Андриевский Р. А. Основы наноструктурного материаловедения. Возможности и проблемы. М. : БИНОМ. Лаборатория знаний, 2012. 252 с.
Диаграмма состояния Ti. N-Ti. B 2 для крупнокристаллических (сплошные линии) и пленочных (штриховые) образцов (размер зерна ~ 10 нм) Андриевский Р. А. Основы наноструктурного материаловедения. Возможности и проблемы. М. : БИНОМ. Лаборатория знаний, 2012. 252 с.
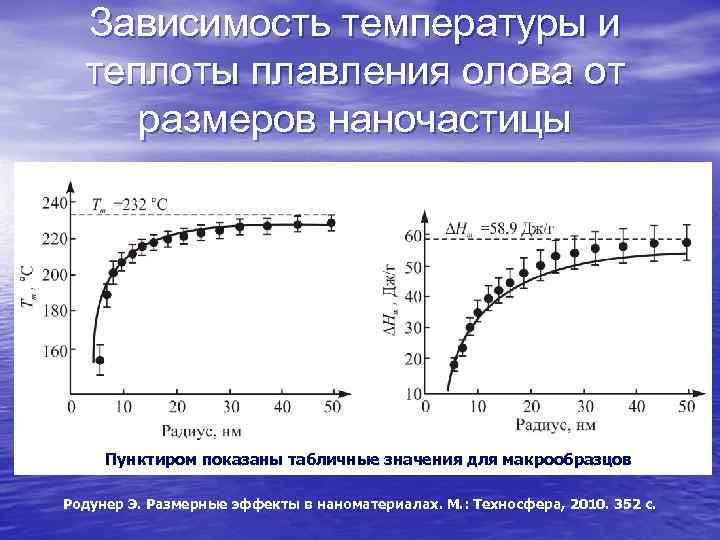 Зависимость температуры и теплоты плавления олова от размеров наночастицы Пунктиром показаны табличные значения для макрообразцов Родунер Э. Размерные эффекты в наноматериалах. М. : Техносфера, 2010. 352 с.
Зависимость температуры и теплоты плавления олова от размеров наночастицы Пунктиром показаны табличные значения для макрообразцов Родунер Э. Размерные эффекты в наноматериалах. М. : Техносфера, 2010. 352 с.
 Реальные твердые тела • Дефекты атомарной структуры - точечные - линейные - плоскостные - объёмные Термодинамически равновесные и неравновесные дефекты • Возбуждения и квазичастицы • Структурочувствительные свойства и кинетические явления
Реальные твердые тела • Дефекты атомарной структуры - точечные - линейные - плоскостные - объёмные Термодинамически равновесные и неравновесные дефекты • Возбуждения и квазичастицы • Структурочувствительные свойства и кинетические явления
 Реальные твердые тела отличаются от идеальных с абсолютно упорядоченной решеткой наличием дефектов структуры и возбуждений. Различают структурные дефекты собственные (в химически чистом кристалле) и примесные (также всегда присутствующие в реальных кристаллах). Дефекты атомной структуры принято классифицировать с позиций их размерности (числа макроскопических измерений). С этой точки зрения они могут быть точечными (0 - мерными), линейными (1 -мерными), плоскостными (2 -мерными) и объёмными (3 -мерными). Кроме них всегда присутствуют равновесные термические колебания (на другом языке – решеточные возбуждения –фононы) и неравновесные электронные возбуждения, вызванные внешними электрическими, магнитными, оптическими полями. В итоге – абсолютное большинство физических свойств определяется не только (а часто и не столько) составом и типом решетки, сколько спектром дефектов в ней. Такие свойства называют структурочувствительными. В первую очередь к ним относятся электронно-оптические и механические, в меньшей степени – тепловые и магнитные.
Реальные твердые тела отличаются от идеальных с абсолютно упорядоченной решеткой наличием дефектов структуры и возбуждений. Различают структурные дефекты собственные (в химически чистом кристалле) и примесные (также всегда присутствующие в реальных кристаллах). Дефекты атомной структуры принято классифицировать с позиций их размерности (числа макроскопических измерений). С этой точки зрения они могут быть точечными (0 - мерными), линейными (1 -мерными), плоскостными (2 -мерными) и объёмными (3 -мерными). Кроме них всегда присутствуют равновесные термические колебания (на другом языке – решеточные возбуждения –фононы) и неравновесные электронные возбуждения, вызванные внешними электрическими, магнитными, оптическими полями. В итоге – абсолютное большинство физических свойств определяется не только (а часто и не столько) составом и типом решетки, сколько спектром дефектов в ней. Такие свойства называют структурочувствительными. В первую очередь к ним относятся электронно-оптические и механические, в меньшей степени – тепловые и магнитные.
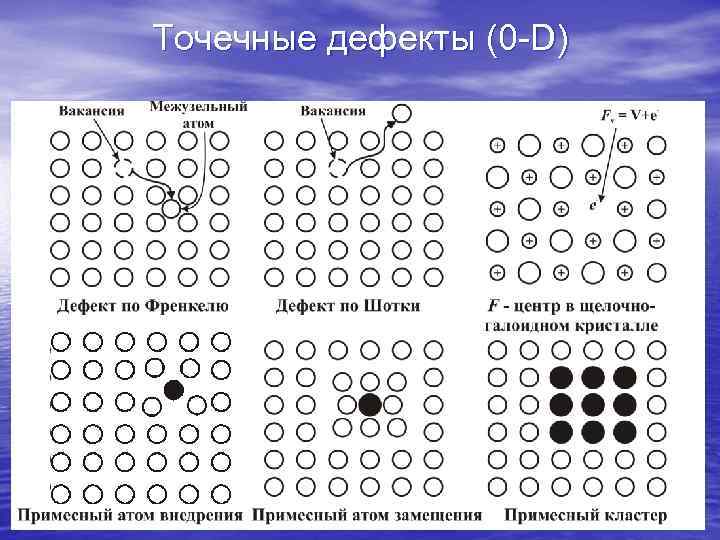 Точечные дефекты (0 -D)
Точечные дефекты (0 -D)
 На слайде представлены примеры некоторых наиболее часто встречающихся точечных дефектов. Следует иметь в виду, что некоторые из собственных дефектов решетки являются термодинамически равновесными и, следовательно, неустранимыми. Например, при предплавильных температурах равновесная концентрация вакансий достигает ~ 10 -4 – 10 -3 от концентрации атомов в решетке. Однако, в подавляющем числе случаев неравновесных дефектов кристалле гораздо больше, чем равновесных.
На слайде представлены примеры некоторых наиболее часто встречающихся точечных дефектов. Следует иметь в виду, что некоторые из собственных дефектов решетки являются термодинамически равновесными и, следовательно, неустранимыми. Например, при предплавильных температурах равновесная концентрация вакансий достигает ~ 10 -4 – 10 -3 от концентрации атомов в решетке. Однако, в подавляющем числе случаев неравновесных дефектов кристалле гораздо больше, чем равновесных.
 Роль точечных дефектов в формировании свойств • • • Электропроводность, электроперенос Диффузия Высокотемпературная ползучесть Теплопроводность Оптические спектры Сорбционные, химические и каталитические свойства реальной поверхности
Роль точечных дефектов в формировании свойств • • • Электропроводность, электроперенос Диффузия Высокотемпературная ползучесть Теплопроводность Оптические спектры Сорбционные, химические и каталитические свойства реальной поверхности
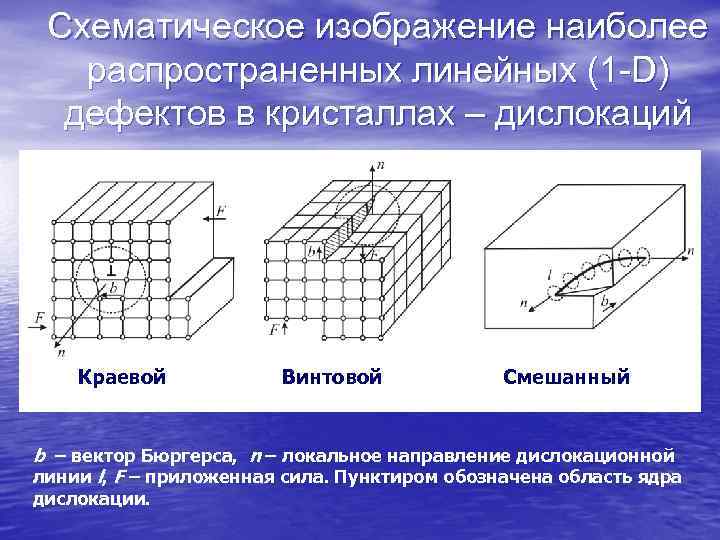 Схематическое изображение наиболее распространенных линейных (1 -D) дефектов в кристаллах – дислокаций Краевой Винтовой Смешанный b – вектор Бюргерса, n – локальное направление дислокационной линии l, F – приложенная сила. Пунктиром обозначена область ядра дислокации.
Схематическое изображение наиболее распространенных линейных (1 -D) дефектов в кристаллах – дислокаций Краевой Винтовой Смешанный b – вектор Бюргерса, n – локальное направление дислокационной линии l, F – приложенная сила. Пунктиром обозначена область ядра дислокации.
 Другой, почти всегда присутствующий в кристаллах вид структурных дефектов – дислокации, представляющие собой квазиодномерное нарушение структуры. Наиболее простые разновидности дислокаций –краевая и винтовая – показаны на слайде. Вокруг линии дислокации возникает локальное поле искажений кристаллической решетки, существенно меняющее её свойства. Дальнодействующие поля упругих искажений вызывают притяжение точечных дефектов и образование соответствующих облаков (Коттрела). Статические и динамические характеристики дислокаций определяют механические свойства кристаллов и сильно влияют на все другие структурочувствительные характеристики (электрические, оптические, магнитные), несмотря на то, что даже при самой высокой их плотности (~ 1012 см/см 3) объём, занимаемый ядрами дислокаций, ничтожно мал по сравнению с объёмом матрицы.
Другой, почти всегда присутствующий в кристаллах вид структурных дефектов – дислокации, представляющие собой квазиодномерное нарушение структуры. Наиболее простые разновидности дислокаций –краевая и винтовая – показаны на слайде. Вокруг линии дислокации возникает локальное поле искажений кристаллической решетки, существенно меняющее её свойства. Дальнодействующие поля упругих искажений вызывают притяжение точечных дефектов и образование соответствующих облаков (Коттрела). Статические и динамические характеристики дислокаций определяют механические свойства кристаллов и сильно влияют на все другие структурочувствительные характеристики (электрические, оптические, магнитные), несмотря на то, что даже при самой высокой их плотности (~ 1012 см/см 3) объём, занимаемый ядрами дислокаций, ничтожно мал по сравнению с объёмом матрицы.
 Роль дислокаций в формировании свойств • • Носители пластической деформации Зародыши разрушения Трубочная диффузия Электронно оптические свойства Аккомодация зерен в поликристаллах Стоки для точечных дефектов Стопора для границ магнитных доменов
Роль дислокаций в формировании свойств • • Носители пластической деформации Зародыши разрушения Трубочная диффузия Электронно оптические свойства Аккомодация зерен в поликристаллах Стоки для точечных дефектов Стопора для границ магнитных доменов
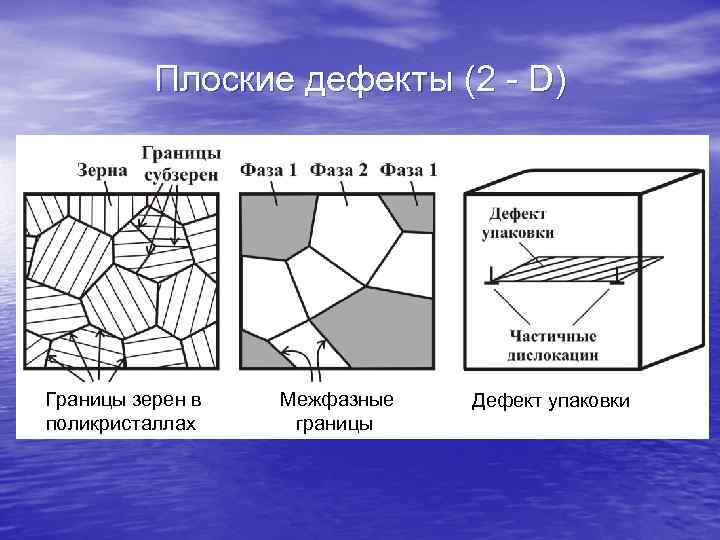 Плоские дефекты (2 - D) Границы зерен в поликристаллах Межфазные границы Дефект упаковки
Плоские дефекты (2 - D) Границы зерен в поликристаллах Межфазные границы Дефект упаковки
 Свободная поверхность твердого тела уже сама по себе является плоским дефектом структуры, т. к. нарушает трансляционную симметрию кристалла (см. подробнее Модуль 4). Внутренние двумерные нарушения порядка представлены границами зерен и субзерен (в поликристаллах), границами фаз ( в многофазных материалах), границами доменов (в поляризованных и намагниченных материалах), дефектами упаковки (между двумя частичными дислокациями, образующимися при расщеплении одной полной). Внутренние и внешние границы могут испускать и поглощать точечные дефекты и дислокации, т. е. с формальной точки зрения участвовать в многочисленных реакциях между структурными дефектами, константы скоростей и равновесия которых зависят от температуры, приложенных механических напряжений, электрических и магнитных полей.
Свободная поверхность твердого тела уже сама по себе является плоским дефектом структуры, т. к. нарушает трансляционную симметрию кристалла (см. подробнее Модуль 4). Внутренние двумерные нарушения порядка представлены границами зерен и субзерен (в поликристаллах), границами фаз ( в многофазных материалах), границами доменов (в поляризованных и намагниченных материалах), дефектами упаковки (между двумя частичными дислокациями, образующимися при расщеплении одной полной). Внутренние и внешние границы могут испускать и поглощать точечные дефекты и дислокации, т. е. с формальной точки зрения участвовать в многочисленных реакциях между структурными дефектами, константы скоростей и равновесия которых зависят от температуры, приложенных механических напряжений, электрических и магнитных полей.
 Схемы наноструктурированных материалов, восстановленные из данных рентгеновской дифракции и мессабауэровской спектроскопии Нанокристаллический металл (все атомы химически одинаковы, светлые кружочки обозначают атомы, находящиеся в межзеренных границах, темные – в нанокристаллитах) Сплав, состоящий из атомов двух сортов, например Cu и Bi (темные кружки – атомы Bi - сегрегированны в границах зерен, светлые кружки – атомы Cu находятся, в основном, в кристаллитах Двухфазый сплав, например, Fe-Ag, из атомов, не смешивающихся ни в жидком ни в твердом состоянии. Однако в разрыхленных межфазных границах (заштрихованы) они могут образовывать твердые растворы
Схемы наноструктурированных материалов, восстановленные из данных рентгеновской дифракции и мессабауэровской спектроскопии Нанокристаллический металл (все атомы химически одинаковы, светлые кружочки обозначают атомы, находящиеся в межзеренных границах, темные – в нанокристаллитах) Сплав, состоящий из атомов двух сортов, например Cu и Bi (темные кружки – атомы Bi - сегрегированны в границах зерен, светлые кружки – атомы Cu находятся, в основном, в кристаллитах Двухфазый сплав, например, Fe-Ag, из атомов, не смешивающихся ни в жидком ни в твердом состоянии. Однако в разрыхленных межфазных границах (заштрихованы) они могут образовывать твердые растворы
 Границы зерен, фаз, доменов обычно имеют толщину несколько атомных диаметров (т. е. ~ 1 нм). Эти слои резко отличаются от матричных своей структурой, т. е. по сути они представляют новую фазу. Её относительный объём и вклад в свойства растет с уменьшением размеров зерна d. При ≈ 1 нм относительная доля этой фазы достигает 50% от объёма всего материала при d ≈ 6 нм. Но и при d ≈ 20 -30 нм наличие таких границ в кристалле может кардинально поменять его свойства.
Границы зерен, фаз, доменов обычно имеют толщину несколько атомных диаметров (т. е. ~ 1 нм). Эти слои резко отличаются от матричных своей структурой, т. е. по сути они представляют новую фазу. Её относительный объём и вклад в свойства растет с уменьшением размеров зерна d. При ≈ 1 нм относительная доля этой фазы достигает 50% от объёма всего материала при d ≈ 6 нм. Но и при d ≈ 20 -30 нм наличие таких границ в кристалле может кардинально поменять его свойства.
 Динамика и взаимодействие дефектов решетки • Подвижность дефектов • Локальные поля деформации и упругой • • • энергии Упругое взаимодействие Внутрикристаллические химические реакции Взаимопревращения дефектов
Динамика и взаимодействие дефектов решетки • Подвижность дефектов • Локальные поля деформации и упругой • • • энергии Упругое взаимодействие Внутрикристаллические химические реакции Взаимопревращения дефектов
 Тепловые свойства твердых тел • • Теплоемкость Тепловое расширение Теплопроводность Температура плавления
Тепловые свойства твердых тел • • Теплоемкость Тепловое расширение Теплопроводность Температура плавления
 Фононы • Колебательные движения атомов около положений равновесия можно описать набором взаимодействующих квазичастиц – ФОНОНОВ • В твердом теле возможен два вида фононов – акустические и оптические • Все тепловые свойства твердых тел определяются свойствами фононного и электронного газов в них • Энергия фононов пропорциональна их частоте • Фононный спектр сплошной и ограничен сверху и снизу предельными частотами
Фононы • Колебательные движения атомов около положений равновесия можно описать набором взаимодействующих квазичастиц – ФОНОНОВ • В твердом теле возможен два вида фононов – акустические и оптические • Все тепловые свойства твердых тел определяются свойствами фононного и электронного газов в них • Энергия фононов пропорциональна их частоте • Фононный спектр сплошной и ограничен сверху и снизу предельными частотами
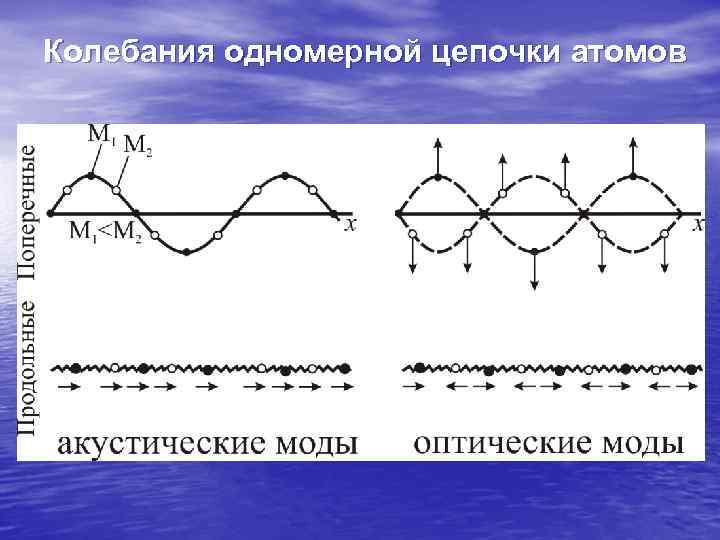 Колебания одномерной цепочки атомов
Колебания одномерной цепочки атомов
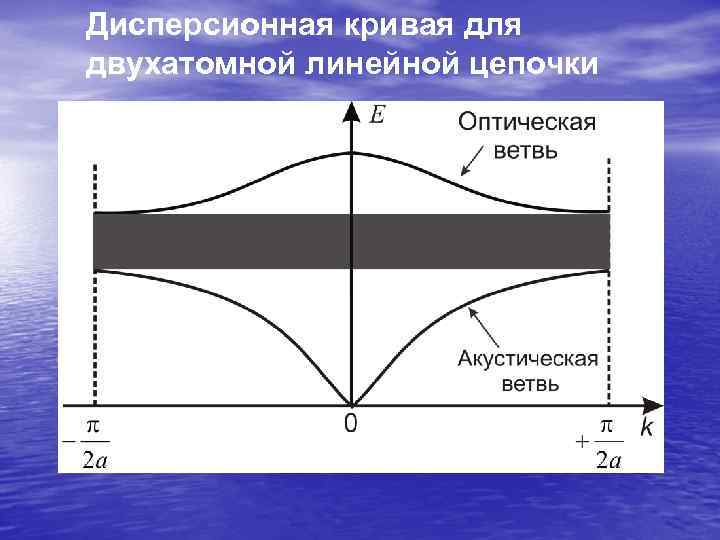 Дисперсионная кривая для двухатомной линейной цепочки
Дисперсионная кривая для двухатомной линейной цепочки
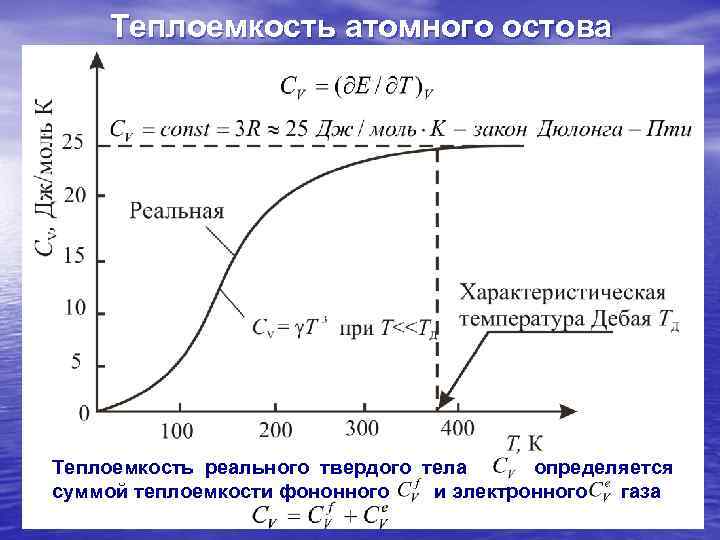 Теплоемкость атомного остова Теплоемкость реального твердого тела определяется суммой теплоемкости фононного и электронного газа
Теплоемкость атомного остова Теплоемкость реального твердого тела определяется суммой теплоемкости фононного и электронного газа
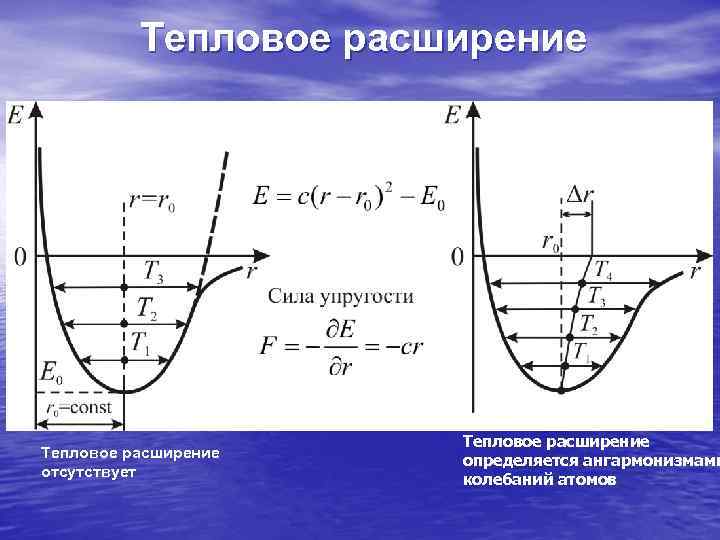 Тепловое расширение Параболический потенциал Тепловое расширение отсутствует Реальный ангармонический потенциал Тепловое расширение определяется ангармонизмами колебаний атомов
Тепловое расширение Параболический потенциал Тепловое расширение отсутствует Реальный ангармонический потенциал Тепловое расширение определяется ангармонизмами колебаний атомов
 Теплопроводность твердых тел Стационарная теплопроводность подчиняется закону Фурье Для анизотропных твердых тел (например, кристаллов) l – симметричный тензор 2 -го ранга
Теплопроводность твердых тел Стационарная теплопроводность подчиняется закону Фурье Для анизотропных твердых тел (например, кристаллов) l – симметричный тензор 2 -го ранга
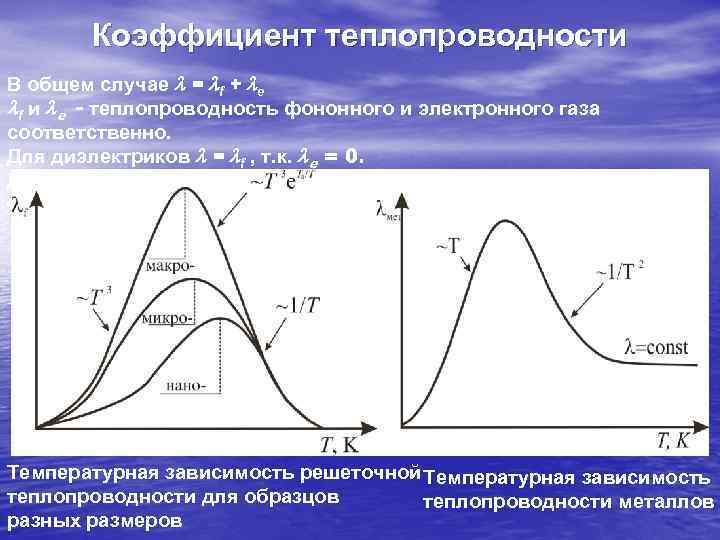 Коэффициент теплопроводности В общем случае l = lf + le lf и le - теплопроводность фононного и электронного газа соответственно. Для диэлектриков l = lf , т. к. le = 0. Для металлов l ≈ le , т. к. le >100 f и действует закон Видемана. Франца /s = LT Температурная зависимость решеточной Температурная зависимость теплопроводности для образцов теплопроводности металлов разных размеров
Коэффициент теплопроводности В общем случае l = lf + le lf и le - теплопроводность фононного и электронного газа соответственно. Для диэлектриков l = lf , т. к. le = 0. Для металлов l ≈ le , т. к. le >100 f и действует закон Видемана. Франца /s = LT Температурная зависимость решеточной Температурная зависимость теплопроводности для образцов теплопроводности металлов разных размеров
 Краткий итог Из сказанного выше следует, что атомная структура наночастиц и наноструктур может сильно отличаться от таковой для макрообразцов того же материала. Это вызывает изменение практически всех физико-химических свойств вещества. Дополнительное обсуждение роли приповерхностных слоев дано в модуле 5.
Краткий итог Из сказанного выше следует, что атомная структура наночастиц и наноструктур может сильно отличаться от таковой для макрообразцов того же материала. Это вызывает изменение практически всех физико-химических свойств вещества. Дополнительное обсуждение роли приповерхностных слоев дано в модуле 5.
 Атомная структура углеродных наночастиц
Атомная структура углеродных наночастиц
 В качестве примера наноструктур рассмотрены новые углеродные материалы – фуллерены, нанотрубки и графен, синтезированные из чрезвычайно распространенных в природе атомов углерода, но поражающие воображение своими уникальными свойствами.
В качестве примера наноструктур рассмотрены новые углеродные материалы – фуллерены, нанотрубки и графен, синтезированные из чрезвычайно распространенных в природе атомов углерода, но поражающие воображение своими уникальными свойствами.
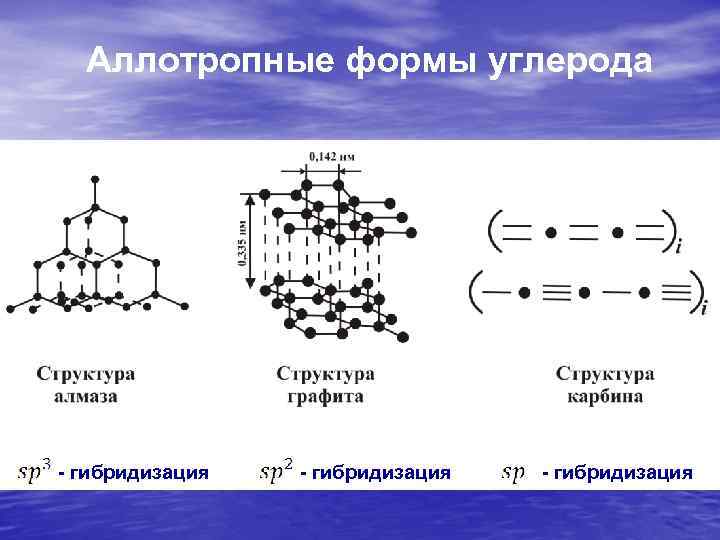 Аллотропные формы углерода - гибридизация
Аллотропные формы углерода - гибридизация
 Чем же вызвано такое многообразие аллотропных форм и атомных структур, образуемых углеродом? В первую очередь возможностью разного типа гибридизации s и р орбиталей валентных электронов (более подробно об электронных структурах см. Модуль 3). Так, sp 3 -гибридизация дает тетрагональную структуру связей в алмазе, sp 2 гибридизация – плоскую гексагональную сетку фуллерена (по 3 связи на каждый атом), а spгибридизация – линейные органические молекулы.
Чем же вызвано такое многообразие аллотропных форм и атомных структур, образуемых углеродом? В первую очередь возможностью разного типа гибридизации s и р орбиталей валентных электронов (более подробно об электронных структурах см. Модуль 3). Так, sp 3 -гибридизация дает тетрагональную структуру связей в алмазе, sp 2 гибридизация – плоскую гексагональную сетку фуллерена (по 3 связи на каждый атом), а spгибридизация – линейные органические молекулы.
 Харолд Крото (слева) и Ричард Смолли, лауреаты Нобелевской премии по химии 1996 г. за открытие фуллеренов
Харолд Крото (слева) и Ричард Смолли, лауреаты Нобелевской премии по химии 1996 г. за открытие фуллеренов
 Лауреаты Нобелевской премии по физике 2010 года - А. Гейм и К. Новоселов А. К. Гейм К. С. Новоселов (за новаторские эксперименты по исследованию двумерного материала графена)
Лауреаты Нобелевской премии по физике 2010 года - А. Гейм и К. Новоселов А. К. Гейм К. С. Новоселов (за новаторские эксперименты по исследованию двумерного материала графена)
 Первооткрывателями фуллеренов считаются Х. Крото и Р. Смолли, получившие за это Нобелевскую премию в 1996 г. Но теоретически их предсказывали еще в 70 -е годы, а астрофизики наблюдали в спектрах межзвездной пыли линии, которые соответствовали этим необычным пространственным углеродным молекулам.
Первооткрывателями фуллеренов считаются Х. Крото и Р. Смолли, получившие за это Нобелевскую премию в 1996 г. Но теоретически их предсказывали еще в 70 -е годы, а астрофизики наблюдали в спектрах межзвездной пыли линии, которые соответствовали этим необычным пространственным углеродным молекулам.
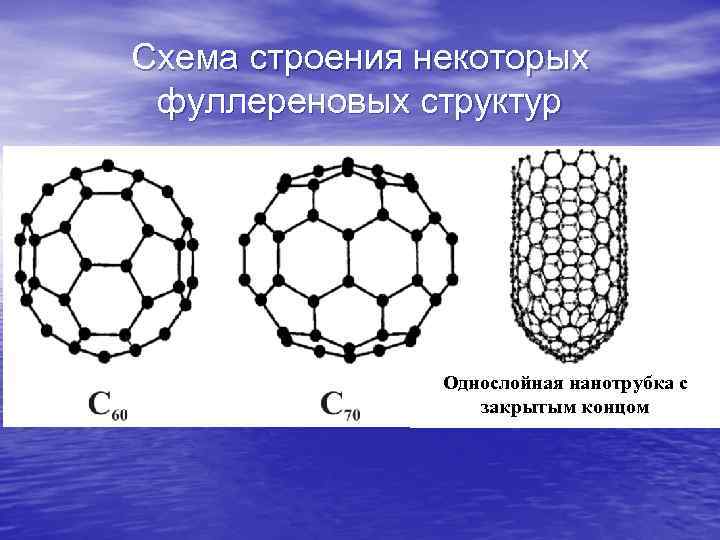 Схема строения некоторых фуллереновых структур Однослойная нанотрубка с закрытым концом
Схема строения некоторых фуллереновых структур Однослойная нанотрубка с закрытым концом
 На слайде показано несколько примеров атомной структуры углеродных наночастиц/молекул, синтезированных Х. Крото с соавторами, Ииджимой и др.
На слайде показано несколько примеров атомной структуры углеродных наночастиц/молекул, синтезированных Х. Крото с соавторами, Ииджимой и др.
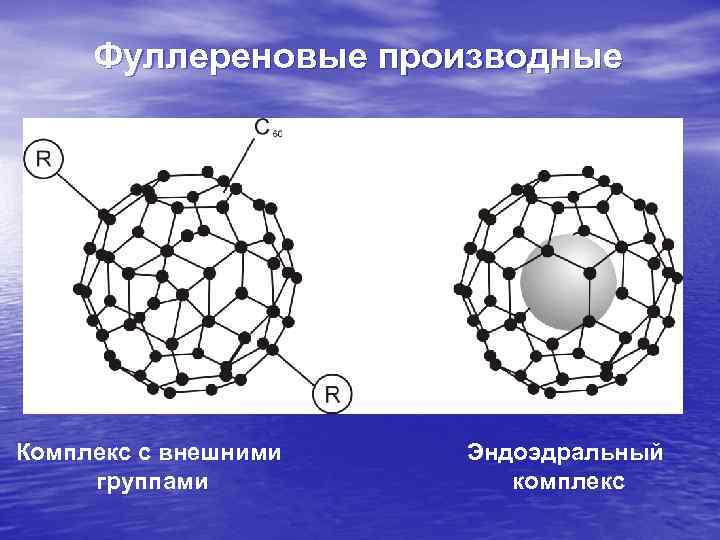 Фуллереновые производные Комплекс с внешними группами Эндоэдральный комплекс
Фуллереновые производные Комплекс с внешними группами Эндоэдральный комплекс
 На фоне изучения простых наноуглеродных структур, показанных на предыдущем слайде были обнаружены и синтезированы специально более сложные. На слайде изображены структурные схемы некоторых производных фуллеренов: комплекс с внешними группами, функционализирующими молекулу С 60 под те или иные задачи, а также эндоэдравный комплекс с чужеродными атомами, помещенными внутрь оболочки. Затем были получены фуллереновые димеры, полимеры, кристаллы, донорно-акцепторные комплексы.
На фоне изучения простых наноуглеродных структур, показанных на предыдущем слайде были обнаружены и синтезированы специально более сложные. На слайде изображены структурные схемы некоторых производных фуллеренов: комплекс с внешними группами, функционализирующими молекулу С 60 под те или иные задачи, а также эндоэдравный комплекс с чужеродными атомами, помещенными внутрь оболочки. Затем были получены фуллереновые димеры, полимеры, кристаллы, донорно-акцепторные комплексы.
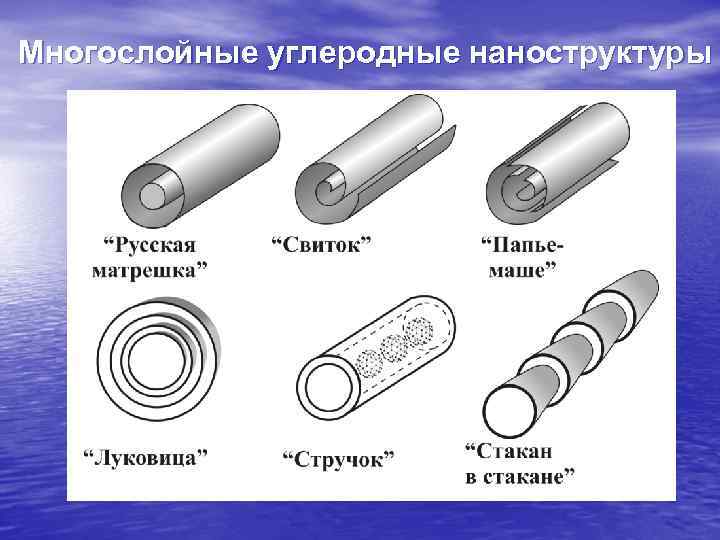 Многослойные углеродные наноструктуры
Многослойные углеродные наноструктуры
 Тщательное изучение продуктов синтеза углеродных наноструктур (о методах синтеза см. Модуль 7) позволило выявить большое разнообразие многослойных структур, часть которых показана на слайде. Особый интерес в последнее время привлекают так называемые «стручки» - нанотрубки с помещенными во внутреннюю полость чужеродными молекулами. Ими могут быть лекарства, горючие газы (водород), и другие полезные вещества, запечатанные в «самые прочные в мире баллоны» , как пишут авторы одной из статей в Nature.
Тщательное изучение продуктов синтеза углеродных наноструктур (о методах синтеза см. Модуль 7) позволило выявить большое разнообразие многослойных структур, часть которых показана на слайде. Особый интерес в последнее время привлекают так называемые «стручки» - нанотрубки с помещенными во внутреннюю полость чужеродными молекулами. Ими могут быть лекарства, горючие газы (водород), и другие полезные вещества, запечатанные в «самые прочные в мире баллоны» , как пишут авторы одной из статей в Nature.
 Морфологические разновидности углеродных нанотрубок и нановолокон Нановолокно Многостенная Бамбукообразное Нановолокно «столбик «елочной «стопка Углеродная нановолокно со сферичесмонет» структуры» чашек» нанотрубка кими секциям Раков Э. Г. Нанотрубки и фуллерены: Учебн. Пособие. – М. : Университетская книга ,
Морфологические разновидности углеродных нанотрубок и нановолокон Нановолокно Многостенная Бамбукообразное Нановолокно «столбик «елочной «стопка Углеродная нановолокно со сферичесмонет» структуры» чашек» нанотрубка кими секциям Раков Э. Г. Нанотрубки и фуллерены: Учебн. Пособие. – М. : Университетская книга ,
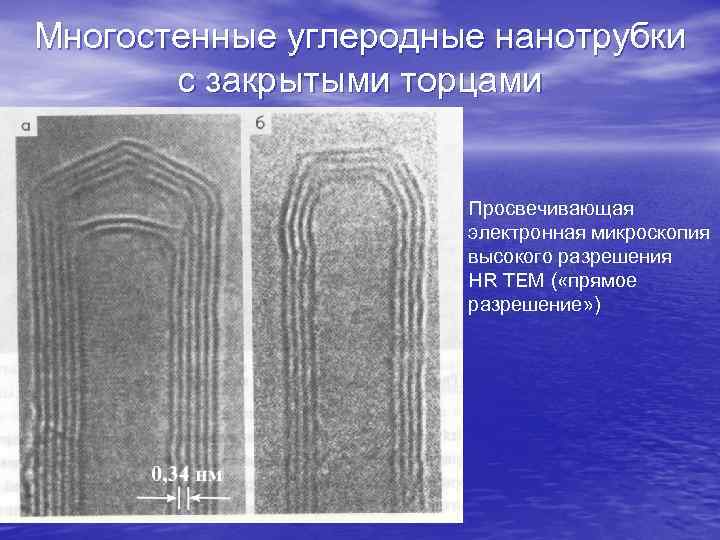 Многостенные углеродные нанотрубки с закрытыми торцами Просвечивающая электронная микроскопия высокого разрешения HR TEM ( «прямое разрешение» )
Многостенные углеродные нанотрубки с закрытыми торцами Просвечивающая электронная микроскопия высокого разрешения HR TEM ( «прямое разрешение» )
 На слайде представлены изображения многостенных углеродных нанотрубок с закрытыми «шапочками» торцами, полученными в просвечивающем электронном микроскопе прямого (атомного) разрешения (HRTEM). Более подробно о микроскопии см. Модуль 6.
На слайде представлены изображения многостенных углеродных нанотрубок с закрытыми «шапочками» торцами, полученными в просвечивающем электронном микроскопе прямого (атомного) разрешения (HRTEM). Более подробно о микроскопии см. Модуль 6.
 Луковичная и трубчатые углеродные наноструктуры HR TEM 5 нм
Луковичная и трубчатые углеродные наноструктуры HR TEM 5 нм
 На слайде показана смесь углеродных наноструктур, которая обычно и получается в процессе синтеза. Варьирование параметрами синтеза позволяет доводить долю желаемого продукта до 95 -98%.
На слайде показана смесь углеродных наноструктур, которая обычно и получается в процессе синтеза. Варьирование параметрами синтеза позволяет доводить долю желаемого продукта до 95 -98%.
 Свойства одностенных нанотрубок зависят от хиральности Модель образования нанотрубок с различной хиральностью при свертывании в цилиндр гексагональной сетки графита Изображение однослойных углеродных нанотрубок, полученные в сканирующем туннельном микроскопе
Свойства одностенных нанотрубок зависят от хиральности Модель образования нанотрубок с различной хиральностью при свертывании в цилиндр гексагональной сетки графита Изображение однослойных углеродных нанотрубок, полученные в сканирующем туннельном микроскопе
 Свойства одностенных фуллереновых молекул и нанотрубок зависят от их диаметра и дефектности. Тщательно выращенные нанотрубки имеют менее одного структурного дефекта на 1012 атомов углерода. Такая степень совершенства практически недостижима для макроструктур. В очень сильной степени свойства нанотрубок зависят от хиральности, определяемой углом между осью трубки и базисным вектором графенового слоя. От этого угла зависят все свойства нанотрубки, но в первую очередь электрические (см. Модуль 3).
Свойства одностенных фуллереновых молекул и нанотрубок зависят от их диаметра и дефектности. Тщательно выращенные нанотрубки имеют менее одного структурного дефекта на 1012 атомов углерода. Такая степень совершенства практически недостижима для макроструктур. В очень сильной степени свойства нанотрубок зависят от хиральности, определяемой углом между осью трубки и базисным вектором графенового слоя. От этого угла зависят все свойства нанотрубки, но в первую очередь электрические (см. Модуль 3).
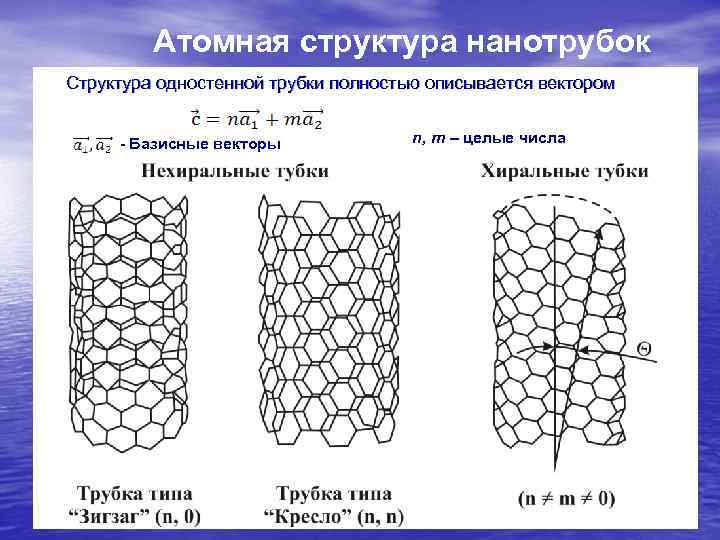 Атомная структура нанотрубок Структура одностенной трубки полностью описывается вектором - Базисные векторы n, m – целые числа
Атомная структура нанотрубок Структура одностенной трубки полностью описывается вектором - Базисные векторы n, m – целые числа
 На слайде изображена структура нанотрубок двух особых конфигураций: типа «зигзаг» и «кресло» , а также структура трубки с промежуточной хиральностью.
На слайде изображена структура нанотрубок двух особых конфигураций: типа «зигзаг» и «кресло» , а также структура трубки с промежуточной хиральностью.
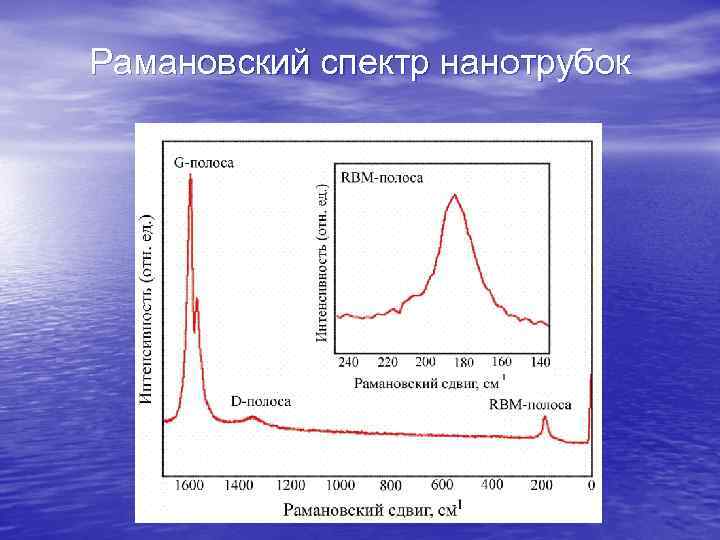 Рамановский спектр нанотрубок
Рамановский спектр нанотрубок
 Помимо высокоразрешающей электронной микроскопии атомную структуру нанотрубок можно установить и по спектрам комбинационного рассеяния (в другой терминологии – рамановская спектроскопия). Она чувствительна к частотам атомных колебаний в молекуле и позволяет выявить симметрию, определить расстояния и углы между связями. Более подробно о рамановской спектроскопии см. Модуль 7.
Помимо высокоразрешающей электронной микроскопии атомную структуру нанотрубок можно установить и по спектрам комбинационного рассеяния (в другой терминологии – рамановская спектроскопия). Она чувствительна к частотам атомных колебаний в молекуле и позволяет выявить симметрию, определить расстояния и углы между связями. Более подробно о рамановской спектроскопии см. Модуль 7.
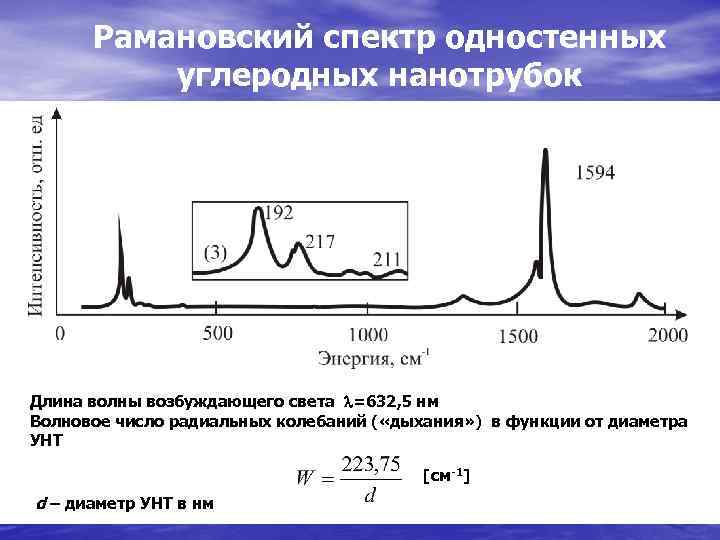 Рамановский спектр одностенных углеродных нанотрубок Длина волны возбуждающего света =632, 5 нм Волновое число радиальных колебаний ( «дыхания» ) в функции от диаметра УНТ [см-1] d – диаметр УНТ в нм
Рамановский спектр одностенных углеродных нанотрубок Длина волны возбуждающего света =632, 5 нм Волновое число радиальных колебаний ( «дыхания» ) в функции от диаметра УНТ [см-1] d – диаметр УНТ в нм



 Контрольные вопросы для самопроверки • От чего зависит агрегатное (фазовое) • • • состояние данного вещества ? Какие типы связи между атомами Вы знаете ? Какова их природа ? Почему при конденсации атомов/молекул они стремятся образовать упорядоченные структуры (в частности, кристаллические) ? Что такое гомогенное и гетерогенное зарождение новой фазы?
Контрольные вопросы для самопроверки • От чего зависит агрегатное (фазовое) • • • состояние данного вещества ? Какие типы связи между атомами Вы знаете ? Какова их природа ? Почему при конденсации атомов/молекул они стремятся образовать упорядоченные структуры (в частности, кристаллические) ? Что такое гомогенное и гетерогенное зарождение новой фазы?
 Продолжение… • Какие типы идеальной кристаллической • • • решетки Вы знаете (14 решеток Бравэ) ? Охарактеризуйте возможные уровни порядка в высокомолекулярных соединениях Чем может отличаться атомная структура макро и нано кристалла? На какие свойства может повлиять изменение атомной структуры наночастиц ?
Продолжение… • Какие типы идеальной кристаллической • • • решетки Вы знаете (14 решеток Бравэ) ? Охарактеризуйте возможные уровни порядка в высокомолекулярных соединениях Чем может отличаться атомная структура макро и нано кристалла? На какие свойства может повлиять изменение атомной структуры наночастиц ?
 Продолжение… • В чем суть дифракционных методов • • • исследования атомной структуры ? Какие частицы используют для зондирования в ва? Равновесные и неравновесные, собственные и примесные дефекты структуры Какие типы (по размерности) атомных дефектов кристаллов Вы знаете? Какую роль играют дефекты структуры в формировании физико химических свойств кристалла?
Продолжение… • В чем суть дифракционных методов • • • исследования атомной структуры ? Какие частицы используют для зондирования в ва? Равновесные и неравновесные, собственные и примесные дефекты структуры Какие типы (по размерности) атомных дефектов кристаллов Вы знаете? Какую роль играют дефекты структуры в формировании физико химических свойств кристалла?
 Продолжение… • Охарактеризуйте 4 класса наноуглеродных • • • структур, исходя из их размерности (0, 1, 2, 3) Какие типы связей атомов углерода Вы знаете ? Решеточные и электронные свойства наноуглеродных структур Каковы потенциальные области применения наноуглеродных материалов?
Продолжение… • Охарактеризуйте 4 класса наноуглеродных • • • структур, исходя из их размерности (0, 1, 2, 3) Какие типы связей атомов углерода Вы знаете ? Решеточные и электронные свойства наноуглеродных структур Каковы потенциальные области применения наноуглеродных материалов?
 Список литературы 1. Ч. Пул, Ф. Оуэнс. Нанотехнологии (перевод с англ. под ред. 2. 3. 4. 5. 6. Ю. И. Головина). М. : Техносфера. 2004. 328 с. П. В. Павлов, А. Ф. Хохлов. Физика твердого тела. Нижний Новгород: Издательство Нижегородского госуниверситета. 1993. 491 с. Ч. Киттель. Введение в физику твердого тела. – М. : Мир. 1978. Э. Г. Раков. Нанотрубки и фуллерены. – М. : Университетская книга, Логос. 2006. 376 с. Фуллерены (Л. Н. Сидоров, М. А. Юровская и др. ) – М. : Экзамен. 2005. 688 с. Ю. И. Головин. Основы нанотехнологий. М. Машиностроение. 2012. 656 с.
Список литературы 1. Ч. Пул, Ф. Оуэнс. Нанотехнологии (перевод с англ. под ред. 2. 3. 4. 5. 6. Ю. И. Головина). М. : Техносфера. 2004. 328 с. П. В. Павлов, А. Ф. Хохлов. Физика твердого тела. Нижний Новгород: Издательство Нижегородского госуниверситета. 1993. 491 с. Ч. Киттель. Введение в физику твердого тела. – М. : Мир. 1978. Э. Г. Раков. Нанотрубки и фуллерены. – М. : Университетская книга, Логос. 2006. 376 с. Фуллерены (Л. Н. Сидоров, М. А. Юровская и др. ) – М. : Экзамен. 2005. 688 с. Ю. И. Головин. Основы нанотехнологий. М. Машиностроение. 2012. 656 с.
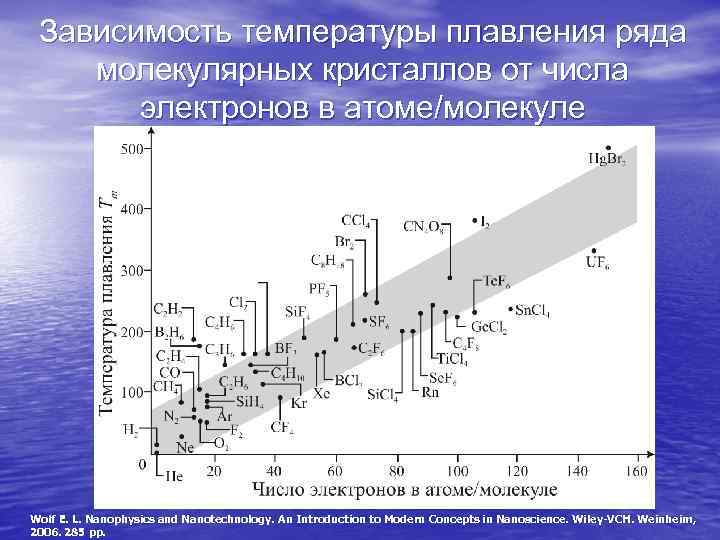 Зависимость температуры плавления ряда молекулярных кристаллов от числа электронов в атоме/молекуле Wolf E. L. Nanophysics and Nanotechnology. An Introduction to Modern Concepts in Nanoscience. Wiley-VCH. Weinheim, 2006. 285 pp.
Зависимость температуры плавления ряда молекулярных кристаллов от числа электронов в атоме/молекуле Wolf E. L. Nanophysics and Nanotechnology. An Introduction to Modern Concepts in Nanoscience. Wiley-VCH. Weinheim, 2006. 285 pp.
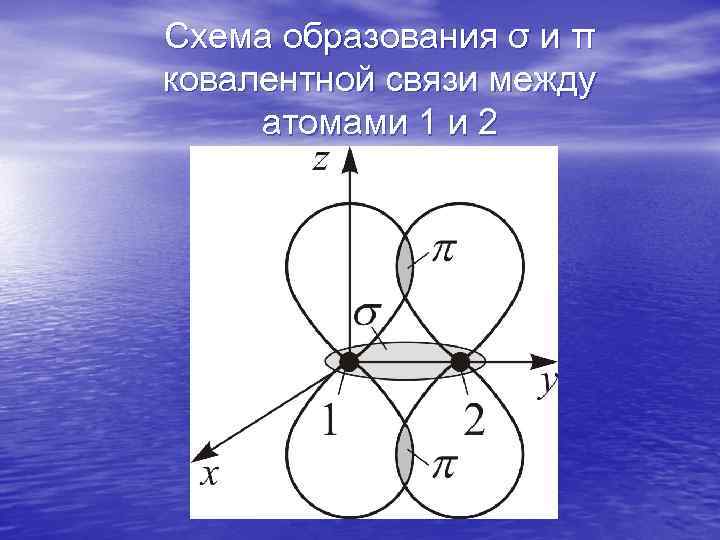 Схема образования σ и π ковалентной связи между атомами 1 и 2
Схема образования σ и π ковалентной связи между атомами 1 и 2
 Индексы Миллера и Миллера-Бравэ для некоторых направлений в базовой плоскости Готтштайн Г. Физико-химические основы материаловедения. М. : БИНОМ, 2009. 400 с.
Индексы Миллера и Миллера-Бравэ для некоторых направлений в базовой плоскости Готтштайн Г. Физико-химические основы материаловедения. М. : БИНОМ, 2009. 400 с.
 Схема построения стереографической проекции E – кристаллографическая плоскость, P – точка пересечения нормали к плоскости E со сферой. a и b - углы, характеризующие положение точки Р на сфере, Р’ – полюс плоскости E в стереографической проекции Готтштайн Г. Физико-химические основы материаловедения. М. : БИНОМ, 2009. 400 с.
Схема построения стереографической проекции E – кристаллографическая плоскость, P – точка пересечения нормали к плоскости E со сферой. a и b - углы, характеризующие положение точки Р на сфере, Р’ – полюс плоскости E в стереографической проекции Готтштайн Г. Физико-химические основы материаловедения. М. : БИНОМ, 2009. 400 с.
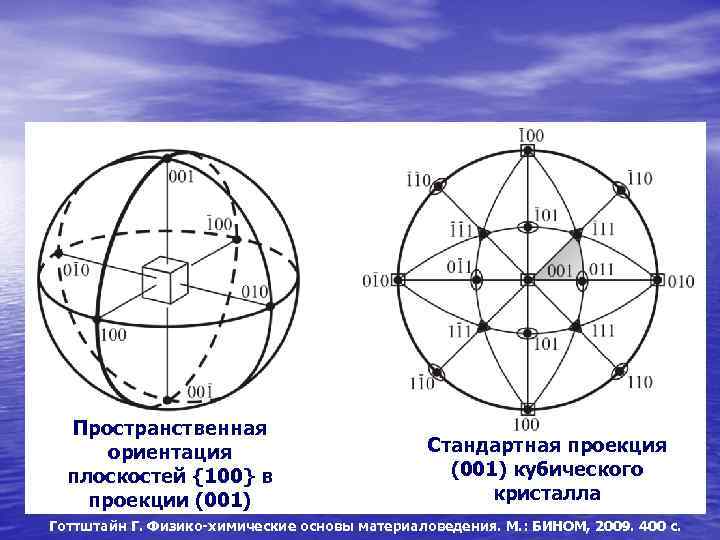 Пространственная ориентация плоскостей {100} в проекции (001) Стандартная проекция (001) кубического кристалла Готтштайн Г. Физико-химические основы материаловедения. М. : БИНОМ, 2009. 400 с.
Пространственная ориентация плоскостей {100} в проекции (001) Стандартная проекция (001) кубического кристалла Готтштайн Г. Физико-химические основы материаловедения. М. : БИНОМ, 2009. 400 с.
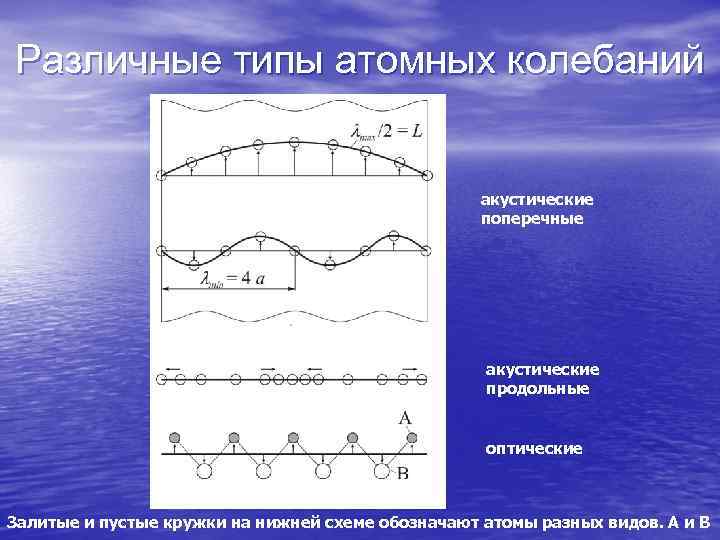 Различные типы атомных колебаний акустические поперечные акустические продольные оптические Залитые и пустые кружки на нижней схеме обозначают атомы разных видов. А и В
Различные типы атомных колебаний акустические поперечные акустические продольные оптические Залитые и пустые кружки на нижней схеме обозначают атомы разных видов. А и В
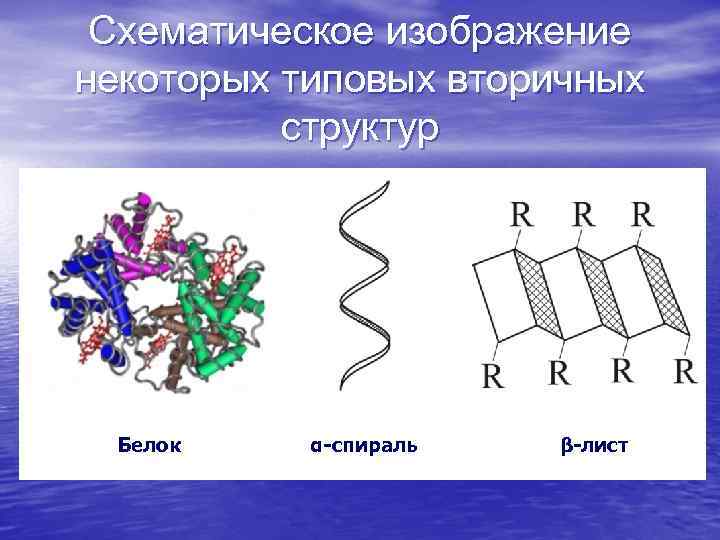 Схематическое изображение некоторых типовых вторичных структур Белок α-спираль β-лист
Схематическое изображение некоторых типовых вторичных структур Белок α-спираль β-лист
 τ – сдвиговые напряжения в жидкости, dv/dy – градиент скорости в направлении, → перпендикулярном вектору скорости потока v
τ – сдвиговые напряжения в жидкости, dv/dy – градиент скорости в направлении, → перпендикулярном вектору скорости потока v
 UD – энергия активации диффузии, n 0 – концентрация атомов в твердом теле
UD – энергия активации диффузии, n 0 – концентрация атомов в твердом теле
 Обратная решетка
Обратная решетка
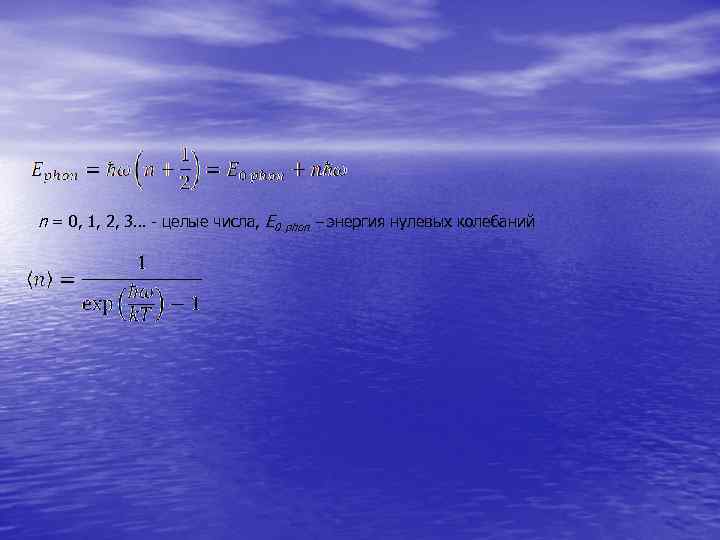 n = 0, 1, 2, 3… - целые числа, E 0 phon – энергия нулевых колебаний
n = 0, 1, 2, 3… - целые числа, E 0 phon – энергия нулевых колебаний




