19-Mo Ni Mn Со Биохимия фиксации N2 (20).ppt
- Количество слайдов: 48

Mo MOLYBDENUM/TUNGSTEN Nitrogenase Xanthine oxidase Aldehyde Oxidoreductase (MOP) Dimethylsulfoxide Reductase Trimethylamine N-Oxide Reductase Dissimilatory Nitrate Reductase Formaldehyde Ferredoxin Oxidoreductase Aldehyde Ferredoxin Oxidoreductase Formate Dehydrogenase H Sulfite Oxidase CO Dehydrogenase Handbook of Metalloproteins

Mo Молибденсодержащие ферменты
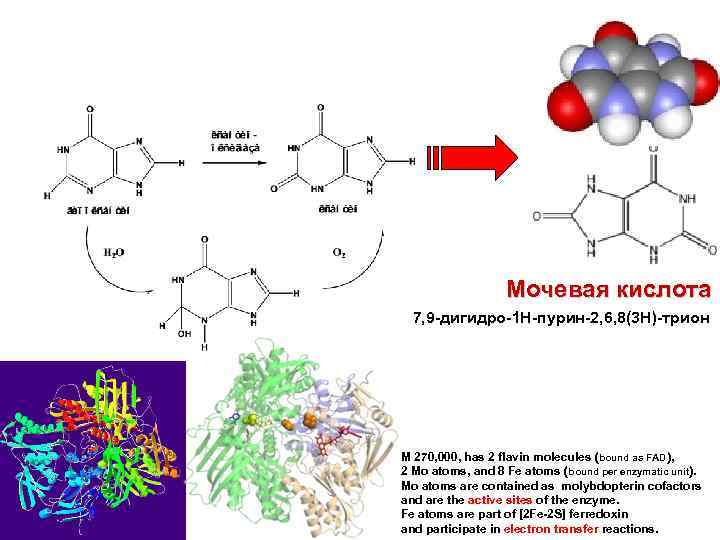
Мочевая кислота 7, 9 -дигидро-1 H-пурин-2, 6, 8(3 H)-трион M 270, 000, has 2 flavin molecules (bound as FAD), 2 Mo atoms, and 8 Fe atoms (bound per enzymatic unit). Mo atoms are contained as molybdopterin cofactors and are the active sites of the enzyme. Fe atoms are part of [2 Fe-2 S] ferredoxin and participate in electron transfer reactions.

Биохимия фиксации атмосферного азота

Фиксация азота N 2 + H 2 → NH 3 G 0’ = - 19 ккал/моль N ≡ N 225 ккал/моль Условия в промышленности: 400 атм, 450 ºC Бактерии, фиксирующие азот, содержат нитрогеназу Условия: 1 атм, комнатная температура Streptomyces thermoautotrophicus опт. темп. 65 ºC
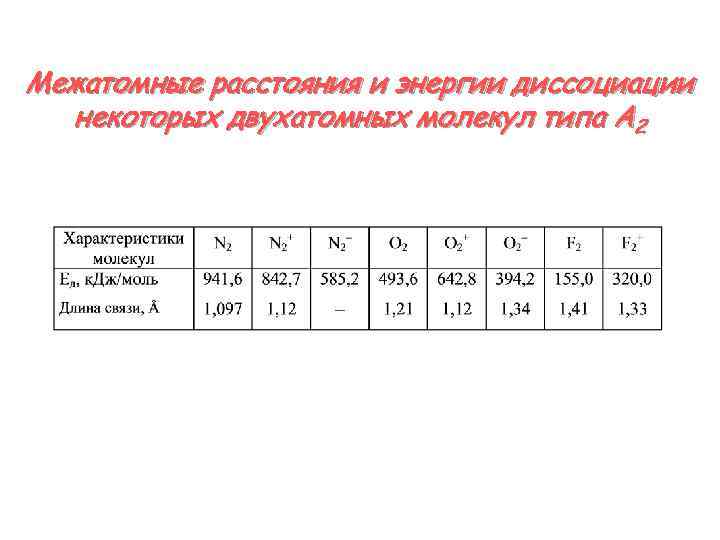
Межатомные расстояния и энергии диссоциации некоторых двухатомных молекул типа A 2
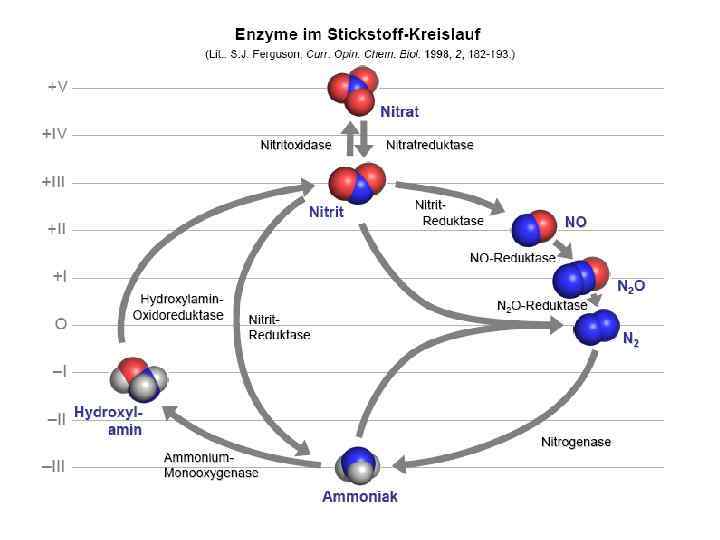
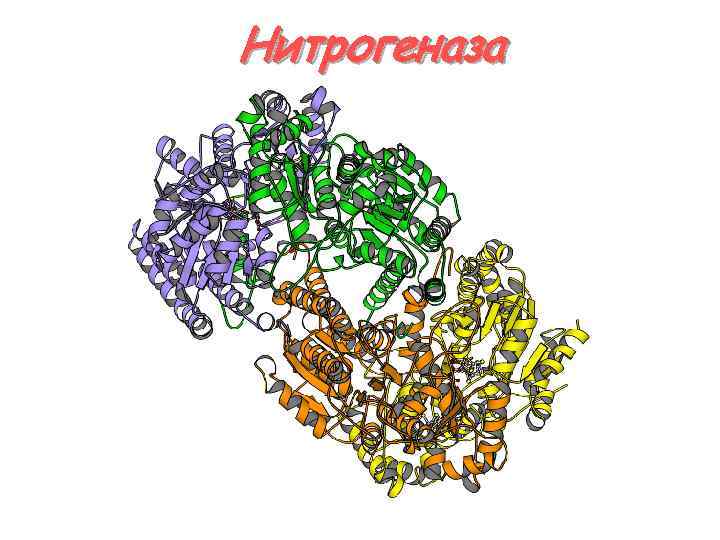
Нитрогеназа
Нитрогеназа
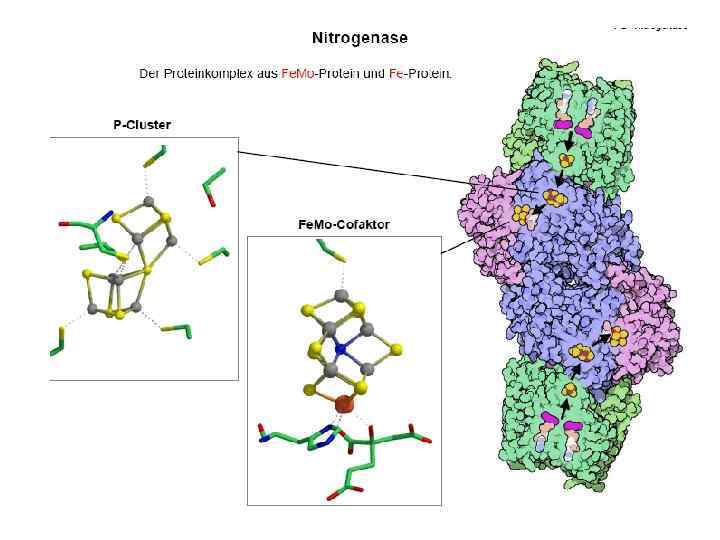
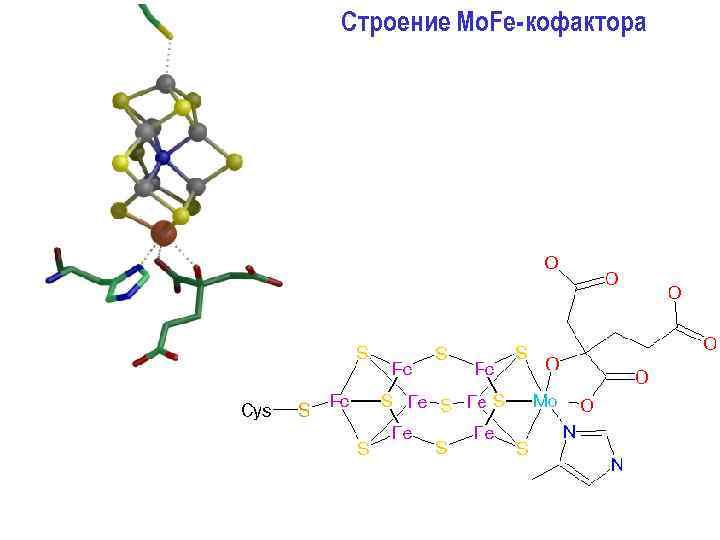
Строение Mo. Fe-кофактора
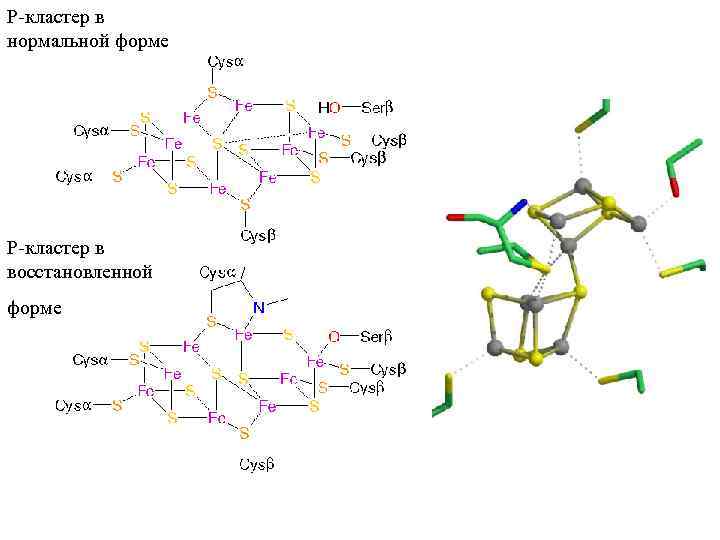
P-кластер в нормальной форме P-кластер в восстановленной форме
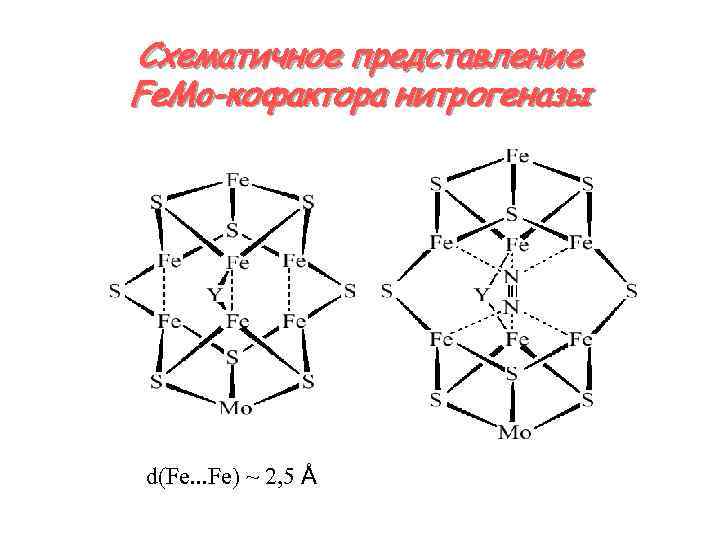
Схематичное представление Fe. Mo-кофактора нитрогеназы d(Fe. . . Fe) ~ 2, 5 Å
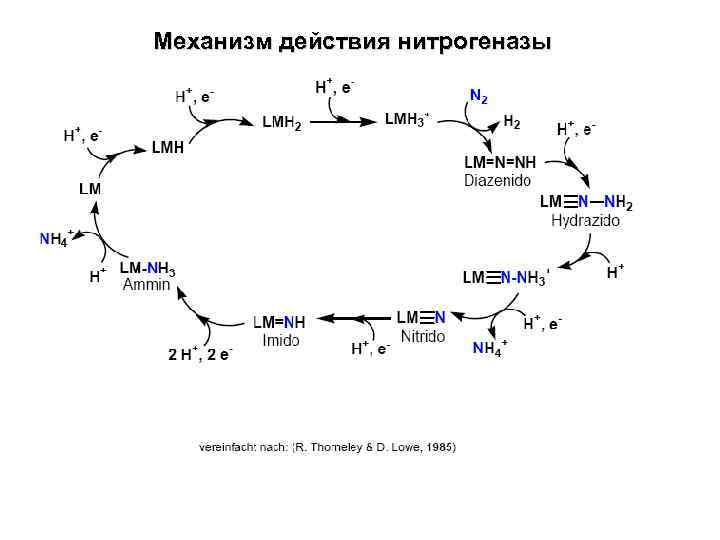
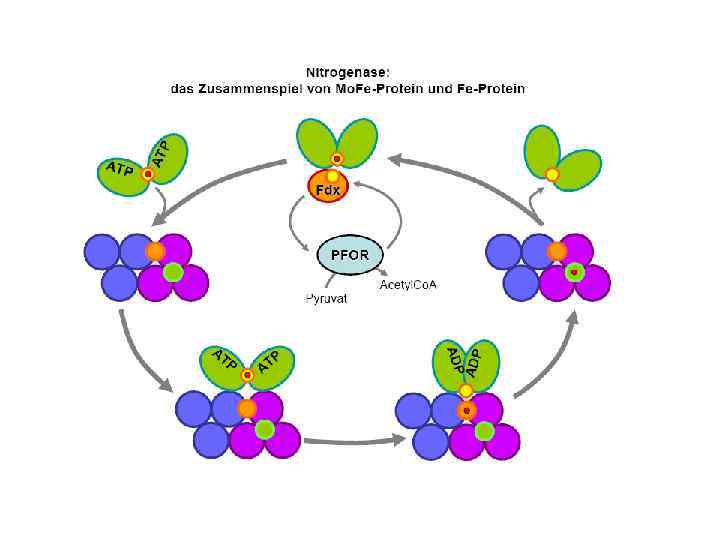
Механизм действия нитрогеназы

Процесс восстановления молекулярного азота на молибденсодержащей нитрогеназе: • восстановление Fe-белка донорами электронов • перенос электронов с восстановленного Fe-белка на Mo. Fe-белок • перенос электронов на молекулу N 2 + 8 e + 8 H+ + 16 Mg. АТФ 2 NH 3 + H 2 + 16 Mg. АДФ+ 16 PO 43 -

Восстановление разнообразных субстратов нитрогеназой

12 International Conference on Bioinorganic Chemistry (ICBIC-12) Newton, W. E. Some Insights into How Nitrogenase Works Menck, E. Mossbauer and EPR Studies of Nitrogenase Holm, R. H. Chemical Approaches to Complex Heterometalsulfur Sites in Biology Pickett, C. Interactions of small molecules at isolated Fe. Moco : relic chemistry of an ancient enzyme ? Seefeldt, L. Insights Into the Nitrogenase Mechanism Hoffman, B. EPR and ENDOR Characterization of Nitrogenase Enzymatic Intermediates

Ni NICKEL Urease Nickel-Iron Hydrogenases Methyl-Coenzyme M Reductase Peptide Deformylase Diphtheria Toxin Repressor: Metal Ion Mediated Control Of Transcription Handbook of Metalloproteins

Ni Никельсодержащие ферменты Оксид углерода дегидрогеназа Carbon-monoxide dehydrogenase Кофактор F 420 гидрогеназа Coenzyme F 420 hydrogenase Цитохром с3 гидрогеназа Cytochrome-c 3 hydrogenase Ферредоксин гидрогеназа Ferredoxin hydrogenase Уреаза Urease
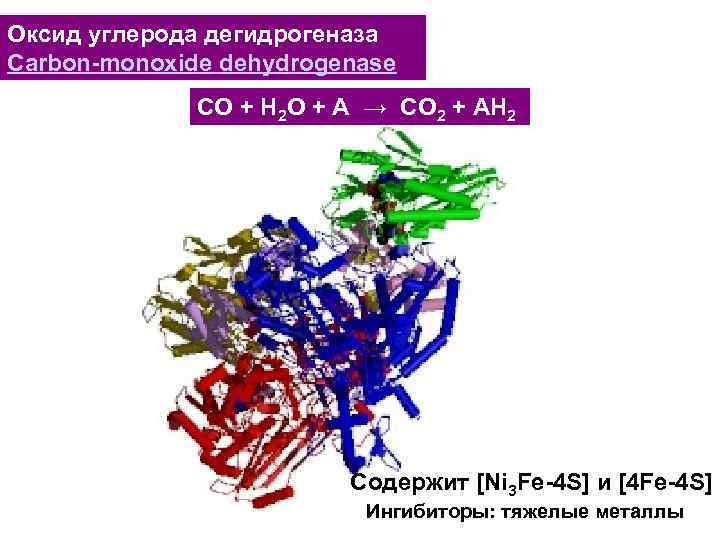
Оксид углерода дегидрогеназа Carbon-monoxide dehydrogenase CO + H 2 O + A → CO 2 + AH 2 Содержит [Ni 3 Fe-4 S] и [4 Fe-4 S] Ингибиторы: тяжелые металлы
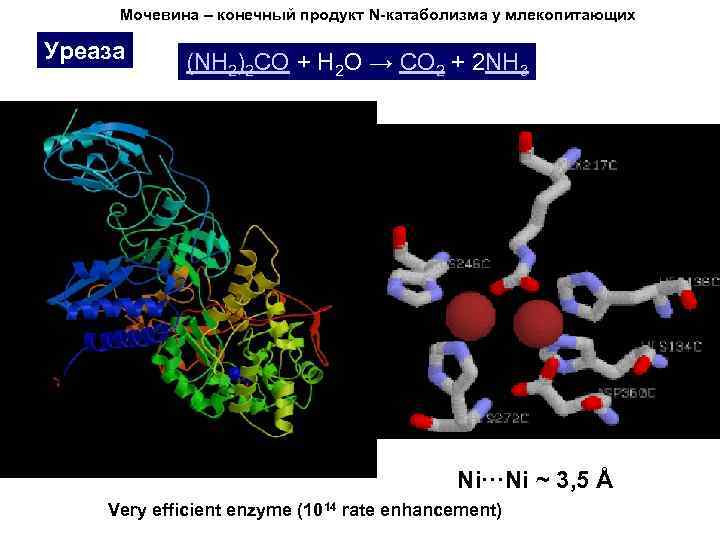
Мочевина – конечный продукт N-катаболизма у млекопитающих Уреаза (NH 2)2 CO + H 2 O → CO 2 + 2 NH 3 Ni···Ni ~ 3, 5 Å Very efficient enzyme (1014 rate enhancement)
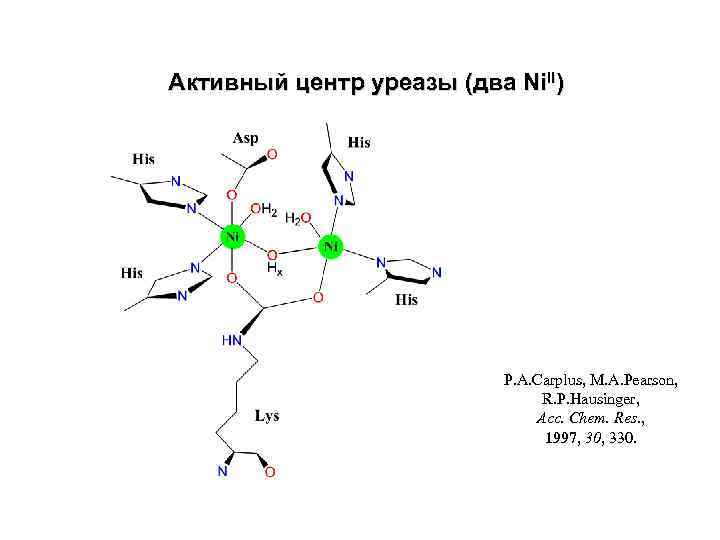
Активный центр уреазы (два Ni. II) P. A. Carplus, M. A. Pearson, R. P. Hausinger, Acc. Chem. Res. , 1997, 30, 330.

Предложенный механизм действия уреазы
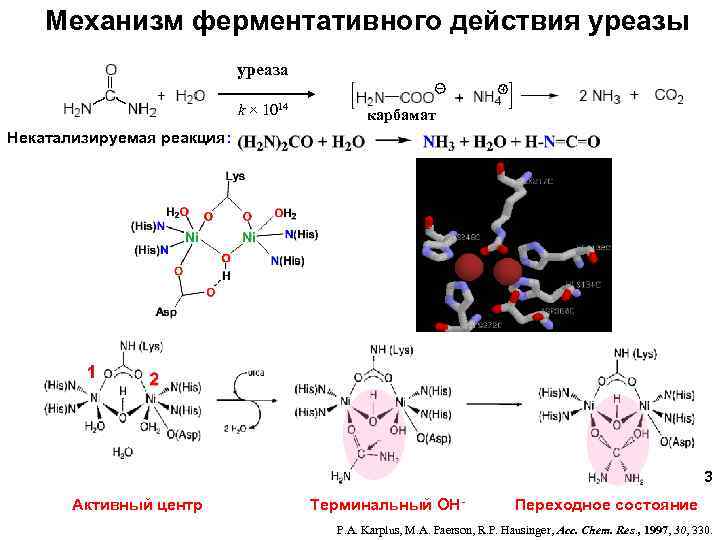
Механизм ферментативного действия уреазы уреаза k × 1014 карбамат Некатализируемая реакция: 3 Активный центр Терминальный OH- Переходное состояние P. A. Karplus, M. A. Paerson, R. P. Hausinger, Acc. Chem. Res. , 1997, 30, 330.
![Синтетические модели активного центра уреазы [Ni 2(OAc)3(tmen)2(urea)]+ [Ni 2(L)(OAc)(Me. OH)2(urea)]0 H. E. Wages, K. Синтетические модели активного центра уреазы [Ni 2(OAc)3(tmen)2(urea)]+ [Ni 2(L)(OAc)(Me. OH)2(urea)]0 H. E. Wages, K.](https://present5.com/presentation/3397782_226162588/image-26.jpg)
Синтетические модели активного центра уреазы [Ni 2(OAc)3(tmen)2(urea)]+ [Ni 2(L)(OAc)(Me. OH)2(urea)]0 H. E. Wages, K. L. Taft, S. J. Lippard, Inorg. Chem. , 1993, 32, 4985. S. Mukherjee, T. Weyhermuller, E. Bothe, K. Wieghardt, P. Chaudhuri, Eur. J. Inorg. Chem. , 2003, 863. Комплексы с координацией Ni-O(C=O уреазы)
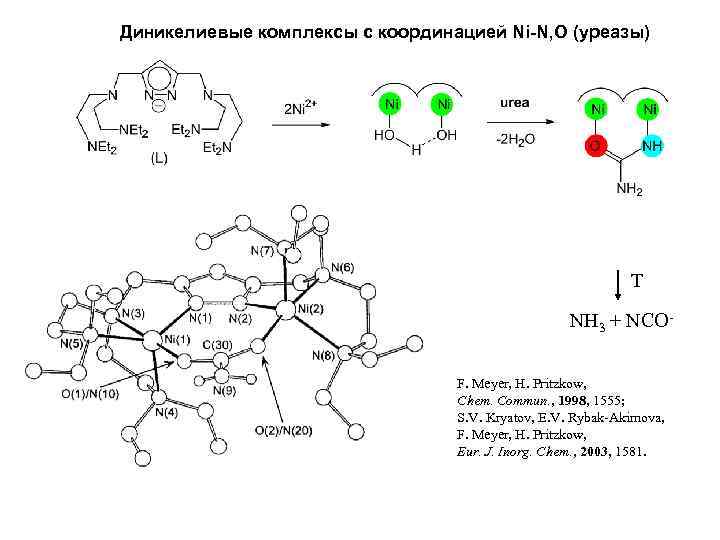
Диникелиевые комплексы с координацией Ni-N, O (уреазы) T NH 3 + NCOF. Meyer, H. Pritzkow, Chem. Commun. , 1998, 1555; S. V. Kryatov, E. V. Rybak-Akimova, F. Meyer, H. Pritzkow, Eur. J. Inorg. Chem. , 2003, 1581.
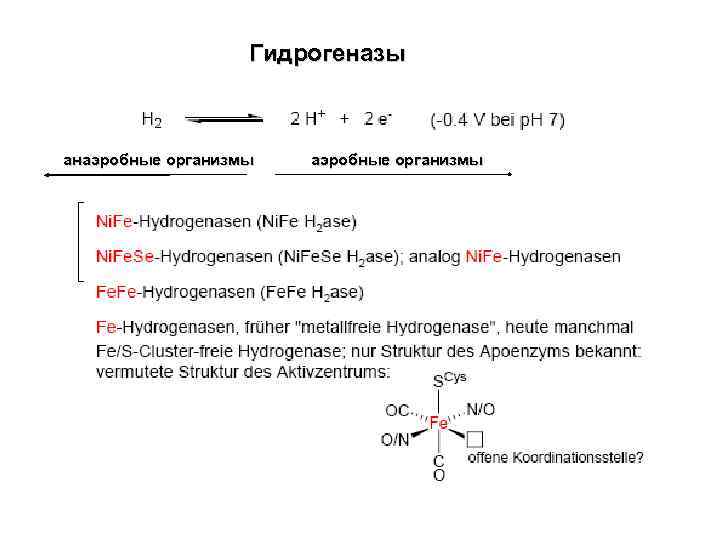
Гидрогеназы анаэробные организмы
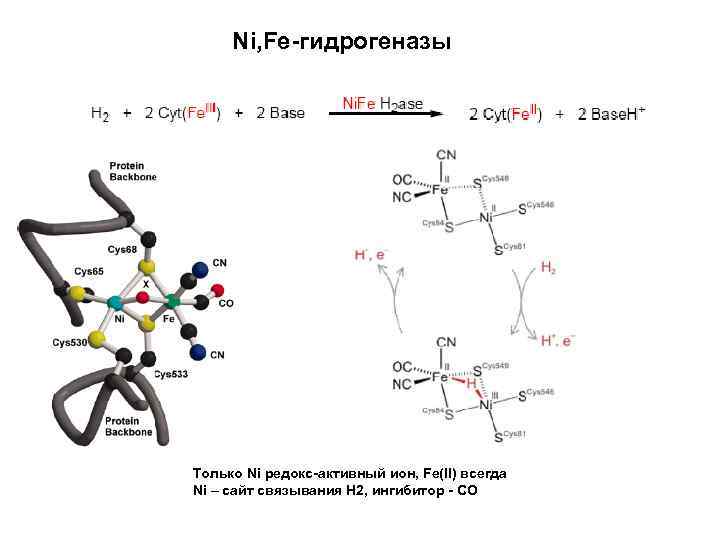
Ni, Fe-гидрогеназы Только Ni редокс-активный ион, Fe(II) всегда Ni – сайт связывания Н 2, ингибитор - СО

Синтетические модели активного центра гидрогеназы

Mn MANGANESE Urease Manganese Superoxide Dismutase Arginase Concanavalin A Aminopeptidase P Handbook of Metalloproteins

Mn Марганецсодержащие ферменты Супероксид дисмутаза Superoxide dismutase (SOD) Аргиназа Arginase

Mn Марганецсодержащие ферменты Супероксид дисмутаза Superoxide dismutase (SOD) M(n+1)+ − SOD + O 2− • → Mn+ − SOD + O 2− • + 2 H+ → M(n+1)+ − SOD + H 2 O 2 M = Cu (n=1) ; Mn (n=2) ; Fe (n=2) ; Ni (n=2)
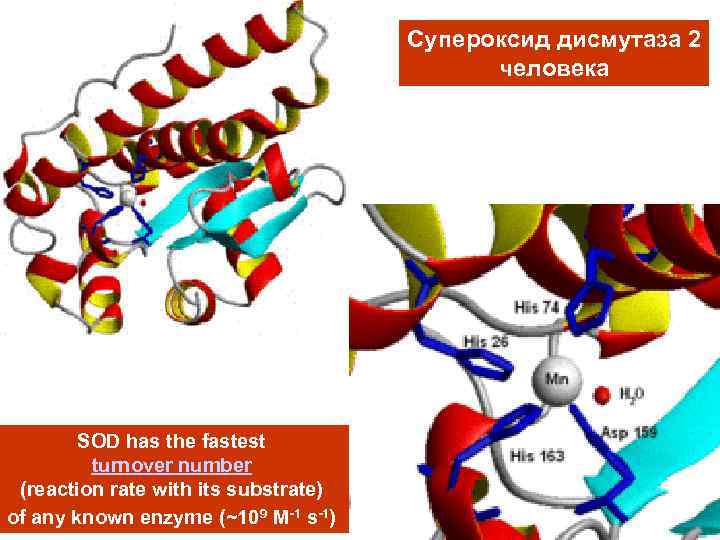
Супероксид дисмутаза 2 человека SOD has the fastest turnover number (reaction rate with its substrate) of any known enzyme (~109 M-1 s-1)
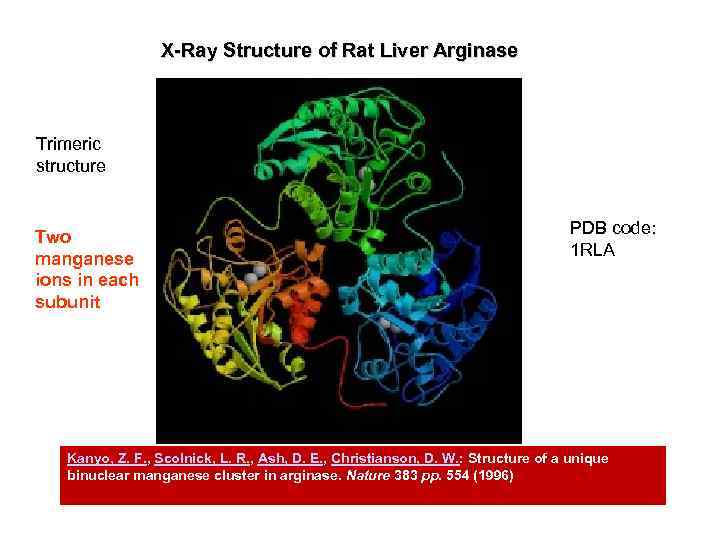
X-Ray Structure of Rat Liver Arginase Trimeric structure Two manganese ions in each subunit PDB code: 1 RLA Kanyo, Z. F. , Scolnick, L. R. , Ash, D. E. , Christianson, D. W. : Structure of a unique binuclear manganese cluster in arginase. Nature 383 pp. 554 (1996)
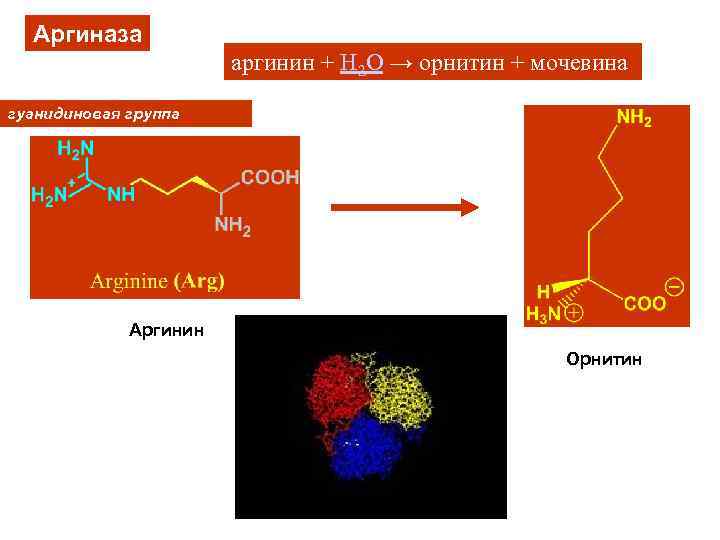
Аргиназа аргинин + H 2 O → орнитин + мочевина гуанидиновая группа Аргинин Орнитин
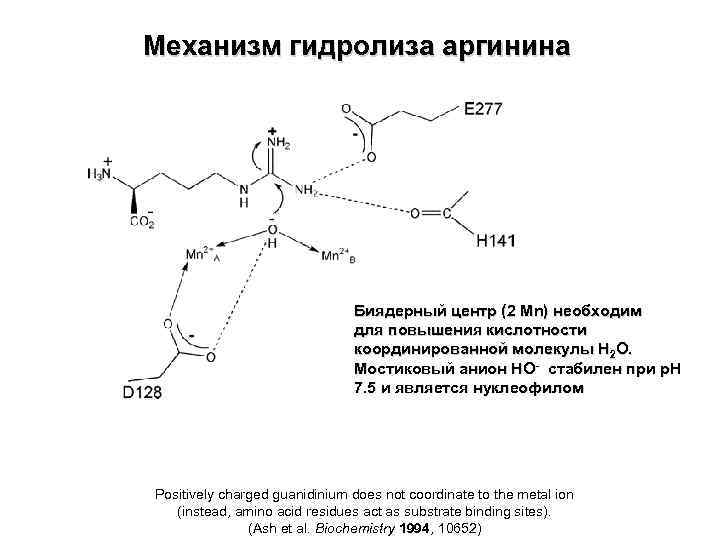
Механизм гидролиза аргинина Биядерный центр (2 Mn) необходим для повышения кислотности координированной молекулы Н 2 О. Мостиковый анион HO- стабилен при p. H 7. 5 и является нуклеофилом Positively charged guanidinium does not coordinate to the metal ion (instead, amino acid residues act as substrate binding sites). (Ash et al. Biochemistry 1994, 10652)
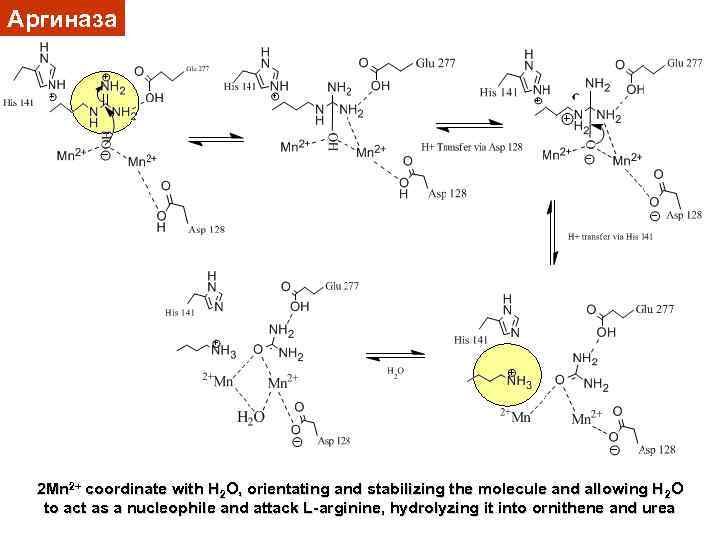
Аргиназа 2 Mn 2+ coordinate with H 2 O, orientating and stabilizing the molecule and allowing H 2 O to act as a nucleophile and attack L-arginine, hydrolyzing it into ornithene and urea
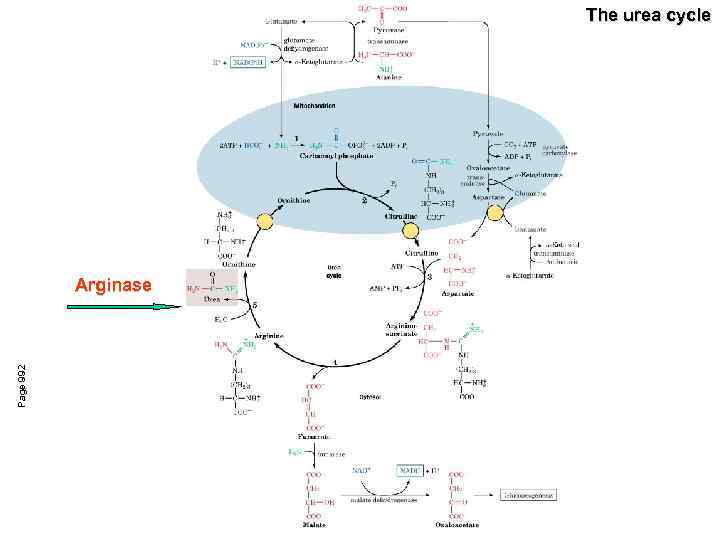
The urea cycle Page 992 Arginase
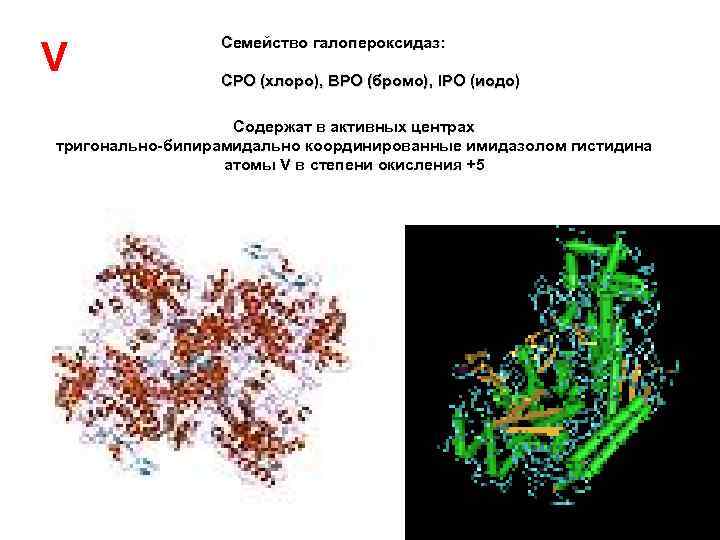
V Семейство галопероксидаз: CPO (хлоро), BPO (бромо), IPO (иодо) Содержат в активных центрах тригонально-бипирамидально координированные имидазолом гистидина атомы V в степени окисления +5
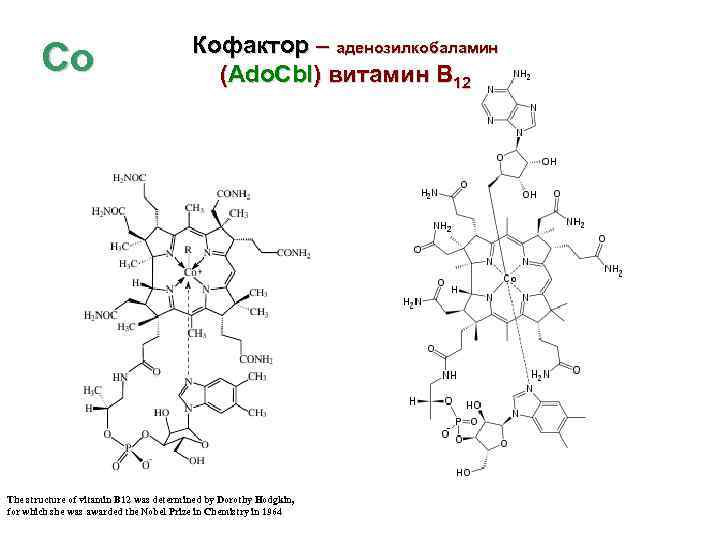
Со Кофактор – аденозилкобаламин (Ado. Cbl) витамин В 12 The structure of vitamin B 12 was determined by Dorothy Hodgkin, for which she was awarded the Nobel Prize in Chemistry in 1964
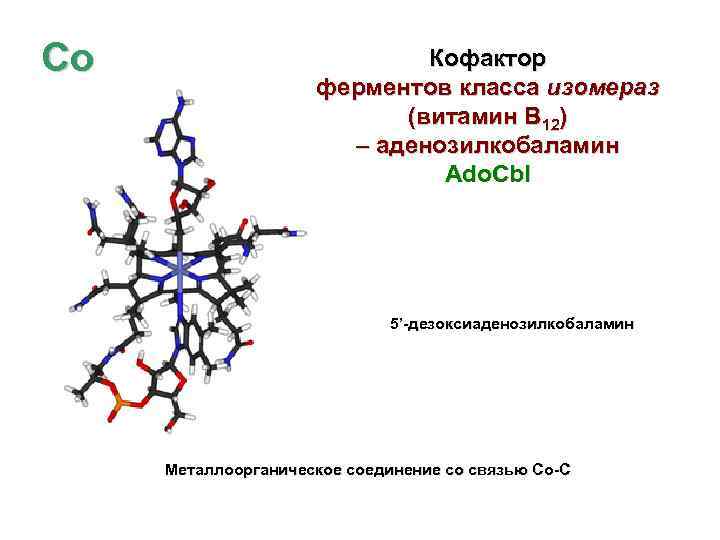
Co Кофактор ферментов класса изомераз (витамин В 12) – аденозилкобаламин Ado. Cbl 5’-дезоксиаденозилкобаламин Металлоорганическое соединение со связью Со-С


UREASE • Catalyzes urea hydrolysis • Very efficient enzyme (1014 rate enhancement) • The first enzyme to be crystallized; retained catalytic activity (Sumner, 1925). Conclusion: enzymes are proteins The first enzyme shown to contain and require nickel (Zerner, 1975)
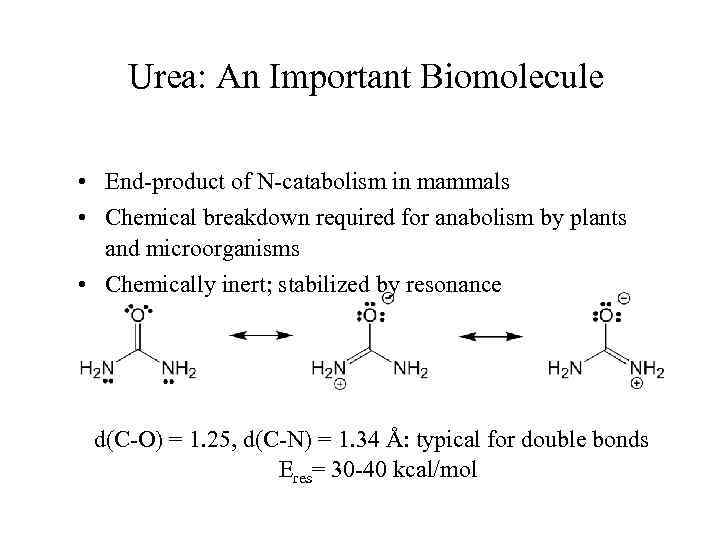
Urea: An Important Biomolecule • End-product of N-catabolism in mammals • Chemical breakdown required for anabolism by plants and microorganisms • Chemically inert; stabilized by resonance d(C-O) = 1. 25, d(C-N) = 1. 34 Å: typical for double bonds Eres= 30 -40 kcal/mol

Urease: A Dinuclear Enzyme • Enzymatic reaction: (NH 2)2 CO + H 2 O NH 2 COO– + NH 4+ (KM~10 -3 M; kcat~103 s-1) • Non-catalyzed reaction: (NH 2)2 CO NCO– + NH 4+ (knon ~ 10 -8 s-1) • Enzyme proficiency: (kcat/KM)/knon ~ 1014
![Urea Transformation at a Dinickel Site T [Ni 2(bdptz)(OH)(urea)2(Me. CN)]+ A. M. Barrios, S. Urea Transformation at a Dinickel Site T [Ni 2(bdptz)(OH)(urea)2(Me. CN)]+ A. M. Barrios, S.](https://present5.com/presentation/3397782_226162588/image-47.jpg)
Urea Transformation at a Dinickel Site T [Ni 2(bdptz)(OH)(urea)2(Me. CN)]+ A. M. Barrios, S. J. Lippard, J. Am. Chem. Soc. , 2000, 122, 9172. NH 4 NCO
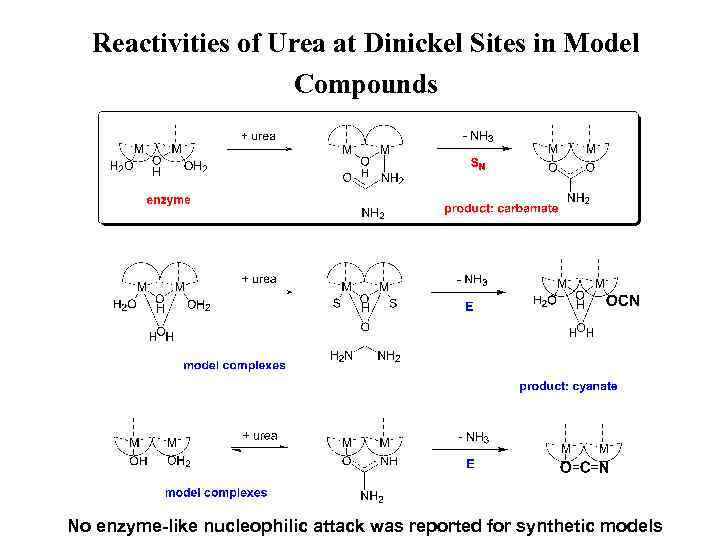
Reactivities of Urea at Dinickel Sites in Model Compounds No enzyme-like nucleophilic attack was reported for synthetic models
19-Mo Ni Mn Со Биохимия фиксации N2 (20).ppt