Митохондриальные заболевания. ГУ МГНЦ РАМН, Москва


Митохондриальные заболевания. ГУ МГНЦ РАМН, Москва
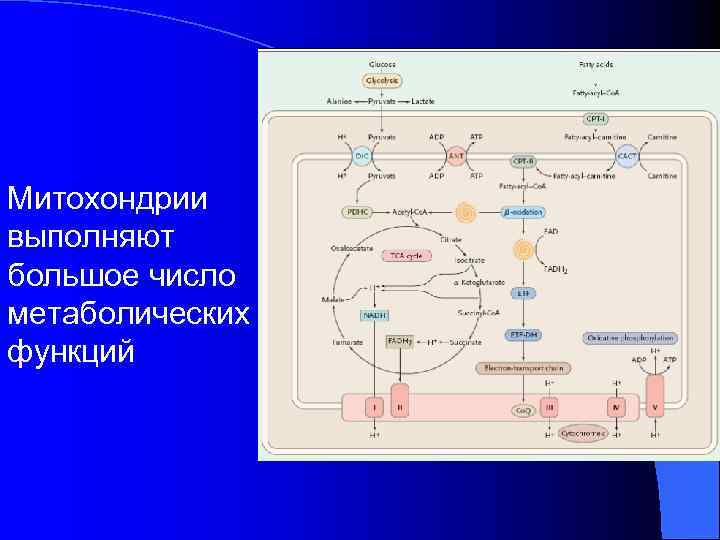
Митохондрии выполняют большое число метаболических функций
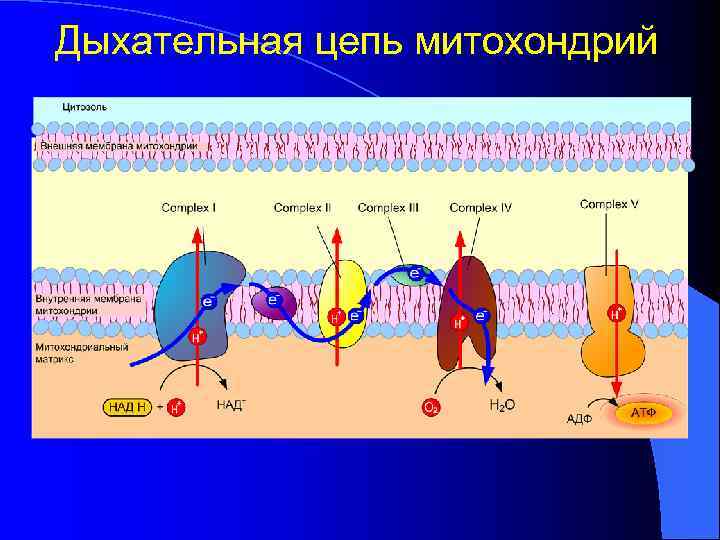
Дыхательная цепь митохондрий

l Митохондриальные заболевания – гетерогенная группа наследственных болезней, обусловленных нарушениями в дыхательной цепи митохондрий
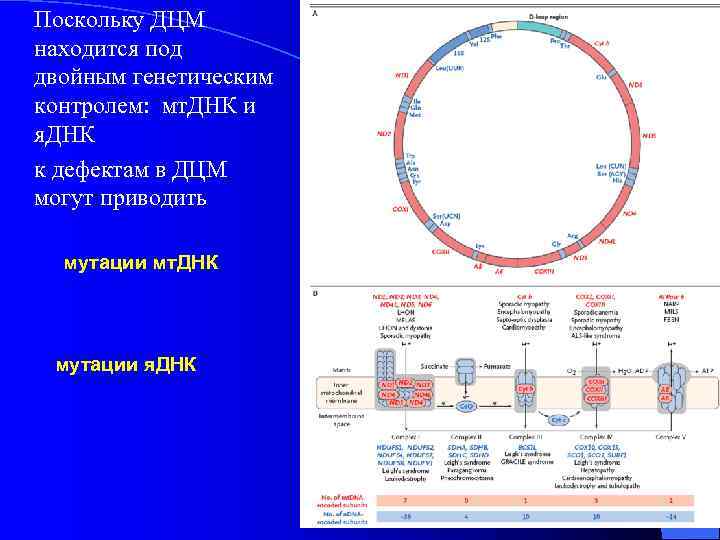
Поскольку ДЦМ находится под двойным генетическим контролем: мт. ДНК и я. ДНК к дефектам в ДЦМ могут приводить мутации мт. ДНК мутации я. ДНК

Классификация митоходриальных болезней Обусловленные мутациями мт. ДНК l Точковые мутации (синдромы LHON, NARP, Ли, MERRF, MELAS, ММС) l Крупные перестройки (синдромы КSS, CPEO, Пирсона) Обусловленные мутациями я. ДНК l Мутации генов, кодирующих КДЦМ и белки, необходимые для их сборки (синдром Ли) l Мутации ядерных генов, вызывающих мутации в мт. ДНК (синдром СPEO/СPEO , болезнь Альперса)

Наследование МБ l МБ могут наследоваться по любому типу (х-сцепленному, АД, АР), в том числе и по цитоплазматическому

МБ обусловленные мутациями мт. ДНК l LHON (атрофия зрительных нервов Лебера) l MELAS (митохондриальная энцефалопатия, лактат-ацидоз, инсультоподобные состояния) l MERRF (миоклонус-эпилепсия, наличие рваных красных волокон в мышечном биоптате) l KSS (синдром Кернс-Сейера) l CPEO (прогрессирующая наружная офтальмоплегия)

Митохондриальная ДНК человека

Особенности митохондриальной ДНК 1. Представляет собой кольцевую молекулу, размером 16569 п. н. , в которой отсутствуют интроны. 2. Наследуется через цитоплазму яйцеклетки. 3. В каждой клетке содержится несколько сотен копий мт. ДНК (за исключением половых клеток) 4. Генетический код отличается от универсального кода я. ДНК 5. Скорость мутаций мт. ДНК ~ в 10 раз выше чем я. ДНК.
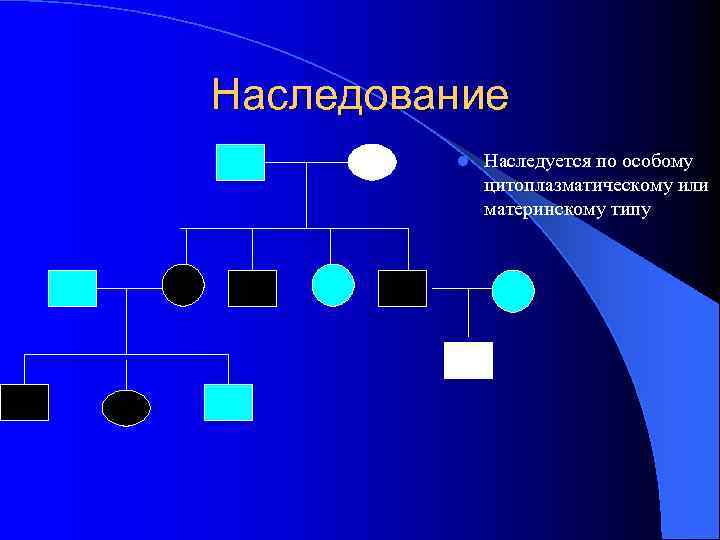
Наследование l Наследуется по особому цитоплазматическому или материнскому типу

Феномен гетероплазмии l Присутствие мутантых и нормальных молекул мт. ДНК в одной клетке или тканях Следствия: l Клиническая картина зависит от процента мутантных молекул в тканях. Чем больше, тем, как правило, тяжелее клинические проявления болезни l Внутрисемейный полиморфизм. В одной родословной могут встречаться пациенты как с тяжелыми так и с легкими проявлениями заболевания

Неравномерное распределение мутантной мт. ДНК l В разных тканях процент мутантной мт. ДНК может быть от 0 -100% Следствия l Клинические проявления зависят от того в каких тканях и в каком проценте присутствует мутантная мт. ДНК l Внутрисемейный полиморфизм. В одной родословной могут встречаться пациенты с поражением разных систем и органов

Клинические проявления МБ l МБ могут манифестировать в любом возрасте, дебютировать с поражения любой системы органов и в любом сочетании l Чаще поражаются органы и ткани наиболее зависимые от энергии окислительного фосфорилирования (скелетная и сердечная мыш. ткань, нервная, эндокринная) Необычное сочетание мультиорганной патологии помогает заподозрить заболевания из этой группы НБ.

Синдром LHON (атрофия зрительных нервов Лебера) Возраст начала заболевания от 12 до 30 л. острая или подострая безболезненная потеря центрального зрения, вызванная тяжелой, обычно билатеральной атрофией зрительного нерва
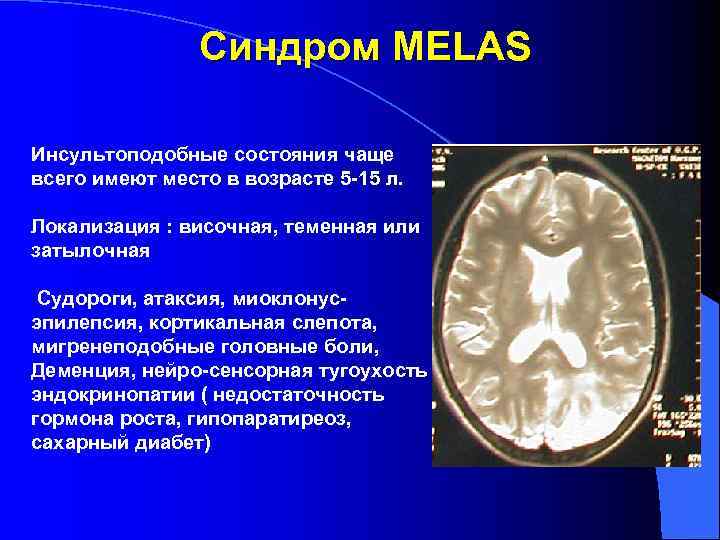
Синдром MELAS Инсультоподобные состояния чаще всего имеют место в возрасте 5 -15 л. Локализация : височная, теменная или затылочная Судороги, атаксия, миоклонус- эпилепсия, кортикальная слепота, мигренеподобные головные боли, Деменция, нейро-сенсорная тугоухость эндокринопатии ( недостаточность гормона роста, гипопаратиреоз, сахарный диабет)

Синдром KSS 1) манифестация до 20 л. ; 2) прогрессирующая наружная офтальмоплегия; 3) пигментная дегенерация сетчатки. - «соль и перец» или пестрая сетчатка -образованием «костных телец» в сочетании с атрофией зрительных нервов, -генерализованная утрата пигментного эпителия сетчатки l Дополнительные симптомы: l высокое содержание белка в ЦСЖ, l блокада сердечной проводимости l мозжечковая симптоматика в виде атаксии, дизартрии l деменция, нейросенсорная тугоухость l эндокринопатии ( недостаточность гормона роста, гипопаратиреоз, сахарный диабет)

МБ, обусловленные мутациями я. ДНК Мутации ~20 различных ядерных генов могут приводить к нарушениями ДЦМ: • Мутации генов, кодирующих КДЦМ • Мутации генов, кодирующих белки, необходимые для сборки КДЦМ • Мутации ядерных генов, вызывающих мутации в мт. ДНК (делеции и истощение)

Синдром Ли (болезнь Ли, подострая некротизирующая энцефаломиелопатия Ли) MIM 256000 l Впервые описан в 1951 г (Denis Leigh) l Самое частое заболевание из группы митохондриальных болезней, манифестирующее в раннем детском возрасте l Мутации, по крайней мере, 15 разных генов могут приводить к заболеванию

Клинические проявления l Возраст дебюта 1 -5 лет l Нарушение психомоторного развития l Мышечная гипотония l Бульбарные нарушения l Нарушение ритма дыхания l Офтальмопарез l Нистагм l Атрофия зрительных нервов l Атаксия l Изменение МР-сигнала в подкорковых образованиях головного мозга
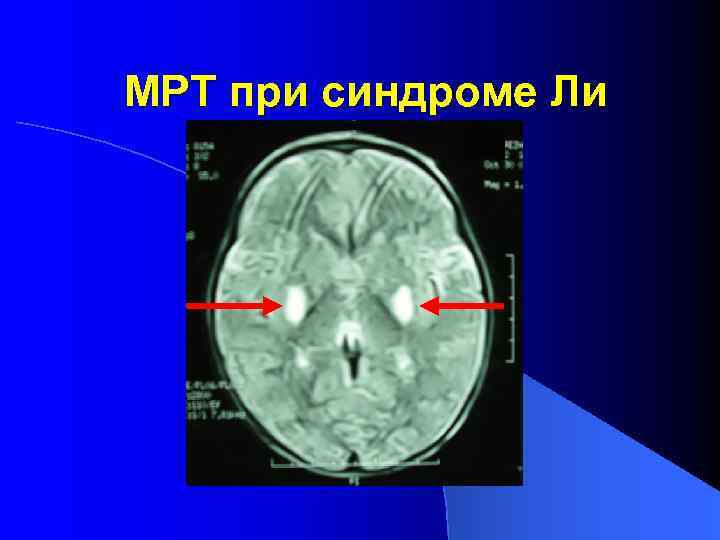
МРТ при синдроме Ли

Диагностика МБ Определение окислительно-восстановительного статуса клетки А. определение концентрации лактата, пирувата и кетоновых тел в крови до после пищевой нагрузки определение концентрации лактата, пирувата и кетоновых тел в крови после нагрузки глюкозой определение концентрации лактата в ЦСЖ Морфологическое исследование мышечного биоптата А. «Рваные красные волокна» Гистохимическое определение ферментов Определение активности ферментов ДНК-диагностика А. Анализ мутаций мт. ДНК Анализ мутаций я. ДНК
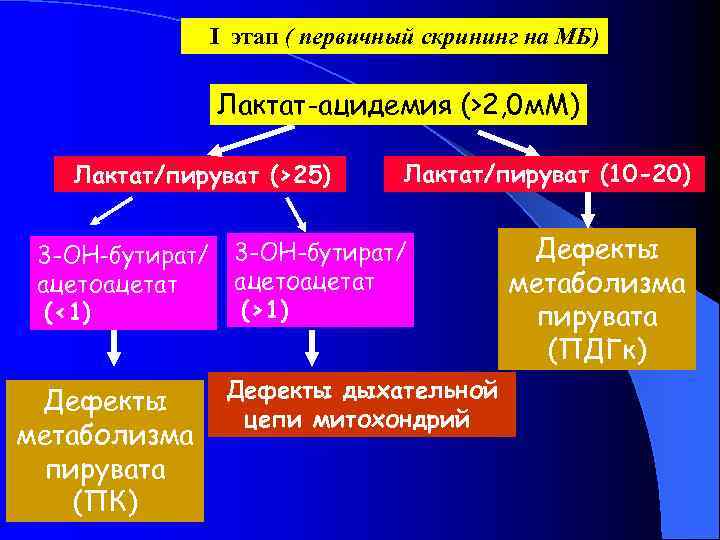
I этап ( первичный скрининг на МБ) Лактат-ацидемия (>2, 0 м. М) Лактат/пируват (>25) Лактат/пируват (10 -20) 3 -ОН-бутират/ Дефекты ацетоацетат метаболизма (<1) (>1) пирувата (ПДГк) Дефекты дыхательной Дефекты цепи митохондрий метаболизма пирувата (ПК)

Концентрация лактата в норме l Синдром LHON (всегда) l Синдром KSS/СPEO (часто) Концентрация лактата повышена Синдром MERRF Синдром MELAS Синдром Ли МБ, обусловленные мутациями я. ДНК

Анализ метаболитов l Позволяет подтвердить диагноз l Не дает возможность точно установить форму заболевания l Концентрация маркерных метаболитов может быть в норме при некоторых формах МБ l Концентрация маркерных метаболитов может быть повышена и при других заболеваниях

Морфологические изменения в мышечной ткани обусловлены периферическим субсарколемным и межфибриллярным накоплением аномальных митохондрий Окраска по Гомори трихром- RRF (красные миофибриллы с рваными краями). не является ни очень чувствительным, ни очень специфичным тестом для выявления пролиферации митохондрий. Гистохимические методы окраски на сукцинатдегидрогеназу (SDH) и цитохром с оксидазу (Сох). SDH-позитивные миофибриллы являются убедительными маркерами пролиферации митохондрий. Наличие SDH-негативных и Сох-негативных миофибрилл характерно для различных клинических фенотипов, обусловленных мутациями я. ДНК и мт. ДНК
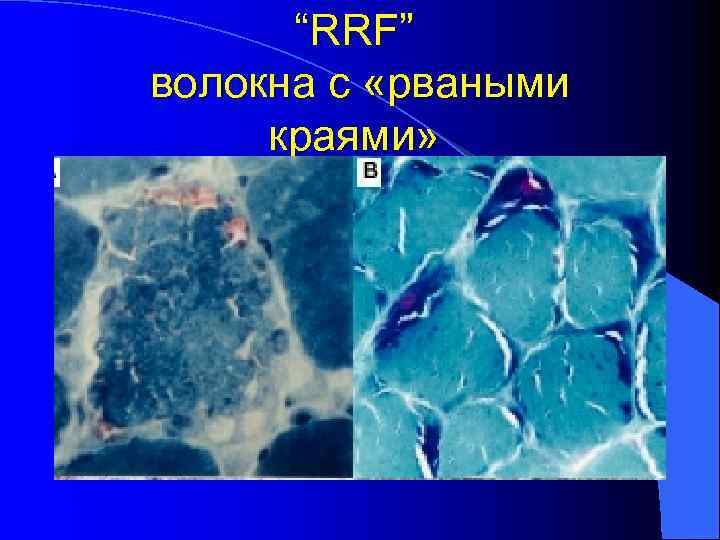
“RRF” волокна с «рваными краями»

Морфологические маркеры l Позволяют подтвердить, но не установить диагноз l Не характерны для синдромов LHON, NARP, болезни Ли и некоторых МБ, обусловленных мутациями я. ДНК l Не позволяют точно установить форму заболевания

Определение активности ферментов l Позволяет точно установить диагноз, если обнаружено значимое снижение активности фермента l При некоторых формах МБ активность ферментов может иметь пограничные значения l Активность фермента может быть снижена только в определенных тканях l Крайне дорогостоящие методы l требуют большого количества биологического материала (ККФ, мышечная ткань)
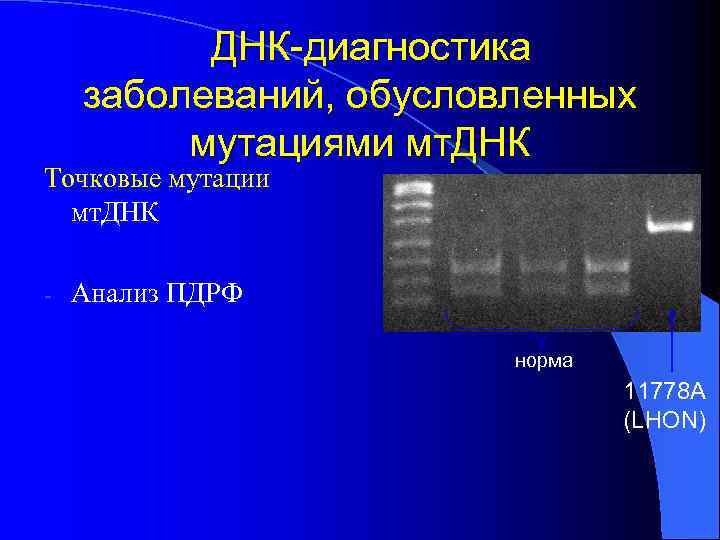
ДНК-диагностика заболеваний, обусловленных мутациями мт. ДНК Точковые мутации мт. ДНК - Анализ ПДРФ норма 11778 А (LHON)

ДНК-диагностика l ДНК-анализ на распространенные мутации мт. ДНК позволяет точно установить диагноз, если мутации обнаружены l Неравномерное распределение мутантной мт. ДНК требует использования ДНК выделенную из различных тканей l Наличие множества ядерных генов, приводящих к МБ затрудняет ДНК- диагностику заболеваний, обусловленных мутациями я. ДНК

Диагностика МБ l Ни один из подходов к диагностике МБ не обладает абсолютной диагностической значимостью ( за исключением случаев с выявлением патогенных мутаций и резко выраженного снижения активности ферментов) l Во многих случаях диагноз может быть установлен только на основании комплексного анализа клинических, генеалогических и лабораторных данных

Лизосомные болезни накопления: диагностика и лечение

Лизосомы l Лизосомы – органеллы окруженные одной мембраной, в матриксе которых содержаться различные ферменты l Основной функцией лизосом является катаболизм крупных Первичная лизосома макромолекул

Ферменты лизосом Наибольшую активность ферменты лизосом проявляют в кислой среде. Около 50 различных гидролаз, отличающихся по субстратной специфичности: l Расщепляют нуклеиновые кислоты Вторичная лизосома l Расщепляют белки l Расщепляют жиры l Отщепляют углеводородные остатки

Лизосомные болезни накопления (ЛБН) l Обусловлены мутациями генов, контролирующих процесс внутрилизосомного гидролиза макромолекул

Лизосомные болезни накопления (ЛБН) - Изменения в первичной структуре фермента - Дефекты белков-активаторов (сапозинов) - Дефекты транспорта ферментов в лизосомы

Лизосомные болезни накопления l Число известных форм – около 40 l Наследуются по аутосомно-рецессивному типу (кроме болезни Фабри и болезни Хантера) l Частота ЛБН в популяции 1: 5000 – 1: 8000 l Частота отдельных форм – крайне низкая: 1: 40 000 – 1: 200 000
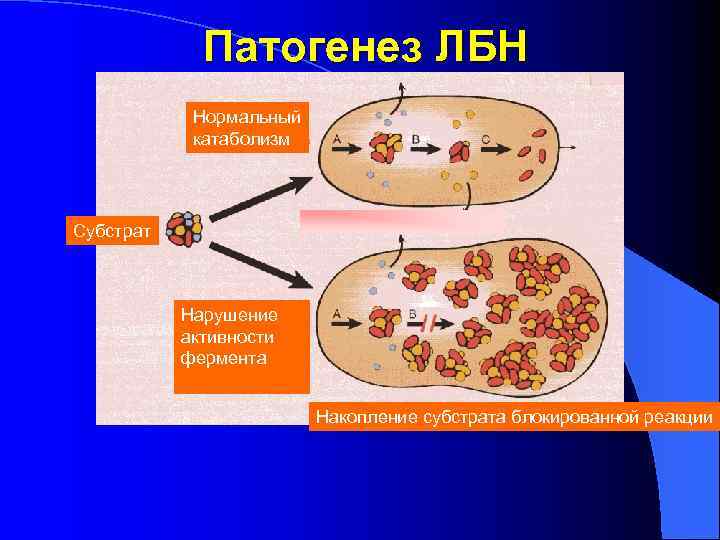
Патогенез ЛБН Нормальный катаболизм Субстрат Нарушение активности фермента Накопление субстрата блокированной реакции

Классификация ЛБН В зависимости от накапливаемых субстратов - Сфинголипидозы (болезнь Гоше, метахроматическая лейкодистрофия, болезнь Краббе) - Ганглиозидозы (болезнь Тея-Сакса, GM 1 - ганглиозидоз) - Мукополисахаридозы - Гликопротеинозы (альфа-маннозидоз) А также - Болезни лизосомного транспорта (муколипидоз) - Нейрональные цероидные липофусцинозы

Клинические проявления ЛБН l Прогрессирующих характер заболевания l Наличие различного по продолжительности интервала нормального развития (от нескольких месяцев до нескольких лет) l Признаки болезней накопления ( увеличение печени и селезенки, изменения со стороны соединительной и костной ткани, вовлечение в патологический процесс многих систем и органов)
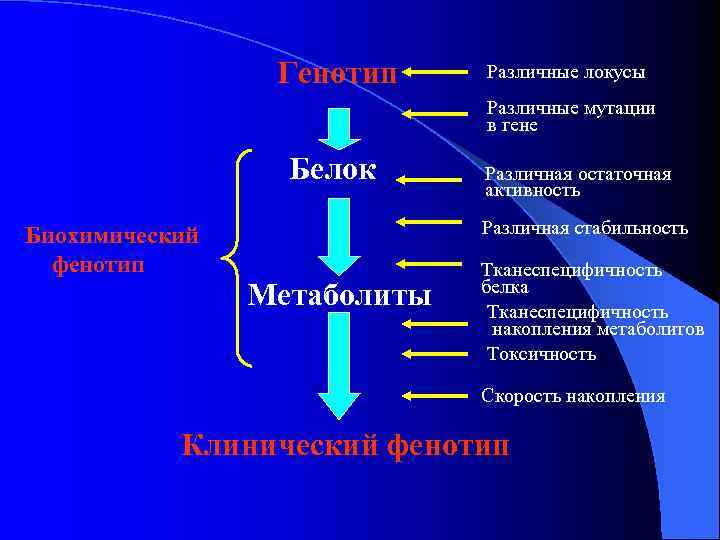
Генотип Различные локусы Различные мутации в гене Белок Различная остаточная активность Биохимический Различная стабильность фенотип Тканеспецифичность белка Метаболиты Тканеспецифичность накопления метаболитов Токсичность Скорость накопления Клинический фенотип

Генетическая гетерогенность Пример - Болезнь Гоше, недостаточность глюкозидазы Мутация N 370 S: Тип 1 ( без патологии нервной системы) Прогрессирующая гепатоспленомегалия Задержка роста Тромбоцитопения, анемия Мутация L 444 P: Тип 2, 3 ( с вовлечением нервной системы) Пpогpессиpующая гепатоспленомегалия Прогрессирующие специфические окуломоторные расстройства Прогрессирующая задержка психомоторного развития, миоклонии Анемия, тpомбоцитопения
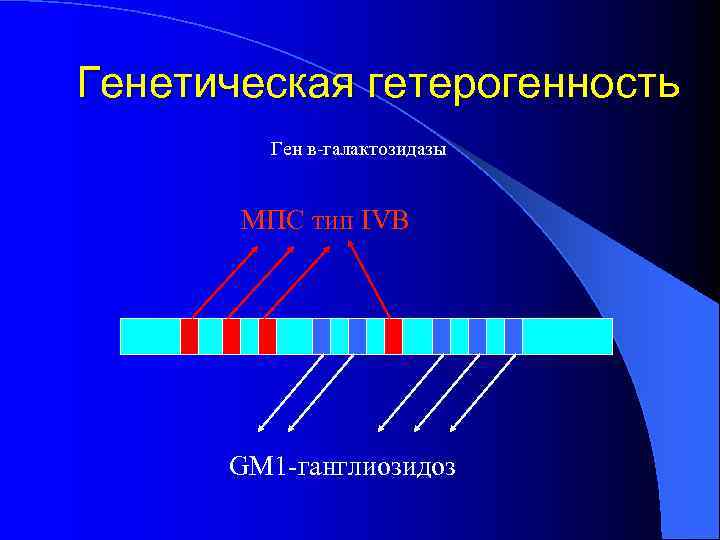
Генетическая гетерогенность Ген в-галактозидазы МПС тип IVB GM 1 -ганглиозидоз
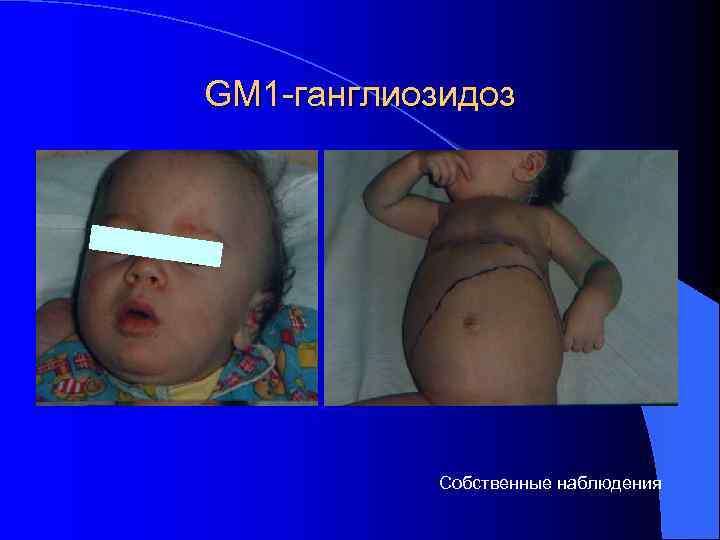
GM 1 -ганглиозидоз Собственные наблюдения
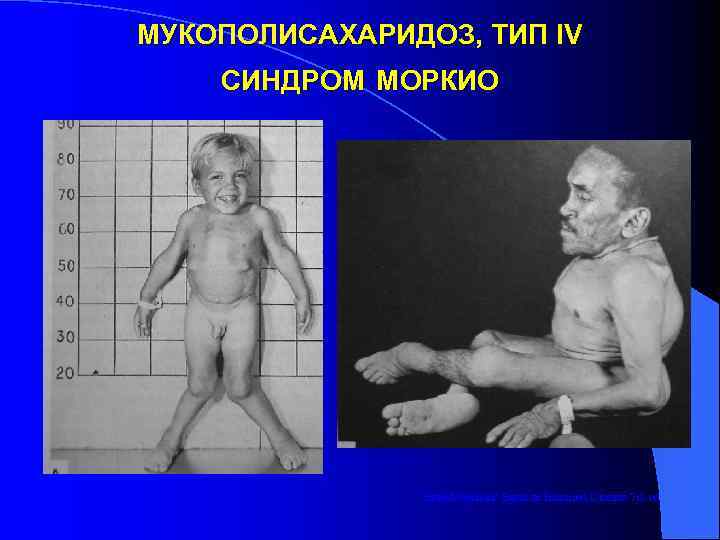
МУКОПОЛИСАХАРИДОЗ, ТИП IV СИНДРОМ МОРКИО from Metabolic Basis of Inherited Disease 7 th ed

Тканеспецифичность накопления метаболитов и их производных При метахроматической лейкодистрофии, болезни Краббе наиболее тяжело поражается нервная система, т. к. субстраты блокированных реакций являются основными компонентами клеток белого вещества, нейронов и периферических нервов.
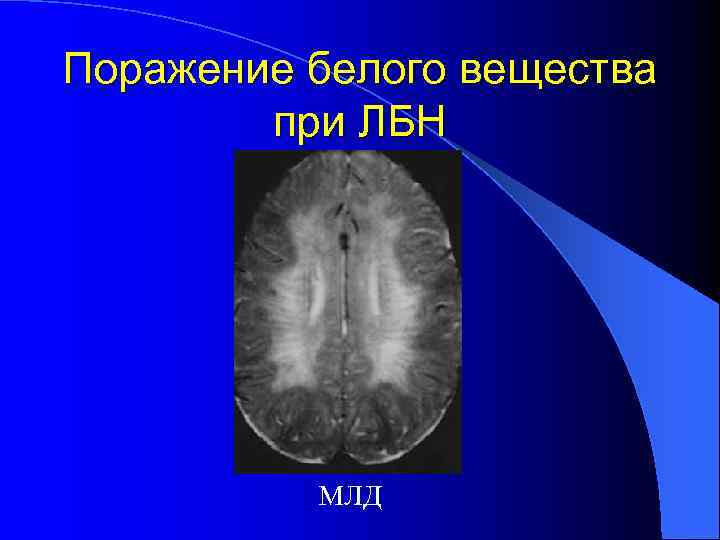
Поражение белого вещества при ЛБН МЛД

Тканеспецифичность накопления метаболитов и их производных l При других ЛБН поражаются не только нервные, но и клетки тканей висцеральных органов, соединительной ткани, костной ткани и крови, т. к. субстраты блокированных реакций входят в состав большинства клеток тканей мезенхимного и/или паренхимного происхождения. l Признаками этих заболеваний являются гепатомегалия или гепатоспленомегалия , гранулярные или ретикулярные инфильтраты в легких, грануломатоз , поражение соединительной ткани.
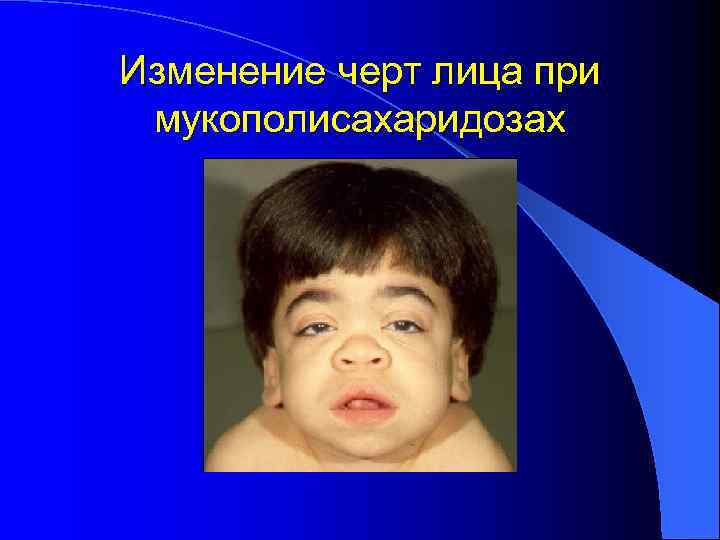
Изменение черт лица при мукополисахаридозах
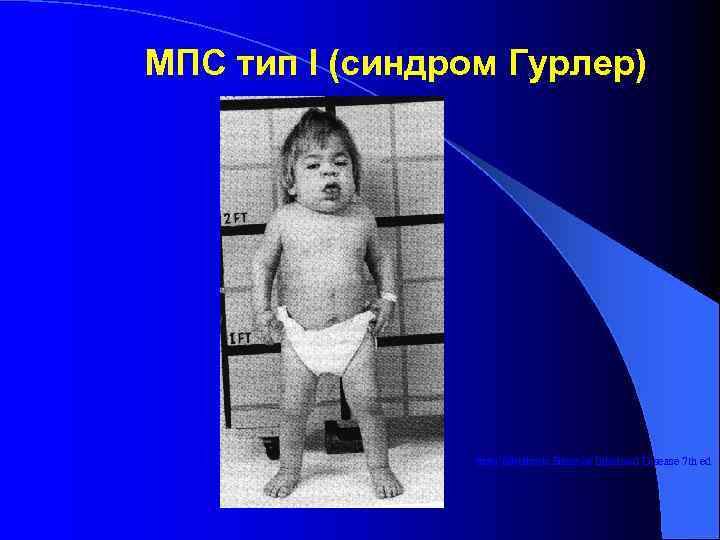
МПС тип I (синдром Гурлер) from Metabolic Basis of Inherited Disease 7 th ed

Множественный дизостоз l Деформации скелета: резко укороченная шея, колообразная или бочкообразная форма грудной клетки, кифоз/кифосколиоз, прогрессирующая тугоподвижность большинства суставов, "когтистая" кисть. l Изменение формы большинства костей: деформации тел позвонков (кубовидной, овальной и/или языкообразной формы), гипоплазия передней части поясничных позвонков, укорочение и утолщение длинных трубчатых костей, дисплазия головок плечевых и бедренных костей, конусообразная деформация метакарпальных костей, утолщение и укорочение средних и проксимальных фаланг, двусторонняя вальгусная деформация бедра, Краниостеноз, "башмакообразная" деформация турецкого седла
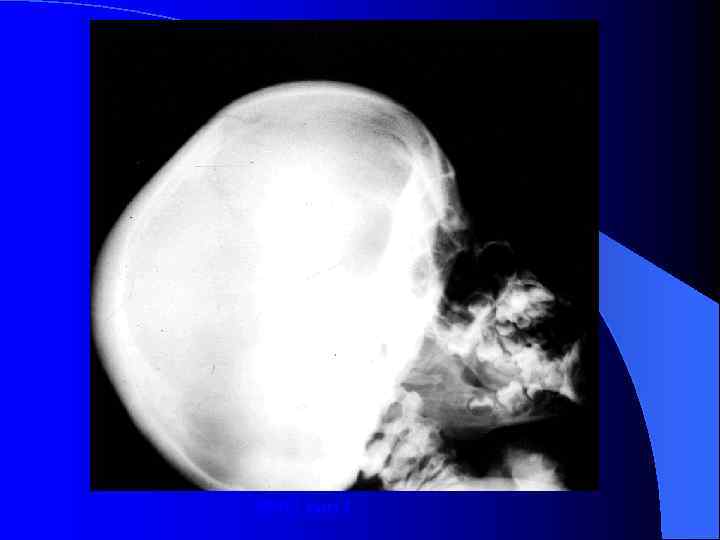
МПС тип I
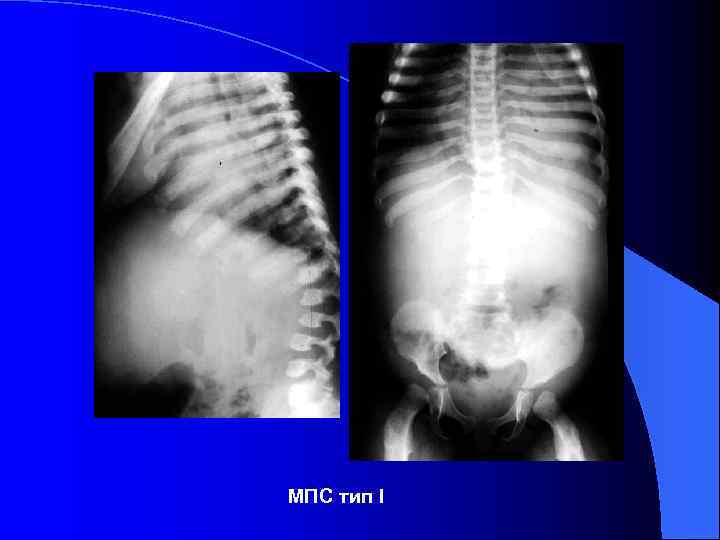
МПС тип I
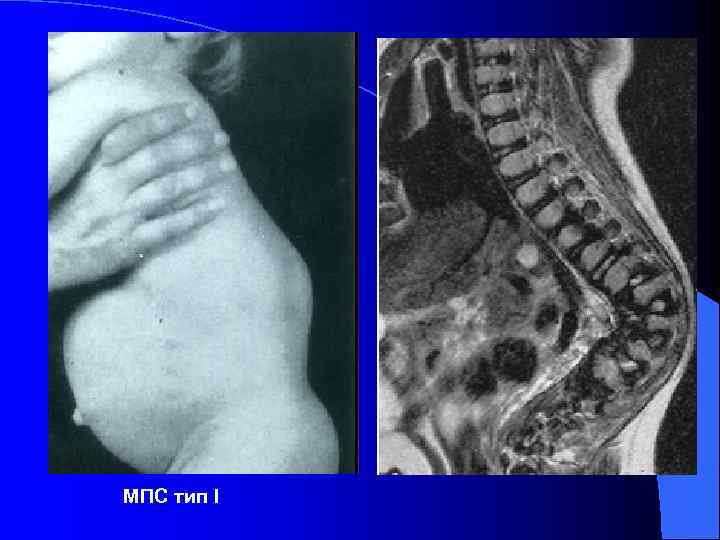
МПС тип I
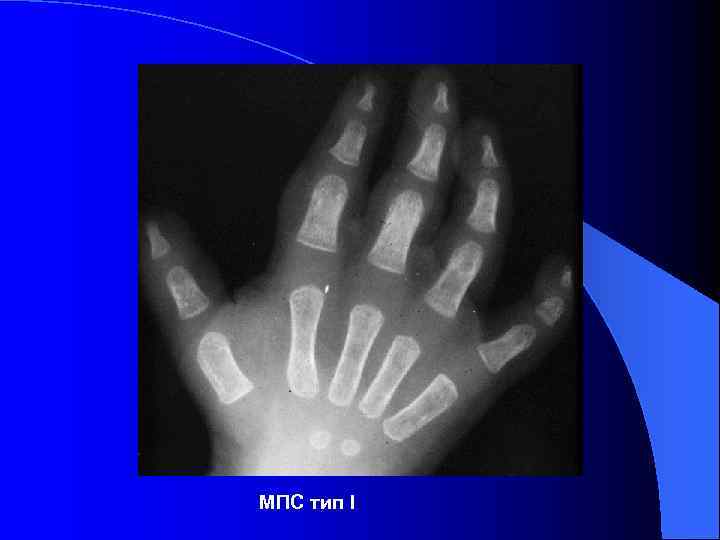
МПС тип I
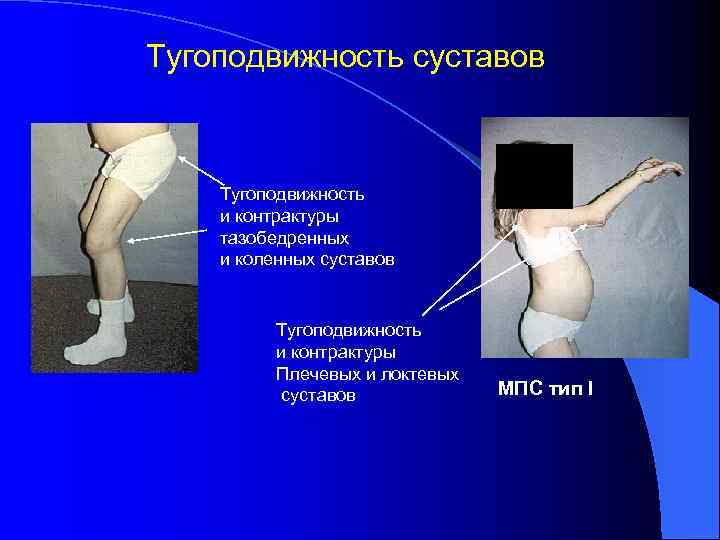
Тугоподвижность суставов Тугоподвижность и контрактуры тазобедренных и коленных суставов Тугоподвижность и контрактуры Плечевых и локтевых суставов МПС тип I
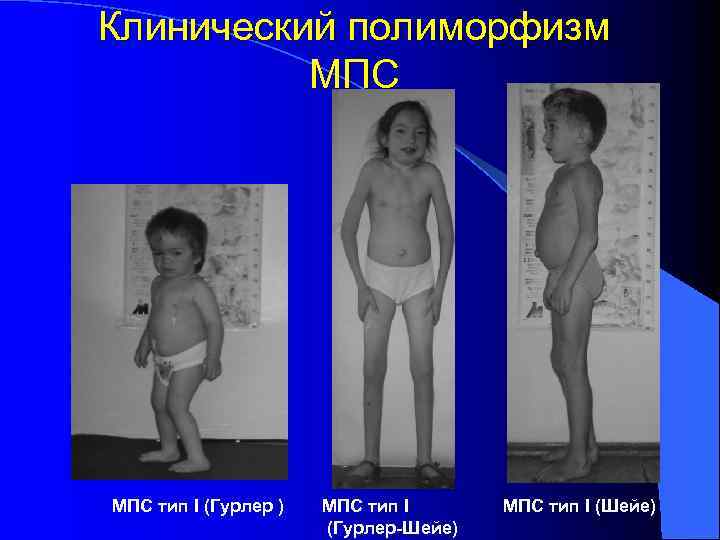
Клинический полиморфизм МПС тип I (Гурлер ) МПС тип I (Шейе) (Гурлер-Шейе)
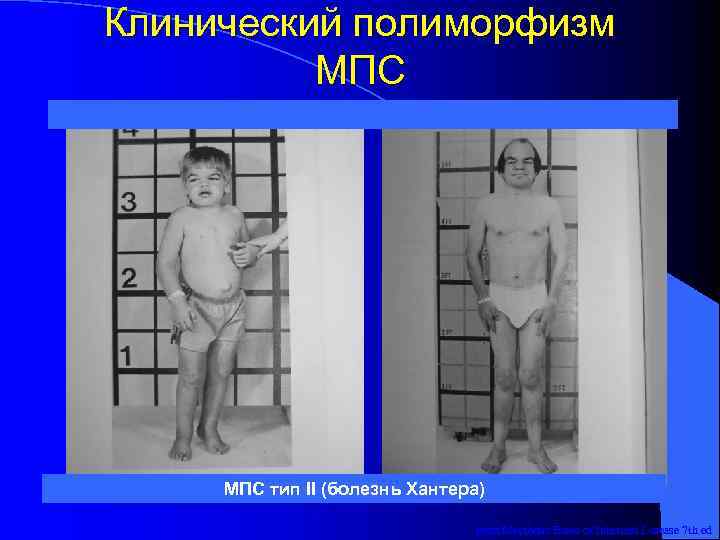
Клинический полиморфизм МПС тип II (болезнь Хантера) from Metabolic Basis of Inherited Disease 7 th ed
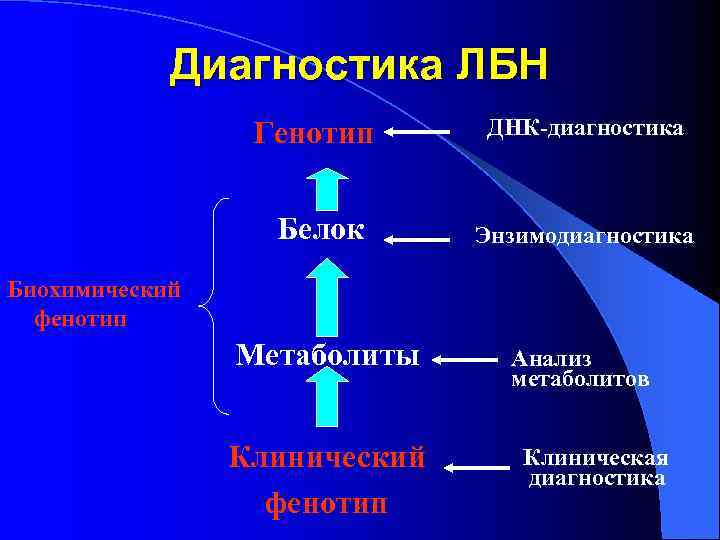
Диагностика ЛБН Генотип ДНК-диагностика Белок Энзимодиагностика Биохимический фенотип Метаболиты Анализ метаболитов Клинический Клиническая диагностика фенотип
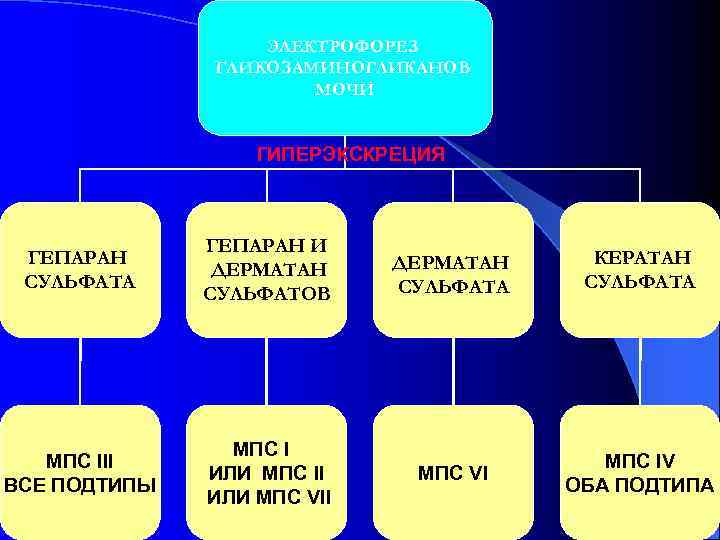
ЭЛЕКТРОФОРЕЗ ГЛИКОЗАМИНОГЛИКАНОВ МОЧИ ГИПЕРЭКСКРЕЦИЯ ГЕПАРАН И ГЕПАРАН ДЕРМАТАН КЕРАТАН ДЕРМАТАН СУЛЬФАТА СУЛЬФАТОВ МПС III МПС IV ИЛИ МПС II МПС VI ВСЕ ПОДТИПЫ ОБА ПОДТИПА ИЛИ МПС VII
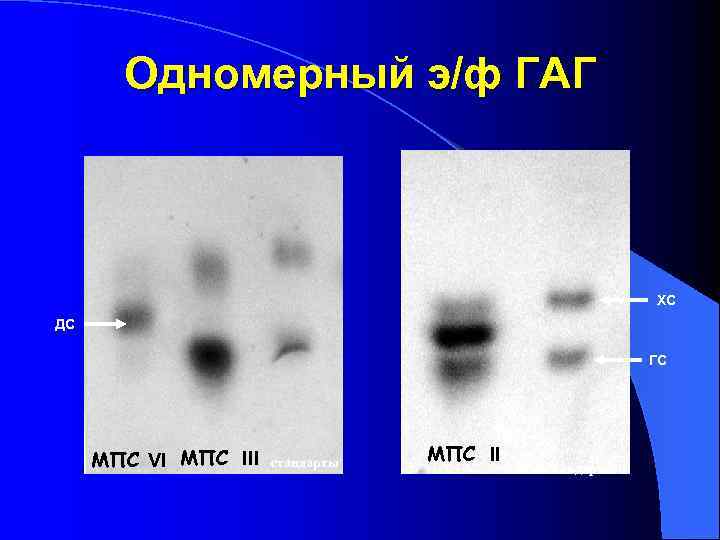
Одномерный э/ф ГАГ ХС ДС ГС МПС VI МПС III стандарты МПС II стандарты

Определение активности лизосомных ферментов l Около 30 форм возможно диагностировать с помощью энзимодиагностики l Биологический материал: лейкоциты периферической крови, плазма крови, культура кожных фибробластов, пренатальная диагностика – ворсины хориона l Субстраты – флуорогенные , хромогенные и радиоактивные l Новые методы – определение активности ферментов в пятнах высушенной крови

ДНК- диагностика ЛБН l Диагностика носительства заболеваний (болезнь Тея-Сакса, болезнь Хантера и болезнь Гоше) l Диагностика заболеваний с неизвестным первичным биохимическим дефектом (НЦЛ кроме 1, 2 типов) l Диагностика метахроматической лейкодистрофии (псевдонедостаточность фермента) l Нарушения белков сапозинов

Лечение лизосомных болезней накопления

Уровень фермента l Фермент-заместительнаятерапия l Фермент-индуцирующая терапия (фармакологические «шапероны» )

Фермент-заместительная терапия - Введение фермента - Трансплантация костного мозга - Клеточная терапия

Фермент-заместительная терапия l. В начале 70 х годов проведены первые клинические испытания для лечения: -Болезни Зандгоффа -Болезни Фабри -Болезни Помпе -Болезни Гоше

Фермент-заместительная терапия l. В начале 80 х годов получен первый препарат для лечения болезни Гоше: l -глюкозидаза, выделенная из плаценты человека l В 1990 х годах проведена первая внутривенная терапия (2 -3 мг/кг) 6 мес. l Получен рекомбинантный фермент в конце 1990 х

Фермент-заместительная терапия l Эффективна при всех формах ЛБН, протекающих без поражения нервной системы. l Побочные эффекты, обусловленные выработкой антител к препарату l Высокая стоимость l Не зависит от типа мутаций

Трансплантация костного мозга Принцип: Замещение клеток реципиента клетками донора с нормальной активностью фермента

Трансплантация костного мозга Примеры заболеваний: Болезнь Краббе Метахроматическая лейкодистрофия Мукополисахаридоз тип 1
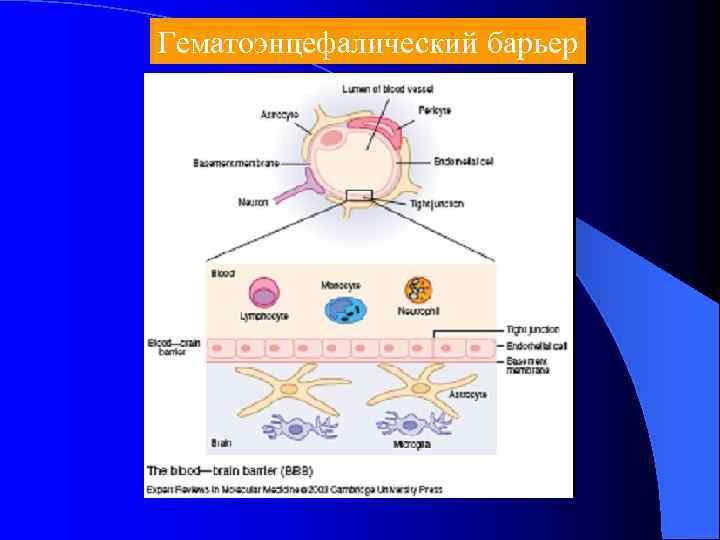
Гематоэнцефалический барьер

Трансплантация костного мозга Возможно проводить при неврологических формах заболевания Длительный терапевтический эффект Не зависит от типа мутации

Трансплантация костного мозга Высокая летальность (посттрансплантационные осложнения, инфекции) Трудность подбора доноров Эффективна только на доклинической стадии Высокая стоимость Не разработаны критерии отбора пациентов для ТКМ

Фермент-индуцирующая терапия l Принцип: Стабилизация белков при их взаимодействии с определенными веществами (химическими шаперонами)

Фермент-индуцирующая терапия l Химические шапероны (неспецифические): - Глицерин - Сахароза/галактоза

Фермент-индуцирующая терапия l Фармакологические шапероны (специфические): - Аналоги субстратов - Кофакторы - Ингибиторы (обратимые)

Фермент-индуцирующая терапия при болезни Тея- Сакса и болезни Зандгоффа

Случай 1 l Пациент С. (м) l Раннее развитие без особенностей. В 5 лет родители отметили увеличение размеров живота, частые носовые кровотечения. По УЗИ - увеличение размеров печени и селезенки. В б/х анализе крови без особенностей. В общем анализе крови- тромбоцитопения. Скелетных нарушений нет, психоречевое развитие соответствует возрастной норме.

Рекомендуемые обследования l 1. Определение гликозаминогликанов в моче l 2. Определение активности глюкозидазы в лейкоцитах крови l 3. Определение активности гексозаминидазы.

Случай 2 l Пациент П. (м) l Раннее развитие без особенностей. В 6 месяцев увеличение размеров печени и селезенки. Ребенок отстает в психо-моторном развитии. Мышечная гипотония. Увеличение размеров головы. В б/х и общем анализе крови без особенностей. Окулист- дегенерация макулы по типу «вишневой косточки» . Скелетных нарушений нет.

Рекомендуемые обследования l 1. Определение гликозаминогликанов в моче l 2. Определение активности глюкозидазы в лейкоцитах крови l 3. Оппределение активности гексозаминидазы

Случай 3 l Пациент П. (ж) l Раннее развитие без особенностей. В 1 год обратились к неврологу. Ребенок отстает в психо-моторном развитии, отмечается агрессивное поведение. Тугоподвижность крупных суставов, жесткие волосы, нейросенсорная тугоухость, гиперплазия десен. В б/х и общем анализе крови без особенностей.

Рекомендуемые обследования l 1. Определение гликозаминогликанов в моче l 2. Определение активности глюкозидазы в лейкоцитах крови l 3. Определение активности гексозаминидазы
Митохондриальные и лизосомные заболевания.ppt
- Количество слайдов: 85

