2008_mkh_EHTC_u_rastenii.ppt
- Количество слайдов: 20

Митохондриальная ЭТЦ
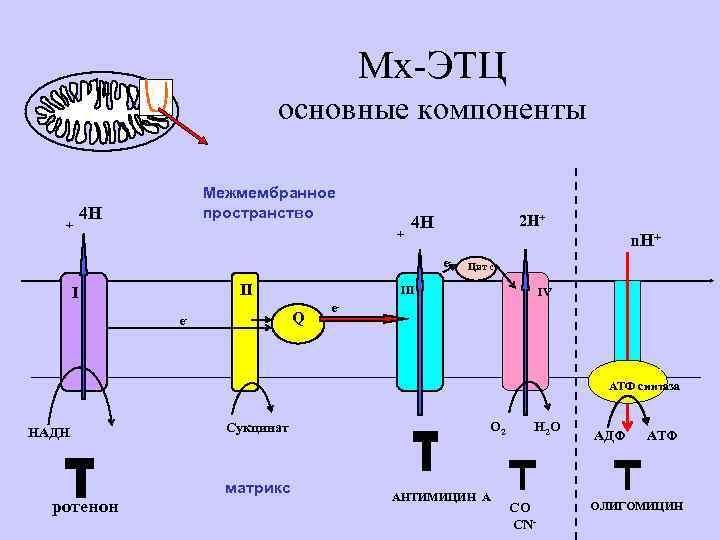
Мх-ЭТЦ основные компоненты + Межмембранное пространство 4 Н + 2 Н+ 4 Н n. Н+ e- II I III Q e- Цит с IV e- АТФ синтаза НАДН ротенон Сукцинат матрикс О 2 АНТИМИЦИН А Н 2 О СО CN- АДФ АТФ ОЛИГОМИЦИН

Электрон по ЭТЦ движется от одного редокс -центра к другому. Движущая сила – окислительновосстановительный потенциал редоксцентров (или переносчиков электронов). Некоторые переносчики являются общими для ЭТЦ всех типов (с. 103 и 164 ФР под ред Ермакова И. П. )

НАД(Ф)Н, ФМН, ФАД
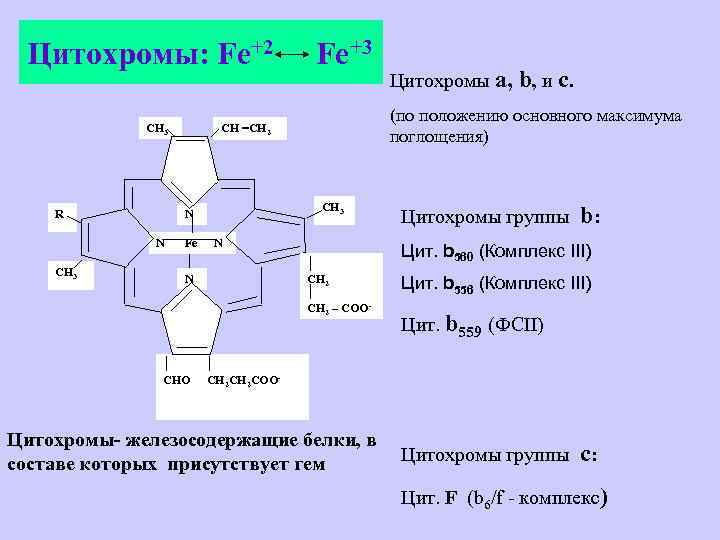
Цитохромы: Fe+2 СН 3 R СН 3 Fe СН 3 N СН 2 – СОО- N СНО Цитохромы а, b, и с. (по положению основного максимума поглощения) СН =СН 2 N N Fe+3 Цитохромы группы b: Цит. b 560 (Комплекс III) Цит. b 556 (Комплекс III) Цит. b 559 (ФСII) СН 2 СОО- Цитохромы- железосодержащие белки, в составе которых присутствует гем Цитохромы группы с: Цит. F (b 6/f - комплекс)
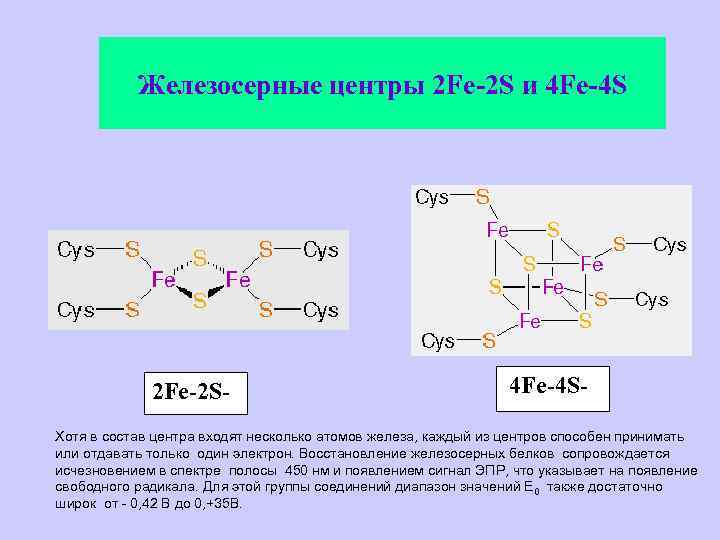
Железосерные центры 2 Fe-2 S и 4 Fe-4 S 2 Fe-2 S- 4 Fe-4 S- Хотя в состав центра входят несколько атомов железа, каждый из центров способен принимать или отдавать только один электрон. Восстановление железосерных белков сопровождается исчезновением в спектре полосы 450 нм и появлением сигнал ЭПР, что указывает на появление свободного радикала. Для этой группы соединений диапазон значений Е 0 также достаточно широк от - 0, 42 В до 0, +35 В.

Хиноны Q (убихиноны, пластохиноны) ОН О. · О 1 е- хинон ( Q) | О- 1 е- 2 Н+ семихинон анион радикал (Q·‾ ) Редокс-превращения в молекуле хинонов | ОН гидрохинон (QН 2)
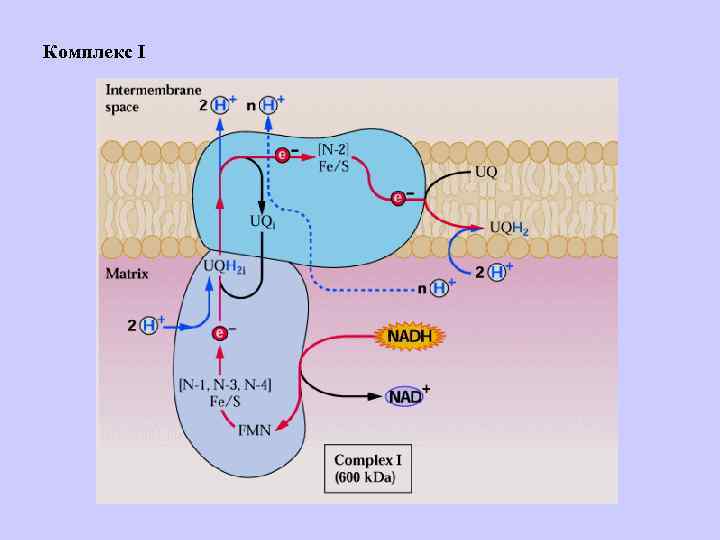
Комплекс I
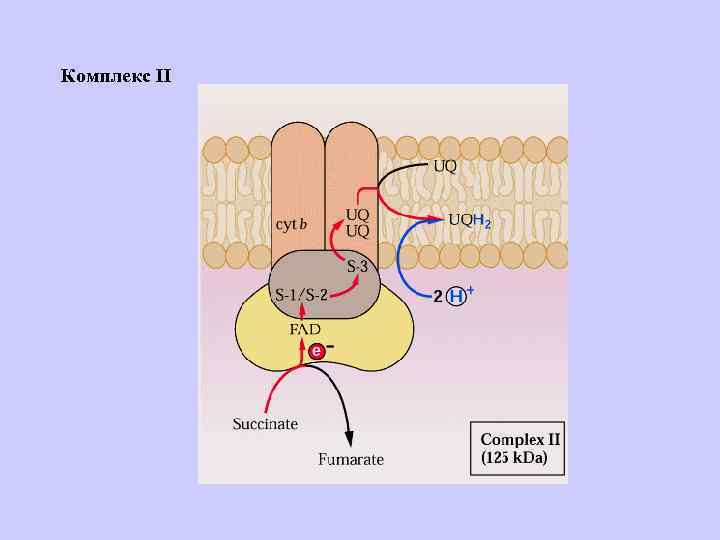
Комплекс II
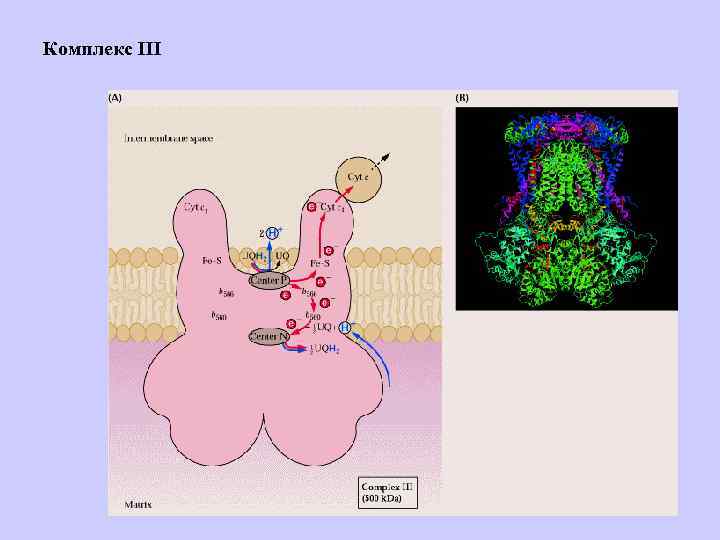
Комплекс III
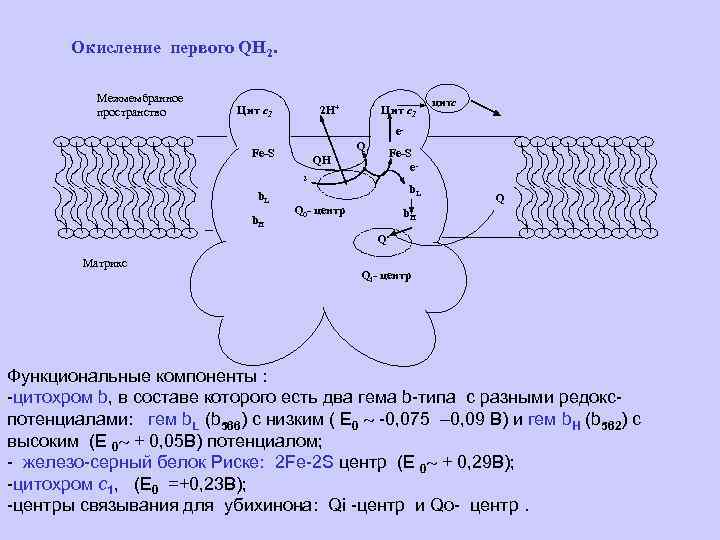
Окисление первого QH 2. Межмембранное пространство Цит с1 2 H+ Цит с1 цитс e. Q Fe-S QH Fe-S e- 2 b. L b. H b. L Q 0 - центр Q b. H Q. - Матрикс Qi- центр Функциональные компоненты : -цитохром b, в составе которого есть два гема b-типа с разными редокспотенциалами: гем b. L (b 566) с низким ( Е 0 -0, 075 – 0, 09 В) и гем b. H (b 562) с высоким (Е 0 + 0, 05 В) потенциалом; - железо-серный белок Риске: 2 Fe-2 S центр (Е 0 + 0, 29 В); -цитохром с1, (Е 0 =+0, 23 В); -центры связывания для убихинона: Qi -центр и Qo- центр.
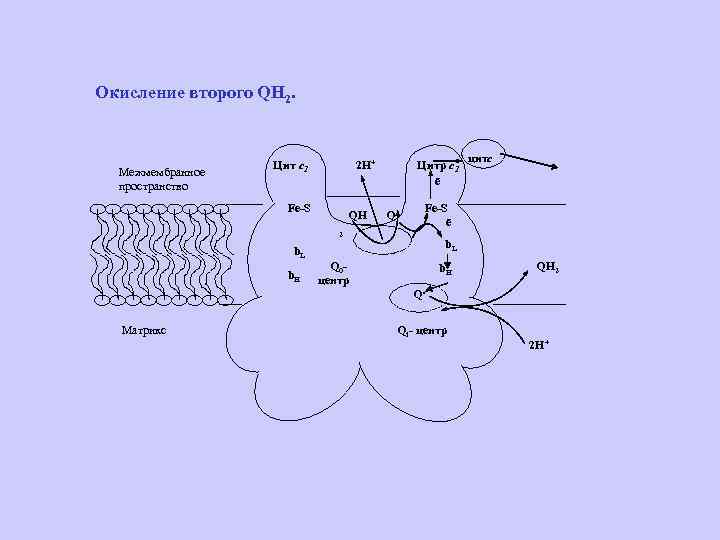
Окисление второго QH 2. Межмембранное пространство Цит с1 2 H+ Fe-S QH Цитр с1 ē Q Fe-S ē 2 b. L b. H Матрикс Q 0 центр цитс b. L b. H QH 2 Q. Qi- центр 2 Н+
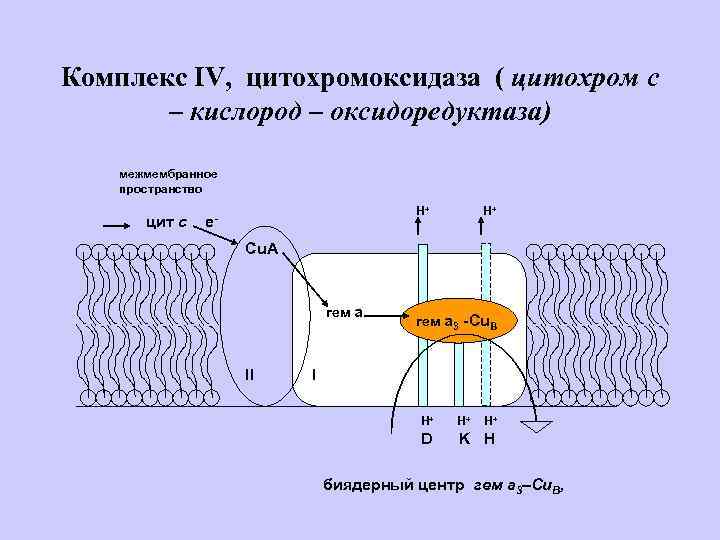
Комплекс IV, цитохромоксидаза ( цитохром с – кислород – оксидоредуктаза) межмембранное пространство цит с H+ e- H+ Cu. A гем а II гем а 3 -Сu. B I H+ H+ H+ D K H биядерный центр гем а 3–Сu. В,
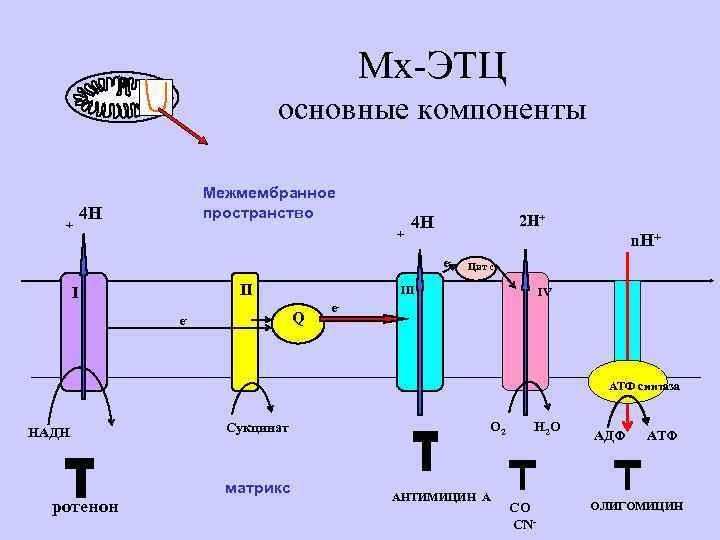
Мх-ЭТЦ основные компоненты + Межмембранное пространство 4 Н + 2 Н+ 4 Н n. Н+ e- II I III Q e- Цит с IV e- АТФ синтаза НАДН ротенон Сукцинат матрикс О 2 АНТИМИЦИН А Н 2 О СО CN- АДФ АТФ ОЛИГОМИЦИН
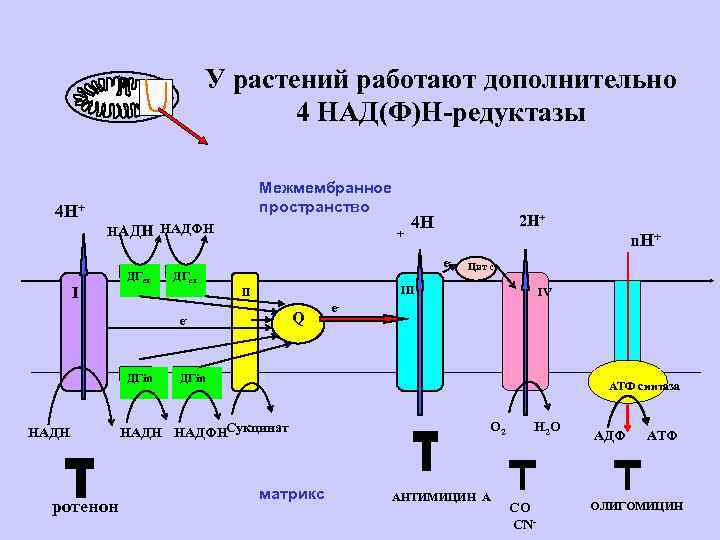
У растений работают дополнительно 4 НАД(Ф)Н-редуктазы 4 Н+ Межмембранное пространство НАДН НАДФН I ДГex + ДГex ротенон Цит с III Q e- НАДН n. Н+ e- II ДГin 2 Н+ 4 Н IV e- ДГin АТФ синтаза НАДН НАДФНСукцинат матрикс О 2 АНТИМИЦИН А Н 2 О СО CN- АДФ АТФ ОЛИГОМИЦИН
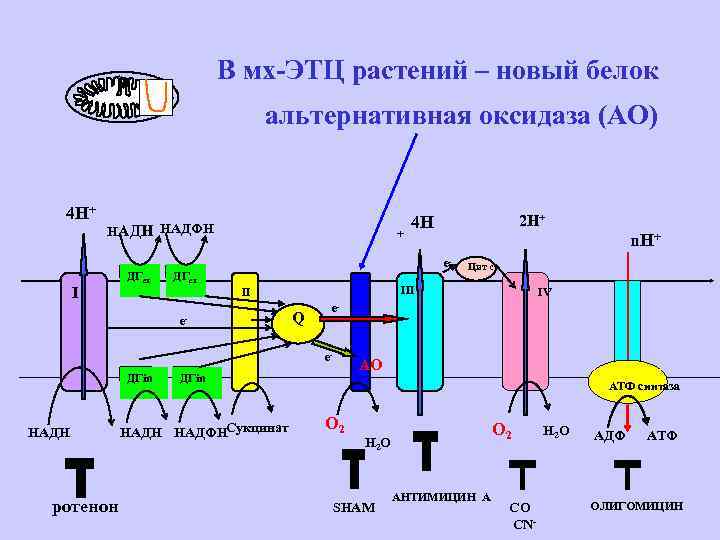
В мх-ЭТЦ растений – новый белок альтернативная оксидаза (АО) 4 Н+ НАДН НАДФН I ДГex + ДГex e- Q ротенон IV e- ДГin НАДН НАДФНСукцинат Цит с III e- НАДН n. Н+ e- II ДГin 2 Н+ 4 Н АО АТФ синтаза О 2 Н 2 О SHAM АНТИМИЦИН А СО CN- Н 2 О АДФ АТФ ОЛИГОМИЦИН

Таким образом, система трансформации энергии включает следующие основные компоненты: - замкнутая сопрягающая мембрана; - локализованная в мембране ЭТЦ; -трансмембранный электрохимический протонный градиент, генерируемый работой цепи; -АТФ синтаза, катализирующая синтез АТФ из АДФ и Фн за счет энергии +.

АТФ-синтетаза ( F 1 F 0 АТФаза, или Н+АТФ-аза F – типа)

Циркуляция ионов через мембраны – фундаментальный процесс клеточной биологии. Другие АТФазы. Н+ АТФазы F- типа, Н+ АТФазы V- типа и Н+ АТФазы Р- типа. Все АТФазы – обратимые сопрягающие системы, которые способны к взаимопревращению энергии ионных градиента и макроэргической связи в молекуле АТФ.
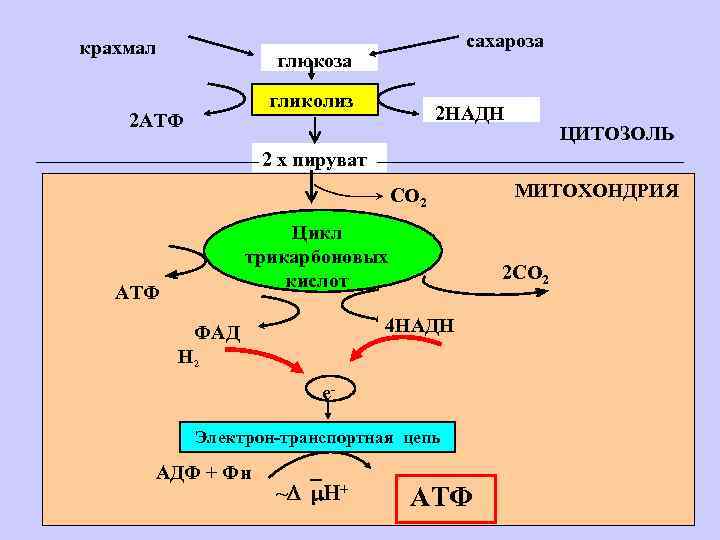
крахмал сахароза глюкоза гликолиз 2 АТФ 2 НАДН ЦИТОЗОЛЬ 2 х пируват СО 2 Цикл трикарбоновых кислот АТФ 2 СО 2 4 НАДН ФАД Н 2 e- Электрон-транспортная цепь АДФ + Фн ~ + МИТОХОНДРИЯ АТФ
2008_mkh_EHTC_u_rastenii.ppt