9b9bf9a692f951bfdfdadcc3f0d0ce19.ppt
- Количество слайдов: 19

Министерство здравоохранения и социального развития Республики Казахстан Новые подходы по совершенствованию системы допуска на рынок лекарственных средств и медицинских изделий 1
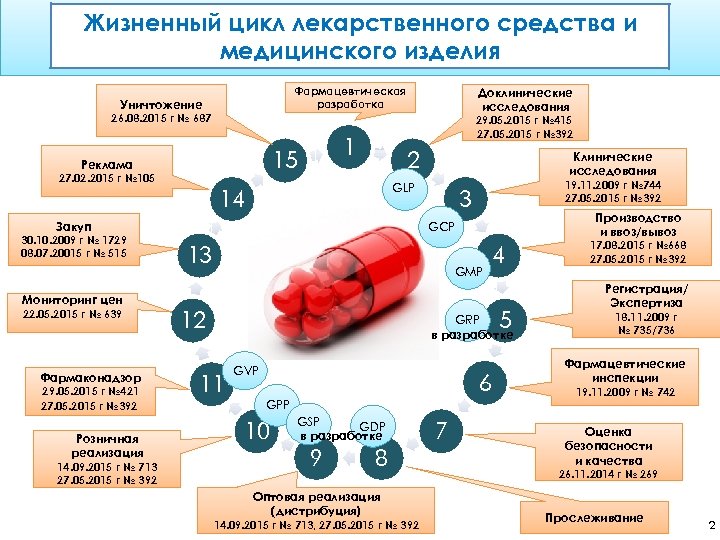
Жизненный цикл лекарственного средства и медицинского изделия Уничтожение Фармацевтическая разработка Доклинические исследования 26. 08. 2015 г № 687 1 15 Реклама 27. 02. 2015 г № 105 29. 05. 2015 г № 415 27. 05. 2015 г № 392 2 GLP 14 Закуп 30. 10. 2009 г № 1729 08. 07. 20015 г № 515 Мониторинг цен 22. 05. 2015 г № 639 Фармаконадзор 29. 05. 2015 г № 421 27. 05. 2015 г № 392 Розничная реализация 14. 09. 2015 г № 713 27. 05. 2015 г № 392 Клинические исследования 19. 11. 2009 г № 744 27. 05. 2015 г № 392 3 Производство и ввоз/вывоз GСP 13 GMP 12 4 5 GRP в разработке 11 GVP 6 GPP 10 GSP GDP в разработке 9 8 Оптовая реализация (дистрибуция) 14. 09. 2015 г № 713, 27. 05. 2015 г № 392 7 17. 08. 2015 г № 668 27. 05. 2015 г № 392 Регистрация/ Экспертиза 18. 11. 2009 г № 735/736 Фармацевтические инспекции 19. 11. 2009 г № 742 Оценка безопасности и качества 26. 11. 2014 г № 269 Прослеживание 2

Объекты фармацевтической деятельности Всего объектов фармацевтической деятельности – 12 368 Расположены в сельской местности – 27% (3340) от общего количества объектов Наличие сертификатов Gx. P и ISO в РК GMP – 9 производителей лекарственных средств (19 площадок) GDP – 40 дистрибьюторов GPP – 23 аптеки ISO – 14 производств медицинских изделий 3

Фармацевтическая разработка (производители и разработчики) 1 3 1 2 1 1 1 5 1 4 1 2 3 4 5 6 1 0 9 8 7 Шаг 1. Цель: Ø Полный охват процесса производства при инспектировании Шаг 2. Шаг 3. Ø Фармацевтическая разработка препарата осуществляется фармацевтическими компаниями Ø Национальным Центром проводится научная оценка данных в процессе фармацевтической экспертизы при регистрации лекарственных средств 4

Доклинические исследования (ДКИ) 1 4 1 3 1 2 1 1 1 0 1 5 1 2 3 4 5 6 9 8 7 Цель: Совершенствование процедуры и обеспечение признания на международном уровне (ЕАЭС и ЕС) ТЕКУЩАЯ СИТУАЦИЯ: Ø Доклинические исследования (ДКИ) проводятся в не аккредитованных на международном уровне испытательных лабораториях НИИ, НЦЭЛС Ø Проведение ДКИ без соблюдения требований надлежащей лабораторной практики (GLP) Ø Специалисты исследовательских организаций не обучены стандарту GLP МЕЖДУНАРОДНЫЙ ОПЫТ: Ø ДКИ проводятся в соответствии с GLP Ø Результаты признаются на международном уровне ПЕРСПЕКТИВНЫЕ ЗАДАЧИ ШАГ 1. Выбор ведущих испытательных лабораторий: Назарбаев Университет, НИИ биотехнологии, АО «НЦ противоинфекционных препаратов» , НИИ микробиологии и вирусологии МОН, НЦЭЛС в 2016 г. , расширение до 10 ИЛ в 2017 -2018 г. г. ШАГ 2. Внедрение, обучение, оснащение стандарту GLP (включено в проект Кодекса РК) ШАГ 3. Аккредитации испытательных лабораторий на проведение ДКИ до 2018 г. , в том числе испытательной лаборатории НЦЭЛС (2016 г) Словацким Агентством по лекарствам входящим в ОЭСР РИСКИ: Ø Результаты не признаются на международном уровне Ø Препятствие выхода отечественных производителей на внешние рынки ОЖИДАЕМЫЙ РЕЗУЛЬТАТ: Ø Ø Ø Признание результатов ДКИ в рамках ЕАЭС и на международном уровне Повышение кадрового потенциала, конкурентоспособности в Средней Азии Внедрение инновационных технологий Привлечение инвестиций в наукоемкую сферу экономики Выход отечественных производителей в рамках ЕАЭС и на внешний рынок 5

Клинические исследования (КИ) 1 1 5 1 4 2 1 3 3 4 1 2 5 1 1 6 1 0 9 8 7 Цель: Совершенствование процедуры и обеспечение признания результатов на международном уровне ( ЕАЭС и ЕС) ТЕКУЩАЯ СИТУАЦИЯ: Ø Аккредитована 1 клиническая база - РГП «Больница Медицинского центра Управления делами Президента РК» ) Ø Недостаточно обученных специалистов по надлежащей клинической практике (GСP) Ø Не все КИ проводятся с соблюдением требований GСP Ø Недостаточная оснащенность клинических баз Ø Отсутствие клинических баз по проведению КИ медицинских изделий МЕЖДУНАРОДНЫЙ ОПЫТ: Ø КИ проводятся в соответствии с GСP Ø Результаты признаются на международном уровне РИСКИ: Ø Необеспечение эффективности и безопасности Ø Непризнание результатов в других странах, кроме СНГ Россия: 750 КИ, 1000 КБ 2015 г. Беларусь: 75 КИ, 60 КБ Казахстан: 12 КИ, 36 КБ ПЕРСПЕКТИВНЫЕ ЗАДАЧИ: ШАГ 1. Выбор клинических баз: на I этапе (2016 г) – Республиканские НИИ и НЦ (5) на II этапе (2017 -2018 г. г. ) - расширение клинических баз - областные больницы и поликлиники (40) ШАГ 2. Внедрение, обучение, оснащение стандарту GCP (включено в проект Кодекса РК) ШАГ 3. Аккредитация клинических баз, в том числе на ISO 14155 GCP для медицинских изделий ШАГ 4. В рамках ЕАЭС обязательное проведение КИ полностью или частично на территории Союза ОЖИДАЕМЫЙ РЕЗУЛЬТАТ: Ø Обеспечение доступа на рынок безопасных и эффективных лекарственных средств и медицинских изделий Ø Признание результатов КИ в рамках ЕАЭС и на международном уровне Ø Получение бесплатного лечения заболеваний дорогостоящими инновационными препаратами Ø Освоение новых технологий, привлечение инвестиций в страну и в медицинские организации 6

1 4 Производство 1 3 1 2 1 1 1 0 1 5 1 2 4 3 5 6 9 8 7 Цель: Обеспечение соответствия локальных производителей требованиям надлежащей производственной практики (GMP) ТЕКУЩАЯ СИТУАЦИЯ: Ø GMP – 9 производителей лекарственных средств (19 площадок) из 51 отечественного производителя Ø ISO 13485 – 11 производителей медицинских изделий из 61 отечественных производителей Ø Не регистрируются лекарственные средства без GMP зарубежных производителей, для отечественных производителей – с 2018 года МЕЖДУНАРОДНЫЙ ОПЫТ: Ø Производство лекарственных средств и медицинских изделий в соответствии с требованиями GMP и ISO Ø Соблюдение требований GMP = гарантия качества Ø Отвественность уполномоченных лиц по качеству (вплоть до уголовной ответственности) и ведение Реестра уполномоченных лиц по качеству ПЕРСПЕКТИВНЫЕ ЗАДАЧИ: Включено в проект Кодекса РК: ШАГ 1. Внедрение GMP и ИСО до 2018 года, обучение субъектов фармацевтического рынка требованиям GMP и ISO. ШАГ 2. Установление отвественности и аттестация уполномоченных лиц по качеству и создание Реестра уполномоченных лиц по качеству ШАГ 3. Запрет на закуп и отзыв лицензий при отсутствии GMP с 2018 года Дополнительно до 2018 года начнет функционировать: Ø по GMP - 6 отечественных производителей Ø по ISO - 3 уполномоченных лиц по качеству РИСКИ: Ø Отсутствие гарантии качества продукции производстве вне GMP ОЖИДАЕМЫЙ РЕЗУЛЬТАТ: Ø Выпуск конкурентоспособной отечественной продукции Ø Выход на рынки ЕАЭС и международные рынки Ø Привлечение зарубежных инвестиций в производство через трансферт технологий 7

Экспертиза и регистрация Цель: Совершенствование экспертизы при государственной регистрации ТЕКУЩАЯ СИТУАЦИЯ: Ø Регистрация лекарственных средств отечественных производителей без GMP Ø Лабораторные испытания при регистрации Ø Аккредитована физико-химическая лаборатория испытательного центра НЦЭЛС на ISO 17025 Европейским директоратом по качеству (сентябрь 2015 года) МЕЖДУНАРОДНЫЙ ОПЫТ: Ø Внедрены все Gx. P Ø Экспертиза без лабораторных испытаний Ø Предрегистрационная инспекция по Gx. P Ø Законодательная ответственность: производителей за качество, субъектов за выполнение требований законодательства (система штрафов, уголовная ответственность) РИСКИ: Ø Возможность выпуска на рынок продукции с недостаточной эффективностью, безопасностью и качеством 1 1 2 1 5 3 4 1 4 3 1 2 1 6 1 1 7 0 9 8 5 ПЕРСПЕКТИВНЫЕ ЗАДАЧИ ШАГ 1. ВКЛЮЧЕНЫ ИЗМЕНЕНИЯ В ЗАКОНОДАТЕЛЬСТВО (Кодекс РК, приказ № 736): Ø отмена лабораторных испытаний производителей лекарственных средств: v стран региона ICH и РК, произведенных по GМP – июль 2016 года v для остальных производителей лекарственных средств - с 2018 года Ø оптимизация экспертизы с учетом опыта ЕС: v экспертиза одного препарата группой экспертов (одновременно фармацевтическая и фармакологическая экспертиза) единый экспертный отчет v электронное взаимодействие с заявителем, с уполномоченным органом путем портального решения) (2017 год) ШАГ 2. АККРЕДИТАЦИЯ ЛАБОРАТОРИЙ НЦЭЛС: 2016 год: Ø фармакологических испытаний на GLP - Словацким Агентством Ø аккредитация испытательной лаборатории по медицинским изделиям на ISO 17025 - Американским аккредитующим органом (IAS) 2017 год преквалификация ВОЗ: Ø лаборатории биологических испытаний Испытательного центра г. Алматы Ø испытательные лаборатории территориальных филиалов г. г. Караганда, Костанай, Павлодар 2019 год преквалификация ВОЗ: Ø референс-лаборатории г. Астана , Ø испытательные лаборатории территориальных филиалов г. г. Актобе, Шымкент ШАГ 3. Разработать и внедрить Надлежащую регуляторную практику (GRP) (2018 г) (включено в проект Кодекса РК) ОЖИДАЕМЫЙ РЕЗУЛЬТАТ: Ø Гармонизация с международными требованиями и ЕАЭС Ø Прозрачность регуляторных действий (внедрение GRP) Ø Обеспечение населения безопасными, эффективными и качественными лекарственными средствами и медицинскими изделиями 8
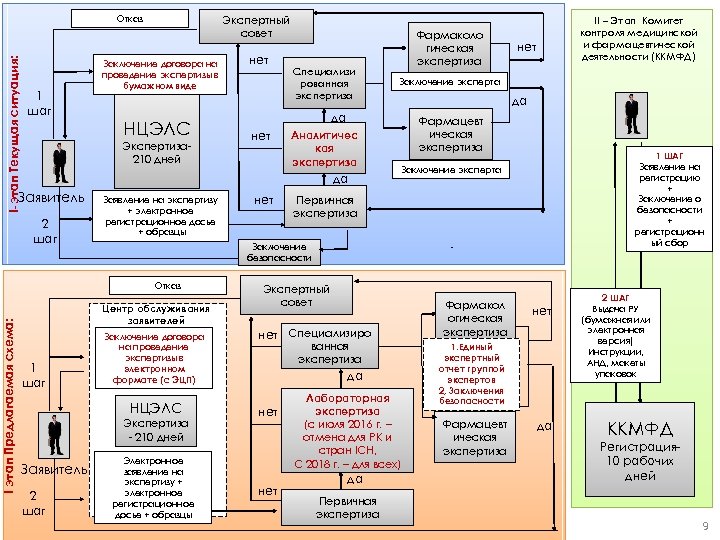
I-этап Текущая ситуация: Отказ 1 шаг Экспертный совет Заключение договора на проведение экспертизы в бумажном виде НЦЭЛС Экспертиза 210 дней Специализи рованная экспертиза нет Аналитичес кая экспертиза 2 шаг Заявление на экспертизу + электронное регистрационное досье + образцы Центр обслуживания заявителей Заключение договора на проведение экспертизы в электронном формате (с ЭЦП) НЦЭЛС Экспертиза - 210 дней Заявитель 2 шаг да Фармацевт ическая экспертиза 1 ШАГ Заявление на регистрацию + Заключение о безопасности + регистрационн ый сбор Заключение эксперта Первичная экспертиза Заключение безопасности Отказ 1 шаг нет Заключение эксперта да да Заявитель I этап Предлагаемая схема: нет Фармаколо гическая экспертиза II – Этап Комитет контроля медицинской и фармацевтической деятельности (ККМФД) Электронное заявление на экспертизу + электронное регистрационное досье + образцы Экспертный совет нет Специализиро ванная экспертиза да нет Лабораторная экспертиза (с июля 2016 г. – отмена для РК и стран ICH, С 2018 г. – для всех) да Первичная экспертиза Фармакол огическая экспертиза нет 1. Единый экспертный отчет группой экспертов 2, Заключения безопасности Фармацевт ическая экспертиза да 2 ШАГ Выдача РУ (бумажная или электронная версия) Инструкции, АНД, макеты упаковок ККМФД Регистрация 10 рабочих дней 9

Фармацевтические инспекции Цель: Непрерывный контроль за безопасностью, эффективностью и качеством на всех этапах жизненного цикла лекарственных средств и медицинских изделий ТЕКУЩАЯ СИТУАЦИЯ: Ø Отсутствие обученного фармацевтического инспектората Ø Отсутствие обязательного требования наличия Gx. P МЕЖДУНАРОДНЫЙ ОПЫТ: Ø Регулярные инспекции всех субъектов обращения на соответствие требованиям Gx. P в до- и после регистрационный период РИСКИ: Ø Не полное обеспечение безопасности, эффективности и качества на всем жизненном цикле продукции 1 3 1 2 1 1 1 5 1 4 1 2 3 4 6 5 1 0 9 8 7 ПЕРСПЕКТИВНЫЕ ЗАДАЧИ: ШАГ 1. Приведение законодательства РК с рекомендациями PIC/S для вступления в PIC/S (включено в проект Кодекса РК в статьи «производство» , «инспекторат» , «регистрация» и др. ) ШАГ 2. Создание системы качества фармацевтического инспектората и обеспечение непрерывного обучения инспекторов, ежегодное участие в заседаниях Комитета PIC/S ШАГ 3. Внеплановые инспекции GMP, GCP, GLP, GVP, ISO 13485 производителей в процессе экспертизы лекарственных средств и медицинских изделий и плановые в пострегистрационный период (1 раз в 3 года) ШАГ 4. Вступление фармацевтического инспектората в систему международного сотрудничества фармацевтических инспекций (PIC/S) (2019 год) ОЖИДАЕМЫЙ РЕЗУЛЬТАТ: Ø Ø Комплексный подход к проведению инспекций Признание результатов инспекций в ЕАЭС и за рубежом Оперативное реагирование на оборот некачественной продукции Эффективный контроль за качеством продукции в пострегистрационный период 10
Оценка безопасности и качества (до 2019 г. ) Цель: Допуск на рынок безопасных , эффективных и качественных зарегистрированных лекарственных средств и изделий медицинского назначения ТЕКУЩАЯ СИТУАЦИЯ: Ø Применяются требования Государственной фармакопеи РК к качеству Ø Контроль каждой серии продукции с проведением лабораторных испытаний Ø Отсутствует контроль качества на рынке (изъятие с рынка), инспектирование МЕЖДУНАРОДНЫЙ ОПЫТ: 1 3 1 2 1 1 1 5 1 4 1 2 3 4 5 1 0 9 8 7 6 ПЕРСПЕКТИВНЫЕ ЗАДАЧИ: ШАГ 1. Внесены изменения в проект приказа МЗСР РК № 269 (с июля 2016 г): до 2019 года: Ø декларирование качества продукции путем отмены лабораторных испытаний лекарственных средств стран региона ICH и РК, произведенных по GМP Ø изъятие продукции с рынка 1 раз в 2 года для контроля качества ШАГ 2. С 2018 г. внедрение системы прослеживания продукции от производителя до конечного потребителя (включено в проект Кодекса РК) ШАГ 3. Переход от контроля качества к обеспечению качества Ø Выборочный контроль качества продукции на рынке Ø Отсутствует контроль каждой серии, партии продукции Ø Система обеспечения качества на всем жизненном цикле (внедрены Gx. P) ОЖИДАЕМЫЙ РЕЗУЛЬТАТ Ø Гармонизация с международными требованиями стран ОЭСР Ø Функционирование эффективной системы пострегистрационного контроля 11
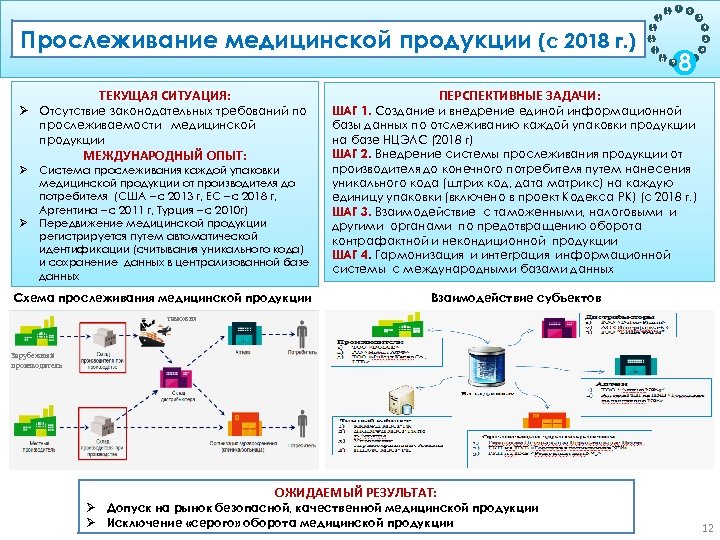
Прослеживание медицинской продукции (с 2018 г. ) Цель: Обеспечение прослеживаемости продукции на жизненном цикле Ø Отсутствие законодательных требований по прослеживаемости медицинской продукции МЕЖДУНАРОДНЫЙ ОПЫТ: Ø 1 2 3 4 5 1 0 9 8 6 7 ПЕРСПЕКТИВНЫЕ ЗАДАЧИ: ТЕКУЩАЯ СИТУАЦИЯ: Ø 1 3 1 2 1 1 1 5 1 4 Система прослеживания каждой упаковки медицинской продукции от производителя до потребителя (США – с 2013 г, ЕС – с 2018 г, Аргентина – с 2011 г, Турция – с 2010 г) Передвижение медицинской продукции регистрируется путем автоматической идентификации (считывания уникального кода) и сохранение данных в централизованной базе данных Схема прослеживания медицинской продукции ШАГ 1. Создание и внедрение единой информационной базы данных по отслеживанию каждой упаковки продукции на базе НЦЭЛС (2018 г) ШАГ 2. Внедрение системы прослеживания продукции от производителя до конечного потребителя путем нанесения уникального кода (штрих код, дата матрикс) на каждую единицу упаковки (включено в проект Кодекса РК) (с 2018 г. ) ШАГ 3. Взаимодействие с таможенными, налоговыми и другими органами по предотвращению оборота контрафактной и некондиционной продукции ШАГ 4. Гармонизация и интеграция информационной системы с международными базами данных Взаимодействие субъектов таможня Зарубежный производитель ОЖИДАЕМЫЙ РЕЗУЛЬТАТ: Ø Допуск на рынок безопасной, качественной медицинской продукции Ø Исключение «серого» оборота медицинской продукции 12
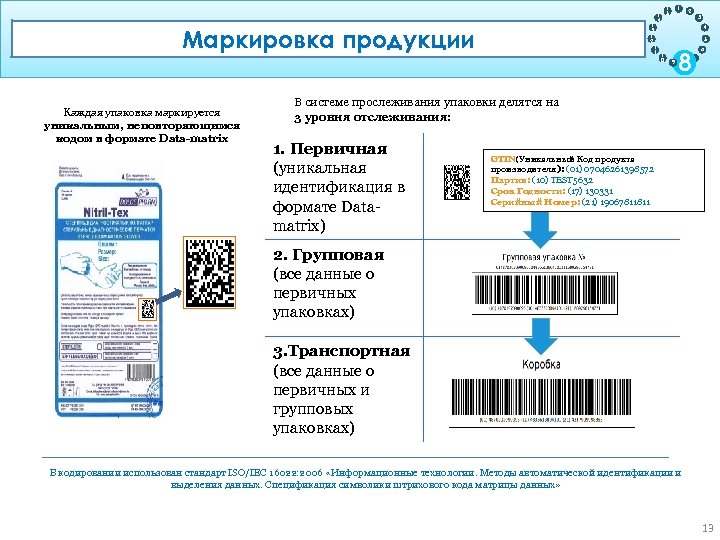
Цель: Маркировка продукции Обеспечение прослеживаемости продукции на жизненном цикле Каждая упаковка маркируется уникальным, неповторяющимся кодом в формате Data-matrix 1 3 1 2 1 1 1 5 1 4 1 2 3 4 5 1 0 9 8 6 7 В системе прослеживания упаковки делятся на 3 уровня отслеживания: 1. Первичная (уникальная идентификация в формате Datamatrix) GTIN(Уникальный Код продукта производителя ): (01) 07046261398572 Партия: (10) TEST 5632 Cрок Годности: (17) 130331 Серийный Номер: (21) 19067811811 2. Групповая (все данные о первичных упаковках) 3. Транспортная (все данные о первичных и групповых упаковках) В кодировании использован стандарт ISO/IEC 16022: 2006 «Информационные технологии. Методы автоматической идентификации и выделения данных. Спецификация символики штрихового кода матрицы данных» 13

Оптовая (дистрибуция) ипродукции на жизненном цикле розничная реализация Цель: Обеспечение прослеживаемости 1 3 1 2 1 1 1 4 1 5 1 2 3 4 5 10 9 8 6 7 Цель: Обеспечение безопасной и качественной медицинской продукцией ТЕКУЩАЯ СИТУАЦИЯ: Ø GDP – 40 дистрибьюторов из 2257 Ø GPP – 23 аптеки из 8063 Ø Реализуемая продукция должна быть зарегистрирована и иметь заключение о безопасности и качестве Ø Дистрибьютор должен иметь систему отзыва продукции МЕЖДУНАРОДНЫЙ ОПЫТ: Ø Оптовая реализация лекарственных средств осуществляется только дистрибьюторами имеющими GDP, розничная реализация - при наличии GPP ПЕРСПЕКТИВНЫЕ ЗАДАЧИ: Включено в проект Кодекса РК ШАГ 1. Внедрение GDP, GPP, GSP до 2018 года ШАГ 2. Обучение субъектов фармацевтического рынка ШАГ 3. Обязательное требования GDP, GPP, GSP с 2018 года РИСКИ: Ø При несоблюдении требований надлежащих практик существует опасность получения продукции потерявшей качество во время транспортировки, хранения и реализации ОЖИДАЕМЫЙ РЕЗУЛЬТАТ: Ø Получение населением безопасной и качественной продукции Ø Обеспечение качества услуг для населения 14

1 15 Фармаконадзор 2 14 3 13 Цель: Обеспечение прослеживаемости продукции на жизненном цикле 4 12 5 11 10 6 9 8 7 Цель: Обеспечение контроля в пострегистрационный период ТЕКУЩАЯ СИТУАЦИЯ: Ø РК с 2008 года является членом международной программы ВОЗ по мониторингу побочных действий (г. Уппсала, Швеция) Ø Низкая активность субъектов здравоохранения в выявлении и предоставлении карт сообщений по побочным действиям Ø Отсутствие ежегодной оценки соотношения польза/риск на зарегистрированные лекарственные средства, непрерывного мониторинга безопасности медицинских изделий Ø Отсутствие штрафных и административных санкций МЕЖДУНАРОДНЫЙ ОПЫТ: Ø Создана система фармаконадзора государства и держателя регистрационного удостоверения Ø Имеется законодательная ответственность держателей регистрационного удостоверения за безопасность лекарственных средств в пострегистрационный период ПЕРСПЕКТИВНЫЕ ЗАДАЧИ: ШАГ 1. Законодательное закрепление ответственности держателей регистрационных удостоверений (включено в проект Кодекса РК, административный Кодекс)(2016 год) ШАГ 2. Обучение субъектов фармацевтического рынка требованиям фармаконадзора (GVP) ШАГ 3. Ежегодная оценка соотношения польза/риск на зарегистрированные лекарственные средства, непрерывный мониторинг и оценка безопасности медицинских изделий (включено в проект Кодекса РК, ст. 71, 85 -1) РИСКИ: Ø Наличие на рынке лекарственных препаратов, у которых изменилось соотношение польза/риск в пострегистрационный период ОЖИДАЕМЫЙ РЕЗУЛЬТАТ: Ø Раннее обнаружение неизвестных побочных действий лекарственных средств Ø Рациональное и безопасное применение лекарственных средств Ø Эффективный мониторинг качества, безопасности, эффективности продукции в пострегистрационный период 15
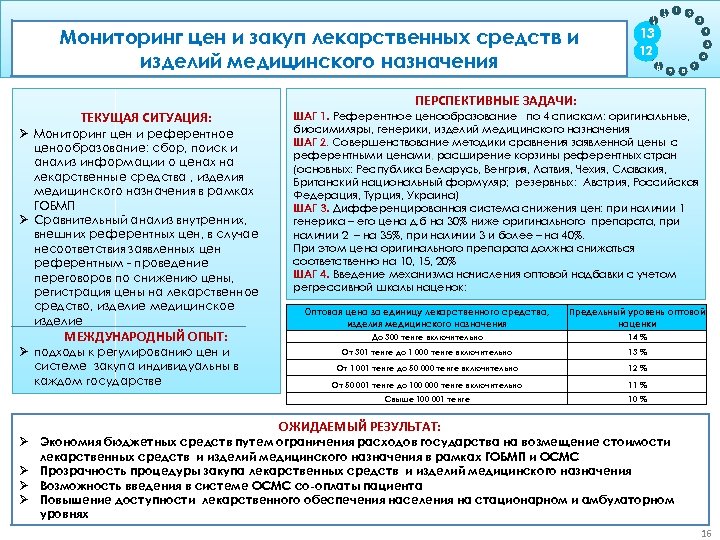
Мониторинг цен и закуп лекарственных средств и Цель: Обеспечение прослеживаемости продукции на жизненном цикле изделий медицинского назначения Цель: Регулирование ценообразования ЛС и системы закупа ТЕКУЩАЯ СИТУАЦИЯ: Ø Мониторинг цен и референтное ценообразование: сбор, поиск и анализ информации о ценах на лекарственные средства , изделия медицинского назначения в рамках ГОБМП Ø Сравнительный анализ внутренних, внешних референтных цен, в случае несоответствия заявленных цен референтным - проведение переговоров по снижению цены, регистрация цены на лекарственное средство, изделие медицинское изделие МЕЖДУНАРОДНЫЙ ОПЫТ: 1 2 3 13 12 1 1 4 5 6 1 0 9 8 7 ПЕРСПЕКТИВНЫЕ ЗАДАЧИ: ШАГ 1. Референтное ценообразование по 4 спискам: оригинальные, биосимиляры, генерики, изделий медицинского назначения ШАГ 2. Совершенствование методики сравнения заявленной цены с референтными ценами, расширение корзины референтных стран (основных: Республика Беларусь, Венгрия, Латвия, Чехия, Славакия, Британский национальный формуляр; резервных: Австрия, Российская Федерация, Турция, Украина) ШАГ 3. Дифференцированная система снижения цен: при наличии 1 генерика – его цена д. б на 30% ниже оригинального препарата, при наличии 2 – на 35%, при наличии 3 и более – на 40%. При этом цена оригинального препарата должна снижаться соответственно на 10, 15, 20% ШАГ 4. Введение механизма начисления оптовой надбавки с учетом регрессивной шкалы наценок: Оптовая цена за единицу лекарственного средства, изделия медицинского назначения Предельный уровень оптовой наценки До 300 тенге включительно 14 % От 301 тенге до 1 000 тенге включительно 13 % От 1 001 тенге до 50 000 тенге включительно 12 % От 50 001 тенге до 100 000 тенге включительно 11 % Свыше 100 001 тенге Ø подходы к регулированию цен и системе закупа индивидуальны в каждом государстве 1 5 1 4 10 % ОЖИДАЕМЫЙ РЕЗУЛЬТАТ: Ø Экономия бюджетных средств путем ограничения расходов государства на возмещение стоимости лекарственных средств и изделий медицинского назначения в рамках ГОБМП и ОСМС Ø Прозрачность процедуры закупа лекарственных средств и изделий медицинского назначения Ø Возможность введения в системе ОСМС со-оплаты пациента Ø Повышение доступности лекарственного обеспечения населения на стационарном и амбулаторном уровнях 16

Реклама прослеживаемости продукции на жизненном цикле медицинской продукции (МП) Обеспечение Цель: Регулирование ценообразования ЛС и системы закупа 14 1 1 5 2 3 1 3 4 1 2 5 1 1 6 1 0 9 8 7 Цель: Этическое продвижение медицинской продукции Ø Ø ТЕКУЩАЯ СИТУАЦИЯ: Законодательство в области рекламы медицинской продукции гармонизировано с международным законодательством (Директивой ЕС) Присутствует неэтическое продвижение лекарственных средств, медицинских изделий и медицинских услуг МЕЖДУНАРОДНЫЙ ОПЫТ: Ø Подходы к регулированию рекламы индивидуальны в каждом государстве ПЕРСПЕКТИВНЫЕ ЗАДАЧИ: ШАГ 1. Внедрение и использование Кодекса этического продвижения медицинской продукции (включено в проект Кодекса РК) ШАГ 2. Внесение изменений в Законодательство РК в части урегулирования интернет-продаж медицинской продукции и рекламы на Интернетресурсах Отпускаемые без рецепта Публичная реклама для населения: СМИ (телевидение, радио, медорганизации) Отпускаемые по рецепту Реклама для специалистов (специализированные издания, конференции) Реклама МП ОЖИДАЕМЫЙ РЕЗУЛЬТАТ: Ø Создание цивилизованного рынка медицинской продукции 17

Уничтожение прослеживаемости продукции на жизненном цикле Цель: Обеспечение Цель: Регулирование ценообразования ЛС и системы закупа 1 4 15 1 2 3 1 3 4 1 2 5 1 1 6 1 0 9 8 7 Цель: недопущение использование недоброкачественной продукции ТЕКУЩАЯ СИТУАЦИЯ: ПЕРСПЕКТИВНЫЕ ЗАДАЧИ: Ø Уничтожение медицинской продукции регламентировано приказом МЗСР РК от 26 августа 2015 года № 687 «Об утверждении Правил уничтожения лекарственных средств, изделий медицинского назначения и медицинской техники, пришедших в негодность, фальсифицированных, с истекшим сроком годности» Ø Уничтожение осуществляется непосредственно субъектом/организацией здравоохранения ШАГ 1. Ввести процедуру вывоза некачественной импортной продукции за пределы РК для дальнейшего уничтожения ШАГ 2. Ввести процедуру уничтожения отечественной продукции комиссией при Акиматах областей, городов Астана и Алматы с привлечением государственных органов МЕЖДУНАРОДНЫЙ ОПЫТ: Ø Подходы к регулированию индивидуальны в каждом государстве ОЖИДАЕМЫЙ РЕЗУЛЬТАТ: Ø Сохранение окружающей среды в стране 18
ОЖИДАЕМЫЕ РЕЗУЛЬТАТЫ СОВЕРШЕНСТВОВАНИЯ СИСТЕМЫ Цель: ДОПУСКА НА РЫНОК ЛЕКАРСТВЕННЫХ СРЕДСТВ И Обеспечение прослеживаемости продукции на жизненном цикле Цель: Регулирование ценообразования ЛС и системы закупа МЕДИЦИНСКИХ ИЗДЕЛИЙ 1 3 1 2 1 1 1 5 1 4 1 2 3 4 5 6 1 0 9 8 7 Гармонизированные подходы к регулированию обращения лекарственных средств и медицинских изделий с международными требованиями стран ОЭСР Обеспечение населения безопасными, эффективными и качественными лекарственными препаратами и медицинскими изделиями Создание эффективной регистрационного контроля системы до-и после Выпуск на рынок конкурентоспособной отечественной фармацевтической продукции 19
9b9bf9a692f951bfdfdadcc3f0d0ce19.ppt