Lektsiya_1-2009.ppt
- Количество слайдов: 67
 МІНІСТЕРСТВО ОХОРОНИ ЗДОРОВ’Я УКРАЇНИ Вінницький національний медичний університет імені М. І. Пирогова кафедра фармації Лекція № 1 з аптечної технології ліків та технології лікарських засобів для студентів ІІІ курсу фармацевтичного факультету спеціальностей “фармація”, “клінічна фармація” Тема: “Технологія лікарських форм як наука. Мета та завдання предмету. Основні поняття і терміни технології лікарських форм. Класифікація лікарських форм. Державне нормування виробництва лікарських препаратів та основна НТД” Лектор: к. ф. н. , доц. Кривов’яз О. В. м. Вінниця, 2012
МІНІСТЕРСТВО ОХОРОНИ ЗДОРОВ’Я УКРАЇНИ Вінницький національний медичний університет імені М. І. Пирогова кафедра фармації Лекція № 1 з аптечної технології ліків та технології лікарських засобів для студентів ІІІ курсу фармацевтичного факультету спеціальностей “фармація”, “клінічна фармація” Тема: “Технологія лікарських форм як наука. Мета та завдання предмету. Основні поняття і терміни технології лікарських форм. Класифікація лікарських форм. Державне нормування виробництва лікарських препаратів та основна НТД” Лектор: к. ф. н. , доц. Кривов’яз О. В. м. Вінниця, 2012
 План лекції o Технологія лікарських форм як наука o Мета та завдання предмету o Основні поняття і терміни технології лікарських форм o Класифікація лікарських форм o Державне нормування виробництва лікарських препаратів та основна нормативно-технічна документація
План лекції o Технологія лікарських форм як наука o Мета та завдання предмету o Основні поняття і терміни технології лікарських форм o Класифікація лікарських форм o Державне нормування виробництва лікарських препаратів та основна нормативно-технічна документація
 Аптечна технологія ліків приготування в аптечних умовах екстемпоральних ЛП, внутрішньоаптечних заготовок і фасування готових ЛП відповідно до вимог ДФУ, діючих наказів та інструкцій МОЗ України.
Аптечна технологія ліків приготування в аптечних умовах екстемпоральних ЛП, внутрішньоаптечних заготовок і фасування готових ЛП відповідно до вимог ДФУ, діючих наказів та інструкцій МОЗ України.
 Завдання фармацевтичної технології 1. Удосконалення існуючих (традиційних) методів виготовлення ЛФ. 2. Удосконалення складів та способів виготовлення (модифікація) традиційних ЛФ. 3. Створення нових методів виготовлення ЛФ на основі розвитку теорії та використання досягнень суміжних наук. 4. Створення ЛФ та систем доставки ЛР до органів та тканин, які були б здатні забезпечити оптимальний фармакологічний ефект, направлений транспорт, регульоване вивільнення, мінімальну побічну дію та зручність використання.
Завдання фармацевтичної технології 1. Удосконалення існуючих (традиційних) методів виготовлення ЛФ. 2. Удосконалення складів та способів виготовлення (модифікація) традиційних ЛФ. 3. Створення нових методів виготовлення ЛФ на основі розвитку теорії та використання досягнень суміжних наук. 4. Створення ЛФ та систем доставки ЛР до органів та тканин, які були б здатні забезпечити оптимальний фармакологічний ефект, направлений транспорт, регульоване вивільнення, мінімальну побічну дію та зручність використання.
 Перераховані задачі вирішують такими методами: o проведення наукових досліджень з використанням сучасних приладів, апаратів, методів аналізу, узагальненням експериментальних та теоретичних досліджень, застосуванням досягнень базових та суміжних наук; o розширення асортименту допоміжних речовин: нових носіїв ЛР, дисперсійних середовищ; речовин, що забезпечують фізико-хімічну, термодинамічну стабільність (стабілізаторів, диспергаторів, структуроутворювачів), антимікробну стабільність ЛФ (консервантів); коригуючих речовин; регуляторів швидкості та ступеня вивільнення діючої речовини, всмоктування, локалізації дії; o удосконалення технологічного процесу, створення та використання засобів механізації; o удосконалення упаковки з використанням сучасних упакувальних матеріалів; o уніфікування прописів лікарів, виготовлення препаратів за уніфікованими прописами в спеціалізованих аптеках у якості внутрішньоаптечної заготовки, на фармацевтичних фабриках, малих підприємствах та фірмах; o введення нових фізико-хімічних методів оцінки якості ЛФ, розробки та використання об’єктивних методів оцінки технологічних параметрів при контролі якості; o біофармацевтичного вивчення ЛФ та ЛП на усіх етапах їх створення (в дослідах in vitro – поза організмом, а також in vivo), використовуючи різні моделі.
Перераховані задачі вирішують такими методами: o проведення наукових досліджень з використанням сучасних приладів, апаратів, методів аналізу, узагальненням експериментальних та теоретичних досліджень, застосуванням досягнень базових та суміжних наук; o розширення асортименту допоміжних речовин: нових носіїв ЛР, дисперсійних середовищ; речовин, що забезпечують фізико-хімічну, термодинамічну стабільність (стабілізаторів, диспергаторів, структуроутворювачів), антимікробну стабільність ЛФ (консервантів); коригуючих речовин; регуляторів швидкості та ступеня вивільнення діючої речовини, всмоктування, локалізації дії; o удосконалення технологічного процесу, створення та використання засобів механізації; o удосконалення упаковки з використанням сучасних упакувальних матеріалів; o уніфікування прописів лікарів, виготовлення препаратів за уніфікованими прописами в спеціалізованих аптеках у якості внутрішньоаптечної заготовки, на фармацевтичних фабриках, малих підприємствах та фірмах; o введення нових фізико-хімічних методів оцінки якості ЛФ, розробки та використання об’єктивних методів оцінки технологічних параметрів при контролі якості; o біофармацевтичного вивчення ЛФ та ЛП на усіх етапах їх створення (в дослідах in vitro – поза організмом, а також in vivo), використовуючи різні моделі.
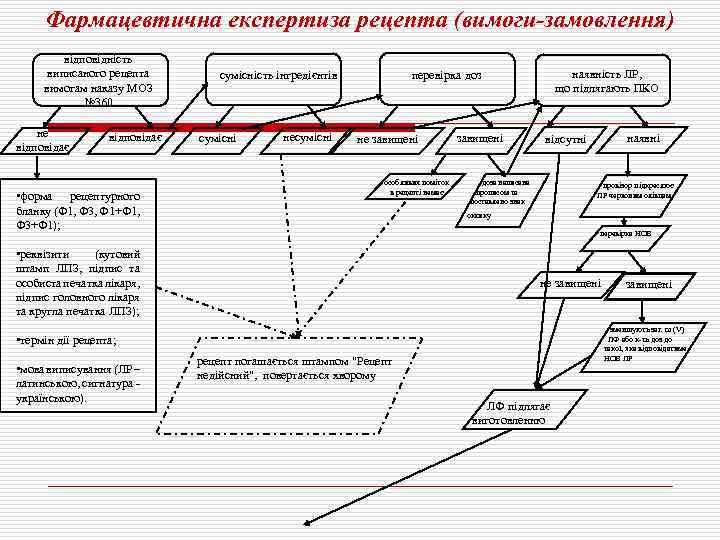 Фармацевтична експертиза рецепта (вимоги-замовлення) відповідність виписаного рецепта вимогам наказу МОЗ № 360 не відповідає • форма рецептурного бланку (Ф 1, Ф 3, Ф 1+Ф 1, Ф 3+Ф 1); сумісність інгредієнтів сумісні несумісні наявність ЛР, що підлягають ПКО перевірка доз не завищені особливих поміток в рецепті немає завищені доза написана прописом та поставлено знак провізор підкреслює ЛР червоним олівцем оклику перевірка НОВ • реквізити (кутовий штамп ЛПЗ, підпис та особиста печатка лікаря, підпис головного лікаря та кругла печатка ЛПЗ); не завищені зменшують заг. m (V) ЛФ або к-ть доз до такої, яка відповідатиме НОВ ЛР • термін дії рецепта; • мова виписування (ЛР – латинською, сигнатура українською). наявні відсутні рецепт погашається штампом "Рецепт недійсний", повертається хворому ЛФ підлягає виготовленню
Фармацевтична експертиза рецепта (вимоги-замовлення) відповідність виписаного рецепта вимогам наказу МОЗ № 360 не відповідає • форма рецептурного бланку (Ф 1, Ф 3, Ф 1+Ф 1, Ф 3+Ф 1); сумісність інгредієнтів сумісні несумісні наявність ЛР, що підлягають ПКО перевірка доз не завищені особливих поміток в рецепті немає завищені доза написана прописом та поставлено знак провізор підкреслює ЛР червоним олівцем оклику перевірка НОВ • реквізити (кутовий штамп ЛПЗ, підпис та особиста печатка лікаря, підпис головного лікаря та кругла печатка ЛПЗ); не завищені зменшують заг. m (V) ЛФ або к-ть доз до такої, яка відповідатиме НОВ ЛР • термін дії рецепта; • мова виписування (ЛР – латинською, сигнатура українською). наявні відсутні рецепт погашається штампом "Рецепт недійсний", повертається хворому ЛФ підлягає виготовленню
 розрахунок кількості інгредієнтів пропису таксування рецепта (визначення вартості ЛФ) видача хворому квитанції для отримання ЛФ після виготовлення (№ квитанції відповідає № рецепта) передача рецепта в асистентську кімнату для виготовлення ЛФ
розрахунок кількості інгредієнтів пропису таксування рецепта (визначення вартості ЛФ) видача хворому квитанції для отримання ЛФ після виготовлення (№ квитанції відповідає № рецепта) передача рецепта в асистентську кімнату для виготовлення ЛФ
 Виготовлення ЛФ Розрахунки кількостей інгредієнтів пропису проводять на звороті ППК (із зазначенням всіх формул, допоміжних речовин, загальної m (V), m (V) однієї дози, кількості виписаних доз). Лицевий бік ППК заповнюють після виготовлення ЛФ (ЛФ недозована) або перед стадією дозування (ЛФ дозована).
Виготовлення ЛФ Розрахунки кількостей інгредієнтів пропису проводять на звороті ППК (із зазначенням всіх формул, допоміжних речовин, загальної m (V), m (V) однієї дози, кількості виписаних доз). Лицевий бік ППК заповнюють після виготовлення ЛФ (ЛФ недозована) або перед стадією дозування (ЛФ дозована).
 До складу ЛФ входять ЛР на ПКО: Оформляють зворотний бік рецепта (в/з) для отримання таких ЛР у спеціаліста, що відповідає за їх зберігання, відпуск, облік: пишуть назву таких ЛР латинською мовою, вказують їх m (цифрами та прописом), дату одержання, свої підписи ставлять провізори, що видали та одержали ЛР. ППК заповнюється тільки на зворотному боці рецепта.
До складу ЛФ входять ЛР на ПКО: Оформляють зворотний бік рецепта (в/з) для отримання таких ЛР у спеціаліста, що відповідає за їх зберігання, відпуск, облік: пишуть назву таких ЛР латинською мовою, вказують їх m (цифрами та прописом), дату одержання, свої підписи ставлять провізори, що видали та одержали ЛР. ППК заповнюється тільки на зворотному боці рецепта.
 Контроль якості ЛФ o колір, запах, смак (лише дитячих ЛФ у випадку сумніву); o однорідність; o відсутність механічних включень; o відхилення в m (V); o відповідність упаковки m (V), виду ЛФ, властивостям інгредієнтів; o якість укупорки; o оформлення; o супровідна документація.
Контроль якості ЛФ o колір, запах, смак (лише дитячих ЛФ у випадку сумніву); o однорідність; o відсутність механічних включень; o відхилення в m (V); o відповідність упаковки m (V), виду ЛФ, властивостям інгредієнтів; o якість укупорки; o оформлення; o супровідна документація.
 Оформлення етикетки емблема медицини / емблема медицини та логотип суб’єкта господарювання / логотип суб’єкта господарювання o номер / назва аптеки, адреса, назва суб’єкта господарювання o номер рецепта або вимоги-замовлення o прізвище та ініціали хворого або номер та назва лікарні / відділення o назва та/або склад ЛЗ Склад ЛЗ пишеться українською та латинською мовами ( однією у разі відсутності місця на етикетці); заповнюється вручну або наноситься штампом o спосіб застосування (доза, частота та час приймання до чи після їжі) o приготував, перевірив, № аналізу o серія (для серійного виготовлення) – відповідає порядковому номеру в журналі лабораторно-фасувальних робіт o дата приготування o термін придатності o ціна o осмоляльність (осмолярність) та іонний склад внутрішньовенних інфузійних розчинів o
Оформлення етикетки емблема медицини / емблема медицини та логотип суб’єкта господарювання / логотип суб’єкта господарювання o номер / назва аптеки, адреса, назва суб’єкта господарювання o номер рецепта або вимоги-замовлення o прізвище та ініціали хворого або номер та назва лікарні / відділення o назва та/або склад ЛЗ Склад ЛЗ пишеться українською та латинською мовами ( однією у разі відсутності місця на етикетці); заповнюється вручну або наноситься штампом o спосіб застосування (доза, частота та час приймання до чи після їжі) o приготував, перевірив, № аналізу o серія (для серійного виготовлення) – відповідає порядковому номеру в журналі лабораторно-фасувальних робіт o дата приготування o термін придатності o ціна o осмоляльність (осмолярність) та іонний склад внутрішньовенних інфузійних розчинів o
 Супровідна документація o наявність рецепта; o наявність № рецепта на упаковці та на етикетці; o наявність та правильність оформлення ППК; o наявність та правильність оформлення сигнатури (у випадку, якщо до складу пропису входять ЛР на ПКО) – сигнатуру віддають хворому замість рецепта, а рецепт залишається та зберігається в аптеці.
Супровідна документація o наявність рецепта; o наявність № рецепта на упаковці та на етикетці; o наявність та правильність оформлення ППК; o наявність та правильність оформлення сигнатури (у випадку, якщо до складу пропису входять ЛР на ПКО) – сигнатуру віддають хворому замість рецепта, а рецепт залишається та зберігається в аптеці.
 Державне нормування виробництва ЛП 1. право на фармацевтичну діяльність; 2. склад ЛП; 3. умови приготування (які забезпечують якість препарату, техніку безпеки та охорону праці персоналу) та власне технологічний процес; 4. контроль якості ЛП на стадіях приготування та готового препарату.
Державне нормування виробництва ЛП 1. право на фармацевтичну діяльність; 2. склад ЛП; 3. умови приготування (які забезпечують якість препарату, техніку безпеки та охорону праці персоналу) та власне технологічний процес; 4. контроль якості ЛП на стадіях приготування та готового препарату.
 Нормативні документи o Державна фармакопея (ДФ), ДЕСТи, ГСТи; o накази, інструкції, методичні вказівки (рекомендації), затверджені МОЗ України; o виробничі технологічні регламенти (для умов промислового виробництва); o тимчасові (ТФС), фармакопейні (ФС) статті, затверджені Фармакологічним та Фармакопейним комітетами МОЗ України.
Нормативні документи o Державна фармакопея (ДФ), ДЕСТи, ГСТи; o накази, інструкції, методичні вказівки (рекомендації), затверджені МОЗ України; o виробничі технологічні регламенти (для умов промислового виробництва); o тимчасові (ТФС), фармакопейні (ФС) статті, затверджені Фармакологічним та Фармакопейним комітетами МОЗ України.
 Державна фармакопея України – збірник державних стандартів якості ЛЗ, який має законодавчий характер.
Державна фармакопея України – збірник державних стандартів якості ЛЗ, який має законодавчий характер.
 Основні терміни та поняття технології лікарських форм
Основні терміни та поняття технології лікарських форм
 Аптека – заклад охорони здоров’я, який функціонує на підставі ліцензії, в якому здійснюється виготовлення та/чи роздрібна реалізація ЛЗ, фармацевтичних та санітарно-гігієнічних товарів за правилами, встановленими чинним законодавством. Фармакологічний засіб (ФЗ) – речовина або суміш речовин зі встановленою фармакологічною активністю, яке є об’єктом клінічних досліджень. Лікарський засіб (ЛЗ) – ФЗ, що отримав позитивні результати клінічних досліджень, та затверджений Фармокологічним та Фармакопейним комітетами МОЗ України. ЛЗ – речовини, що застосовуються для профілактики, діагностики та лікування хвороби, попередження вагітності, отримані з крові, плазми крові, а також органів, тканин людини чи тварини, рослин, мікроорганізмів, мінералів методом синтеза чи з застосуванням біологічних технологій. Лікарська рослинна сировина (ЛРС) – рослинна сировина, дозволена уповноваженим на те органом у встановленому порядку для медичного застосування. Лікарська речовина (субстанція) (ЛР) – речовина рослинного, тваринного, мікробного або синтетичного походження, яка володіє фармакологічною активністю та призначена для виробництва ЛП.
Аптека – заклад охорони здоров’я, який функціонує на підставі ліцензії, в якому здійснюється виготовлення та/чи роздрібна реалізація ЛЗ, фармацевтичних та санітарно-гігієнічних товарів за правилами, встановленими чинним законодавством. Фармакологічний засіб (ФЗ) – речовина або суміш речовин зі встановленою фармакологічною активністю, яке є об’єктом клінічних досліджень. Лікарський засіб (ЛЗ) – ФЗ, що отримав позитивні результати клінічних досліджень, та затверджений Фармокологічним та Фармакопейним комітетами МОЗ України. ЛЗ – речовини, що застосовуються для профілактики, діагностики та лікування хвороби, попередження вагітності, отримані з крові, плазми крові, а також органів, тканин людини чи тварини, рослин, мікроорганізмів, мінералів методом синтеза чи з застосуванням біологічних технологій. Лікарська рослинна сировина (ЛРС) – рослинна сировина, дозволена уповноваженим на те органом у встановленому порядку для медичного застосування. Лікарська речовина (субстанція) (ЛР) – речовина рослинного, тваринного, мікробного або синтетичного походження, яка володіє фармакологічною активністю та призначена для виробництва ЛП.
 Терапевтична широта – інтервал доз від мінімальної терапевтичної до мінімальної смертельної. Терапевтичний індекс – відношення мінімальної смертельної дози до мінімальної терапевтичної. Стабільність – властивість ЛЗ (ФЗ) зберігати свої фізико-хімічні та мікробіологічні властивості протягом визначеного часу з моменту його випуску. Термін придатності – затвердженний законодавчим органом на основі результатів спеціального дослідження час зберігання ЛЗ, протягом якого препарат зберігає свої фізико-хімічні, мікробіологічні та терапевтичні властивості без змін або змінює їх у встановлених для нього межах при дотриманні умов зберігання. Допоміжні речовини – додаткові органічні або неорганічні речовини, які використовують у процесі виробництва готових ЛФ для надання їм необхідних властивостей. Лікарська форма (ЛФ) – зручний для застосування стан, який надається ЛЗ-бу або ЛРС-ні, при якому досягається необхідний лікувальний ефект. Лікарські препарати (ЛП) – дозовані ЛЗ у визначеній ЛФ. ЛП – це готовий продукт, який використовують з лікувальною, профілактичною, діагностичною метою, тобто ЛП готують з ЛЗ, надаючи їм за допомогою допоміжних речовин зручний для використання стан (ЛФ), завдяки чому досягається необхідний ефект.
Терапевтична широта – інтервал доз від мінімальної терапевтичної до мінімальної смертельної. Терапевтичний індекс – відношення мінімальної смертельної дози до мінімальної терапевтичної. Стабільність – властивість ЛЗ (ФЗ) зберігати свої фізико-хімічні та мікробіологічні властивості протягом визначеного часу з моменту його випуску. Термін придатності – затвердженний законодавчим органом на основі результатів спеціального дослідження час зберігання ЛЗ, протягом якого препарат зберігає свої фізико-хімічні, мікробіологічні та терапевтичні властивості без змін або змінює їх у встановлених для нього межах при дотриманні умов зберігання. Допоміжні речовини – додаткові органічні або неорганічні речовини, які використовують у процесі виробництва готових ЛФ для надання їм необхідних властивостей. Лікарська форма (ЛФ) – зручний для застосування стан, який надається ЛЗ-бу або ЛРС-ні, при якому досягається необхідний лікувальний ефект. Лікарські препарати (ЛП) – дозовані ЛЗ у визначеній ЛФ. ЛП – це готовий продукт, який використовують з лікувальною, профілактичною, діагностичною метою, тобто ЛП готують з ЛЗ, надаючи їм за допомогою допоміжних речовин зручний для використання стан (ЛФ), завдяки чому досягається необхідний ефект.
 Принципи класифікації ЛФ o o шляхи введення; способи призначення; агрегатний стан; властивості дисперсійного середовища.
Принципи класифікації ЛФ o o шляхи введення; способи призначення; агрегатний стан; властивості дисперсійного середовища.
 Класифікація ЛФ з урахуванням шляхів введення ентеральні (через ШКТ) пероральні: пероральні • таблетки • капсули • драже • гранули • порошки • мікрокапсули • розчини • суспензії • емульсії • настої • відвари • настойки • сиропи • желе парентеральні (у вигляді ін’єкцій) сублінгвальні: сублінгвальні • таблетки • капсули • драже • порошки • таблетки для жування • розчини • порошки і таблетки для отримання розчинів • суспензії • емульсії • ліпосомальні системи • таблетки та капсули для імплантацій ректальні • супозиторії • капсули • мазі • піно- та плівкоутворюючі аерозолі • розчини • суспензії (у вигляді мікро • емульсії клізм та зрошення) NB! Для ЛР списків А та/чи Б в складу даних ЛФ перевірка доз проводиться!!! проводиться
Класифікація ЛФ з урахуванням шляхів введення ентеральні (через ШКТ) пероральні: пероральні • таблетки • капсули • драже • гранули • порошки • мікрокапсули • розчини • суспензії • емульсії • настої • відвари • настойки • сиропи • желе парентеральні (у вигляді ін’єкцій) сублінгвальні: сублінгвальні • таблетки • капсули • драже • порошки • таблетки для жування • розчини • порошки і таблетки для отримання розчинів • суспензії • емульсії • ліпосомальні системи • таблетки та капсули для імплантацій ректальні • супозиторії • капсули • мазі • піно- та плівкоутворюючі аерозолі • розчини • суспензії (у вигляді мікро • емульсії клізм та зрошення) NB! Для ЛР списків А та/чи Б в складу даних ЛФ перевірка доз проводиться!!! проводиться
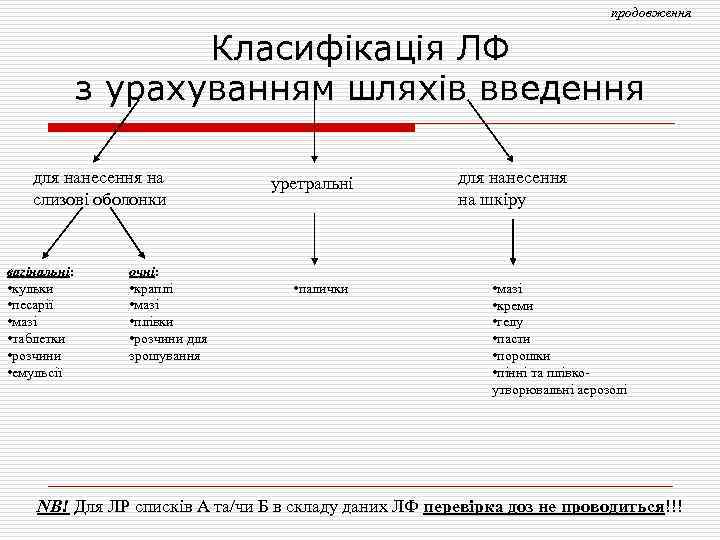 продовження Класифікація ЛФ з урахуванням шляхів введення для нанесення на слизові оболонки вагінальні: вагінальні • кульки • песарії • мазі • таблетки • розчини • емульсії очні: очні • краплі • мазі • плівки • розчини для зрошування уретральні • палички для нанесення на шкіру • мазі • креми • гелу • пасти • порошки • пінні та плівкоутворювальні аерозолі NB! Для ЛР списків А та/чи Б в складу даних ЛФ перевірка доз не проводиться!!! проводиться
продовження Класифікація ЛФ з урахуванням шляхів введення для нанесення на слизові оболонки вагінальні: вагінальні • кульки • песарії • мазі • таблетки • розчини • емульсії очні: очні • краплі • мазі • плівки • розчини для зрошування уретральні • палички для нанесення на шкіру • мазі • креми • гелу • пасти • порошки • пінні та плівкоутворювальні аерозолі NB! Для ЛР списків А та/чи Б в складу даних ЛФ перевірка доз не проводиться!!! проводиться
 Накази, інструкції, методичні вказівки (рекомендації), затверджені МОЗ України 1. 2. 3. 4. 5. 6. 7. 8. Закон України “Про лікарські засоби” від 14. 02. 1997 р. Наказ МОЗ України № 275 від 15. 05. 2006 р. “Про затвердження Інструкції із санітарно-протиепідемічного режиму аптечних закладів” Наказ МОЗ України № 44 від 16. 03. 1993 р. “Про організацію зберігання в аптечних установах різних груп лікарських засобів та виробів медичного призначення” Наказ МОЗ України № 360 від 19. 07. 2005 р. “Про затвердження Правил виписування рецептів та вимог-замовлень на лікарські засоби і вироби медичного призначення, Порядку відпуску лікарських засобів і виробів медичного призначення з аптек та їх структурних підрозділів, Інструкції про порядок зберігання, обліку та знищення рецептурних бланків та вимог-замовлень” Наказ МОЗ України № 626 від 15. 12. 2004 р. “Про затвердження Правил виробництва (виготовлення) лікарських засобів в умовах аптеки” Наказ МОЗ України № 11 “Про затвердження обігу наркотичних засобів, психотропних речовин та прекурсорів в державних і комунальних закладах охорони здоров’я” Наказ МОЗ України № 197 від 07. 09. 1993 р. “Про затвердження Інструкції по приготуванню в аптеках лікарських форм з рідким дисперсійним середовищем” Наказ МОЗ України № 8 від 15. 01. 2003 р. “Про затвердження переліків допоміжних речовин та барвників, дозволених для застосування у виробництві лікарських засобів, що (лікарські засоби) реєструються в Україні та виготовляються в аптечних умовах за рецептами лікарів і замовленнями лікувальнопрофілактичних закладів”
Накази, інструкції, методичні вказівки (рекомендації), затверджені МОЗ України 1. 2. 3. 4. 5. 6. 7. 8. Закон України “Про лікарські засоби” від 14. 02. 1997 р. Наказ МОЗ України № 275 від 15. 05. 2006 р. “Про затвердження Інструкції із санітарно-протиепідемічного режиму аптечних закладів” Наказ МОЗ України № 44 від 16. 03. 1993 р. “Про організацію зберігання в аптечних установах різних груп лікарських засобів та виробів медичного призначення” Наказ МОЗ України № 360 від 19. 07. 2005 р. “Про затвердження Правил виписування рецептів та вимог-замовлень на лікарські засоби і вироби медичного призначення, Порядку відпуску лікарських засобів і виробів медичного призначення з аптек та їх структурних підрозділів, Інструкції про порядок зберігання, обліку та знищення рецептурних бланків та вимог-замовлень” Наказ МОЗ України № 626 від 15. 12. 2004 р. “Про затвердження Правил виробництва (виготовлення) лікарських засобів в умовах аптеки” Наказ МОЗ України № 11 “Про затвердження обігу наркотичних засобів, психотропних речовин та прекурсорів в державних і комунальних закладах охорони здоров’я” Наказ МОЗ України № 197 від 07. 09. 1993 р. “Про затвердження Інструкції по приготуванню в аптеках лікарських форм з рідким дисперсійним середовищем” Наказ МОЗ України № 8 від 15. 01. 2003 р. “Про затвердження переліків допоміжних речовин та барвників, дозволених для застосування у виробництві лікарських засобів, що (лікарські засоби) реєструються в Україні та виготовляються в аптечних умовах за рецептами лікарів і замовленнями лікувальнопрофілактичних закладів”
 Наказ МОЗ України № 44 від 16. 03. 1993 р. “Про організацію зберігання в аптечних установах різних груп лікарських засобів та виробів медичного призначення”
Наказ МОЗ України № 44 від 16. 03. 1993 р. “Про організацію зберігання в аптечних установах різних груп лікарських засобів та виробів медичного призначення”
 Вимоги до упорядкування і експлуатації приміщень для зберігання o o o В приміщеннях для зберігання повинна підтримуваться певна температура і вологість повітря, періодичність перевірки яких здійснюється не рідше 1 разу на добу. Для спостереження за цими параметрами складські приміщення необхідно забезпечить термометрами і гігрометрами, які кріпляться на внутрішніх стінах сховища віддалік від нагрівальних приладів на висоті (1. 5 -1. 7) м від підлоги та віддалі не менш 3 м від дверей. В кожному відділі має бути заведена карта обліку температури та відносної вологості. Приміщення для зберігання обладнати припливно-витяжною вентиляцією з механічним спонуканням Приміщення для зберігання обладнуються приладами центрального опалення. Не допускається опалення приміщень газовими приладами з відкритим полум'ям або електронагрівальними приладами з відкритою електроспіраллю Встановлення стелажів здійснюється таким чином, щоб вони знаходились на відстані (0. 6 -0. 7) м від зовнішніх стін, не менше ніж 0. 5 м від стелі та не менш ніж 0. 25 м від підлоги. Стелажі по відношеннюдо вікон повинні бути розташовані так, щоб проходи були освітлені, а відстань між стелажами становила не менш 0. 75 м для забезпечення вільного доступу до товару Підлога приміщень періодично (але не рідше одного разу в день) прибирається вологим способом із застосуванням дозволених миючих засобів
Вимоги до упорядкування і експлуатації приміщень для зберігання o o o В приміщеннях для зберігання повинна підтримуваться певна температура і вологість повітря, періодичність перевірки яких здійснюється не рідше 1 разу на добу. Для спостереження за цими параметрами складські приміщення необхідно забезпечить термометрами і гігрометрами, які кріпляться на внутрішніх стінах сховища віддалік від нагрівальних приладів на висоті (1. 5 -1. 7) м від підлоги та віддалі не менш 3 м від дверей. В кожному відділі має бути заведена карта обліку температури та відносної вологості. Приміщення для зберігання обладнати припливно-витяжною вентиляцією з механічним спонуканням Приміщення для зберігання обладнуються приладами центрального опалення. Не допускається опалення приміщень газовими приладами з відкритим полум'ям або електронагрівальними приладами з відкритою електроспіраллю Встановлення стелажів здійснюється таким чином, щоб вони знаходились на відстані (0. 6 -0. 7) м від зовнішніх стін, не менше ніж 0. 5 м від стелі та не менш ніж 0. 25 м від підлоги. Стелажі по відношеннюдо вікон повинні бути розташовані так, щоб проходи були освітлені, а відстань між стелажами становила не менш 0. 75 м для забезпечення вільного доступу до товару Підлога приміщень періодично (але не рідше одного разу в день) прибирається вологим способом із застосуванням дозволених миючих засобів
 Зберігають окремо: oтоксикологічні групи: список А (отруйні та наркотичні речовини), список Б (сильнодіючі речовини) та загальний список; o. ЛЗ списків А і Б повинні зберігатися: ь у відповідності з фармакологічними групами; ь в залежності від способу вживання; ь ЛЗ “ангро” у відповідності з агрегатним станом (рідкі, сипучі, газоподібні); ь у відповідності з фізико-хімічними властивостями ЛЗ та впливом різних факторів навколишнього середовища: ь з урахуванням установлених термінів придітності для ЛЗ; ь з урахуванням характеру різних ЛФ. • ВМП слід зберігати окремо за групами: ь ь гумові вироби; вироби з пластмас; перев’язочні засоби та допоміжні матеріали; вироби медичної техніки.
Зберігають окремо: oтоксикологічні групи: список А (отруйні та наркотичні речовини), список Б (сильнодіючі речовини) та загальний список; o. ЛЗ списків А і Б повинні зберігатися: ь у відповідності з фармакологічними групами; ь в залежності від способу вживання; ь ЛЗ “ангро” у відповідності з агрегатним станом (рідкі, сипучі, газоподібні); ь у відповідності з фізико-хімічними властивостями ЛЗ та впливом різних факторів навколишнього середовища: ь з урахуванням установлених термінів придітності для ЛЗ; ь з урахуванням характеру різних ЛФ. • ВМП слід зберігати окремо за групами: ь ь гумові вироби; вироби з пластмас; перев’язочні засоби та допоміжні матеріали; вироби медичної техніки.
 Вимоги, які пред'являються до зберігання різних груп лікарських засобів та виробів медичного призначення o o o o - які вимагають захисту від світла; - які вимагають захисту від дії вологи; - які вимагають захисту від випаровування; - які вимагають захисту від дії підвищеної температури; - які вимагають захисту від поинженої температури; - які вимагають захисту від дії газів, що містяться в навколишньому середовищи; - пахучі, барвні; - дезінфікуючі засоби.
Вимоги, які пред'являються до зберігання різних груп лікарських засобів та виробів медичного призначення o o o o - які вимагають захисту від світла; - які вимагають захисту від дії вологи; - які вимагають захисту від випаровування; - які вимагають захисту від дії підвищеної температури; - які вимагають захисту від поинженої температури; - які вимагають захисту від дії газів, що містяться в навколишньому середовищи; - пахучі, барвні; - дезінфікуючі засоби.
 пахучих ЛЗ o o o o Перелік аміаку розчин валідол дьоготь іхтіол йодоформ камфора ксероформ метилсаліцилат нашатирно-анісові краплі скипидар тимол фенол формальдегіду розчин хлорамін Б ефірні олії o o o летких ЛЗ аміаку розчин бромкамфора йодоформ камфора метилсаліцилат ментол тимол формальдегід хлоралгідрат ефірні олії
пахучих ЛЗ o o o o Перелік аміаку розчин валідол дьоготь іхтіол йодоформ камфора ксероформ метилсаліцилат нашатирно-анісові краплі скипидар тимол фенол формальдегіду розчин хлорамін Б ефірні олії o o o летких ЛЗ аміаку розчин бромкамфора йодоформ камфора метилсаліцилат ментол тимол формальдегід хлоралгідрат ефірні олії
 Перелік барвних ЛЗ o акрихін o діамантовий зелений o індигокармін для ін’єкцій o калію перманганат o метиленовий синій o рибофлавін o фурацилін o етакридину лактат
Перелік барвних ЛЗ o акрихін o діамантовий зелений o індигокармін для ін’єкцій o калію перманганат o метиленовий синій o рибофлавін o фурацилін o етакридину лактат
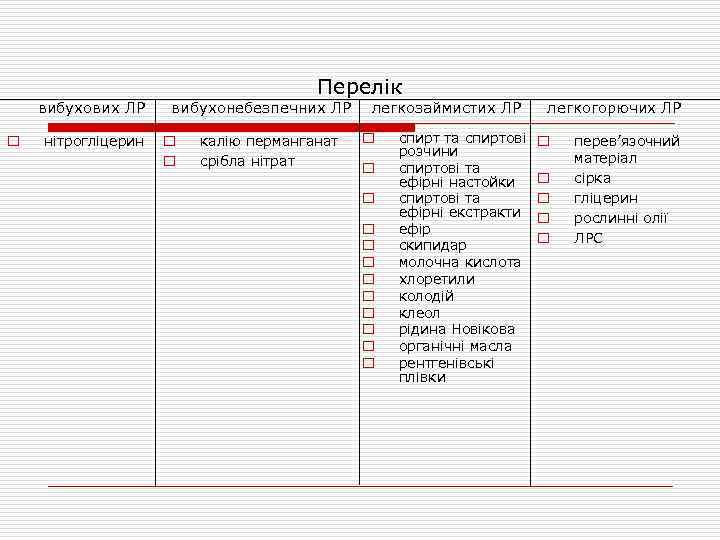 вибухових ЛР o нітрогліцерин Перелік вибухонебезпечних ЛР o o калію перманганат срібла нітрат легкозаймистих ЛР o o o спирт та спиртові розчини спиртові та ефірні настойки спиртові та ефірні екстракти ефір скипидар молочна кислота хлоретили колодій клеол рідина Новікова органічні масла рентгенівські плівки легкогорючих ЛР o o o перев’язочний матеріал сірка гліцерин рослинні олії ЛРС
вибухових ЛР o нітрогліцерин Перелік вибухонебезпечних ЛР o o калію перманганат срібла нітрат легкозаймистих ЛР o o o спирт та спиртові розчини спиртові та ефірні настойки спиртові та ефірні екстракти ефір скипидар молочна кислота хлоретили колодій клеол рідина Новікова органічні масла рентгенівські плівки легкогорючих ЛР o o o перев’язочний матеріал сірка гліцерин рослинні олії ЛРС
 Наказ МОЗ України № 360 від 19. 07. 2005 р. “Про затвердження Правил виписування рецептів та вимогзамовлень на лікарські засоби і вироби медичного призначення, Порядку відпуску лікарських засобів і виробів медичного призначення з аптек та їх структурних підрозділів, Інструкції про порядок зберігання, обліку та знищення рецептурних бланків та вимог-замовлень”
Наказ МОЗ України № 360 від 19. 07. 2005 р. “Про затвердження Правил виписування рецептів та вимогзамовлень на лікарські засоби і вироби медичного призначення, Порядку відпуску лікарських засобів і виробів медичного призначення з аптек та їх структурних підрозділів, Інструкції про порядок зберігання, обліку та знищення рецептурних бланків та вимог-замовлень”
 Форма рецептурного бланка № 1 (ф-1) для виписування лікарських засобів і виробів медичного призначення, що відпускаються за повну вартість, безоплатно, з оплатою 50%, і таких, що підлягають предметно-кількісному обліку (розмір 105 х 150) Назва закладу (штамп закладу) Код закладу за ЗКУД Код закладу за ЗКПО Медична документація ф-1 ____________________________ Номер рецепта N______ РЕЦЕПТ "________ 20 _ р. (дорослий, дитячий (дата виписки рецепта) потрібне підкреслити) ____________________________ За повну вартість Безоплатно Оплата 50% ____________________________ Прізвище, ім'я та по батькові і вік хворого ______________________ Адреса хворого або номер медичної карти амбулаторного хворого _______________ Прізвище, ім'я та по батькові лікаря _______________________________________________________ I Rp: I I ____________________________ Підпис та особиста печатка лікаря (розбірливо) М. П.
Форма рецептурного бланка № 1 (ф-1) для виписування лікарських засобів і виробів медичного призначення, що відпускаються за повну вартість, безоплатно, з оплатою 50%, і таких, що підлягають предметно-кількісному обліку (розмір 105 х 150) Назва закладу (штамп закладу) Код закладу за ЗКУД Код закладу за ЗКПО Медична документація ф-1 ____________________________ Номер рецепта N______ РЕЦЕПТ "________ 20 _ р. (дорослий, дитячий (дата виписки рецепта) потрібне підкреслити) ____________________________ За повну вартість Безоплатно Оплата 50% ____________________________ Прізвище, ім'я та по батькові і вік хворого ______________________ Адреса хворого або номер медичної карти амбулаторного хворого _______________ Прізвище, ім'я та по батькові лікаря _______________________________________________________ I Rp: I I ____________________________ Підпис та особиста печатка лікаря (розбірливо) М. П.
 Пам'ятка лікарю (друкується на зворотному боці рецептурного бланка) Код лікувально-профілактичного закладу друкується друкарським способом або ставиться штамп. Рецепт виписується латинською мовою, розбірливо, чітко, чорнилом або кульковою ручкою, виправлення забороняються. На одному рецептурному бланку виписується: одне найменування лікарського засобу, що вміщує отруйні або наркотичні лікарські засоби або 1 -3 найменування інших лікарських засобів. Дозволяються тільки прийняті правилами скорочення позначень. Тверді і сипучі речовини в грамах (0, 01; 0, 5; 1, 0), рідкі – в мілілітрах, грамах і краплях. Спосіб вживання пишеться державною мовою відповідно до Закону України "Про мови в Українській РСР", забороняється обмежуватись загальними вказівками: "Внутрішнє", "Зовнішнє", "Відомо" і т. ін. ____________ Штамп аптеки ____________ № лікарської форми індивідуального виготовлення Перевірив Відпустив __________________________ Прийняв Виготовив
Пам'ятка лікарю (друкується на зворотному боці рецептурного бланка) Код лікувально-профілактичного закладу друкується друкарським способом або ставиться штамп. Рецепт виписується латинською мовою, розбірливо, чітко, чорнилом або кульковою ручкою, виправлення забороняються. На одному рецептурному бланку виписується: одне найменування лікарського засобу, що вміщує отруйні або наркотичні лікарські засоби або 1 -3 найменування інших лікарських засобів. Дозволяються тільки прийняті правилами скорочення позначень. Тверді і сипучі речовини в грамах (0, 01; 0, 5; 1, 0), рідкі – в мілілітрах, грамах і краплях. Спосіб вживання пишеться державною мовою відповідно до Закону України "Про мови в Українській РСР", забороняється обмежуватись загальними вказівками: "Внутрішнє", "Зовнішнє", "Відомо" і т. ін. ____________ Штамп аптеки ____________ № лікарської форми індивідуального виготовлення Перевірив Відпустив __________________________ Прийняв Виготовив
 Спеціальний рецептурний бланк форми N 3 для виписування наркотичних та психотропних лікарських засобів Ідентифікаційний код згідно Код згідно з ДКУД _______ з ЄДРПОУ ______________ Медична документація ф-3 (назва закладу) (штамп закладу) РЕЦЕПТ на право одержання лікарського засобу, що містить наркотичну чи психотропну речовину (документ суворої звітності) Серія _______ № _______ 200__ р. Прізвище та ініціали, вік хворого _______________________________ Адреса хворого та номер медичної картки амбулаторного хворого Історія хвороби (амбулаторна картка) № _____ Прізвище та ініціали лікаря ___________________ Rp: ___________________ Підпис і особиста Печатка лікувального печатка лікаря (розбірливо) закладу
Спеціальний рецептурний бланк форми N 3 для виписування наркотичних та психотропних лікарських засобів Ідентифікаційний код згідно Код згідно з ДКУД _______ з ЄДРПОУ ______________ Медична документація ф-3 (назва закладу) (штамп закладу) РЕЦЕПТ на право одержання лікарського засобу, що містить наркотичну чи психотропну речовину (документ суворої звітності) Серія _______ № _______ 200__ р. Прізвище та ініціали, вік хворого _______________________________ Адреса хворого та номер медичної картки амбулаторного хворого Історія хвороби (амбулаторна картка) № _____ Прізвище та ініціали лікаря ___________________ Rp: ___________________ Підпис і особиста Печатка лікувального печатка лікаря (розбірливо) закладу
 Рецепт o кутовий штамп ЗОЗ o підпис та особиста печатка лікаря o підпис керівника ЗОЗ та кругла печатка суб’єкта господарювання (на Ф-1, які залишаються в аптеці, та на Ф-3) o виписується чітко та розбірливо чорнилом або кульковою ручкою o специфічні помітки та вказівки лікаря додатково завіряються його підписом та печаткою
Рецепт o кутовий штамп ЗОЗ o підпис та особиста печатка лікаря o підпис керівника ЗОЗ та кругла печатка суб’єкта господарювання (на Ф-1, які залишаються в аптеці, та на Ф-3) o виписується чітко та розбірливо чорнилом або кульковою ручкою o специфічні помітки та вказівки лікаря додатково завіряються його підписом та печаткою
 Ф-1 за повну вартість: oнесильнодіючі та сильнодіючі ЛР за індивідуальними прописами. !!!Підпис та особиста печатка лікаря. !!! Термін дії – 1 місяць !!! Зберігання – не зберігаються за повну вартість: o. ЛР, що підлягають ПКО, крім наркотичних та психотропних; oнаркотичні та психотропні ЛР в суміші з фармакологічно-активними ЛР. !!!Підпис та особиста печатка лікаря. !!! Додатково підпис керівника та печатка ЗОЗ !!! Термін дії – 1 місяць !!! Зберігання – 1 рік, не враховуючи поточного у замкнених шафах безоплатно чи на пільгових умовах: o несильнодіючі та сильнодіючі ЛР за індивідуальними прописами; !!!Підпис та особиста печатка лікаря. !!! Додатково підпис керівника та печатка ЗОЗ !!! Термін дії – 1 місяць !!! Зберігання – 3 роки, не враховуючи поточного у замкнених шафах Ф-3 за повну вартість: oнаркотичні та психотропні ЛР в чистому вигляді; o наркотичні та психотропні ЛР в суміші з індиферентними речовинами. !!!Підпис та особиста печатка лікаря. !!! Додатково підпис керівника та печатка ЗОЗ !!! Термін дії – 5 днів !!! Зберігання – 5 років, не враховуючи поточного у вогнетривких сейфах
Ф-1 за повну вартість: oнесильнодіючі та сильнодіючі ЛР за індивідуальними прописами. !!!Підпис та особиста печатка лікаря. !!! Термін дії – 1 місяць !!! Зберігання – не зберігаються за повну вартість: o. ЛР, що підлягають ПКО, крім наркотичних та психотропних; oнаркотичні та психотропні ЛР в суміші з фармакологічно-активними ЛР. !!!Підпис та особиста печатка лікаря. !!! Додатково підпис керівника та печатка ЗОЗ !!! Термін дії – 1 місяць !!! Зберігання – 1 рік, не враховуючи поточного у замкнених шафах безоплатно чи на пільгових умовах: o несильнодіючі та сильнодіючі ЛР за індивідуальними прописами; !!!Підпис та особиста печатка лікаря. !!! Додатково підпис керівника та печатка ЗОЗ !!! Термін дії – 1 місяць !!! Зберігання – 3 роки, не враховуючи поточного у замкнених шафах Ф-3 за повну вартість: oнаркотичні та психотропні ЛР в чистому вигляді; o наркотичні та психотропні ЛР в суміші з індиферентними речовинами. !!!Підпис та особиста печатка лікаря. !!! Додатково підпис керівника та печатка ЗОЗ !!! Термін дії – 5 днів !!! Зберігання – 5 років, не враховуючи поточного у вогнетривких сейфах
 Ф-1+Ф-1 безоплатно чи на пільгових умовах: o. ЛР, що підлягають ПКО, крім наркотичних та психотропних; oнаркотичні та психотропні ЛР в суміші з фармакологічно-активними ЛР. !!!Підпис та особиста печатка лікаря. !!! Додатково підпис керівника та печатка ЗОЗ !!! Термін дії – 1 місяць !!! Зберігання – 3 роки, не враховуючи поточного у замкнених шафах Ф-3+Ф-1 безоплатно чи на пільгових умовах: oнаркотичні та психотропні ЛР в чистому вигляді; o наркотичні та психотропні ЛР в суміші з індиферентними речовинами. !!!Підпис та особиста печатка лікаря. !!! Додатково підпис керівника та печатка ЗОЗ !!! Термін дії – 5 днів !!! Зберігання – 5 років, не враховуючи поточного у вогнетривких сейфах
Ф-1+Ф-1 безоплатно чи на пільгових умовах: o. ЛР, що підлягають ПКО, крім наркотичних та психотропних; oнаркотичні та психотропні ЛР в суміші з фармакологічно-активними ЛР. !!!Підпис та особиста печатка лікаря. !!! Додатково підпис керівника та печатка ЗОЗ !!! Термін дії – 1 місяць !!! Зберігання – 3 роки, не враховуючи поточного у замкнених шафах Ф-3+Ф-1 безоплатно чи на пільгових умовах: oнаркотичні та психотропні ЛР в чистому вигляді; o наркотичні та психотропні ЛР в суміші з індиферентними речовинами. !!!Підпис та особиста печатка лікаря. !!! Додатково підпис керівника та печатка ЗОЗ !!! Термін дії – 5 днів !!! Зберігання – 5 років, не враховуючи поточного у вогнетривких сейфах
 СИГНАТУРА _____________ назва населеного пункту Аптека № _______ Рецепт № ____ Прізвище, ім’я та по батькові і вік хворого _________________________________________________ Rр: Прізвище, ім’я та по батькові__________________________________ Приготував _____________________________ Перевірив ______________________________ Відпустив ______________________________ Дата ___________________ Ціна ___________ Для повторного відпуску ліків необхідний новий рецепт лікаря.
СИГНАТУРА _____________ назва населеного пункту Аптека № _______ Рецепт № ____ Прізвище, ім’я та по батькові і вік хворого _________________________________________________ Rр: Прізвище, ім’я та по батькові__________________________________ Приготував _____________________________ Перевірив ______________________________ Відпустив ______________________________ Дата ___________________ Ціна ___________ Для повторного відпуску ліків необхідний новий рецепт лікаря.
 ПЕРЕЛІК лікарських засобів, що підлягають ПКО в закладах охорони здоров'я 1. Наркотичні лікарські засоби. 2. Психотропні лікарські засоби. 3. Отруйні та сильнодіючі лікарські засоби (за міжнародними непатентованими назвами): атропін та його солі (порошок), буторфанол, клонідин, тетракаїн (порошок), трамадол, тригексифенідил. 4. Наркотичні (психотропні) комбіновані лікарські засоби, які містять на одиницю дози (у перерахунку на безводну основу): кодеїну декстропропоксифену фенобарбіталу ефедрину псевдоефедрину фенілпропаноламіну ерготаміну ергометрину більше більше 10 мг 50 мг 20 мг 15 мг 30 мг 2 мг 0, 2 мг
ПЕРЕЛІК лікарських засобів, що підлягають ПКО в закладах охорони здоров'я 1. Наркотичні лікарські засоби. 2. Психотропні лікарські засоби. 3. Отруйні та сильнодіючі лікарські засоби (за міжнародними непатентованими назвами): атропін та його солі (порошок), буторфанол, клонідин, тетракаїн (порошок), трамадол, тригексифенідил. 4. Наркотичні (психотропні) комбіновані лікарські засоби, які містять на одиницю дози (у перерахунку на безводну основу): кодеїну декстропропоксифену фенобарбіталу ефедрину псевдоефедрину фенілпропаноламіну ерготаміну ергометрину більше більше 10 мг 50 мг 20 мг 15 мг 30 мг 2 мг 0, 2 мг
 Норми одноразового відпуску (НОВ) ЛР --------------------------------------------------Назва наркотичного засобу, | Граничнодопустима для психотропної речовини, | відпуску кількість прекурсору | у складі наркотичного | (психотропного) | комбінованого | лікарського засобу на 1 | рецепт --------------------------------------------------Кодеїн 0, 2 г Декстропропоксифен 0, 6 г Фенобарбітал 1 г Ефедрину гідрохлорид 0, 6 г Псевдоефедрин 0, 6 г Фенілпропаноламін 0, 6 г Ерготамін 0, 02 г Ергометрин 0, 002 г (у перерахунку на безводну основу)
Норми одноразового відпуску (НОВ) ЛР --------------------------------------------------Назва наркотичного засобу, | Граничнодопустима для психотропної речовини, | відпуску кількість прекурсору | у складі наркотичного | (психотропного) | комбінованого | лікарського засобу на 1 | рецепт --------------------------------------------------Кодеїн 0, 2 г Декстропропоксифен 0, 6 г Фенобарбітал 1 г Ефедрину гідрохлорид 0, 6 г Псевдоефедрин 0, 6 г Фенілпропаноламін 0, 6 г Ерготамін 0, 02 г Ергометрин 0, 002 г (у перерахунку на безводну основу)
 Отруйні ЛР, що підлягають ПКО o o o o o атропіну сульфат миш’яковистий ангідрид натрію арсенат кристалічний ртуті дийодид ртуті дихлорид (сулема) ртуті оксиціанід ртуті ціанід срібла нітрат (ляпіс) стрихніну нітрат
Отруйні ЛР, що підлягають ПКО o o o o o атропіну сульфат миш’яковистий ангідрид натрію арсенат кристалічний ртуті дийодид ртуті дихлорид (сулема) ртуті оксиціанід ртуті ціанід срібла нітрат (ляпіс) стрихніну нітрат
 Наркотичні ЛР, що підлягають ПКО o o o етилморфіну гідрохлорид кодеїну фосфат кокаїну гідрохлорид морфіну гідрохлорид омнопон опію екстракт сухий опію настойка проста опію порошок промедол фенамін
Наркотичні ЛР, що підлягають ПКО o o o етилморфіну гідрохлорид кодеїну фосфат кокаїну гідрохлорид морфіну гідрохлорид омнопон опію екстракт сухий опію настойка проста опію порошок промедол фенамін
 Наказ МОЗ України № 275 від 15. 05. 2006 р. “Про затвердження Інструкції із санітарнопротиепідемічного режиму аптечних закладів”
Наказ МОЗ України № 275 від 15. 05. 2006 р. “Про затвердження Інструкції із санітарнопротиепідемічного режиму аптечних закладів”
 Виробничі приміщення аптечних закладів – приміщення та/або зони, у яких виробляються (виготовляються), контролюються, упакову-ються та етикетуються, приймаються, зберігаються та відпускаються (відвантажуються) ЛЗ.
Виробничі приміщення аптечних закладів – приміщення та/або зони, у яких виробляються (виготовляються), контролюються, упакову-ються та етикетуються, приймаються, зберігаються та відпускаються (відвантажуються) ЛЗ.
 Прибирання приміщень o o o o Підлога Стіни, двері Стеля, віконне скло, рами Вікна ззовні Устаткування приміщень ззовні Шафи в матеріальних кімнатах зсередини Раковини, санітарні вузли Санітарний день 1 раз за зміну 1 раз на тиждень 1 раз на місяць в теплу пору року щоденно 1 раз на тиждень щоденно 1 раз на місяць
Прибирання приміщень o o o o Підлога Стіни, двері Стеля, віконне скло, рами Вікна ззовні Устаткування приміщень ззовні Шафи в матеріальних кімнатах зсередини Раковини, санітарні вузли Санітарний день 1 раз за зміну 1 раз на тиждень 1 раз на місяць в теплу пору року щоденно 1 раз на тиждень щоденно 1 раз на місяць
 Вимоги до приміщень, устаткування аптечних закладів та санітарно-гігієнічні вимоги при виробництві (виготовленні) ліків в умовах аптеки
Вимоги до приміщень, устаткування аптечних закладів та санітарно-гігієнічні вимоги при виробництві (виготовленні) ліків в умовах аптеки
 Виготовлення (виробництво) стерильних лікарських засобів повинно здійснюватися в чистих зонах (приміщеннях) в асептичних умовах o o o o асептичний блок складається із шлюзу, асептичної асистентської, приміщення для отримання води для ін'єкцій, фасування, закупорювання та стерилізації ліків. Можливе суміщення асистентської та фасувальної кімнати; приміщення асептичного блока повинні бути максимально ізольовані від інших приміщень аптеки, раціонально взаємопов'язані між собою для забезпечення прямопоточних робочих процесів і скорочення потоку руху ліків у процесі їх виробництва (виготовлення); обладнані шлюзами, які захищають ззовні повітря асептичної асистентської від контамінації; вікна в асептичній асистентській повинні бути герметично зачинені; асептичний блок обладнується припливно-витяжною вентиляцією з перевагою припливу повітря перед витяганням, яка забезпечує не менше ніж 10 -кратний обмін повітря за годину. Система вентиляції повітря повинна враховувати: розмір приміщення, обладнання, персонал, що перебуває у ньому, і мати відповідні фільтри. перед входом в асептичний блок, заготовчу (дефектарську), асистентську кімнату на підлозі повинні бути гумові килимки, змочені дезінфекційним розчином. для миття рук персоналу в шлюзах асептичного блоку, заготовчій, асистентській, мийній і туалеті повинні бути установлені раковини (рукомийники), які доцільно обладнати педальними кранами з ліктьовими приводами, фотоелементами тощо. Безпосередньо біля раковин установлюють пристрої, у яких повинні постійно бути засоби для дезінфекції рук і мийні засоби. Висушування рук проводиться електрорушниками або рушниками разового користування (останні - у разі виготовлення ліків за нестерильних умов). Користуватися раковинами у виробничих приміщеннях особам, які не зайняті в процесі виготовлення і фасування ліків, забороняється. у мийній кімнаті повинні бути виділені і промарковані раковини для миття посуду, що призначається для приготування ін'єкційних розчинів і очних крапель, ліків для внутрішнього вживання, зовнішніх лікарських форм. У цих самих раковинах миється посуд, що використовується при виготовленні даних лікарських форм. Забороняється користуватися цими раковинами для миття рук.
Виготовлення (виробництво) стерильних лікарських засобів повинно здійснюватися в чистих зонах (приміщеннях) в асептичних умовах o o o o асептичний блок складається із шлюзу, асептичної асистентської, приміщення для отримання води для ін'єкцій, фасування, закупорювання та стерилізації ліків. Можливе суміщення асистентської та фасувальної кімнати; приміщення асептичного блока повинні бути максимально ізольовані від інших приміщень аптеки, раціонально взаємопов'язані між собою для забезпечення прямопоточних робочих процесів і скорочення потоку руху ліків у процесі їх виробництва (виготовлення); обладнані шлюзами, які захищають ззовні повітря асептичної асистентської від контамінації; вікна в асептичній асистентській повинні бути герметично зачинені; асептичний блок обладнується припливно-витяжною вентиляцією з перевагою припливу повітря перед витяганням, яка забезпечує не менше ніж 10 -кратний обмін повітря за годину. Система вентиляції повітря повинна враховувати: розмір приміщення, обладнання, персонал, що перебуває у ньому, і мати відповідні фільтри. перед входом в асептичний блок, заготовчу (дефектарську), асистентську кімнату на підлозі повинні бути гумові килимки, змочені дезінфекційним розчином. для миття рук персоналу в шлюзах асептичного блоку, заготовчій, асистентській, мийній і туалеті повинні бути установлені раковини (рукомийники), які доцільно обладнати педальними кранами з ліктьовими приводами, фотоелементами тощо. Безпосередньо біля раковин установлюють пристрої, у яких повинні постійно бути засоби для дезінфекції рук і мийні засоби. Висушування рук проводиться електрорушниками або рушниками разового користування (останні - у разі виготовлення ліків за нестерильних умов). Користуватися раковинами у виробничих приміщеннях особам, які не зайняті в процесі виготовлення і фасування ліків, забороняється. у мийній кімнаті повинні бути виділені і промарковані раковини для миття посуду, що призначається для приготування ін'єкційних розчинів і очних крапель, ліків для внутрішнього вживання, зовнішніх лікарських форм. У цих самих раковинах миється посуд, що використовується при виготовленні даних лікарських форм. Забороняється користуватися цими раковинами для миття рук.
 o o o o Матеріали, які застосовуються в оздобленні "чистих"приміщень, повинні мати механічну міцність, що сприяє їх санітарній обробці без пошкоджень, незначному водопоглиненню. Вони не піддаються корозії, легко чистяться, миються та дезінфікуються. Стелі, стіни і підлога приміщень для приготування ліків в асептичних умовах повинні бути оздоблені таким чином, щоб не було виступів, карнизів, тріщин, та покриті матеріалами, що допускають вологе прибирання та дезінфекцію. Двері та вікна повинні бути щільно підігнані і не мати щілин. Стерилізацію окремих об'єктів здійснюють у стерилізаторах згідно з вимогами цієї Інструкції (додаток 1). Контроль за ефективністю роботи стерилізаторів здійснюєтьсяза допомогою максимальних термометрів, а також хімічних та біологічних індикаторів промислового виготовлення, зареєстрованих МОЗ України та дозволених до використання в Україні. Облік результатів контролю здійснюють відповідно до інструкцій виробника. З метою досягнення стерильності всі предмети, устаткування та меблі, які вносяться в асептичний блок, попередньо дезінфікують згідно з інструктивнометодичними документами, затвердженими МОЗ України, на конкретний дезінфекційний засіб. Категорично забороняється зберігати в асептичному блоці устаткування, що не використовується. Прибирання приміщень для виготовлення лікарських засобів в асептичних умовах проводиться не рідше 1 разу за зміну в кінці роботи вологим способом із застосуванням дезінфекційних засобів. Один раз на тиждень проводять генеральне прибирання асептичного блоку, суворо дотримуючись послідовності стадій прибирання асептичного блоку: починають прибирання з асептичної асистентської. Спочатку миють та дезінфікують стелю, потім стіни і двері від стелі допідлоги. Далі миють і дезінфікують стаціонарне устаткування і востанню чергу - підлогу, застосовуючи дезінфекційний розчин. Для протирання підлоги застосовують ганчірки з тканини ззагорненими краями. Для протирання стель, стін і устаткування рекомендуються поролонові губки та серветки з капрону. Після кожного прибирання асептичних приміщень матеріал, який при цьому застосовувався, дезінфікують, просушують і зберігають у чистих промаркованих контейнерах із щільно закритою кришкою. У разі виявлення в повітрі асептичного блоку грибів при обробці приміщення та устаткування розчином перекису водню з мийними засобами його концентрацію збільшують до 4%, а за наявності спороутворювальної мікрофлори - до 6%.
o o o o Матеріали, які застосовуються в оздобленні "чистих"приміщень, повинні мати механічну міцність, що сприяє їх санітарній обробці без пошкоджень, незначному водопоглиненню. Вони не піддаються корозії, легко чистяться, миються та дезінфікуються. Стелі, стіни і підлога приміщень для приготування ліків в асептичних умовах повинні бути оздоблені таким чином, щоб не було виступів, карнизів, тріщин, та покриті матеріалами, що допускають вологе прибирання та дезінфекцію. Двері та вікна повинні бути щільно підігнані і не мати щілин. Стерилізацію окремих об'єктів здійснюють у стерилізаторах згідно з вимогами цієї Інструкції (додаток 1). Контроль за ефективністю роботи стерилізаторів здійснюєтьсяза допомогою максимальних термометрів, а також хімічних та біологічних індикаторів промислового виготовлення, зареєстрованих МОЗ України та дозволених до використання в Україні. Облік результатів контролю здійснюють відповідно до інструкцій виробника. З метою досягнення стерильності всі предмети, устаткування та меблі, які вносяться в асептичний блок, попередньо дезінфікують згідно з інструктивнометодичними документами, затвердженими МОЗ України, на конкретний дезінфекційний засіб. Категорично забороняється зберігати в асептичному блоці устаткування, що не використовується. Прибирання приміщень для виготовлення лікарських засобів в асептичних умовах проводиться не рідше 1 разу за зміну в кінці роботи вологим способом із застосуванням дезінфекційних засобів. Один раз на тиждень проводять генеральне прибирання асептичного блоку, суворо дотримуючись послідовності стадій прибирання асептичного блоку: починають прибирання з асептичної асистентської. Спочатку миють та дезінфікують стелю, потім стіни і двері від стелі допідлоги. Далі миють і дезінфікують стаціонарне устаткування і востанню чергу - підлогу, застосовуючи дезінфекційний розчин. Для протирання підлоги застосовують ганчірки з тканини ззагорненими краями. Для протирання стель, стін і устаткування рекомендуються поролонові губки та серветки з капрону. Після кожного прибирання асептичних приміщень матеріал, який при цьому застосовувався, дезінфікують, просушують і зберігають у чистих промаркованих контейнерах із щільно закритою кришкою. У разі виявлення в повітрі асептичного блоку грибів при обробці приміщення та устаткування розчином перекису водню з мийними засобами його концентрацію збільшують до 4%, а за наявності спороутворювальної мікрофлори - до 6%.
 o o o Особи, які беруть участь у виготовленні ліків в асептичних умовах, увійшовши до шлюзу, узувають спеціальне взуття, миють і дезінфікують руки, одягають стерильний халат, марлеву маску в чотири шари, яку змінюють кожні 4 години, шапочку (при цьому волосся ретельно забирають), бахіли. Оптимальним є застосування брючного костюма з капюшоном або комбінезона. Після вдягання стерильного технологічного одягу персонал повинен обполоснути руки водою для ін'єкцій і обробити їх дезінфекційним розчином. На оброблені руки персоналу, зайнятого на ділянці виготовлення, фасування та закупорювання розчинів, що не підлягають термічній стерилізації, повинні бути надіті стерильні хірургічні рукавички. Для миття рук оптимально використовувати такі сорти туалетного мила, які мають високу піноутворювальну здатність. Не слід застосовувати сорти мила, у які додані спеціальні компоненти (сульсенове, дігтярне, карболове, борно-тимолове). Після закінчення роботи руки обмивають теплою водою і обробляють пом'якшувальними засобами. Персонал асептичного блоку повинен суворо дотримуватись правил особистої гігієни. Вхід зі шлюзу до приміщення, у якому виготовляють і фасують ліки в асептичних умовах, у нестерильному технологічному одязі заборонено. Забороняється також виходити за межі асептичного блоку в стерильному технологічному одязі. У разі потреби виходу з асептичного блоку персонал повинен пройти через шлюз, зняти технологічний одяг. При поверненні персонал знову повинен пройти повну обробку. Персонал, який працює в асептичному блоці, повинен не менше 1 разу на рік проходити інструктаж за вимогами, що встановлені до роботи в зазначених приміщеннях. Після проведення інструктажу персонал повинен письмово підтвердити факт його проведення, поставивши підпис та вказавши дату. Технологічний одяг стерилізують в біксах і зберігають в закритому стані, але не більше 3 діб. Взуття перед початком і в кінці роботи дезінфікують із зовнішнього боку і зберігають у шлюзах у закритих шафах, ящиках. Дозволяється використання одноразових стерильних пов'язок (респіраторів), технологічного одягу та спеціального взуття. Лікарські й допоміжні речовини, які використовують для виготовлення ліків в асептичних умовах, зберігають в асептичному блоці в щільно закритих шафах у штангласах відповідно до їх фізико-хімічних властивостей, в умовах, які унеможливлюють їхзабруднення. Штангласи перед кожним заповненням миють істерилізують.
o o o Особи, які беруть участь у виготовленні ліків в асептичних умовах, увійшовши до шлюзу, узувають спеціальне взуття, миють і дезінфікують руки, одягають стерильний халат, марлеву маску в чотири шари, яку змінюють кожні 4 години, шапочку (при цьому волосся ретельно забирають), бахіли. Оптимальним є застосування брючного костюма з капюшоном або комбінезона. Після вдягання стерильного технологічного одягу персонал повинен обполоснути руки водою для ін'єкцій і обробити їх дезінфекційним розчином. На оброблені руки персоналу, зайнятого на ділянці виготовлення, фасування та закупорювання розчинів, що не підлягають термічній стерилізації, повинні бути надіті стерильні хірургічні рукавички. Для миття рук оптимально використовувати такі сорти туалетного мила, які мають високу піноутворювальну здатність. Не слід застосовувати сорти мила, у які додані спеціальні компоненти (сульсенове, дігтярне, карболове, борно-тимолове). Після закінчення роботи руки обмивають теплою водою і обробляють пом'якшувальними засобами. Персонал асептичного блоку повинен суворо дотримуватись правил особистої гігієни. Вхід зі шлюзу до приміщення, у якому виготовляють і фасують ліки в асептичних умовах, у нестерильному технологічному одязі заборонено. Забороняється також виходити за межі асептичного блоку в стерильному технологічному одязі. У разі потреби виходу з асептичного блоку персонал повинен пройти через шлюз, зняти технологічний одяг. При поверненні персонал знову повинен пройти повну обробку. Персонал, який працює в асептичному блоці, повинен не менше 1 разу на рік проходити інструктаж за вимогами, що встановлені до роботи в зазначених приміщеннях. Після проведення інструктажу персонал повинен письмово підтвердити факт його проведення, поставивши підпис та вказавши дату. Технологічний одяг стерилізують в біксах і зберігають в закритому стані, але не більше 3 діб. Взуття перед початком і в кінці роботи дезінфікують із зовнішнього боку і зберігають у шлюзах у закритих шафах, ящиках. Дозволяється використання одноразових стерильних пов'язок (респіраторів), технологічного одягу та спеціального взуття. Лікарські й допоміжні речовини, які використовують для виготовлення ліків в асептичних умовах, зберігають в асептичному блоці в щільно закритих шафах у штангласах відповідно до їх фізико-хімічних властивостей, в умовах, які унеможливлюють їхзабруднення. Штангласи перед кожним заповненням миють істерилізують.
 o o o o Аптечний посуд миють згідно з технологічними інструкціями, затвердженими суб'єктом господарювання з дотриманням вимог миття аптечного посуду. Наявність на посуді залишків мийних засобів і ступінь чистоти посуду перевіряють відповідно до методик, затверджених суб'єктом господарювання. Після миття посуд стерилізують, закупорюють і зберігають в щільно закритих шафах, пофарбованих зсередини світлою олійною фарбою або покритих пластиком. Строк зберігання стерильного посуду (у тому числі балонів), що використовується для виготовлення і фасування ліків васептичних умовах, не більше 24 годин. Крупноємні балони, як виняток, після миття дозволяється знезаражувати гострою парою протягом 30 хв. Після стерилізації (або знезараження) ємкості закривають стерильними пробками, фольгою або обв'язують стерильним пергаментом і зберігають не більше 24 годин в умовах, що унеможливлюють забруднення. Підготовка і миття пробок та алюмінієвих ковпачків для закупорювання розчинів для ін'єкцій та очних крапель проводиться згідно з технологічними інструкціями, затвердженими суб'єктом господарювання, дотримуючись вимог обробки та контролю якості обробки посуду та пробок. Допоміжний матеріал (вата, марля, пергаментний папір, фільтри й інше) стерилізують у біксах або банках з притертою пробкою і зберігають у закритому стані не більше 3 діб. На біксах або банках повинні бути прикріплені бирки із зазначеними на них датами стерилізації. Після розкриття біксів або банок матеріали можуть використовуватися протягом 24 годин. Після кожного забору матеріалу бікс (банку) щільно закривають. Забір проводять стерильним пінцетом, який з метою забезпечення стерильності міститься у дезінфекційному розчині. При цьому слід мати на увазі, що допоміжний матеріал для стерилізації повинен укладатися в бікси (банки) у готовому для використання стані (пергамент та фільтрувальний папір, марлю ріжуть на шматки потрібного розміру; з вати роблять тампони). Застосування засобів малої механізації для виготовлення розчинів для ін'єкцій та очних крапель допускається за умови, якщо є можливість їхнього знезаражування і стерилізації. Концентровані розчини, напівфабрикати, внутрішньоаптечну заготовку виготовляють в асептичних умовах і зберігають відповідно до їх фізико-хімічних властивостей та встановлених строків придатності в умовах, які виключають їхзабруднення. При роботі в асептичному блоці для записів використовують попередньо нарізані аркуші рослинного пергаменту або кальки. Папір зберігають у пластмасових папках або пакетах. Писати можна тільки кульковою ручкою, яку один раз за зміну протирають спиртом етиловим 70% або спирто-ефірною сумішшю. Записи проводять на столі, розташованому поблизу місцевої витяжної системи.
o o o o Аптечний посуд миють згідно з технологічними інструкціями, затвердженими суб'єктом господарювання з дотриманням вимог миття аптечного посуду. Наявність на посуді залишків мийних засобів і ступінь чистоти посуду перевіряють відповідно до методик, затверджених суб'єктом господарювання. Після миття посуд стерилізують, закупорюють і зберігають в щільно закритих шафах, пофарбованих зсередини світлою олійною фарбою або покритих пластиком. Строк зберігання стерильного посуду (у тому числі балонів), що використовується для виготовлення і фасування ліків васептичних умовах, не більше 24 годин. Крупноємні балони, як виняток, після миття дозволяється знезаражувати гострою парою протягом 30 хв. Після стерилізації (або знезараження) ємкості закривають стерильними пробками, фольгою або обв'язують стерильним пергаментом і зберігають не більше 24 годин в умовах, що унеможливлюють забруднення. Підготовка і миття пробок та алюмінієвих ковпачків для закупорювання розчинів для ін'єкцій та очних крапель проводиться згідно з технологічними інструкціями, затвердженими суб'єктом господарювання, дотримуючись вимог обробки та контролю якості обробки посуду та пробок. Допоміжний матеріал (вата, марля, пергаментний папір, фільтри й інше) стерилізують у біксах або банках з притертою пробкою і зберігають у закритому стані не більше 3 діб. На біксах або банках повинні бути прикріплені бирки із зазначеними на них датами стерилізації. Після розкриття біксів або банок матеріали можуть використовуватися протягом 24 годин. Після кожного забору матеріалу бікс (банку) щільно закривають. Забір проводять стерильним пінцетом, який з метою забезпечення стерильності міститься у дезінфекційному розчині. При цьому слід мати на увазі, що допоміжний матеріал для стерилізації повинен укладатися в бікси (банки) у готовому для використання стані (пергамент та фільтрувальний папір, марлю ріжуть на шматки потрібного розміру; з вати роблять тампони). Застосування засобів малої механізації для виготовлення розчинів для ін'єкцій та очних крапель допускається за умови, якщо є можливість їхнього знезаражування і стерилізації. Концентровані розчини, напівфабрикати, внутрішньоаптечну заготовку виготовляють в асептичних умовах і зберігають відповідно до їх фізико-хімічних властивостей та встановлених строків придатності в умовах, які виключають їхзабруднення. При роботі в асептичному блоці для записів використовують попередньо нарізані аркуші рослинного пергаменту або кальки. Папір зберігають у пластмасових папках або пакетах. Писати можна тільки кульковою ручкою, яку один раз за зміну протирають спиртом етиловим 70% або спирто-ефірною сумішшю. Записи проводять на столі, розташованому поблизу місцевої витяжної системи.
 o o o Забороняється використання асептичної асистентської для проведення досліджень з контролю стерильності та інших мікробіологічних робіт. Персоналу, який не працює в асептичному блоці, вхід у ці приміщення категорично забороняється. Забороняється повторне використання аптечного посуду та пробок для виробництва (виготовлення) в умовах аптеки ін'єкційних лікарських засобів, якщо інше не передбачено відповідною нормативно-технічною документацією.
o o o Забороняється використання асептичної асистентської для проведення досліджень з контролю стерильності та інших мікробіологічних робіт. Персоналу, який не працює в асептичному блоці, вхід у ці приміщення категорично забороняється. Забороняється повторне використання аптечного посуду та пробок для виробництва (виготовлення) в умовах аптеки ін'єкційних лікарських засобів, якщо інше не передбачено відповідною нормативно-технічною документацією.
 Асептичний блок oшлюз oасептична асистентська oприміщення для отримання води для ін’єкцій oприміщення для фасування, закупорювання та стерилізації ліків Можливе суміщення асистентської та фасувальної кімнат
Асептичний блок oшлюз oасептична асистентська oприміщення для отримання води для ін’єкцій oприміщення для фасування, закупорювання та стерилізації ліків Можливе суміщення асистентської та фасувальної кімнат
 Вимоги до особистої гігієни персоналу o Перед початком зміни забезпечується чистими рушниками для особистого користування o На робочих місцях та в кишенях халатів забороняється зберігати особисті речі окрім чистої носової хустинки o Коротко підстрижені нігті, не покриті лаком o Відсутні каблучки на пальцях o Відсутній макіяж
Вимоги до особистої гігієни персоналу o Перед початком зміни забезпечується чистими рушниками для особистого користування o На робочих місцях та в кишенях халатів забороняється зберігати особисті речі окрім чистої носової хустинки o Коротко підстрижені нігті, не покриті лаком o Відсутні каблучки на пальцях o Відсутній макіяж
 Санітарно-гігієнічні вимоги при виготовленні нестерильних ЛФ o o o o Лікарські засоби, що використовуються для виготовлення нестерильних лікарських форм, повинні зберігатися в щільно закритих штангласах (або іншій тарі) в умовах, що виключають їх забруднення. Штангласи, що використовують для зберігання лікарських засобів, до заповнення миють і стерилізують. Допоміжний матеріал, що необхідний для виготовлення і фасування ліків, готують, стерилізують і зберігають відповідно довимог цієї Інструкції. Аптечний посуд миють та стерилізують згідно зтехнологічними інструкціями, затвердженими суб'єктом господарювання, дотримуючись вимог стерилізації окремих об'єктів. Строк зберігання стерильного посуду, який використовується для виготовлення нестерильних лікарських форм, не більше трьох діб. Поліетиленові пробки для закупорки ліків, які виготовляються і фасуються в аптеках, а також пластмасові гвинтові пробки миють, стерилізують і зберігають згідно з технологічними інструкціями, затвердженими суб'єктом господарювання, дотримуючись вимог обробки та контролю якості обробки аптечного посуду тапробок. Засоби малої механізації, які використовуються при виготовленні і фасуванні ліків, миють і дезінфікують згідно здоданою до них інструкцією. Якщо в інструкції з цього приводу немає вказівок, то після закінчення роботи обладнання розбирають, очищають робочі частини від залишку лікарських речовин, промивають гарячою водою (55 +- 5) град. C, після чого дезінфікують або стерилізують в залежності від властивостей матеріалу, з якого воно виготовлено. Дезінфекційний розчин змивають з обладнання гарячою водою, ополіскують його водою очищеною і зберігають в умовах, що унеможливлюють забруднення. На початку кожної зміни ваги, шпателі, ножиці та інший дрібний аптечний інвентар протирають розчином перекису водню 3% або спирто-ефірною сумішшю (1: 1). Бюреткові установки і піпетки не рідше 1 разуна 10 днів, попередньо звільнивши їх від концентрату, миютьгарячою водою (55 +- 5) град. C із суспензією гірчичного порошку або розчином перекису водню 3% з 0, 5% мийного засобу, потім промивають водою очищеною з обов'язковим контролем змивних вод на залишкові кількості мийних засобів. Зливні крани бюреткових установок до початку роботи очищають від нашарувань солей розчинів, екстрактів, настойок і протирають спирто-ефірною сумішшю (1: 1). Після кожного відважування або відмірювання лікарських речовин із штангласу шийку та пробку штангласу, а також ручні ваги витирають одноразовою марлевою серветкою. Витирати штангласи таваги особистим рушником забороняється. Лійки під час фільтрування або проціджування рідких ліків, а також ступки з порошковою або мазевою масою до розважування і викладання в тару накривають продезінфікованими пластмасовими або металевими пластинками. Для діставання зі ступок мазей або порошків використовують пластмасові пластинки або рентгенівську плівку, звільнену від емульсії. Використання картону не допускається. Після виготовлення мазей залишки жиру прибирають за допомогою картону, паперу, лігніну, використаний посуд миють і стерилізують. Паперові та вощані капсули, шпателі, нитки, резинки обхватні тощо, що використовують для роботи, зберігаються в ящиках асистентського (фасувального) столу, що повинні щодня митися. Допоміжні матеріали зберігають у приміщенні для зберігання, у закритих шафах, скринях в умовах, що виключають їх забруднення.
Санітарно-гігієнічні вимоги при виготовленні нестерильних ЛФ o o o o Лікарські засоби, що використовуються для виготовлення нестерильних лікарських форм, повинні зберігатися в щільно закритих штангласах (або іншій тарі) в умовах, що виключають їх забруднення. Штангласи, що використовують для зберігання лікарських засобів, до заповнення миють і стерилізують. Допоміжний матеріал, що необхідний для виготовлення і фасування ліків, готують, стерилізують і зберігають відповідно довимог цієї Інструкції. Аптечний посуд миють та стерилізують згідно зтехнологічними інструкціями, затвердженими суб'єктом господарювання, дотримуючись вимог стерилізації окремих об'єктів. Строк зберігання стерильного посуду, який використовується для виготовлення нестерильних лікарських форм, не більше трьох діб. Поліетиленові пробки для закупорки ліків, які виготовляються і фасуються в аптеках, а також пластмасові гвинтові пробки миють, стерилізують і зберігають згідно з технологічними інструкціями, затвердженими суб'єктом господарювання, дотримуючись вимог обробки та контролю якості обробки аптечного посуду тапробок. Засоби малої механізації, які використовуються при виготовленні і фасуванні ліків, миють і дезінфікують згідно здоданою до них інструкцією. Якщо в інструкції з цього приводу немає вказівок, то після закінчення роботи обладнання розбирають, очищають робочі частини від залишку лікарських речовин, промивають гарячою водою (55 +- 5) град. C, після чого дезінфікують або стерилізують в залежності від властивостей матеріалу, з якого воно виготовлено. Дезінфекційний розчин змивають з обладнання гарячою водою, ополіскують його водою очищеною і зберігають в умовах, що унеможливлюють забруднення. На початку кожної зміни ваги, шпателі, ножиці та інший дрібний аптечний інвентар протирають розчином перекису водню 3% або спирто-ефірною сумішшю (1: 1). Бюреткові установки і піпетки не рідше 1 разуна 10 днів, попередньо звільнивши їх від концентрату, миютьгарячою водою (55 +- 5) град. C із суспензією гірчичного порошку або розчином перекису водню 3% з 0, 5% мийного засобу, потім промивають водою очищеною з обов'язковим контролем змивних вод на залишкові кількості мийних засобів. Зливні крани бюреткових установок до початку роботи очищають від нашарувань солей розчинів, екстрактів, настойок і протирають спирто-ефірною сумішшю (1: 1). Після кожного відважування або відмірювання лікарських речовин із штангласу шийку та пробку штангласу, а також ручні ваги витирають одноразовою марлевою серветкою. Витирати штангласи таваги особистим рушником забороняється. Лійки під час фільтрування або проціджування рідких ліків, а також ступки з порошковою або мазевою масою до розважування і викладання в тару накривають продезінфікованими пластмасовими або металевими пластинками. Для діставання зі ступок мазей або порошків використовують пластмасові пластинки або рентгенівську плівку, звільнену від емульсії. Використання картону не допускається. Після виготовлення мазей залишки жиру прибирають за допомогою картону, паперу, лігніну, використаний посуд миють і стерилізують. Паперові та вощані капсули, шпателі, нитки, резинки обхватні тощо, що використовують для роботи, зберігаються в ящиках асистентського (фасувального) столу, що повинні щодня митися. Допоміжні матеріали зберігають у приміщенні для зберігання, у закритих шафах, скринях в умовах, що виключають їх забруднення.
 Об’єкти бактеріологічного контролю o вода очищена та вода для ін’єкцій o ЛЗ, виготовлені в аптеці o аптечний посуд, пробки та інші допоміжні матеріали o інвентар, устаткування, що використовуються у приміщеннях з виготовлення ЛЗ o руки й одяг персоналу, що задіяний у процесі виготовлення ЛЗ o повітряне середовище у приміщеннях з виготовлення ЛЗ
Об’єкти бактеріологічного контролю o вода очищена та вода для ін’єкцій o ЛЗ, виготовлені в аптеці o аптечний посуд, пробки та інші допоміжні матеріали o інвентар, устаткування, що використовуються у приміщеннях з виготовлення ЛЗ o руки й одяг персоналу, що задіяний у процесі виготовлення ЛЗ o повітряне середовище у приміщеннях з виготовлення ЛЗ
 Наказ МОЗ України № 626 від 15. 12. 2004 р. “Про затвердження Правил виробництва (виготовлення) ЛЗ в умовах аптеки”
Наказ МОЗ України № 626 від 15. 12. 2004 р. “Про затвердження Правил виробництва (виготовлення) ЛЗ в умовах аптеки”
 Основні терміни o асистентська окреме відповідно обладнане виробниче приміщення для виробництва (виготовлення) лікарських засобів в аптеці; o асептичний блок - комплекс виробничих приміщень, до складу якого входять шлюз, асептична асистентська, приміщення для фасування, закупорювання та стерилізації ліків; o валідація - документальне підтвердження того, що певна методика, процес, обладнання, діяльність або система дій приводять до очікуваного гарантованого результату; o виготовлення лікарських засобів - виготовлення лікарських засобів (далі - ЛЗ) в аптеці за рецептами лікарів та на замовлення лікувально-профілактичних закладів (далі - ЛПЗ);
Основні терміни o асистентська окреме відповідно обладнане виробниче приміщення для виробництва (виготовлення) лікарських засобів в аптеці; o асептичний блок - комплекс виробничих приміщень, до складу якого входять шлюз, асептична асистентська, приміщення для фасування, закупорювання та стерилізації ліків; o валідація - документальне підтвердження того, що певна методика, процес, обладнання, діяльність або система дій приводять до очікуваного гарантованого результату; o виготовлення лікарських засобів - виготовлення лікарських засобів (далі - ЛЗ) в аптеці за рецептами лікарів та на замовлення лікувально-профілактичних закладів (далі - ЛПЗ);
 o виробничі приміщення - приміщення в аптеках, у яких виробляються (виготовляються), контролюються, пакуються, маркуються та зберігаються вироблені лікарські засоби; o внутрішньоаптечна заготовка концентровані розчини і напівфабрикати, що використовуються в аптеці для виготовлення готових ЛЗ, та ЛЗ, виготовлені за часто повторюваними прописами; o внутрішньоаптечний контроль - комплекс запобіжних заходів та видів контролю, який здійснюється безпосередньо в аптеці; o контамінація забруднення концентрованих розчинів, напівфабрикатів та готових лікарських засобів; o концентровані розчини (концентрати) внутрішньоаптечна заготовка у недозованому вигляді, яка застосовується для виробництва (виготовлення) лікарських засобів з рідким дисперсійним середовищем, шляхом розведення чи в суміші з іншими лікарськими речовинами; o лікарська форма - наданий лікарському засобу зручний для вживання стан, при якому забезпечується необхідний лікувальний ефект;
o виробничі приміщення - приміщення в аптеках, у яких виробляються (виготовляються), контролюються, пакуються, маркуються та зберігаються вироблені лікарські засоби; o внутрішньоаптечна заготовка концентровані розчини і напівфабрикати, що використовуються в аптеці для виготовлення готових ЛЗ, та ЛЗ, виготовлені за часто повторюваними прописами; o внутрішньоаптечний контроль - комплекс запобіжних заходів та видів контролю, який здійснюється безпосередньо в аптеці; o контамінація забруднення концентрованих розчинів, напівфабрикатів та готових лікарських засобів; o концентровані розчини (концентрати) внутрішньоаптечна заготовка у недозованому вигляді, яка застосовується для виробництва (виготовлення) лікарських засобів з рідким дисперсійним середовищем, шляхом розведення чи в суміші з іншими лікарськими речовинами; o лікарська форма - наданий лікарському засобу зручний для вживання стан, при якому забезпечується необхідний лікувальний ефект;
 o напівфабрикати - недозований вид внутрішньоаптечної заготовки, попередньо виготовлені в аптеці суміші двох чи більше лікарських речовин, що взяті у співвідношеннях, які найчастіше зустрічаються у прописах на лікарські засоби. Використовуються самостійно після розфасування або в суміші з іншими інгредієнтами; o серія лікарського засобу - визначена кількість однорідної продукції (лікарського засобу), виготовленої в умовах аптеки з певної кількості сировини відповідно до технологічної інструкції в єдиному технологічному процесі від одного завантаження в одиниці ємностного обладнання; - технологічна інструкція - внутрішній документ суб'єкта господарювання, що належить до категорії виробничих інструкцій, у якому визначено технологічні методи, технічні засоби, норми та нормативи виробництва лікарського засобу, методи контролю, і встановлює якісні та кількісні показники лікарського засобу, їх допустимі межі, вимоги до його упаковки, маркування, умов зберігання, терміну придатності; o чисте приміщення (зона) - приміщення (зона), у якому контролюється концентрація завішених у повітрі часток і яке побудоване і використовується таким чином, щоб звести до мінімуму надходження, утворення і втримання цих часток у середині приміщення.
o напівфабрикати - недозований вид внутрішньоаптечної заготовки, попередньо виготовлені в аптеці суміші двох чи більше лікарських речовин, що взяті у співвідношеннях, які найчастіше зустрічаються у прописах на лікарські засоби. Використовуються самостійно після розфасування або в суміші з іншими інгредієнтами; o серія лікарського засобу - визначена кількість однорідної продукції (лікарського засобу), виготовленої в умовах аптеки з певної кількості сировини відповідно до технологічної інструкції в єдиному технологічному процесі від одного завантаження в одиниці ємностного обладнання; - технологічна інструкція - внутрішній документ суб'єкта господарювання, що належить до категорії виробничих інструкцій, у якому визначено технологічні методи, технічні засоби, норми та нормативи виробництва лікарського засобу, методи контролю, і встановлює якісні та кількісні показники лікарського засобу, їх допустимі межі, вимоги до його упаковки, маркування, умов зберігання, терміну придатності; o чисте приміщення (зона) - приміщення (зона), у якому контролюється концентрація завішених у повітрі часток і яке побудоване і використовується таким чином, щоб звести до мінімуму надходження, утворення і втримання цих часток у середині приміщення.
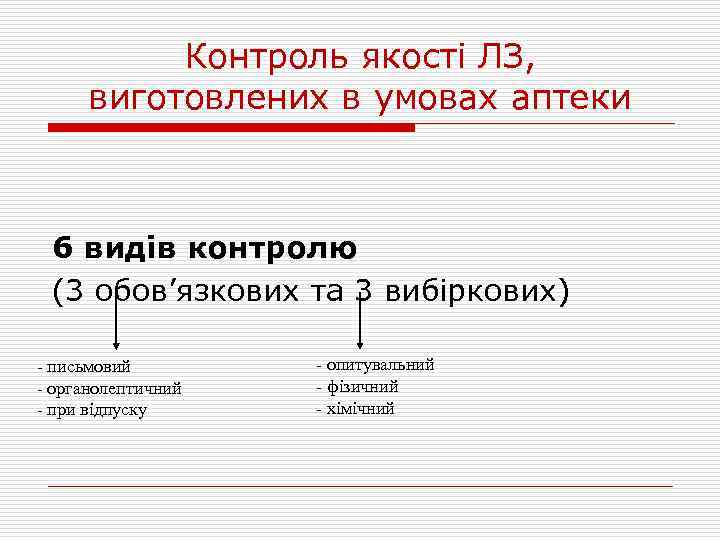 Контроль якості ЛЗ, виготовлених в умовах аптеки 6 видів контролю (3 обов’язкових та 3 вибіркових) - письмовий - органолептичний - при відпуску - опитувальний - фізичний - хімічний
Контроль якості ЛЗ, виготовлених в умовах аптеки 6 видів контролю (3 обов’язкових та 3 вибіркових) - письмовий - органолептичний - при відпуску - опитувальний - фізичний - хімічний
 Письмовий контроль o o o o o При виробництві (виготовленні) усіх лікарських засобів за індивідуальними рецептами (прописами) та на замовлення (вимоги) ЛПЗ заповнюються паспорти письмового контролю, крім тих, що виготовляються серіями на замовлення ЛПЗ, для яких найменування та кількість вихідних речовин зазначається у відповідному журналі У паспорті письмового контролю зазначаються: дата, номер рецепта (замовлення), узяті лікарські речовини та їх кількість; число доз; загальна маса чи об'єм лікарської форми, проставляються підписи осіб, які приготували, розфасували та перевірили вироблений лікарський засіб. Запис у паспорті письмового контролю повинен відображати технологію (порядок змішування інгредієнтів) і робиться латинською мовою з пам'яті негайно після приготування лікарського засобу. При використанні напівфабрикатів і концентратів у паспорті зазначається їх концентрація, відібрана кількість та серія. Якщо до складу лікарської форми входять отруйні речовини, наркотичні і психотропні лікарські засоби та ті, що підлягають предметно-кількісному обліку, то письмовий контроль заповнюється тільки на зворотному боці рецепта. У паспорті письмового контроля зазначаються використані при розрахунках коефіцієнти водопоглинання для лікарської рослинної сировини, коефіцієнти збільшення об'єму водних розчинів при розчиненні лікарських речовин. У разі, якщо лікарські засоби виробляються/виготовляються та відпускаються однією і тією самою особою, паспорт письмового контролю заповнюється у процесі виробництва/виготовлення лікарського засобу. Паспорт письмового контролю зберігається в аптеці протягом двох місяців. Виготовлені лікарські засоби, рецепти та заповнені паспорти письмового контролю передаються на перевірку провізору-аналітику або особі, яка виконує його функції. Контроль полягає у перевірці дотримання правил технології (послідовності змішування), відповідності записів у паспорті письмового контролю пропису в рецепті, правильності проведених розрахунків. Якщо провізором-аналітиком або особою, яка виконує його функції, проводиться фізичний та хімічний контроль лікарського засобу, то на паспорті проставляються номер аналізу та його підпис. При виробництві (виготовленні) ін'єкційних лікарських засобів та внутрішньовенних інфузійних лікарських засобів усі стадії виготовлення (виробництва) та контролю якості реєструються у відповідному журналі. При виробництві концентратів, напівфабрикатів, внутрішньоаптечної заготовки і розфасовці лікарських засобів всі записи проводяться в журналі.
Письмовий контроль o o o o o При виробництві (виготовленні) усіх лікарських засобів за індивідуальними рецептами (прописами) та на замовлення (вимоги) ЛПЗ заповнюються паспорти письмового контролю, крім тих, що виготовляються серіями на замовлення ЛПЗ, для яких найменування та кількість вихідних речовин зазначається у відповідному журналі У паспорті письмового контролю зазначаються: дата, номер рецепта (замовлення), узяті лікарські речовини та їх кількість; число доз; загальна маса чи об'єм лікарської форми, проставляються підписи осіб, які приготували, розфасували та перевірили вироблений лікарський засіб. Запис у паспорті письмового контролю повинен відображати технологію (порядок змішування інгредієнтів) і робиться латинською мовою з пам'яті негайно після приготування лікарського засобу. При використанні напівфабрикатів і концентратів у паспорті зазначається їх концентрація, відібрана кількість та серія. Якщо до складу лікарської форми входять отруйні речовини, наркотичні і психотропні лікарські засоби та ті, що підлягають предметно-кількісному обліку, то письмовий контроль заповнюється тільки на зворотному боці рецепта. У паспорті письмового контроля зазначаються використані при розрахунках коефіцієнти водопоглинання для лікарської рослинної сировини, коефіцієнти збільшення об'єму водних розчинів при розчиненні лікарських речовин. У разі, якщо лікарські засоби виробляються/виготовляються та відпускаються однією і тією самою особою, паспорт письмового контролю заповнюється у процесі виробництва/виготовлення лікарського засобу. Паспорт письмового контролю зберігається в аптеці протягом двох місяців. Виготовлені лікарські засоби, рецепти та заповнені паспорти письмового контролю передаються на перевірку провізору-аналітику або особі, яка виконує його функції. Контроль полягає у перевірці дотримання правил технології (послідовності змішування), відповідності записів у паспорті письмового контролю пропису в рецепті, правильності проведених розрахунків. Якщо провізором-аналітиком або особою, яка виконує його функції, проводиться фізичний та хімічний контроль лікарського засобу, то на паспорті проставляються номер аналізу та його підпис. При виробництві (виготовленні) ін'єкційних лікарських засобів та внутрішньовенних інфузійних лікарських засобів усі стадії виготовлення (виробництва) та контролю якості реєструються у відповідному журналі. При виробництві концентратів, напівфабрикатів, внутрішньоаптечної заготовки і розфасовці лікарських засобів всі записи проводяться в журналі.
 Опитувальний контроль o o Опитувальний контроль застосовується вибірково для ЛЗ, що виготовляються за індивідуальними прописами. Проводиться після виробництва (виготовлення) фармацевтом (провізором) не більше як п'яти лікарських форм. При проведенні опитувального контролю провізораналітик або персонал називає перший інгредієнт, який входить до складу лікарської форми, а в складних лікарських формах зазначає також його кількість, після чого фармацевт (провізор) називає з пам'яті всі взяті ним для виробництва інгредієнти та їх кількість. При використанні напівфабрикатів (концентратів) фармацевт (провізор) називає також їх склад і концентрацію.
Опитувальний контроль o o Опитувальний контроль застосовується вибірково для ЛЗ, що виготовляються за індивідуальними прописами. Проводиться після виробництва (виготовлення) фармацевтом (провізором) не більше як п'яти лікарських форм. При проведенні опитувального контролю провізораналітик або персонал називає перший інгредієнт, який входить до складу лікарської форми, а в складних лікарських формах зазначає також його кількість, після чого фармацевт (провізор) називає з пам'яті всі взяті ним для виробництва інгредієнти та їх кількість. При використанні напівфабрикатів (концентратів) фармацевт (провізор) називає також їх склад і концентрацію.
 Органолептичний контроль o o o Органолептичний контроль є обов'язковим видом контролю і полягає в перевірці зовнішнього вигляду лікарського засобу, у тому числі якості закупорювання, її кольору, запаху, однорідності змішування, відсутності механічних включень у рідких лікарських формах. Однорідність умісту порошків перевіряється за вмістом діючої речовини в одиниці дозованого лікарського засобу, мазей, супозиторіїв за методикою визначення однорідності відповідно до вимог ДФУ. Перевірка здійснюється вибірково в кожного фармацевта (провізора) протягом робочого дня. Результати органолептичного контролю лікарських засобів реєструються в журналі
Органолептичний контроль o o o Органолептичний контроль є обов'язковим видом контролю і полягає в перевірці зовнішнього вигляду лікарського засобу, у тому числі якості закупорювання, її кольору, запаху, однорідності змішування, відсутності механічних включень у рідких лікарських формах. Однорідність умісту порошків перевіряється за вмістом діючої речовини в одиниці дозованого лікарського засобу, мазей, супозиторіїв за методикою визначення однорідності відповідно до вимог ДФУ. Перевірка здійснюється вибірково в кожного фармацевта (провізора) протягом робочого дня. Результати органолептичного контролю лікарських засобів реєструються в журналі
 Фізичний контроль полягає в перевірці загальної маси або об'єму лікарського засобу, кількості та маси окремих доз, що входять в цю лікарську форму (але не менше трьох доз). o Перевіряються: - кожна серія фасовки та внутрішньоаптечної заготовки в кількості трьох - п'яти одиниць фасовки або одиниць заготовки; - лікарські засоби, вироблені за індивідуальними рецептами, замовленнями (вимогами) вибірково протягом робочого дня з урахуванням усіх видів лікарських форм, вироблених за день; - лікарські засоби, що вимагають стерилізації, після розфасовки до їх стерилізації; - лікарські засоби для дітей віком до 1 року; - отруйні, наркотичні (психотропні) лікарські засоби; - лікарські форми, призначені для новонароджених, до їх стерилізації. o Результати фізичного контролю реєструються в журналі, допустимі норми відхилень наведені в таблиці. o
Фізичний контроль полягає в перевірці загальної маси або об'єму лікарського засобу, кількості та маси окремих доз, що входять в цю лікарську форму (але не менше трьох доз). o Перевіряються: - кожна серія фасовки та внутрішньоаптечної заготовки в кількості трьох - п'яти одиниць фасовки або одиниць заготовки; - лікарські засоби, вироблені за індивідуальними рецептами, замовленнями (вимогами) вибірково протягом робочого дня з урахуванням усіх видів лікарських форм, вироблених за день; - лікарські засоби, що вимагають стерилізації, після розфасовки до їх стерилізації; - лікарські засоби для дітей віком до 1 року; - отруйні, наркотичні (психотропні) лікарські засоби; - лікарські форми, призначені для новонароджених, до їх стерилізації. o Результати фізичного контролю реєструються в журналі, допустимі норми відхилень наведені в таблиці. o
 Контроль при відпуску Контролю при відпуску підлягають усі виготовлені в аптеках лікарські засоби. Цей вид контролю здійснює провізор аптеки, який відпускає ліки. o При цьому перевіряється відповідність: - упаковки лікарських засобів - фізико-хімічним властивостям інгредієнтів, що входять до їх складу; - оформлення лікарських засобів - вимогам чинних нормативних документів; - зазначених у рецепті доз отруйних та наркотичних (психотропних) ЛЗ віку хворого; - номера на рецепті та номера на етикетці; прізвища хворого на квитанції - прізвищу на етикетці, у рецепті або його копії; - відповідність складу лікарського засобу, указаному на етикетці, - пропису в рецепті. o Особа, яка відпустила лікарський засіб, зобов'язана поставити свій підпис та дату відпуску на зворотному боці рецепта (замовлення) та в паспорті письмового контролю. o
Контроль при відпуску Контролю при відпуску підлягають усі виготовлені в аптеках лікарські засоби. Цей вид контролю здійснює провізор аптеки, який відпускає ліки. o При цьому перевіряється відповідність: - упаковки лікарських засобів - фізико-хімічним властивостям інгредієнтів, що входять до їх складу; - оформлення лікарських засобів - вимогам чинних нормативних документів; - зазначених у рецепті доз отруйних та наркотичних (психотропних) ЛЗ віку хворого; - номера на рецепті та номера на етикетці; прізвища хворого на квитанції - прізвищу на етикетці, у рецепті або його копії; - відповідність складу лікарського засобу, указаному на етикетці, - пропису в рецепті. o Особа, яка відпустила лікарський засіб, зобов'язана поставити свій підпис та дату відпуску на зворотному боці рецепта (замовлення) та в паспорті письмового контролю. o
 Маркування (оформлення) ЛЗ, виготовлених в умовах аптеки ь ь Основні етикетки в залежності від способу використання: – “Внутрішнє” – “Зовнішнє” – “Для ін’єкцій” – “Для інфузій” в залежності від ЛФ: – “Порошки” – “Мікстура” – “Очні краплі” – “Вушні краплі” – “Назальні краплі”
Маркування (оформлення) ЛЗ, виготовлених в умовах аптеки ь ь Основні етикетки в залежності від способу використання: – “Внутрішнє” – “Зовнішнє” – “Для ін’єкцій” – “Для інфузій” в залежності від ЛФ: – “Порошки” – “Мікстура” – “Очні краплі” – “Вушні краплі” – “Назальні краплі”
 Маркування (оформлення) ЛЗ, виготовлених в умовах аптеки Попереджувальні написи: – “Зберігати в прохолодному місці” – “Зберігати в захищеному від світла місці” – “Перед уживанням збовтувати” – “Берегти від дітей” – “Дитячий” – “Серцевий” – “Берегти від вогню” – “Поводитись обережно!” – “Стерильно” – “Виготовлено асептично” – “Отрута” Контейнери, у яких відпускають отруйні лікарські засоби, оформляють попереджувальними написами "Отрута" (із зображенням перехрещених кісток і черепа), "Поводитись обережно!", а на етикетці повинні бути вказані назва розчину українською мовою та його концентрація.
Маркування (оформлення) ЛЗ, виготовлених в умовах аптеки Попереджувальні написи: – “Зберігати в прохолодному місці” – “Зберігати в захищеному від світла місці” – “Перед уживанням збовтувати” – “Берегти від дітей” – “Дитячий” – “Серцевий” – “Берегти від вогню” – “Поводитись обережно!” – “Стерильно” – “Виготовлено асептично” – “Отрута” Контейнери, у яких відпускають отруйні лікарські засоби, оформляють попереджувальними написами "Отрута" (із зображенням перехрещених кісток і черепа), "Поводитись обережно!", а на етикетці повинні бути вказані назва розчину українською мовою та його концентрація.
 Текст етикетки o емблема медицини / емблема медицини та логотип суб’єкта господарювання / логотип суб’єкта господарювання o номер / назва аптеки, адреса, назва суб’єкта господарювання o номер рецепта або вимоги-замовлення o прізвище та ініціали хворого або номер та назва лікарні / відділення o назва та/або склад ЛЗ Склад ЛЗ пишеться українською та латинською мовами ( однією у разі відсутності місця на етикетці); заповнюється вручну або наноситься штампом o спосіб застосування (доза, частота та час приймання до чи після їжі) o приготував, перевірив, № аналізу o серія (для серійного виготовлення) – відповідає порядковому номеру в журналі лабораторно-фасувальних робіт o дата приготування o термін придатності o ціна o осмоляльність (осмолярність) та іонний склад внутрішньовенних інфузійних розчинів
Текст етикетки o емблема медицини / емблема медицини та логотип суб’єкта господарювання / логотип суб’єкта господарювання o номер / назва аптеки, адреса, назва суб’єкта господарювання o номер рецепта або вимоги-замовлення o прізвище та ініціали хворого або номер та назва лікарні / відділення o назва та/або склад ЛЗ Склад ЛЗ пишеться українською та латинською мовами ( однією у разі відсутності місця на етикетці); заповнюється вручну або наноситься штампом o спосіб застосування (доза, частота та час приймання до чи після їжі) o приготував, перевірив, № аналізу o серія (для серійного виготовлення) – відповідає порядковому номеру в журналі лабораторно-фасувальних робіт o дата приготування o термін придатності o ціна o осмоляльність (осмолярність) та іонний склад внутрішньовенних інфузійних розчинів


