РиДК_Тема 1.pptx
- Количество слайдов: 118

Министерство образования и науки Российской Федерации Дальневосточный федеральный университет Кафедра клеточной биологии и генетики А. П. Анисимов РЕПРОДУКЦИЯ И ДИФФЕРЕНЦИРОВКА КЛЕТОК Часть I. Базовый уровень Конспект-презентация лекционного курса Владивосток 2017


Настоящее учебное пособие подготовлено в форме конспекта-презентации лекционного спецкурса, читаемого автором на протяжении многих лет для студентовбиологов, специализирующихся по профилю «Клеточная биология» . Не считая исторического введения, в нем есть три большие темы. Первая тема посвящена структуре и общим процессам митотического (клеточного) цикла; вторая – динамике пролиферативных процессов в онтогенезе, от первых делений зиготы до зрелых тканей с особенностями их кинетики и дифференцировки; в третьей теме рассматриваются молекулярно-генетические механизмы регуляции клеточного размножения и дифференцировки, представляющие сложную иерархию взаимодействий различных факторов – от средовых до генетических. К настоящему времени по этим проблемам накоплен и продолжает расти огромный научный материал. Отразить его с достаточной полнотой в одном учебном (семестровом) пособии не представляется возможным, поэтому предлагаем настоящий спецкурс «Репродукция и дифференцировка клеток» лишь как «Часть I – Базовый уровень» . Это означает, что без этих начальных знаний невозможно осваивать самые актуальные материалы по структуре и генетической мобильности хроматина, биологии и технологии стволовых клеток, регенерации тканей и органов, злокачественной трансформации клеток и другим проблемам, которые, как хотелось бы автору, должны быть отражены в Части II под условным названием «Актуальные проблемы» . К сотрудничеству в этой сложной работе, а также к полезной критике данного пособия приглашаю специалистов. В нашем пособии минимум текста, но достаточно иллюстраций, что обычно любят студенты, поскольку позволяет удовлетворительно усвоить на базовом уровне учебный материал. Учебное пособие могут использовать, кроме биологических цитологов, гистологов и эмбриологов, генетики, физиологи, биохимики, а также студенты биомедицинского профиля (лечебники, биофизики, биохимики) и другие специалисты, которым потребны современные знания в области клеточной биологии.

ВВЕДЕНИЕ 1. Проблема репродукции и дифференциации клеток в клеточной теории (История проблемы, до 1953 г. ) • • • 17 в. 1665 г. – Роберт Гук = открытие клеток у растений. 1671 г. – Грю, 1675 г. – Мальпиги = у животных. До 19 в. Новых принципиальных положений не высказано. Начало 19 в. = формируется клеточная теория: 1802 – Бриссо-Мирбе, 1809 – Ламарк, 1824 – Дютроше = все организмы состоят из клеток. 1830 – Ян Пуркинье = описание клеточного ядра (зародышевый пузырек яйца курицы). 1831 – итальянец Роберт Броун = обнаружил ядро в растительной клетке. Ввел термин nucleus. Идея о постоянном наличии ядра во всех клетках. Роль ядра – неизвестна. (=Комочек слизи, питательные вещества. . . ). 1838 -39 – Теодор Шванн (немецкий зоолог) = окончательная и наиболее полная формулировка клеточной теории.
Одним из постулатов в клеточной теории Т. Шванна принята идея М. Шлейдена об эндогенном цитогенезисе в форме «свободного клеткообразования» из недифференцированной бластемы: = В слизистой массе зародыша (бластеме) образуются зернышки, вокруг которых конденсируется слизь и появляется оболочка – формируется цитобласт (=ядро). Конденсация продолжается, образуется вторая оболочка – получается молодая клетка (=цит). По Шванну, у животных цитобластема находится в межклеточном веществе.

• В то же время, уже в 1824 г. наблюдали деление клеток (деление бластомеров раннего зародыша). 1832 – деление перегородками у нитчатых водорослей. • Но эти факты не принимались как универсальный способ клеткообразования. Поведение и роль ядра не понимали. • 1847 – Горянинов (акад. Петербургской АН) допускал Шлейденовский цитогенезис для возникновения первых в эволюции клеток. Но в индивидуальном развитии признавал деление (перегородками, почкованием). • 1841 -1852 – Ремак. Его первые наблюдения – • деление клеток крови цыпленка. Дал описание и обзор фактов по делению клеток и ядер перегородками и почкованием (позже Флемминг назвал такое деление амитозом). Утверждал, что это универсальное явление. = Большой толчок к исследованию деления клеток. • 1855 -1859 – Рудольф Вирхов. «Целлюлярная патология» . Полностью развенчал теорию цитогенезиса Шлейдена, которая господствовала благодаря авторитету Шванна. Вирхов (1858): все клетки образуются путем деления! (Omnis cellula e cellulae!).

• Однако Вирхов митоза не знал. Его видели, видели перестройки ядра, но полной картины и объяснения не было. Накапливались отдельные сведения о поведении ядра, рисовали мета- и анафазы, не понимая сути. • 1867 – Гофмейстер = наблюдал митоз у растений. 1873 – Шнейдер (зоолог) = первое описание последовательных картин митоза на дробящихся яйцах плоского червя. Это наблюдение осталось неизвестным для биологов. 1874 – Бючли = редукционное деление у нематод и улиток. Но по его заключению, ядро выталкивается из клетки, а новообразование ядер и клеток происходит из вакуолек и зернышек цитоплазмы, все от Шлейдена). 1876 – Ван Бенеден = открыл клеточный центр.

1879 – Вальтер Флемминг = первое верное описание последовательных фаз митоза Клетки кожи саламандры, крупные хромосомы. Термины Флеминга: «митоз» , «амитоз» (то, что рисовал Ремак), «хроматин» и др. По Флеммингу: хроматин превращается в нити, идет продольное расщепление нитей и расхождение к полюсам. (термин «хромосома» позднее дал Вальдейер, 1883).

• • • Лавина работ. «Ядро затмило цитоплазму» . Особо отметим цикл работ Ван Бенедена – дробление у аскариды. Но объяснения смысла продольного расщепления хромосом не было. 1883 – Вильгельм Ру, крупнейший биолог-теоретик: зернышки ядра соединяются в нити, они (зернышки) разнокачественные. Только продольное расщепление нитей обеспечивает равноценное разделение содержимого ядра по двум клеткам. Это величайшая догадка и, по сути, теория митоза. 1884 -85 – О. Гертвиг, Страсбургер, Рабль. Сформулирована гипотеза: ядро – носитель наследственности. Открыт закон постоянства числа хромосом в соматических клетках одного биологического вида. Эта идея наиболее развита Августом Вейсманом в его учении о зародышевой и соматической плазме. Дальнейшее развитие этой концепции – вся теория гена Томаса Моргана. Оформление цитогенетики с хромосомной теорией наследственности (Сеттон, нач. 20 в. ). 1896 – Э. Вильсон (американский цитолог). Первая капитальная сводка по цитологии и цитогенетике: «Клетка и ее роль в развитии и наследственности» (русский перевод 1936, 1940).

• Параллельно с морфологическими наблюдениями развиваются и биохимические. 1868 – Мишер = обнаружил новый класс органических соединений – нуклеопротеиды (из ядер лимфоцитов, гноя). 1872 – в ядрах спермы лосося обнаружены протамины и НК. 1889 – получены чистые НК, свободные от белка. • Однако в начале 20 в. наследственный материал связывали с белками. Н. Кольцов = идея самоудвоения белков хромосом. • Лишь в 40 -х годах выявлены различия ДНК (ТНК) и РНК и установлена их локализация (Фельген, Розенбек, Белозерский, Девидсон). • Возникло предположение о связи ДНК с хромосомами и ее роли в хранении и передаче наследственной информации. • 1953 – Уотсон и Крик = расшифровка структуры ДНК и механизма репликации. Позже Крик = расшифровка генетического кода (ЦДМБ). • 1953 – Говард и Пелк = сформулированы понятие митотического цикла. Сошлись биохимические и цитологические работы. Начало современного этапа в изучении механизмов репродукции и дифференцировки клеток. • 1953 – умер Сталин = начало освобождение генетики и цитологии в СССР от засилия лысенковщины.

2. Актуальность новых исследований • Кто и для чего изучает репродукцию и дифференцировку клеток? Проблемы репродукции и дифференцировки клеток имеют междисциплинарное значение. Трудно найти другое направление, в котором так тесно переплетались бы интересы разных биологических и медицинских наук. При этом вопросы репродукции (размножения) и дифференцировки (специализации) клеток тесно взаимосвязаны между собой. Дифференцировка начинается «из-под» репродукции, в ходе митотических циклов. Рассматривая дифференцировку, исходим из клеточного цикла; изучая циклы, неизбежно выходим на дифференцировку. • Чьи же это проблемы? • Цитология (в узком смысле). Морфология митоза, цикл хромосом и др. клеточных структур, связь митоза и дифференцировки с клеточным метаболизмом. • Биология развития. Гаметогенез, в т. ч. специфический цикл мейоза. Репродукция и дифференцировка клеток как механизм эмбрионального морфогенеза (дробление, гаструляция, органогенез). • Гистология. Нормальный и репаративный гистогенез. Физиологическая регенерация (обновление) тканей и органов.

• Частные гистофизиологические дисциплины. Особенно гематология и иммунология. Без знания динамики и механизмов регуляции клеточной репродукции и дифференцировки такие дисциплины не состоятельны. • Онкология и радиобиология. Малигнизация (опухолевая трансформация) клеток. Именно задачи онкологии и радиобиологической защиты стали главным стимулом развития этих проблем в 50 -60 -е годы прошлого века и сохраняются по сей день. Задача: понять механизмы контроля, регуляции клеточного цикла, дифференцировки и смерти (апоптоза) клеток, чтобы ими управлять в патологических ситуациях. • Молекулярная биология и генетика. Регуляторы клеточного цикла и дифференцировки – молекулы, главным образом белки, кодируемые соответствующими генами (гены клеточного цикла и дифференцировки). Белковые регуляторы специфичны к тканевым клеткам-мишеням. Тут задействованы разнообразные гормоны, олигопептидные факторы роста, стимуляторы и ингибиторы, разнообразные молекулы-рецепторы, действующие в мембранах, цитоплазме и хромосомах на уровне сигналинга, активации транскрипции и трансляции. Ряд химических канцерогенов имеют сродство с регуляторами пролиферации (размножения) клеток. Открытие и изучение онкогенов и антионкогенов – молекулярно-генетическая проблема. Внутриклеточные сети молекулярного сигналинга – пути к управлению этими процессами.

• Аналитическая и препаративная химия, фармакология. Получение чистых препаратов – стимуляторов и ингибиторов репродукции и дифференцировки клеток. • Биотехнология. Клеточно-тканевая инженерия, заместительная терапия. Проблема стволовых клеток. Культивирование стволовых клеток, их искусственная детерминация и пересадка в организм, к больным органам. Выращивание тканей и органов in vitro. • Таким образом, проблемы репродукции и дифференцировки клеток – междисциплинарная область биологии, медицины, биотехнологии. Это область интересов синтетической науки – клеточной биологии.

ТЕМА 1. КЛЕТОЧНЫЙ ЦИКЛ

1. Общая характеристика клеточного (митотического) цикла • Опыты Говарда и Пелка (1953). Открытие митотического цикла. Корешки конского боба Vicia faba, меристема. Авторадиография с 35 РО 4. • РНК из препаратов экстрагировали, так что метка получалась только от ДНК. • Показано, что синтез ДНК (редупликация хромосом) происходит посреди интерфазы. Рассчитаны параметры цикла: Т = 27 ч (реально 24 ч) - время генерации, продолжительность цикла. Выделены G 1, S, G 2, M – периоды (фазы) митотического цикла: S – synthesis – синтетический; G 1 – gap – пресинтетический, или постмитотический; G 2 – постсинтетический, или премитотический; M – mitosis – митоз). • Определение митотического цикла: Митотический цикл – циклическая последовательность взаимосвязанных и упорядоченных процессов, обеспечивающих подготовку к митотическому делению клетки и сам митоз.
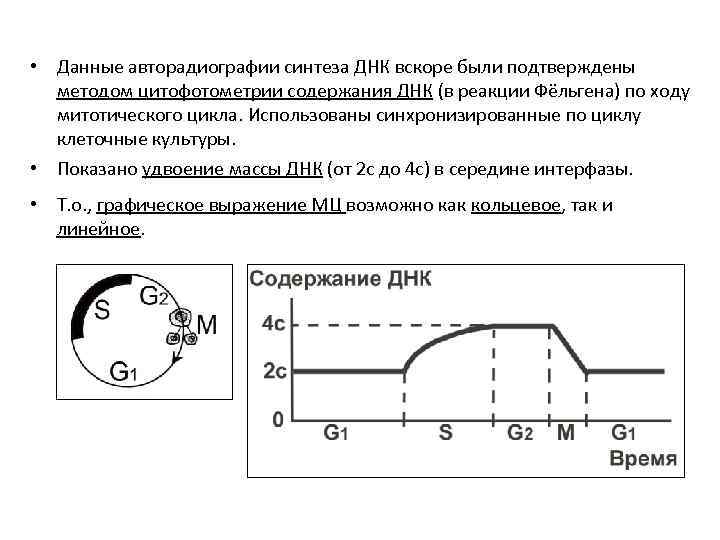
• Данные авторадиографии синтеза ДНК вскоре были подтверждены методом цитофотометрии содержания ДНК (в реакции Фёльгена) по ходу митотического цикла. Использованы синхронизированные по циклу клеточные культуры. • Показано удвоение массы ДНК (от 2 с до 4 с) в середине интерфазы. • Т. о. , графическое выражение МЦ возможно как кольцевое, так и линейное.
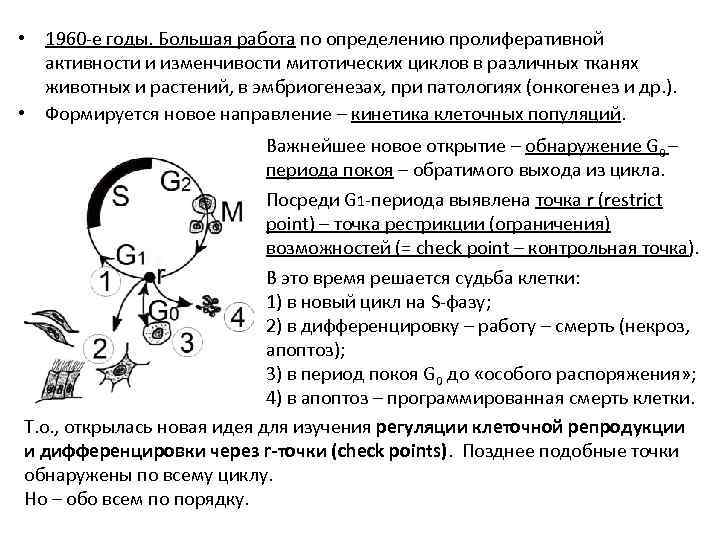
• 1960 -е годы. Большая работа по определению пролиферативной активности и изменчивости митотических циклов в различных тканях животных и растений, в эмбриогенезах, при патологиях (онкогенез и др. ). • Формируется новое направление – кинетика клеточных популяций. Важнейшее новое открытие – обнаружение G 0 – периода покоя – обратимого выхода из цикла. Посреди G 1 -периода выявлена точка r (restrict point) – точка рестрикции (ограничения) возможностей (= check point – контрольная точка). В это время решается судьба клетки: 1) в новый цикл на S-фазу; 2) в дифференцировку – работу – смерть (некроз, апоптоз); 3) в период покоя G 0 до «особого распоряжения» ; 4) в апоптоз – программированная смерть клетки. Т. о. , открылась новая идея для изучения регуляции клеточной репродукции и дифференцировки через r-точки (check points). Позднее подобные точки обнаружены по всему циклу. Но – обо всем по порядку.

2. Методы изучения клеточного цикла и пролиферативной активности клеток • 2. 1. Авторадиография Включение в ДНК 14 С- или 3 Н-нуклеозидов (аденозин, тимидин и др. ). Тейлор (1957) впервые применил 3 Н-тимидин. Простота и безопасность в работе, высокое разрешение, точность локализации метки (мелкозернистые ядерные фотоэмульсии с Ag+). - Импульсная метка = оценка индекса меченых S-фазных ядер (ИМЯ), 0 -10 -20 -. . . -50…%. ИМЯ=30% - Насыщение меткой = оценка пролиферативного пула (Р), 0 -100%.
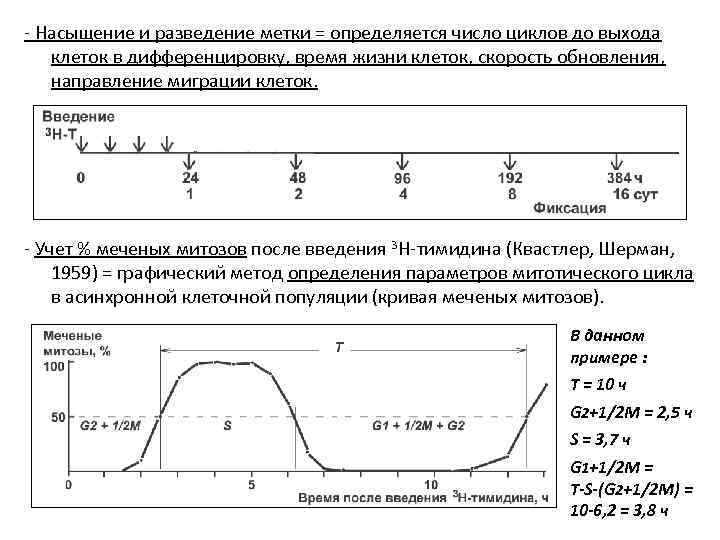
- Насыщение и разведение метки = определяется число циклов до выхода клеток в дифференцировку, время жизни клеток, скорость обновления, направление миграции клеток. - Учет % меченых митозов после введения 3 Н-тимидина (Квастлер, Шерман, 1959) = графический метод определения параметров митотического цикла в асинхронной клеточной популяции (кривая меченых митозов). В данном примере : T = 10 ч G 2+1/2 M = 2, 5 ч S = 3, 7 ч G 1+1/2 M = T-S-(G 2+1/2 M) = 10 -6, 2 = 3, 8 ч
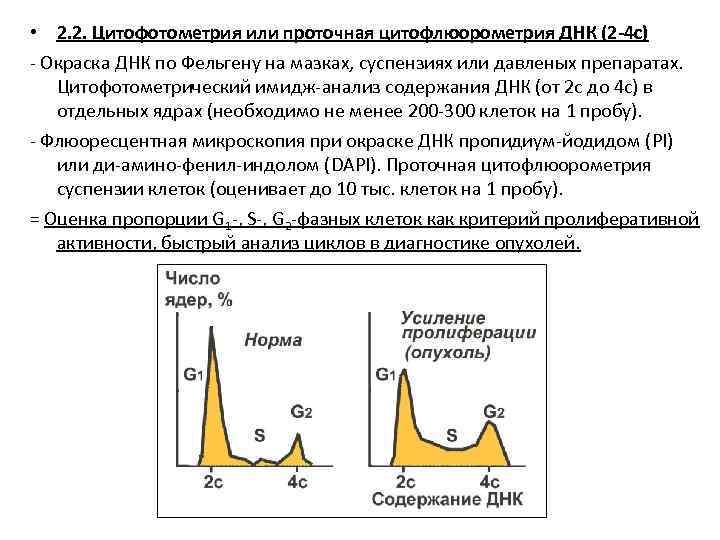
• 2. 2. Цитофотометрия или проточная цитофлюорометрия ДНК (2 -4 с) - Окраска ДНК по Фельгену на мазках, суспензиях или давленых препаратах. Цитофотометрический имидж-анализ содержания ДНК (от 2 с до 4 с) в отдельных ядрах (необходимо не менее 200 -300 клеток на 1 пробу). - Флюоресцентная микроскопия при окраске ДНК пропидиум-йодидом (PI) или ди-амино-фенил-индолом (DAPI). Проточная цитофлюорометрия суспензии клеток (оценивает до 10 тыс. клеток на 1 пробу). = Оценка пропорции G 1 -, S-, G 2 -фазных клеток как критерий пролиферативной активности, быстрый анализ циклов в диагностике опухолей.
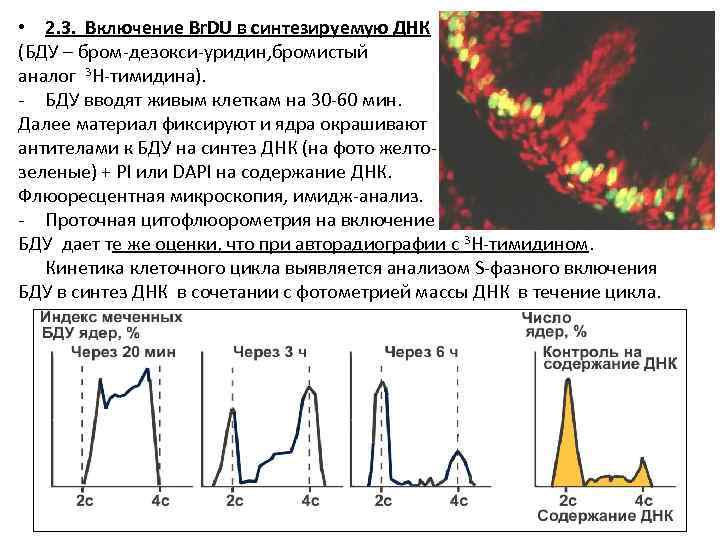
• 2. 3. Включение Br. DU в синтезируемую ДНК (БДУ – бром-дезокси-уридин, бромистый аналог 3 Н-тимидина). - БДУ вводят живым клеткам на 30 -60 мин. Далее материал фиксируют и ядра окрашивают антителами к БДУ на синтез ДНК (на фото желтозеленые) + PI или DAPI на содержание ДНК. Флюоресцентная микроскопия, имидж-анализ. - Проточная цитофлюорометрия на включение БДУ дает те же оценки, что при авторадиографии с 3 Н-тимидином. Кинетика клеточного цикла выявляется анализом S-фазного включения БДУ в синтез ДНК в сочетании с фотометрией массы ДНК в течение цикла.
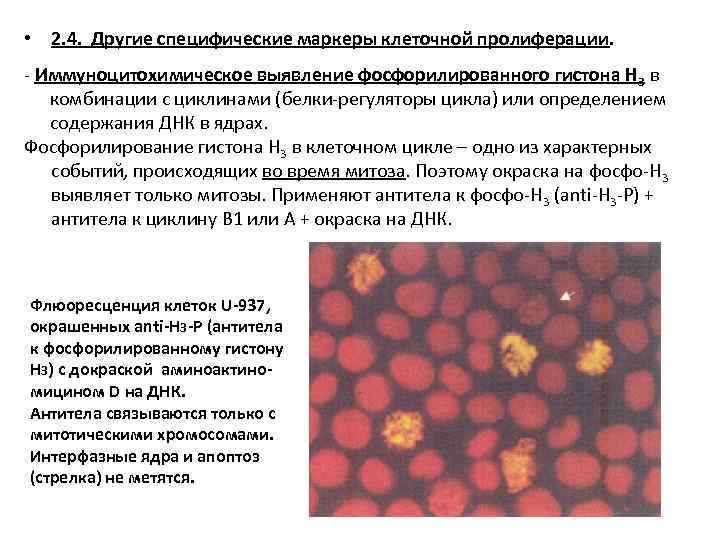
• 2. 4. Другие специфические маркеры клеточной пролиферации. - Иммуноцитохимическое выявление фосфорилированного гистона Н 3 в комбинации с циклинами (белки-регуляторы цикла) или определением содержания ДНК в ядрах. Фосфорилирование гистона Н 3 в клеточном цикле – одно из характерных событий, происходящих во время митоза. Поэтому окраска на фосфо-Н 3 выявляет только митозы. Применяют антитела к фосфо-Н 3 (anti-H 3 -P) + антитела к циклину B 1 или А + окраска на ДНК. Флюоресценция клеток U-937, окрашенных anti-H 3 -P (антитела к фосфорилированному гистону Н 3) с докраской аминоактиномицином D на ДНК. Антитела связываются только с митотическими хромосомами. Интерфазные ядра и апоптоз (стрелка) не метятся.

= Проточная цитофлюорометрия на фосфо-Н 3 выявляет митотический индекс – % клеток в М-фазе по отношению ко всем клеткам или другим фазам цикла (если сочетать с оценкой содержания ДНК):

- Иммуноцитохимическое выявление белка Ki-67 в циклирующих клетках. Моноклональные антитела Ki-67 были получены в Кильском университете (Univ. of Kiel), Германия. 67 – номер удачного клона. Сам белок Ki-67 – это антиген неясной локализации, связанный с пролиферацией; выявляется во всех активных фазах митотического цикла: G 1, S, C 2, M, но только не в G 0. = Проточная цитофлюорометрия оценивает общий пролиферативный пул и соотношение клеток в разных периодах цикла. В нормальных (не опухолевых) клетках преобладает G 0 -период (по сути дифференцировка), хотя есть и циклирующие клетки. В опухоли G 0 -клетки практически отсутствуют, всё пролиферирует).

- Иммуноцитохимическое выявление циклоспецифического антигена PCNA (Proliferating Cell Nuclear Antigen) с помощью соответствующих антител. PCNA – одна из субъединиц ДНК-полимеразного комплекса, поэтому anti. PCNA связывается только в S-фазных ядрах. Это – филогенетически древние (консервативные) молекулы. Имеют значительную гомологию у животных, дрожжей, растений. = Проточная цитофлюорометрия выявляет в ядрах уровень экспрессии PCNA в сочетании с оценкой содержания ДНК (для определения фаз цикла) – фактически это S-фазный индекс (ИМЯ в авторадиографии с 3 Нтимидином).

3. Репликация ДНК • 3. 1. Подготовка к синтезу ДНК. • Подготовка к синтезу ДНК запускается во 2 -й половине G 1 -периода, после точки check point (точка r). • Для синтеза ДНК необходимо наличие 4 видов дезоксирибонуклеотидов (ДНтидов): тимидиловый ТТФ, адениловый АТФ, гуаниловый ГТФ и цитидиловый ЦТФ. • Метаболический фонд нуклеотидов невелик. В основном он состоит из рибонуклеозидов, которые и являются источником образования дезоксирибонуклеотидов. Для этого происходит: энзиматическое восстановление рибозы до дезоксирибозы: РНзиды преобразуются в ДНзиды; и далее фосфорилирование: нуклеозиды переходят в нуклеотиды.
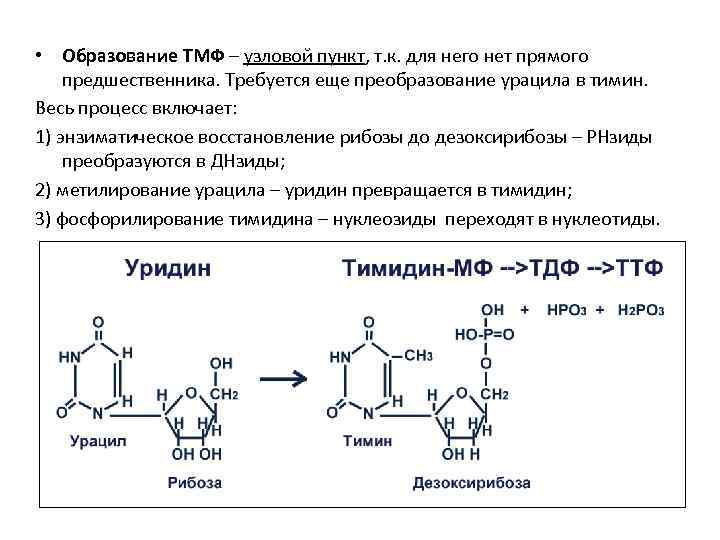
• Образование ТМФ – узловой пункт, т. к. для него нет прямого предшественника. Требуется еще преобразование урацила в тимин. Весь процесс включает: 1) энзиматическое восстановление рибозы до дезоксирибозы – РНзиды преобразуются в ДНзиды; 2) метилирование урацила – уридин превращается в тимидин; 3) фосфорилирование тимидина – нуклеозиды переходят в нуклеотиды.

• Фосфорилирование нуклеозидов происходит с помощью специфических киназ. Но не все киназы имеются всегда в одинаковом количестве. Адениловая, гуаниловая и цитидиловая киназы имеются всегда, а тимидиловая киназа практически отсутствует в покоящихся клетках и появляется только в цикле, в короткий срок перед S-фазой. • С другой стороны, происходит катаболизм предшественников. Кислая фосфатаза способна дефосфорилировать ТМФ, выступая антагонистом киназы. [Опыты с 3 Н-тимидином. У земляной белки (низкая физиологическая активность) включение тимидина слабое, у золотистого хомячка (высокая активность) – сильное. Оказалось, что у белки резко увеличена активность ферментов катаболизма тимидина и др. нуклеотидов. Возможно, те же различия имеются у мидии и гребешка? ]. • Т. о. , активность киназ тимидиловой системы и их антагонистов фосфатаз управляет пулом тимидинфосфатов и является лимитирующим фактором в подготовке к репликации ДНК. Синтез и распад нуклеотидов перед S-фазой – один из механизмов регуляции цикла (с помощью специальных киназ и циклинов, Глава 3).

• 3. 2. Полуконсервативный механизм репликации ДНК. • Молекула ДНК – двухцепочечная. Теоретически возможны 3 способа ее репликации: консервативный, полуконсервативный, дисперсный. • При разработке модели строения и удвоения ДНК Уотсон и Крик исходили гипотетически из полуконсервативного принципа: разрыв водородных связей, расхождение цепей, достройка на них комплементарных цепей (в соответствии с правилом Чаргафа: А-Т, Г-Ц). В результате каждая новая молекула ДНК должна иметь одну нить от исходной молекулы, а вторую вновь синтезированную. • Но метода доказательства не было. А уже появились наблюдения фрагментации ДНК, сестринских хроматидных обменов (СХО). Позднее СХО были определены как мутации, но сначала это могло свидетельствовать в пользу дисперсного механизма репликации ДНК. • Первые исследования выполнены изотопными методами.
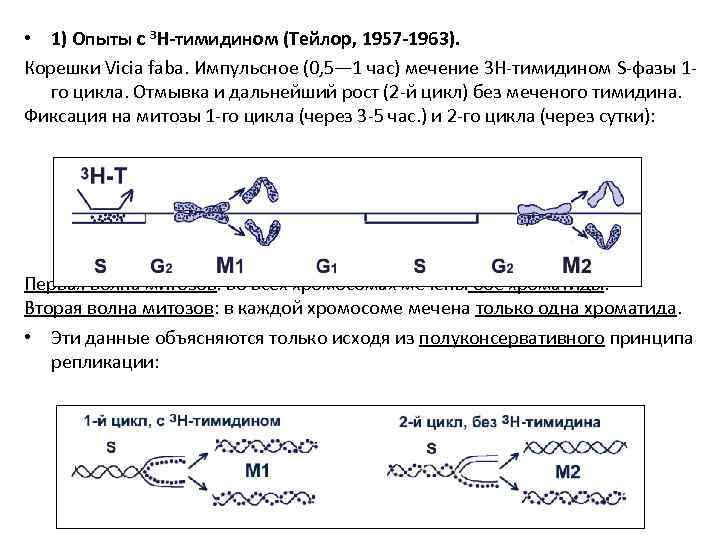
• 1) Опыты с 3 Н-тимидином (Тейлор, 1957 -1963). Корешки Vicia faba. Импульсное (0, 5— 1 час) мечение 3 Н-тимидином S-фазы 1 го цикла. Отмывка и дальнейший рост (2 -й цикл) без меченого тимидина. Фиксация на митозы 1 -го цикла (через 3 -5 час. ) и 2 -го цикла (через сутки): Первая волна митозов: во всех хромосомах мечены обе хроматиды. Вторая волна митозов: в каждой хромосоме мечена только одна хроматида. • Эти данные объясняются только исходя из полуконсервативного принципа репликации:
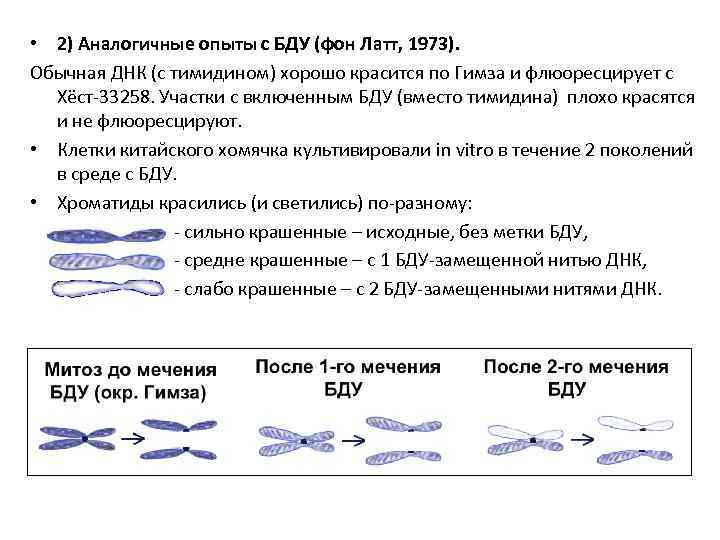
• 2) Аналогичные опыты с БДУ (фон Латт, 1973). Обычная ДНК (с тимидином) хорошо красится по Гимза и флюоресцирует с Хёст-33258. Участки с включенным БДУ (вместо тимидина) плохо красятся и не флюоресцируют. • Клетки китайского хомячка культивировали in vitro в течение 2 поколений в среде с БДУ. • Хроматиды красились (и светились) по-разному: - сильно крашенные – исходные, без метки БДУ, - средне крашенные – с 1 БДУ-замещенной нитью ДНК, - слабо крашенные – с 2 БДУ-замещенными нитями ДНК.

• 3) Опыты c 14 N и 15 N на E. coli (Месельсон, Сталь, 1957, 1958). У бактерий одна кольцевая хромосома, упакованная в нуклеоид. Удвоение ДНК происходит за 20 -30 мин, и сразу наступает деление клетки. • Биохимический подход. Разработан метод равновесного центрифугирования в солевом растворе для разделения ДНК разной удельной плотности: легкая с 14 N и тяжелая 15 N. • E. coli выращивали 10 поколений на среде с 15 NH 4 Cl. Практически весь азот заместился на тяжелый 15 N. Далее культура перенесена на среду с обычным 14 NH 4 Cl. Начался синтез легкой ДНК. В первом и втором циклах ДНК выделяли и центрифугировали.
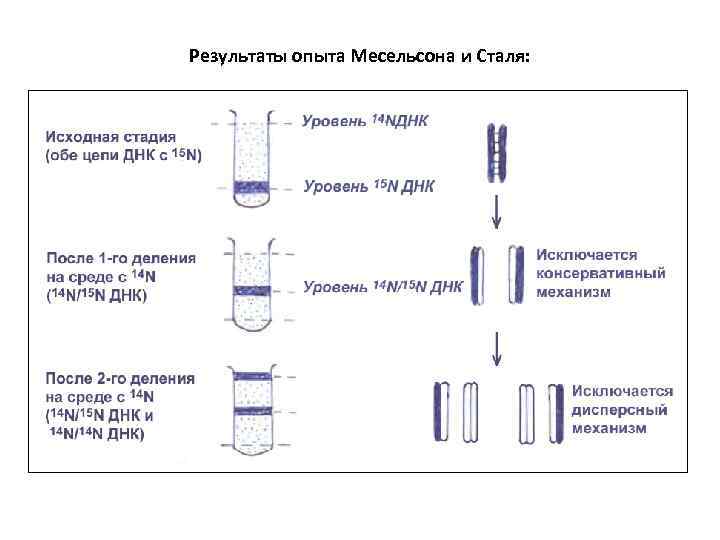
Результаты опыта Месельсона и Сталя:
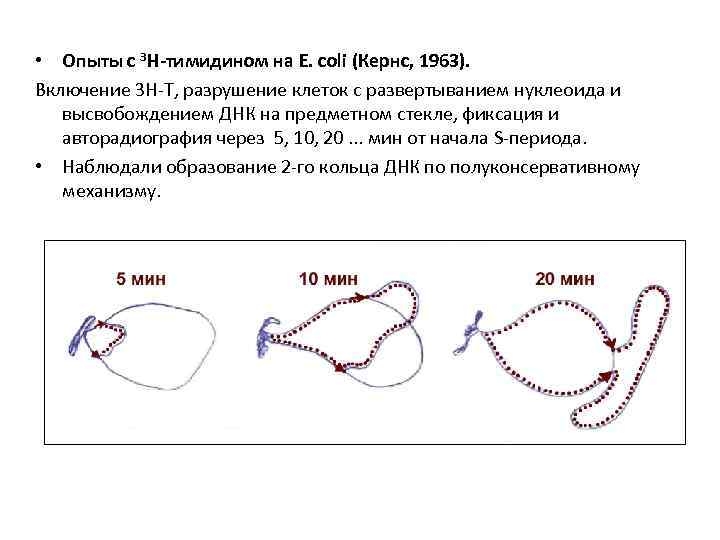
• Опыты с 3 Н-тимидином на E. сoli (Кернс, 1963). Включение 3 Н-Т, разрушение клеток с развертыванием нуклеоида и высвобождением ДНК на предметном стекле, фиксация и авторадиография через 5, 10, 20. . . мин от начала S-периода. • Наблюдали образование 2 -го кольца ДНК по полуконсервативному механизму.
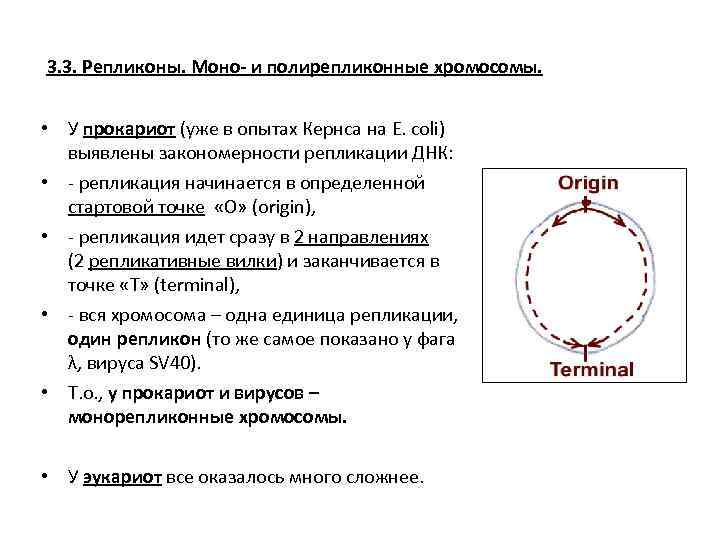
3. 3. Репликоны. Моно- и полирепликонные хромосомы. • У прокариот (уже в опытах Кернса на E. сoli) выявлены закономерности репликации ДНК: • - репликация начинается в определенной стартовой точке «О» (origin), • - репликация идет сразу в 2 направлениях (2 репликативные вилки) и заканчивается в точке «T» (terminal), • - вся хромосома – одна единица репликации, один репликон (то же самое показано у фага λ, вируса SV 40). • Т. о. , у прокариот и вирусов – монорепликонные хромосомы. • У эукариот все оказалось много сложнее.

• Информация к размышлению: - В 2 n наборе хромосом человека содержится 6 пкг (6 х10 -12 г) ДНК (6 х109 пн). то около 2 м, по 20 -80 мм в отдельных хромосомах (сравни с 2 мм у E. сoli). - Скорость репликации у эукариот (50 пн/сек) на порядок ниже, чем у прокариот (500 пн/сек). С такой скоростью при монорепликонной организации хромосом период синтеза ДНК длился бы сотни часов; на самом деле он занимает до 5 -10 ч. - Уже в ранних работах (Тейлор, 1960) показано, что импульсная метка 3 Н-Т обнаруживается сразу во многих участках хромосомы. Особенно хорошо это видно на политенных хромосомах дрозофилы. Каждый диск (хромомер) – отдельный репликон? • Т. о. , по длине хромосомы имеется множество точек инициации синтеза ДНК. Каждый автономно реплицирующийся участок– репликон. Хромосомы эукариот полирепликонные.
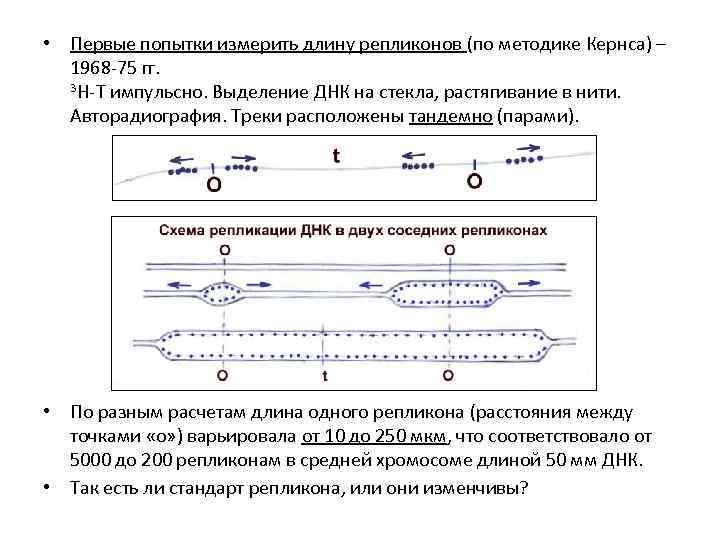
• Первые попытки измерить длину репликонов (по методике Кернса) – 1968 -75 гг. 3 Н-Т импульсно. Выделение ДНК на стекла, растягивание в нити. Авторадиография. Треки расположены тандемно (парами). • По разным расчетам длина одного репликона (расстояния между точками «о» ) варьировала от 10 до 250 мкм, что соответствовало от 5000 до 200 репликонам в средней хромосоме длиной 50 мм ДНК. • Так есть ли стандарт репликона, или они изменчивы?

• Дополнительная информация к размышлению. У одного и того же организма длительность S-фазы (t. S) на разных стадиях развития и в разных зачатках (органах) сильно меняется. У саламандры: эмбриональные клетки ранней бластулы - t. S = 1 ч; дифференцированные взрослые клетки - t. S = 48 ч; премейотический синтез в сперматоцитах - t. S = 200 ч. У морского ежа: первые деления дробления - Т = 1, 5 -2 ч, t. S = 0, 8 ч; поздняя гаструла - Т = 50 -60 ч, t. S = 25 -30 ч. У дрозофилы: первые циклы дробления - Т = 10 мин, t. S = 3, 5 мин ! (расчетная длина репликона = 3 -4 мкм). клеточная культура от взрослых мух - все на порядок больше. Т. о. , время S-фазы удлиняется от нескольких минут до нескольких часов. При этом во всех случаях скорость движения репликативных вилок примерно одинаковая! Следовательно, в ходе развития уменьшается число точек инициации и, соответственно, увеличивается длина репликонов. Большинство точек, активных на ранних стадиях, не используются (отключаются) на более поздних стадиях.

• Сформировано представление о нескольких уровнях репликонной организации хромосом (Андреева, 1983): • Репликоны I порядка (элементарные) : 0, 7 мкм, различимы при ЭМ авторадиографии (соответствуют нуклеомерам хроматина). • Репликоны II порядка : 3 – 5 мкм, минимальные при светооптической авторадиографии (= часть петельного домена). • Репликон III порядка : 15 – 20 мкм, основной репликон с терминаторами (точки t); был известен как ARS – autonomously replicating sequences (= 2 половинки соседних петельных доменов хромонемы). В точках «о» находятся консенсусные последовательности из 11 нп: -АТТТАТАТТТА-. • Репликоны IV порядка : 150 – 200 мкм, самая крупная единица, 100 -300 штук на хромосому (= один хромомер, или диск политенной хромосомы).

• Т. о. , в онтогенезе большинство точек «о» постепенно теряют инициирующую активность, длина регистрируемых репликонов, соответственно, увеличивается. • Сначала, в раннем эмбриогенезе, включены все элементарные репликоны, потом по 1 точке в репликонах II порядка, далее III, IV. • Имеем сложный многоуровневый (иерархичный) механизм регуляции репликации ДНК. Иерархические уровни репликации ДНК отражают дискретность структурной организации хроматина.

3. 4. Хронология синтеза ДНК. Рано и поздно реплицирующиеся участки • В первых циклах дробления зиготы репликоны инициируются почти одновременно. В делящихся (стволовых) клетках взрослого организма соседние малые репликоны (I-II порядков) тоже синхронизированы (последовательное расположение тандемов). Но репликоны III-IV порядков инициируются асинхронно. Т. о. , по длине хромосомы и при сравнении разных хромосом наблюдается асинхронность репликации ДНК. • Однако это не означает беспорядочности репликации. Время начала и окончания репликации в тех или иных хромосомах (график репликации) сохраняется неизменным в ряду клеточных делений. Каждая хромосома характеризуется высокой стабильностью порядка репликации, имеет специфический рисунок репликации.
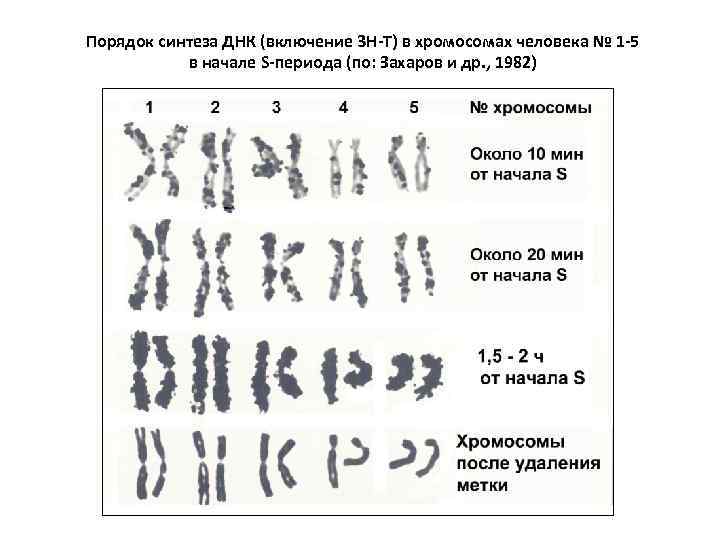
Порядок синтеза ДНК (включение 3 Н-Т) в хромосомах человека № 1 -5 в начале S-периода (по: Захаров и др. , 1982)
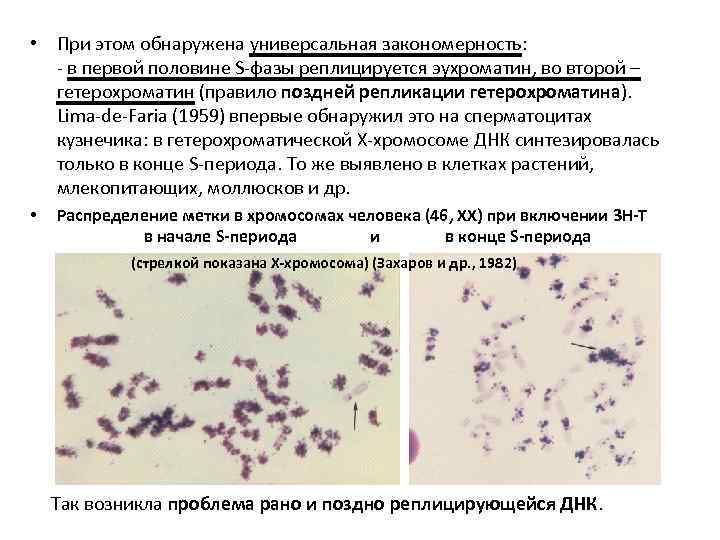
• При этом обнаружена универсальная закономерность: - в первой половине S-фазы реплицируется эухроматин, во второй – гетерохроматин (правило поздней репликации гетерохроматина). Lima-de-Faria (1959) впервые обнаружил это на сперматоцитах кузнечика: в гетерохроматической Х-хромосоме ДНК синтезировалась только в конце S-периода. То же выявлено в клетках растений, млекопитающих, моллюсков и др. • Распределение метки в хромосомах человека (46, ХХ) при включении 3 Н-Т в начале S-периода и в конце S-периода (стрелкой показана Х-хромосома) (Захаров и др. , 1982) Так возникла проблема рано и поздно реплицирующейся ДНК.

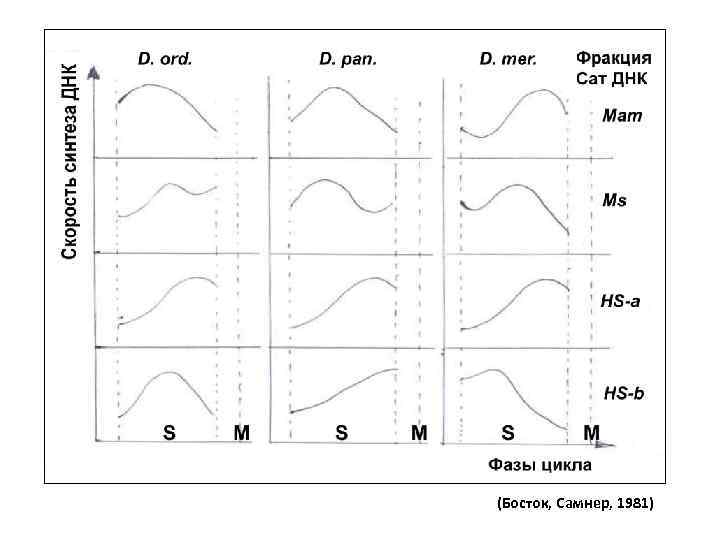
Справка. В интерфазе клеточного цикла, при переходе хромосом в хроматин определенные участки остаются в конденсированном состоянии; различимы эухроматин и гетерохроматин (Heitz, 1928). Гетерохроматин локализован в основном по периферии ядра. Brown (1966): гетерохроматин есть факультативный и структурный (конститутивный). Факультативный гетерохроматин – не работающие конденсированные гены. Яркий пример – Х-хромосома (тельце Бара, половой хроматин) у млекопитающих и человека. Структурный гетерохроматин – постоянно конденсированный в одних и тех же районах обеих гомологичных хромосом (теломерный, центромерный, интеркалярный, околоядрышковый). Образован разными видами сателлитной ДНК, многоповторными последовательностями нуклеотидов. • • Оказалось, что правило Лима-де-Фария справедливо только для факультативного гетерохроматина, который действительно реплицируется в конце S-фазы. Сат. ДНК реплицируется на протяжении всего S-периода, причем каждая фракция имеет свой пик синтеза в определенной части S. Пример: на 3 видах кенгуровых крыс выявляли время репликации разных фракций сат. ДНК:
(Босток, Самнер, 1981)

• Выводы: по репликации гетерохроматиновой ДНК: • - Синтез разных фракций сат. ДНК может идти в начале, середине или конце S-фазы; • - Хронология репликации видоспецифична; • - Распространенное представление о поздней репликации гетерохроматина справедливо только в отношении факультативного гетерохроматина. • - Эухроматиновая ДНК реплицируется преимущественно в первой половине S-фазы, но отдельные локусы реплицируются в середине и даже в конце S-фазы. Например, репликация ядрышковых организаторов: NB: У хомячка и крысы гены р. РНК (ЯОР) локализованы в 1 паре хромосом, у человека – в 5 парах. Каждая пара хромосом имеет свой график репликации. (Босток, Самнер, 1981)
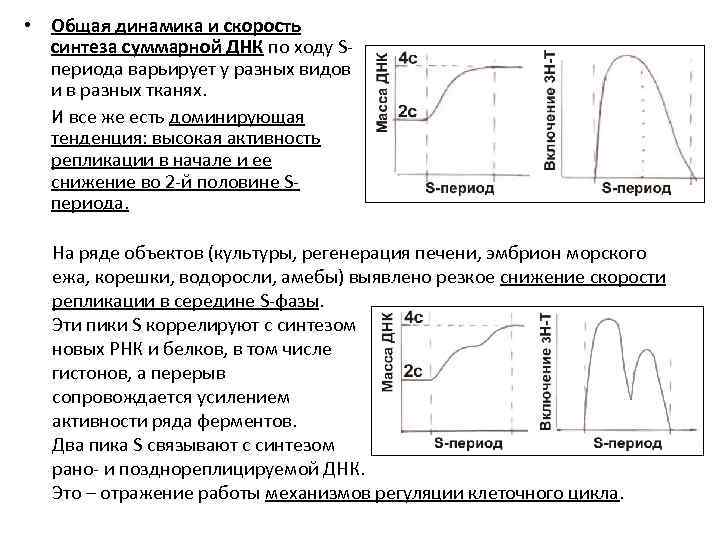
• Общая динамика и скорость синтеза суммарной ДНК по ходу Sпериода варьирует у разных видов и в разных тканях. И все же есть доминирующая тенденция: высокая активность репликации в начале и ее снижение во 2 -й половине Sпериода. На ряде объектов (культуры, регенерация печени, эмбрион морского ежа, корешки, водоросли, амебы) выявлено резкое снижение скорости репликации в середине S-фазы. Эти пики S коррелируют с синтезом новых РНК и белков, в том числе гистонов, а перерыв сопровождается усилением активности ряда ферментов. Два пика S связывают с синтезом рано- и позднореплицируемой ДНК. Это – отражение работы механизмов регуляции клеточного цикла.

• 3. 5. Особенности репликации теломерной ДНК. • Теломерная ДНК – консервативная сателлитная высокоповторная ДНК. • Выделена, клонирована и расшифрована у многих организмов: - человек и другие позвоночные (более 100 видов): ………………. . (TTAGGG)n; - беспозвоночные: та же или близкая последовательность; - тетрахимена: …………. . (TTGGGG)n; - растения: ……………… (TTTAGGG)n. • Число повторов (n) варьирует у разных видов: максимальное n у мыши – 100 тыс. нп, у обезьяны – 25 тыс. нп, у человека – 12 тыс. нп. • Но число повторов не одинаково и в разных типах клеток одного организма, например у человека в разных зрелых клетках n= 250 -1500 нп.

Роль теломерной сат. ДНК : Обеспечивает индивидуальность и интактность хромосом. При утрате теломеров образуются индуцированные концы хромосом, которые деградируют или связываются с другими хромосомами (в митозе образуются мосты). • • Предотвращают разрушение эухроматической (=генетической) части хромосомы при множественной репликации. Концы хромосом сокращаются в каждом цикле из-за недорепликации по последнему РНК-праймеру (по модели Оказаки). Сокращается теломерная (сателлитная!) ДНК, а геномная ДНК до поры до времени защищена. За теломером имеется субтеломерный участок (другая сат. ДНК, разная у разных видов). Это дополнительный буфер между теломером и генами. • На этом построена теломерная гипотеза старения клеток (основана А. М. Оловниковым, 1970 -е годы): Соматические клетки при каждом делении теряют часть теломерных повторов, которые изначально защищают генетическую зону от укорочения (разрушения). Когда теломеры и субтеломеры израсходуются, разрушаются концевые гены, разрушаются хромосомы. Клетка погибает. •
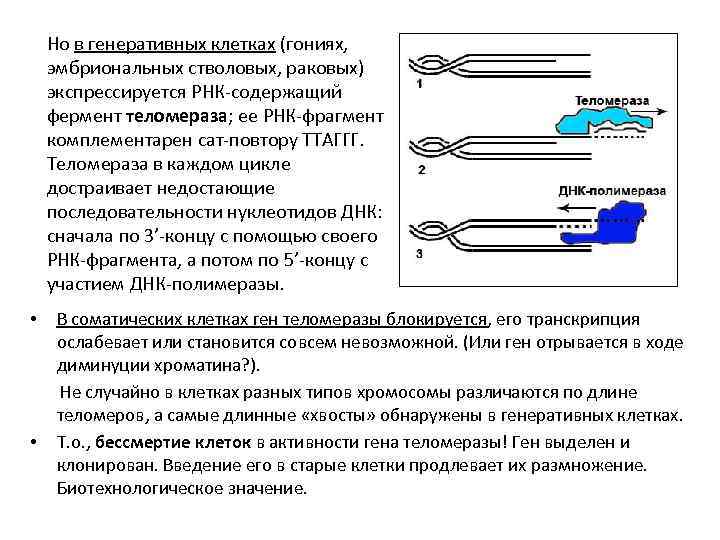
Но в генеративных клетках (гониях, эмбриональных стволовых, раковых) экспрессируется РНК-содержащий фермент теломераза; ее РНК-фрагмент комплементарен сат-повтору ТТАГГГ. Теломераза в каждом цикле достраивает недостающие последовательности нуклеотидов ДНК: сначала по 3’-концу с помощью своего РНК-фрагмента, а потом по 5’-концу с участием ДНК-полимеразы. В соматических клетках ген теломеразы блокируется, его транскрипция ослабевает или становится совсем невозможной. (Или ген отрывается в ходе диминуции хроматина? ). Не случайно в клетках разных типов хромосомы различаются по длине теломеров, а самые длинные «хвосты» обнаружены в генеративных клетках. • Т. о. , бессмертие клеток в активности гена теломеразы! Ген выделен и клонирован. Введение его в старые клетки продлевает их размножение. Биотехнологическое значение. •

• 3. 6. Репаративный синтез ДНК. • В ДНК постоянно возникают ошибки и нарушения по азотистым основаниям или сахаро-фосфатному остову. Ошибки – спонтанные (происходят при репликации или рекомбинации ДНК). Нарушения – индуцированные (происходят под действием УФ света, R-лучей, химических веществ). • Но в клетке есть гены, обеспечивающие синтез не только реплицирующих, но и репарирующих ферментов. Обычно эти ферменты совмещены в ДНК-полимеразных комплексах.
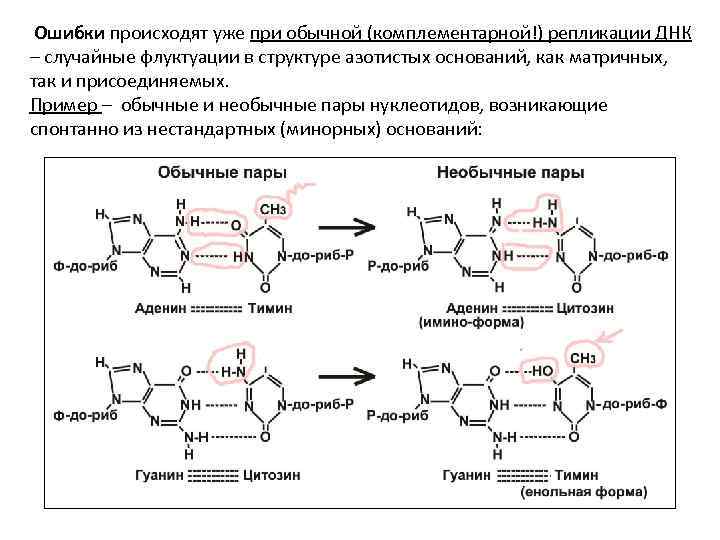
Ошибки происходят уже при обычной (комплементарной!) репликации ДНК – случайные флуктуации в структуре азотистых оснований, как матричных, так и присоединяемых. Пример – обычные и необычные пары нуклеотидов, возникающие спонтанно из нестандартных (минорных) оснований:

• В этих случаях рост цепи сразу останавливается, и экзонуклеаза (домен в составе ДНК-полимеразы Pol I) удаляет необычный нуклеотид. Т. о. , уже в репликативной вилке, контролируется каждый новый нуклеотид. В случае мутации гена экзонуклеазы Pol I неправильные нуклеотиды не устраняются и закрепляются в форме новых мутаций. • В репарации и репликации участвуют также: Pol II (заполняет пробелы между фрагментами Оказаки), Pol III (ключевая полимераза по хромосомной ДНК E. coli), ДНК-лигазы (соединяют цепи ДНК при репликации, репарации и рекомбинации), топоизомеразы I и II (разрывы и сшивки на «острие» репликативной вилки – шарнир). • Нарушения (повреждения) – нарушения остова ДНК, модификации оснований или ошибочные спаривания оснований при рекомбинации (в ходе кроссинговера). 2 -цепочечные повреждения в одном месте, в том числе 2 -цепочечные разрывы, они всегда летальны. (Уникальное исключение – Т 4 -лигаза E. coli: при внедрении фага Т 4 соединяет 2 -цепочечные фрагменты на концах разрыва. ) •
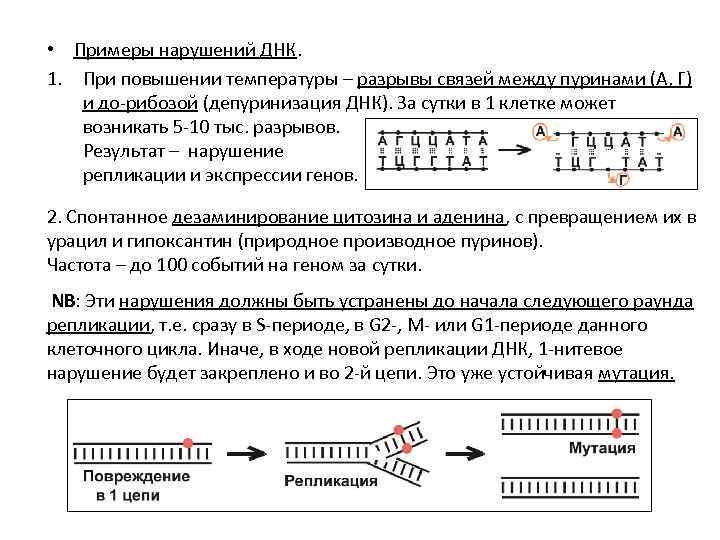
• Примеры нарушений ДНК. 1. При повышении температуры – разрывы связей между пуринами (А, Г) и до-рибозой (депуринизация ДНК). За сутки в 1 клетке может возникать 5 -10 тыс. разрывов. Результат – нарушение репликации и экспрессии генов. 2. Спонтанное дезаминирование цитозина и аденина, с превращением их в урацил и гипоксантин (природное производное пуринов). Частота – до 100 событий на геном за сутки. NB: Эти нарушения должны быть устранены до начала следующего раунда репликации, т. е. сразу в S-периоде, в G 2 -, M- или G 1 -периоде данного клеточного цикла. Иначе, в ходе новой репликации ДНК, 1 -нитевое нарушение будет закреплено и во 2 -й цепи. Это уже устойчивая мутация.
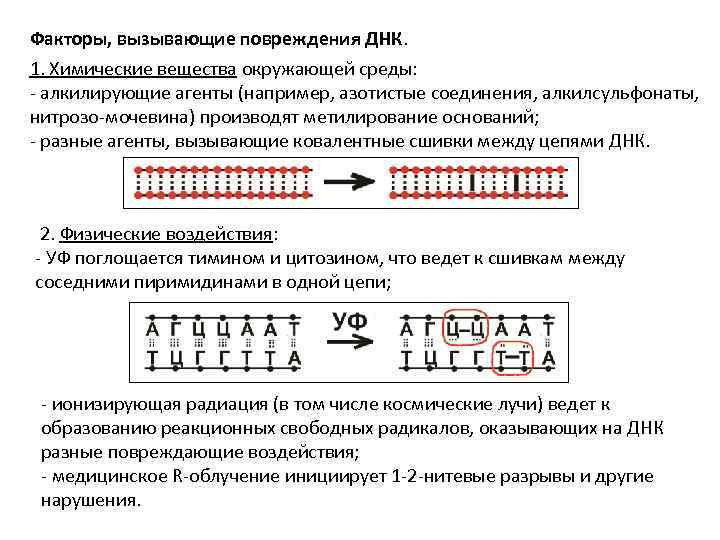
Факторы, вызывающие повреждения ДНК. 1. Химические вещества окружающей среды: - алкилирующие агенты (например, азотистые соединения, алкилсульфонаты, нитрозо-мочевина) производят метилирование оснований; - разные агенты, вызывающие ковалентные сшивки между цепями ДНК. 2. Физические воздействия: - УФ поглощается тимином и цитозином, что ведет к сшивкам между соседними пиримидинами в одной цепи; - ионизирующая радиация (в том числе космические лучи) ведет к образованию реакционных свободных радикалов, оказывающих на ДНК разные повреждающие воздействия; - медицинское R-облучение инициирует 1 -2 -нитевые разрывы и другие нарушения.

• Как это восстанавливается до начала следующей репликации? 1. Прямое восстановление исходной структуры: - специальные ферменты могут просто снимать метильные группы, полученные под действием алкилирующих агентов; - ферменты фотолиазы (фотореактивирующие ферменты бактерий и низших эукариот) под действием видимого света превращают пиримидиновые димеры, полученные при УФ облучении, в нормальные мономеры.
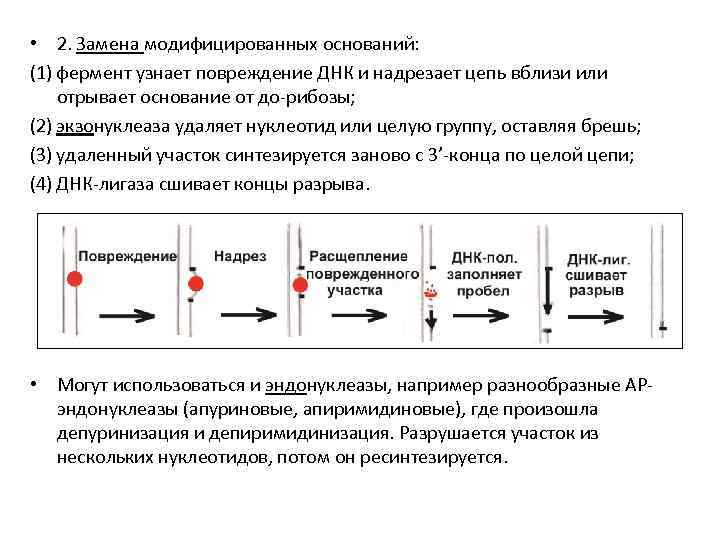
• 2. Замена модифицированных оснований: (1) фермент узнает повреждение ДНК и надрезает цепь вблизи или отрывает основание от до-рибозы; (2) экзонуклеаза удаляет нуклеотид или целую группу, оставляя брешь; (3) удаленный участок синтезируется заново с 3’-конца по целой цепи; (4) ДНК-лигаза сшивает концы разрыва. • Могут использоваться и эндонуклеазы, например разнообразные APэндонуклеазы (апуриновые, апиримидиновые), где произошла депуринизация и депиримидинизация. Разрушается участок из нескольких нуклеотидов, потом он ресинтезируется.
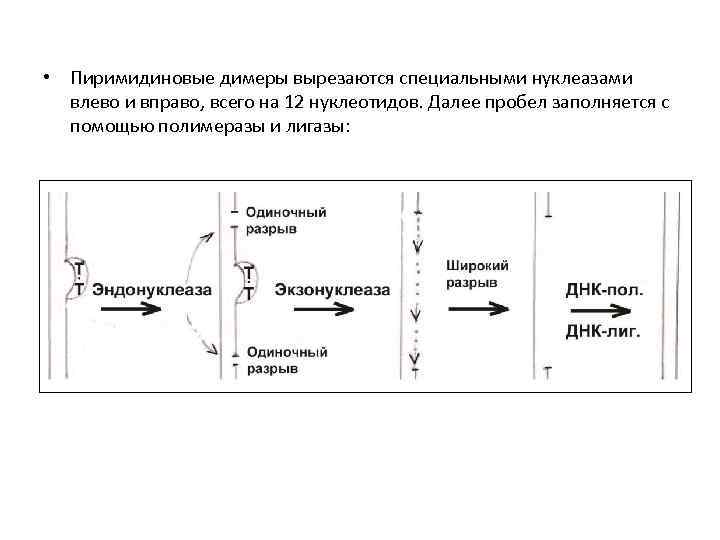
• Пиримидиновые димеры вырезаются специальными нуклеазами влево и вправо, всего на 12 нуклеотидов. Далее пробел заполняется с помощью полимеразы и лигазы:

Значение репарации ДНК. • • Повреждения ДНК блокируют репликацию (передачу информации в ряду поколений) или сохраняются в геномах потомков в форме мутаций. Поврежденная ДНК еще более уязвима. Поэтому повреждения надо устранять. Мутации по генам ферментов репарации – прямой путь к мутациям структурных генов, т. е. к разнообразным генетическим заболеваниям, включая онкологические. В частности, у людей с пигментной ксеродермой нарушена способность к выщеплению пиримидиновых димеров из УФ-облученной ДНК (мутация в 1 из 9 генов). Даже при слабом воздействии солнечного света развивается рак кожи.

4. Синтез РНК и белков в клеточном цикле • Размножение клеток, как правило, сопровождается их ростом, примерно в 2 раза на цикл. • (Старое представление о «критической массе» , необходимой для начала деления. Опыты с амебой: периодическое отрезание части цитоплазмы ведет к бесконечной задержке митоза. ) • Исключения: дробление зиготы и некоторые специальные случаи. • В основе роста клетки лежат синтезы РНК и белков (транскрипция и трансляция генетической программы).

• 4. 1. Синтез РНК. • Необходим синтез и процессинг 3 форм РНК – и. РНК, т. РНК, р. РНК (не считая регуляторных мя. РНК). • Гены пре-и. РНК (10 -80 s РНК) локализованы диффузно по эухроматину всех хромосом. Это уникальные или умеренно (10 -20) повторенные последовательности; в геноме человека около 25 тыс. таких генов. Пре-и. РНК – подвергается процессингу и сплайсингу в перихроматиновых гранулах – информоферах (разрушается до 80 -90 % интронной РНК). Готовая и. РНК (сшитые экзонные фрагменты) выходит через ядерные поры в цитоплазму, связывается с новыми белками и образует информосомы. • Гены пре-т. РНК (4 s РНК) – локализованы так же диффузно; это умеренные повторы. В геноме 61 вид генов т. РНК (по числу кодонов). Процессинг идет без сплайсинга. • Гены пре-р. РНК (45 s РНК) – локализованы в ядрышках (ЯОР, NOR), они присутствуют в фибриллярных центрах и фибриллярном компоненте ядрышка. Это 1 вид гена, он образует умеренные повторы. У человека до 500 повторов в 5 парах хромосом. 45 s РНК процессирует без сплайсинга до 18 s, 28 s и 5, 8 s р. РНК. (5 s р. РНК синтезируется на других хромосомах).
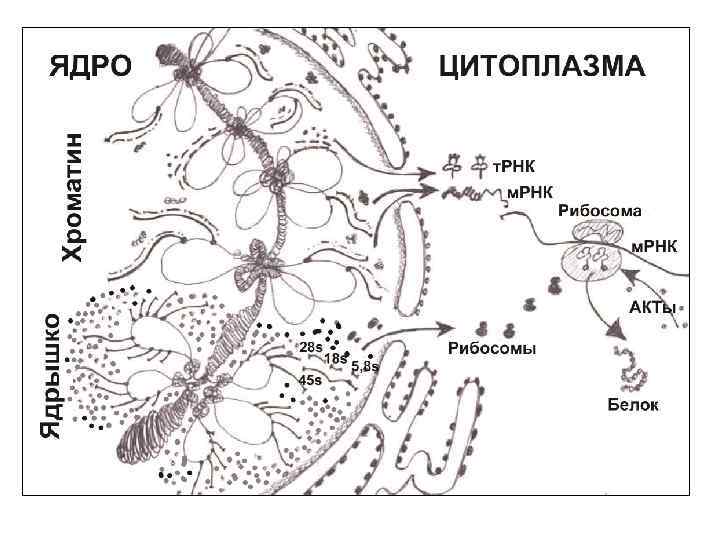

• Количество РНК в клетке вне цикла остается постоянным, т. к. синтез и распад уравновешены. Но при вступлении клетки в митотический цикл синтезы начинают преобладать, и общее содержание РНК увеличивается. • - Данные цитофотометрии: общая масса РНК или только р. РНК в ходе интерфазы примерно удваивается. • - Морфологические данные: увеличение объема ядрышек в циклирующих клетках (регенерирующая печень, крипты кишечного эпителия и др. ). • Динамика синтеза и процессинга РНК исследуется на синхронизированных клеточных культурах (или в асинхронных клеточных популяциях) при одновременном учете ДНК (фаза цикла) и РНК. Оценивают включение в РНК 3 Н-уридина или флуоресцентно меченного урацила (в форме УТФ), активность РНК-полимеразы I (ядрышковая), РНК-полимеразы-II (хроматиновая).

• В 1960 -е годы установлено: - Все основные синтезы, в том числе синтез РНК, идут в интерфазе; (NB: понятие «синтетический период» интерфазы (S) – относится только к синтезу ДНК; все другие синтезы идут на протяжении всей интерфазы, хотя скорости изменяются. ) • - Митоз – инертная, не активная фаза; синтез РНК прерывается от поздней профазы до ранней телофазы вследствие компактизации эухроматина; • - В интерфазе транскрипция прерывается только в реплицируемых участках хроматина (синтезы РНК и ДНК взаимоисключены в 1 пуфе политенной хромосомы). Позже выявлено, что разные формы РНК имеют свои максимумы синтеза.

• Синтез р. РНК (ядрышковая, рибосомная) – показано разобщение транскрипции и процессинга. • Volpe et al. (1976). Культура клеток человека He. La, синхронизированная по фазам цикла. Импульсная метка 3 Н-уридина, интервал проб – 1 час. • Суммарную РНК выделяли и фракционировали центрифугированием по скорости седиментации в градиенте сахарозы. Выделяли ядрышковые фракции РНК: 45 s (первичный транскрипт), 32 s (промежуточный процессинг), 28 s и 18 s (конечные р. РНК формы). • Радиоактивность фракций РНК, отражающую скорость синтеза (45 s) или процессинга (32 s, 28 s, 18 s), оценивали сценциляционным счетчиком. • Результат:
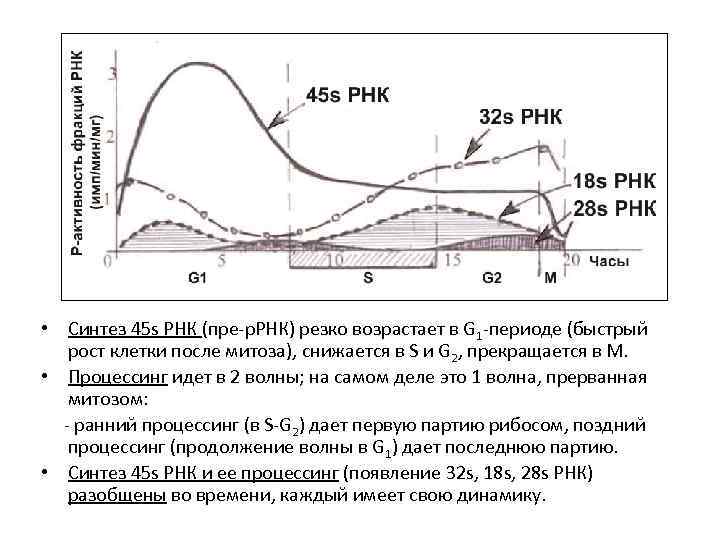
• Синтез 45 s РНК (пре-р. РНК) резко возрастает в G 1 -периоде (быстрый рост клетки после митоза), снижается в S и G 2, прекращается в M. • Процессинг идет в 2 волны; на самом деле это 1 волна, прерванная митозом: - ранний процессинг (в S-G 2) дает первую партию рибосом, поздний процессинг (продолжение волны в G 1) дает последнюю партию. • Синтез 45 s РНК и ее процессинг (появление 32 s, 18 s, 28 s РНК) разобщены во времени, каждый имеет свою динамику.

• Синтез и. РНК – показан эффект дозы генов. • Многочисленные исследования по включению 3 Н-уридина в суммарную РНК ядра или только в РНК хроматина (без ядрышка). Отсюда разнобой результатов. • Детальные исследования группы Pfeiffer (1968) на синхронизированной культуре He. La, подтвержденные позже на других объектах (др. культуры, растения, инфузории, плесень). • Применяли 3 Н-уридин импульсно (0, 5 -1 час) в разных точках цикла. • Результат:
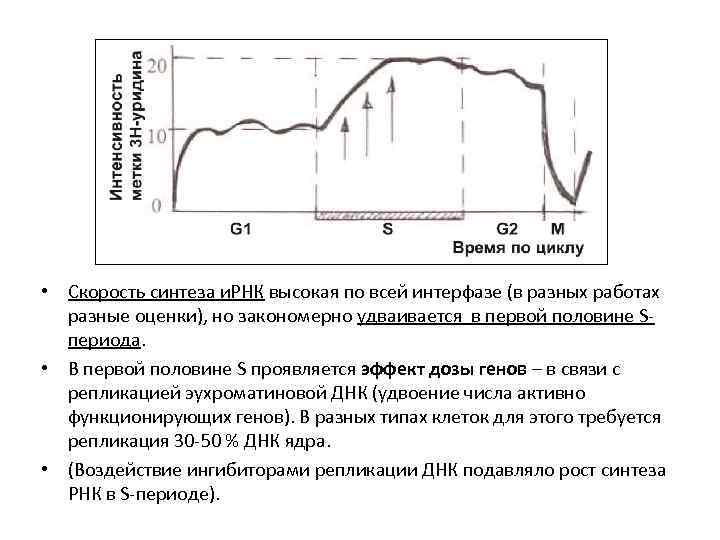
• Скорость синтеза и. РНК высокая по всей интерфазе (в разных работах разные оценки), но закономерно удваивается в первой половине Sпериода. • В первой половине S проявляется эффект дозы генов – в связи с репликацией эухроматиновой ДНК (удвоение числа активно функционирующих генов). В разных типах клеток для этого требуется репликация 30 -50 % ДНК ядра. • (Воздействие ингибиторами репликации ДНК подавляло рост синтеза РНК в S-периоде).

• NB: Четкая зависимость синтеза РНК от дозы генов выявляется не всегда. • Надо учитывать: • Артефакты: несовершенство методик, плохая синхронизация цикла. • Различия клеток: степень их митотической потентности (стволовости), степень дифференцировки, т. е. разное соотношение ауто- и гетеросинтезов РНК. • Изменения активности РНК-полимераз или их поступления в ядро. • Колебания пула нуклеотидов – общих предшественников РНК и ДНК. • Возможность изменения проницаемости мембран и т. д. и т. п.

• 4. 2. Синтез белков. • Синтез белков выявляют по включению в живые клетки меченых аминокислот: 3 Н- или 14 С- лейцин, глицин, пролин, метионин и др. • Радиоактивную метку регистрируют на микроскопических препаратах (авторадиография) или в выделенных белках (счетчиком). • Используют клеточные культуры, синхронизированные по фазам цикла. • Результаты по синтезу общих (суммарных) белков очень различаются в зависимости от типа клеток, их возраста, используемого предшественника и др. факторов. • Но есть и общие тенденции.
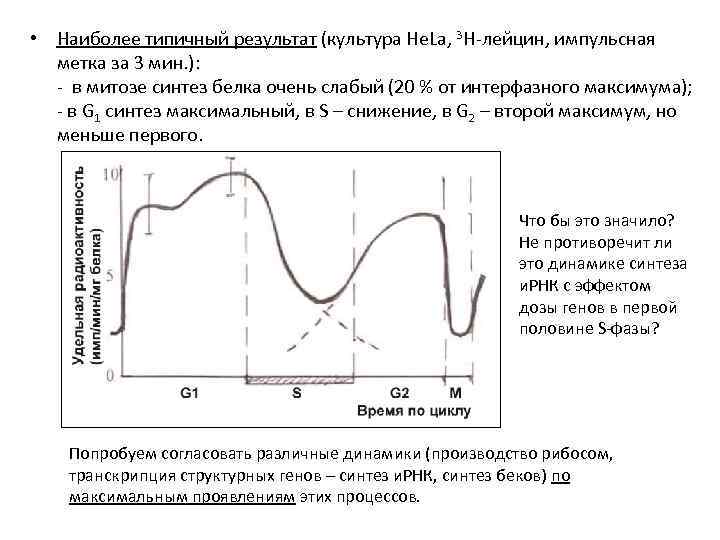
• Наиболее типичный результат (культура He. La, 3 Н-лейцин, импульсная метка за 3 мин. ): - в митозе синтез белка очень слабый (20 % от интерфазного максимума); - в G 1 синтез максимальный, в S – снижение, в G 2 – второй максимум, но меньше первого. Что бы это значило? Не противоречит ли это динамике синтеза и. РНК с эффектом дозы генов в первой половине S-фазы? Попробуем согласовать различные динамики (производство рибосом, транскрипция структурных генов – синтез и. РНК, синтез беков) по максимальным проявлениям этих процессов.
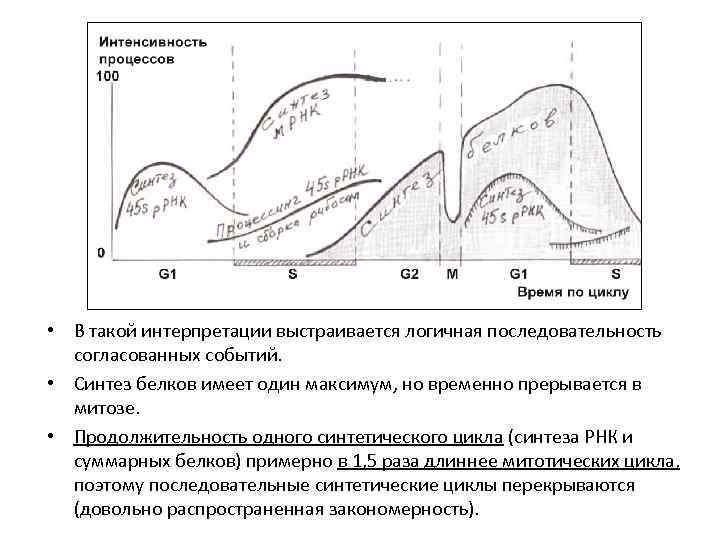
• В такой интерпретации выстраивается логичная последовательность согласованных событий. • Синтез белков имеет один максимум, но временно прерывается в митозе. • Продолжительность одного синтетического цикла (синтеза РНК и суммарных белков) примерно в 1, 5 раза длиннее митотических цикла, поэтому последовательные синтетические циклы перекрываются (довольно распространенная закономерность).
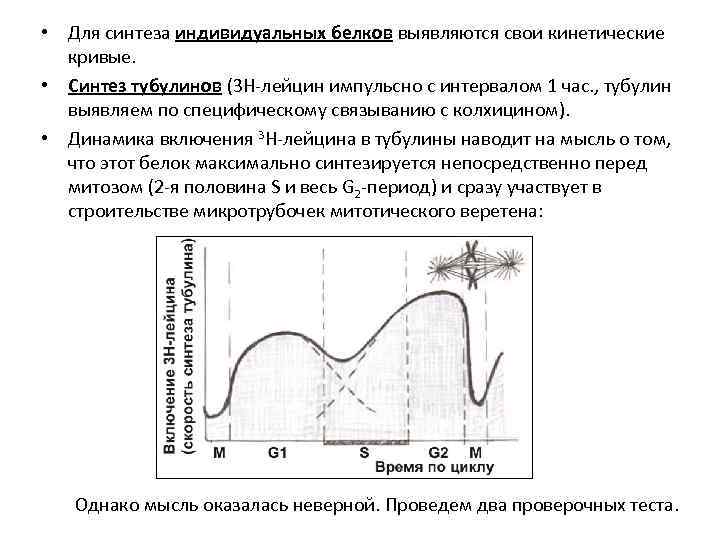
• Для синтеза индивидуальных белков выявляются свои кинетические кривые. • Синтез тубулинов (3 Н-лейцин импульсно с интервалом 1 час. , тубулин выявляем по специфическому связыванию с колхицином). • Динамика включения 3 Н-лейцина в тубулины наводит на мысль о том, что этот белок максимально синтезируется непосредственно перед митозом (2 -я половина S и весь G 2 -период) и сразу участвует в строительстве микротрубочек митотического веретена: Однако мысль оказалась неверной. Проведем два проверочных теста.
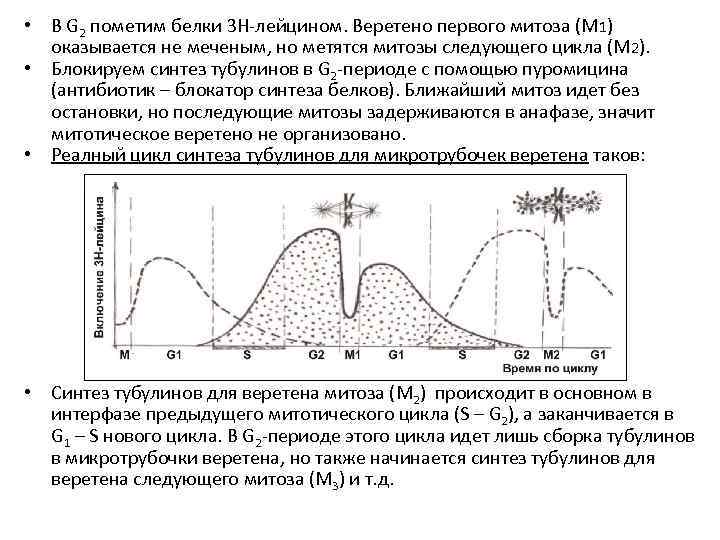
• В G 2 пометим белки 3 Н-лейцином. Веретено первого митоза (М 1) оказывается не меченым, но метятся митозы следующего цикла (М 2). • Блокируем синтез тубулинов в G 2 -периоде с помощью пуромицина (антибиотик – блокатор синтеза белков). Ближайший митоз идет без остановки, но последующие митозы задерживаются в анафазе, значит митотическое веретено не организовано. • Реалный цикл синтеза тубулинов для микротрубочек веретена таков: • Синтез тубулинов для веретена митоза (М 2) происходит в основном в интерфазе предыдущего митотического цикла (S – G 2), а заканчивается в G 1 – S нового цикла. В G 2 -периоде этого цикла идет лишь сборка тубулинов в микротрубочки веретена, но также начинается синтез тубулинов для веретена следующего митоза (М 3) и т. д.
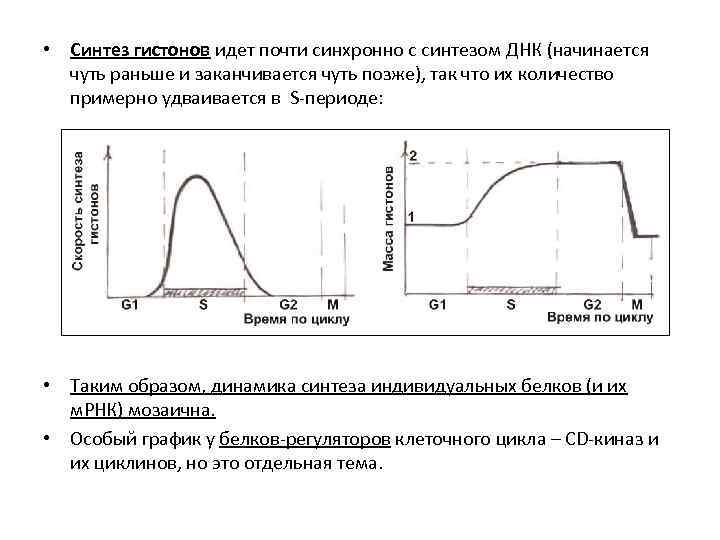
• Синтез гистонов идет почти синхронно с синтезом ДНК (начинается чуть раньше и заканчивается чуть позже), так что их количество примерно удваивается в S-периоде: • Таким образом, динамика синтеза индивидуальных белков (и их м. РНК) мозаична. • Особый график у белков-регуляторов клеточного цикла – CD-киназ и их циклинов, но это отдельная тема.

5. Митоз. Хромосомный цикл В митозе связаны воедино преобразования хромосом – хромосомный цикл, формирование и работа веретена – центросомный цикл и разделение клеточного тела – цитокинетический цикл. Начнем с хромосомного цикла. 5. 1. Концепция структурной непрерывности хромосом В интерфазе клеточного цикла морфологически обособленные хромосомы не видны. Однако они здесь присутствуют в форме хроматина – в деконденсированном (декомпактизованном, деспирализованном) состоянии. - В конденсированном состоянии (метаболически не активном), в процессе митоза, выполняется функция разделения генетического материала. - В деконденсированном состоянии, в интерфазе, - функции репликации и транскрипции. При этом каждая хромосома в цикле остается цельной непрерывной нитью, деконденсация происходит без разборки, без разрывов, а пространственная организация хроматина обеспечена связями с ядерным матриксом и ламиной ядерной оболочки.
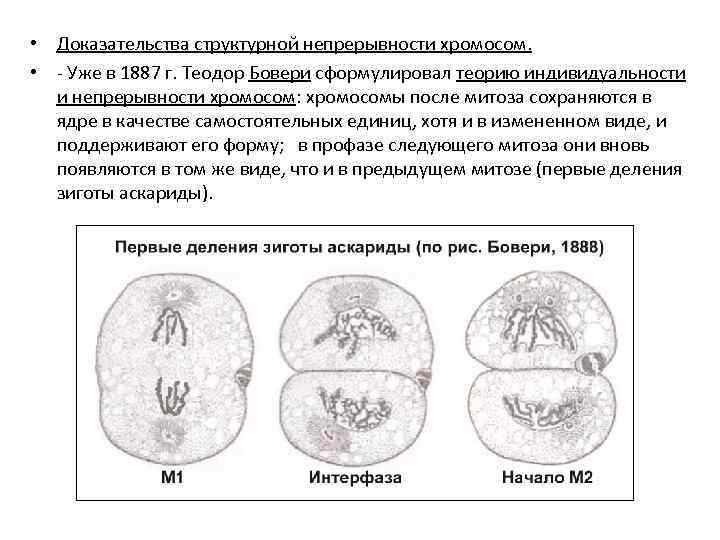
• Доказательства структурной непрерывности хромосом. • - Уже в 1887 г. Теодор Бовери сформулировал теорию индивидуальности и непрерывности хромосом: хромосомы после митоза сохраняются в ядре в качестве самостоятельных единиц, хотя и в измененном виде, и поддерживают его форму; в профазе следующего митоза они вновь появляются в том же виде, что и в предыдущем митозе (первые деления зиготы аскариды).
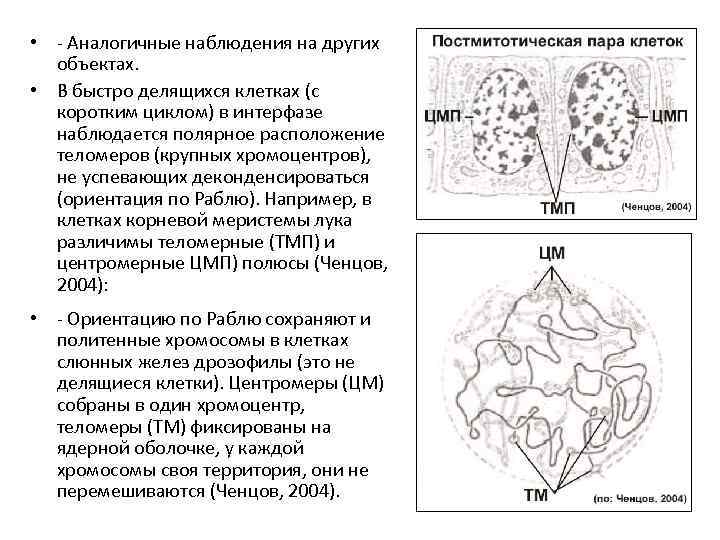
• - Аналогичные наблюдения на других объектах. • В быстро делящихся клетках (с коротким циклом) в интерфазе наблюдается полярное расположение теломеров (крупных хромоцентров), не успевающих деконденсироваться (ориентация по Раблю). Например, в клетках корневой меристемы лука различимы теломерные (ТМП) и центромерные ЦМП) полюсы (Ченцов, 2004): • - Ориентацию по Раблю сохраняют и политенные хромосомы в клетках слюнных желез дрозофилы (это не делящиеся клетки). Центромеры (ЦМ) собраны в один хромоцентр, теломеры (ТМ) фиксированы на ядерной оболочке, у каждой хромосомы своя территория, они не перемешиваются (Ченцов, 2004).
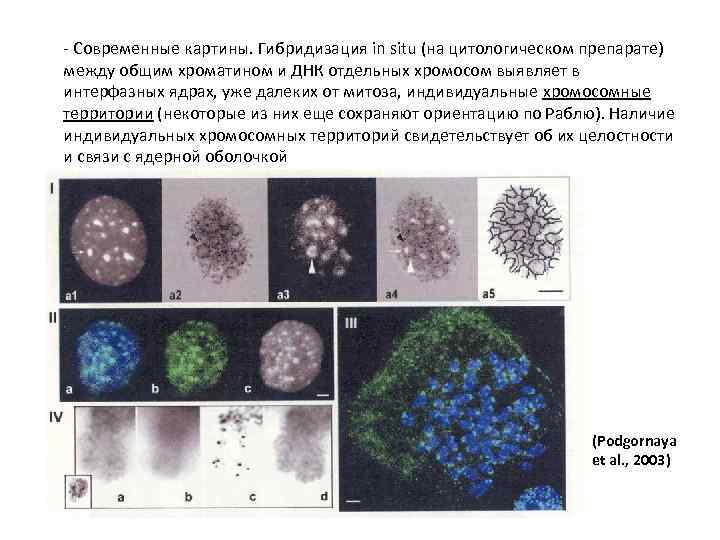
- Современные картины. Гибридизация in situ (на цитологическом препарате) между общим хроматином и ДНК отдельных хромосом выявляет в интерфазных ядрах, уже далеких от митоза, индивидуальные хромосомные территории (некоторые из них еще сохраняют ориентацию по Раблю). Наличие индивидуальных хромосомных территорий свидетельствует об их целостности и связи с ядерной оболочкой (Podgornaya et al. , 2003)

• - Постоянство хромосомной территории для гетерохроматической Ххромосомы в ядрах у особей женского пола млекопитающих (половой хроматин, тельце Барра). • - Закономерное расположение определенных хромосом сохраняется и в метафазной пластинке. Это означает, что в интерфазном ядре они как-то фиксированы и сохраняют целостность, не рассыпаются на фрагменты. • - Работы по доказательству полуконсервативного механизма репликации ДНК. Во 2 -м делении в хромосомах одна хроматида мечена, другая нет. Значит, ДНК хроматиды в интерфазе не распадается, сохраняет индивидуальную целостность. • - По данным формальной генетики, в процессах кроссинговера, скрещивания, при хромосомных разрывах функциональной единицей выступает хроматида. Сцепленное наследование признаков (Морган) – тоже следствие неизменного линейного расположения генов в хроматиде. • - У дрозофилы и др. объектов биохимическое определение молекулярной массы ДНК (центрифугирование, электрофорез) дало полное совпадение с расчетной молекулярной массой (исходя из размера митотических хромосом). Т. о. , хромосома – одна гигантская молекула ДНК, ее длина не изменяется в клеточном цикле.
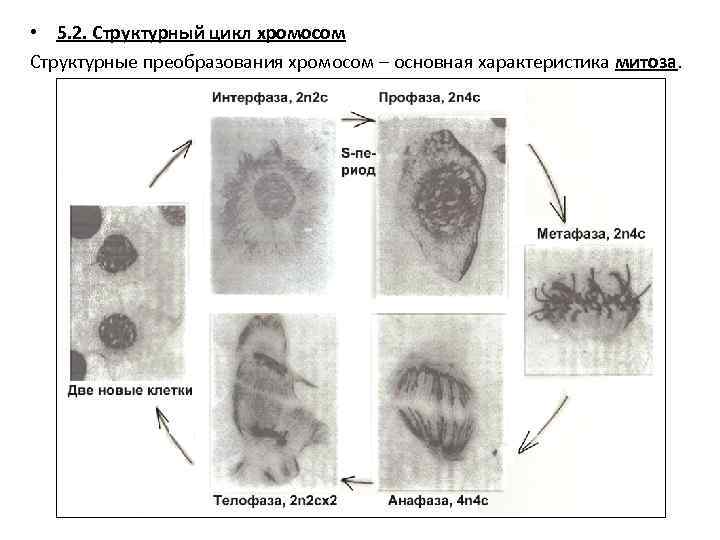
• 5. 2. Структурный цикл хромосом Структурные преобразования хромосом – основная характеристика митоза.

• • • Интерфаза. Хромосомы не видны, они деконденсированы до хроматина. Бывают различимы крупные блоки гетерохроматина, обычно прицентромерного и теломерного. Удвоение ДНК (хроматид) визуально определяется только по объему и плотности ядра. Генетическая формула клетки: 2 n 2 c → 2 n 4 c. Профаза. Появляются нитевидные хромосомы (плотный клубок, рыхлый клубок – процесс компактизации). Они сначала длинные и тонкие. Иногда видно, что они уже двойные – это сестринские хроматиды. Начинает разрушаться ядерная оболочка. Генетическая формула клетки: 2 n 4 c. Прометафаза. Компактизация продолжается. Центромерные участки хромосом под действием нитей веретена выталкиваются к экватору клетки. Ядерная оболочка распалась. Генетическая формула клетки: 2 n 4 c. Метафаза. Максимальная компактизация хромосом. Все они бихроматидные. Плечи разделены, но центромеры пока еще связаны. Т. к. все центромеры собраны в экваторе (под действие веретена), хромосомы организованы в виде метафазной пластинки. Генетическая формула клетки: 2 n 4 c. Анафаза. Сохраняется максимальная компактизация. Хроматиды разделяются и под действием веретена расходятся к его полюсам. Генетическая формула клетки: 4 n 4 c. Телофаза. Формируются дочерние ядра. Начинается деконденсация хромосом, они представляют плотный клубок. Происходит цитокинез. Клетки входят в новую интерфазу. Генетическая формула клетки: 2 n 2 c х 2.

• У разных видов животных и растений метафазная пластинка выглядит по-разному, так как различны параметры кариотипа: число хромосом, их размеры и форма. Диплоидные (2 n) хромосомные наборы: 1 – 22 хромосомы жабы Bufo arenarum; 2 – 140 хромосом ящерицы. Tupinambis teguixin; 3 – 12 хромосом чернушки Nigella orientalis (сем. лютиковые); 4 – 208 хромосом камчатского краба Paralithodes camtschatica; 5 – 46 хромосом человека Homo sapiens; 6 – 23 хромосомы прямокрылого насекомого Chromacris miles; 7 – 8 хромосом сложноцветного растения Hypochoeris tweedie. NB: Все рисунки выполнены при одном увеличении (Мюнтцинг, 1967).
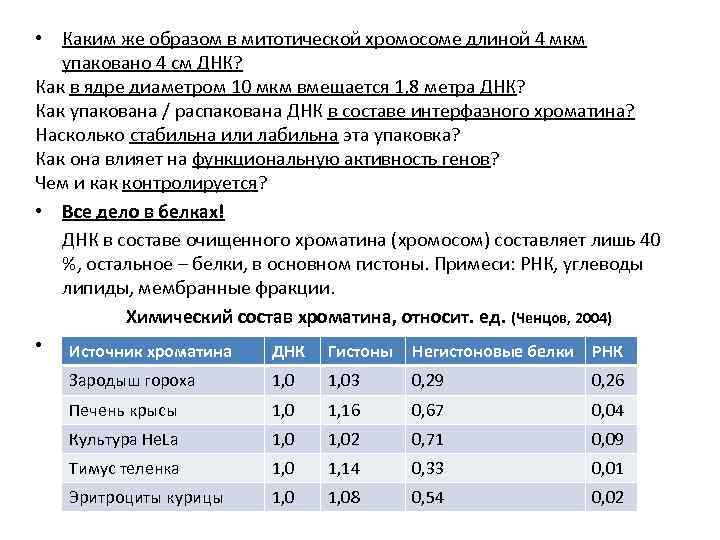
• Каким же образом в митотической хромосоме длиной 4 мкм упаковано 4 см ДНК? Как в ядре диаметром 10 мкм вмещается 1, 8 метра ДНК? Как упакована / распакована ДНК в составе интерфазного хроматина? Насколько стабильна или лабильна эта упаковка? Как она влияет на функциональную активность генов? Чем и как контролируется? • Все дело в белках! ДНК в составе очищенного хроматина (хромосом) составляет лишь 40 %, остальное – белки, в основном гистоны. Примеси: РНК, углеводы липиды, мембранные фракции. Химический состав хроматина, относит. ед. (Ченцов, 2004) • Источник хроматина ДНК Гистоны Негистоновые белки РНК Зародыш гороха 1, 03 0, 29 0, 26 Печень крысы 1, 0 1, 16 0, 67 0, 04 Культура He. La 1, 02 0, 71 0, 09 Тимус теленка 1, 0 1, 14 0, 33 0, 01 Эритроциты курицы 1, 08 0, 54 0, 02

• Гистоны отвечают за низшие уровни компактизации. Это оснóвные (щелочные) белки, богатые лизином и аргинином. Весьма однообразны и консервативны. У эукариот всего 5 -7 типов гистонов (Н 1, Н 2 А, Н 2 В, Н 3, Н 4, Н 5. . . ). • Н 3 и Н 4 – аргининбогатые гистоны, самые консервативные (у коровы и гороха различия всего по 2 аминокислотам). • Н 2 А и Н 2 В – умеренно лизинбогатые. Имеется межвидовая вариабельность. • Н 1 – большое семейство лизинбогатых гистонов, самые щелочные (легко отделяются от хроматина в 0, 5 М солевых растворах). Наименее консервативные, имеются межвидовые и даже межтканевые вариации. • Н 5 – содержит много аргинина и серина. Замещает гистон Н 1 в эритроцитах низших позвоночных.

• NB: С помощью положительных зарядов лизина и аргинина гистоны образуют нековалентные (солевые, ионные, электростатические) связи с фосфатными группами ДНК. (В растворах с высокой ионной силой: 1 -2 М Na. Cl – все гистоны полностью отделяются от ДНК. ) Поэтому хроматиновый ДНП-комплекс имеет лабильную организацию. Для всех гистонов (особенно Н 1) характерно кластерное распределение лизина и аргинина на N- и С-концах молекулы. Именно концы молекулы (щелочные, положительно заряженные) взаимодействуют с ДНК и соседними гистонами. Средние участки нейтральны и образуют 3 -4 α-спиральных домена. (Ченцов, 2004)
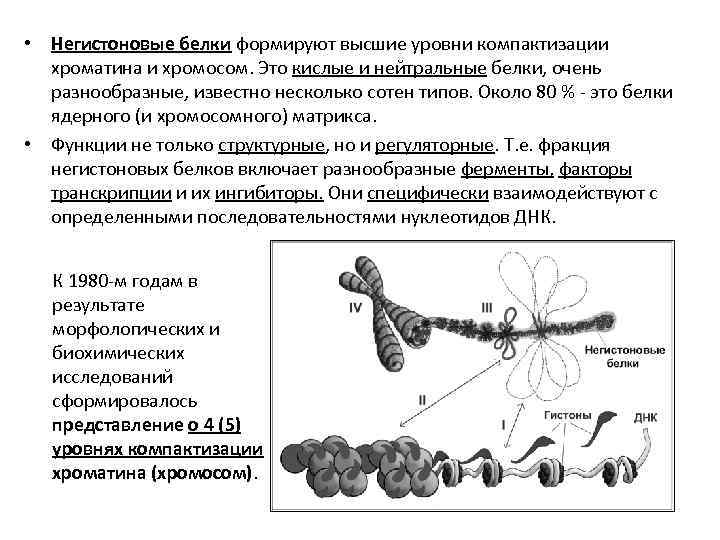
• Негистоновые белки формируют высшие уровни компактизации хроматина и хромосом. Это кислые и нейтральные белки, очень разнообразные, известно несколько сотен типов. Около 80 % - это белки ядерного (и хромосомного) матрикса. • Функции не только структурные, но и регуляторные. Т. е. фракция негистоновых белков включает разнообразные ферменты, факторы транскрипции и их ингибиторы. Они специфически взаимодействуют с определенными последовательностями нуклеотидов ДНК. К 1980 -м годам в результате морфологических и биохимических исследований сформировалось представление о 4 (5) уровнях компактизации хроматина (хромосом).

• (I) Нуклеосомная фибрилла диаметром 10 нм. (1 нм = 0, 001 мкм). Хроматин в щелочной среде с низкой ионной силой распадается на тонкие фибриллы типа «бусы на нитке» . «Бусы» – ДНК-гистоновые глобулы диаметром 10 -11 нм, скорость седиментации – 11 S. «Нитка» – отрезки ДНК (толщина 2 нм) длиной около 20 нм (разрушается ДНКазой). Микрококковая нуклеаза режет хроматин на отрезки, кратные 200 нп (200, 400, 600. . . нп) и 11 S (11 S, 22 S, 33 S…). Т. о. , выявляются мономеры (элементарные частицы хроматина), их димеры, тримеры. . . Элементарные частицы получили название нуклеосомы. (Ченцов, 2004)

• Максимальная нуклеосома (11 S) включает: фрагмент ДНК около 200 нп, сердцевину (кор) из 8 гистонов – октамер (2 х. Н 2 А, 2 х. Н 2 В, 2 х. Н 3, 2 х. Н 4) и одну молекулу гистона Н 1. Вокруг кора 146 нп образуют 1, 75 оборота, остальные 54+ нп (8 -114) образуют свободный линкер. Гистоны Н 1 расположены поверх нуклеосом, (Альбертс и др. , 1994) взаимодействуя с кором и линкером. • Минимальная нуклеосома – то же без линкера и Н 1. • Коэффициент компактизации ДНК в нуклеосомной фибрилле = 6 -7 х. • NB: гистон Н 1 для образования самих нуклеосом не требуется, но участвует в стягивании соседних нуклеосом при формировании следующего уровня компактизации. • Нуклеосомная структура хроматина устанавливается сразу в момент репликации ДНК, так как синтез гистонов немного опережает синтез ДНК. Старые и новые октамеры гистонов (коровые частицы) распределяются между сестринскими цепями ДНК случайным образом. В репликативной вилке, а также под РНК-полимеразой при синтезе РНК нуклеосомы, вероятно, расщепляются в полунуклеосомы, не сползая с ДНК.
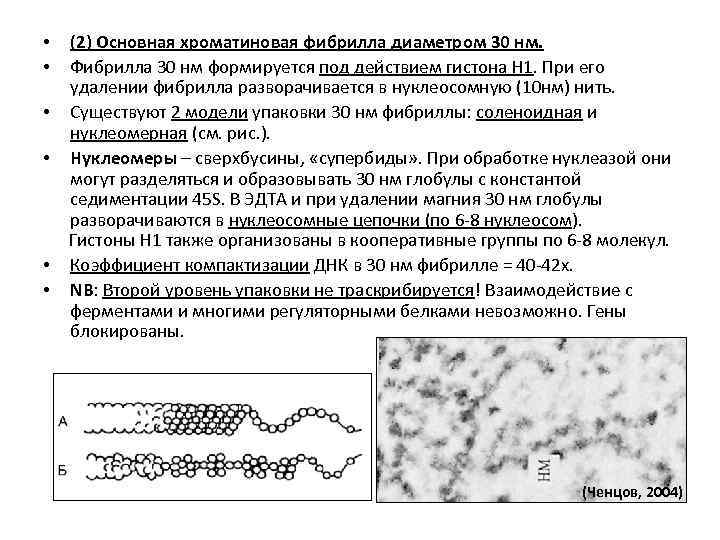
(2) Основная хроматиновая фибрилла диаметром 30 нм. Фибрилла 30 нм формируется под действием гистона Н 1. При его удалении фибрилла разворачивается в нуклеосомную (10 нм) нить. • Существуют 2 модели упаковки 30 нм фибриллы: соленоидная и нуклеомерная (см. рис. ). • Нуклеомеры – сверхбусины, «супербиды» . При обработке нуклеазой они могут разделяться и образовывать 30 нм глобулы с константой седиментации 45 S. В ЭДТА и при удалении магния 30 нм глобулы разворачиваются в нуклеосомные цепочки (по 6 -8 нуклеосом). Гистоны Н 1 также организованы в кооперативные группы по 6 -8 молекул. • Коэффициент компактизации ДНК в 30 нм фибрилле = 40 -42 х. • NB: Второй уровень упаковки не траскрибируется! Взаимодействие с ферментами и многими регуляторными белками невозможно. Гены блокированы. • • (Ченцов, 2004)
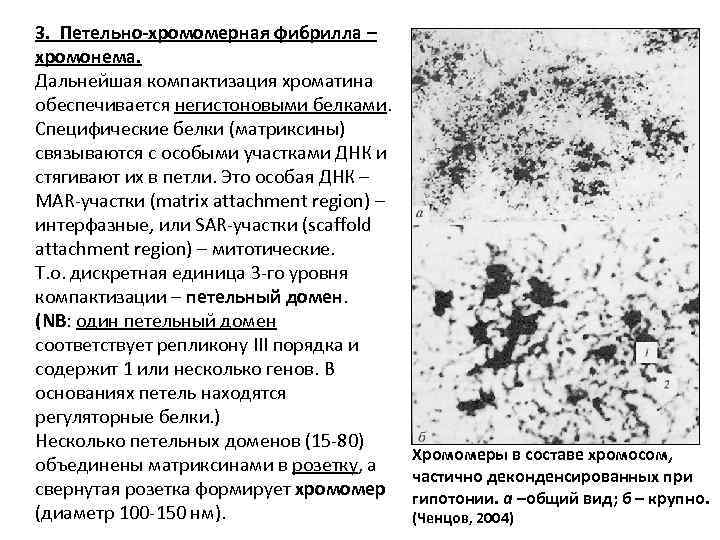
3. Петельно-хромомерная фибрилла – хромонема. Дальнейшая компактизация хроматина обеспечивается негистоновыми белками. Специфические белки (матриксины) связываются с особыми участками ДНК и стягивают их в петли. Это особая ДНК – MAR-участки (matrix attachment region) – интерфазные, или SAR-участки (scaffold attachment region) – митотические. Т. о. дискретная единица 3 -го уровня компактизации – петельный домен. (NB: один петельный домен соответствует репликону III порядка и содержит 1 или несколько генов. В основаниях петель находятся регуляторные белки. ) Несколько петельных доменов (15 -80) Хромомеры в составе хромосом, объединены матриксинами в розетку, а частично деконденсированных при свернутая розетка формирует хромомер гипотонии. а –общий вид; б – крупно. (диаметр 100 -150 нм). (Ченцов, 2004)
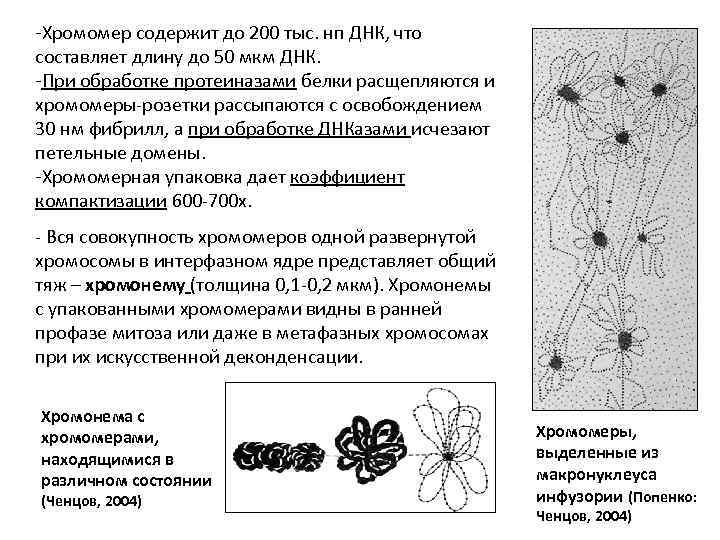
-Хромомер содержит до 200 тыс. нп ДНК, что составляет длину до 50 мкм ДНК. -При обработке протеиназами белки расщепляются и хромомеры-розетки рассыпаются с освобождением 30 нм фибрилл, а при обработке ДНКазами исчезают петельные домены. -Хромомерная упаковка дает коэффициент компактизации 600 -700 х. - Вся совокупность хромомеров одной развернутой хромосомы в интерфазном ядре представляет общий тяж – хромонему (толщина 0, 1 -0, 2 мкм). Хромонемы с упакованными хромомерами видны в ранней профазе митоза или даже в метафазных хромосомах при их искусственной деконденсации. Хромонема с хромомерами, находящимися в различном состоянии (Ченцов, 2004) Хромомеры, выделенные из макронуклеуса инфузории (Попенко: Ченцов, 2004)
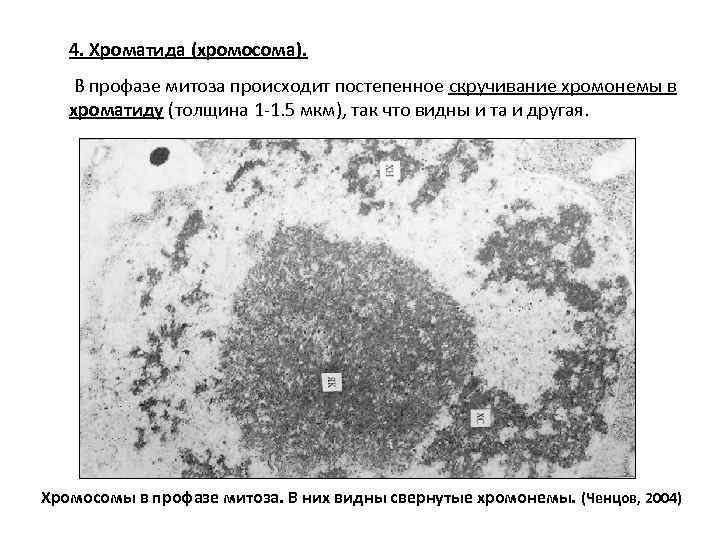
4. Хроматида (хромосома). В профазе митоза происходит постепенное скручивание хромонемы в хроматиду (толщина 1 -1. 5 мкм), так что видны и та и другая. Хромосомы в профазе митоза. В них видны свернутые хромонемы. (Ченцов, 2004)
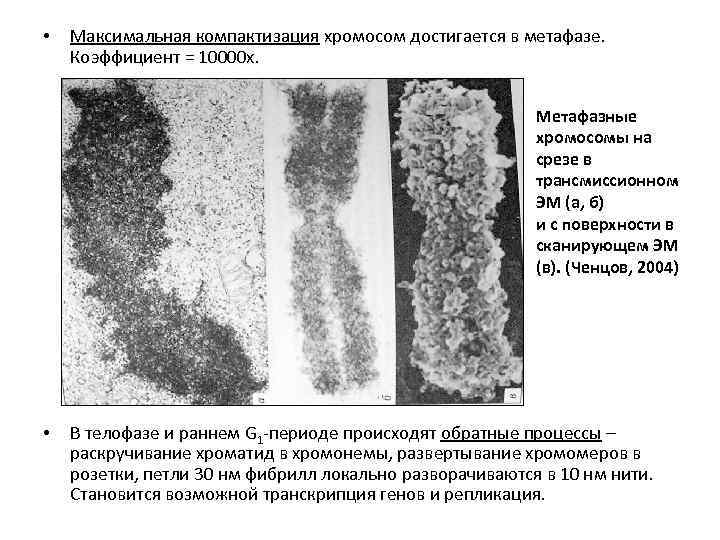
• Максимальная компактизация хромосом достигается в метафазе. Коэффициент = 10000 х. Метафазные хромосомы на срезе в трансмиссионном ЭМ (а, б) и с поверхности в сканирующем ЭМ (в). (Ченцов, 2004) • В телофазе и раннем G 1 -периоде происходят обратные процессы – раскручивание хроматид в хромонемы, развертывание хромомеров в розетки, петли 30 нм фибрилл локально разворачиваются в 10 нм нити. Становится возможной транскрипция генов и репликация.
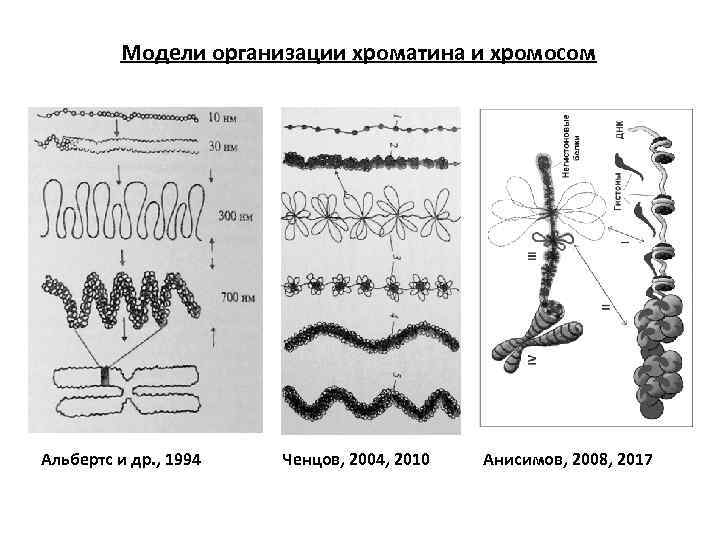
Модели организации хроматина и хромосом Альбертс и др. , 1994 Ченцов, 2004, 2010 Анисимов, 2008, 2017

6. Митоз. Цикл митотического веретена Веретено обеспечивает расхождение хромосом в митозе. Это совокупность микротрубочек и моторных белков-транслокаторов. Цикл веретена в целом согласован с циклом хромосом, что обеспечивает синхронность процессов. 6. 1. Микротрубочки (25 нм) – элементы цитоскелета, состоят из белков тубулинов и микротрубочко-ассоциированных протеинов (MAPs). Локализация МТ различна : бывают одиночные МТ, рыхлые пучки, центриоли и базальные тельца (3 х9), аксонема ресничек и жгутиков (2 х9 + 2). Во время митоза большая часть МТ входит в состав митотического веретена. Полимеризация МТ. Субъединицы α- и β-тубулина (5 нм) образуют гетеродимеры, потом кольца (нуклеация), потом трубочки в 13 продольных протофиламентов. Полимеризация сопровождается гидролизом ГТФ до ГДФ. Димеры изначально поляризованы, поэтому и каждая МТ оказывается полярной. Быстро растущий плюс-конец и медленно растущий или разбираемый минус-конец (разная скорость гидролиза ГТФ, до его полной остановки). (по: Campbell, 1996)
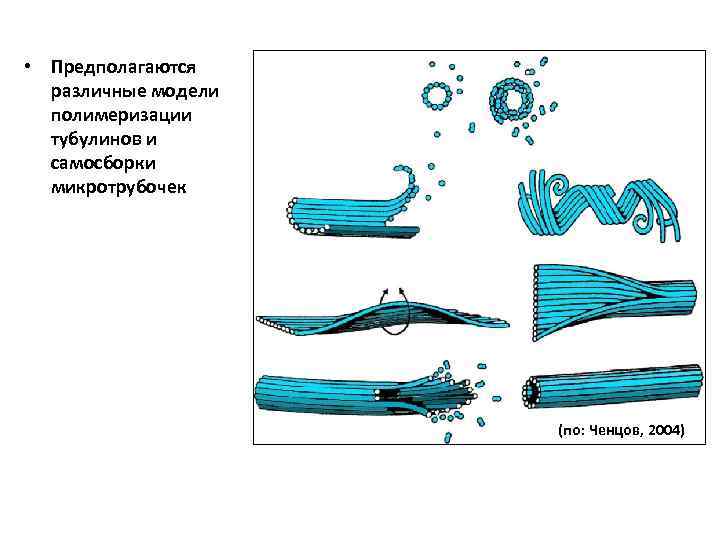
• Предполагаются различные модели полимеризации тубулинов и самосборки микротрубочек (по: Ченцов, 2004)

• NB: Рост на +конце преобладает (быстрый гидролиз ГТФ) = удлинение МТ. Но при недостатке тубулинов и ГТФ МТ могут разбираться с двух концов = полная разборка. Разборка усиливается при понижении температуры и в присутствии Са 2+. • Колхицин (алкалоид) связывается с тубулином и препятствует полимеризации МТ = разборка цитоплазматических МТ (потеря формы клеток) и МТ митотического веретена. То же с колцемидом и нокодозолом, но после отмывки МТ восстанавливаются. • Таксол, напротив, способствует полимеризации тубулина, даже при низких концентрациях = избыточный рост МТ. • MAP-белки ускоряют полимеризацию = стабилизируют МТ в дифференцированных клетках. • ВЫВОД: МТ являются очень динамичными структурами, способны быстро возникать и разрушаться. Время полужизни МТ = около 5 мин! За 15 мин. обновляется около 80% МТ. • В дифференцированных клетках до 20 % МТ стабилизированы, «живут» несколько часов (дополнительные MAPs, ацетилирование по лизину, удаление терминального тирозина).
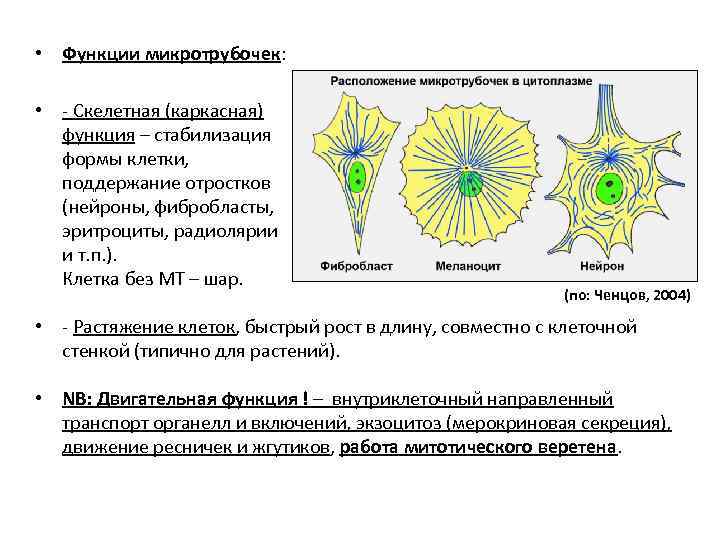
• Функции микротрубочек: • - Скелетная (каркасная) функция – стабилизация формы клетки, поддержание отростков (нейроны, фибробласты, эритроциты, радиолярии и т. п. ). Клетка без МТ – шар. (по: Ченцов, 2004) • - Растяжение клеток, быстрый рост в длину, совместно с клеточной стенкой (типично для растений). • NB: Двигательная функция ! – внутриклеточный направленный транспорт органелл и включений, экзоцитоз (мерокриновая секреция), движение ресничек и жгутиков, работа митотического веретена.

• Механизм движения органелл по микротрубочкам. • 1960 -е годы. В аксонах нервных клеток открыт быстрый транспорт веществ – намного более быстрый, чем общий ток цитоплазмы. Скорость = 20 -40 см/сут. • Это оказалось перемещение вакуолей (везикул) и гранул по микротрубочкам. • Т. о. , микротрубочки – не просто направляющие пути для перемещения органелл. Это «рельсы» , по которым движутся «локомотивы» , без них это движение невозможно. • NB: Транспорт по микротрубочкам идет в двух противоположных направлениях. (Ченцов, 2004)
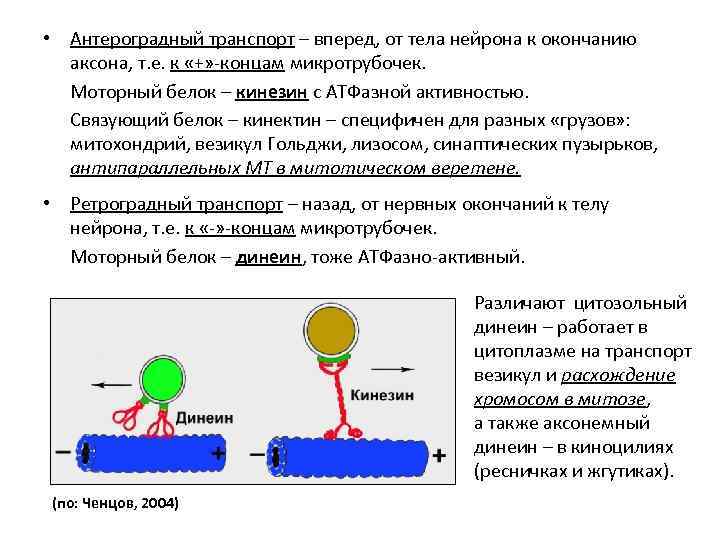
• Антероградный транспорт – вперед, от тела нейрона к окончанию аксона, т. е. к «+» -концам микротрубочек. Моторный белок – кинезин с АТФазной активностью. Связующий белок – кинектин – специфичен для разных «грузов» : митохондрий, везикул Гольджи, лизосом, синаптических пузырьков, антипараллельных МТ в митотическом веретене. • Ретроградный транспорт – назад, от нервных окончаний к телу нейрона, т. е. к «-» -концам микротрубочек. Моторный белок – динеин, тоже АТФазно-активный. Различают цитозольный динеин – работает в цитоплазме на транспорт везикул и расхождение хромосом в митозе, а также аксонемный динеин – в киноцилиях (ресничках и жгутиках). (по: Ченцов, 2004)
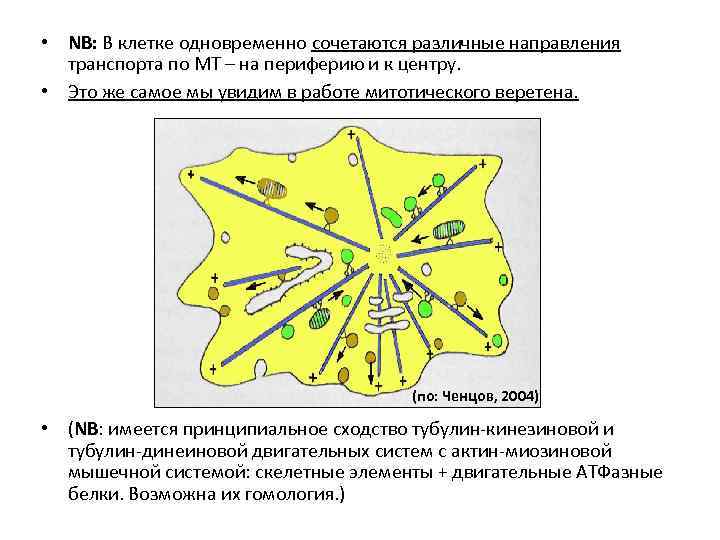
• NB: В клетке одновременно сочетаются различные направления транспорта по МТ – на периферию и к центру. • Это же самое мы увидим в работе митотического веретена. (по: Ченцов, 2004) • (NB: имеется принципиальное сходство тубулин-кинезиновой и тубулин-динеиновой двигательных систем с актин-миозиновой мышечной системой: скелетные элементы + двигательные АТФазные белки. Возможна их гомология. )
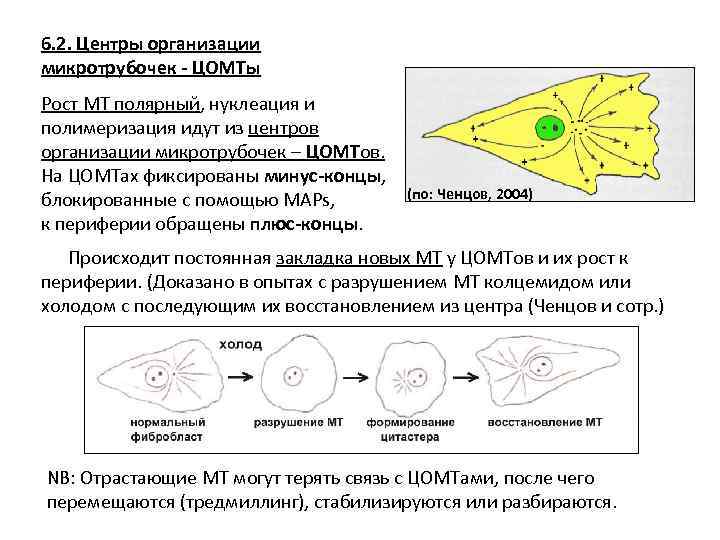
6. 2. Центры организации микротрубочек - ЦОМТы Рост МТ полярный, нуклеация и полимеризация идут из центров организации микротрубочек – ЦОМТов. На ЦОМТах фиксированы минус-концы, блокированные с помощью МАРs, к периферии обращены плюс-концы. (по: Ченцов, 2004) Происходит постоянная закладка новых МТ у ЦОМТов и их рост к периферии. (Доказано в опытах с разрушением МТ колцемидом или холодом с последующим их восстановлением из центра (Ченцов и сотр. ) NB: Отрастающие МТ могут терять связь с ЦОМТами, после чего перемещаются (тредмиллинг), стабилизируются или разбираются.
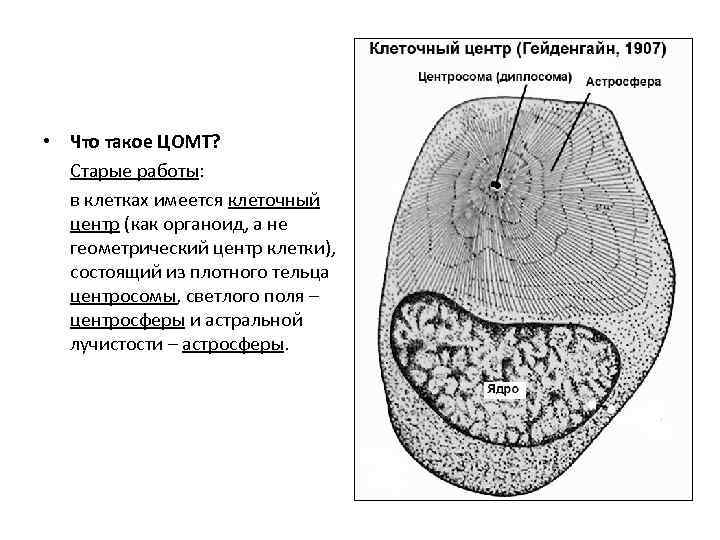
• Что такое ЦОМТ? Старые работы: в клетках имеется клеточный центр (как органоид, а не геометрический центр клетки), состоящий из плотного тельца центросомы, светлого поля – центросферы и астральной лучистости – астросферы.
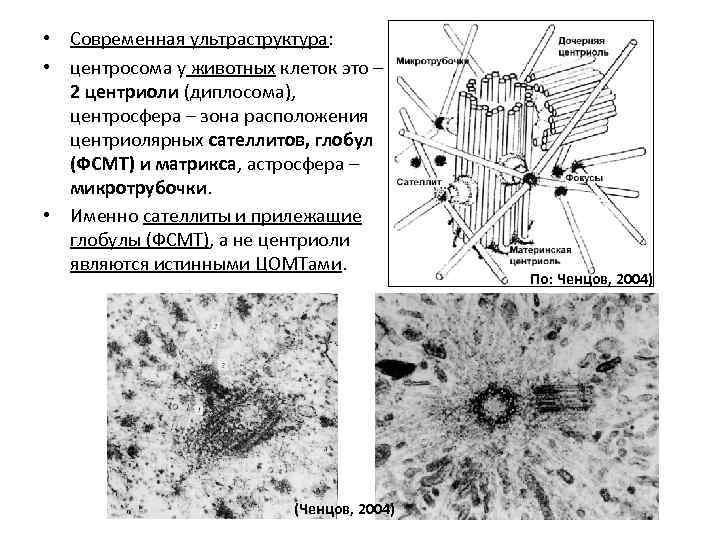
• Современная ультраструктура: • центросома у животных клеток это – 2 центриоли (диплосома), центросфера – зона расположения центриолярных сателлитов, глобул (ФСМТ) и матрикса, астросфера – микротрубочки. • Именно сателлиты и прилежащие глобулы (ФСМТ), а не центриоли являются истинными ЦОМТами. (Ченцов, 2004) По: Ченцов, 2004)

• NB: Пара центриолей – материнская и дочерняя. Воспроизводятся в клеточном цикле по консервативному принципу: отрастанием сбоку. Механизм не известен. Центриоли имеют разный возраст. Сателлиты и ФСМТ имеются только на материнской центриоли. • NB: У высших растений, низших грибов, некоторых простейших ЦОМТы не имеют четкой локализации, так как в них нет центриолей. Диффузный ЦОМТ-материал локализован на периферии клеточного ядра (снаружи или внутри), откуда МТ расходятся радиально. Это подтверждает, что истинные ЦОМТы – не центриоли, а прилежащий материал. Сами центриоли – лишь «пассажиры» , расходящиеся с гарантией в дочерние клетки во время митоза (аналогия Ю. С. Ченцова). • А функция центриолей – это потенциальные базальные тельца киноцилий (ресничек и жгутиков).
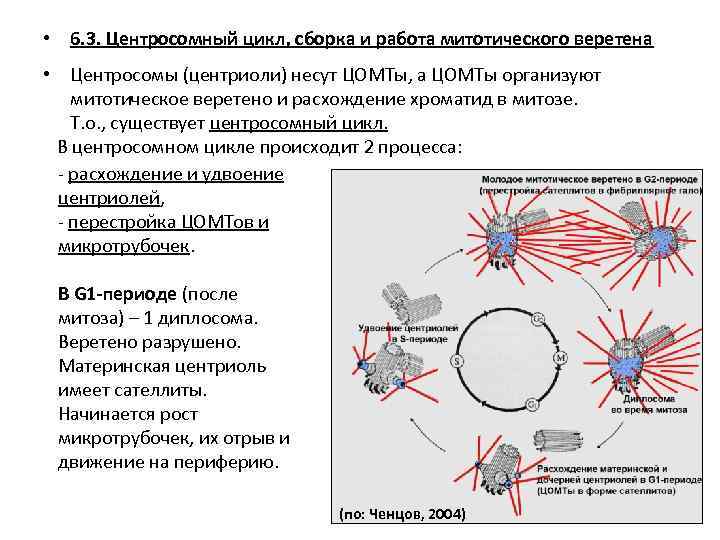
• 6. 3. Центросомный цикл, сборка и работа митотического веретена • Центросомы (центриоли) несут ЦОМТы, а ЦОМТы организуют митотическое веретено и расхождение хроматид в митозе. Т. о. , существует центросомный цикл. В центросомном цикле происходит 2 процесса: - расхождение и удвоение центриолей, - перестройка ЦОМТов и микротрубочек. В G 1 -периоде (после митоза) – 1 диплосома. Веретено разрушено. Материнская центриоль имеет сателлиты. Начинается рост микротрубочек, их отрыв и движение на периферию. (по: Ченцов, 2004)
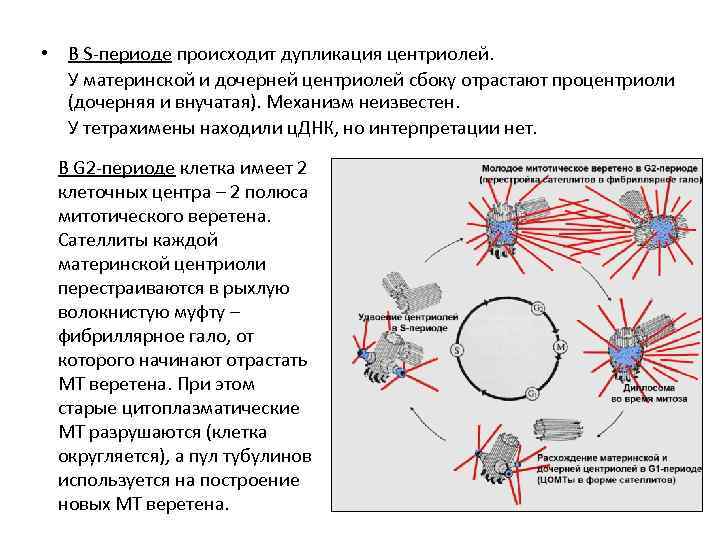
• В S-периоде происходит дупликация центриолей. У материнской и дочерней центриолей сбоку отрастают процентриоли (дочерняя и внучатая). Механизм неизвестен. У тетрахимены находили ц. ДНК, но интерпретации нет. В G 2 -периоде клетка имеет 2 клеточных центра – 2 полюса митотического веретена. Сателлиты каждой материнской центриоли перестраиваются в рыхлую волокнистую муфту – фибриллярное гало, от которого начинают отрастать МТ веретена. При этом старые цитоплазматические МТ разрушаются (клетка округляется), а пул тубулинов используется на построение новых МТ веретена.
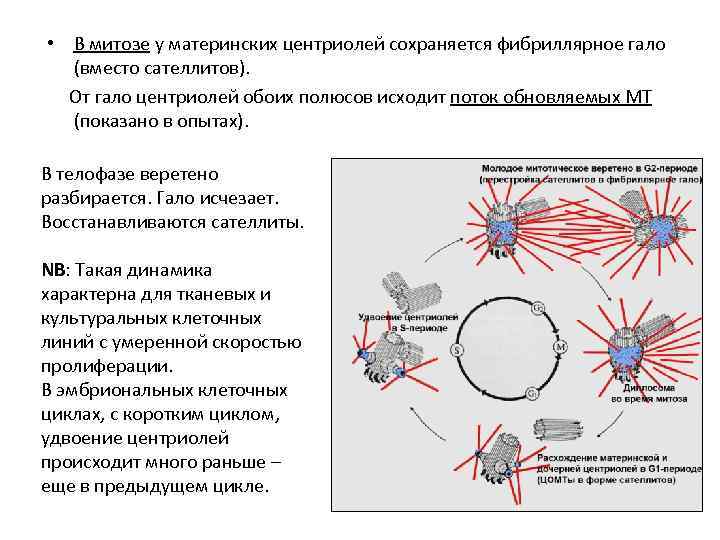
• В митозе у материнских центриолей сохраняется фибриллярное гало (вместо сателлитов). От гало центриолей обоих полюсов исходит поток обновляемых МТ (показано в опытах). В телофазе веретено разбирается. Гало исчезает. Восстанавливаются сателлиты. NB: Такая динамика характерна для тканевых и культуральных клеточных линий с умеренной скоростью пролиферации. В эмбриональных клеточных циклах, с коротким циклом, удвоение центриолей происходит много раньше – еще в предыдущем цикле.
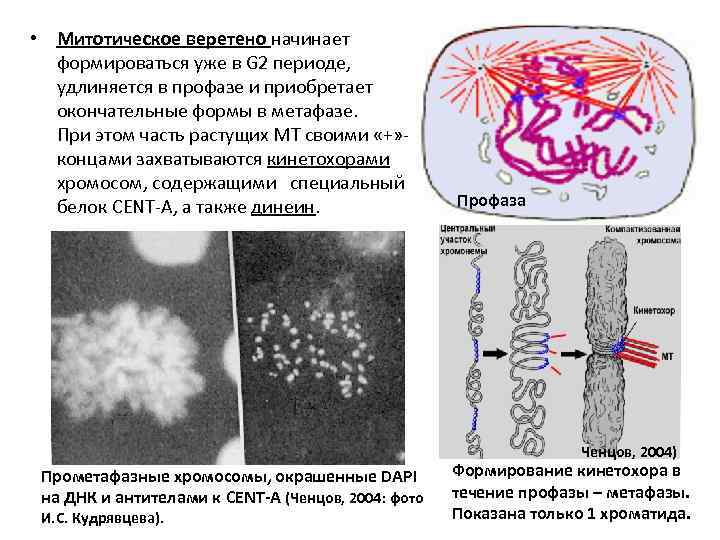
• Митотическое веретено начинает формироваться уже в G 2 периоде, удлиняется в профазе и приобретает окончательные формы в метафазе. При этом часть растущих МТ своими «+» - концами захватываются кинетохорами хромосом, содержащими специальный белок CENT-A, а также динеин. Профаза Ченцов, 2004) Прометафазные хромосомы, окрашенные DAPI на ДНК и антителами к CENT-A (Ченцов, 2004: фото И. С. Кудрявцева). Формирование кинетохора в течение профазы – метафазы. Показана только 1 хроматида.
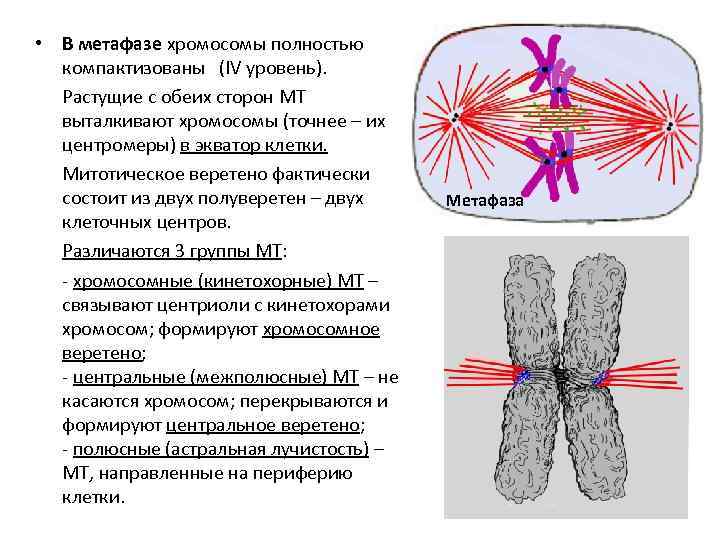
• В метафазе хромосомы полностью компактизованы (IV уровень). Растущие с обеих сторон МТ выталкивают хромосомы (точнее – их центромеры) в экватор клетки. Митотическое веретено фактически состоит из двух полуверетен – двух клеточных центров. Различаются 3 группы МТ: - хромосомные (кинетохорные) МТ – связывают центриоли с кинетохорами хромосом; формируют хромосомное веретено; - центральные (межполюсные) МТ – не касаются хромосом; перекрываются и формируют центральное веретено; - полюсные (астральная лучистость) – МТ, направленные на периферию клетки. Метафаза
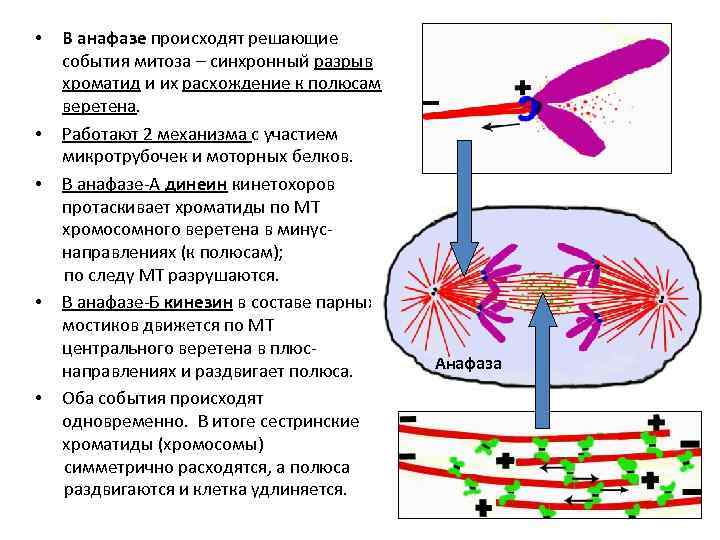
• • • В анафазе происходят решающие события митоза – синхронный разрыв хроматид и их расхождение к полюсам веретена. Работают 2 механизма с участием микротрубочек и моторных белков. В анафазе-А динеин кинетохоров протаскивает хроматиды по МТ хромосомного веретена в минуснаправлениях (к полюсам); по следу МТ разрушаются. В анафазе-Б кинезин в составе парных мостиков движется по МТ центрального веретена в плюснаправлениях и раздвигает полюса. Оба события происходят одновременно. В итоге сестринские хроматиды (хромосомы) симметрично расходятся, а полюса раздвигаются и клетка удлиняется. Анафаза
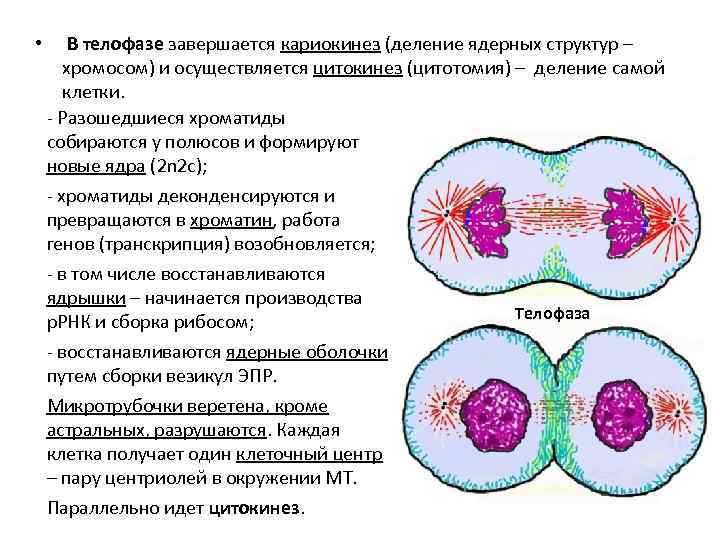
• В телофазе завершается кариокинез (деление ядерных структур – хромосом) и осуществляется цитокинез (цитотомия) – деление самой клетки. - Разошедшиеся хроматиды собираются у полюсов и формируют новые ядра (2 n 2 c); - хроматиды деконденсируются и превращаются в хроматин, работа генов (транскрипция) возобновляется; - в том числе восстанавливаются ядрышки – начинается производства Телофаза р. РНК и сборка рибосом; - восстанавливаются ядерные оболочки путем сборки везикул ЭПР. Микротрубочки веретена, кроме астральных, разрушаются. Каждая клетка получает один клеточный центр – пару центриолей в окружении МТ. Параллельно идет цитокинез.
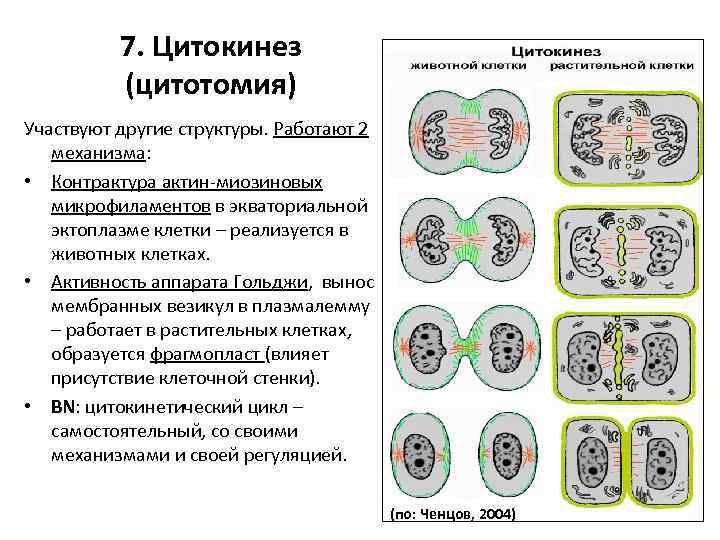
7. Цитокинез (цитотомия) Участвуют другие структуры. Работают 2 механизма: • Контрактура актин-миозиновых микрофиламентов в экваториальной эктоплазме клетки – реализуется в животных клетках. • Активность аппарата Гольджи, вынос мембранных везикул в плазмалемму – работает в растительных клетках, образуется фрагмопласт (влияет присутствие клеточной стенки). • BN: цитокинетический цикл – самостоятельный, со своими механизмами и своей регуляцией. (по: Ченцов, 2004)
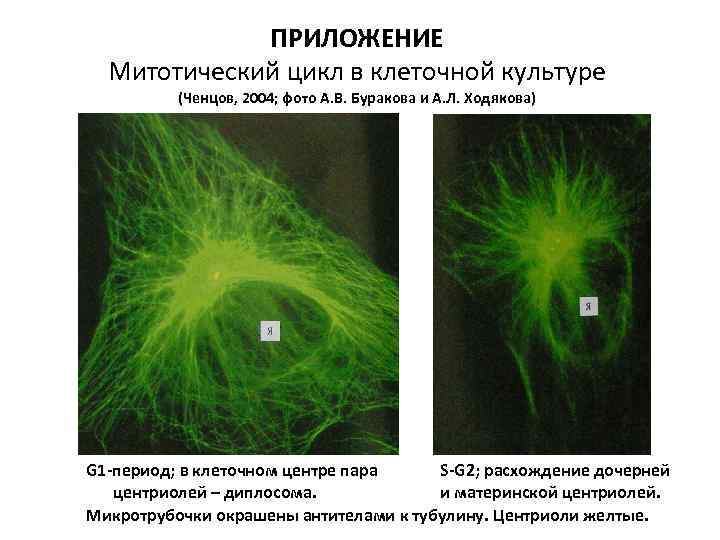
ПРИЛОЖЕНИЕ Митотический цикл в клеточной культуре (Ченцов, 2004; фото А. В. Буракова и А. Л. Ходякова) G 1 -период; в клеточном центре пара S-G 2; расхождение дочерней центриолей – диплосома. и материнской центриолей. Микротрубочки окрашены антителами к тубулину. Центриоли желтые.
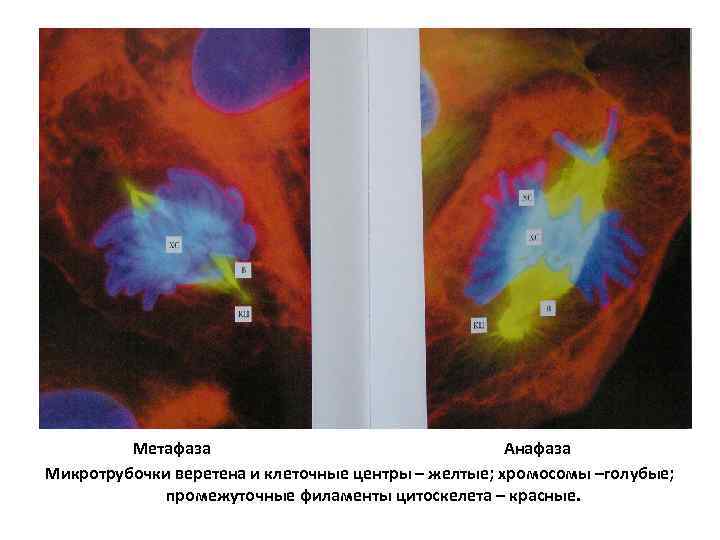
Метафаза Анафаза Микротрубочки веретена и клеточные центры – желтые; хромосомы –голубые; промежуточные филаменты цитоскелета – красные.
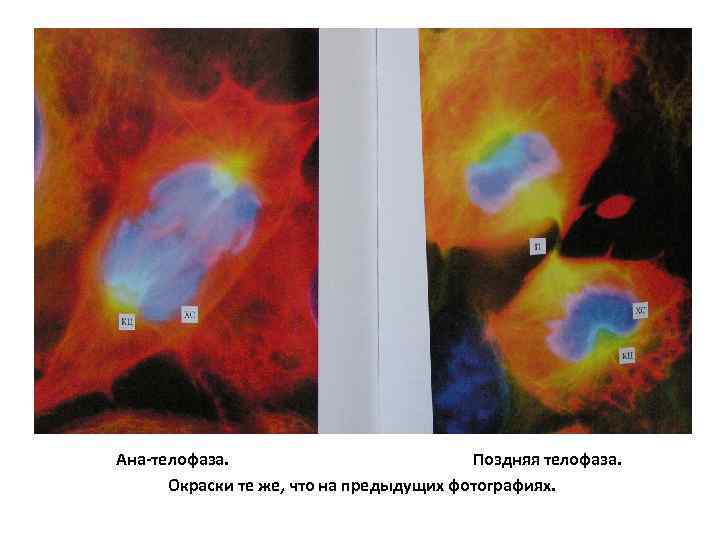
Ана-телофаза. Поздняя телофаза. Окраски те же, что на предыдущих фотографиях.

• Т. о. , митотический цикл – сочетание трех относительно независимых циклов: - хромосомный цикл; - центросомный цикл; - цитокинетический цикл. • Каждый цикл имеет свою регуляцию. В норме эти циклы согласованы, но возможны рассогласования, приводящие к нарушениям митоза с различными последствиями.
РиДК_Тема 1.pptx