ГИ.pptx
- Количество слайдов: 43
 Минимально-инвазивная хирургия в лечении нетравматических внутримозговых гематом гипертензивного генеза
Минимально-инвазивная хирургия в лечении нетравматических внутримозговых гематом гипертензивного генеза
 Сосудистые заболевания мозга актуальная медицинская и социальная проблема. Сегодня в мире около 9 млн человек страдают цереброваскулярными болезнями. Основное место среди них занимают инсульты, каждый год поражающие от 5, 6 до 6, 6 млн человек и уносящие 4, 6 млн жизней; смертность от цереброваскулярных заболеваний находится на 3 м (после заболеваний сердца и опухолей всех локализаций) месте и достигает в экономически развитых странах 11 12 %. Многие миллионы людей становятся инвалидами. Инсульт — это очень тяжелое и опасное заболевание, сопровождающееся поражением сосуда, а затем центральной нервной системы. Слово «инсульт» образовано от латинского insulto — «скакать, прыгать» и обозначает «приступ, удар, натиск» . По определению ВОЗ: Инсульт — быстро развивающееся фокальное или глобальное нарушение функций мозга, длящееся более 24 ч или приводящее к смерти, при исключении иного генеза заболевания.
Сосудистые заболевания мозга актуальная медицинская и социальная проблема. Сегодня в мире около 9 млн человек страдают цереброваскулярными болезнями. Основное место среди них занимают инсульты, каждый год поражающие от 5, 6 до 6, 6 млн человек и уносящие 4, 6 млн жизней; смертность от цереброваскулярных заболеваний находится на 3 м (после заболеваний сердца и опухолей всех локализаций) месте и достигает в экономически развитых странах 11 12 %. Многие миллионы людей становятся инвалидами. Инсульт — это очень тяжелое и опасное заболевание, сопровождающееся поражением сосуда, а затем центральной нервной системы. Слово «инсульт» образовано от латинского insulto — «скакать, прыгать» и обозначает «приступ, удар, натиск» . По определению ВОЗ: Инсульт — быстро развивающееся фокальное или глобальное нарушение функций мозга, длящееся более 24 ч или приводящее к смерти, при исключении иного генеза заболевания.
 Кровоизлияние в головной мозг, или геморрагический инсульт, – клиническая форма, возникающая из за разрыва интрацеребрального сосуда или повышенной проницаемости его стенки и проникновения крови в паренхиму мозга.
Кровоизлияние в головной мозг, или геморрагический инсульт, – клиническая форма, возникающая из за разрыва интрацеребрального сосуда или повышенной проницаемости его стенки и проникновения крови в паренхиму мозга.
 Среди причинных факторов ВМК выделяются 3 основные группы: 1. гипертоническая ангиопатия перфорирующих артерий 2. Артериальные аневризмы, артериовенозные мальформации; кавернозные ангиомы 3. Амилоидная ангиопатия. Ведущим фактором (до 90% всех ВМК) является гипертоническая ангиопатия.
Среди причинных факторов ВМК выделяются 3 основные группы: 1. гипертоническая ангиопатия перфорирующих артерий 2. Артериальные аневризмы, артериовенозные мальформации; кавернозные ангиомы 3. Амилоидная ангиопатия. Ведущим фактором (до 90% всех ВМК) является гипертоническая ангиопатия.
 Для гипертензивных ВК характерна типичная локализация. Наиболее часто наблюдаются гипертензивные ВК в подкорковые узлы (у 25 30% пациентов) и зрительный бугор (10 20%). Такое расположение внутримозговых гематом связано с особенностями кровоснабжения полосатого тела и зрительного бугра: перфорирующие артерии отходят от средней мозговой артерии (СМА) под прямым углом, количество сосудистых анастомозов между артериями крайне малое, поэтому при сосудистых церебральных кризах не обеспечивается достаточная амортизация, что приводит к разрыву одной из ветвей.
Для гипертензивных ВК характерна типичная локализация. Наиболее часто наблюдаются гипертензивные ВК в подкорковые узлы (у 25 30% пациентов) и зрительный бугор (10 20%). Такое расположение внутримозговых гематом связано с особенностями кровоснабжения полосатого тела и зрительного бугра: перфорирующие артерии отходят от средней мозговой артерии (СМА) под прямым углом, количество сосудистых анастомозов между артериями крайне малое, поэтому при сосудистых церебральных кризах не обеспечивается достаточная амортизация, что приводит к разрыву одной из ветвей.
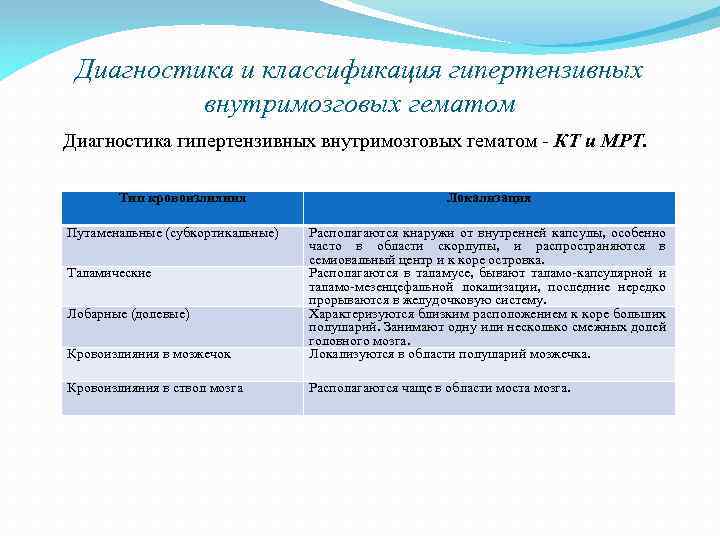 Диагностика и классификация гипертензивных внутримозговых гематом Диагностика гипертензивных внутримозговых гематом КТ и МРТ. Тип кровоизлияния Путаменальные (субкортикальные) Локализация Кровоизлияния в мозжечок Располагаются кнаружи от внутренней капсулы, особенно часто в области скорлупы, и распространяются в семиовальный центр и к коре островка. Располагаются в таламусе, бывают таламо капсулярной и таламо мезенцефальной локализации, последние нередко прорываются в желудочковую систему. Характеризуются близким расположением к коре больших полушарий. Занимают одну или несколько смежных долей головного мозга. Локализуются в области полушарий мозжечка. Кровоизлияния в ствол мозга Располагаются чаще в области моста мозга. Таламические Лобарные (долевые)
Диагностика и классификация гипертензивных внутримозговых гематом Диагностика гипертензивных внутримозговых гематом КТ и МРТ. Тип кровоизлияния Путаменальные (субкортикальные) Локализация Кровоизлияния в мозжечок Располагаются кнаружи от внутренней капсулы, особенно часто в области скорлупы, и распространяются в семиовальный центр и к коре островка. Располагаются в таламусе, бывают таламо капсулярной и таламо мезенцефальной локализации, последние нередко прорываются в желудочковую систему. Характеризуются близким расположением к коре больших полушарий. Занимают одну или несколько смежных долей головного мозга. Локализуются в области полушарий мозжечка. Кровоизлияния в ствол мозга Располагаются чаще в области моста мозга. Таламические Лобарные (долевые)
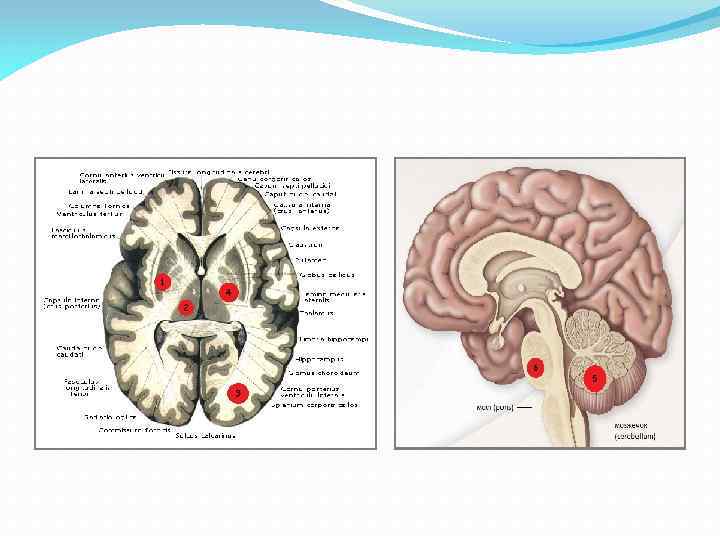
 По данным Сарибекяна А. С. и соавт. (2003 г. ) выделяют 11 типов гипертензивных гематом: Лобарный (субкортикаьный) Путаменально паллидарный Путаменально капсулярно таламический Таламо капсулярный Таламический Таламо стволовой Таламо капсулярно стволовой Мозжечковый Изолированно стволовой
По данным Сарибекяна А. С. и соавт. (2003 г. ) выделяют 11 типов гипертензивных гематом: Лобарный (субкортикаьный) Путаменально паллидарный Путаменально капсулярно таламический Таламо капсулярный Таламический Таламо стволовой Таламо капсулярно стволовой Мозжечковый Изолированно стволовой
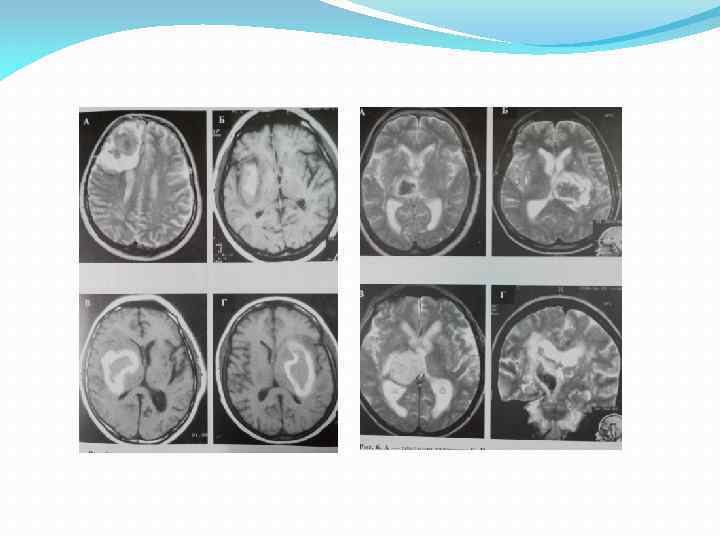
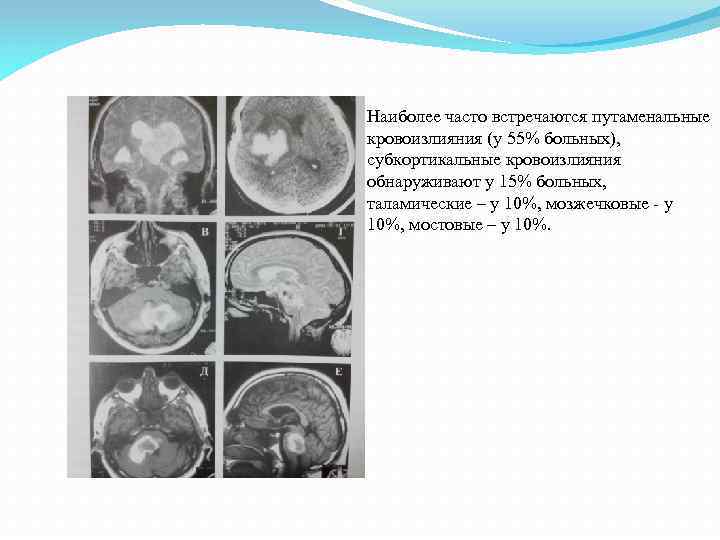 Наиболее часто встречаются путаменальные кровоизлияния (у 55% больных), субкортикальные кровоизлияния обнаруживают у 15% больных, таламические – у 10%, мозжечковые у 10%, мостовые – у 10%.
Наиболее часто встречаются путаменальные кровоизлияния (у 55% больных), субкортикальные кровоизлияния обнаруживают у 15% больных, таламические – у 10%, мозжечковые у 10%, мостовые – у 10%.
 Формула для расчета объема гематомы: V = Ах. Вх. Схπ/6 где А, В, С – это длина, ширина и высота гематомы, π – 3. 14 (Hatori и соавт. , 2004). Приемлемо применение упрощенного варианта (Kothari R и соавт. , 1996): V = Ах. Вх. Сх/2
Формула для расчета объема гематомы: V = Ах. Вх. Схπ/6 где А, В, С – это длина, ширина и высота гематомы, π – 3. 14 (Hatori и соавт. , 2004). Приемлемо применение упрощенного варианта (Kothari R и соавт. , 1996): V = Ах. Вх. Сх/2
 Хирургическое лечение внутримозговых гематом гипертензивного генеза Хирургическое лечение больных ГИ – проблема, в решении которой участвуют нейрохирурги, неврологи, реаниматологи, врачи неотложной помощи, эксперты лучевой диагностики и организаторы здравоохранения. Невзирая на отсутствие доказанного преимущества хирургического лечения ГИ перед консервативным, количество больных, оперированных насчет данного заболевания, неуклонно растет. Это обусловлено высокими показателями летальности и инвалидизации проведении только консервативной терапии. Вмешательство будет оправданным, если оно приведет к понижению летальности и улучшит функциональные исходы в сравнении с таковыми при консервативной терапии.
Хирургическое лечение внутримозговых гематом гипертензивного генеза Хирургическое лечение больных ГИ – проблема, в решении которой участвуют нейрохирурги, неврологи, реаниматологи, врачи неотложной помощи, эксперты лучевой диагностики и организаторы здравоохранения. Невзирая на отсутствие доказанного преимущества хирургического лечения ГИ перед консервативным, количество больных, оперированных насчет данного заболевания, неуклонно растет. Это обусловлено высокими показателями летальности и инвалидизации проведении только консервативной терапии. Вмешательство будет оправданным, если оно приведет к понижению летальности и улучшит функциональные исходы в сравнении с таковыми при консервативной терапии.
 Основная цель хирургического лечения больных ГИ заключается в максимально полном удалении сгустков крови при минимальном повреждении окружающей паренхимы мозга с целью уменьшения масс эффекта, снижения локального и общего ВЧД, уменьшения высвобождения из гематомы нейротоксических веществ. Имеются четкие патогенетические предпосылки к раннему хирургическому лечению больных геморрагическим инсультом. Это подтверждается многочисленными исследованиями, показавшими, что чем раньше выполнена операция, тем лучше результат. Тем не менее имеются сообщения о положительном эффекте операций, проведенных даже на 3 4 неделе после кровоизлияния.
Основная цель хирургического лечения больных ГИ заключается в максимально полном удалении сгустков крови при минимальном повреждении окружающей паренхимы мозга с целью уменьшения масс эффекта, снижения локального и общего ВЧД, уменьшения высвобождения из гематомы нейротоксических веществ. Имеются четкие патогенетические предпосылки к раннему хирургическому лечению больных геморрагическим инсультом. Это подтверждается многочисленными исследованиями, показавшими, что чем раньше выполнена операция, тем лучше результат. Тем не менее имеются сообщения о положительном эффекте операций, проведенных даже на 3 4 неделе после кровоизлияния.
 Хирургическое лечение обычно проводят при: субкортикальной и путаменальной гематоме объемом более 20 см 3, сопровождающейся неврологическим дефицитом; кровоизлиянии в мозжечок объемом более 15 см 3, компрессии IV желудочка и/или острой окклюзионной гидроцефалии. Обсуждается целесообразность хирургического вмешательства при: гематоме таламуса объемом более 10 см 3, сопровождающейся неврологическим дефицитом; при гематомах ствола, сопровождающихся грубым неврологическим дефицитом.
Хирургическое лечение обычно проводят при: субкортикальной и путаменальной гематоме объемом более 20 см 3, сопровождающейся неврологическим дефицитом; кровоизлиянии в мозжечок объемом более 15 см 3, компрессии IV желудочка и/или острой окклюзионной гидроцефалии. Обсуждается целесообразность хирургического вмешательства при: гематоме таламуса объемом более 10 см 3, сопровождающейся неврологическим дефицитом; при гематомах ствола, сопровождающихся грубым неврологическим дефицитом.
 Операции по поводу ГИ можно разделить на 2 группы: жизнеспасающие и функциональные. В первом случае вмешательство направлено на устранение поражений жизненно важных структур мозга (ствол), во втором на восстановление функции важных проводящих путей, например, внутренней капсулы. Граница между ними весьма приблизительная. Поэтому многие функциональные операции при ВМГ в конечном счете можно рассматривать как жизнеспасающие.
Операции по поводу ГИ можно разделить на 2 группы: жизнеспасающие и функциональные. В первом случае вмешательство направлено на устранение поражений жизненно важных структур мозга (ствол), во втором на восстановление функции важных проводящих путей, например, внутренней капсулы. Граница между ними весьма приблизительная. Поэтому многие функциональные операции при ВМГ в конечном счете можно рассматривать как жизнеспасающие.
 Критерии отбора больных на операцию по жизненным показаниям. Формальные критерии: Возраст – до 78 лет. Тяжесть состояния – кроме комы II III. Локализация – любая, кроме обширного поражения среднего мозга. Объем гематомы: Ø более 50 см 3 (лобарные и латеральные) Ø более 40 см 3 (смешанные) Ø более 20 см 3 (медиальные) Ø более 16 см 3 (мозжечковые). Время от начала инсульта – без ограничений. Сопутствующие заболевания – без ограничений. Неформальные критерии: Неблагоприятный прогноз исхода хирургического лечения. Предполагаемая большая трудоемкость и значительные некомпенсируемые трудозатраты на хирургическое лечение (нерентабельность).
Критерии отбора больных на операцию по жизненным показаниям. Формальные критерии: Возраст – до 78 лет. Тяжесть состояния – кроме комы II III. Локализация – любая, кроме обширного поражения среднего мозга. Объем гематомы: Ø более 50 см 3 (лобарные и латеральные) Ø более 40 см 3 (смешанные) Ø более 20 см 3 (медиальные) Ø более 16 см 3 (мозжечковые). Время от начала инсульта – без ограничений. Сопутствующие заболевания – без ограничений. Неформальные критерии: Неблагоприятный прогноз исхода хирургического лечения. Предполагаемая большая трудоемкость и значительные некомпенсируемые трудозатраты на хирургическое лечение (нерентабельность).
 Критерии отбора больных на операцию по функциональным показаниям Формальные критерии: Возраст – до 78 лет. Тяжесть состояния – сознание ясное/легкое оглушение. Локализация – все типы. Объем гематомы – от 15 до 50 см 3 в зависимости от локализации. Двигательные нарушения – выраженные без тенденций к регрессу. Время от начала инсульта – без ограничений. Сопутствующие заболевания (противопоказания к операции): 1. Трудно контролируемая артериальная гипертензия 2. Острая сердечная или легочная патология 3. Острая почечная или печеночная недостаточность 4. Высокий риск ТЭЛА 5. Коагулопатии. Неформальные критерии: Предполагаемая большая трудоемкость и значительные некомпенсируемые трудозатраты на хирургическое лечение (нерентабельность).
Критерии отбора больных на операцию по функциональным показаниям Формальные критерии: Возраст – до 78 лет. Тяжесть состояния – сознание ясное/легкое оглушение. Локализация – все типы. Объем гематомы – от 15 до 50 см 3 в зависимости от локализации. Двигательные нарушения – выраженные без тенденций к регрессу. Время от начала инсульта – без ограничений. Сопутствующие заболевания (противопоказания к операции): 1. Трудно контролируемая артериальная гипертензия 2. Острая сердечная или легочная патология 3. Острая почечная или печеночная недостаточность 4. Высокий риск ТЭЛА 5. Коагулопатии. Неформальные критерии: Предполагаемая большая трудоемкость и значительные некомпенсируемые трудозатраты на хирургическое лечение (нерентабельность).
 Современная хирургия ВМГ должна отвечать следующим требованиям: точность, малоинвазивность доступа, максимальная сохранность окружающих нервных структур и тканей, уменьшение длительности операции, наиболее полная эвакуация (высокая радикальность), способствующая регрессу внутричерепного гипертензионного и дислокационного синдромов.
Современная хирургия ВМГ должна отвечать следующим требованиям: точность, малоинвазивность доступа, максимальная сохранность окружающих нервных структур и тканей, уменьшение длительности операции, наиболее полная эвакуация (высокая радикальность), способствующая регрессу внутричерепного гипертензионного и дислокационного синдромов.
 Открытые транскортикальные операции показаны в 3 случаях: при субкортикальных гематомах; при гематомах мозжечка; при путаменальных кровоизлияниях, при которых быстро развивается ухудшение состояния, таким больным требуется немедленная декомпрессия. Остановимся подробнее на малотравматичных методах удаления гематом, к которым относят операции с использованием стереотаксического и эндоскопического инстументария.
Открытые транскортикальные операции показаны в 3 случаях: при субкортикальных гематомах; при гематомах мозжечка; при путаменальных кровоизлияниях, при которых быстро развивается ухудшение состояния, таким больным требуется немедленная декомпрессия. Остановимся подробнее на малотравматичных методах удаления гематом, к которым относят операции с использованием стереотаксического и эндоскопического инстументария.
 Стереотаксическая аспирация. Начало внедрения стереотаксического метода относится к 1889 г. , когда российский профессор анатомии Д. Н. Зернов разработал энцефалометр. В этом устройстве уже содержались элементы современного стереотаксического аппарата — фиксатор головы в определенном положении, неподвижный «экватор» и подвижный «меридиан» с делением на градусы. С помощью энцефалометра определяли координаты некоторых корковых полей и подкорковых образований головного мозга человека. Исследователи предполагали, что энцефалометр и аналогичные устройства могут быть успешно применены при хирургических операциях на головном мозге.
Стереотаксическая аспирация. Начало внедрения стереотаксического метода относится к 1889 г. , когда российский профессор анатомии Д. Н. Зернов разработал энцефалометр. В этом устройстве уже содержались элементы современного стереотаксического аппарата — фиксатор головы в определенном положении, неподвижный «экватор» и подвижный «меридиан» с делением на градусы. С помощью энцефалометра определяли координаты некоторых корковых полей и подкорковых образований головного мозга человека. Исследователи предполагали, что энцефалометр и аналогичные устройства могут быть успешно применены при хирургических операциях на головном мозге.
 Координаты изгиба лентикулостриарной артерии, что являлось точкой цели (ТЦ), определяли по костным ориентирам на краниограммах. На боковой краниограмме, учитывая дивергенцию, ТЦ определяли как пересечение двух линий: первая длиной 16, 1± 2, 5 мм — кверху от заднего края турецкого седла, вторая длиной 28, 9± 3, 4 мм – кзади и вверх от места пересечения базального уровня фронтального синуса и переднего края средней черепной ямки. На другой краниограмме отмечали расстояние 30 мм от средней плоскости. Таким образом получали координаты ТЦ.
Координаты изгиба лентикулостриарной артерии, что являлось точкой цели (ТЦ), определяли по костным ориентирам на краниограммах. На боковой краниограмме, учитывая дивергенцию, ТЦ определяли как пересечение двух линий: первая длиной 16, 1± 2, 5 мм — кверху от заднего края турецкого седла, вторая длиной 28, 9± 3, 4 мм – кзади и вверх от места пересечения базального уровня фронтального синуса и переднего края средней черепной ямки. На другой краниограмме отмечали расстояние 30 мм от средней плоскости. Таким образом получали координаты ТЦ.

 Стереотаксическая эвакуация ВМГ методом их механического разрушения Первая операция стереотаксического удаления ВМГ с использованием КТ диагностики выполнена Е. О. Backlund и Н. von Holst. Для этого авторами создано специальное устройство, которое функционировало по принципу водного винта, предложенному Архимедом. Устройство состоит из канюли длиной 20 см, наружным диаметром 4 мм, а также введенного в нее сверла типа спирали Архимеда. На “мозговом” конце канюли имеются 2 небольших отверстия, на наружном конце — боковой отводящий канал в виде трубки, через которую эвакуируют содержимое НВМГ и поддерживают разрежение. Ротационное движение спирали осуществляет хирург.
Стереотаксическая эвакуация ВМГ методом их механического разрушения Первая операция стереотаксического удаления ВМГ с использованием КТ диагностики выполнена Е. О. Backlund и Н. von Holst. Для этого авторами создано специальное устройство, которое функционировало по принципу водного винта, предложенному Архимедом. Устройство состоит из канюли длиной 20 см, наружным диаметром 4 мм, а также введенного в нее сверла типа спирали Архимеда. На “мозговом” конце канюли имеются 2 небольших отверстия, на наружном конце — боковой отводящий канал в виде трубки, через которую эвакуируют содержимое НВМГ и поддерживают разрежение. Ротационное движение спирали осуществляет хирург.
 Спираль Архимеда это плоская кривая, которую вырисовывает точка, движущаяся с постоянной скоростью от центра окружности по ее радиусу, окружность которого вращается также с постоянной угловой скоростью.
Спираль Архимеда это плоская кривая, которую вырисовывает точка, движущаяся с постоянной скоростью от центра окружности по ее радиусу, окружность которого вращается также с постоянной угловой скоростью.
 Прибор Переседова Канделя
Прибор Переседова Канделя
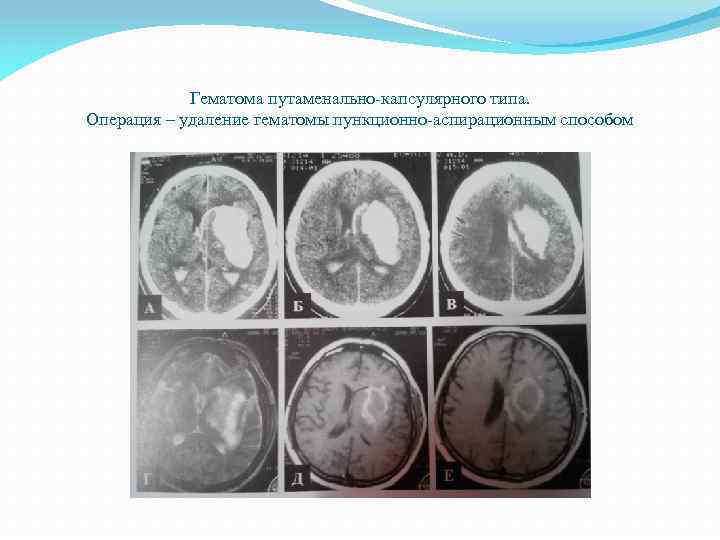 Гематома путаменально капсулярного типа. Операция – удаление гематомы пункционно аспирационным способом
Гематома путаменально капсулярного типа. Операция – удаление гематомы пункционно аспирационным способом
 Стереотаксическая эвакуация ВМГ после тромболитического растворения их содержимого Впервые лизис таламических ВМГ с применением урокиназы в целях полного удаления в подострой и хронической стадиях осуществили Е. Doi и соавторы. Фермент вводили в полость ВМГ через катетер по 6000 ЕД через каждые 4 ч до полного разжижения содержимого и удаления под контролем КТ. Последующий опыт стереотаксического удаления ВМГ по данным КТ показал, что без воздействия фермента эвакуируется лишь жидкая фракция, которая, как правило, не превышает 33% первоначального объема. Операцию выполняли под местным обезболиванием, делали фрезевое отверстие, в центр ВМГ вводили силиконовый катетер с наружным диаметром 3, 5 мм, внутренним — 2, 1 мм. Жидкую часть ВМГ эвакуировали шприцем. Затем в ее полость с помощью катетера вводили 6000 ЕД урокиназы, разведенной в 5 мл изотонического раствора натрия хлорида. Величину остаточной ВМГ контролировали с помощью КТ. Урокиназу повторно вводили через 6– 12 ч, а кратность введения зависела от скорости разжижения содержимого ВМГ до его полного удаления. Продолжительность операции 3– 7 сут.
Стереотаксическая эвакуация ВМГ после тромболитического растворения их содержимого Впервые лизис таламических ВМГ с применением урокиназы в целях полного удаления в подострой и хронической стадиях осуществили Е. Doi и соавторы. Фермент вводили в полость ВМГ через катетер по 6000 ЕД через каждые 4 ч до полного разжижения содержимого и удаления под контролем КТ. Последующий опыт стереотаксического удаления ВМГ по данным КТ показал, что без воздействия фермента эвакуируется лишь жидкая фракция, которая, как правило, не превышает 33% первоначального объема. Операцию выполняли под местным обезболиванием, делали фрезевое отверстие, в центр ВМГ вводили силиконовый катетер с наружным диаметром 3, 5 мм, внутренним — 2, 1 мм. Жидкую часть ВМГ эвакуировали шприцем. Затем в ее полость с помощью катетера вводили 6000 ЕД урокиназы, разведенной в 5 мл изотонического раствора натрия хлорида. Величину остаточной ВМГ контролировали с помощью КТ. Урокиназу повторно вводили через 6– 12 ч, а кратность введения зависела от скорости разжижения содержимого ВМГ до его полного удаления. Продолжительность операции 3– 7 сут.
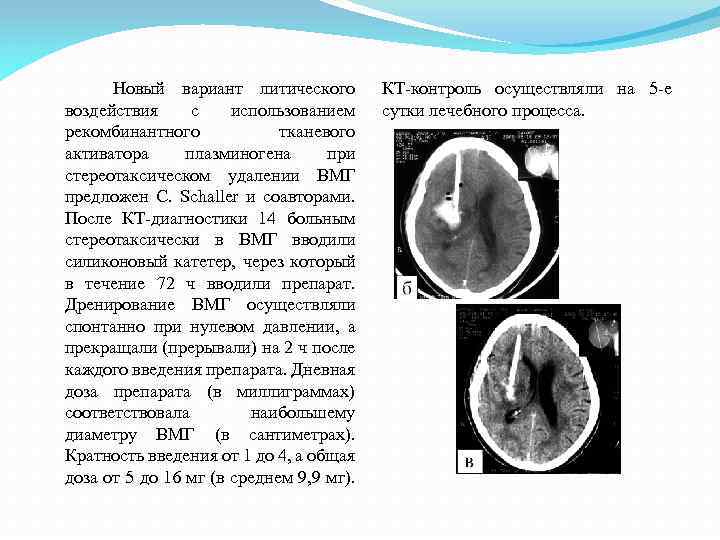 Новый вариант литического КТ контроль осуществляли на 5 е воздействия с использованием сутки лечебного процесса. рекомбинантного тканевого активатора плазминогена при стереотаксическом удалении ВМГ предложен С. Schaller и соавторами. После КТ диагностики 14 больным стереотаксически в ВМГ вводили силиконовый катетер, через который в течение 72 ч вводили препарат. Дренирование ВМГ осуществляли спонтанно при нулевом давлении, а прекращали (прерывали) на 2 ч после каждого введения препарата. Дневная доза препарата (в миллиграммах) соответствовала наибольшему диаметру ВМГ (в сантиметрах). Кратность введения от 1 до 4, а общая доза от 5 до 16 мг (в среднем 9, 9 мг).
Новый вариант литического КТ контроль осуществляли на 5 е воздействия с использованием сутки лечебного процесса. рекомбинантного тканевого активатора плазминогена при стереотаксическом удалении ВМГ предложен С. Schaller и соавторами. После КТ диагностики 14 больным стереотаксически в ВМГ вводили силиконовый катетер, через который в течение 72 ч вводили препарат. Дренирование ВМГ осуществляли спонтанно при нулевом давлении, а прекращали (прерывали) на 2 ч после каждого введения препарата. Дневная доза препарата (в миллиграммах) соответствовала наибольшему диаметру ВМГ (в сантиметрах). Кратность введения от 1 до 4, а общая доза от 5 до 16 мг (в среднем 9, 9 мг).
 В монографии В. В. Крылова и соавторов представлены результаты лечения 73 пациентов по поводу ВМГ с использованием безрамочно КТ нейронавигационного пункционного метода локального фибринолиза. Объем ВМГ от 15 до 61 см³. Один из основных критериев отбора — уровень бодрствования пациента — должен быть не менее 9 баллов по ШКГ. Фибринолиз осуществляли с использованием рекомбинантной проурокиназы. Продолжительность операции в среднем (22± 5) мин. У 91% больных достигнуто радикальное удаление ВМГ. Повторная гематома возникла у 16 ( 22 %) из 73 больных, умерли 17 (23%). Как полезное дополнение авторы разработали методику быстрой санации внутрижелудочковых кровоизлияний, предусматривающую наружное дренирование желудочков мозга и интратекальное введение рекомбинантной проурокиназы. Пункционный метод локального фибринолиза содержимого ВМГ может быть осуществлен и с помощью интраоперационного ультразвукового (УЗ) сканирования
В монографии В. В. Крылова и соавторов представлены результаты лечения 73 пациентов по поводу ВМГ с использованием безрамочно КТ нейронавигационного пункционного метода локального фибринолиза. Объем ВМГ от 15 до 61 см³. Один из основных критериев отбора — уровень бодрствования пациента — должен быть не менее 9 баллов по ШКГ. Фибринолиз осуществляли с использованием рекомбинантной проурокиназы. Продолжительность операции в среднем (22± 5) мин. У 91% больных достигнуто радикальное удаление ВМГ. Повторная гематома возникла у 16 ( 22 %) из 73 больных, умерли 17 (23%). Как полезное дополнение авторы разработали методику быстрой санации внутрижелудочковых кровоизлияний, предусматривающую наружное дренирование желудочков мозга и интратекальное введение рекомбинантной проурокиназы. Пункционный метод локального фибринолиза содержимого ВМГ может быть осуществлен и с помощью интраоперационного ультразвукового (УЗ) сканирования
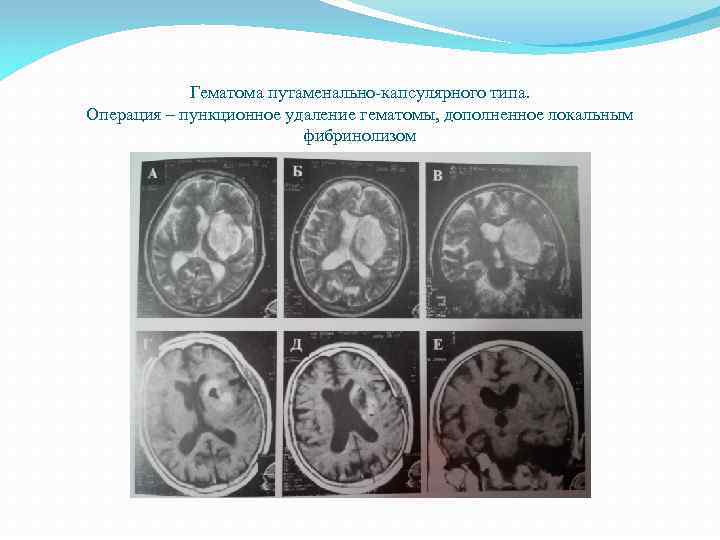 Гематома путаменально капсулярного типа. Операция – пункционное удаление гематомы, дополненное локальным фибринолизом
Гематома путаменально капсулярного типа. Операция – пункционное удаление гематомы, дополненное локальным фибринолизом
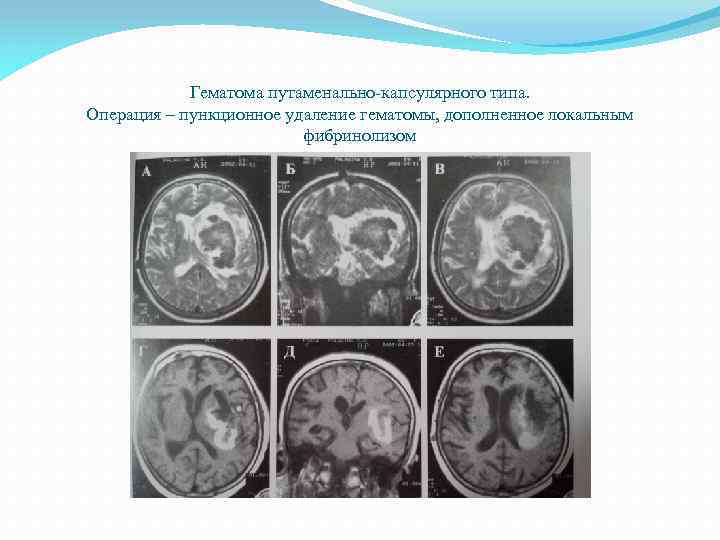 Гематома путаменально капсулярного типа. Операция – пункционное удаление гематомы, дополненное локальным фибринолизом
Гематома путаменально капсулярного типа. Операция – пункционное удаление гематомы, дополненное локальным фибринолизом
 Использование навигационной станции Medtronic Stealth Station Treon Plus
Использование навигационной станции Medtronic Stealth Station Treon Plus
 АКТИЛИЗЕ Тромболитик. Рекомбинантный человеческий тканевой активатор плазминогена, гликопротеин, который непосредственно активизирует превращение плазминогена в плазмин.
АКТИЛИЗЕ Тромболитик. Рекомбинантный человеческий тканевой активатор плазминогена, гликопротеин, который непосредственно активизирует превращение плазминогена в плазмин.
 Недостатки и преимущества использования стереотаксического способа удаления ВМГ Имеется ряд преимуществ метода: возможность выполнения под местной анестезией, минимальная инвазивность (нет необходимости выполнять краниотомию, кортикотомию). Тем не менее, у этого метода также имеется несколько недостатков: необходимость в специальном оборудовании и времени для его установки и расчетов, выполнение пункции вслепую (возможна травматизация нервных структур и сосудов), отсутствие возможности визуализации в полости гематомы (нормальные и патологические сосуды, стенки полости гематомы), невозможность гемостаза (трудность контроля кровотечения), также невозможность взятия биопсии. Кроме того, пункционное лечение эффективно при жидкой ВМГ. Если же ВМГ представлена сгустками, то возникают затруднения в ее полном удалении. В настоящее время отечественные нейрохирурги с этой целью дополнительно используют локальный фибринолиз. В профессиональной печати имеются противоречивые мнения на этот счет. В целом, стереотаксическая хирургия ВМГ имеет большие перспективы и в будущем станет стандартом нейрохирургического лечения ВМГ.
Недостатки и преимущества использования стереотаксического способа удаления ВМГ Имеется ряд преимуществ метода: возможность выполнения под местной анестезией, минимальная инвазивность (нет необходимости выполнять краниотомию, кортикотомию). Тем не менее, у этого метода также имеется несколько недостатков: необходимость в специальном оборудовании и времени для его установки и расчетов, выполнение пункции вслепую (возможна травматизация нервных структур и сосудов), отсутствие возможности визуализации в полости гематомы (нормальные и патологические сосуды, стенки полости гематомы), невозможность гемостаза (трудность контроля кровотечения), также невозможность взятия биопсии. Кроме того, пункционное лечение эффективно при жидкой ВМГ. Если же ВМГ представлена сгустками, то возникают затруднения в ее полном удалении. В настоящее время отечественные нейрохирурги с этой целью дополнительно используют локальный фибринолиз. В профессиональной печати имеются противоречивые мнения на этот счет. В целом, стереотаксическая хирургия ВМГ имеет большие перспективы и в будущем станет стандартом нейрохирургического лечения ВМГ.
 Эндоскопическая эвакуация. Эндоскопия является новой альтернативой лечения гипертензивных внутримозговых кровоизлияний. Все манипуляции выполняют исключительно под эндоскопическим контролем при помощи эндоскопических инструментов, введенных через фрезевое отверстие расположенное вблизи от гематомы. Длительность операции составляет от 65 до 114 мин, в среднем 82 мин. Пункционным путем нейроэндоскоп вводят в полость гематомы непосредственно через ткань мозга. ВМГ удаляют порционными промываниями и при возможности с помощью эндоскопических инструментов. Большие сгустки фрагментируют и также удаляют. Некоторые авторы указывают на отсутствие необходимости удаления сгустков, фиксированных к стенкам полости ВМГ.
Эндоскопическая эвакуация. Эндоскопия является новой альтернативой лечения гипертензивных внутримозговых кровоизлияний. Все манипуляции выполняют исключительно под эндоскопическим контролем при помощи эндоскопических инструментов, введенных через фрезевое отверстие расположенное вблизи от гематомы. Длительность операции составляет от 65 до 114 мин, в среднем 82 мин. Пункционным путем нейроэндоскоп вводят в полость гематомы непосредственно через ткань мозга. ВМГ удаляют порционными промываниями и при возможности с помощью эндоскопических инструментов. Большие сгустки фрагментируют и также удаляют. Некоторые авторы указывают на отсутствие необходимости удаления сгустков, фиксированных к стенкам полости ВМГ.
 Детали хирургической техники Пациент находится на спине, операцию выполняют под общей анестезией (эндотрахеальный наркоз). В зависимости от локализации ВМГ выполняют поперечный линейный разрез кожи и апо невроза , 5 1 — 3 см. Надкостницу рассекают дугообразно основанием противоположно разрезу кожи. Разрез кожи и надкостницы при эндоскопическом удалении ВМГ с прорывом в желудочки мозга лучше проводить в разных проекциях с целью профилактики ликвореи в послеоперационном периоде. При этом важными считаются следующие детали выбора эндоскопического доступа: минимизация траектории транскортикального доступа до центра ВМГ, возможное ограничение прохождения этой траектории через функционально значимые мозговые структуры (внутренняя капсула, предцентральная извилина, проекция сильвиевой щели) и при необходимости возможность перехода к открытой краниотомии (микрохирургическая операция в случае трудности контроля гемостаза). После этого крестообразно вскрывают твердую мозговую оболочку и с предварительной коагуляцией пиальных сосудов производят энцефалотомию длиной око ло мм. Трубку направитель вместе с обтуратором вводят в мозг 5 на глубину залегания ВМГ (расчет по КТ или нейронавигационно).
Детали хирургической техники Пациент находится на спине, операцию выполняют под общей анестезией (эндотрахеальный наркоз). В зависимости от локализации ВМГ выполняют поперечный линейный разрез кожи и апо невроза , 5 1 — 3 см. Надкостницу рассекают дугообразно основанием противоположно разрезу кожи. Разрез кожи и надкостницы при эндоскопическом удалении ВМГ с прорывом в желудочки мозга лучше проводить в разных проекциях с целью профилактики ликвореи в послеоперационном периоде. При этом важными считаются следующие детали выбора эндоскопического доступа: минимизация траектории транскортикального доступа до центра ВМГ, возможное ограничение прохождения этой траектории через функционально значимые мозговые структуры (внутренняя капсула, предцентральная извилина, проекция сильвиевой щели) и при необходимости возможность перехода к открытой краниотомии (микрохирургическая операция в случае трудности контроля гемостаза). После этого крестообразно вскрывают твердую мозговую оболочку и с предварительной коагуляцией пиальных сосудов производят энцефалотомию длиной око ло мм. Трубку направитель вместе с обтуратором вводят в мозг 5 на глубину залегания ВМГ (расчет по КТ или нейронавигационно).
 Обычно используют ригидные эндоскопы с тремя различными углами обзора в 0, 30, 70°, светопроницаемые трубки направители диаметром 6 мм и длиной 10 см, угловые канюли для аспирации диаметром 3 мм, оснащенные монополярной коагуляцией. В некоторых исследованиях описано использование гибкого эндоскопа.
Обычно используют ригидные эндоскопы с тремя различными углами обзора в 0, 30, 70°, светопроницаемые трубки направители диаметром 6 мм и длиной 10 см, угловые канюли для аспирации диаметром 3 мм, оснащенные монополярной коагуляцией. В некоторых исследованиях описано использование гибкого эндоскопа.
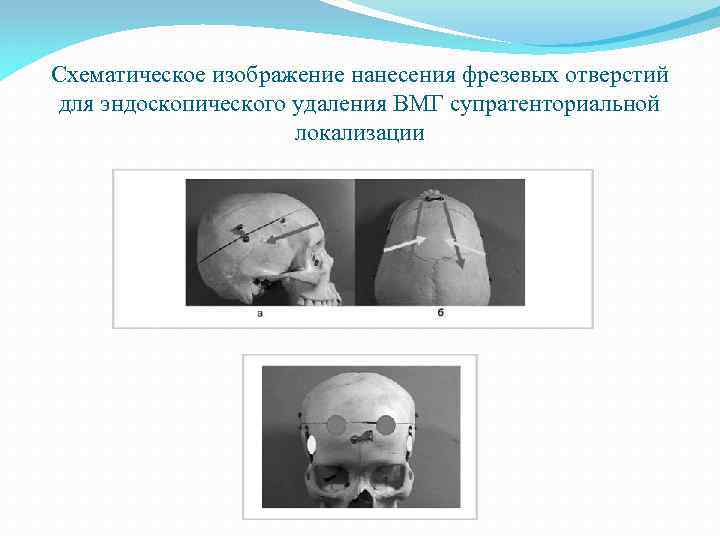 Схематическое изображение нанесения фрезевых отверстий для эндоскопического удаления ВМГ супратенториальной локализации
Схематическое изображение нанесения фрезевых отверстий для эндоскопического удаления ВМГ супратенториальной локализации
 Преимущества прямого ригидного эндоскопа по сравнению с управляемым гибким: — более качественное изображение (отличная резкость, отсутствие зернистости); — конструкция, допускающая получение 10 кратного увеличения, которое является достаточным для детального осмотра полости ВМГ, идентификации основных анатомических ориенти ров, визуализации содержимого опухоли с кровоиз лиянием; — обеспечение боковой визуализации струк тур, находящихся за пределами прямой видимости в условиях узкого и глубокого операционного канала за счет угла обзора 30°; — небольшой внешний диаметр, что позволяет одновременно с эндоскопом манипулировать раз личным микроинструментарием в случаях перехода на эндоскопическую поддержку; — возможность жесткой фиксации эндоскопа с помощью специально разработанного держателя.
Преимущества прямого ригидного эндоскопа по сравнению с управляемым гибким: — более качественное изображение (отличная резкость, отсутствие зернистости); — конструкция, допускающая получение 10 кратного увеличения, которое является достаточным для детального осмотра полости ВМГ, идентификации основных анатомических ориенти ров, визуализации содержимого опухоли с кровоиз лиянием; — обеспечение боковой визуализации струк тур, находящихся за пределами прямой видимости в условиях узкого и глубокого операционного канала за счет угла обзора 30°; — небольшой внешний диаметр, что позволяет одновременно с эндоскопом манипулировать раз личным микроинструментарием в случаях перехода на эндоскопическую поддержку; — возможность жесткой фиксации эндоскопа с помощью специально разработанного держателя.
 Недостатки применения гибкого управляемого эндоскопа — более низкое, чем при использовании жесткого эндоскопа, качество изображения, недостаточное для уверенной ориентации в полости ВМГ в связи с большой зернистостью и меньшей степенью увеличения; — довольно большой диаметр трубки, допускающий введение эндоскопа в сфеноидальный синус, но затрудняющий соосное манипулирование другим инструментарием; — опасность повреждения металлическими ин струментами гибкого дистального сегмента эндоскопа в случаях с эндоскопической поддержкой; — отсутствие возможности жесткой фиксации эндоскопа в полости ВМГ в оптимальной позиции.
Недостатки применения гибкого управляемого эндоскопа — более низкое, чем при использовании жесткого эндоскопа, качество изображения, недостаточное для уверенной ориентации в полости ВМГ в связи с большой зернистостью и меньшей степенью увеличения; — довольно большой диаметр трубки, допускающий введение эндоскопа в сфеноидальный синус, но затрудняющий соосное манипулирование другим инструментарием; — опасность повреждения металлическими ин струментами гибкого дистального сегмента эндоскопа в случаях с эндоскопической поддержкой; — отсутствие возможности жесткой фиксации эндоскопа в полости ВМГ в оптимальной позиции.
 Недостатки и преимущества использования эндоскопического способа удаления ВМГ К недостаткам эндоскопического удаления ВМГ можно отнести следующие: необходимость специ ального эндоскопического оборудования (камера, эндоскопы, мониторы, эндоскопическое оборудование и т. д. ), специального тренинга для нейрохирурга, невозможность в некоторых случаях полного гемостаза в полости ВМГ, ограничение использова ния качестве монометода в при ВМГ, образованных разорвавшимися аневризмами и АВМ. Эндоскопическая аспирация гематом по сравнению с открытыми способами имеет ряд преимуществ: позволяет снизить травматичность и длительность операции, добиться лучшего контроля и радикальности удаления при большом объеме ВМГ, а также получить прицельную биопсию сомнительных участков паренхимы мозга (случаи кровоизлияния в опухоль). Минимальная инвазивность достигается умень шением лощади краниотомии п в несколько раз (диаметр отверстия 2 см в отличие от 5— 8 см при открытой краниотомии), твердая мозговая оболочка вскрывается на меньшем протяжении, ткань мозга, сосуды и черепные нервы подвергаются меньшей тракции. Используя современные системы навигации, можно рассчитать еще более точную траекторию эндоскопического вмешательства. Уменьшение времени операции, глубины наркоза, кровопотери и последующих костно пластических вмешательств на черепе являются важными преимуществами эн доскопического етода лечения ВМГ, особенно у детей и лиц старческого м возраста, а также при исходно тяжелом состоянии пациента.
Недостатки и преимущества использования эндоскопического способа удаления ВМГ К недостаткам эндоскопического удаления ВМГ можно отнести следующие: необходимость специ ального эндоскопического оборудования (камера, эндоскопы, мониторы, эндоскопическое оборудование и т. д. ), специального тренинга для нейрохирурга, невозможность в некоторых случаях полного гемостаза в полости ВМГ, ограничение использова ния качестве монометода в при ВМГ, образованных разорвавшимися аневризмами и АВМ. Эндоскопическая аспирация гематом по сравнению с открытыми способами имеет ряд преимуществ: позволяет снизить травматичность и длительность операции, добиться лучшего контроля и радикальности удаления при большом объеме ВМГ, а также получить прицельную биопсию сомнительных участков паренхимы мозга (случаи кровоизлияния в опухоль). Минимальная инвазивность достигается умень шением лощади краниотомии п в несколько раз (диаметр отверстия 2 см в отличие от 5— 8 см при открытой краниотомии), твердая мозговая оболочка вскрывается на меньшем протяжении, ткань мозга, сосуды и черепные нервы подвергаются меньшей тракции. Используя современные системы навигации, можно рассчитать еще более точную траекторию эндоскопического вмешательства. Уменьшение времени операции, глубины наркоза, кровопотери и последующих костно пластических вмешательств на черепе являются важными преимуществами эн доскопического етода лечения ВМГ, особенно у детей и лиц старческого м возраста, а также при исходно тяжелом состоянии пациента.
 NB! Являясь минимально травматической операцией, эндоскопическое удаление внутримозговой гематомы не всегда позволяет решить вопрос полного гемостаза. Начиная операцию по эндоскопическому удалению внутримозговой гематомы, нейрохирург должен рассматривать возможность перевода ее в микрохирургическое удаление внутримозговой гематомы с эндоскопической поддержкой.
NB! Являясь минимально травматической операцией, эндоскопическое удаление внутримозговой гематомы не всегда позволяет решить вопрос полного гемостаза. Начиная операцию по эндоскопическому удалению внутримозговой гематомы, нейрохирург должен рассматривать возможность перевода ее в микрохирургическое удаление внутримозговой гематомы с эндоскопической поддержкой.
 Проведено сравнение двух методов лечения ВМГ: эндоскопического удаления и стереотаксической аспирации. По основным показателям (продолжительность операции — 72/100 мин, степень удаления кровоизлияния 95/75%, длительность нахождения в палате интенсивной терапии — 4, 2/6, 9 суток; шкала функционального исхода Глазго) пред почтение отдано эндоскопическому удалению ВМГ. По данным рандомизированного исследования при сравнении стереотаксически–эндоскопического метода удаления и медикаментозного лечения ВМГ установлено, что эндоскопический метод характеризуется минимальной травматичностью и другими преимуществами: летальность — соответственно 20 и 50%, степень удаления кровоизлияния — 80%, более высокая степень функционального исхода и др. В другом рандомизированном исследовании сравнивали три способа удаления ВМГ у пациентов без коматозного состояния: эндоскопическая техника, стереотаксическая аспирация и краниотомия с эвакуацией кровоизлияния. Оценивали основные показатели (послеоперационная летальность — соответственно 0, 6, 7 и 13, 3%, степень удаления свертков крови, потеря крови во время операции, функциональный исход по различным шкалам и др. ). Оптимальные достижения отмечены применении эндоскопической техники.
Проведено сравнение двух методов лечения ВМГ: эндоскопического удаления и стереотаксической аспирации. По основным показателям (продолжительность операции — 72/100 мин, степень удаления кровоизлияния 95/75%, длительность нахождения в палате интенсивной терапии — 4, 2/6, 9 суток; шкала функционального исхода Глазго) пред почтение отдано эндоскопическому удалению ВМГ. По данным рандомизированного исследования при сравнении стереотаксически–эндоскопического метода удаления и медикаментозного лечения ВМГ установлено, что эндоскопический метод характеризуется минимальной травматичностью и другими преимуществами: летальность — соответственно 20 и 50%, степень удаления кровоизлияния — 80%, более высокая степень функционального исхода и др. В другом рандомизированном исследовании сравнивали три способа удаления ВМГ у пациентов без коматозного состояния: эндоскопическая техника, стереотаксическая аспирация и краниотомия с эвакуацией кровоизлияния. Оценивали основные показатели (послеоперационная летальность — соответственно 0, 6, 7 и 13, 3%, степень удаления свертков крови, потеря крови во время операции, функциональный исход по различным шкалам и др. ). Оптимальные достижения отмечены применении эндоскопической техники.


