 Минералы 2
Минералы 2
 • К настоящему времени около 4000 минералов признаны самостоятельными минеральными видами. • • В результате в современной систематике минералы объединяются в классы по признаку общего аниона или анионной группы. • Исключение составляют самородные элементы, которые встречаются в природе сами по себе, не образуя соединений.
• К настоящему времени около 4000 минералов признаны самостоятельными минеральными видами. • • В результате в современной систематике минералы объединяются в классы по признаку общего аниона или анионной группы. • Исключение составляют самородные элементы, которые встречаются в природе сами по себе, не образуя соединений.
 КЛАССИФИКАЦИЯ МИНЕРАЛОВ Класс Минерал (пример) Самородные элементы Золото Химическая формула Au Карбиды Муассанит Si. C Сульфиды и сульфосоли Киноварь Энаргит Hg. S Cu 3 As. S 4 Оксиды Гематит Fe 2 O 3 Гидроксиды Брусит Mg(OH)2 Галогениды Флюорит Ca. F 2 Карбонаты Кальцит Ca. CO 3 Нитраты Калиевая селитра KNO 3 Бораты Бура Na 2 B 4 O 5(OH)4× 8 H 2 O Фосфаты Апатит Ca 5(PO 4)3 F Сульфаты Гипс Ca. SO 4× 2 H 2 O Хроматы Крокоит Pb. Cr. O 4 Вольфраматы Шеелит Ca. WO 4 Силикаты Альбит Na. Al. Si 3 O 8
КЛАССИФИКАЦИЯ МИНЕРАЛОВ Класс Минерал (пример) Самородные элементы Золото Химическая формула Au Карбиды Муассанит Si. C Сульфиды и сульфосоли Киноварь Энаргит Hg. S Cu 3 As. S 4 Оксиды Гематит Fe 2 O 3 Гидроксиды Брусит Mg(OH)2 Галогениды Флюорит Ca. F 2 Карбонаты Кальцит Ca. CO 3 Нитраты Калиевая селитра KNO 3 Бораты Бура Na 2 B 4 O 5(OH)4× 8 H 2 O Фосфаты Апатит Ca 5(PO 4)3 F Сульфаты Гипс Ca. SO 4× 2 H 2 O Хроматы Крокоит Pb. Cr. O 4 Вольфраматы Шеелит Ca. WO 4 Силикаты Альбит Na. Al. Si 3 O 8
 • Классы самородных элементов и сульфидов. • не относятся к породообразующим, но многие из них являются ценными полезными ископаемыми. • Из наиболее распространенных минералов можно назвать серу S, возникающую в процессе возгонки паров при вулканических извержениях, а также в поверхностных условиях при химических изменениях минералов классов сульфидов и сульфатов и биогенным путем. Используется в химической промышленности для получения серной кислоты, в сельском хозяйстве и в ряде других отраслей. • Графит С связан преимущественно с процессами метаморфизма. Широко применяется в металлургии, для производства электродов и др. • К этому же классу относятся такие ценные минералы, как алмаз, золото, платина и др.
• Классы самородных элементов и сульфидов. • не относятся к породообразующим, но многие из них являются ценными полезными ископаемыми. • Из наиболее распространенных минералов можно назвать серу S, возникающую в процессе возгонки паров при вулканических извержениях, а также в поверхностных условиях при химических изменениях минералов классов сульфидов и сульфатов и биогенным путем. Используется в химической промышленности для получения серной кислоты, в сельском хозяйстве и в ряде других отраслей. • Графит С связан преимущественно с процессами метаморфизма. Широко применяется в металлургии, для производства электродов и др. • К этому же классу относятся такие ценные минералы, как алмаз, золото, платина и др.
 • К классу сульфидов принадлежат многочисленные рудные минералы. • Галенит, или свинцовый блеск Pb. S, - основная руда свинца. • Сфалерит, или цинковая обманка Zn. S, - основная руда цинка • Одним из наиболее распространенных минералов класса сульфидов является пирит Fe. S 2. Используется для изготовления серной кислоты. • Халькопирит Cu. Fe. S 2 – главная руда меди • • Происхождение сульфидов связано главным образом с горячими водными растворами (гидротермальными). Они часто встречаются в кварцевых жилах вместе со многими минералами класса самородных элементов
• К классу сульфидов принадлежат многочисленные рудные минералы. • Галенит, или свинцовый блеск Pb. S, - основная руда свинца. • Сфалерит, или цинковая обманка Zn. S, - основная руда цинка • Одним из наиболее распространенных минералов класса сульфидов является пирит Fe. S 2. Используется для изготовления серной кислоты. • Халькопирит Cu. Fe. S 2 – главная руда меди • • Происхождение сульфидов связано главным образом с горячими водными растворами (гидротермальными). Они часто встречаются в кварцевых жилах вместе со многими минералами класса самородных элементов
 • Класс галоидных соединений. • соли фтористо-, бромисто-, хлористо-, йодистоводородных кислот. Наиболее распространенными являются хлориды, образующиеся главным образом при испарении вод поверхностных бассейнов. • Галит Na. CI. Используется в пищевой промышленности, в химической для получения хлора, натрия и их производных. • Сильвин КСl - близок по происхождению и по физическим свойствам к галиту, с которым часто образует единые агрегаты. Применяется в основном как сырье для калийных удобрений, в химической промышленности. • Фториды связаны преимущественно с гидротермальными, а также с магматическими и пневматолитовыми процессами. В экзогенных условиях образуются редко. К ним относится флюорит - Ca. F 2. Используется в металлургической, химической, керамической промышленности, прозрачные разновидности – в оптике.
• Класс галоидных соединений. • соли фтористо-, бромисто-, хлористо-, йодистоводородных кислот. Наиболее распространенными являются хлориды, образующиеся главным образом при испарении вод поверхностных бассейнов. • Галит Na. CI. Используется в пищевой промышленности, в химической для получения хлора, натрия и их производных. • Сильвин КСl - близок по происхождению и по физическим свойствам к галиту, с которым часто образует единые агрегаты. Применяется в основном как сырье для калийных удобрений, в химической промышленности. • Фториды связаны преимущественно с гидротермальными, а также с магматическими и пневматолитовыми процессами. В экзогенных условиях образуются редко. К ним относится флюорит - Ca. F 2. Используется в металлургической, химической, керамической промышленности, прозрачные разновидности – в оптике.
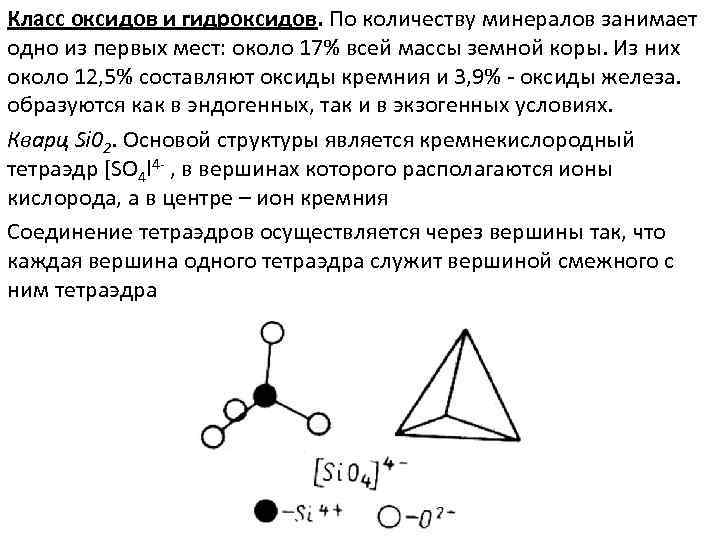 Класс оксидов и гидроксидов. По количеству минералов занимает одно из первых мест: около 17% всей массы земной коры. Из них около 12, 5% составляют оксиды кремния и 3, 9% - оксиды железа. образуются как в эндогенных, так и в экзогенных условиях. Кварц Si 02. Основой структуры является кремнекислородный тетраэдр [SO 4 l 4 - , в вершинах которого располагаются ионы кислорода, а в центре – ион кремния Соединение тетраэдров осуществляется через вершины так, что каждая вершина одного тетраэдра служит вершиной смежного с ним тетраэдра
Класс оксидов и гидроксидов. По количеству минералов занимает одно из первых мест: около 17% всей массы земной коры. Из них около 12, 5% составляют оксиды кремния и 3, 9% - оксиды железа. образуются как в эндогенных, так и в экзогенных условиях. Кварц Si 02. Основой структуры является кремнекислородный тетраэдр [SO 4 l 4 - , в вершинах которого располагаются ионы кислорода, а в центре – ион кремния Соединение тетраэдров осуществляется через вершины так, что каждая вершина одного тетраэдра служит вершиной смежного с ним тетраэдра
 • Кварц встречается в виде зернистых агрегатов, плотных масс, зерен в породах, в пустотах образует кристаллы и их сростки. Сингония гексагональная (подсингония тригональная). Цвет разнообразный - бесцветный, белый, серый, встречаются окрашенные разности. Окраска лежит в основе выделения разновидностей кварца: горный хрусталь - бесцветные прозрачные кристаллы; дымчатый кварц - серо-дымчатые, бурые; аметист - фиолетовые кристаллы; морион - черные и др. • Кварц выделяется при кристаллизации магмы, выпадает из горячих растворов и паров, возникает в процессе метаморфизма. В экзогенных условиях образуется редко. Химически устойчив в любых условиях.
• Кварц встречается в виде зернистых агрегатов, плотных масс, зерен в породах, в пустотах образует кристаллы и их сростки. Сингония гексагональная (подсингония тригональная). Цвет разнообразный - бесцветный, белый, серый, встречаются окрашенные разности. Окраска лежит в основе выделения разновидностей кварца: горный хрусталь - бесцветные прозрачные кристаллы; дымчатый кварц - серо-дымчатые, бурые; аметист - фиолетовые кристаллы; морион - черные и др. • Кварц выделяется при кристаллизации магмы, выпадает из горячих растворов и паров, возникает в процессе метаморфизма. В экзогенных условиях образуется редко. Химически устойчив в любых условиях.
 • Халцедон Si. O 2 – скрытокристаллический минерал, образующий плотные, часто натечные массы. • красного или оранжевого цвета – сердолик, с окраской, располагающейся полосами, – агат и др. Связан с гидротермальными процессами, сопровождающими вулканическую деятельность, возникает в экзогенных условиях. Кварц и халцедон используются в стекольной, химической промышленностях, в строительстве, горный хрусталь (пьезокварц) – в оптике и радиотехнике. Красиво окрашенные разновидности применяются в ювелирном деле. • Опал Si. O 2. n. H 2 O – аморфный минерал. Образует плотные, часто натечные массы, слагает некоторые осадочные породы органогенного происхождения. Образуется при выветривании силикатов, в результате жизнедеятельности некоторых организмов; выпадает и из горячих растворов, образуя гейзериты. Используется в ювелирном деле как поделочный камень, в строительстве как абразивный материал.
• Халцедон Si. O 2 – скрытокристаллический минерал, образующий плотные, часто натечные массы. • красного или оранжевого цвета – сердолик, с окраской, располагающейся полосами, – агат и др. Связан с гидротермальными процессами, сопровождающими вулканическую деятельность, возникает в экзогенных условиях. Кварц и халцедон используются в стекольной, химической промышленностях, в строительстве, горный хрусталь (пьезокварц) – в оптике и радиотехнике. Красиво окрашенные разновидности применяются в ювелирном деле. • Опал Si. O 2. n. H 2 O – аморфный минерал. Образует плотные, часто натечные массы, слагает некоторые осадочные породы органогенного происхождения. Образуется при выветривании силикатов, в результате жизнедеятельности некоторых организмов; выпадает и из горячих растворов, образуя гейзериты. Используется в ювелирном деле как поделочный камень, в строительстве как абразивный материал.
 • Гематит Fe 2 О 3, образует плотные мелкокристаллические агрегаты чешуйчатого строения, скрытокристаллические массы (красный железняк), а также желваки (конкреции) радиально-лучистого или скорлуповатого строения. • Магнетит, или магнитный железняк Fe 304, обычно образует плотные кристаллические агрегаты. По свойствам напоминает кристаллическую разновидность гематита, но отличается от него черным цветом черты и магнитными свойствами. • Образование гематита и магнетита связано главным образом с эндогенными процессами – магматическими, гидротермальными и метаморфическими. Гематит может возникать и в экзогенных условиях (при выветривании, в морской среде). Месторождения руд, связанных с этими минералами, широко распространены, в том числе на Урале.
• Гематит Fe 2 О 3, образует плотные мелкокристаллические агрегаты чешуйчатого строения, скрытокристаллические массы (красный железняк), а также желваки (конкреции) радиально-лучистого или скорлуповатого строения. • Магнетит, или магнитный железняк Fe 304, обычно образует плотные кристаллические агрегаты. По свойствам напоминает кристаллическую разновидность гематита, но отличается от него черным цветом черты и магнитными свойствами. • Образование гематита и магнетита связано главным образом с эндогенными процессами – магматическими, гидротермальными и метаморфическими. Гематит может возникать и в экзогенных условиях (при выветривании, в морской среде). Месторождения руд, связанных с этими минералами, широко распространены, в том числе на Урале.
 • Лимонит, или бурый железняк, - это, строго говоря, не один минерал, а агрегат близких по составу минералов - гётита Fe. OOH, гидрогётита Fe. OOH. n. Н 2 О, лепидокрокита Fe. O(OH) и глинистых частиц, соотношения которых непостоянны. • образует плотные натечные или землистые рыхлые массы, конкреции и оолиты. Часто можно наблюдать в одном образце переходы плотных разностей в рыхлые. Цвет у рыхлых разностей охристо-желтый, у плотных – черный; черта соответственно желто-бурая или бурая. Образование связано с выветриванием железосодержащих минералов, а также с выпадением из поверхностных вод, причем в этом процессе большую роль играют микроорганизмы.
• Лимонит, или бурый железняк, - это, строго говоря, не один минерал, а агрегат близких по составу минералов - гётита Fe. OOH, гидрогётита Fe. OOH. n. Н 2 О, лепидокрокита Fe. O(OH) и глинистых частиц, соотношения которых непостоянны. • образует плотные натечные или землистые рыхлые массы, конкреции и оолиты. Часто можно наблюдать в одном образце переходы плотных разностей в рыхлые. Цвет у рыхлых разностей охристо-желтый, у плотных – черный; черта соответственно желто-бурая или бурая. Образование связано с выветриванием железосодержащих минералов, а также с выпадением из поверхностных вод, причем в этом процессе большую роль играют микроорганизмы.
 • Боксит является ценным полезным ископаемым на алюминий. Подобно лимониту, представляет собой агрегат минералов – оксидов и гидроксидов алюминия: диаспора Аl. OOН, гидраргиллита Аl(ОН)3, бемита Аl. O(ОН) с примесью оксидов железа, оксида кремния и др. Встречаются в виде землистых рыхлых или твердых масс, часто образуют оолитовые скопления. Цвет белый, серый, желтый, чаще красный, буро-красный. • Образуются при выветривании горных пород, которые богаты минералами, содержащими алюминий, и при последующем переотложении продуктов выветривания.
• Боксит является ценным полезным ископаемым на алюминий. Подобно лимониту, представляет собой агрегат минералов – оксидов и гидроксидов алюминия: диаспора Аl. OOН, гидраргиллита Аl(ОН)3, бемита Аl. O(ОН) с примесью оксидов железа, оксида кремния и др. Встречаются в виде землистых рыхлых или твердых масс, часто образуют оолитовые скопления. Цвет белый, серый, желтый, чаще красный, буро-красный. • Образуются при выветривании горных пород, которые богаты минералами, содержащими алюминий, и при последующем переотложении продуктов выветривания.
 • Класс карбонатов также объединяет широко распространенных минералов. Образование связано главным образом с поверхностными химическими и биохимическими процессами, а также с метаморфическими и гидротермальными • Кальцит Са[СО 3] – один из наиболее распространенных в земной коре минералов. Встречается в виде кристаллических и скрытокристаллических агрегатов различной плотности, в пустотах в виде разнообразных натечных форм, кристаллов и их сростков. Цвет разнообразный. Применение: в строительстве, в металлургической и химической промышленностях, как поделочный камень, исландский шпат – в оптике. • Доломит Ca. Mg[СO 3]2. Используется в металлургии и строительстве. • Реже встречается сидерит Fе [СО 3], слагающий кристаллические и землистые агрегаты, образующий округлые конкреции и оолиты. Является важной железной рудой. Крупные месторождения имеются на Южном Урале.
• Класс карбонатов также объединяет широко распространенных минералов. Образование связано главным образом с поверхностными химическими и биохимическими процессами, а также с метаморфическими и гидротермальными • Кальцит Са[СО 3] – один из наиболее распространенных в земной коре минералов. Встречается в виде кристаллических и скрытокристаллических агрегатов различной плотности, в пустотах в виде разнообразных натечных форм, кристаллов и их сростков. Цвет разнообразный. Применение: в строительстве, в металлургической и химической промышленностях, как поделочный камень, исландский шпат – в оптике. • Доломит Ca. Mg[СO 3]2. Используется в металлургии и строительстве. • Реже встречается сидерит Fе [СО 3], слагающий кристаллические и землистые агрегаты, образующий округлые конкреции и оолиты. Является важной железной рудой. Крупные месторождения имеются на Южном Урале.
 • класс сульфатов • осаждаются в поверхностных водоемах, образуются при окислении сульфидов и серы в зонах выветривания, реже связаны с вулканической деятельностью. • Ангидрит Ca[SO 4] – образует плотные мелкокристаллические скопления. Используется для производства цемента, для поделок. • Гипс Ca[SO 4]. 2 H 2 O является наиболее распространенным минералом класса сульфатов. Встречается в виде мелкокристаллических и землистых агрегатов, отдельных кристаллов и их сростков. Используется в строительстве, в химической промышленности, медицине и др. .
• класс сульфатов • осаждаются в поверхностных водоемах, образуются при окислении сульфидов и серы в зонах выветривания, реже связаны с вулканической деятельностью. • Ангидрит Ca[SO 4] – образует плотные мелкокристаллические скопления. Используется для производства цемента, для поделок. • Гипс Ca[SO 4]. 2 H 2 O является наиболее распространенным минералом класса сульфатов. Встречается в виде мелкокристаллических и землистых агрегатов, отдельных кристаллов и их сростков. Используется в строительстве, в химической промышленности, медицине и др. .
![• Класс фосфатов. Наиболее распространенным является апатит Са 5[РO 4]3(F, ОН, Cl) (содержание • Класс фосфатов. Наиболее распространенным является апатит Са 5[РO 4]3(F, ОН, Cl) (содержание](https://present5.com/presentation/3/23191453_150731414.pdf-img/23191453_150731414.pdf-15.jpg) • Класс фосфатов. Наиболее распространенным является апатит Са 5[РO 4]3(F, ОН, Cl) (содержание фтора, хлора и гидроксильной группы колеблется). Происхождение магматическое. Широко используется для производства удобрения и в химической промышленности. • В поверхностных условиях возникает скрытокристаллический минерал того же состава - фосфорит. Образует землистые агрегаты, конкреции, псевдоморфозы по органическим остаткам. Обычно содержит примесь песчаных и глинистых частиц. Образуется в бассейнах в результате жизнедеятельности и последующей переработки организмов. Используется, как и апатит, для производства удобрений и в химической промышленности.
• Класс фосфатов. Наиболее распространенным является апатит Са 5[РO 4]3(F, ОН, Cl) (содержание фтора, хлора и гидроксильной группы колеблется). Происхождение магматическое. Широко используется для производства удобрения и в химической промышленности. • В поверхностных условиях возникает скрытокристаллический минерал того же состава - фосфорит. Образует землистые агрегаты, конкреции, псевдоморфозы по органическим остаткам. Обычно содержит примесь песчаных и глинистых частиц. Образуется в бассейнах в результате жизнедеятельности и последующей переработки организмов. Используется, как и апатит, для производства удобрений и в химической промышленности.
 Класс силикатов • Широко распространены в земной коре (свыше 78%). Образуются преимущественно в эндогенных условиях. • Многие минералы этого класса являются породообразующими. • характеризуются сложным химическим составом и внутренним строением.
Класс силикатов • Широко распространены в земной коре (свыше 78%). Образуются преимущественно в эндогенных условиях. • Многие минералы этого класса являются породообразующими. • характеризуются сложным химическим составом и внутренним строением.
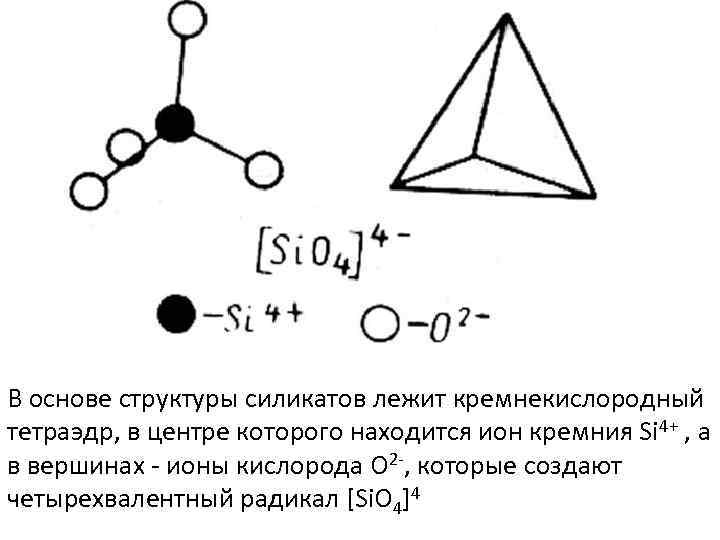 В основе структуры силикатов лежит кремнекислородный тетраэдр, в центре которого находится ион кремния Si 4+ , а в вершинах - ионы кислорода О 2 -, которые создают четырехвалентный радикал [Si. O 4]4
В основе структуры силикатов лежит кремнекислородный тетраэдр, в центре которого находится ион кремния Si 4+ , а в вершинах - ионы кислорода О 2 -, которые создают четырехвалентный радикал [Si. O 4]4
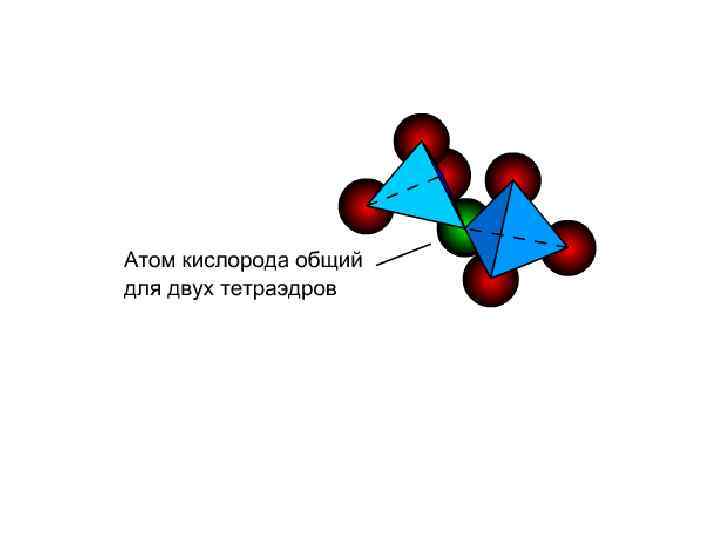
 • Частичная замена четырехвалентных ионов кремния трехвалентными ионами алюминия приводит к возникновению у такого соединения некоторого дополнительного отрицательного заряда. • Минералы с подобным строением называются алюмосиликатами. Примером минерала силиката является оливин - (Mg, Fe)2[Si. O 4], алюмосиликата – ортоклаз K[Al. Si 3 O 8].
• Частичная замена четырехвалентных ионов кремния трехвалентными ионами алюминия приводит к возникновению у такого соединения некоторого дополнительного отрицательного заряда. • Минералы с подобным строением называются алюмосиликатами. Примером минерала силиката является оливин - (Mg, Fe)2[Si. O 4], алюмосиликата – ортоклаз K[Al. Si 3 O 8].
 • Кремнекислородные и алюмокремнекислородные тетраэдры в пространстве могут различно сочетаться друг с другом, что определяет кристаллическую структуру минералов и лежит в основе их современной классификации.
• Кремнекислородные и алюмокремнекислородные тетраэдры в пространстве могут различно сочетаться друг с другом, что определяет кристаллическую структуру минералов и лежит в основе их современной классификации.
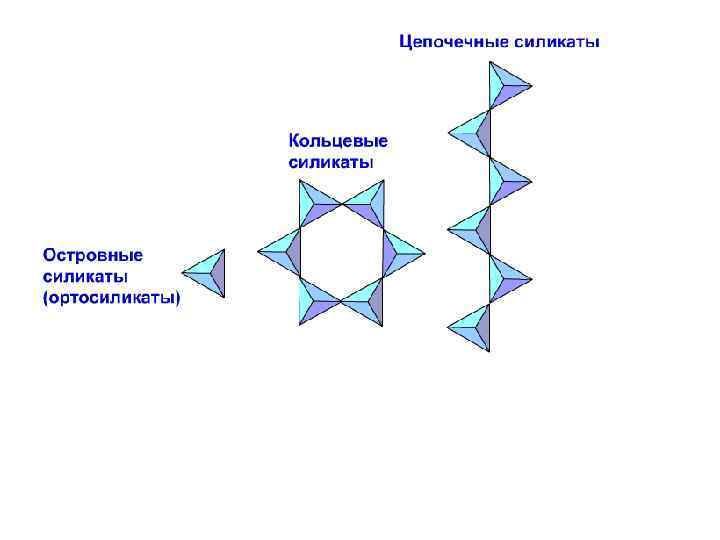
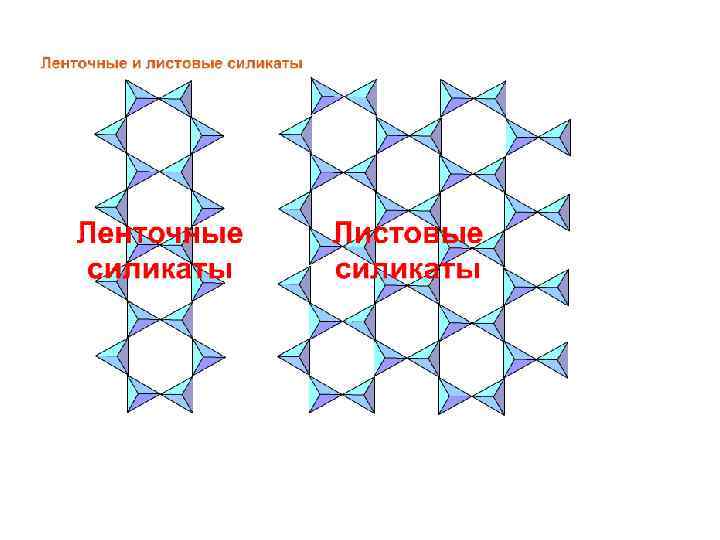
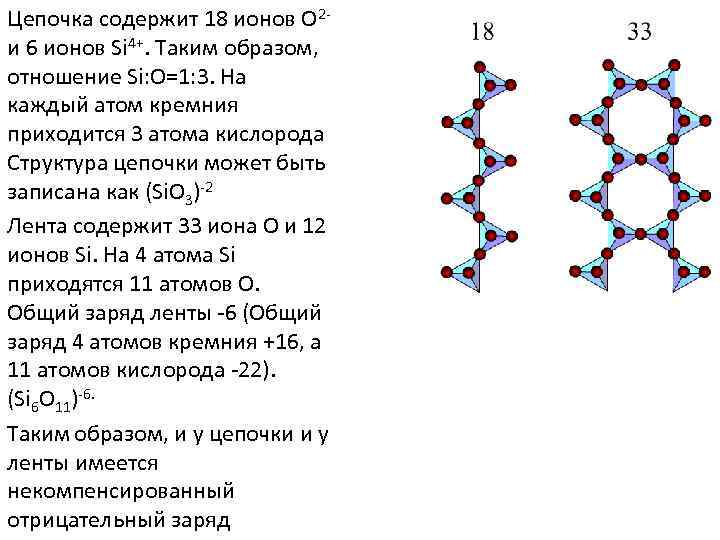 Цепочка содержит 18 ионов О 2 и 6 ионов Si 4+. Таким образом, отношение Si: O=1: 3. На каждый атом кремния приходится 3 атома кислорода. Структура цепочки может быть записана как (Si. O 3)-2 Лента содержит 33 иона О и 12 ионов Si. На 4 атома Si приходятся 11 атомов О. Общий заряд ленты -6 (Общий заряд 4 атомов кремния +16, а 11 атомов кислорода -22). (Si 6 O 11)-6. Таким образом, и у цепочки и у ленты имеется некомпенсированный отрицательный заряд
Цепочка содержит 18 ионов О 2 и 6 ионов Si 4+. Таким образом, отношение Si: O=1: 3. На каждый атом кремния приходится 3 атома кислорода. Структура цепочки может быть записана как (Si. O 3)-2 Лента содержит 33 иона О и 12 ионов Si. На 4 атома Si приходятся 11 атомов О. Общий заряд ленты -6 (Общий заряд 4 атомов кремния +16, а 11 атомов кислорода -22). (Si 6 O 11)-6. Таким образом, и у цепочки и у ленты имеется некомпенсированный отрицательный заряд
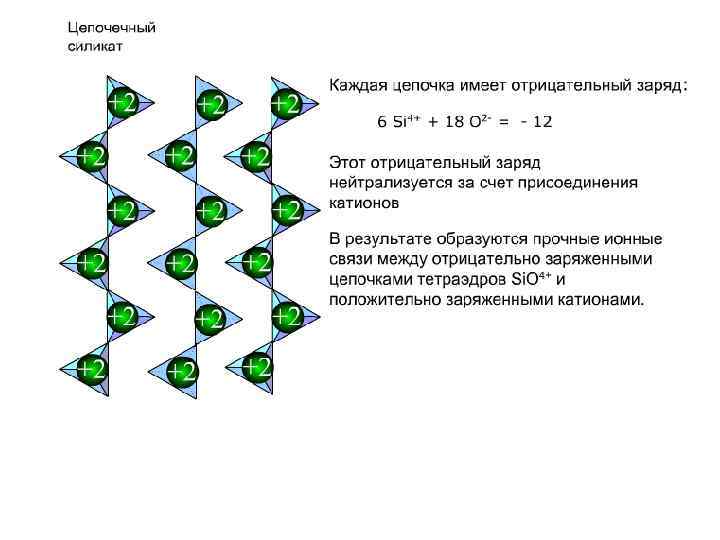
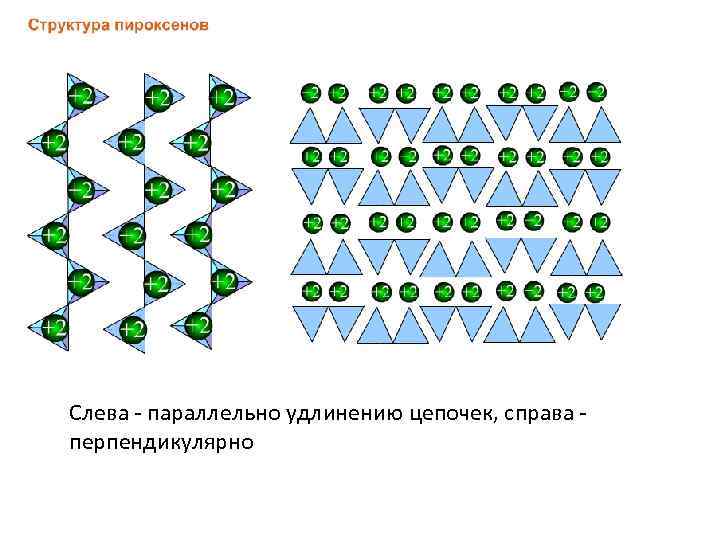 Слева - параллельно удлинению цепочек, справа - перпендикулярно
Слева - параллельно удлинению цепочек, справа - перпендикулярно
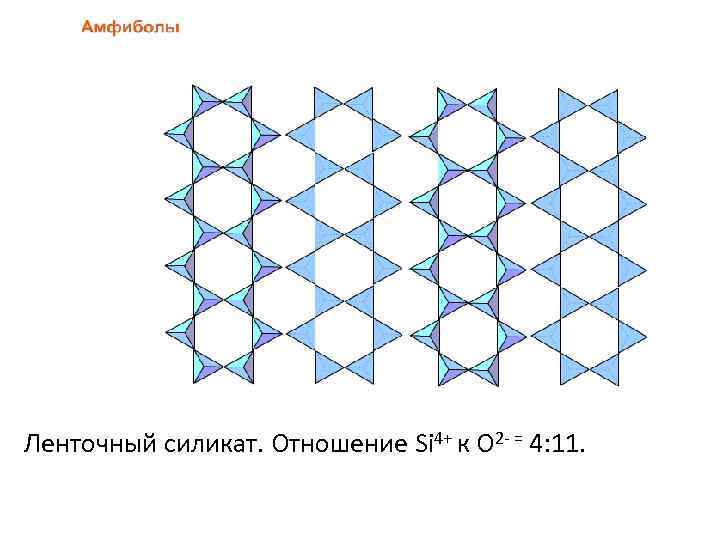 Ленточный силикат. Отношение Si 4+ к O 2 - = 4: 11.
Ленточный силикат. Отношение Si 4+ к O 2 - = 4: 11.
 • Трехмерно соединяясь в пространстве через ионы кислорода, кремнекислородные тетраэдры создают структуру, называемую каркасной. • Отрицательный заряд тетраэдров обеспечивает присоединение к каркасной структуре катионов и образование каркасных алюмосиликатов. К ним относятся, например, полевые шпаты
• Трехмерно соединяясь в пространстве через ионы кислорода, кремнекислородные тетраэдры создают структуру, называемую каркасной. • Отрицательный заряд тетраэдров обеспечивает присоединение к каркасной структуре катионов и образование каркасных алюмосиликатов. К ним относятся, например, полевые шпаты
 • Внутренняя структура силикатов и алюмосиликатов в значительной степени обусловливает их свойства: минералы с островной структурой, характеризующейся плотной упаковкой ионов, часто образуют изометричные кристаллы, обладают большой твердостью, плотностью и несовершенной спайностью. Минералы со слоевой структурой образуют таблитчатые кристаллы с весьма совершенной спайностью, параллельной "слоям" структуры.
• Внутренняя структура силикатов и алюмосиликатов в значительной степени обусловливает их свойства: минералы с островной структурой, характеризующейся плотной упаковкой ионов, часто образуют изометричные кристаллы, обладают большой твердостью, плотностью и несовершенной спайностью. Минералы со слоевой структурой образуют таблитчатые кристаллы с весьма совершенной спайностью, параллельной "слоям" структуры.
 Минералы с линейно вытянутыми структурами (цепочечными и ленточными) образуют призматические кристаллы, обладающие хорошо выраженной спайностью в двух направлениях вдоль длинной оси структуры.
Минералы с линейно вытянутыми структурами (цепочечными и ленточными) образуют призматические кристаллы, обладающие хорошо выраженной спайностью в двух направлениях вдоль длинной оси структуры.


![Островной силикат. Оливин (Mg, Fe)2[Si. O 4], член изоморфного ряда форстерит (бесцветный) Mg 2[Si. Островной силикат. Оливин (Mg, Fe)2[Si. O 4], член изоморфного ряда форстерит (бесцветный) Mg 2[Si.](https://present5.com/presentation/3/23191453_150731414.pdf-img/23191453_150731414.pdf-32.jpg) Островной силикат. Оливин (Mg, Fe)2[Si. O 4], член изоморфного ряда форстерит (бесцветный) Mg 2[Si. O 4] и фаялит (черный) Fe 2[Si. O 4]. Встречается обычно в виде зернистых агрегатов или отдельных зерен.
Островной силикат. Оливин (Mg, Fe)2[Si. O 4], член изоморфного ряда форстерит (бесцветный) Mg 2[Si. O 4] и фаялит (черный) Fe 2[Si. O 4]. Встречается обычно в виде зернистых агрегатов или отдельных зерен.


