Миненкова О. ФАГОВАЯ ТЕРАПИЯ 2014 Фредерик Туорт 1877-1950





























13406-phage_therapy_2.ppt
- Количество слайдов: 56
 Миненкова О. ФАГОВАЯ ТЕРАПИЯ 2014
Миненкова О. ФАГОВАЯ ТЕРАПИЯ 2014
 Фредерик Туорт 1877-1950 Феликс Д’Эрелль 1873-1949
Фредерик Туорт 1877-1950 Феликс Д’Эрелль 1873-1949
 Использование фаговой терапии, имея слабое представление о фагах и о микробиологии. Неправильные методы приготовления и хранения. Использование моно фагов при инфекциях, вызываемых несколькими различными бактериями. Появление резистентных штаммов бактерий. Они могут возникнуть путем селекции резистентных мутантов или путем лизогенизации. Неправильная классификация фагов или ошибки в отношении титра препаратов. Неудача в нейтрализации низких значений желудочного рН при исполь-зовании пероральных препаратов. Специфическая инактивация бактериофагов в крови. Высвобождение эндотоксинов вследствие массивного лизиса бактерий внутри организма. Основные причины неудач первых экспериментов
Использование фаговой терапии, имея слабое представление о фагах и о микробиологии. Неправильные методы приготовления и хранения. Использование моно фагов при инфекциях, вызываемых несколькими различными бактериями. Появление резистентных штаммов бактерий. Они могут возникнуть путем селекции резистентных мутантов или путем лизогенизации. Неправильная классификация фагов или ошибки в отношении титра препаратов. Неудача в нейтрализации низких значений желудочного рН при исполь-зовании пероральных препаратов. Специфическая инактивация бактериофагов в крови. Высвобождение эндотоксинов вследствие массивного лизиса бактерий внутри организма. Основные причины неудач первых экспериментов
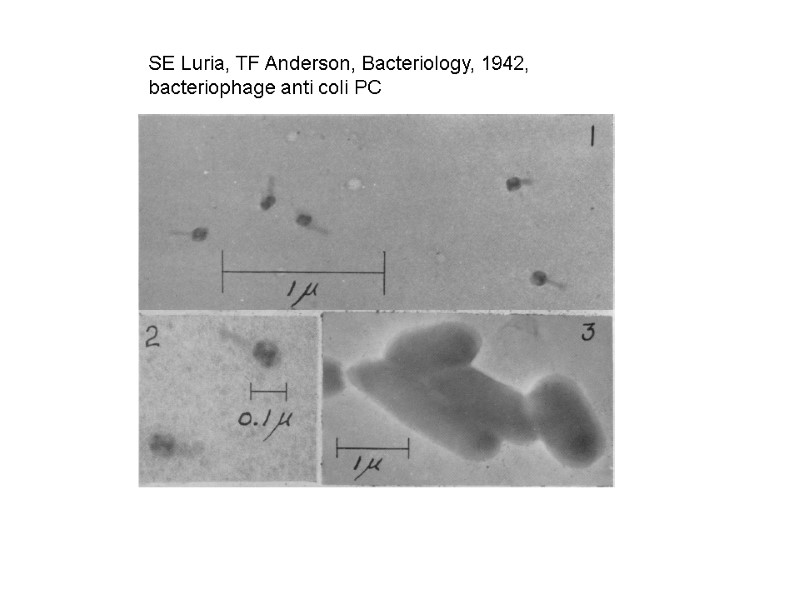
 SE Luria, TF Anderson, Bacteriology, 1942, bacteriophage anti coli PC
SE Luria, TF Anderson, Bacteriology, 1942, bacteriophage anti coli PC
 Нобелевская премия по Физиологии и Медицине была присуждена в 1969 г группе по изучению фагов
Нобелевская премия по Физиологии и Медицине была присуждена в 1969 г группе по изучению фагов
 Frederick Sanger 1913 Получил вторую Нобелевскую премию по химии в 1980 г.
Frederick Sanger 1913 Получил вторую Нобелевскую премию по химии в 1980 г.
 George P Smith, 1941. Основатель метода фаговый дисплей.
George P Smith, 1941. Основатель метода фаговый дисплей.
 Для терапии может быть использован только вирулентный фаг. Среды для приготовления фага должны были содержать минимально возможное количество высокомолекулярных белков. Для терапии использовалось две категории бактериофагов - ранее подобранные коктейли и адаптированные фаги. Эффективность маловирулентных штаммов повышалась с помощью повторных пассажей на одном и том же бактериальном штамме. Фаги использовались несколькими способами: местное применение, подкожные инъекции (для стафилококка), перорально, внутривенно и в виде инъекций в плевру и перикард. Потенциальная нейтрализация фага антителами могла быть предотвращена заменой одного фага другим, отличающимся серологически. Обзоры Института Пастера. Франция
Для терапии может быть использован только вирулентный фаг. Среды для приготовления фага должны были содержать минимально возможное количество высокомолекулярных белков. Для терапии использовалось две категории бактериофагов - ранее подобранные коктейли и адаптированные фаги. Эффективность маловирулентных штаммов повышалась с помощью повторных пассажей на одном и том же бактериальном штамме. Фаги использовались несколькими способами: местное применение, подкожные инъекции (для стафилококка), перорально, внутривенно и в виде инъекций в плевру и перикард. Потенциальная нейтрализация фага антителами могла быть предотвращена заменой одного фага другим, отличающимся серологически. Обзоры Института Пастера. Франция
 Исследования в других странах: Польша Институт Иммунологии и Экспериментальной Медицины, Вроцлав, с 1954 г США Эксперименты Дюбо и Мортона на мышах, лечение тифоидной лихорадки Грузия Центр фаговой терапии в Институте Элиава, с 1930 г
Исследования в других странах: Польша Институт Иммунологии и Экспериментальной Медицины, Вроцлав, с 1954 г США Эксперименты Дюбо и Мортона на мышах, лечение тифоидной лихорадки Грузия Центр фаговой терапии в Институте Элиава, с 1930 г
 1.Фармакокинетика: адсорбция распределение метаболизм выведение 2. Фармакодинамика: безопасность иммуногенность размножение фага лизогения: Лизогенная бактерия не погибает в результате инфекции, устойчива к заражению другими фагами того же типа. Лизогенные фаги способны к конверсии бактерии, могут менять бактериальный фенотип и приводить к повышению вирулентности бактерий. Такие фаги способны к трансдукции и могут передавать бактериальные гены последующим инфицированным бактериям 3. Фаг как пробиотик
1.Фармакокинетика: адсорбция распределение метаболизм выведение 2. Фармакодинамика: безопасность иммуногенность размножение фага лизогения: Лизогенная бактерия не погибает в результате инфекции, устойчива к заражению другими фагами того же типа. Лизогенные фаги способны к конверсии бактерии, могут менять бактериальный фенотип и приводить к повышению вирулентности бактерий. Такие фаги способны к трансдукции и могут передавать бактериальные гены последующим инфицированным бактериям 3. Фаг как пробиотик

 Фаговые гидролазы (лизины) рузрушают пептидогликан, образуются на финальной стадии заражения, очень эффективны в случае Грам-положительных бактерий. N-концевой домен – каталитический, C-концевой связывающий. Делятся на 4 класса в зависимости от расщепляемых связей: N-ацетилмураномидазы (лизоцимы) N-ацетил-b-D-глюкозаминидазы (гликозидазы) N-ацетилмурамоил-L-аланин амидазы L-аланоил-D-глутамат эндопептидазы Фаговые ферменты
Фаговые гидролазы (лизины) рузрушают пептидогликан, образуются на финальной стадии заражения, очень эффективны в случае Грам-положительных бактерий. N-концевой домен – каталитический, C-концевой связывающий. Делятся на 4 класса в зависимости от расщепляемых связей: N-ацетилмураномидазы (лизоцимы) N-ацетил-b-D-глюкозаминидазы (гликозидазы) N-ацетилмурамоил-L-аланин амидазы L-аланоил-D-глутамат эндопептидазы Фаговые ферменты
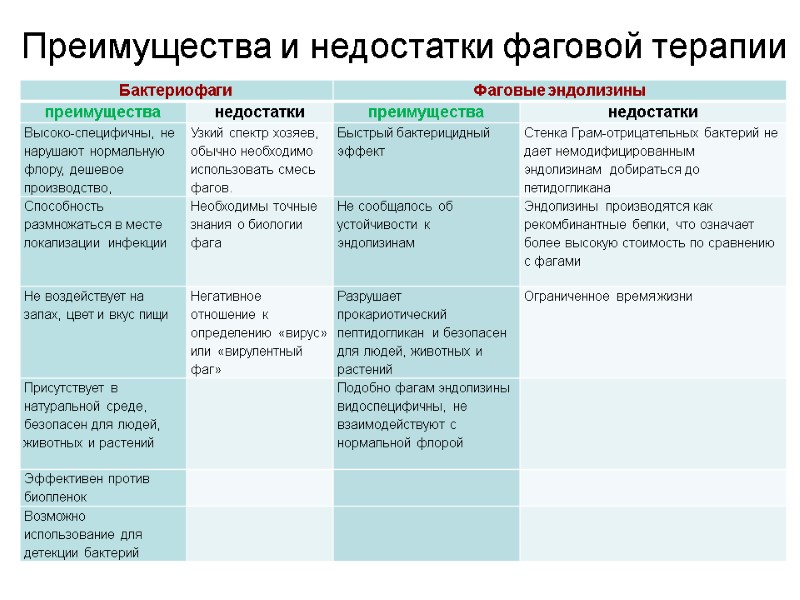
 Преимущества и недостатки фаговой терапии
Преимущества и недостатки фаговой терапии

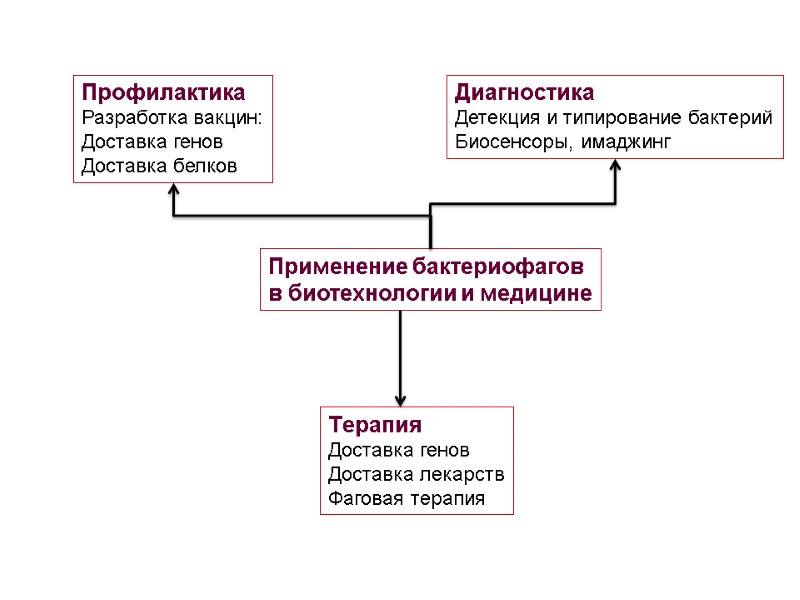
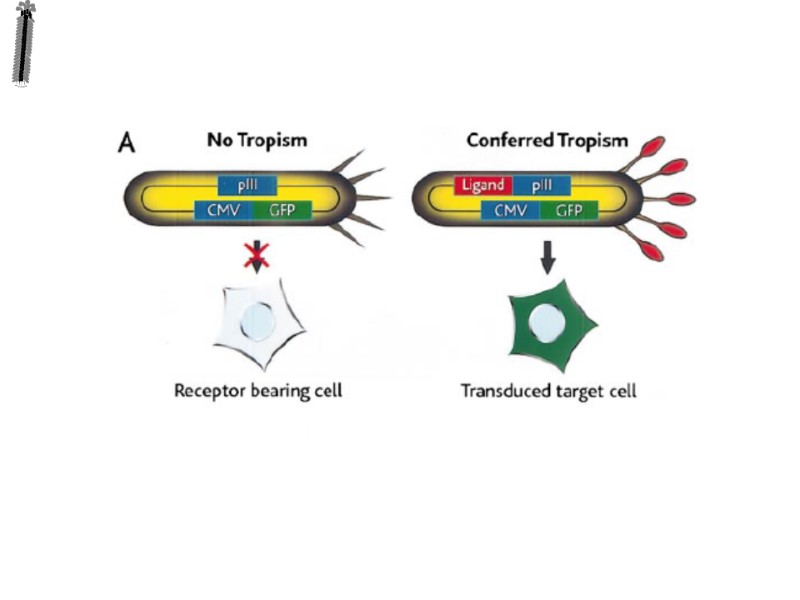
 Применение бактериофагов в биотехнологии и медицине Диагностика Детекция и типирование бактерий Биосенсоры, имаджинг Профилактика Разработка вакцин: Доставка генов Доставка белков Терапия Доставка генов Доставка лекарств Фаговая терапия
Применение бактериофагов в биотехнологии и медицине Диагностика Детекция и типирование бактерий Биосенсоры, имаджинг Профилактика Разработка вакцин: Доставка генов Доставка белков Терапия Доставка генов Доставка лекарств Фаговая терапия
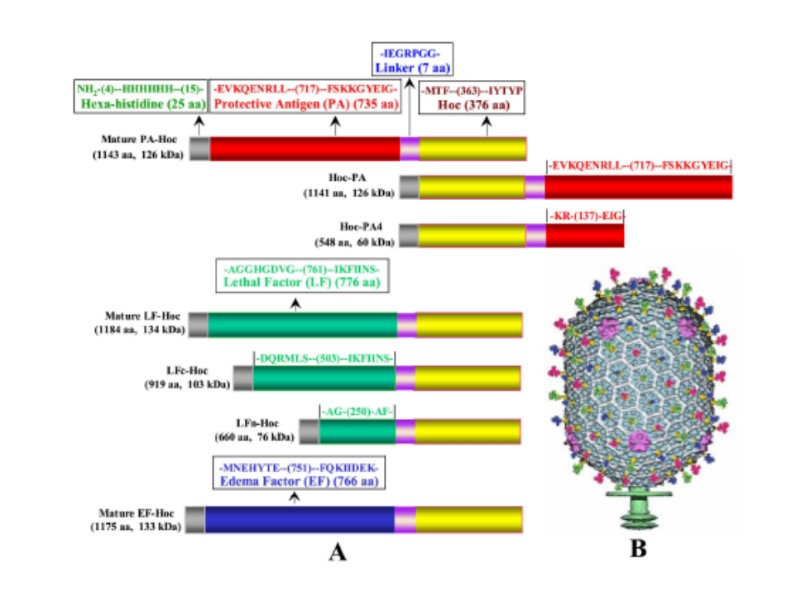
 T4 architecture: major coat protein gp23 (49 kDa, 930 copies) vertex protein gp24 (46 kDa, 55 copies) portal protein gp20 (61 kDa, 12 copies) decoration proteins: Hoc (highly antigenic outer capsid protein, 36 kDa, 155 copies) Soc (small outer capsid protein, 9 kDa, 810 copies) Anthrax toxin proteins – protective antigen (PA, 83 kDa) lethal factor (LF, 90 kDa) edema factor (EF, 89 kDa)
T4 architecture: major coat protein gp23 (49 kDa, 930 copies) vertex protein gp24 (46 kDa, 55 copies) portal protein gp20 (61 kDa, 12 copies) decoration proteins: Hoc (highly antigenic outer capsid protein, 36 kDa, 155 copies) Soc (small outer capsid protein, 9 kDa, 810 copies) Anthrax toxin proteins – protective antigen (PA, 83 kDa) lethal factor (LF, 90 kDa) edema factor (EF, 89 kDa)

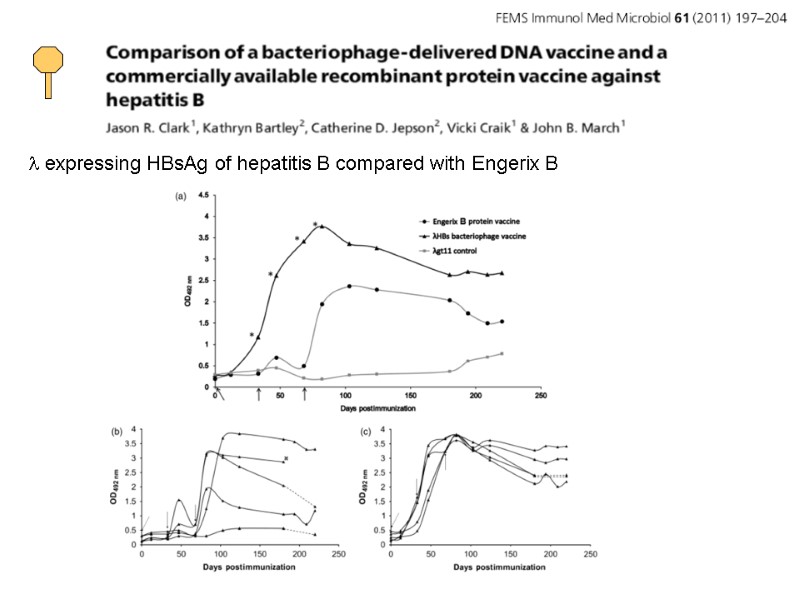
 l expressing HBsAg of hepatitis B compared with Engerix B
l expressing HBsAg of hepatitis B compared with Engerix B
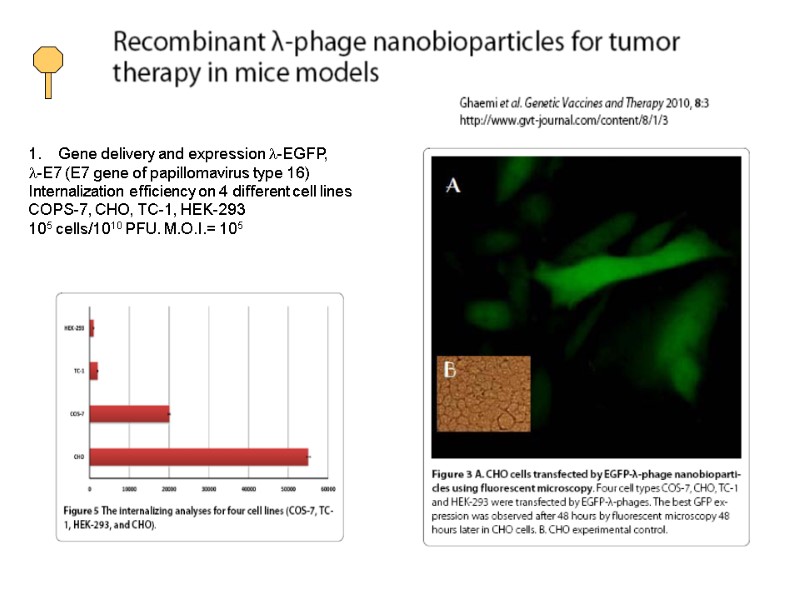
 Gene delivery and expression l-EGFP, l-E7 (E7 gene of papillomavirus type 16) Internalization efficiency on 4 different cell lines COPS-7, CHO, TC-1, HEK-293 105 cells/1010 PFU. M.O.I.= 105
Gene delivery and expression l-EGFP, l-E7 (E7 gene of papillomavirus type 16) Internalization efficiency on 4 different cell lines COPS-7, CHO, TC-1, HEK-293 105 cells/1010 PFU. M.O.I.= 105
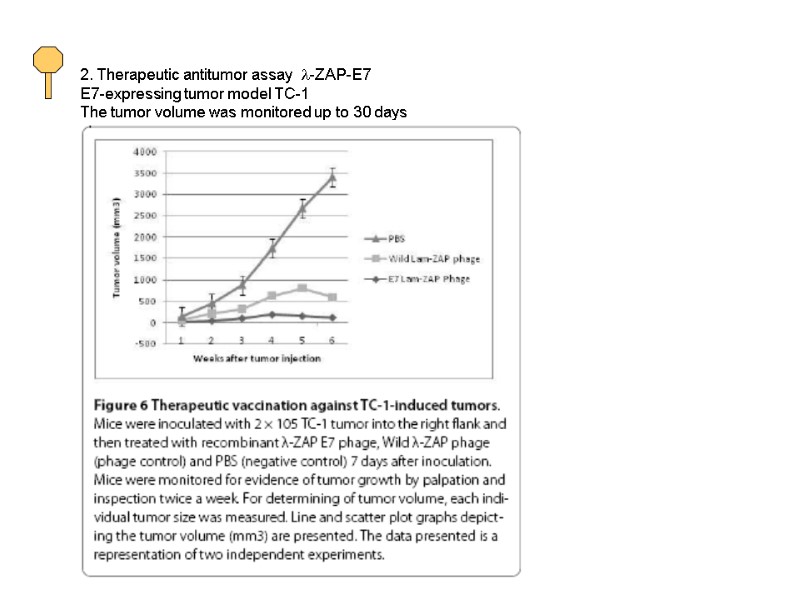
 2. Therapeutic antitumor assay l-ZAP-E7 E7-expressing tumor model TC-1 The tumor volume was monitored up to 30 days
2. Therapeutic antitumor assay l-ZAP-E7 E7-expressing tumor model TC-1 The tumor volume was monitored up to 30 days
 nanoparticles
nanoparticles

 human polyclonal sera against staphylococci (4-5% target specific) streptococci rabbit protein A-purified IgG against E. coli O78 Growth inhibition of target bacteria Staphylococcus aureus Streptococcus pyogenes E. coli O78 1010 phage/107 bacteria = 15 mg of free antibiotic Improvement factor 20.000
human polyclonal sera against staphylococci (4-5% target specific) streptococci rabbit protein A-purified IgG against E. coli O78 Growth inhibition of target bacteria Staphylococcus aureus Streptococcus pyogenes E. coli O78 1010 phage/107 bacteria = 15 mg of free antibiotic Improvement factor 20.000
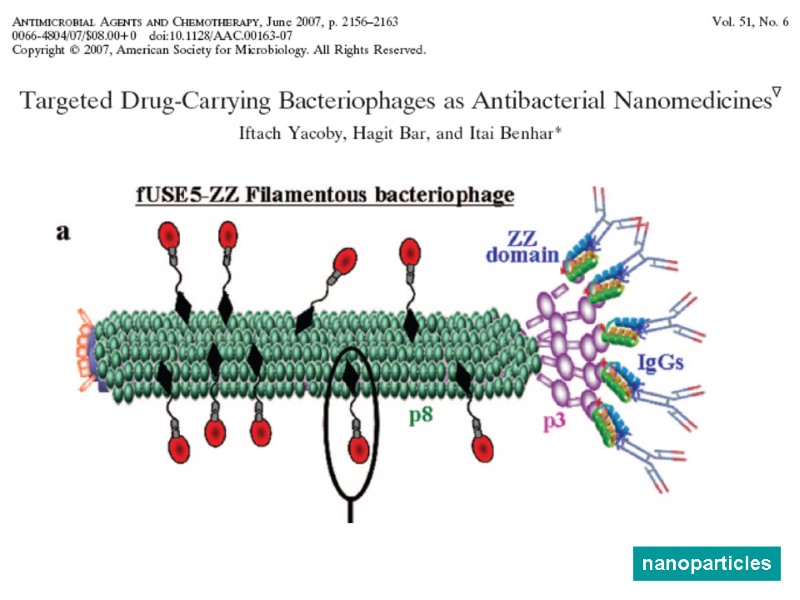
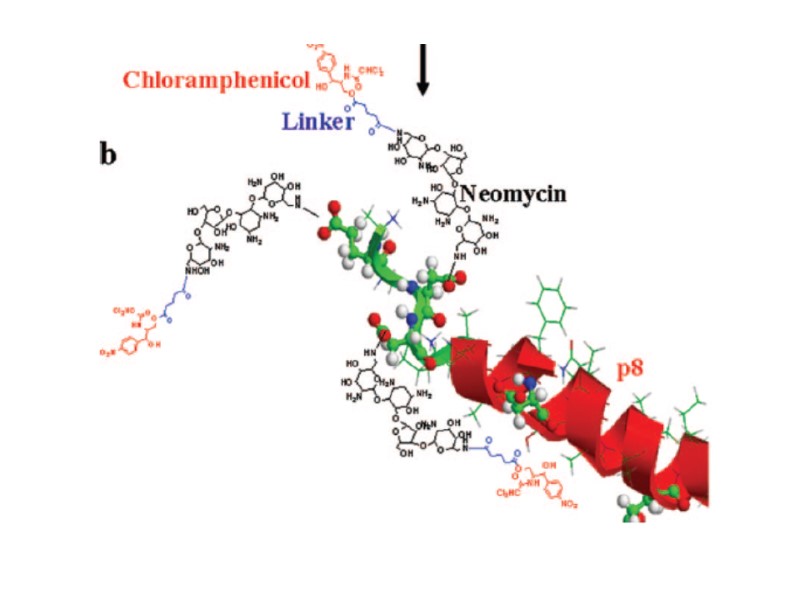
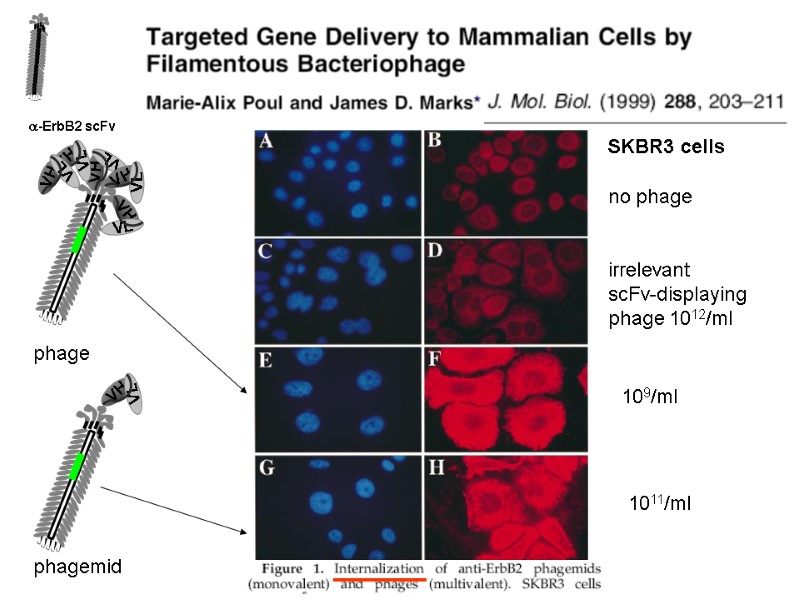
 Form: targeted drug-carring phage nanoparticles – genetically modified and chemically manipulated filamentous bacteriophage. Targeted moieties – anti-ERB2 trastusumab – anti EGFR cetuximab Drugs – hygromycin conjugated to phage by a covalent amide bond – doxorubicin conjugated though genetically-egineered cathepsin-B site Targeting to receptors of cancer cellsendocytosisintracellular degradation drug releasecell inhibition with factor >1000 over free drug (in vitro)
Form: targeted drug-carring phage nanoparticles – genetically modified and chemically manipulated filamentous bacteriophage. Targeted moieties – anti-ERB2 trastusumab – anti EGFR cetuximab Drugs – hygromycin conjugated to phage by a covalent amide bond – doxorubicin conjugated though genetically-egineered cathepsin-B site Targeting to receptors of cancer cellsendocytosisintracellular degradation drug releasecell inhibition with factor >1000 over free drug (in vitro)

 a-ErbB2 scFv phage phagemid SKBR3 cells no phage irrelevant scFv-displaying phage 1012/ml 109/ml 1011/ml
a-ErbB2 scFv phage phagemid SKBR3 cells no phage irrelevant scFv-displaying phage 1012/ml 109/ml 1011/ml
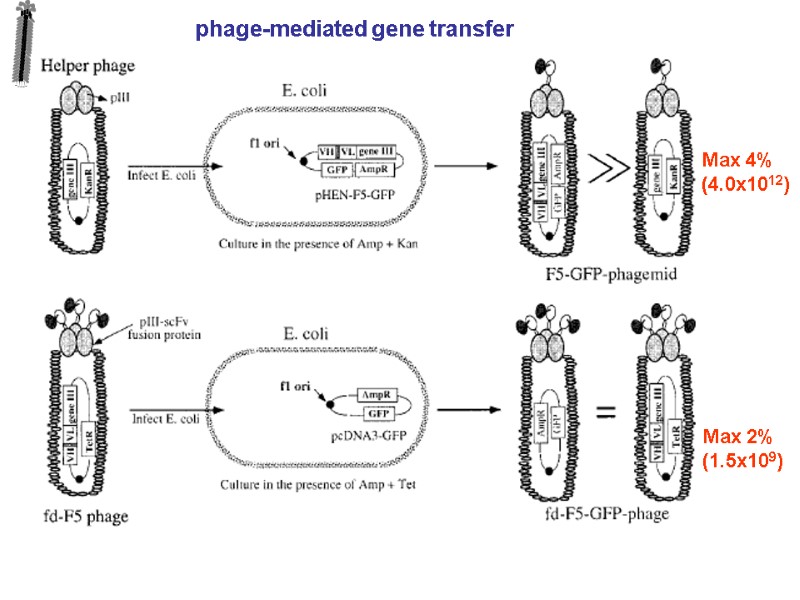
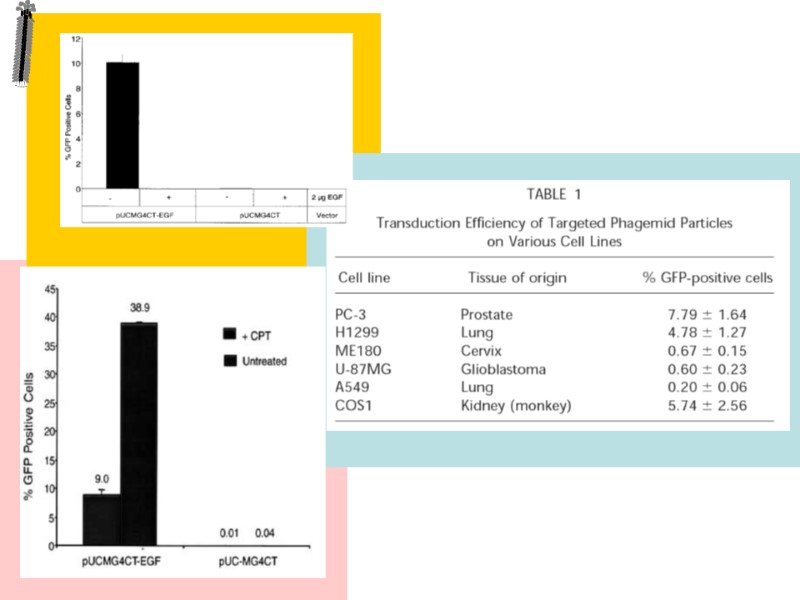
 phage-mediated gene transfer Max 4% (4.0x1012) Max 2% (1.5x109)
phage-mediated gene transfer Max 4% (4.0x1012) Max 2% (1.5x109)


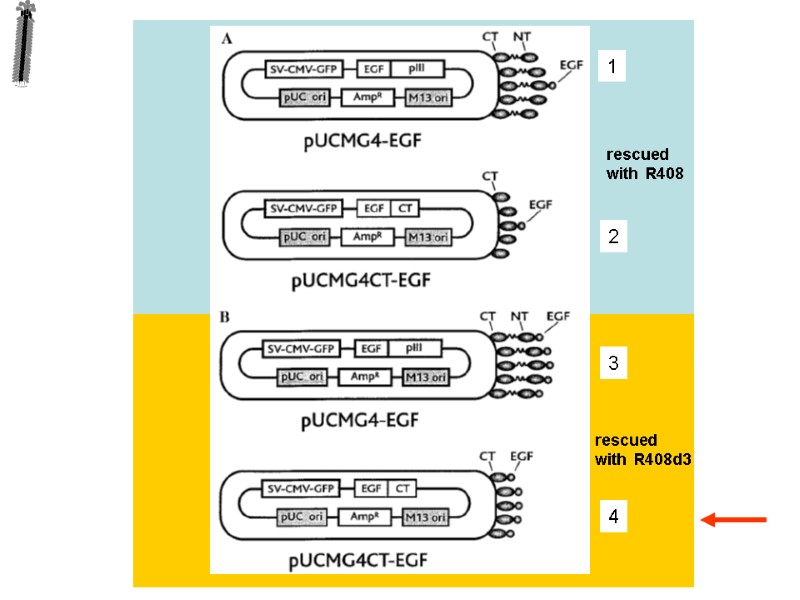
 rescued with R408 rescued with R408d3 1 2 3 4
rescued with R408 rescued with R408d3 1 2 3 4
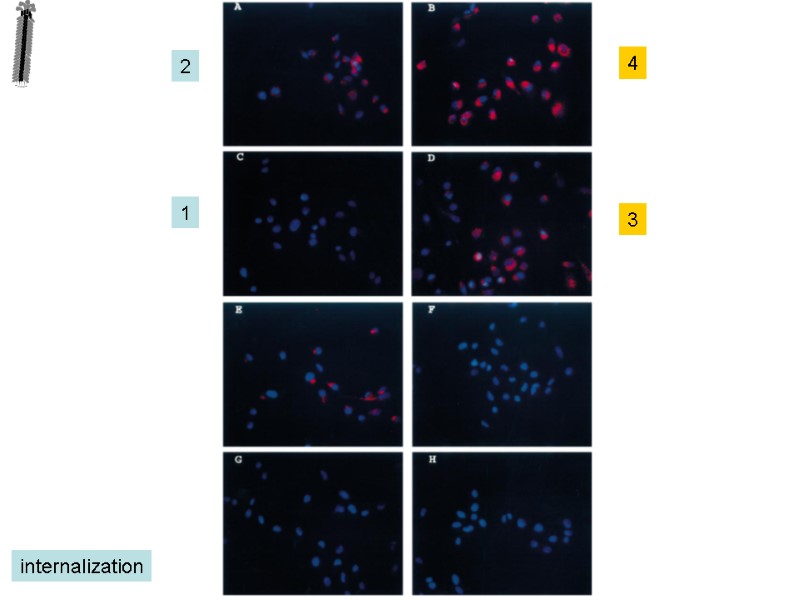
 2 4 1 3 internalization
2 4 1 3 internalization
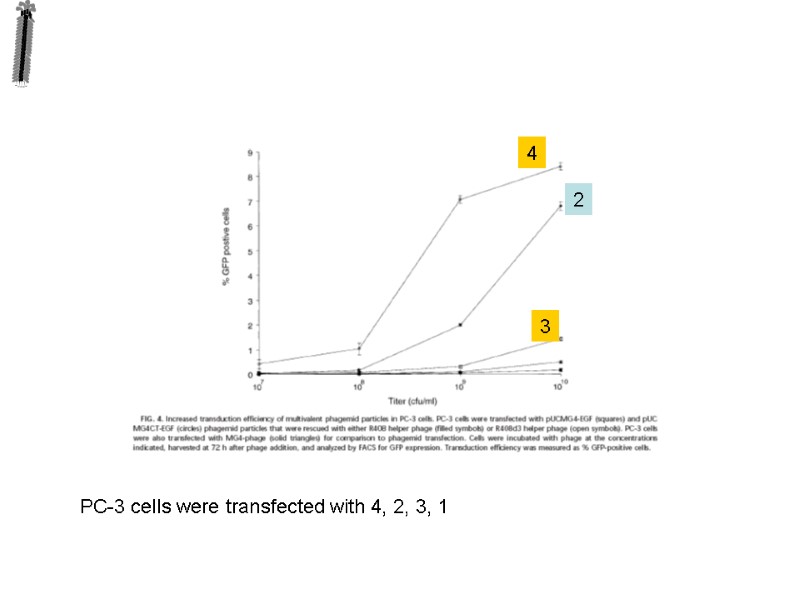
 PC-3 cells were transfected with 4, 2, 3, 1 4 3 2
PC-3 cells were transfected with 4, 2, 3, 1 4 3 2

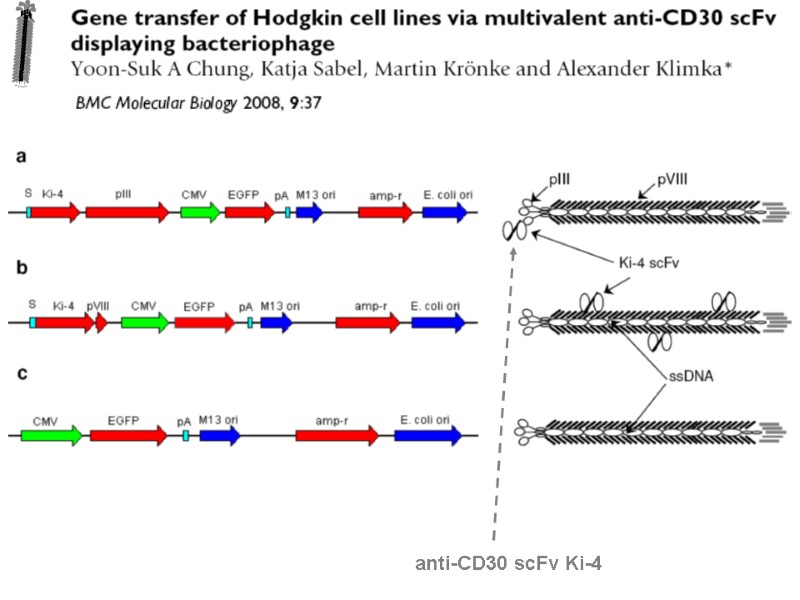
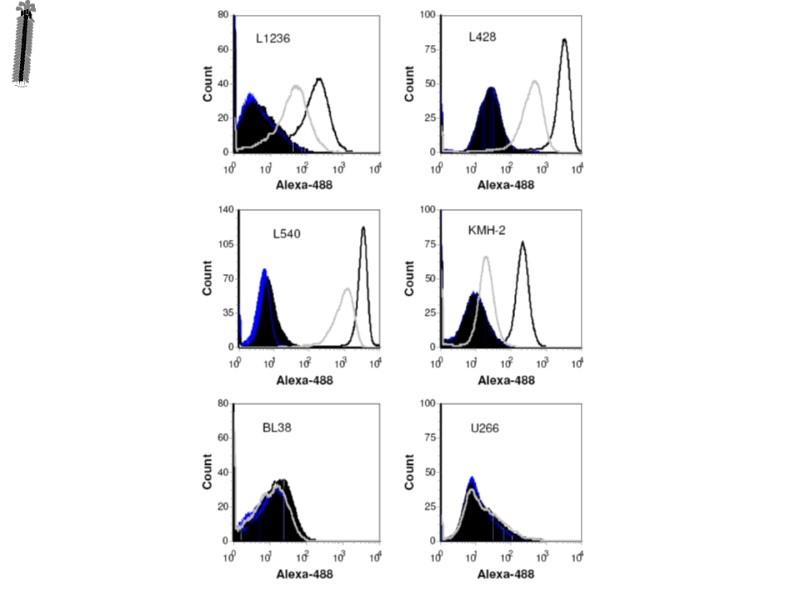
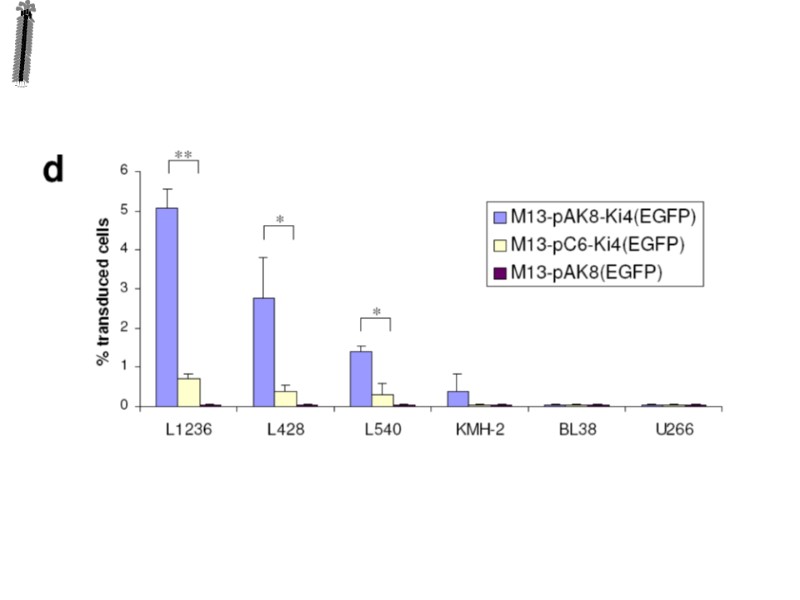
 anti-CD30 scFv Ki-4
anti-CD30 scFv Ki-4



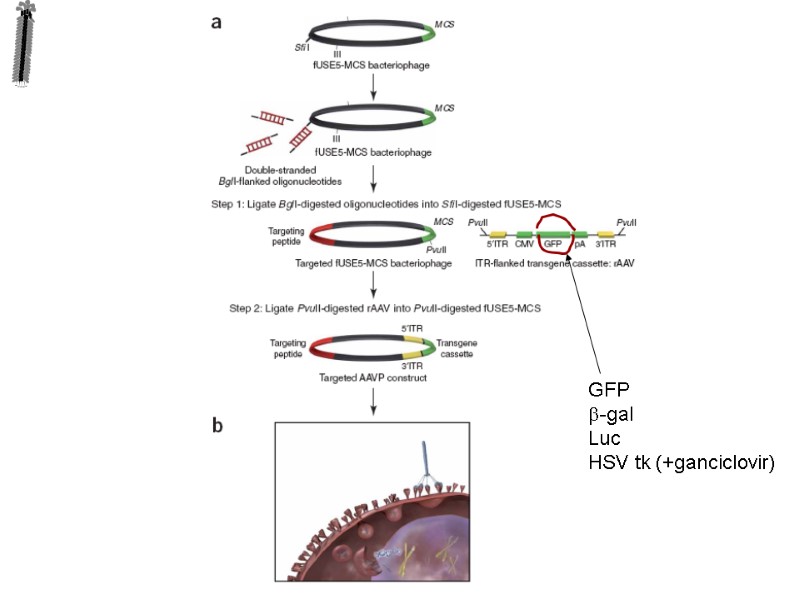
 Wild-type AAV is atractive for gene therapy researchers due to the features: Lack of pathogenicity. It can infect dividing and non-dividing cells It has the ability to stably integrate into the host cell genome at a specific site (designated AAVS1) in the human chromosome 19 4. This integrative capacity can be eliminated by removal of the rep and cap from the DNA of the vector. ITRs Inverted Terminal Repeat 130-145 b sequences AAVP =AAV/phage fd phage displaying double cyclic peptide CDCRGDCFC (termed RGD-4C) The RGD-4C peptide binds to an integrins, a cell-surface receptors overexpressed in both tumors and endothelial cells
Wild-type AAV is atractive for gene therapy researchers due to the features: Lack of pathogenicity. It can infect dividing and non-dividing cells It has the ability to stably integrate into the host cell genome at a specific site (designated AAVS1) in the human chromosome 19 4. This integrative capacity can be eliminated by removal of the rep and cap from the DNA of the vector. ITRs Inverted Terminal Repeat 130-145 b sequences AAVP =AAV/phage fd phage displaying double cyclic peptide CDCRGDCFC (termed RGD-4C) The RGD-4C peptide binds to an integrins, a cell-surface receptors overexpressed in both tumors and endothelial cells
 GFP b-gal Luc HSV tk (+ganciclovir)
GFP b-gal Luc HSV tk (+ganciclovir)
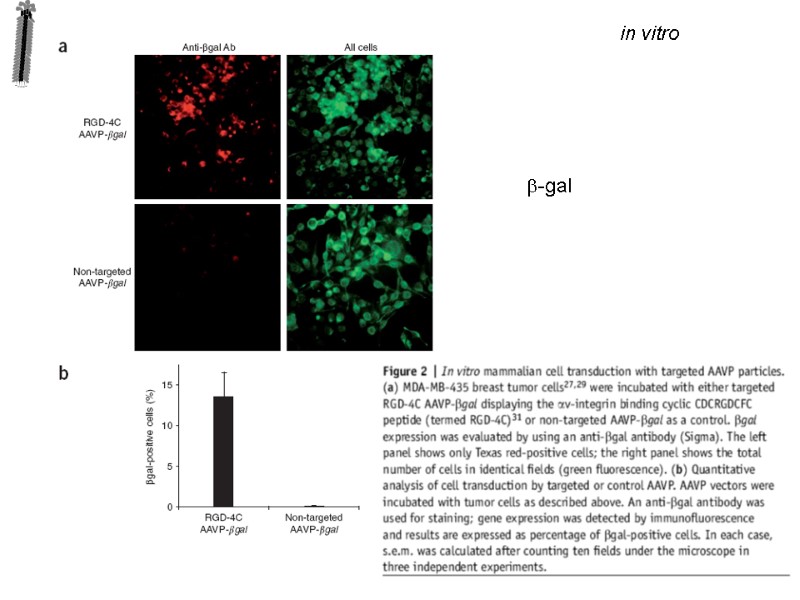
 in vitro b-gal
in vitro b-gal
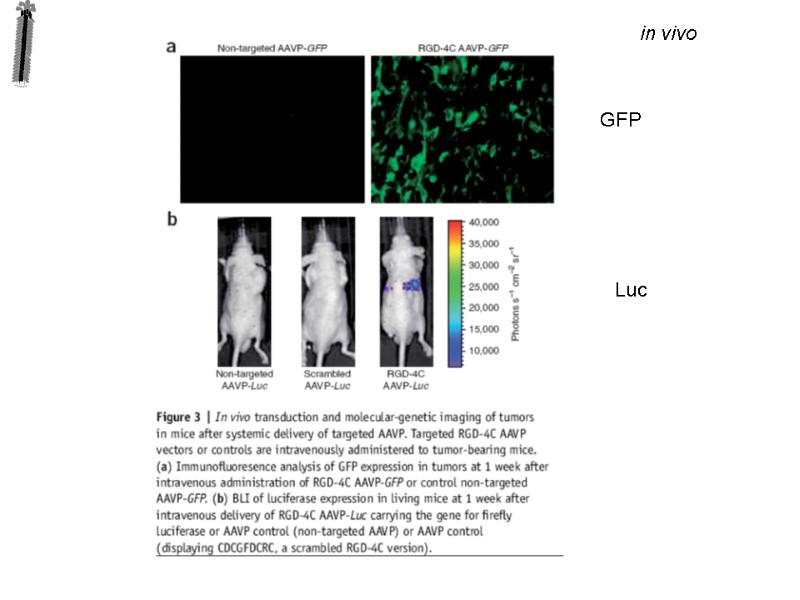
 in vivo GFP Luc
in vivo GFP Luc
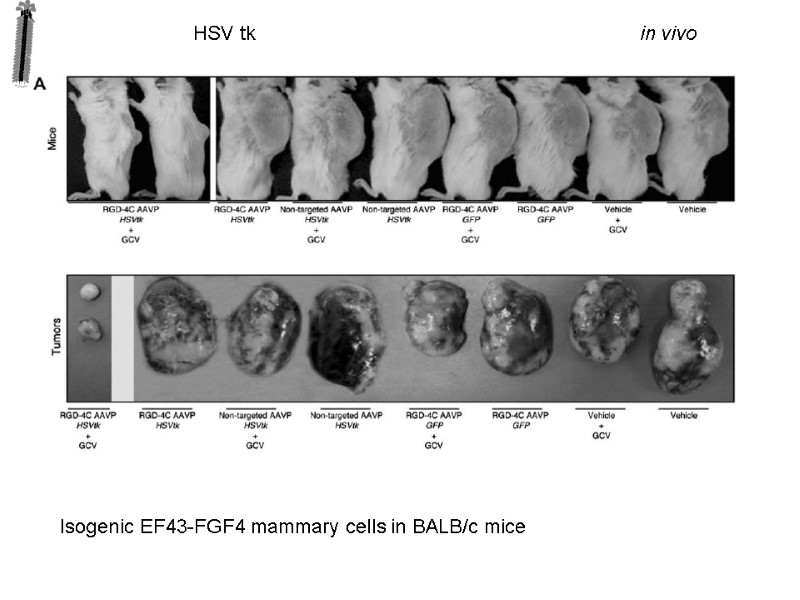
 in vivo HSV tk Isogenic EF43-FGF4 mammary cells in BALB/c mice
in vivo HSV tk Isogenic EF43-FGF4 mammary cells in BALB/c mice
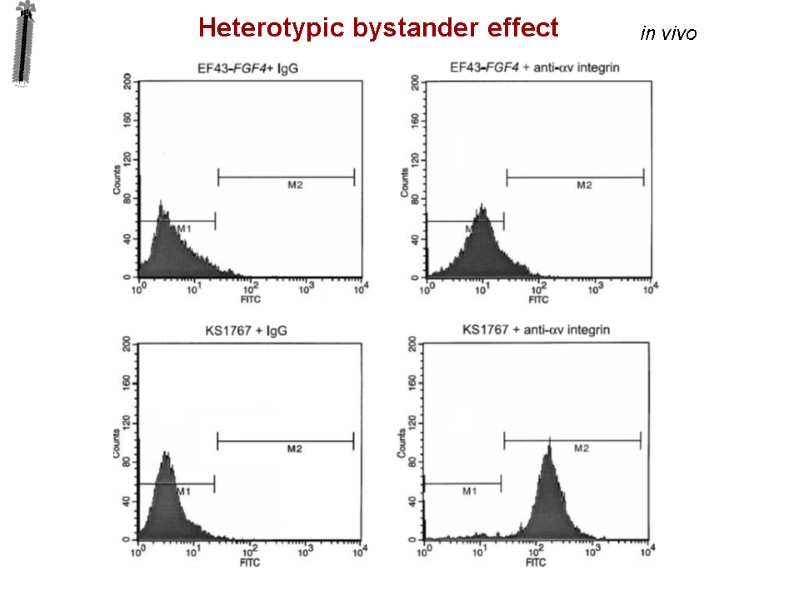
 in vivo Heterotypic bystander effect
in vivo Heterotypic bystander effect
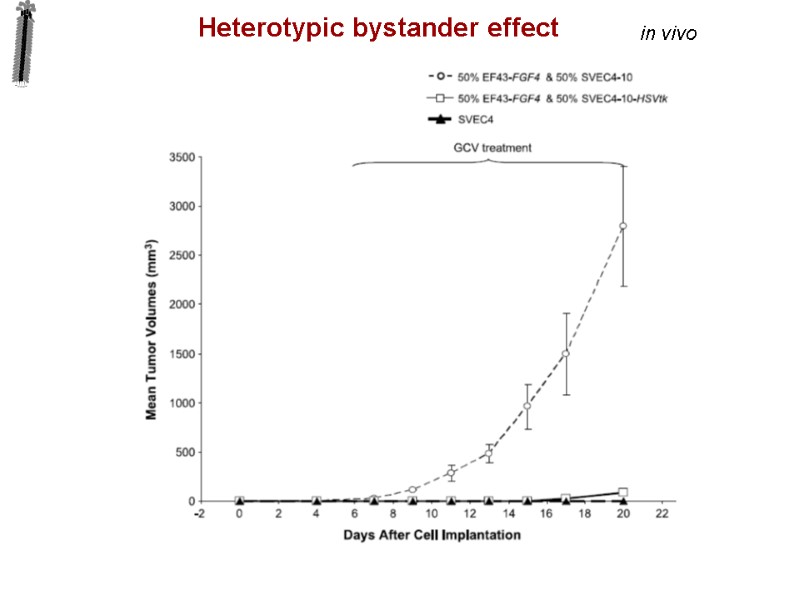
 in vivo Heterotypic bystander effect
in vivo Heterotypic bystander effect













