Лекция 5 МИГРАЦИЯ ЭНЕРГИИ ПРИ ФОТОСИНТЕЗЕ.ppt
- Количество слайдов: 30
 МИГРАЦИЯ ЭНЕРГИИ ПРИ ФОТОСИНТЕЗЕ ЭНЕРГЕТИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ В АНТЕННЫХ КОМПЛЕКСАХ И РЕАКЦИОННЫХ ЦЕНТРАХ 1. Механизм поглощения света молекулой пигмента 2. Виды дезактивации молекулы хлорофилла 3. МЕХАНИЗМЫ МИГРАЦИИ ЭНЕРГИИ МЕЖДУ ПИГМЕНТАМИ 4. ЭНЕРГЕТИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ ПИГМЕНТОВ В ССА 5. ЭНЕРГЕТИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ АНТЕННЫХ КОМПЛЕКСОВ ФС I И ФС II
МИГРАЦИЯ ЭНЕРГИИ ПРИ ФОТОСИНТЕЗЕ ЭНЕРГЕТИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ В АНТЕННЫХ КОМПЛЕКСАХ И РЕАКЦИОННЫХ ЦЕНТРАХ 1. Механизм поглощения света молекулой пигмента 2. Виды дезактивации молекулы хлорофилла 3. МЕХАНИЗМЫ МИГРАЦИИ ЭНЕРГИИ МЕЖДУ ПИГМЕНТАМИ 4. ЭНЕРГЕТИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ ПИГМЕНТОВ В ССА 5. ЭНЕРГЕТИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ АНТЕННЫХ КОМПЛЕКСОВ ФС I И ФС II
 1. МЕХАНИЗМ ПОГЛОЩЕНИЯ СВЕТА МОЛЕКУЛОЙ ПИГМЕНТА ДВА ТИПА ИЗМЕНЕНИЙ В МОЛЕКУЛЯРНОЙ СТРУКТУРЕ 1 Ø перестройка электронной структуры молекулы пигмента Ø переход в возбужденное состояние Ø возникает энергия электронного возбуждения Первичное поглощение в ССА 2 ü возбужденная молекула пигмента может отдать электрон акцептору ü происходит химическое изменение молекулы пигмента В ядре РЦ и ЭТЦ Оба изменения электронной структуры молекулы пигмента обратимы.
1. МЕХАНИЗМ ПОГЛОЩЕНИЯ СВЕТА МОЛЕКУЛОЙ ПИГМЕНТА ДВА ТИПА ИЗМЕНЕНИЙ В МОЛЕКУЛЯРНОЙ СТРУКТУРЕ 1 Ø перестройка электронной структуры молекулы пигмента Ø переход в возбужденное состояние Ø возникает энергия электронного возбуждения Первичное поглощение в ССА 2 ü возбужденная молекула пигмента может отдать электрон акцептору ü происходит химическое изменение молекулы пигмента В ядре РЦ и ЭТЦ Оба изменения электронной структуры молекулы пигмента обратимы.
 Е = Еэл + Екол + Евращ Еэл- энергия отдельных электронов и зависит от их расположения на энергетических уровнях Екол- энергия колебательного движения ядер колебания влияют на расположение электронов относительно ядра и изменяют электронную энергию молекулярной орбитали (электронный уровень энергии состоит из многих колебательных подуровней (КП). ) Евращ- энергия вращательного движения отдельных атомов или групп атомов в молекуле ΔЕ=0, 01 э. В
Е = Еэл + Екол + Евращ Еэл- энергия отдельных электронов и зависит от их расположения на энергетических уровнях Екол- энергия колебательного движения ядер колебания влияют на расположение электронов относительно ядра и изменяют электронную энергию молекулярной орбитали (электронный уровень энергии состоит из многих колебательных подуровней (КП). ) Евращ- энергия вращательного движения отдельных атомов или групп атомов в молекуле ΔЕ=0, 01 э. В
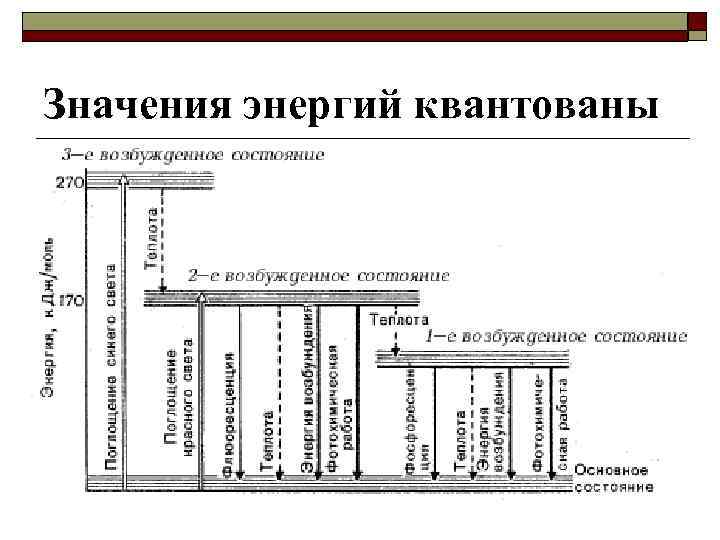 Значения энергий квантованы
Значения энергий квантованы
 В поглощении света участвуют q q Ø o o 18 -членная циклическая система двойных связей Неподеленные электроны атомов азота и кислорода Электроны идентичны, но имеют противоположно направленные спины (↑↓) Спин - момент количества движения (механический момент) Величина спина всех электронов одинакова Спин может иметь - 2 ориентации относительно внешнего магнитного поля параллельное (↑↑) и антипараллельное (↑↓) o o Электроны с противоположно направленными спинами называются спаренными. Молекула, у которой все электроны спарены не обладает магнитным моментом и называется синглетной
В поглощении света участвуют q q Ø o o 18 -членная циклическая система двойных связей Неподеленные электроны атомов азота и кислорода Электроны идентичны, но имеют противоположно направленные спины (↑↓) Спин - момент количества движения (механический момент) Величина спина всех электронов одинакова Спин может иметь - 2 ориентации относительно внешнего магнитного поля параллельное (↑↑) и антипараллельное (↑↓) o o Электроны с противоположно направленными спинами называются спаренными. Молекула, у которой все электроны спарены не обладает магнитным моментом и называется синглетной
 18 -членная циклическая система двойных связей С=С связь состоит из σ-связи и π-связи Атомные орбитали, участвующие в образовании связей В невоэбужденном состоянии - σ –и π-соединяющие орбитали, В возбужденном состоянии - σ –π-разрыхляющие орбитали. Переход электрона π →π* Чтобы перевести электрон требуется тем меньше энергии, чем больше сопряженных связей в молекуле. При наличии 7 и более сопряженных двойных связей – видимая область спектра
18 -членная циклическая система двойных связей С=С связь состоит из σ-связи и π-связи Атомные орбитали, участвующие в образовании связей В невоэбужденном состоянии - σ –и π-соединяющие орбитали, В возбужденном состоянии - σ –π-разрыхляющие орбитали. Переход электрона π →π* Чтобы перевести электрон требуется тем меньше энергии, чем больше сопряженных связей в молекуле. При наличии 7 и более сопряженных двойных связей – видимая область спектра
 Неподеленные электроны атомов азота и кислорода Атомные орбитали, не участвующие в образовании связей, т. е. не объединяющиеся в молекулярные орбитали, называют несвязывающими или n-орбиталями o При возбуждении они также могут переходить на π* Переход электрона n →π* o
Неподеленные электроны атомов азота и кислорода Атомные орбитали, не участвующие в образовании связей, т. е. не объединяющиеся в молекулярные орбитали, называют несвязывающими или n-орбиталями o При возбуждении они также могут переходить на π* Переход электрона n →π* o
 Физическая реакция поглощения света молекулой хлорофилла Μ+hν→Μ* ΔЕ=ЕΜ* - ЕΜ ΔЕ= hν = (h * с)/λ ν – частота излучения h – постоянная Планка с – скорость света λ – длина волны Переход молекулы в возбужденное состояние происходит при переходе одного любого электрона в возбужденное состояние ОДНОЭЛЕКТРОННЫЙ ПРОЦЕСС o Молекула по химической структуре, составу не отличается от невозбужденной o Имеет несколько деформированное электронное облако o Cодержит избыточные запасы энергии o Разница энергии между Μ и Μ* равна энергии поглощенного кванта света
Физическая реакция поглощения света молекулой хлорофилла Μ+hν→Μ* ΔЕ=ЕΜ* - ЕΜ ΔЕ= hν = (h * с)/λ ν – частота излучения h – постоянная Планка с – скорость света λ – длина волны Переход молекулы в возбужденное состояние происходит при переходе одного любого электрона в возбужденное состояние ОДНОЭЛЕКТРОННЫЙ ПРОЦЕСС o Молекула по химической структуре, составу не отличается от невозбужденной o Имеет несколько деформированное электронное облако o Cодержит избыточные запасы энергии o Разница энергии между Μ и Μ* равна энергии поглощенного кванта света
 МЕХАНИЗМ ПОГЛОЩЕНИЯ СВЕТА МОЛЕКУЛОЙ ПИГМЕНТА o Молекула переходит на один из возбужденных КП электронного У, принадлежащего молекулярной π* орбитали. o Переход не меняет направление электронного спина и происходит за 10 -15 с. Основное синглетное состояния (S 0) → возбужденное синглетное состояние (S 1), (S 2). o S 1 - 662 нм (1, 87 э. В) o S 2 - 430 нм (2, 88 э. В) o Время жизни (S 1 -2) весьма мало Время жизни - время, в течение которого число молекул в этом состоянии уменьшается от 100 до 37%. o
МЕХАНИЗМ ПОГЛОЩЕНИЯ СВЕТА МОЛЕКУЛОЙ ПИГМЕНТА o Молекула переходит на один из возбужденных КП электронного У, принадлежащего молекулярной π* орбитали. o Переход не меняет направление электронного спина и происходит за 10 -15 с. Основное синглетное состояния (S 0) → возбужденное синглетное состояние (S 1), (S 2). o S 1 - 662 нм (1, 87 э. В) o S 2 - 430 нм (2, 88 э. В) o Время жизни (S 1 -2) весьма мало Время жизни - время, в течение которого число молекул в этом состоянии уменьшается от 100 до 37%. o
 ВИДЫ ДЕЗАКТИВАЦИИ МОЛЕКУЛЫ ХЛОРОФИЛЛА 1. 2. 3. 4. 5. 6. 7. ВНУТРЕННЯЯ КОНВЕРСИЯ КОЛЕБАТЕЛЬНАЯ РЕЛАКСАЦИЯ ФЛУОРЕСЦЕНЦИЯ ИНТЕРКОМБИНАЦИОННАЯ КОНВЕРСИЯ ФОСФОРЕСЦЕНЦИЯ МЕЖМОЛЕКУЛЯРНЫЙ ПЕРЕНОС ИЛИ МИГРАЦИЯ ЭНЕРГИИ ФОТОХИМИЧЕСКИЕ РЕАКЦИИ
ВИДЫ ДЕЗАКТИВАЦИИ МОЛЕКУЛЫ ХЛОРОФИЛЛА 1. 2. 3. 4. 5. 6. 7. ВНУТРЕННЯЯ КОНВЕРСИЯ КОЛЕБАТЕЛЬНАЯ РЕЛАКСАЦИЯ ФЛУОРЕСЦЕНЦИЯ ИНТЕРКОМБИНАЦИОННАЯ КОНВЕРСИЯ ФОСФОРЕСЦЕНЦИЯ МЕЖМОЛЕКУЛЯРНЫЙ ПЕРЕНОС ИЛИ МИГРАЦИЯ ЭНЕРГИИ ФОТОХИМИЧЕСКИЕ РЕАКЦИИ
 ВНУТРИМОЛЕКУЛЯРНЫЕ БЕЗЫЛУЧАТЕЛЬНЫЕ ПРОЦЕССЫ КОЛЕБАТЕЛЬНАЯ РЕЛАКСАЦИЯ И ВНУТРЕННЯЯ КОНВЕРСИЯ (S 2)→ (S 1) 10 -10 -10 -12. с, (S 2)→ (S 2) 10 -9 -10 -12. с, (S 2)→ (S 1) 10 -9 -10 -12. с, (S 0)→ (S 0) 10 -9 -10 -12. с, o o o КОЛЕБАТЕЛЬНАЯ РЕЛАКСАЦИЯ - «соскальзывание» на самый низший колебательный подуровень возбужденного электронного уровня Многоступенчатый процесс Происходит до достижения самого низшего КП. При каждом переходе теряется квант энергии (разница между соседними КП, тепло, ИК) СТОЛКНОВЕНИЕ С ДРУГИМИ НЕВОЗБУЖДЕННЫМИ молекулами. которые поглощают тепловую энергию. 10 -9 -10 -12. с
ВНУТРИМОЛЕКУЛЯРНЫЕ БЕЗЫЛУЧАТЕЛЬНЫЕ ПРОЦЕССЫ КОЛЕБАТЕЛЬНАЯ РЕЛАКСАЦИЯ И ВНУТРЕННЯЯ КОНВЕРСИЯ (S 2)→ (S 1) 10 -10 -10 -12. с, (S 2)→ (S 2) 10 -9 -10 -12. с, (S 2)→ (S 1) 10 -9 -10 -12. с, (S 0)→ (S 0) 10 -9 -10 -12. с, o o o КОЛЕБАТЕЛЬНАЯ РЕЛАКСАЦИЯ - «соскальзывание» на самый низший колебательный подуровень возбужденного электронного уровня Многоступенчатый процесс Происходит до достижения самого низшего КП. При каждом переходе теряется квант энергии (разница между соседними КП, тепло, ИК) СТОЛКНОВЕНИЕ С ДРУГИМИ НЕВОЗБУЖДЕННЫМИ молекулами. которые поглощают тепловую энергию. 10 -9 -10 -12. с
 ВНУТРЕННЯЯ КОНВЕРСИЯ o o ВК- переход из состояния S 2 на колебательный подуровень S 1, имеющий ту же энергию. 10 -10 -10 -12 с Чередование безызлучательных процессов до достижения (S 0) уровня. растраченная энергия распределяется между окружающими молекулами.
ВНУТРЕННЯЯ КОНВЕРСИЯ o o ВК- переход из состояния S 2 на колебательный подуровень S 1, имеющий ту же энергию. 10 -10 -10 -12 с Чередование безызлучательных процессов до достижения (S 0) уровня. растраченная энергия распределяется между окружающими молекулами.
 ФЛУОРЕСЦЕНЦИЯ o o (S 1, 2)→ (S 0) 10 -9 -10 -5 с, Переход на один из КП состояния (S 0) Излучение кванта света На практике наблюдается почти всегда при переходе (S 1)→ (S 0) Правило Стокса Энергия высвеченного кванта меньше, чем поглощенного (разность теряется при колебательной релаксации) Длина волны флуоресценции больше, чем длина волны поглощения. o
ФЛУОРЕСЦЕНЦИЯ o o (S 1, 2)→ (S 0) 10 -9 -10 -5 с, Переход на один из КП состояния (S 0) Излучение кванта света На практике наблюдается почти всегда при переходе (S 1)→ (S 0) Правило Стокса Энергия высвеченного кванта меньше, чем поглощенного (разность теряется при колебательной релаксации) Длина волны флуоресценции больше, чем длина волны поглощения. o
 ИНТЕРКОМБИНАЦИОННАЯ КОНВЕРСИЯ Результат столкновения возбужденных молекул с другими молекулами Спин электрона, находящегося на π* орбитали переворачивается. направление спинов эл-нов становится одинаковым (параллельным) и молекула приобретает магнитный момент. Такое состояние называют ТРИПЛЕТНЫМ. Процесс маловероятен и происходит редко.
ИНТЕРКОМБИНАЦИОННАЯ КОНВЕРСИЯ Результат столкновения возбужденных молекул с другими молекулами Спин электрона, находящегося на π* орбитали переворачивается. направление спинов эл-нов становится одинаковым (параллельным) и молекула приобретает магнитный момент. Такое состояние называют ТРИПЛЕТНЫМ. Процесс маловероятен и происходит редко.
 ФОСФОРЕСЦЕНЦИЯ o o o Молекула может вернуться из Т в S 0 только, если спин электрона снова перевернется. Поворот спина маловероятен Время жизни Т-состояния больше чем у возбужденного S-состояния (10 -5 -10 -3 с, иногда 10 с) Переход Т → (S 0), с излучением кванта света Энергия излученного кванта меньше, чем поглощенного, и меньше чем флуоресценции. Растрата энергии в ходе КР.
ФОСФОРЕСЦЕНЦИЯ o o o Молекула может вернуться из Т в S 0 только, если спин электрона снова перевернется. Поворот спина маловероятен Время жизни Т-состояния больше чем у возбужденного S-состояния (10 -5 -10 -3 с, иногда 10 с) Переход Т → (S 0), с излучением кванта света Энергия излученного кванта меньше, чем поглощенного, и меньше чем флуоресценции. Растрата энергии в ходе КР.
 МЕЖМОЛЕКУЛЯРНЫЙ ПЕРЕНОС ИЛИ МИГРАЦИЯ ЭНЕРГИИ Д(S 1) + А(S 0)→ Д(S 0) + А(S 1) Передача энергии другой молекуле того же или иного вещества, которая находится в основном состоянии. o o o o Молекула-акцептор переходит в возбужденное состояние. Электрон с разрыхляющей орбитали молекулы донора (Д) переходит на такую же орбиталь молекулы акцептора (А) Переход уравновешивается переходом другого электрона со связывающей орбитали молекулы А на такую же орбиталь молекулы Д Суммарный спин системы при этом сохраняется. Молекулы Д и А находятся очень близко друг к другу и ∆Е Д больше или равна ∆Е А. Скорость переноса - 10 -12 -10 -15 с
МЕЖМОЛЕКУЛЯРНЫЙ ПЕРЕНОС ИЛИ МИГРАЦИЯ ЭНЕРГИИ Д(S 1) + А(S 0)→ Д(S 0) + А(S 1) Передача энергии другой молекуле того же или иного вещества, которая находится в основном состоянии. o o o o Молекула-акцептор переходит в возбужденное состояние. Электрон с разрыхляющей орбитали молекулы донора (Д) переходит на такую же орбиталь молекулы акцептора (А) Переход уравновешивается переходом другого электрона со связывающей орбитали молекулы А на такую же орбиталь молекулы Д Суммарный спин системы при этом сохраняется. Молекулы Д и А находятся очень близко друг к другу и ∆Е Д больше или равна ∆Е А. Скорость переноса - 10 -12 -10 -15 с
 ФОТОХИМИЧЕСКИЕ РЕАКЦИИ o выполнение химической работы. o Хлорофилл Донирование (отдача электрона на окисленную форму окислительно-восстановительной системы). o В возбужденном состоянии хлорофилл является гораздо большим восстановителем, чем в основном. o Окислительно-восстановительные превращения хлорофилла определяют его участие в первичных фотохимических реакциях.
ФОТОХИМИЧЕСКИЕ РЕАКЦИИ o выполнение химической работы. o Хлорофилл Донирование (отдача электрона на окисленную форму окислительно-восстановительной системы). o В возбужденном состоянии хлорофилл является гораздо большим восстановителем, чем в основном. o Окислительно-восстановительные превращения хлорофилла определяют его участие в первичных фотохимических реакциях.
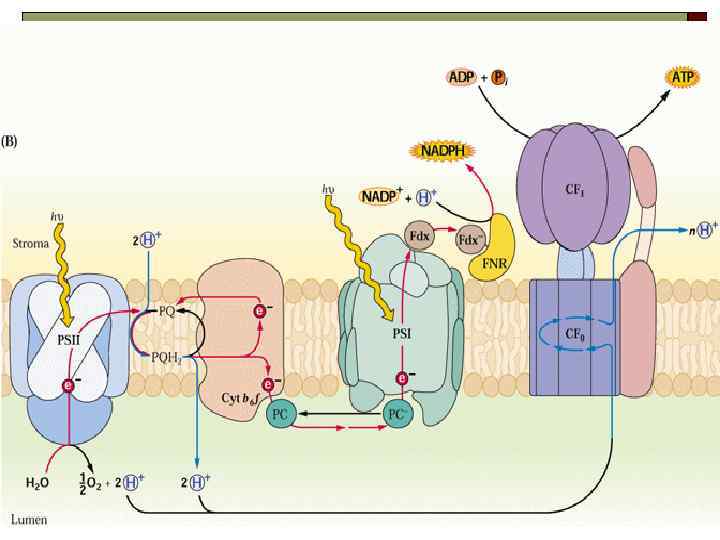
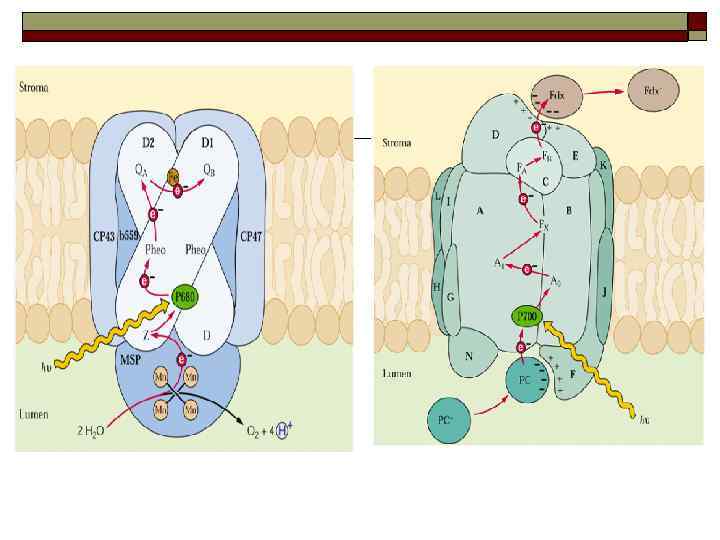
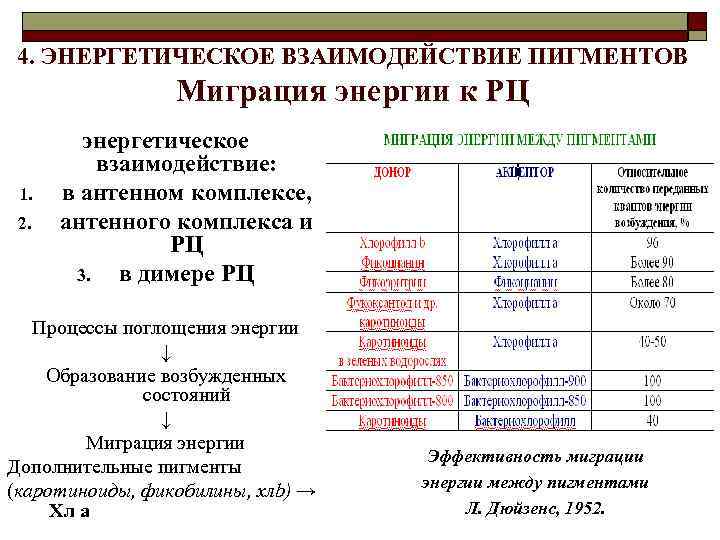 4. ЭНЕРГЕТИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ ПИГМЕНТОВ Миграция энергии к РЦ 1. 2. энергетическое взаимодействие: в антенном комплексе, антенного комплекса и РЦ 3. в димере РЦ Процессы поглощения энергии ↓ Образование возбужденных состояний ↓ Миграция энергии Дополнительные пигменты (каротиноиды, фикобилины, хлb) → Хл а Эффективность миграции энергии между пигментами Л. Дюйзенс, 1952.
4. ЭНЕРГЕТИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ ПИГМЕНТОВ Миграция энергии к РЦ 1. 2. энергетическое взаимодействие: в антенном комплексе, антенного комплекса и РЦ 3. в димере РЦ Процессы поглощения энергии ↓ Образование возбужденных состояний ↓ Миграция энергии Дополнительные пигменты (каротиноиды, фикобилины, хлb) → Хл а Эффективность миграции энергии между пигментами Л. Дюйзенс, 1952.
 1. Индуктивный резонанс (Т. Ферстер 1948) Электрон в возбужденном состоянии осциллирующий диполь, создающий переменное электрическое поле o o o Вызывает осцилляции в соседней молекуле Без переноса заряда Без предварительной флуоресценции Эффективность переноса энергии в ССК: o положение энергетических уровней o время жизни o «геометрия» - расстояния и ориентации o Скорость переноса – 10 -9 с
1. Индуктивный резонанс (Т. Ферстер 1948) Электрон в возбужденном состоянии осциллирующий диполь, создающий переменное электрическое поле o o o Вызывает осцилляции в соседней молекуле Без переноса заряда Без предварительной флуоресценции Эффективность переноса энергии в ССК: o положение энергетических уровней o время жизни o «геометрия» - расстояния и ориентации o Скорость переноса – 10 -9 с
 2. ЭКСИТОННОЕ ВЗАИМОДЕЙСТВИЕ (А. Френкель, 1931) По мере увеличения плотности и упорядоченности пигментов система приближается по характеру к кристаллической решетке q Коллективное возбуждение всего комплекса пигментов q Наблюдается при очень плотной упаковке пигментов q Пигменты одного типа q Ориентированы определенным образом Скорость переноса выше – 10 -12 - 10 -15 с q
2. ЭКСИТОННОЕ ВЗАИМОДЕЙСТВИЕ (А. Френкель, 1931) По мере увеличения плотности и упорядоченности пигментов система приближается по характеру к кристаллической решетке q Коллективное возбуждение всего комплекса пигментов q Наблюдается при очень плотной упаковке пигментов q Пигменты одного типа q Ориентированы определенным образом Скорость переноса выше – 10 -12 - 10 -15 с q
 3. Полупроводниковый механизм В центре с пониженной энергией ионизации может произойти перенос электрона q Движение электронов «в зоне проводимости» белка q Наблюдается в системах с определенной периодичностью расположения атомов белка q Если при этом сливаются первые возбужденные орбиты отдельных атомов q ЭТЦ
3. Полупроводниковый механизм В центре с пониженной энергией ионизации может произойти перенос электрона q Движение электронов «в зоне проводимости» белка q Наблюдается в системах с определенной периодичностью расположения атомов белка q Если при этом сливаются первые возбужденные орбиты отдельных атомов q ЭТЦ
 4. ВЗАИМОДЕЙСТВИЕ ПИГМЕНТОВ В АНТЕННОМ КОМПЛЕКСЕ Миграция энергии в комплексе различных пигментов идет от периферических молекул пигментов в антенном комплексе в сторону пигментов с более низким возбужденным уровнем E = ħν = ħc/λ ↓ Поток энергии направлен в сторону более длинноволновых форм пигментов Хл b 650…→ …Хл а 670 …→ …Хл а 683 …→ …Хл b 650 → …П 700 o взаимодействие пигментов с различными аминокислотами белка → большой набор различных спектральных форм → широкий и сильно перекрывающийся спектр поглощения. o В итоге энергия достигает РЦ, пигмент которого имеет наиболее длинноволновой максимум – наименьшую энергию электронного возбуждения. Среднее время перехода энергии возбуждения пигмент-пигмент - 10 -12 – 10 -11 с. o
4. ВЗАИМОДЕЙСТВИЕ ПИГМЕНТОВ В АНТЕННОМ КОМПЛЕКСЕ Миграция энергии в комплексе различных пигментов идет от периферических молекул пигментов в антенном комплексе в сторону пигментов с более низким возбужденным уровнем E = ħν = ħc/λ ↓ Поток энергии направлен в сторону более длинноволновых форм пигментов Хл b 650…→ …Хл а 670 …→ …Хл а 683 …→ …Хл b 650 → …П 700 o взаимодействие пигментов с различными аминокислотами белка → большой набор различных спектральных форм → широкий и сильно перекрывающийся спектр поглощения. o В итоге энергия достигает РЦ, пигмент которого имеет наиболее длинноволновой максимум – наименьшую энергию электронного возбуждения. Среднее время перехода энергии возбуждения пигмент-пигмент - 10 -12 – 10 -11 с. o
 4. ВЗАИМОДЕЙСТВИЕ ПИГМЕНТОВ В АНТЕННОМ КОМПЛЕКСЕ Пигменты o o o o Жестко организованы Определенным образом ориентированы (не очень строго: дипольные моменты не строго параллельны) Мономер ССК II содержит 7 молекул хлорофилла а, 5 молекулы хлорофилла b 2 молекулы лютеина. пигмент-пигментное расстояние = 0, 9— 1, 4 нм (метод электронной кристаллографии). значительная сила экситонного сопряжения между пигментами
4. ВЗАИМОДЕЙСТВИЕ ПИГМЕНТОВ В АНТЕННОМ КОМПЛЕКСЕ Пигменты o o o o Жестко организованы Определенным образом ориентированы (не очень строго: дипольные моменты не строго параллельны) Мономер ССК II содержит 7 молекул хлорофилла а, 5 молекулы хлорофилла b 2 молекулы лютеина. пигмент-пигментное расстояние = 0, 9— 1, 4 нм (метод электронной кристаллографии). значительная сила экситонного сопряжения между пигментами
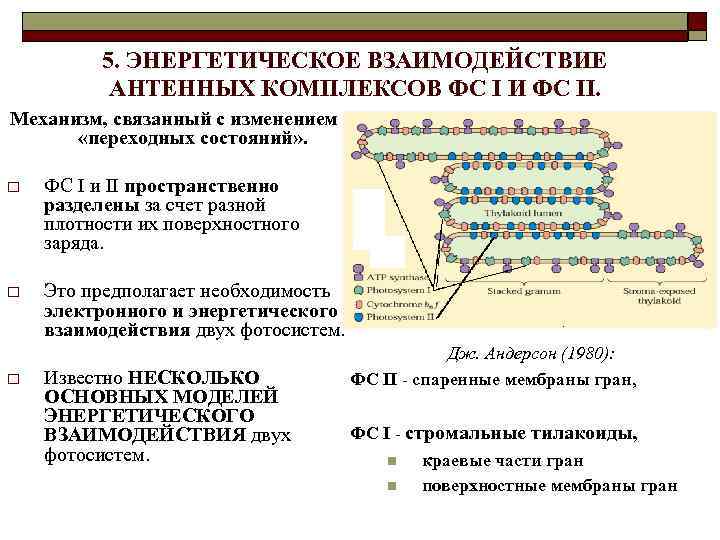 5. ЭНЕРГЕТИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ АНТЕННЫХ КОМПЛЕКСОВ ФС I И ФС II. Механизм, связанный с изменением «переходных состояний» . o ФС I и II пространственно разделены за счет разной плотности их поверхностного заряда. o Это предполагает необходимость электронного и энергетического взаимодействия двух фотосистем. o Известно НЕСКОЛЬКО ОСНОВНЫХ МОДЕЛЕЙ ЭНЕРГЕТИЧЕСКОГО ВЗАИМОДЕЙСТВИЯ двух фотосистем. Дж. Андерсон (1980): ФС II - спаренные мембраны гран, ФС I - стромальные тилакоиды, n краевые части гран n поверхностные мембраны гран
5. ЭНЕРГЕТИЧЕСКОЕ ВЗАИМОДЕЙСТВИЕ АНТЕННЫХ КОМПЛЕКСОВ ФС I И ФС II. Механизм, связанный с изменением «переходных состояний» . o ФС I и II пространственно разделены за счет разной плотности их поверхностного заряда. o Это предполагает необходимость электронного и энергетического взаимодействия двух фотосистем. o Известно НЕСКОЛЬКО ОСНОВНЫХ МОДЕЛЕЙ ЭНЕРГЕТИЧЕСКОГО ВЗАИМОДЕЙСТВИЯ двух фотосистем. Дж. Андерсон (1980): ФС II - спаренные мембраны гран, ФС I - стромальные тилакоиды, n краевые части гран n поверхностные мембраны гран
 МОДЕЛИ ЭНЕРГЕТИЧЕСКОГО ВЗАИМОДЕЙСТВИЯ ДВУХ ФОТОСИСТЕМ 1. q q Теория «пакетов» (N. Boardman, J. Anderson, 1973) Каждый из двух РЦ имеет свой собственный ССК Оба РЦ изолированы друг от друга и энергетически не взаимодействуют. 2. Теория «перелива» (spilover) o o o Два типа РЦ имеют единую светособирающую антенну Конкурируют за энергию возбуждения. Происходит перелив энергии к I или I I 3. Модель Батлера (W. Batler, 1974). o o Связана с механизмом «spilover» : каждый из двух РЦ имеет небольшие «фокусирующие» антенны, структурно связанные с общей светособирающей антенной. Специальный регуляторный механизм, обеспечивающий приток энергии к РЦ I или II.
МОДЕЛИ ЭНЕРГЕТИЧЕСКОГО ВЗАИМОДЕЙСТВИЯ ДВУХ ФОТОСИСТЕМ 1. q q Теория «пакетов» (N. Boardman, J. Anderson, 1973) Каждый из двух РЦ имеет свой собственный ССК Оба РЦ изолированы друг от друга и энергетически не взаимодействуют. 2. Теория «перелива» (spilover) o o o Два типа РЦ имеют единую светособирающую антенну Конкурируют за энергию возбуждения. Происходит перелив энергии к I или I I 3. Модель Батлера (W. Batler, 1974). o o Связана с механизмом «spilover» : каждый из двух РЦ имеет небольшие «фокусирующие» антенны, структурно связанные с общей светособирающей антенной. Специальный регуляторный механизм, обеспечивающий приток энергии к РЦ I или II.
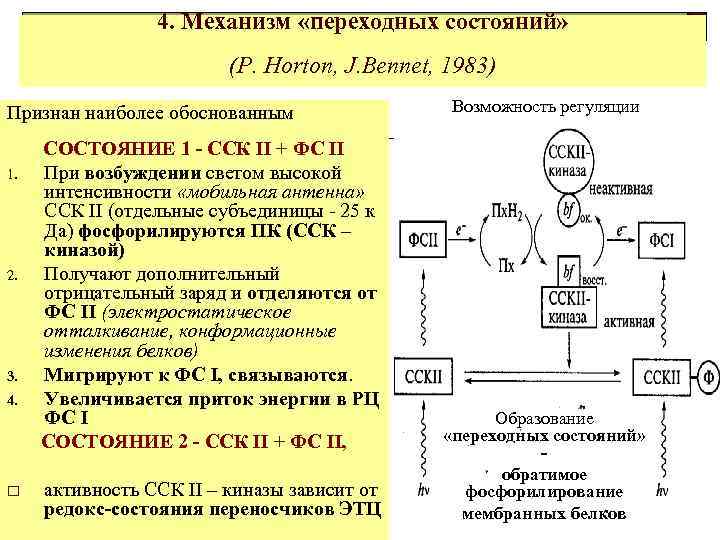 4. Механизм «переходных состояний» (P. Horton, J. Bennet, 1983) Признан наиболее обоснованным Возможность регуляции Образование «переходных - ССК II + ФС II СОСТОЯНИЕ 1 состояний» -обратимое фосфорилирование мембранных белков 1. 1. 2. 2. 3. 4. 3. 4. o o o При возбуждении светом высокой интенсивности «мобильная. ФС II антенна» СОСТОЯНИЕ 1 - ССК II + ССК II (отдельные субъединицы - 25 к При возбуждении светом высокой Да) фосфорилируются ПК (ССК II интенсивности «мобильная антенна» ССК – киназой)субъединицы - 25 к Да) (отдельные фосфорилируются ПК (ССК – киназой) Получают дополнительныйи отделяются от отрицательный заряд и отделяются от ФС II (электростатическое отталкивание, конформационные изменения отталкивание, конформационные белков) изменения белков) Мигрируют к ФС I, связываются. Увеличивается к ФС I, связываются. Мигрируют приток энергии в РЦ ФС I СОСТОЯНИЕ - ССК II Увеличивается 2 приток + ФС II, в РЦ энергии ФС I активность ССК II – киназы зависит от редокс. СОСТОЯНИЕ 2 - ССК II + ФС II, состояния переносчиков ЭТЦ Возможность регуляции активность ССК II – киназы зависит от редокс-состояния переносчиков ЭТЦ Образование «переходных состояний» обратимое фосфорилирование мембранных белков
4. Механизм «переходных состояний» (P. Horton, J. Bennet, 1983) Признан наиболее обоснованным Возможность регуляции Образование «переходных - ССК II + ФС II СОСТОЯНИЕ 1 состояний» -обратимое фосфорилирование мембранных белков 1. 1. 2. 2. 3. 4. 3. 4. o o o При возбуждении светом высокой интенсивности «мобильная. ФС II антенна» СОСТОЯНИЕ 1 - ССК II + ССК II (отдельные субъединицы - 25 к При возбуждении светом высокой Да) фосфорилируются ПК (ССК II интенсивности «мобильная антенна» ССК – киназой)субъединицы - 25 к Да) (отдельные фосфорилируются ПК (ССК – киназой) Получают дополнительныйи отделяются от отрицательный заряд и отделяются от ФС II (электростатическое отталкивание, конформационные изменения отталкивание, конформационные белков) изменения белков) Мигрируют к ФС I, связываются. Увеличивается к ФС I, связываются. Мигрируют приток энергии в РЦ ФС I СОСТОЯНИЕ - ССК II Увеличивается 2 приток + ФС II, в РЦ энергии ФС I активность ССК II – киназы зависит от редокс. СОСТОЯНИЕ 2 - ССК II + ФС II, состояния переносчиков ЭТЦ Возможность регуляции активность ССК II – киназы зависит от редокс-состояния переносчиков ЭТЦ Образование «переходных состояний» обратимое фосфорилирование мембранных белков
 o Миграция энергии возбуждения в массе пигментов внешних и внутренних антенных комплексов ФС I и ФС II завершается процессом «захвата» энергии реакционными центрами, где происходит фотохимическая реакция разделения зарядов o энергия электронного возбуждения преобразуется в химическую форму энергии. o Эффективность миграции энергии к РЦ очень высока (вероятность потери энергии - не более 1015%). o Пигменты ССА поглощают фотоны большей энергии (меньшей длины волны), чем пигменты РЦ. Поэтому, как только энергия достигла Р 700 или Р 680 обратного переноса энергии уже не происходит и происходит фотохимические реакции.
o Миграция энергии возбуждения в массе пигментов внешних и внутренних антенных комплексов ФС I и ФС II завершается процессом «захвата» энергии реакционными центрами, где происходит фотохимическая реакция разделения зарядов o энергия электронного возбуждения преобразуется в химическую форму энергии. o Эффективность миграции энергии к РЦ очень высока (вероятность потери энергии - не более 1015%). o Пигменты ССА поглощают фотоны большей энергии (меньшей длины волны), чем пигменты РЦ. Поэтому, как только энергия достигла Р 700 или Р 680 обратного переноса энергии уже не происходит и происходит фотохимические реакции.
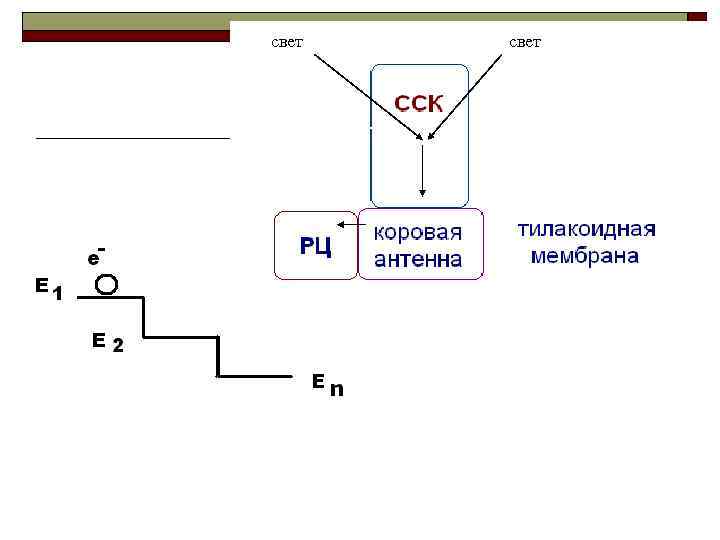 свет
свет


