 МГУ имени М. В. Ломоносова Химический факультет Кафедра химической энзимологии ГЛЮКОЗОКСИДАЗА Подготовил: студент 508 гр. Андреев Е. А. Москва-2011
МГУ имени М. В. Ломоносова Химический факультет Кафедра химической энзимологии ГЛЮКОЗОКСИДАЗА Подготовил: студент 508 гр. Андреев Е. А. Москва-2011
![Общие сведения о ферменте[1] Фермент глюкозооксидаза (β-D-Glucose: oxygen 1 -oxidoreductase, GOD/GOx, EC 1. 1. Общие сведения о ферменте[1] Фермент глюкозооксидаза (β-D-Glucose: oxygen 1 -oxidoreductase, GOD/GOx, EC 1. 1.](https://present5.com/presentation/5324338_23289756/image-2.jpg) Общие сведения о ферменте[1] Фермент глюкозооксидаза (β-D-Glucose: oxygen 1 -oxidoreductase, GOD/GOx, EC 1. 1. 3. 4) – впервые был открыт Мюллером в 1928 году Реакция: β-D-Glc + O 2 → δ-glucono-1, 5 -lactone + H 2 O 2 Источники: • • • Красные водоросли Цитрусовые Насекомые Бактерии Плесневые грибы 1. Glucose oxidase: an ideal enzyme, Biosensors&Bioelectronics, 1992, V. 7, pp 165 -185
Общие сведения о ферменте[1] Фермент глюкозооксидаза (β-D-Glucose: oxygen 1 -oxidoreductase, GOD/GOx, EC 1. 1. 3. 4) – впервые был открыт Мюллером в 1928 году Реакция: β-D-Glc + O 2 → δ-glucono-1, 5 -lactone + H 2 O 2 Источники: • • • Красные водоросли Цитрусовые Насекомые Бактерии Плесневые грибы 1. Glucose oxidase: an ideal enzyme, Biosensors&Bioelectronics, 1992, V. 7, pp 165 -185
![Структурные особенности GOD[2, 3] I˚ структура - 583 АК Состоит из двух субъединиц ≈80 Структурные особенности GOD[2, 3] I˚ структура - 583 АК Состоит из двух субъединиц ≈80](https://present5.com/presentation/5324338_23289756/image-3.jpg) Структурные особенности GOD[2, 3] I˚ структура - 583 АК Состоит из двух субъединиц ≈80 к. Да, 2 молекулы FAD и гликозилированные участки (11 -16% масс. ) Субстрат фиксируется 9 водородными связями и взаимодействиями гидрофобных участков 2. Glucose oxidase from Aspergillus niger: cloning, gene sequense, secretion from Saccharomyces cerevisiea and kinetic analysis from yeast-derived enzime, Journal of Biological Chemistry, 1990, V. 265, № 7, pp 3793 -3802 3. Aspects of the mechanism of catalysis of glucose oxidase: a docking, molecular mechanics and quantum chemical study. Journal of Computer-Aided Molecular Design , 1998, V. 12, № 5, pp 425 -440
Структурные особенности GOD[2, 3] I˚ структура - 583 АК Состоит из двух субъединиц ≈80 к. Да, 2 молекулы FAD и гликозилированные участки (11 -16% масс. ) Субстрат фиксируется 9 водородными связями и взаимодействиями гидрофобных участков 2. Glucose oxidase from Aspergillus niger: cloning, gene sequense, secretion from Saccharomyces cerevisiea and kinetic analysis from yeast-derived enzime, Journal of Biological Chemistry, 1990, V. 265, № 7, pp 3793 -3802 3. Aspects of the mechanism of catalysis of glucose oxidase: a docking, molecular mechanics and quantum chemical study. Journal of Computer-Aided Molecular Design , 1998, V. 12, № 5, pp 425 -440
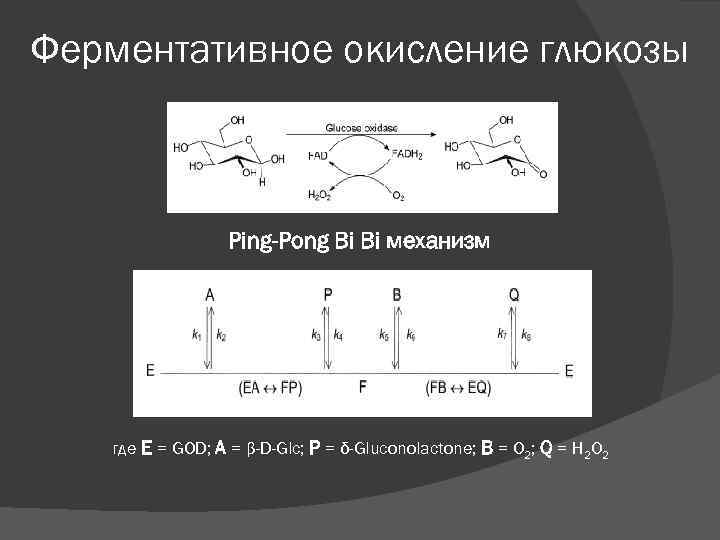 Ферментативное окисление глюкозы Ping-Pong Bi Bi механизм где E = GOD; A = β-D-Glc; P = δ-Gluconolactone; B = O 2; Q = H 2 O 2
Ферментативное окисление глюкозы Ping-Pong Bi Bi механизм где E = GOD; A = β-D-Glc; P = δ-Gluconolactone; B = O 2; Q = H 2 O 2
![Механизм окисления глюкозы[4] Восстановительная стадия 4. Glucose oxidase from Aspergillus niger: mechanism of action Механизм окисления глюкозы[4] Восстановительная стадия 4. Glucose oxidase from Aspergillus niger: mechanism of action](https://present5.com/presentation/5324338_23289756/image-5.jpg) Механизм окисления глюкозы[4] Восстановительная стадия 4. Glucose oxidase from Aspergillus niger: mechanism of action with molecular oxygen, quinones and one-electrone acceptors , The International Journal of Biochemistry & Cell Biology, 2005, V. 37, pp 731 -740
Механизм окисления глюкозы[4] Восстановительная стадия 4. Glucose oxidase from Aspergillus niger: mechanism of action with molecular oxygen, quinones and one-electrone acceptors , The International Journal of Biochemistry & Cell Biology, 2005, V. 37, pp 731 -740
![Механизм окисления глюкозы[3, 4] Окислительная стадия O 2 в основном состоянии парамагнетик и не Механизм окисления глюкозы[3, 4] Окислительная стадия O 2 в основном состоянии парамагнетик и не](https://present5.com/presentation/5324338_23289756/image-6.jpg) Механизм окисления глюкозы[3, 4] Окислительная стадия O 2 в основном состоянии парамагнетик и не взаимодействует с диамагнитным окружением активного центра GOD В ходе окислительной полуреакции образуются O 2 и FADH •
Механизм окисления глюкозы[3, 4] Окислительная стадия O 2 в основном состоянии парамагнетик и не взаимодействует с диамагнитным окружением активного центра GOD В ходе окислительной полуреакции образуются O 2 и FADH •
![Субстратная специфичность GOD[4] Субстратная специфичность GOD[4]](https://present5.com/presentation/5324338_23289756/image-7.jpg) Субстратная специфичность GOD[4]
Субстратная специфичность GOD[4]