27_Межмолекулярное взаимодействие.ppt
- Количество слайдов: 15

Межмолекулярное взаимодействие Лекция 27 по курсу «Общая химия»

Слабее, чем химическая связь Ион–диполь Ион–неполярная молекула Водородная связь Диполь–неполярная молекула Диполь–диполь 2 неполярных молекулы
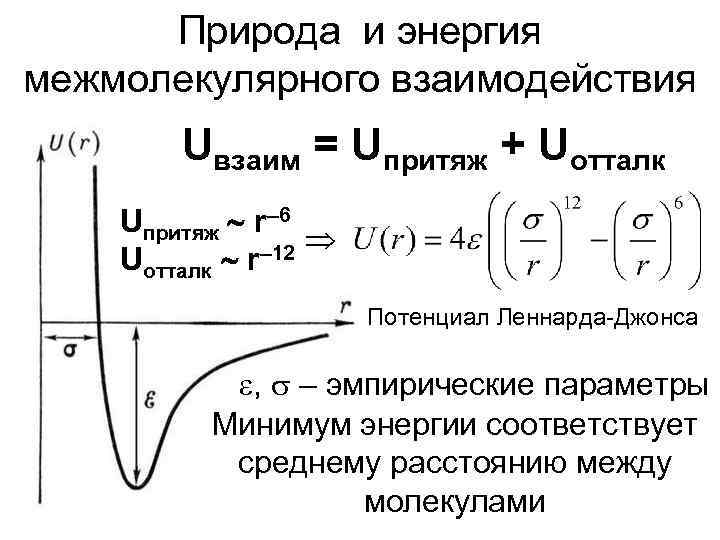
Природа и энергия межмолекулярного взаимодействия Uвзаим = Uпритяж + Uотталк Uпритяж r– 6 – 12 Uотталк r Потенциал Леннарда-Джонса , – эмпирические параметры Минимум энергии соответствует среднему расстоянию между молекулами
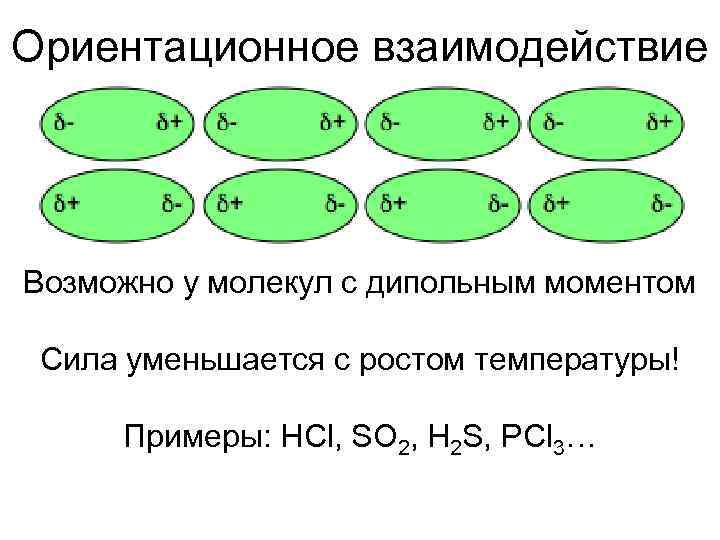
Ориентационное взаимодействие Возможно у молекул с дипольным моментом Сила уменьшается с ростом температуры! Примеры: HCl, SO 2, H 2 S, PCl 3…
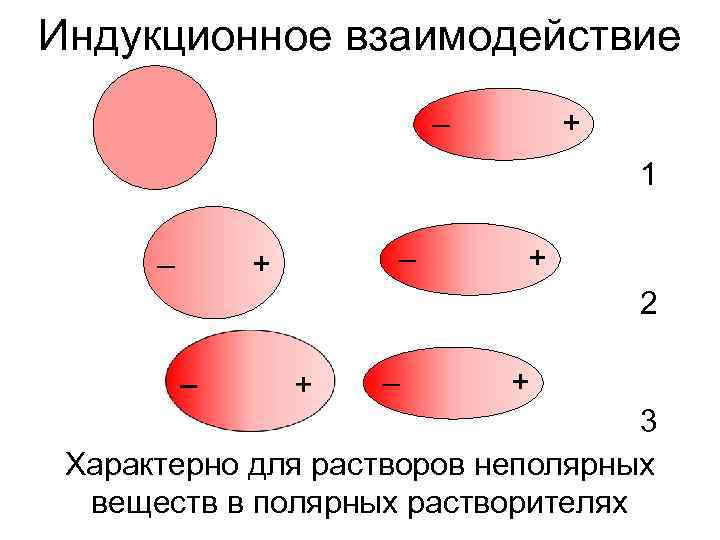
Индукционное взаимодействие – + 1 – + 2 – + 3 Характерно для растворов неполярных веществ в полярных растворителях

Дисперсионное взаимодействие Мгновенные диполи – + – 1 + 2 – + 3 Характерно для неполярных веществ Сила пропорциональна поляризуемости

«Полуковалентное» межмолекулярное взаимодействие Взаимодействие между молекулами Br 2, I 2 сильнее, чем рассчитанное дисперсионное Причина: . . : I. . . I : : I. . . I : . . Дополнительное «дативное» взаимодействие (по типу донорно-акцепторного)

Природа водородной связи Радиусы Н: Орбитальный: 78 пм Ковалентный: 30 пм Вандерваальсов: 120 пм Катион H+: 10– 5 пм Причина? Катион – ядро без электронной оболочки! В соединениях с электроотрицательными элементами атом Н – “почти катион” Проникает в чужую электронную оболочку

Водородная связь: факты Энергия: от 5 -10% до 30% ковалентной связи Длина: в 1. 5– 2. 5 раза больше ковалентной Геометрия: линейная

Водородная связь: требования к строению частиц X–H…Y Атом Х Атом Y Высокая ЭО (F, O, N, Высокая ЭО или реже Cl или Br) или отрицательный заряд атом связан с другими ЭО атомами/группами Элемент II периода Хотя бы одна неподеленная пара

Водородная связь и свойства вещества 1. 2. 3. 4. Пористая ажурная структура Аномально высокие Тпл и Ткип Повышенная теплоемкость Гидрофильность

Внутримолекулярная водородная связь Ацетилсалициловая кислота (действующее начало аспирина) орто-Нитрофенол Последствия? Ослабляется ассоциация молекул о-Нитрофенол перегоняется с водяным паром

Водородные связи в белках C=O…H–N Фиксируют вторичную структуру белка

Водородные связи в углеводах Целлюлоза
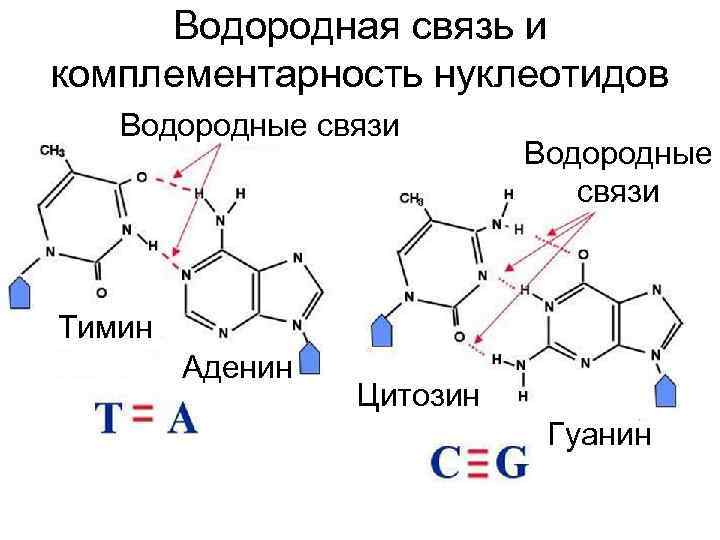
Водородная связь и комплементарность нуклеотидов Водородные связи Тимин Аденин Цитозин Гуанин
27_Межмолекулярное взаимодействие.ppt