международные стандарты.ppt
- Количество слайдов: 36
 Международные стандарты по НАДЛЕЖАЩЕЙ ПРАКТИКЕ
Международные стандарты по НАДЛЕЖАЩЕЙ ПРАКТИКЕ
 История Ветхий Завет, в 1 главе Книги пророка Даниила- первое открытое сравнительное исследование ¡ Сравнительное исследование 6 методов лечения цинги (Джеймс Линд) ¡ При Николае I, по заказу Министерства внутренних Дел в Санкт-Петербурге: первое в мире проспективное исследование с применением плацебо: гомеопатическое лечение vs аллопатическое лечение vs без лечения ¡
История Ветхий Завет, в 1 главе Книги пророка Даниила- первое открытое сравнительное исследование ¡ Сравнительное исследование 6 методов лечения цинги (Джеймс Линд) ¡ При Николае I, по заказу Министерства внутренних Дел в Санкт-Петербурге: первое в мире проспективное исследование с применением плацебо: гомеопатическое лечение vs аллопатическое лечение vs без лечения ¡
 История ¡ ¡ ¡ Конец 19 - начало 20 века: Подлог, подделка торговых марок, загрязненные продукты и препараты 1932 -1972 - Tuskegee Syphilis Study в США (200 больных без лечения!) 1937(США) Раствор сульфаниламида в диэтиленгликоле (107 детей умерли!) Германия период нацизма- исследования на узниках концлагерей США, 50 -е годы исследования на заключенных с обещанием досрочного освобождения США, Европа, 50 -60 -е годы- исследования на недееспособных пациентах (пожилые в приютах, психически больные)
История ¡ ¡ ¡ Конец 19 - начало 20 века: Подлог, подделка торговых марок, загрязненные продукты и препараты 1932 -1972 - Tuskegee Syphilis Study в США (200 больных без лечения!) 1937(США) Раствор сульфаниламида в диэтиленгликоле (107 детей умерли!) Германия период нацизма- исследования на узниках концлагерей США, 50 -е годы исследования на заключенных с обещанием досрочного освобождения США, Европа, 50 -60 -е годы- исследования на недееспособных пациентах (пожилые в приютах, психически больные)
 История ¡ ¡ ¡ 1914 г. – Верховный Суд США поддержал определение о том, что хирург, выполняющий, операцию без согласия больного совершает «физическое насилие, по которому он обязан возместить ущерб» В 1938 г. в США был принят Закон о пищевых продуктах, лекарствах и косметических средствах (FDA) В 1962 г. , в США был принят закон, определяющий правила проведения медицинских экспериментов по исследованию лекарственных средств- Drug amendment act (DAA).
История ¡ ¡ ¡ 1914 г. – Верховный Суд США поддержал определение о том, что хирург, выполняющий, операцию без согласия больного совершает «физическое насилие, по которому он обязан возместить ущерб» В 1938 г. в США был принят Закон о пищевых продуктах, лекарствах и косметических средствах (FDA) В 1962 г. , в США был принят закон, определяющий правила проведения медицинских экспериментов по исследованию лекарственных средств- Drug amendment act (DAA).
 Стандарты качества клинических исследований ¡ ¡ ¡ GCP – “Good Clinical Practice”, Надлежащая клиническая практика GMP – “Good Manufactured Practice”производство GLP – “Good Laboratory Practice”, Надлежащая лабораторная практика GDP - Надлежащая дистрибьюторская практика GRP - регистрация GPP – розничная торговля
Стандарты качества клинических исследований ¡ ¡ ¡ GCP – “Good Clinical Practice”, Надлежащая клиническая практика GMP – “Good Manufactured Practice”производство GLP – “Good Laboratory Practice”, Надлежащая лабораторная практика GDP - Надлежащая дистрибьюторская практика GRP - регистрация GPP – розничная торговля
 Стандарт GCP - международный стандарт этических норм и качества научных исследований, описывающий правила разработки, проведения, ведения документации и отчётности об исследованиях, которые подразумевают участие человека в качестве испытуемого (клинические исследования).
Стандарт GCP - международный стандарт этических норм и качества научных исследований, описывающий правила разработки, проведения, ведения документации и отчётности об исследованиях, которые подразумевают участие человека в качестве испытуемого (клинические исследования).
 Соответствие исследования этому стандарту говорит о публичном соблюдении: прав участников исследования ¡ правил по обеспечению их безопасности ¡ стремления к ненанесению вреда ¡ требований к достоверности исследований ¡
Соответствие исследования этому стандарту говорит о публичном соблюдении: прав участников исследования ¡ правил по обеспечению их безопасности ¡ стремления к ненанесению вреда ¡ требований к достоверности исследований ¡
 ¡ В большинстве стран 1960 -е и 1970 -е годыувеличение количества законов и рекомендаций для изучения безопасности, качества и эффективности новых медицинских продуктов. ¡ Официальные инстанции различных стран требовали данные об эффективности и безопасности для регистрации препарата и разрешения на его медицинское применение согласно национальным требованиям. Необходимость повтора одних и тех же исследований в разных странах.
¡ В большинстве стран 1960 -е и 1970 -е годыувеличение количества законов и рекомендаций для изучения безопасности, качества и эффективности новых медицинских продуктов. ¡ Официальные инстанции различных стран требовали данные об эффективности и безопасности для регистрации препарата и разрешения на его медицинское применение согласно национальным требованиям. Необходимость повтора одних и тех же исследований в разных странах.
 Правила GСP ¡ ¡ ¡ Впервые появились в США в 1978 г. в форме проекта. С 1980 г. начались инспекционные проверки хода клинических испытаний на соответствие этому стандарту 1987 г. правила GСP были приняты во Франции, в 1989 г. – в скандинавских странах и Японии. В 1990 г. Комиссией ЕC были опубликованы так называемые Европейские правила GСP, получившие официальный статус во всех странах Сообщества в 1991 г. Правила надлежащей клинической практики ВОЗ были подготовлены в 1991– 93 гг.
Правила GСP ¡ ¡ ¡ Впервые появились в США в 1978 г. в форме проекта. С 1980 г. начались инспекционные проверки хода клинических испытаний на соответствие этому стандарту 1987 г. правила GСP были приняты во Франции, в 1989 г. – в скандинавских странах и Японии. В 1990 г. Комиссией ЕC были опубликованы так называемые Европейские правила GСP, получившие официальный статус во всех странах Сообщества в 1991 г. Правила надлежащей клинической практики ВОЗ были подготовлены в 1991– 93 гг.
 Страны-участники ¡ ¡ ¡ ¡ ¡ Бельгия, Бразилия, Дания, Замбия, Индонезия, Китай, Россия, США, Швеция, Япония.
Страны-участники ¡ ¡ ¡ ¡ ¡ Бельгия, Бразилия, Дания, Замбия, Индонезия, Китай, Россия, США, Швеция, Япония.
 ¡ Окончательный вариант документа был утвержден в 1993 г. на 6 заседании Комитета экспертов ВОЗ по использованию основных лекарств и опубликован в качестве приложения к докладу Комитета в 1995 г. ( отражает глобальный консенсус министерств здравоохранения всех 190 с лишним стран-членов Организации).
¡ Окончательный вариант документа был утвержден в 1993 г. на 6 заседании Комитета экспертов ВОЗ по использованию основных лекарств и опубликован в качестве приложения к докладу Комитета в 1995 г. ( отражает глобальный консенсус министерств здравоохранения всех 190 с лишним стран-членов Организации).
 Сентябрь 1992 г. - начало разработки согласованных правил GCP ¡ 1 мая 1996 г. - принятие окончательного варианта ¡ 17 июля 1996 г. - правила одобрены официальными инстанциями ЕС ¡ 17 января 1997 г. - вступили в действие в ЕС ¡
Сентябрь 1992 г. - начало разработки согласованных правил GCP ¡ 1 мая 1996 г. - принятие окончательного варианта ¡ 17 июля 1996 г. - правила одобрены официальными инстанциями ЕС ¡ 17 января 1997 г. - вступили в действие в ЕС ¡
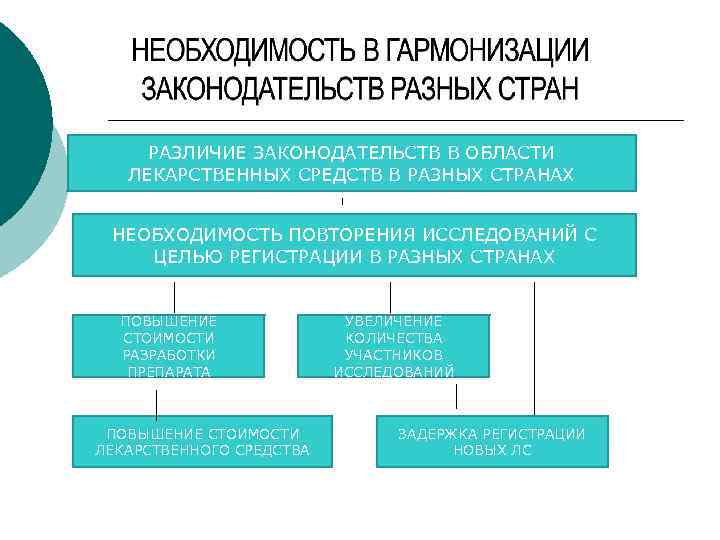 РАЗЛИЧИЕ ЗАКОНОДАТЕЛЬСТВ В ОБЛАСТИ ЛЕКАРСТВЕННЫХ СРЕДСТВ В РАЗНЫХ СТРАНАХ НЕОБХОДИМОСТЬ ПОВТОРЕНИЯ ИССЛЕДОВАНИЙ С ЦЕЛЬЮ РЕГИСТРАЦИИ В РАЗНЫХ СТРАНАХ ПОВЫШЕНИЕ СТОИМОСТИ РАЗРАБОТКИ ПРЕПАРАТА ПОВЫШЕНИЕ СТОИМОСТИ ЛЕКАРСТВЕННОГО СРЕДСТВА УВЕЛИЧЕНИЕ КОЛИЧЕСТВА УЧАСТНИКОВ ИССЛЕДОВАНИЙ ЗАДЕРЖКА РЕГИСТРАЦИИ НОВЫХ ЛС
РАЗЛИЧИЕ ЗАКОНОДАТЕЛЬСТВ В ОБЛАСТИ ЛЕКАРСТВЕННЫХ СРЕДСТВ В РАЗНЫХ СТРАНАХ НЕОБХОДИМОСТЬ ПОВТОРЕНИЯ ИССЛЕДОВАНИЙ С ЦЕЛЬЮ РЕГИСТРАЦИИ В РАЗНЫХ СТРАНАХ ПОВЫШЕНИЕ СТОИМОСТИ РАЗРАБОТКИ ПРЕПАРАТА ПОВЫШЕНИЕ СТОИМОСТИ ЛЕКАРСТВЕННОГО СРЕДСТВА УВЕЛИЧЕНИЕ КОЛИЧЕСТВА УЧАСТНИКОВ ИССЛЕДОВАНИЙ ЗАДЕРЖКА РЕГИСТРАЦИИ НОВЫХ ЛС
 В связи с этим разные страны начали процесс гармонизации и сближения законов, регулирующих порядок исследований лекарственных средств
В связи с этим разные страны начали процесс гармонизации и сближения законов, регулирующих порядок исследований лекарственных средств
 ICН ¡ Международная конференция по гармонизации требований к лекарствам (ICН) разрабатывала свои рекомендации по GCP в период с 1992 по 1996 гг.
ICН ¡ Международная конференция по гармонизации требований к лекарствам (ICН) разрабатывала свои рекомендации по GCP в период с 1992 по 1996 гг.
 ICН ¡ Правила ICН являются результатом процесса гармонизации, в котором участвуют контрольноразрешительные органы и инновационная фармацевтическая промышленность Евросоюза, США и Японии (отсюда одно из названий конференции – «трехсторонняя инициатива» ).
ICН ¡ Правила ICН являются результатом процесса гармонизации, в котором участвуют контрольноразрешительные органы и инновационная фармацевтическая промышленность Евросоюза, США и Японии (отсюда одно из названий конференции – «трехсторонняя инициатива» ).
 ¡ Усиление требований к защите субъектов исследования ¡ Необходимость обеспечения доступа к участию в КИ представителей популяций, недостаточно представленных в них ¡ Необходимость оценивать риски исследования не только по отношению к субъектам исследования, но и по отношению к обществу ¡ Усиление значимости эпидемиологических исследований ¡ Последние изменения внесены на 59 -й Генеральной ассамблее WMA, Сеул, Южная Корея, октябрь 2008 г.
¡ Усиление требований к защите субъектов исследования ¡ Необходимость обеспечения доступа к участию в КИ представителей популяций, недостаточно представленных в них ¡ Необходимость оценивать риски исследования не только по отношению к субъектам исследования, но и по отношению к обществу ¡ Усиление значимости эпидемиологических исследований ¡ Последние изменения внесены на 59 -й Генеральной ассамблее WMA, Сеул, Южная Корея, октябрь 2008 г.
 ¡ Усиление требований к публичности проводимых клинических исследований: размещение информации о любом КИ в открытых для всех базах данных до начала набора участников ¡ Ответственность за публикации результатов исследований не только автора и издателя, но и редактора ¡ Необходимость публиковать не только положительные и отрицательные результаты, но и информацию о проведенных исследованиях с неубедительными результатами ¡ Последние изменения внесены на 59 -й Генеральной ассамблее WMA, Сеул, Южная Корея, октябрь 2008 г.
¡ Усиление требований к публичности проводимых клинических исследований: размещение информации о любом КИ в открытых для всех базах данных до начала набора участников ¡ Ответственность за публикации результатов исследований не только автора и издателя, но и редактора ¡ Необходимость публиковать не только положительные и отрицательные результаты, но и информацию о проведенных исследованиях с неубедительными результатами ¡ Последние изменения внесены на 59 -й Генеральной ассамблее WMA, Сеул, Южная Корея, октябрь 2008 г.
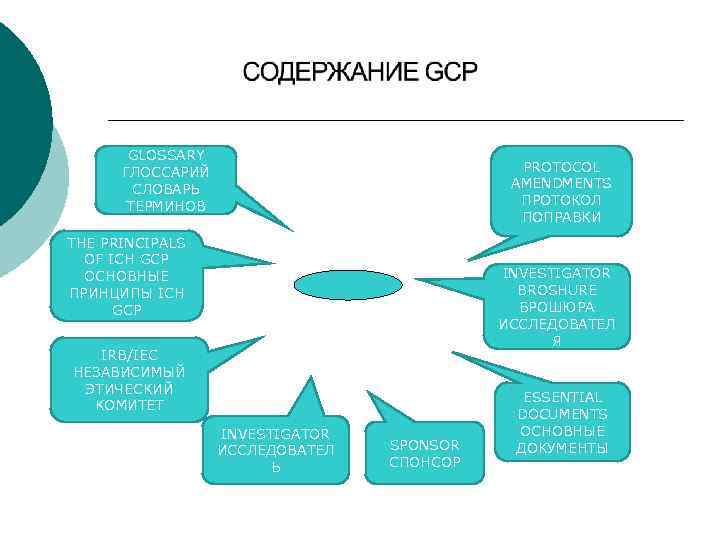 GLOSSARY ГЛОССАРИЙ СЛОВАРЬ ТЕРМИНОВ PROTOCOL AMENDMENTS ПРОТОКОЛ ПОПРАВКИ THE PRINCIPALS OF ICH GCP ОСНОВНЫЕ ПРИНЦИПЫ ICH GCP INVESTIGATOR BROSHURE БРОШЮРА ИССЛЕДОВАТЕЛ Я IRB/IEC НЕЗАВИСИМЫЙ ЭТИЧЕСКИЙ КОМИТЕТ INVESTIGATOR ИССЛЕДОВАТЕЛ Ь SPONSOR СПОНСОР ESSENTIAL DOCUMENTS ОСНОВНЫЕ ДОКУМЕНТЫ
GLOSSARY ГЛОССАРИЙ СЛОВАРЬ ТЕРМИНОВ PROTOCOL AMENDMENTS ПРОТОКОЛ ПОПРАВКИ THE PRINCIPALS OF ICH GCP ОСНОВНЫЕ ПРИНЦИПЫ ICH GCP INVESTIGATOR BROSHURE БРОШЮРА ИССЛЕДОВАТЕЛ Я IRB/IEC НЕЗАВИСИМЫЙ ЭТИЧЕСКИЙ КОМИТЕТ INVESTIGATOR ИССЛЕДОВАТЕЛ Ь SPONSOR СПОНСОР ESSENTIAL DOCUMENTS ОСНОВНЫЕ ДОКУМЕНТЫ
 ¡ ¡ Международная: Хельсинская декларация Правила ICH GCP Казахстанская: Кодекс РК «О здоровье народа и системе здравоохранения» - сентябрь 2009 г. Постановления и нормативные акты уполномоченных органов
¡ ¡ Международная: Хельсинская декларация Правила ICH GCP Казахстанская: Кодекс РК «О здоровье народа и системе здравоохранения» - сентябрь 2009 г. Постановления и нормативные акты уполномоченных органов
 КАЗАХСТАНСКИЕ ЗАКОНОДАТЕЛЬНЫЕ ОСНОВЫ ПРОВЕДЕНИЯ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ
КАЗАХСТАНСКИЕ ЗАКОНОДАТЕЛЬНЫЕ ОСНОВЫ ПРОВЕДЕНИЯ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ
 Стандарты качества клинических исследований доклинические исследования (GLP) ¡ клинические исследования (GCP) ¡ регистрация (GRP) ¡ производство (GMP) ¡ дистрибьюция (GDP) ¡ розничная торговля (GPP) ¡
Стандарты качества клинических исследований доклинические исследования (GLP) ¡ клинические исследования (GCP) ¡ регистрация (GRP) ¡ производство (GMP) ¡ дистрибьюция (GDP) ¡ розничная торговля (GPP) ¡
 ¡ Приказ МЗ РК от 14 февраля 2005 года № 53 «Об утверждении Инструкции по проведению клинических исследований и (или) испытаний фармакологических и лекарственных средств в РК» ¡ ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ КАЗАХСТАН НАДЛЕЖАЩАЯ КЛИНИЧЕСКАЯ ПРАКТИКА. СТ РК 1616 -2006. Дата введения -29 декабря 2006 ¡ ПРОЕКТ «Правила проведения клинических исследований и (или) испытаний фармакологических и лекарственных средств, изделий медицинского назначения и медицинской техники» - сентябрь 2009
¡ Приказ МЗ РК от 14 февраля 2005 года № 53 «Об утверждении Инструкции по проведению клинических исследований и (или) испытаний фармакологических и лекарственных средств в РК» ¡ ГОСУДАРСТВЕННЫЙ СТАНДАРТ РЕСПУБЛИКИ КАЗАХСТАН НАДЛЕЖАЩАЯ КЛИНИЧЕСКАЯ ПРАКТИКА. СТ РК 1616 -2006. Дата введения -29 декабря 2006 ¡ ПРОЕКТ «Правила проведения клинических исследований и (или) испытаний фармакологических и лекарственных средств, изделий медицинского назначения и медицинской техники» - сентябрь 2009
 является установление единых со странами Европейского союза, Соединенными штатами Америки и Японией правил, что должно способствовать взаимному признанию данных клинических исследований уполномоченными органами названных стран.
является установление единых со странами Европейского союза, Соединенными штатами Америки и Японией правил, что должно способствовать взаимному признанию данных клинических исследований уполномоченными органами названных стран.
 Статья 29 Граждане Республики Казахстан имеют право на охрану здоровья. ¡
Статья 29 Граждане Республики Казахстан имеют право на охрану здоровья. ¡
 ¡ ¡ ¡ ¡ Статья 74. Общие положения Статья 174. Порядок ввоза, вывоза тканей Статья 180. Проведение медико-биологических экспериментов, 3. Клинические исследования с участием человека (пациента или добровольца) при условии получения положительных результатов доклинических (неклинических) исследований могут проводиться только с его письменного информированного согласия. 4. Клинические исследования с участием несовершеннолетних могут проводиться: параллельно с исследованиями на лицах, достигших совершеннолетия только с письменного информированного согласия их законных представителей
¡ ¡ ¡ ¡ Статья 74. Общие положения Статья 174. Порядок ввоза, вывоза тканей Статья 180. Проведение медико-биологических экспериментов, 3. Клинические исследования с участием человека (пациента или добровольца) при условии получения положительных результатов доклинических (неклинических) исследований могут проводиться только с его письменного информированного согласия. 4. Клинические исследования с участием несовершеннолетних могут проводиться: параллельно с исследованиями на лицах, достигших совершеннолетия только с письменного информированного согласия их законных представителей
 ¡ Законы Республики Казахстан от 13 января 2004 года № 522 -II «О лекарственных средствах» с изменениями и дополнениями по состоянию на 07. 2006 ЗАКОН РК О «ЛЕКАРСТВЕННЫХ СРЕДСТВАХ» ГЛАВА 4. Разработка, исследования и (или) испытания Статья 19. 3. Клинические испытания проводятся в порядке, установленном уполномоченным органом. Статья 20. Права пациента.
¡ Законы Республики Казахстан от 13 января 2004 года № 522 -II «О лекарственных средствах» с изменениями и дополнениями по состоянию на 07. 2006 ЗАКОН РК О «ЛЕКАРСТВЕННЫХ СРЕДСТВАХ» ГЛАВА 4. Разработка, исследования и (или) испытания Статья 19. 3. Клинические испытания проводятся в порядке, установленном уполномоченным органом. Статья 20. Права пациента.
 ИНСТРУКЦИЯ разработана в соответствии с учетом норм, применяемых в международной практике, с целью детализации процедуры проведения клинических испытаний и установления единых требований к планированию, проведению, документальному оформлению и контролю клинических испытаний в РК, призванных гарантировать защиту прав, безопасность и охрану здоровья лиц, участвующих в испытаниях, а также обеспечить достоверность и точность получаемой в ходе испытания информации.
ИНСТРУКЦИЯ разработана в соответствии с учетом норм, применяемых в международной практике, с целью детализации процедуры проведения клинических испытаний и установления единых требований к планированию, проведению, документальному оформлению и контролю клинических испытаний в РК, призванных гарантировать защиту прав, безопасность и охрану здоровья лиц, участвующих в испытаниях, а также обеспечить достоверность и точность получаемой в ходе испытания информации.
 п. 2 Правовая основа для проведения КИ: Решение принимает уполномоченный орган на основании рекомендации Национального центра о возможности или отказе в проведении клинических испытаний. Договор о проведении клинических исследований ЛС между спонсором/CRO и исследовательским центром.
п. 2 Правовая основа для проведения КИ: Решение принимает уполномоченный орган на основании рекомендации Национального центра о возможности или отказе в проведении клинических испытаний. Договор о проведении клинических исследований ЛС между спонсором/CRO и исследовательским центром.
 п. 3. Проведение КИ 20. Клинические испытания проводятся в клинических базах, действующих в соответствии с положением о клинической базе согласно положению 7.
п. 3. Проведение КИ 20. Клинические испытания проводятся в клинических базах, действующих в соответствии с положением о клинической базе согласно положению 7.
 Основные функции: 1. оценка деятельности локальных комиссий по вопросам этики по проведению этической оценки КИ; 7. подготовка заключений о целесообразности проведения КИ при проведении межгосударственных мультицентровых исследований; 8. оповещение исследователей и других заинтересованных сторон о серьезных побочных реакциях или риска для участников исследования при проведении межгосударственных мультицентровых исследований; 9. рассмотрение спорных вопросов, возникших до начала, в ходе проведения или после завершения КИ.
Основные функции: 1. оценка деятельности локальных комиссий по вопросам этики по проведению этической оценки КИ; 7. подготовка заключений о целесообразности проведения КИ при проведении межгосударственных мультицентровых исследований; 8. оповещение исследователей и других заинтересованных сторон о серьезных побочных реакциях или риска для участников исследования при проведении межгосударственных мультицентровых исследований; 9. рассмотрение спорных вопросов, возникших до начала, в ходе проведения или после завершения КИ.
 ¡ Обязательным условием проведения клинических исследований является оформление документов о страховании жизни и здоровья участвующих в исследованиях пациентов и добровольцев…
¡ Обязательным условием проведения клинических исследований является оформление документов о страховании жизни и здоровья участвующих в исследованиях пациентов и добровольцев…
 В новом проекте внесено предложение: к «страхованию здоровья пациентов» добавить еще и «страхование гражданской ответственности лиц, осуществляющих проведение клинических исследований лекарственного средства» .
В новом проекте внесено предложение: к «страхованию здоровья пациентов» добавить еще и «страхование гражданской ответственности лиц, осуществляющих проведение клинических исследований лекарственного средства» .
 ¡ Обязательно ¡ Австрия ¡ Франция ¡ Ирландия ¡ Греция ¡ Португалия ¡ Россия Не обязательно Бельгия Англия Италия Нидерланды Германия Швеция Великобритания Дания Испания
¡ Обязательно ¡ Австрия ¡ Франция ¡ Ирландия ¡ Греция ¡ Португалия ¡ Россия Не обязательно Бельгия Англия Италия Нидерланды Германия Швеция Великобритания Дания Испания
 СПАСИБО ЗА ВНИМАНИЕ!
СПАСИБО ЗА ВНИМАНИЕ!


