Л-3-Элементы кристаллографии.ppt
- Количество слайдов: 19
 Межатомные связи в твердых телах
Межатомные связи в твердых телах
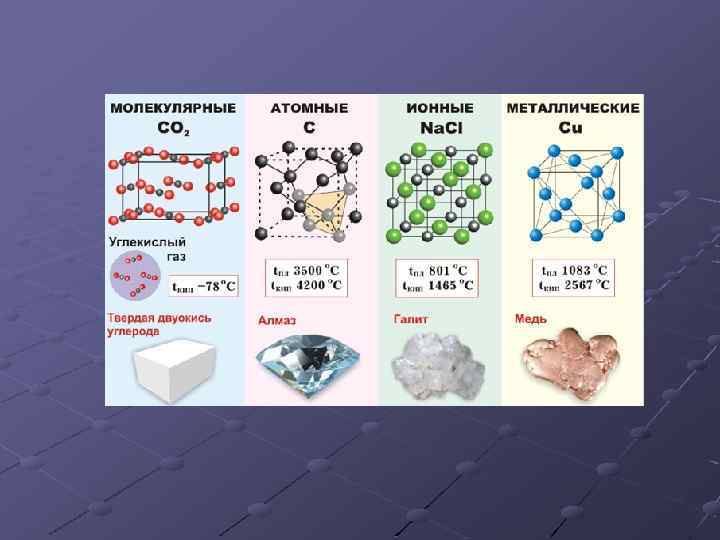
 Межатомные связи в материалах 1. 2. 3. 4. Связь Ван-дер-Ваальса (молекулярная) Ионная связь Ковалентная связь (атомная) Металлическая связь В зависимости от вида частиц, находящихся в узлах кристаллической решетки и типа связей между ними кристаллы бывают четырех типов: четырех типов молекулярные, атомные, ионные и металлические
Межатомные связи в материалах 1. 2. 3. 4. Связь Ван-дер-Ваальса (молекулярная) Ионная связь Ковалентная связь (атомная) Металлическая связь В зависимости от вида частиц, находящихся в узлах кристаллической решетки и типа связей между ними кристаллы бывают четырех типов: четырех типов молекулярные, атомные, ионные и металлические
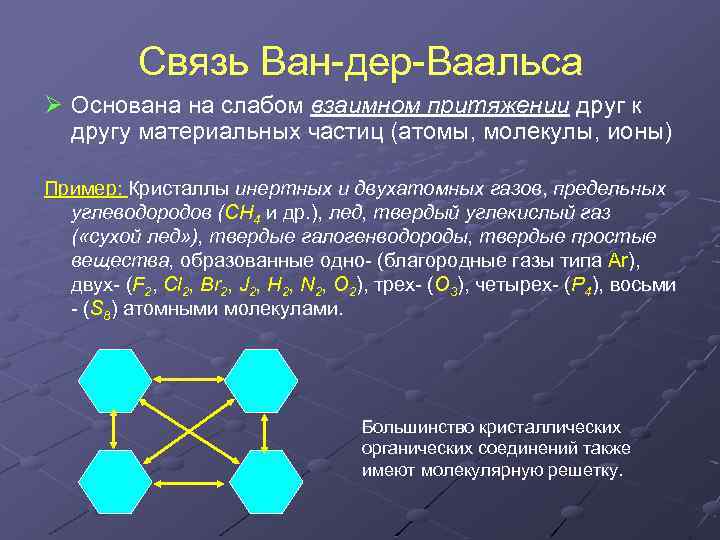 Связь Ван-дер-Ваальса Ø Основана на слабом взаимном притяжении друг к другу материальных частиц (атомы, молекулы, ионы) Пример: Кристаллы инертных и двухатомных газов, предельных углеводородов (CH 4 и др. ), лед, твердый углекислый газ ( «сухой лед» ), твердые галогенводороды, твердые простые вещества, образованные одно- (благородные газы типа Ar), двух- (F 2, Cl 2, Br 2, J 2, H 2, N 2, O 2), трех- (O 3), четырех- (P 4), восьми - (S 8) атомными молекулами. Большинство кристаллических органических соединений также имеют молекулярную решетку.
Связь Ван-дер-Ваальса Ø Основана на слабом взаимном притяжении друг к другу материальных частиц (атомы, молекулы, ионы) Пример: Кристаллы инертных и двухатомных газов, предельных углеводородов (CH 4 и др. ), лед, твердый углекислый газ ( «сухой лед» ), твердые галогенводороды, твердые простые вещества, образованные одно- (благородные газы типа Ar), двух- (F 2, Cl 2, Br 2, J 2, H 2, N 2, O 2), трех- (O 3), четырех- (P 4), восьми - (S 8) атомными молекулами. Большинство кристаллических органических соединений также имеют молекулярную решетку.
 Молекулярными называют кристаллические решётки, в узлах которых располагаются молекулы. Химические связи в них молекулы ковалентные, как полярные, так и неполярные. Молекулы в таких кристаллических решетках соединены между собой сравнительно слабыми водородными, межмолекулярными и электростатическими силами. Поэтому вещества с молекулярной решеткой имеют малую твердость и низкие температуры плавления. Они малорастворимы в воде, не проводят электрический ток и обладают высокой летучестью. Пример: кристаллическая решётка I 2 Вещества с МКР при обычных условиях находятся в газообразном или жидком состоянии
Молекулярными называют кристаллические решётки, в узлах которых располагаются молекулы. Химические связи в них молекулы ковалентные, как полярные, так и неполярные. Молекулы в таких кристаллических решетках соединены между собой сравнительно слабыми водородными, межмолекулярными и электростатическими силами. Поэтому вещества с молекулярной решеткой имеют малую твердость и низкие температуры плавления. Они малорастворимы в воде, не проводят электрический ток и обладают высокой летучестью. Пример: кристаллическая решётка I 2 Вещества с МКР при обычных условиях находятся в газообразном или жидком состоянии
 Ионная связь Ø Основана на перераспределении электронов внешнего уровня между соседними атомами. ~ Один атом отдает, а другой принимает один или несколько электронов. ~ Атомы становятся ионами с разными зарядами (+ или -) ~ Между ионами действуют электростатические силы притяжения
Ионная связь Ø Основана на перераспределении электронов внешнего уровня между соседними атомами. ~ Один атом отдает, а другой принимает один или несколько электронов. ~ Атомы становятся ионами с разными зарядами (+ или -) ~ Между ионами действуют электростатические силы притяжения
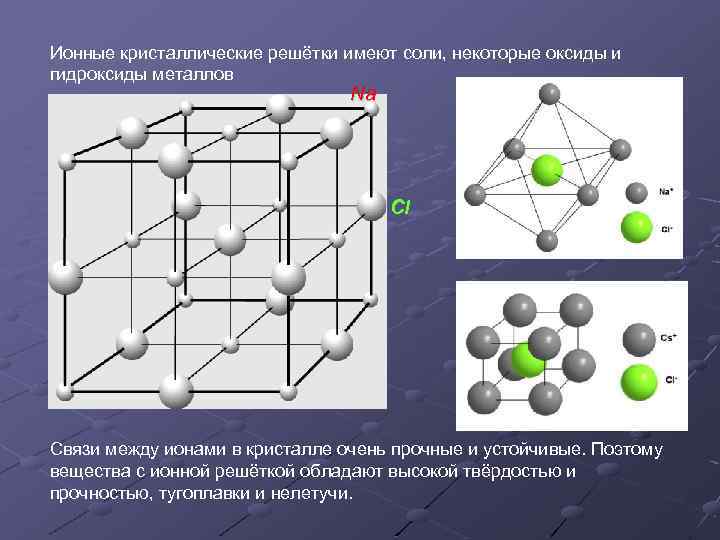 Ионные кристаллические решётки имеют соли, некоторые оксиды и гидроксиды металлов Na Cl Связи между ионами в кристалле очень прочные и устойчивые. Поэтому вещества с ионной решёткой обладают высокой твёрдостью и прочностью, тугоплавки и нелетучи.
Ионные кристаллические решётки имеют соли, некоторые оксиды и гидроксиды металлов Na Cl Связи между ионами в кристалле очень прочные и устойчивые. Поэтому вещества с ионной решёткой обладают высокой твёрдостью и прочностью, тугоплавки и нелетучи.
 Ковалентная связь Ø Основана на обобществлении электронов незаполненных электронных оболочек разных атомов с образованием стабильных электронных конфигураций типа инертных газов, неметаллических атомных и молекулярных соединений. Пример: молекула хлора Cl 2 Распределение электронов в атоме Cl – 1 s 22 p 63 s 23 p 5 Cl + Cl Cl
Ковалентная связь Ø Основана на обобществлении электронов незаполненных электронных оболочек разных атомов с образованием стабильных электронных конфигураций типа инертных газов, неметаллических атомных и молекулярных соединений. Пример: молекула хлора Cl 2 Распределение электронов в атоме Cl – 1 s 22 p 63 s 23 p 5 Cl + Cl Cl
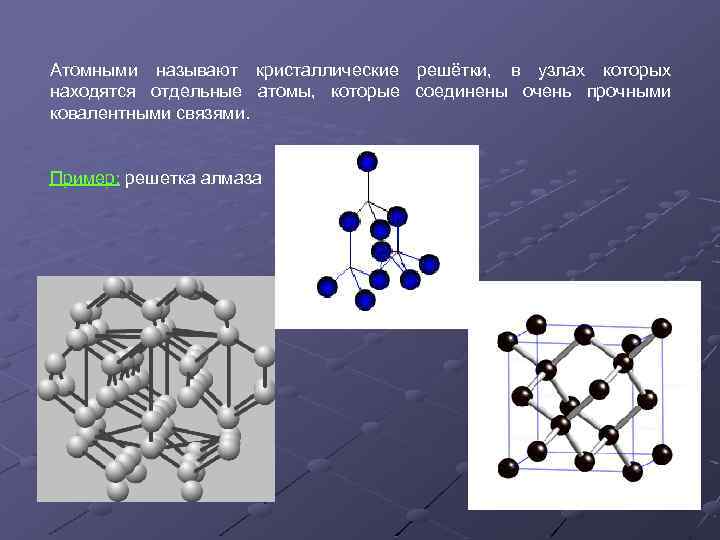 Атомными называют кристаллические решётки, в узлах которых находятся отдельные атомы, которые соединены очень прочными ковалентными связями. Пример: решетка алмаза
Атомными называют кристаллические решётки, в узлах которых находятся отдельные атомы, которые соединены очень прочными ковалентными связями. Пример: решетка алмаза
 Металлическая связь Ø Обусловлена потерей валентных электронов с последней оболочки атома материала и превращением его в положительно заряженный ион. + - - - - + + Металлическими называют решётки, в узлах которых находятся атомы и ионы металла. - + - - Такие решетки обуславливают особые физические свойства металлов: пластичность, ковкость, металлический блеск, высокая электро- и теплопроводность и т. д.
Металлическая связь Ø Обусловлена потерей валентных электронов с последней оболочки атома материала и превращением его в положительно заряженный ион. + - - - - + + Металлическими называют решётки, в узлах которых находятся атомы и ионы металла. - + - - Такие решетки обуславливают особые физические свойства металлов: пластичность, ковкость, металлический блеск, высокая электро- и теплопроводность и т. д.
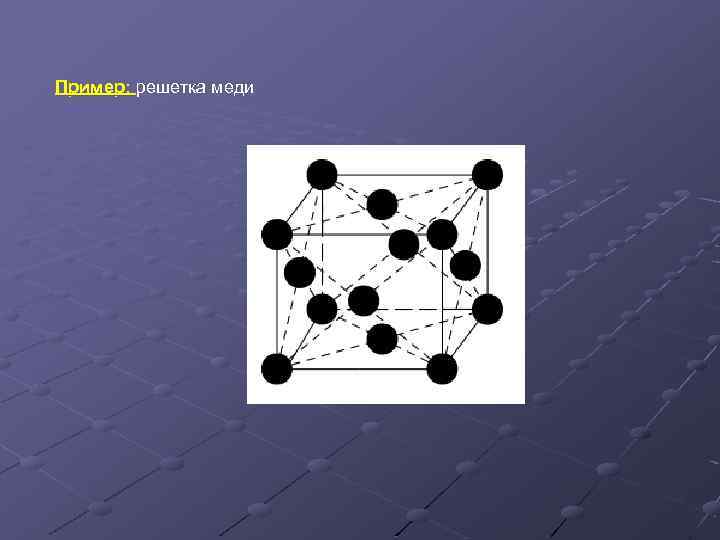 Пример: решетка меди
Пример: решетка меди
 Полиморфизм кристаллов ПОЛИМОРФИЗМ (от греч. polymorphos-многообразный) - способность ПОЛИМОРФИЗМ polymorphos кристаллических тел существовать в двух или нескольких формах с различной кристаллической структурой и демонстрирующих различные свойства при одном и том же химическом составе. Такие формы называются полиморфными модификациями (их принято обозначать греческими буквами α, β, γ и т. д. ) α, β, γ Взаимные превращения полиморфными переходами. полиморфных модификаций называются Полиморфизм простых (однокомпонентных) твердых тел называют аллотропией. Разные кристаллические формы одного и того же элемента, аллотропией. такие, как графит и алмаз, называют аллотропами Частный случай полиморфизма – политипизм (политипия). Политипные полиморфизма модификации представляют собой различные варианты наложения одинаковых двухмерных структурных фрагментов; при этом два параметра решетки неизменны, а третий меняется, оставаясь кратным постоянной величине. Например, для Si. C известно более 40 политипных модификаций (политипов). Политипия наблюдается также у Zn. S, Cd. I 2, глинистых минералов и др.
Полиморфизм кристаллов ПОЛИМОРФИЗМ (от греч. polymorphos-многообразный) - способность ПОЛИМОРФИЗМ polymorphos кристаллических тел существовать в двух или нескольких формах с различной кристаллической структурой и демонстрирующих различные свойства при одном и том же химическом составе. Такие формы называются полиморфными модификациями (их принято обозначать греческими буквами α, β, γ и т. д. ) α, β, γ Взаимные превращения полиморфными переходами. полиморфных модификаций называются Полиморфизм простых (однокомпонентных) твердых тел называют аллотропией. Разные кристаллические формы одного и того же элемента, аллотропией. такие, как графит и алмаз, называют аллотропами Частный случай полиморфизма – политипизм (политипия). Политипные полиморфизма модификации представляют собой различные варианты наложения одинаковых двухмерных структурных фрагментов; при этом два параметра решетки неизменны, а третий меняется, оставаясь кратным постоянной величине. Например, для Si. C известно более 40 политипных модификаций (политипов). Политипия наблюдается также у Zn. S, Cd. I 2, глинистых минералов и др.
 Типичный пример полиморфных форм (аллотропных состояний) - модификации углерода: углерода алмаз и лонсдейлит, в которых атомы объединены ковалентными связями алмаз лонсдейлит в пространственный каркас; графит, в структуре которого имеются слои графит наиболее прочно связанных атомов; карбин, построенный из бесконечных карбин линейных цепочек, фуллерены и графен как производная структура от фуллерены графен графита. Все эти модификации резко различаются по свойствам.
Типичный пример полиморфных форм (аллотропных состояний) - модификации углерода: углерода алмаз и лонсдейлит, в которых атомы объединены ковалентными связями алмаз лонсдейлит в пространственный каркас; графит, в структуре которого имеются слои графит наиболее прочно связанных атомов; карбин, построенный из бесконечных карбин линейных цепочек, фуллерены и графен как производная структура от фуллерены графен графита. Все эти модификации резко различаются по свойствам.
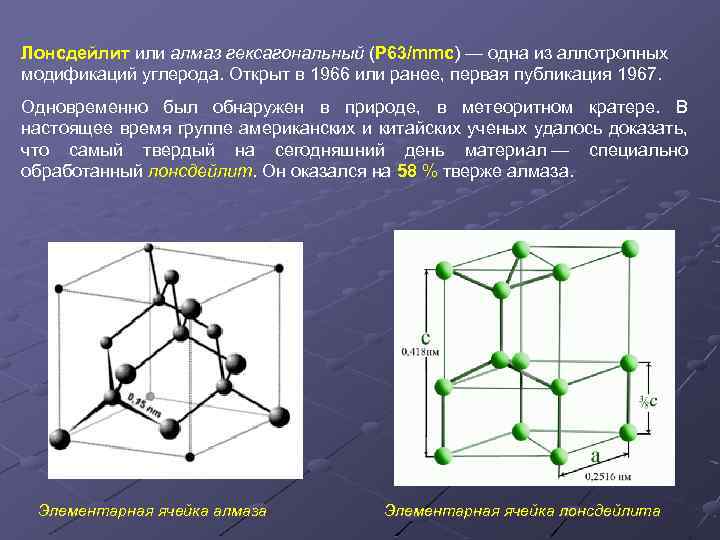 Лонсдейлит или алмаз гексагональный (P 63/mmc) — одна из аллотропных Лонсдейлит mmc модификаций углерода. Открыт в 1966 или ранее, первая публикация 1967. Одновременно был обнаружен в природе, в метеоритном кратере. В настоящее время группе американских и китайских ученых удалось доказать, что самый твердый на сегодняшний день материал — специально обработанный лонсдейлит. Он оказался на 58 % тверже алмаза. лонсдейлит 58 Элементарная ячейка алмаза Элементарная ячейка лонсдейлита
Лонсдейлит или алмаз гексагональный (P 63/mmc) — одна из аллотропных Лонсдейлит mmc модификаций углерода. Открыт в 1966 или ранее, первая публикация 1967. Одновременно был обнаружен в природе, в метеоритном кратере. В настоящее время группе американских и китайских ученых удалось доказать, что самый твердый на сегодняшний день материал — специально обработанный лонсдейлит. Он оказался на 58 % тверже алмаза. лонсдейлит 58 Элементарная ячейка алмаза Элементарная ячейка лонсдейлита
 Карбин — аллотропная форма углерода на основе sp-гибридизации углеродных гибридизации атомов. Состоит из углеродных фрагментов с тройной (–С≡С–), или (–С≡С–) двойной кумулированной (=С=С=) связью. Может быть линейным или (=С=С=) образовывать циклические структуры Фуллерены, бакиболы или букиболы — молекулярные соединения, принадлежащие классу аллотропных форм углерода и представляющие собой выпуклые замкнутые многогранники, составленные из чётного числа трёхкоординированных атомов углерода. Вид вращающегося бакибола C 60 Фуллерен C 540
Карбин — аллотропная форма углерода на основе sp-гибридизации углеродных гибридизации атомов. Состоит из углеродных фрагментов с тройной (–С≡С–), или (–С≡С–) двойной кумулированной (=С=С=) связью. Может быть линейным или (=С=С=) образовывать циклические структуры Фуллерены, бакиболы или букиболы — молекулярные соединения, принадлежащие классу аллотропных форм углерода и представляющие собой выпуклые замкнутые многогранники, составленные из чётного числа трёхкоординированных атомов углерода. Вид вращающегося бакибола C 60 Фуллерен C 540
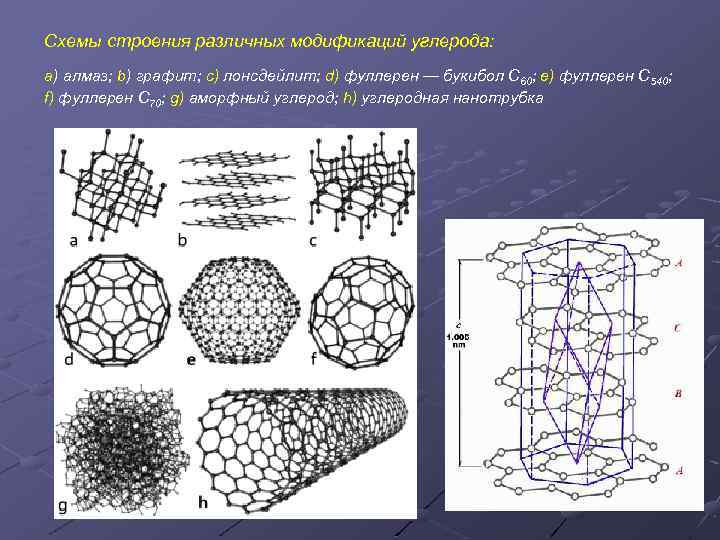 Схемы строения различных модификаций углерода: a) алмаз; b) графит; c) лонсдейлит; d) фуллерен — букибол C 60; e) фуллерен C 540; f) фуллерен C 70; g) аморфный углерод; h) углеродная нанотрубка
Схемы строения различных модификаций углерода: a) алмаз; b) графит; c) лонсдейлит; d) фуллерен — букибол C 60; e) фуллерен C 540; f) фуллерен C 70; g) аморфный углерод; h) углеродная нанотрубка
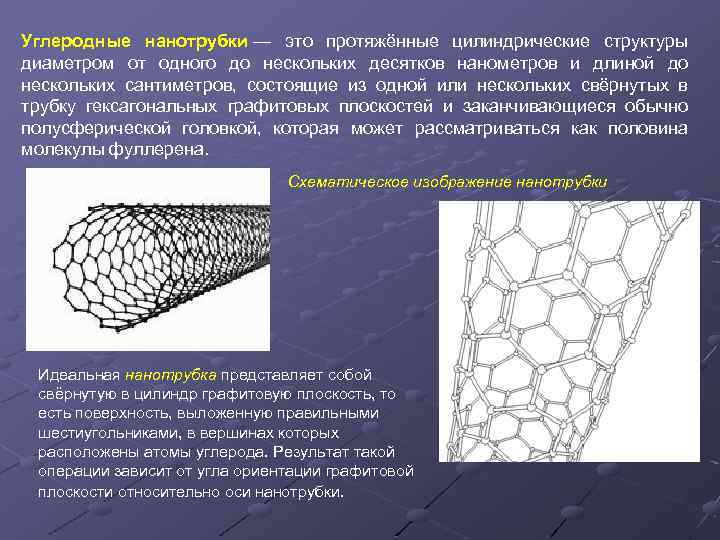 Углеродные нанотрубки — это протяжённые цилиндрические структуры нанотрубки диаметром от одного до нескольких десятков нанометров и длиной до нескольких сантиметров, состоящие из одной или нескольких свёрнутых в трубку гексагональных графитовых плоскостей и заканчивающиеся обычно полусферической головкой, которая может рассматриваться как половина молекулы фуллерена. Схематическое изображение нанотрубки Идеальная нанотрубка представляет собой нанотрубка свёрнутую в цилиндр графитовую плоскость, то есть поверхность, выложенную правильными шестиугольниками, в вершинах которых расположены атомы углерода. Результат такой операции зависит от угла ориентации графитовой плоскости относительно оси нанотрубки.
Углеродные нанотрубки — это протяжённые цилиндрические структуры нанотрубки диаметром от одного до нескольких десятков нанометров и длиной до нескольких сантиметров, состоящие из одной или нескольких свёрнутых в трубку гексагональных графитовых плоскостей и заканчивающиеся обычно полусферической головкой, которая может рассматриваться как половина молекулы фуллерена. Схематическое изображение нанотрубки Идеальная нанотрубка представляет собой нанотрубка свёрнутую в цилиндр графитовую плоскость, то есть поверхность, выложенную правильными шестиугольниками, в вершинах которых расположены атомы углерода. Результат такой операции зависит от угла ориентации графитовой плоскости относительно оси нанотрубки.
 Графен (graphene) — двумерная аллотропная модификация углерода, образованная слоем атомов углерода толщиной в один атом, находящихся в sp 2 – гибридизации и соединённых посредством σ- и π-связей в гексагональную двумерную кристаллическую решетку. Его можно представить как одну плоскость графита, отделённую от объёмного кристалла. По оценкам, графен обладает большой механической жесткостью и хорошей теплопроводностью (~1 ТПа и ~5× 103 Вт·м− 1·К− 1 соответственно). Высокая подвижность носителей заряда (максимальная подвижность электронов среди всех известных материалов) делает его перспективным материалом для использования в самых различных приложениях, в частности, как будущую основу наноэлектроники и возможную замену кремния в интегральных микросхемах. Графен действительно уникален. Кроме своей уникальной одноатомной толщины, графен в 10 раз прочнее стали и представляет собой превосходный проводник даже при комнатной температуре. Несмотря на невероятную прочность, графен обладает приличной гибкостью и может подвергаться 20% деформации без последствий для кристаллической решетки.
Графен (graphene) — двумерная аллотропная модификация углерода, образованная слоем атомов углерода толщиной в один атом, находящихся в sp 2 – гибридизации и соединённых посредством σ- и π-связей в гексагональную двумерную кристаллическую решетку. Его можно представить как одну плоскость графита, отделённую от объёмного кристалла. По оценкам, графен обладает большой механической жесткостью и хорошей теплопроводностью (~1 ТПа и ~5× 103 Вт·м− 1·К− 1 соответственно). Высокая подвижность носителей заряда (максимальная подвижность электронов среди всех известных материалов) делает его перспективным материалом для использования в самых различных приложениях, в частности, как будущую основу наноэлектроники и возможную замену кремния в интегральных микросхемах. Графен действительно уникален. Кроме своей уникальной одноатомной толщины, графен в 10 раз прочнее стали и представляет собой превосходный проводник даже при комнатной температуре. Несмотря на невероятную прочность, графен обладает приличной гибкостью и может подвергаться 20% деформации без последствий для кристаллической решетки.
 С точки зрения термодинамики, полиморфные модификации обычно являются самостоятельными фазами. Полиморфные переходы, согласно принятой в термодинамике классификации, подразделяются на переходы I и II рода. Последние (в отличие от переходов первого рода) не сопровождаются скачкообразным изменением энтропии; теплоемкость в точке такого перехода проходит через высокий и острый максимум. Изменение кристаллической структуры при переходе второго рода невелико, а в некоторых случаях практически отсутствует (напр. , при переходе γ-Fe в α-Fe, происходящем при 769°С, теряются ферромагнитные свойства). γ-Fe α-Fe Переходами второго рода часто являются переходы типа порядок - беспорядок. Упрощенная фазовая диаграмма углерода: заштрихованы области, где аллотропные модификации могут быть метастабильны. (diamond — алмаз, graphite — графит, liquid — жидкость, vapor — газ) — газ
С точки зрения термодинамики, полиморфные модификации обычно являются самостоятельными фазами. Полиморфные переходы, согласно принятой в термодинамике классификации, подразделяются на переходы I и II рода. Последние (в отличие от переходов первого рода) не сопровождаются скачкообразным изменением энтропии; теплоемкость в точке такого перехода проходит через высокий и острый максимум. Изменение кристаллической структуры при переходе второго рода невелико, а в некоторых случаях практически отсутствует (напр. , при переходе γ-Fe в α-Fe, происходящем при 769°С, теряются ферромагнитные свойства). γ-Fe α-Fe Переходами второго рода часто являются переходы типа порядок - беспорядок. Упрощенная фазовая диаграмма углерода: заштрихованы области, где аллотропные модификации могут быть метастабильны. (diamond — алмаз, graphite — графит, liquid — жидкость, vapor — газ) — газ


