4_mekhmy_vz-vl_khim_sv.ppt
- Количество слайдов: 47
 Механизмы взаимного влияния Алёхина Е. А.
Механизмы взаимного влияния Алёхина Е. А.
 Содержание Межмолекулярные взаимодействия Типы и характеристики химических связей Внутримолекулярные электронные взаимодействия Литература Алёхина Е. А.
Содержание Межмолекулярные взаимодействия Типы и характеристики химических связей Внутримолекулярные электронные взаимодействия Литература Алёхина Е. А.
 Механизмы взаимного влияния Межмолекулярное взаимодействие – это взаимодействие кинетически независимых частиц вещества (атомов, нейтральных молекул, одно или многозарядных ионов), приводящих к изменению агрегатного состояния и его свойств. Алёхина Е. А.
Механизмы взаимного влияния Межмолекулярное взаимодействие – это взаимодействие кинетически независимых частиц вещества (атомов, нейтральных молекул, одно или многозарядных ионов), приводящих к изменению агрегатного состояния и его свойств. Алёхина Е. А.
 Межмолекулярные взаимодействия Выражение для потенциальной энергии межмолекулярного взаимодействия имеет вид: Е = Еприт + Еотт, где: Е – энергия межмолекулярного взаимодействия, Еприт – энергия притяжения, Еприт – энергия отталкивания Алёхина Е. А.
Межмолекулярные взаимодействия Выражение для потенциальной энергии межмолекулярного взаимодействия имеет вид: Е = Еприт + Еотт, где: Е – энергия межмолекулярного взаимодействия, Еприт – энергия притяжения, Еприт – энергия отталкивания Алёхина Е. А.
 Межмолекулярные взаимодействия Энергия притяжения представляет собой сумму: Еприт = Еор + Еинд + Едисп + Ерез, где: Еор – энергия ориентационного взаимодействия, Еинд – энергия индукционного взаимодействия, Едисп – энергия дисперсионного взаимодействия, Ерез – энергия резонансного взаимодействия (обычно пренебрегают) Алёхина Е. А.
Межмолекулярные взаимодействия Энергия притяжения представляет собой сумму: Еприт = Еор + Еинд + Едисп + Ерез, где: Еор – энергия ориентационного взаимодействия, Еинд – энергия индукционного взаимодействия, Едисп – энергия дисперсионного взаимодействия, Ерез – энергия резонансного взаимодействия (обычно пренебрегают) Алёхина Е. А.
 ипы и характеристики химических связе органических соединений • Электронная структура атома углерода • Валентные состояния и типы гибридизации атома углерода в органических соединениях • Различные виды перекрывания атомных орбиталей • Типы химических связей • Характеристики химических связей Алёхина Е. А.
ипы и характеристики химических связе органических соединений • Электронная структура атома углерода • Валентные состояния и типы гибридизации атома углерода в органических соединениях • Различные виды перекрывания атомных орбиталей • Типы химических связей • Характеристики химических связей Алёхина Е. А.
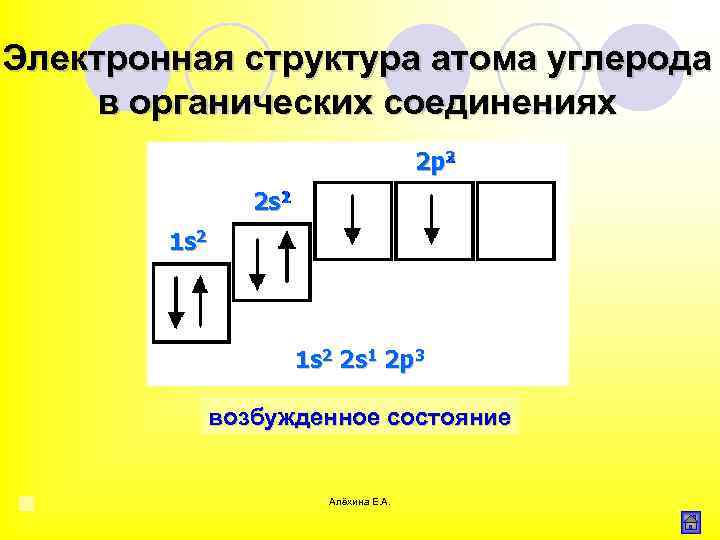 Электронная структура атома углерода в органических соединениях 3 2 p 2 1 2 s 2 1 3 1 s 2 2 p 2 возбужденное состояние основное состояние Алёхина Е. А.
Электронная структура атома углерода в органических соединениях 3 2 p 2 1 2 s 2 1 3 1 s 2 2 p 2 возбужденное состояние основное состояние Алёхина Е. А.
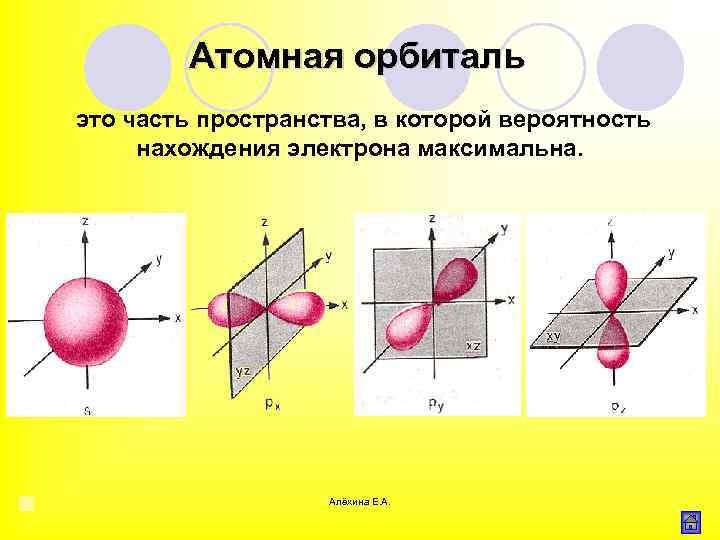 Атомная орбиталь это часть пространства, в которой вероятность нахождения электрона максимальна. Алёхина Е. А.
Атомная орбиталь это часть пространства, в которой вероятность нахождения электрона максимальна. Алёхина Е. А.
 Гибридизация в биологии Гибридизация в химии – это выравнивание электронных облаков по форме и энергии Алёхина Е. А.
Гибридизация в биологии Гибридизация в химии – это выравнивание электронных облаков по форме и энергии Алёхина Е. А.
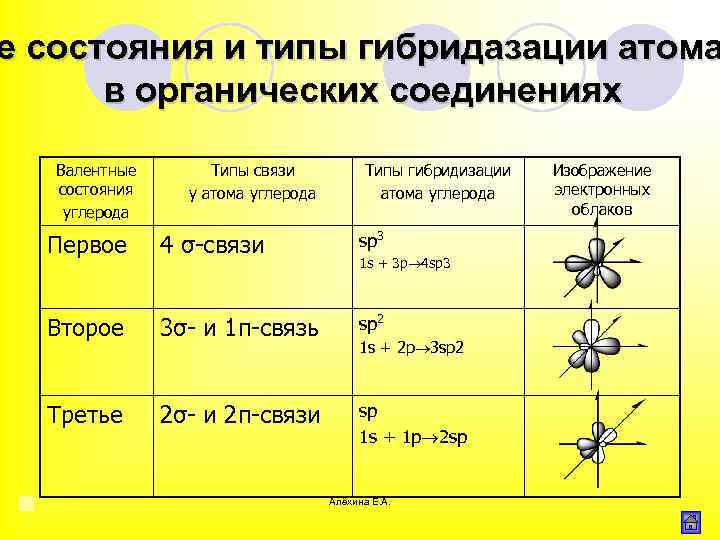 е состояния и типы гибридазации атома в органических соединениях Валентные состояния углерода Типы связи у атома углерода Типы гибридизации атома углерода Первое 4 σ связи sp 3 Второе 3σ и 1π связь sp 2 Третье 2σ и 2π связи sp 1 s + 1 p 2 sp 1 s + 3 p 4 sp 3 1 s + 2 p 3 sp 2 Алёхина Е. А. Изображение электронных облаков
е состояния и типы гибридазации атома в органических соединениях Валентные состояния углерода Типы связи у атома углерода Типы гибридизации атома углерода Первое 4 σ связи sp 3 Второе 3σ и 1π связь sp 2 Третье 2σ и 2π связи sp 1 s + 1 p 2 sp 1 s + 3 p 4 sp 3 1 s + 2 p 3 sp 2 Алёхина Е. А. Изображение электронных облаков
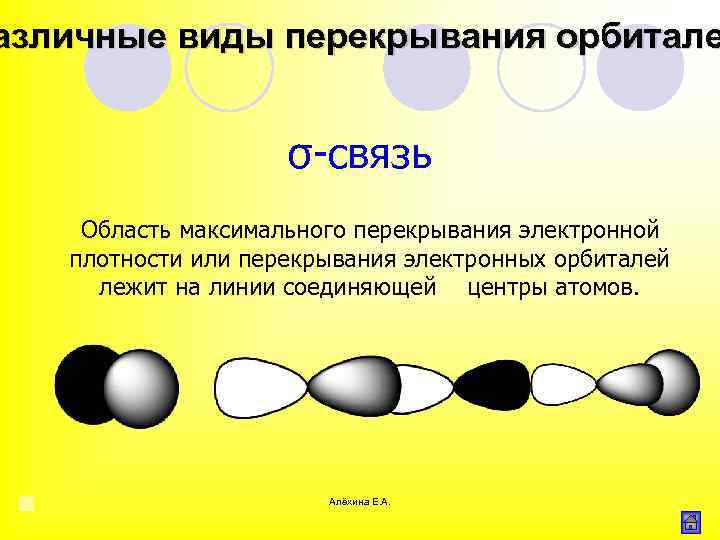 азличные виды перекрывания орбитале σ связь Область максимального перекрывания электронной плотности или перекрывания электронных орбиталей лежит на линии соединяющей центры атомов. Алёхина Е. А.
азличные виды перекрывания орбитале σ связь Область максимального перекрывания электронной плотности или перекрывания электронных орбиталей лежит на линии соединяющей центры атомов. Алёхина Е. А.
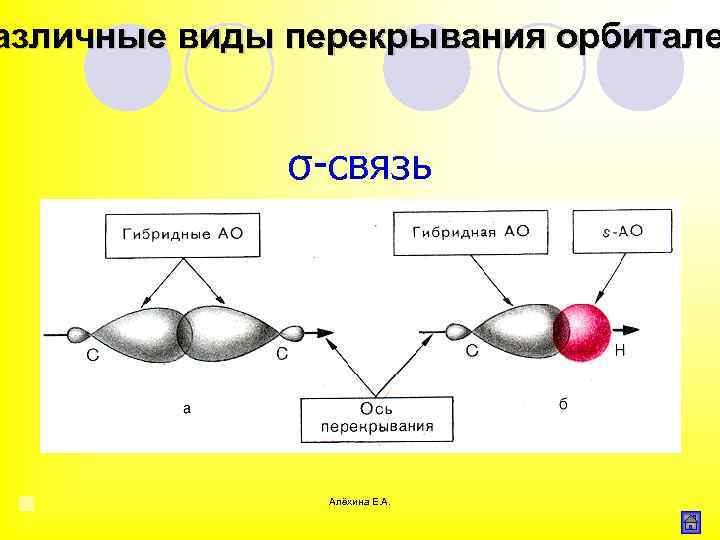 азличные виды перекрывания орбитале σ связь Алёхина Е. А.
азличные виды перекрывания орбитале σ связь Алёхина Е. А.
 азличные виды перекрывания орбитале -связь Связь образованная при перекрывании р- орбиталей соседних атомов Алёхина Е. А.
азличные виды перекрывания орбитале -связь Связь образованная при перекрывании р- орбиталей соседних атомов Алёхина Е. А.
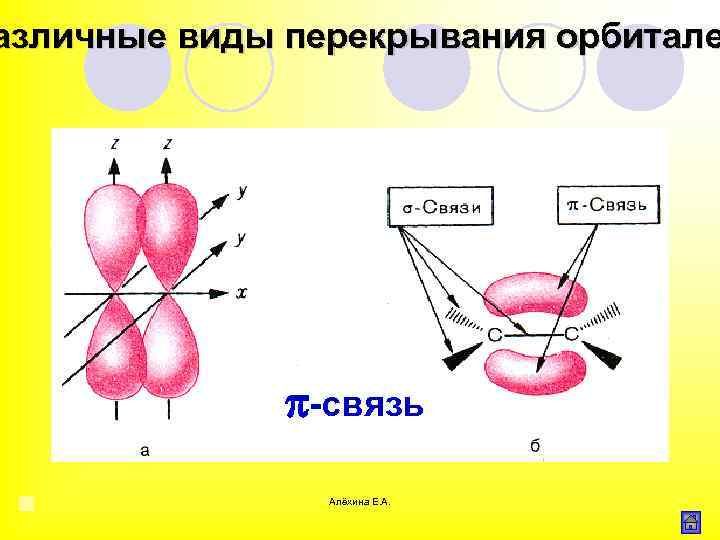 азличные виды перекрывания орбитале π-связь Алёхина Е. А.
азличные виды перекрывания орбитале π-связь Алёхина Е. А.
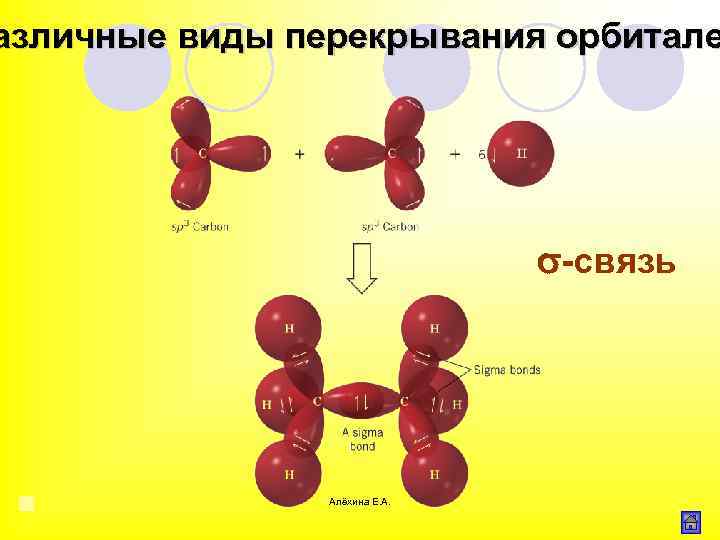 азличные виды перекрывания орбитале -связь Алёхина Е. А.
азличные виды перекрывания орбитале -связь Алёхина Е. А.
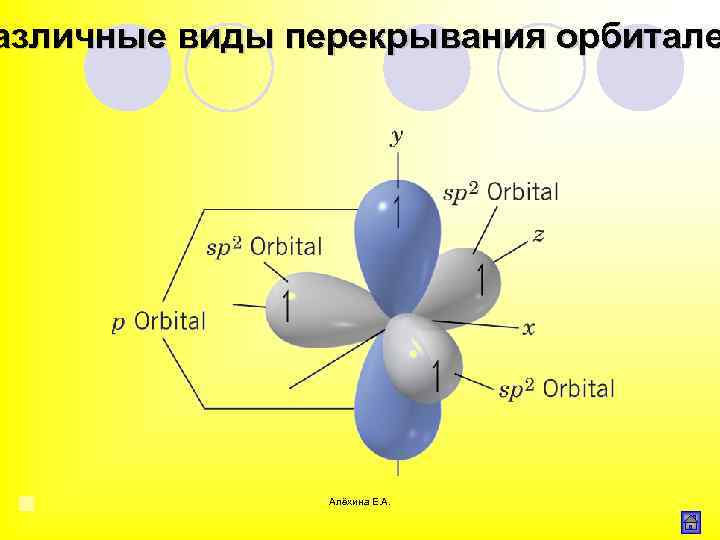 азличные виды перекрывания орбитале Алёхина Е. А.
азличные виды перекрывания орбитале Алёхина Е. А.
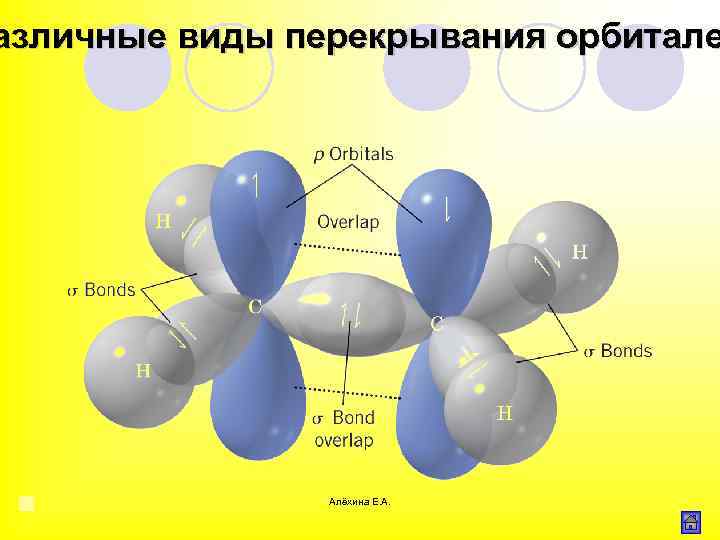 азличные виды перекрывания орбитале Алёхина Е. А.
азличные виды перекрывания орбитале Алёхина Е. А.
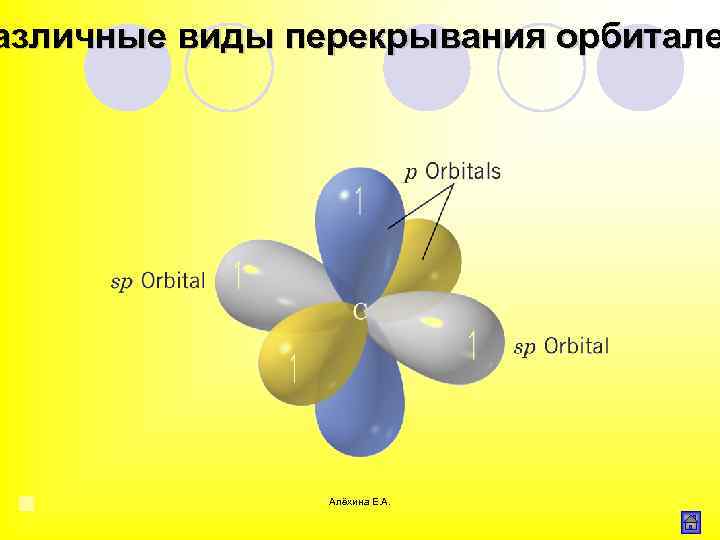 азличные виды перекрывания орбитале Алёхина Е. А.
азличные виды перекрывания орбитале Алёхина Е. А.
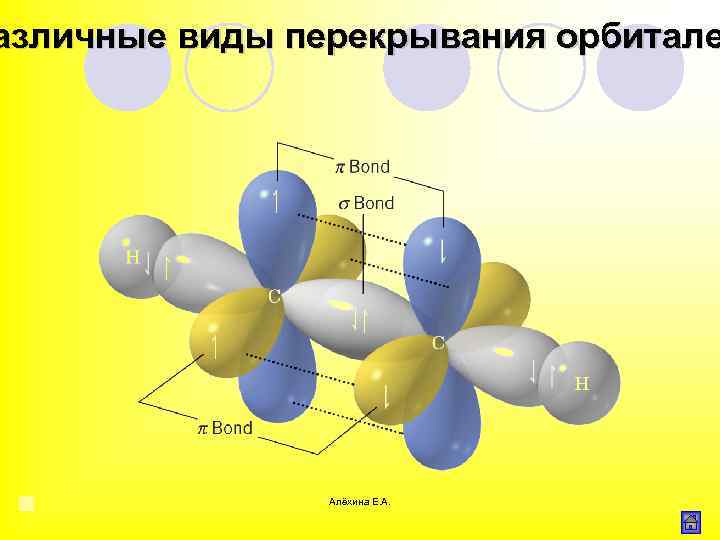 азличные виды перекрывания орбитале Алёхина Е. А.
азличные виды перекрывания орбитале Алёхина Е. А.
 Основные типы химической связи в органических соединениях Ионная (гетерополярная) связь СН 3 СООNa Ковалентная (гомеополярная) связь СН 3, Cl Cl Донорноакцепторная (координационная) связь : NH 3 + Н+ 3 HN: +Н [NH 4]+ CH 3 NH 2 + Н+ CH 3 NH 3+ Семи(полу)полярная связь А: + В А+: В– (или А В) Водородная связь Внутримолекулярная (ДНК и РНК) Алёхина Е. А. Межмолекулярная (вода, спирты, карб. кислоты)
Основные типы химической связи в органических соединениях Ионная (гетерополярная) связь СН 3 СООNa Ковалентная (гомеополярная) связь СН 3, Cl Cl Донорноакцепторная (координационная) связь : NH 3 + Н+ 3 HN: +Н [NH 4]+ CH 3 NH 2 + Н+ CH 3 NH 3+ Семи(полу)полярная связь А: + В А+: В– (или А В) Водородная связь Внутримолекулярная (ДНК и РНК) Алёхина Е. А. Межмолекулярная (вода, спирты, карб. кислоты)
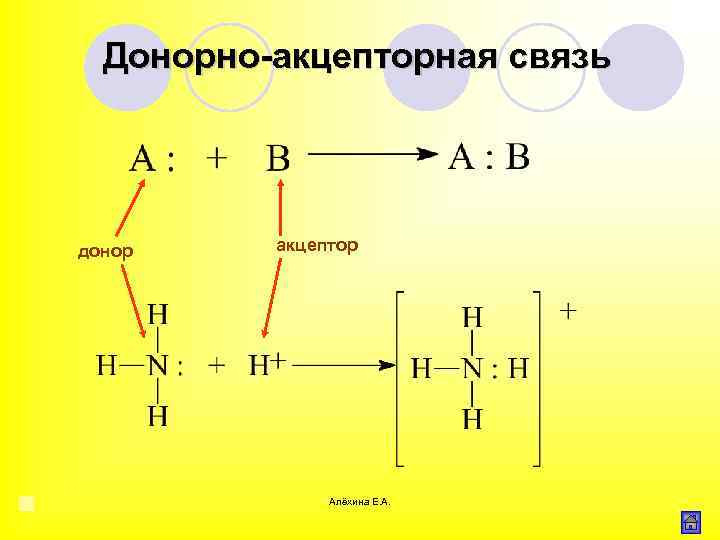 Донорно-акцепторная связь донор акцептор Алёхина Е. А.
Донорно-акцепторная связь донор акцептор Алёхина Е. А.
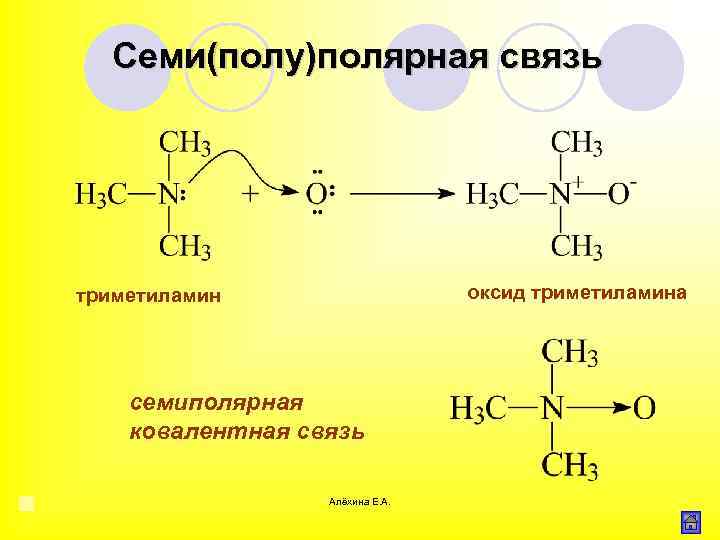 Семи(полу)полярная связь оксид триметиламина триметиламин семиполярная ковалентная связь Алёхина Е. А.
Семи(полу)полярная связь оксид триметиламина триметиламин семиполярная ковалентная связь Алёхина Е. А.
 Водородная связь осуществляется при участии электроно дефицитного атома водорода, ковалентно связанного с электро отрицательным атомом (фтор, кислород, азот). Он способен к дополнительному электростатическому взаимодействию с другим атомом, имеющим неподеленную пару электронов. Энергия водородных связей значительно меньше, чем ковалентных, т. е. они менее прочные. Существуют меж и внутримолекулярные водородные связи, т. е. возникающие между атомами разных или одной и той же молекулы. 12, 5— 20 к. Дж/моль Алёхина Е. А.
Водородная связь осуществляется при участии электроно дефицитного атома водорода, ковалентно связанного с электро отрицательным атомом (фтор, кислород, азот). Он способен к дополнительному электростатическому взаимодействию с другим атомом, имеющим неподеленную пару электронов. Энергия водородных связей значительно меньше, чем ковалентных, т. е. они менее прочные. Существуют меж и внутримолекулярные водородные связи, т. е. возникающие между атомами разных или одной и той же молекулы. 12, 5— 20 к. Дж/моль Алёхина Е. А.
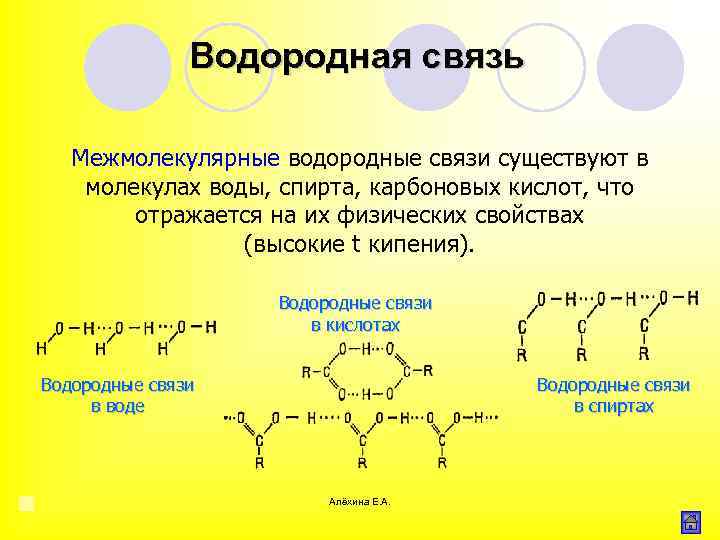 Водородная связь Межмолекулярные водородные связи существуют в молекулах воды, спирта, карбоновых кислот, что отражается на их физических свойствах (высокие t кипения). Водородные связи в кислотах Водородные связи в воде Водородные связи в спиртах Алёхина Е. А.
Водородная связь Межмолекулярные водородные связи существуют в молекулах воды, спирта, карбоновых кислот, что отражается на их физических свойствах (высокие t кипения). Водородные связи в кислотах Водородные связи в воде Водородные связи в спиртах Алёхина Е. А.
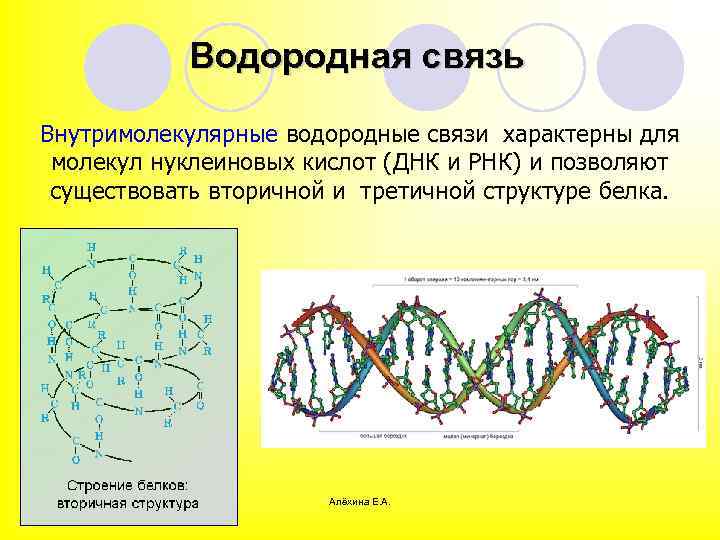 Водородная связь Внутримолекулярные водородные связи характерны для молекул нуклеиновых кислот (ДНК и РНК) и позволяют существовать вторичной и третичной структуре белка. Алёхина Е. А.
Водородная связь Внутримолекулярные водородные связи характерны для молекул нуклеиновых кислот (ДНК и РНК) и позволяют существовать вторичной и третичной структуре белка. Алёхина Е. А.
 Характеристики химической связи в органических соединениях Прочность связи Энергия связи – энергия, затрачиваемая на разрыв этой связи или выделяющаяся при ее образовании в расчете на 1 моль частиц. Длина – равновесное расстояние между центрами ядер. Значения длины С С связи колеблются от 1, 204 до 1, 543 А, в зависимости от типа гибридизации. Валентный угол для sp 3 гибридных он равен 109, 5 , для sp 2 гибридных – 120 , для sp гибридных – 180. Полярность (поляризуемость) Дипольный момент для ковалентных связей от 0 до 3, для координационных 2 7, для ионных выше 7. Алёхина Е. А.
Характеристики химической связи в органических соединениях Прочность связи Энергия связи – энергия, затрачиваемая на разрыв этой связи или выделяющаяся при ее образовании в расчете на 1 моль частиц. Длина – равновесное расстояние между центрами ядер. Значения длины С С связи колеблются от 1, 204 до 1, 543 А, в зависимости от типа гибридизации. Валентный угол для sp 3 гибридных он равен 109, 5 , для sp 2 гибридных – 120 , для sp гибридных – 180. Полярность (поляризуемость) Дипольный момент для ковалентных связей от 0 до 3, для координационных 2 7, для ионных выше 7. Алёхина Е. А.
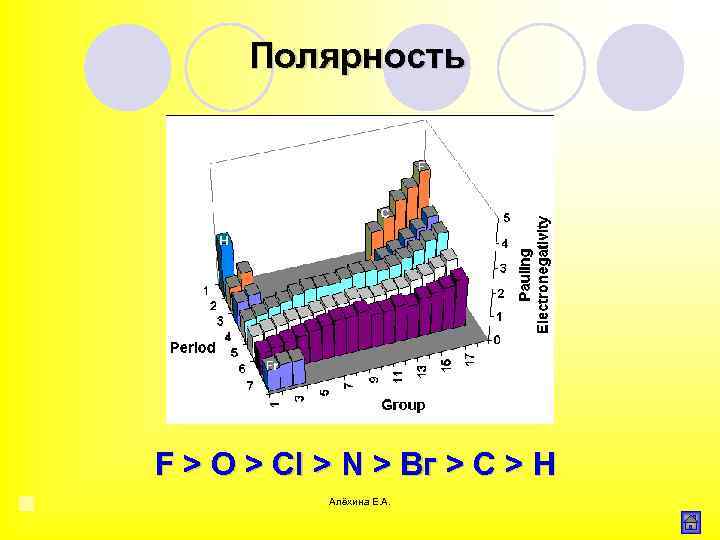 Полярность F > O > Сl > N > Вг > С > Н Алёхина Е. А.
Полярность F > O > Сl > N > Вг > С > Н Алёхина Е. А.
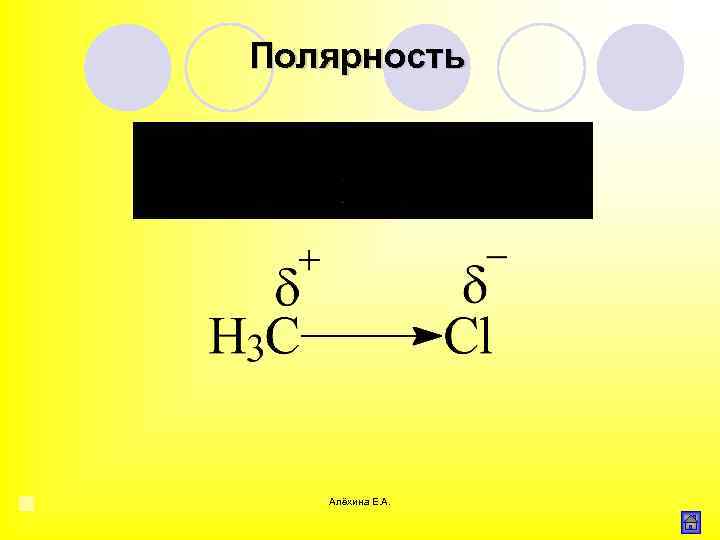 Полярность Алёхина Е. А.
Полярность Алёхина Е. А.
 Поляризуемость способность изменять свою полярность, например, под влиянием внешнего воздействия. -связи поляризуются гораздо легче, чем -связи Алёхина Е. А.
Поляризуемость способность изменять свою полярность, например, под влиянием внешнего воздействия. -связи поляризуются гораздо легче, чем -связи Алёхина Е. А.
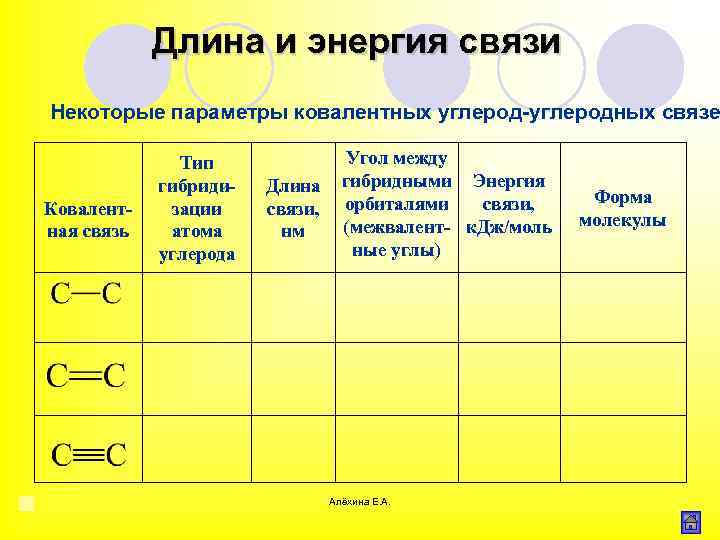 Длина и энергия связи Некоторые параметры ковалентных углерод-углеродных связе Ковалентная связь Тип гибридизации атома углерода Длина связи, нм Угол между гибридными Энергия орбиталями связи, (межвалент- к. Дж/моль ные углы) Алёхина Е. А. Форма молекулы
Длина и энергия связи Некоторые параметры ковалентных углерод-углеродных связе Ковалентная связь Тип гибридизации атома углерода Длина связи, нм Угол между гибридными Энергия орбиталями связи, (межвалент- к. Дж/моль ные углы) Алёхина Е. А. Форма молекулы
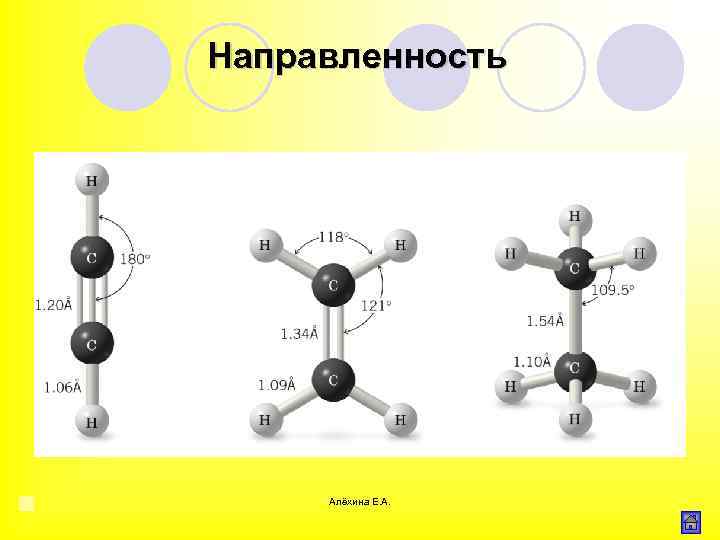 Направленность Алёхина Е. А.
Направленность Алёхина Е. А.
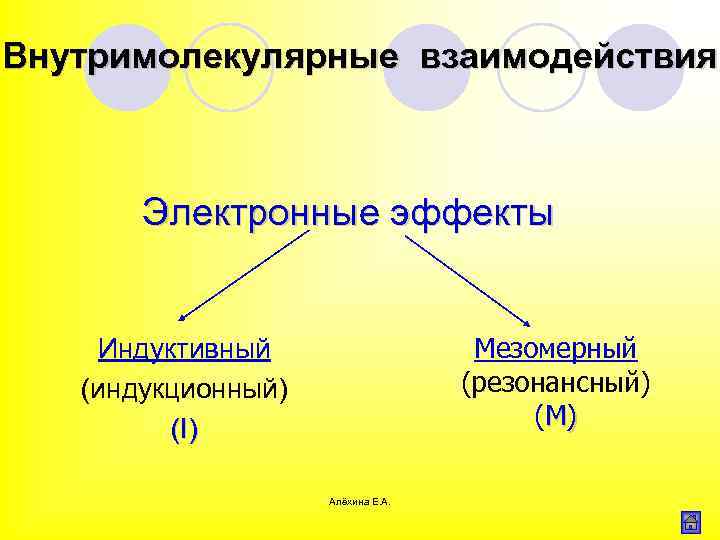 Внутримолекулярные взаимодействия Электронные эффекты Мезомерный (резонансный) (M) Индуктивный (индукционный) (I) Алёхина Е. А.
Внутримолекулярные взаимодействия Электронные эффекты Мезомерный (резонансный) (M) Индуктивный (индукционный) (I) Алёхина Е. А.
 Индуктивный эффект (I) смещение электронной плотности по связи в сторону более электроотрицательного атома элемента или группы атомов. Например: СН 3 – СН 2 Cl – –I Знак эффекта определяется зарядом, приобретаемым заместителем после смещения электронной плотности В цепи индуктивный эффект затухает Алёхина Е. А.
Индуктивный эффект (I) смещение электронной плотности по связи в сторону более электроотрицательного атома элемента или группы атомов. Например: СН 3 – СН 2 Cl – –I Знак эффекта определяется зарядом, приобретаемым заместителем после смещения электронной плотности В цепи индуктивный эффект затухает Алёхина Е. А.
 Индуктивный эффект (I) Знак эффекта определяется зарядом, приобретаемым заместителем после смещения электронной плотности или Если смещение электронной плотности от углеродной основы, то «–» , а если не углеродную основу, то «+» ). Алёхина Е. А.
Индуктивный эффект (I) Знак эффекта определяется зарядом, приобретаемым заместителем после смещения электронной плотности или Если смещение электронной плотности от углеродной основы, то «–» , а если не углеродную основу, то «+» ). Алёхина Е. А.
 Отрицательный индуктивный эффект ( • Дают те атомы и группы атомов, которые обладают большей электроотрицательностью, чем углерод. • Они оттягивают электронную плотность на себя. Х = Hal; СN; NO 2; OH; CHO; COOH; COOR и т. д. Алёхина Е. А.
Отрицательный индуктивный эффект ( • Дают те атомы и группы атомов, которые обладают большей электроотрицательностью, чем углерод. • Они оттягивают электронную плотность на себя. Х = Hal; СN; NO 2; OH; CHO; COOH; COOR и т. д. Алёхина Е. А.
 Положительный индуктивный эффект (+ • Дают атомы и группы атомы, которые имеют элетроотрицательность меньшую по сравнению с углеродом. • Отдают свою электронную плотность. где Х= СН 3; CH 2–CH 3 и т. д. Алёхина Е. А.
Положительный индуктивный эффект (+ • Дают атомы и группы атомы, которые имеют элетроотрицательность меньшую по сравнению с углеродом. • Отдают свою электронную плотность. где Х= СН 3; CH 2–CH 3 и т. д. Алёхина Е. А.
 Индуктивный эффект Закономерности изменения величины и знака индуктивного эффекта 1. Величина индуктивного эффекта растет с увеличением заряда заместителя NR 2< NO 2< NR 3<=NR 2 Индуктивный эффект Алёхина Е. А.
Индуктивный эффект Закономерности изменения величины и знака индуктивного эффекта 1. Величина индуктивного эффекта растет с увеличением заряда заместителя NR 2< NO 2< NR 3<=NR 2 Индуктивный эффект Алёхина Е. А.
 Индуктивный эффект Закономерности изменения величины и знака индуктивного эффекта 2. Чем больше электроотрицательность, тем сильнее отрицательный индуктивный эффект. В изоэлектронном ряду он растет слева направо, в группах снизу вверх. =CR 3< NR 2
Индуктивный эффект Закономерности изменения величины и знака индуктивного эффекта 2. Чем больше электроотрицательность, тем сильнее отрицательный индуктивный эффект. В изоэлектронном ряду он растет слева направо, в группах снизу вверх. =CR 3< NR 2
 Индуктивный эффект Закономерности изменения величины и знака индуктивного эффекта 3. У заместителей с кратными связями чем больше кратность, тем сильнее отрицательный индуктивный эффект NR 2 < =NR < I растет Алёхина Е. А. N
Индуктивный эффект Закономерности изменения величины и знака индуктивного эффекта 3. У заместителей с кратными связями чем больше кратность, тем сильнее отрицательный индуктивный эффект NR 2 < =NR < I растет Алёхина Е. А. N
 Индуктивный эффект Закономерности изменения величины и знака индуктивного эффекта 4. Алкильные группы проявляют положительный индуктивный эффект тем сильнее, чем выше разветвленность CH 3< CH 2 CH 3< CH(CH 3)2< C(CH 3)3 + I растет Алёхина Е. А.
Индуктивный эффект Закономерности изменения величины и знака индуктивного эффекта 4. Алкильные группы проявляют положительный индуктивный эффект тем сильнее, чем выше разветвленность CH 3< CH 2 CH 3< CH(CH 3)2< C(CH 3)3 + I растет Алёхина Е. А.
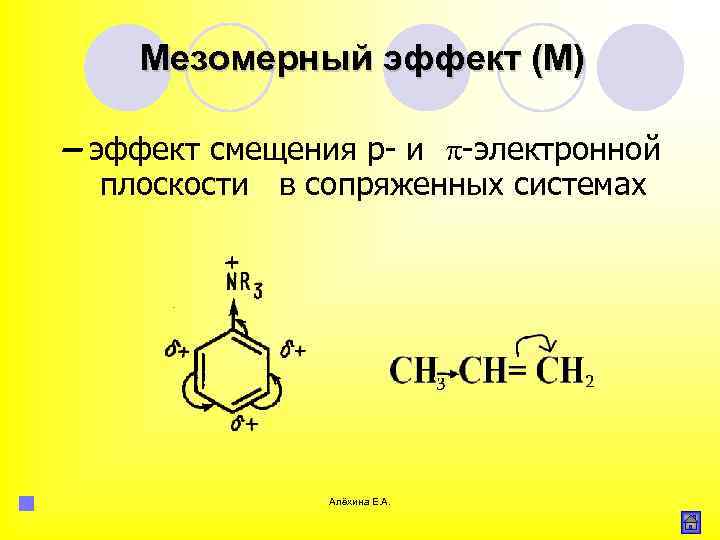 Мезомерный эффект (М) – эффект смещения р и электронной плоскости в сопряженных системах Алёхина Е. А.
Мезомерный эффект (М) – эффект смещения р и электронной плоскости в сопряженных системах Алёхина Е. А.
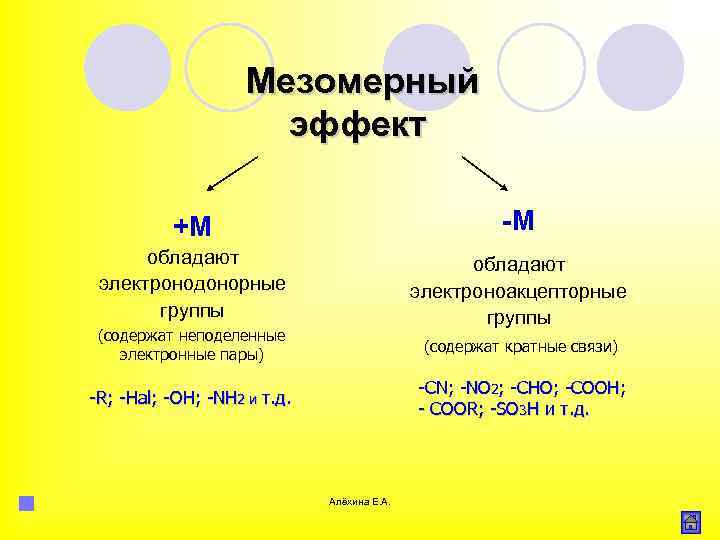 Мезомерный эффект +М -М обладают электронодонорные группы обладают электроноакцепторные группы (содержат неподеленные электронные пары) (содержат кратные связи) СN; NO 2; CHO; COOH; COOR; SO 3 H и т. д. R; Hal; OH; NH 2 и т. д. Алёхина Е. А.
Мезомерный эффект +М -М обладают электронодонорные группы обладают электроноакцепторные группы (содержат неподеленные электронные пары) (содержат кратные связи) СN; NO 2; CHO; COOH; COOR; SO 3 H и т. д. R; Hal; OH; NH 2 и т. д. Алёхина Е. А.
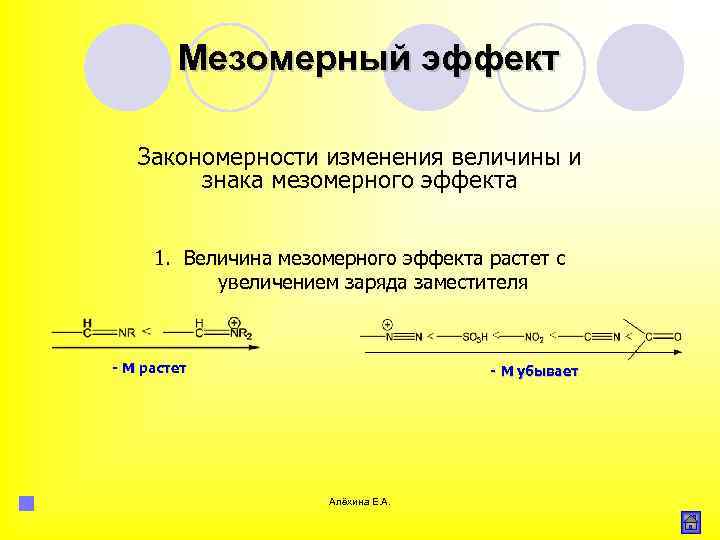 Мезомерный эффект Закономерности изменения величины и знака мезомерного эффекта 1. Величина мезомерного эффекта растет с увеличением заряда заместителя - М растет - М убывает Алёхина Е. А.
Мезомерный эффект Закономерности изменения величины и знака мезомерного эффекта 1. Величина мезомерного эффекта растет с увеличением заряда заместителя - М растет - М убывает Алёхина Е. А.
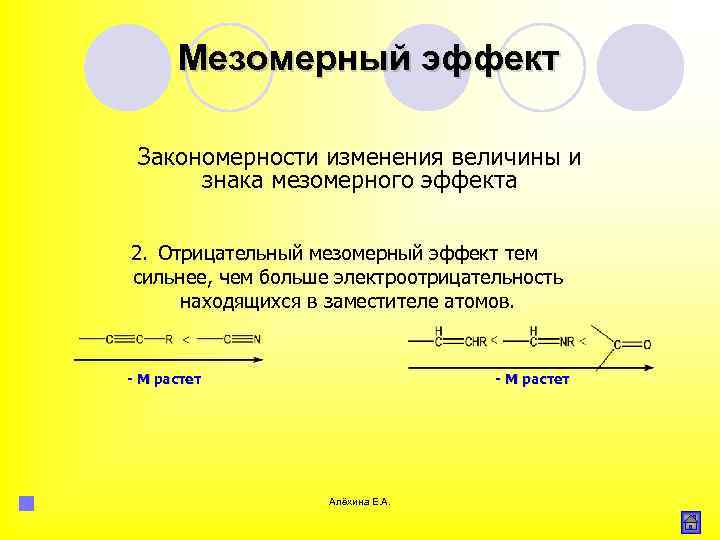 Мезомерный эффект Закономерности изменения величины и знака мезомерного эффекта 2. Отрицательный мезомерный эффект тем сильнее, чем больше электроотрицательность находящихся в заместителе атомов. - М растет Алёхина Е. А.
Мезомерный эффект Закономерности изменения величины и знака мезомерного эффекта 2. Отрицательный мезомерный эффект тем сильнее, чем больше электроотрицательность находящихся в заместителе атомов. - М растет Алёхина Е. А.
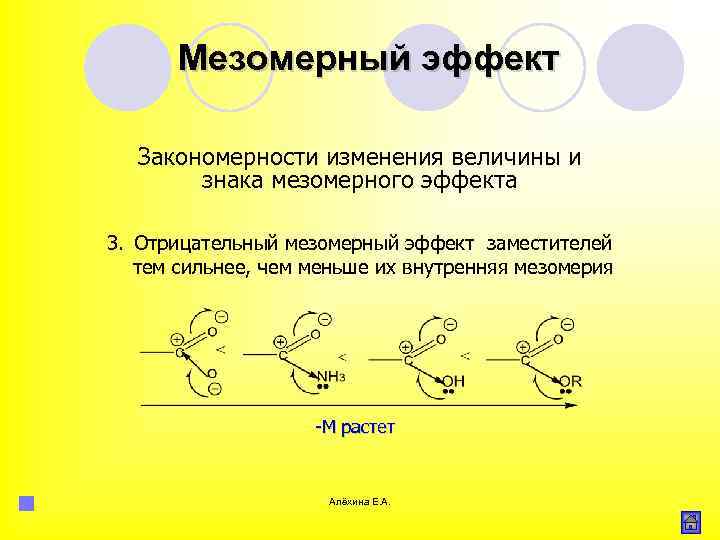 Мезомерный эффект Закономерности изменения величины и знака мезомерного эффекта 3. Отрицательный мезомерный эффект заместителей тем сильнее, чем меньше их внутренняя мезомерия М растет Алёхина Е. А.
Мезомерный эффект Закономерности изменения величины и знака мезомерного эффекта 3. Отрицательный мезомерный эффект заместителей тем сильнее, чем меньше их внутренняя мезомерия М растет Алёхина Е. А.
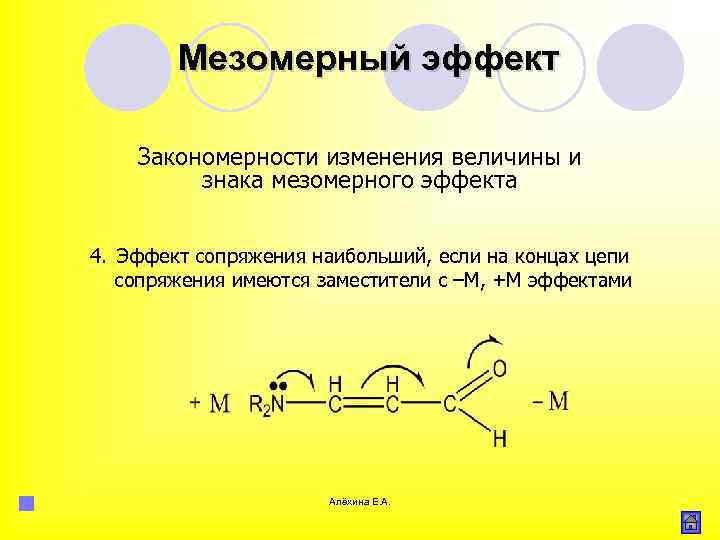 Мезомерный эффект Закономерности изменения величины и знака мезомерного эффекта 4. Эффект сопряжения наибольший, если на концах цепи сопряжения имеются заместители с –М, +М эффектами Алёхина Е. А.
Мезомерный эффект Закономерности изменения величины и знака мезомерного эффекта 4. Эффект сопряжения наибольший, если на концах цепи сопряжения имеются заместители с –М, +М эффектами Алёхина Е. А.
 Литература 1. 2. 3. 4. 5. Ким А. М. Органическая химия. – Новосибирск: Сиб. унив. изд-во, 2004. – 842 с. Перекалин В. В. и др. Органическая химия. – М. : Просвещение, – М. , 1982. – 560 с. Степаненко Б. Н. Курс органической химии. В 2 -х т. – М. : Высшая школа, 1981. Травень В. Ф. Органическая химия. В 2 -х т. – М. : ИКЦ «Академкнига» , 2005. Шабаров Ю. С. Органическая химия. В 2 -х т. – М. : Химия, 1996. Алёхина Е. А.
Литература 1. 2. 3. 4. 5. Ким А. М. Органическая химия. – Новосибирск: Сиб. унив. изд-во, 2004. – 842 с. Перекалин В. В. и др. Органическая химия. – М. : Просвещение, – М. , 1982. – 560 с. Степаненко Б. Н. Курс органической химии. В 2 -х т. – М. : Высшая школа, 1981. Травень В. Ф. Органическая химия. В 2 -х т. – М. : ИКЦ «Академкнига» , 2005. Шабаров Ю. С. Органическая химия. В 2 -х т. – М. : Химия, 1996. Алёхина Е. А.


