Механизмы реакций в органической химии.ppt
- Количество слайдов: 85
 Механизмы реакций в органической химии
Механизмы реакций в органической химии
 Что такое механизм реакции?
Что такое механизм реакции?
 Классификация реакций • По числу исходных и конечных веществ: 1. Присоединение 2. Отщепление (элиминирование) 3. Замещение
Классификация реакций • По числу исходных и конечных веществ: 1. Присоединение 2. Отщепление (элиминирование) 3. Замещение
 Классификация реакций • По механизму разрыва связей: 1. Гомолитические (радикальные) радикалы 2. Гетеролитические (ионные) ионы
Классификация реакций • По механизму разрыва связей: 1. Гомолитические (радикальные) радикалы 2. Гетеролитические (ионные) ионы
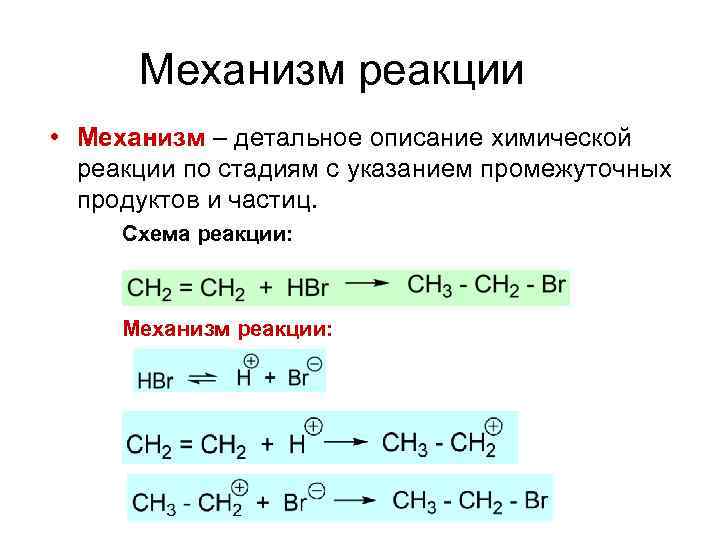 Механизм реакции • Механизм – детальное описание химической реакции по стадиям с указанием промежуточных продуктов и частиц. Схема реакции: Механизм реакции:
Механизм реакции • Механизм – детальное описание химической реакции по стадиям с указанием промежуточных продуктов и частиц. Схема реакции: Механизм реакции:
 Классификация реакций по типу реагентов 1. Радикальные Радикал –химически активная частица с неспаренным электроном. 2. Электрофильные Электрофил – электронодефицитная частица или молекула с электронодефицитным атомом. 3. Нуклеофильные Нуклеофил – анион или нейтральная молекула, имеющая атом с неподеленной электронной парой.
Классификация реакций по типу реагентов 1. Радикальные Радикал –химически активная частица с неспаренным электроном. 2. Электрофильные Электрофил – электронодефицитная частица или молекула с электронодефицитным атомом. 3. Нуклеофильные Нуклеофил – анион или нейтральная молекула, имеющая атом с неподеленной электронной парой.
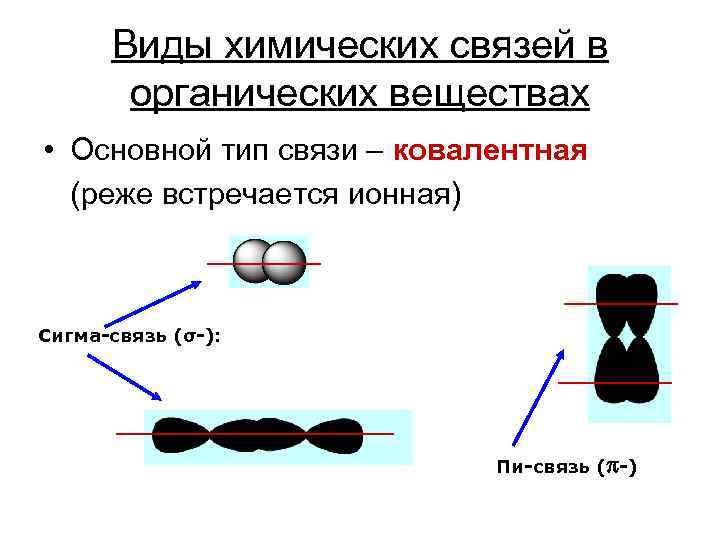 Виды химических связей в органических веществах • Основной тип связи – ковалентная (реже встречается ионная) Сигма-связь (σ-): Пи-связь ( -)
Виды химических связей в органических веществах • Основной тип связи – ковалентная (реже встречается ионная) Сигма-связь (σ-): Пи-связь ( -)
 АЛКАНЫ- алифатические (жирные) углеводороды «Алифатос» -масло, жир (греч). Cn. H 2 n+2 Предельные, насыщенные углеводороды
АЛКАНЫ- алифатические (жирные) углеводороды «Алифатос» -масло, жир (греч). Cn. H 2 n+2 Предельные, насыщенные углеводороды
 Гомологический ряд: CH 4 - метан C 2 H 6 - этан C 3 H 8 - пропан C 4 H 10 - бутан C 5 H 12 - пентан т. д. С 6 Н 14 - гексан С 7 Н 16 - гептан С 8 Н 18 - октан С 9 Н 20 - нонан С 10 Н 22 – декан и С 390 Н 782 –ноноконтатриктан (1985 г )
Гомологический ряд: CH 4 - метан C 2 H 6 - этан C 3 H 8 - пропан C 4 H 10 - бутан C 5 H 12 - пентан т. д. С 6 Н 14 - гексан С 7 Н 16 - гептан С 8 Н 18 - октан С 9 Н 20 - нонан С 10 Н 22 – декан и С 390 Н 782 –ноноконтатриктан (1985 г )
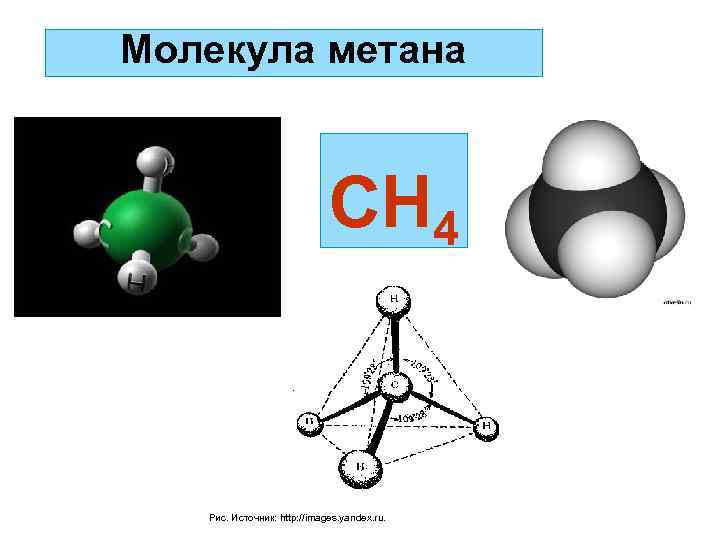 Молекула метана СН 4 Рис. Источник: http: //images. yandex. ru.
Молекула метана СН 4 Рис. Источник: http: //images. yandex. ru.
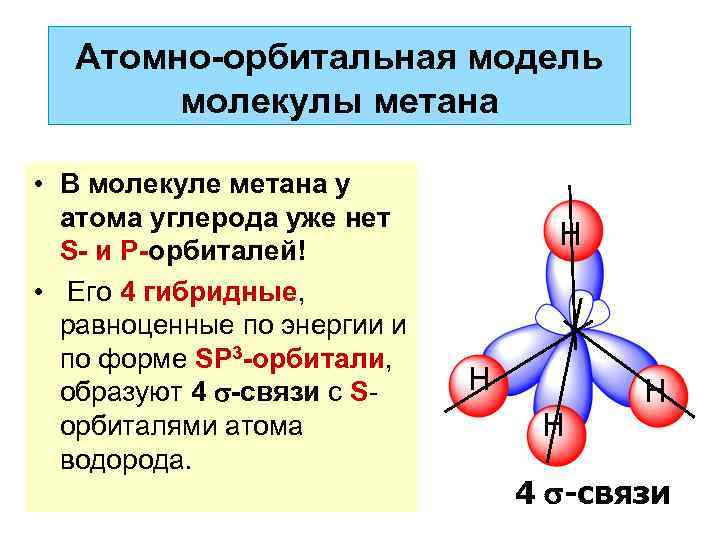 Атомно-орбитальная модель молекулы метана • В молекуле метана у атома углерода уже нет S- и Р-орбиталей! • Его 4 гибридные, равноценные по энергии и по форме SP 3 -орбитали, образуют 4 -связи с Sорбиталями атома водорода. Н Н 4 -связи
Атомно-орбитальная модель молекулы метана • В молекуле метана у атома углерода уже нет S- и Р-орбиталей! • Его 4 гибридные, равноценные по энергии и по форме SP 3 -орбитали, образуют 4 -связи с Sорбиталями атома водорода. Н Н 4 -связи
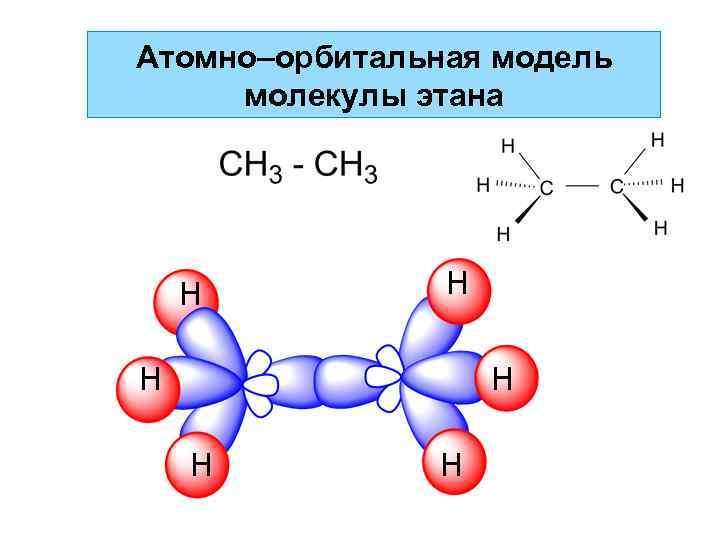 Атомно–орбитальная модель молекулы этана Н Н Н
Атомно–орбитальная модель молекулы этана Н Н Н
 Реакция нитрования • Коновалов Дмитрий Петрович (1856 -1928) • 1880 год. Первая удачная попытка оживить «химических мертвецов» , которыми считались алканы. • Нашел условия нитрования алканов. Рис. Источник: http: //images. yandex. ru.
Реакция нитрования • Коновалов Дмитрий Петрович (1856 -1928) • 1880 год. Первая удачная попытка оживить «химических мертвецов» , которыми считались алканы. • Нашел условия нитрования алканов. Рис. Источник: http: //images. yandex. ru.
 Химические свойства I. Реакции с разрывом С-Н-связей (реакции замещения): 1. галогенирование 2. нитрование 3. сульфохлорирование II. Реакции с разрывом С-С-связей: 1. горение 2. крекинг 3. изомеризация
Химические свойства I. Реакции с разрывом С-Н-связей (реакции замещения): 1. галогенирование 2. нитрование 3. сульфохлорирование II. Реакции с разрывом С-С-связей: 1. горение 2. крекинг 3. изомеризация
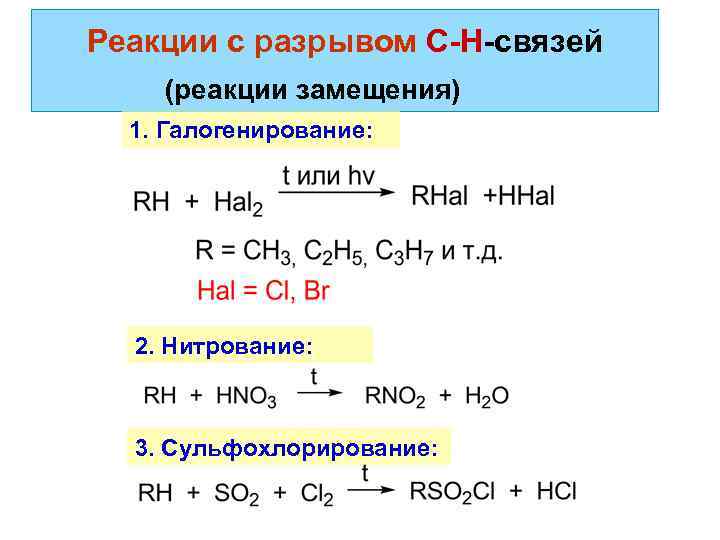 Реакции с разрывом С-Н-связей (реакции замещения) 1. Галогенирование: 2. Нитрование: 3. Сульфохлорирование:
Реакции с разрывом С-Н-связей (реакции замещения) 1. Галогенирование: 2. Нитрование: 3. Сульфохлорирование:
 Механизм реакций замещения Механизм свободнорадикальный, цепной
Механизм реакций замещения Механизм свободнорадикальный, цепной
 Как найти химика? Если хочешь найти химика, спроси, что такое моль и неионизованный. И если тот начнет говорить о пушных зверях и организации труда, спокойно уходи. Писатель-фантаст, популяризатор науки Айзек Азимов (1920– 1992) Рис. Источник: http: //images. yandex. ru.
Как найти химика? Если хочешь найти химика, спроси, что такое моль и неионизованный. И если тот начнет говорить о пушных зверях и организации труда, спокойно уходи. Писатель-фантаст, популяризатор науки Айзек Азимов (1920– 1992) Рис. Источник: http: //images. yandex. ru.
 1. Реакция галогенирования • Хлорирование: RH + Cl 2 hv RCl + HCl • Бромирование: RH + Br 2 hv RBr + HBr • Например, хлорирование метана: CH 4 + Cl 2 CH 3 Cl + HCl
1. Реакция галогенирования • Хлорирование: RH + Cl 2 hv RCl + HCl • Бромирование: RH + Br 2 hv RBr + HBr • Например, хлорирование метана: CH 4 + Cl 2 CH 3 Cl + HCl
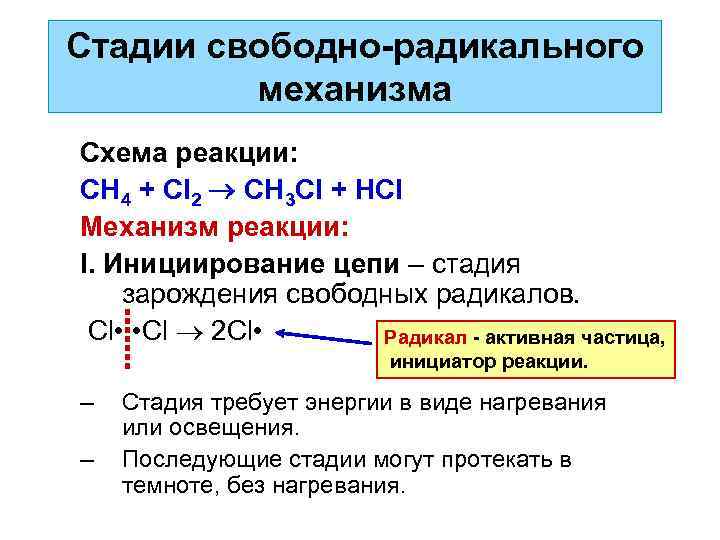 Стадии свободно-радикального механизма Схема реакции: CH 4 + Cl 2 CH 3 Cl + HCl Механизм реакции: I. Инициирование цепи – стадия зарождения свободных радикалов. Cl • • Cl 2 Cl • Радикал - активная частица, инициатор реакции. – – Стадия требует энергии в виде нагревания или освещения. Последующие стадии могут протекать в темноте, без нагревания.
Стадии свободно-радикального механизма Схема реакции: CH 4 + Cl 2 CH 3 Cl + HCl Механизм реакции: I. Инициирование цепи – стадия зарождения свободных радикалов. Cl • • Cl 2 Cl • Радикал - активная частица, инициатор реакции. – – Стадия требует энергии в виде нагревания или освещения. Последующие стадии могут протекать в темноте, без нагревания.
 Стадии свободно-радикального механизма II. Рост цепи – основная стадия. CH 4 + Cl • HCl + CH 3 • + Cl 2 CH 3 Cl + Cl • Стадия может включать несколько подстадий, на каждой из которых образуется новый радикал, но не Н • !!! На II, основной стадии, обязательно образуется основной продукт!
Стадии свободно-радикального механизма II. Рост цепи – основная стадия. CH 4 + Cl • HCl + CH 3 • + Cl 2 CH 3 Cl + Cl • Стадия может включать несколько подстадий, на каждой из которых образуется новый радикал, но не Н • !!! На II, основной стадии, обязательно образуется основной продукт!
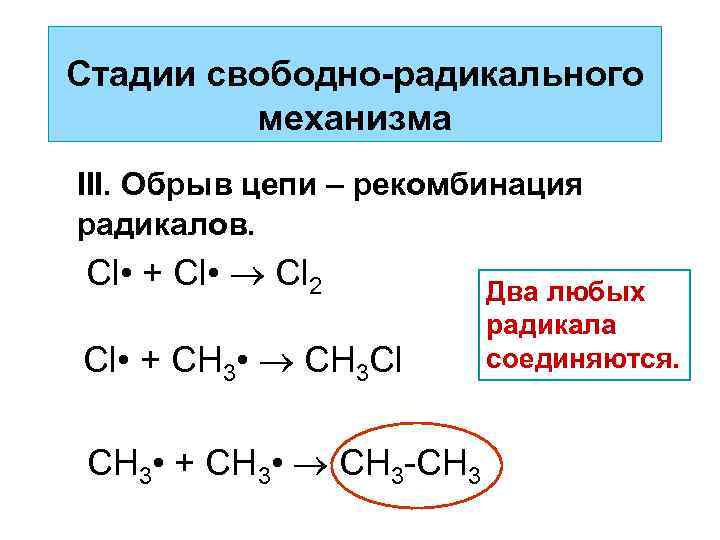 Стадии свободно-радикального механизма III. Обрыв цепи – рекомбинация радикалов. Cl • + Cl • Cl 2 Cl • + CH 3 • CH 3 Cl CH 3 • + CH 3 • CH 3 -CH 3 Два любых радикала соединяются.
Стадии свободно-радикального механизма III. Обрыв цепи – рекомбинация радикалов. Cl • + Cl • Cl 2 Cl • + CH 3 • CH 3 Cl CH 3 • + CH 3 • CH 3 -CH 3 Два любых радикала соединяются.
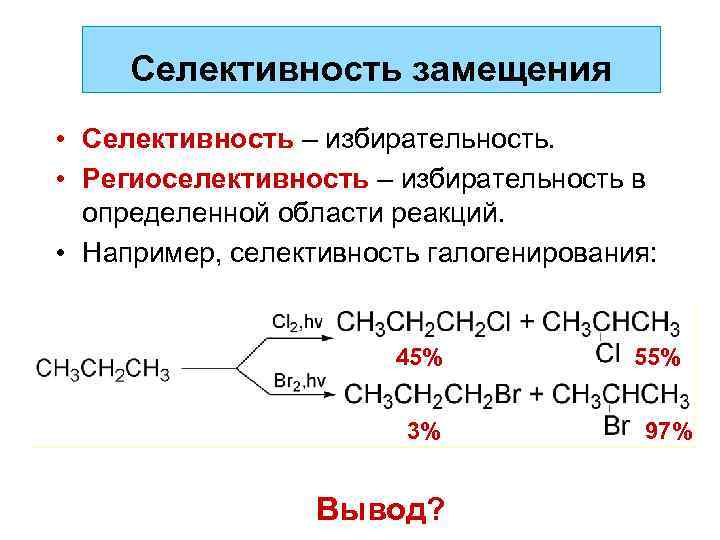 Селективность замещения • Селективность – избирательность. • Региоселективность – избирательность в определенной области реакций. • Например, селективность галогенирования: 45% 3% Вывод? 55% 97%
Селективность замещения • Селективность – избирательность. • Региоселективность – избирательность в определенной области реакций. • Например, селективность галогенирования: 45% 3% Вывод? 55% 97%
 Селективность галогенирования зависит от следующих факторов: • Условия реакции. При низких температурах идет более селективно. • Природа галогена. Чем активнее галоген, тем менее избирательна реакция. F 2 реагирует очень энергично, с разрушением С-С-связей. I 2 не реагирует с алканами в указанных условиях. • Строение алкана.
Селективность галогенирования зависит от следующих факторов: • Условия реакции. При низких температурах идет более селективно. • Природа галогена. Чем активнее галоген, тем менее избирательна реакция. F 2 реагирует очень энергично, с разрушением С-С-связей. I 2 не реагирует с алканами в указанных условиях. • Строение алкана.
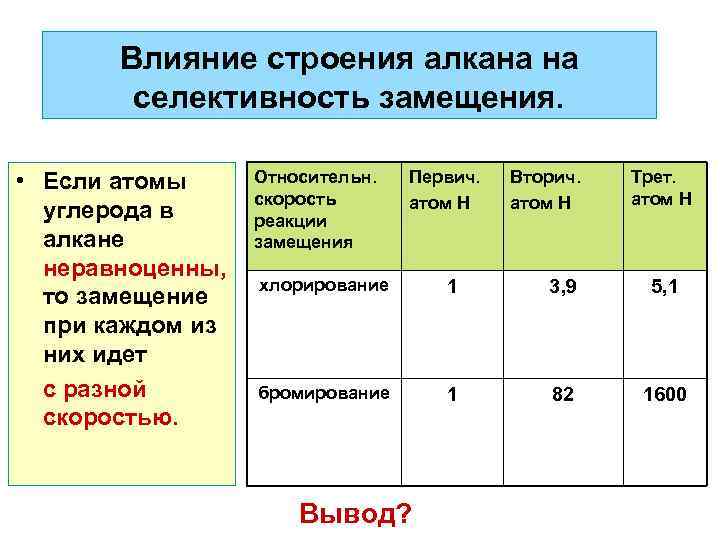 Влияние строения алкана на селективность замещения. • Если атомы углерода в алкане неравноценны, то замещение при каждом из них идет с разной скоростью. Относительн. скорость реакции замещения Первич. атом Н Вторич. атом Н Трет. атом Н хлорирование 1 3, 9 5, 1 бромирование 1 82 1600 Вывод?
Влияние строения алкана на селективность замещения. • Если атомы углерода в алкане неравноценны, то замещение при каждом из них идет с разной скоростью. Относительн. скорость реакции замещения Первич. атом Н Вторич. атом Н Трет. атом Н хлорирование 1 3, 9 5, 1 бромирование 1 82 1600 Вывод?
 Для отрыва третичного атома водорода требуется меньше энергии, чем для отрыва вторичного и первичного! Формула алкана Результат гомолиза ЕД, к. Дж/моль СН 4 СН 3 • + Н • 435 СН 3 - СН 3 С 2 Н 5 • + Н • 410 СН 3 СН 2 СН 3 (СН 3)2 СН • + Н • 395 (СН 3)3 СН (СН 3)3 С • + Н • 377
Для отрыва третичного атома водорода требуется меньше энергии, чем для отрыва вторичного и первичного! Формула алкана Результат гомолиза ЕД, к. Дж/моль СН 4 СН 3 • + Н • 435 СН 3 - СН 3 С 2 Н 5 • + Н • 410 СН 3 СН 2 СН 3 (СН 3)2 СН • + Н • 395 (СН 3)3 СН (СН 3)3 С • + Н • 377
 Направление протекания реакций • Любая реакция протекает преимущественно в направлении образования более устойчивой промежуточной частицы!
Направление протекания реакций • Любая реакция протекает преимущественно в направлении образования более устойчивой промежуточной частицы!
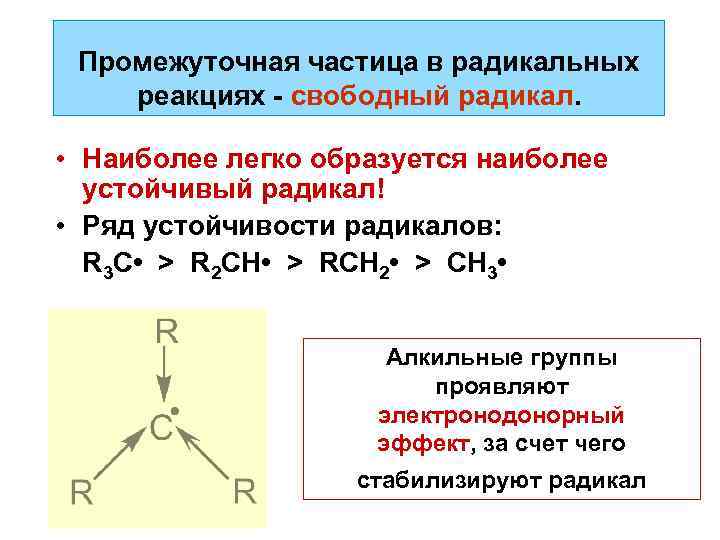 Промежуточная частица в радикальных реакциях - свободный радикал. • Наиболее легко образуется наиболее устойчивый радикал! • Ряд устойчивости радикалов: R 3 C • > R 2 CH • > RCH 2 • > CH 3 • Алкильные группы проявляют электронодонорный эффект, за счет чего стабилизируют радикал
Промежуточная частица в радикальных реакциях - свободный радикал. • Наиболее легко образуется наиболее устойчивый радикал! • Ряд устойчивости радикалов: R 3 C • > R 2 CH • > RCH 2 • > CH 3 • Алкильные группы проявляют электронодонорный эффект, за счет чего стабилизируют радикал
 Реакция сульфохлорирования Схема реакции: RH + Cl 2 + SO 2 RSO 2 Cl + HCl Механизм реакции: 1. Cl • • Cl 2 Cl • 2. RH + Cl • R • + HCl R • + SO 2 RSO 2 • + Cl 2 RSO 2 Cl + Cl • и т. д. 3. 2 Cl • Cl 2 и т. д.
Реакция сульфохлорирования Схема реакции: RH + Cl 2 + SO 2 RSO 2 Cl + HCl Механизм реакции: 1. Cl • • Cl 2 Cl • 2. RH + Cl • R • + HCl R • + SO 2 RSO 2 • + Cl 2 RSO 2 Cl + Cl • и т. д. 3. 2 Cl • Cl 2 и т. д.
 Реакция Коновалова Д. П. Нитрование по Коновалову проводят действием разбавленной азотной кислоты при температуре 140 о. С. Схема реакции: RH + HNO 3 RNO 2 + H 2 O
Реакция Коновалова Д. П. Нитрование по Коновалову проводят действием разбавленной азотной кислоты при температуре 140 о. С. Схема реакции: RH + HNO 3 RNO 2 + H 2 O
 Механизм реакции Коновалова HNO 3 N 2 O 4 1. N 2 O 4 2 NO 2 • 2. RH + NO 2 • R • + HNO 2 R • + HNO 3 RNO 2 + • OH RH + • OH R • + H 2 O и т. д. 3. Обрыв цепи.
Механизм реакции Коновалова HNO 3 N 2 O 4 1. N 2 O 4 2 NO 2 • 2. RH + NO 2 • R • + HNO 2 R • + HNO 3 RNO 2 + • OH RH + • OH R • + H 2 O и т. д. 3. Обрыв цепи.
 Приведите схему и механизм реакции монобромирования 2 -метилпропана
Приведите схему и механизм реакции монобромирования 2 -метилпропана
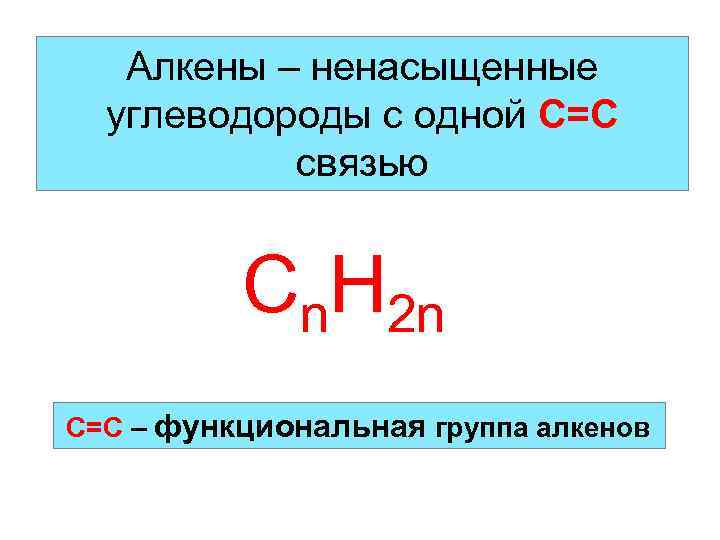 Алкены – ненасыщенные углеводороды с одной С=С связью Cn. H 2 n С=С – функциональная группа алкенов
Алкены – ненасыщенные углеводороды с одной С=С связью Cn. H 2 n С=С – функциональная группа алкенов
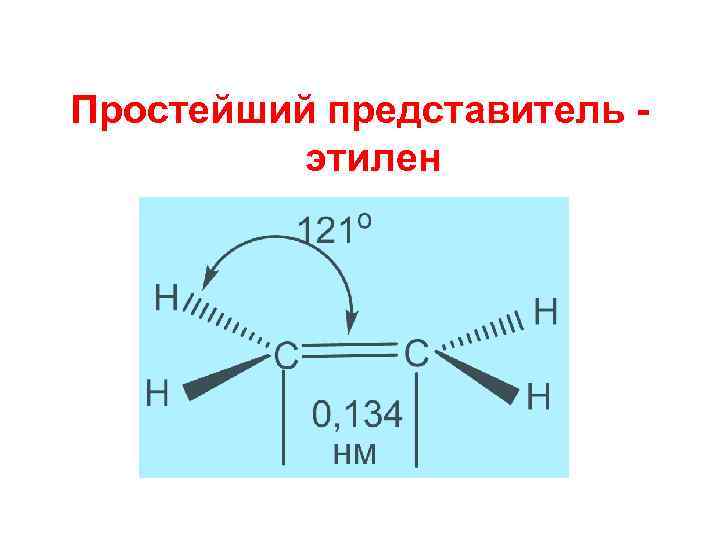 Простейший представитель этилен
Простейший представитель этилен
 Этилен, выделяемый яблоками, ускоряет созревание плодов и ягод: Рис. Источник: http: //images. yandex. ru.
Этилен, выделяемый яблоками, ускоряет созревание плодов и ягод: Рис. Источник: http: //images. yandex. ru.
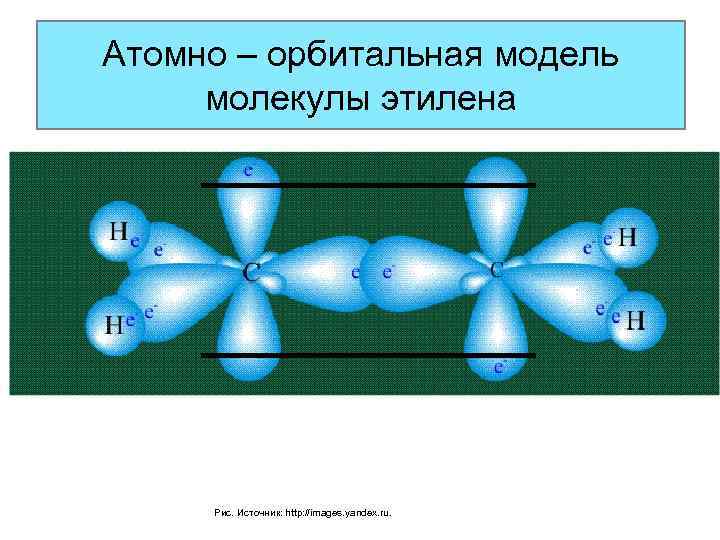 Атомно – орбитальная модель молекулы этилена Рис. Источник: http: //images. yandex. ru.
Атомно – орбитальная модель молекулы этилена Рис. Источник: http: //images. yandex. ru.
 Химические свойства алкенов • Общая характеристика Алкены – реакционноспособный класс соединений. Они вступают в многочисленные реакции, большинство из которых идут за счет разрыва менее прочной пи-связи. Е С-С (σ-) ~ 350 Кдж/моль Е С=С ( -) ~ 260 Кдж/моль
Химические свойства алкенов • Общая характеристика Алкены – реакционноспособный класс соединений. Они вступают в многочисленные реакции, большинство из которых идут за счет разрыва менее прочной пи-связи. Е С-С (σ-) ~ 350 Кдж/моль Е С=С ( -) ~ 260 Кдж/моль
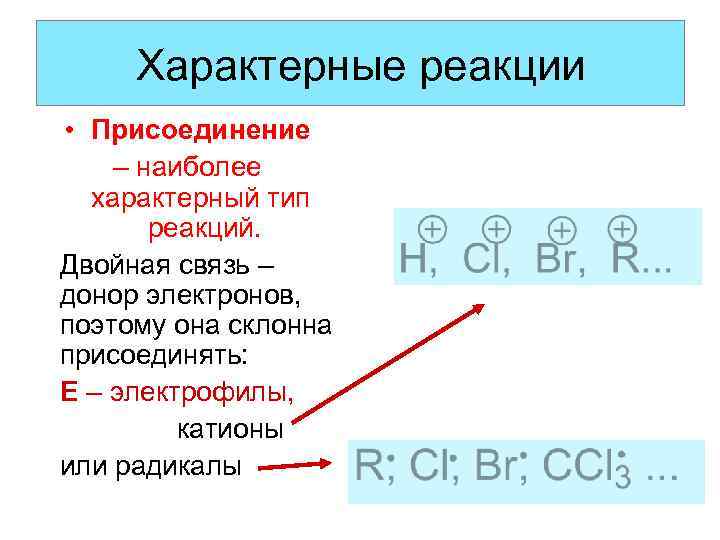 Характерные реакции • Присоединение – наиболее характерный тип реакций. Двойная связь – донор электронов, поэтому она склонна присоединять: Е – электрофилы, катионы или радикалы
Характерные реакции • Присоединение – наиболее характерный тип реакций. Двойная связь – донор электронов, поэтому она склонна присоединять: Е – электрофилы, катионы или радикалы
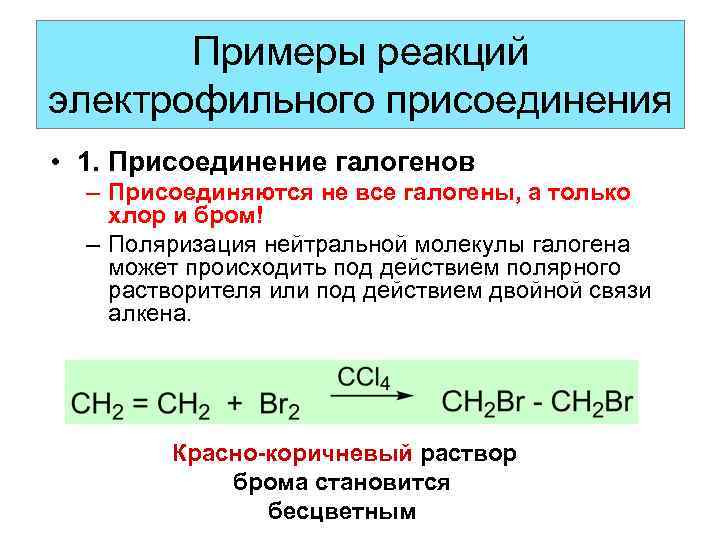 Примеры реакций электрофильного присоединения • 1. Присоединение галогенов – Присоединяются не все галогены, а только хлор и бром! – Поляризация нейтральной молекулы галогена может происходить под действием полярного растворителя или под действием двойной связи алкена. Красно-коричневый раствор брома становится бесцветным
Примеры реакций электрофильного присоединения • 1. Присоединение галогенов – Присоединяются не все галогены, а только хлор и бром! – Поляризация нейтральной молекулы галогена может происходить под действием полярного растворителя или под действием двойной связи алкена. Красно-коричневый раствор брома становится бесцветным
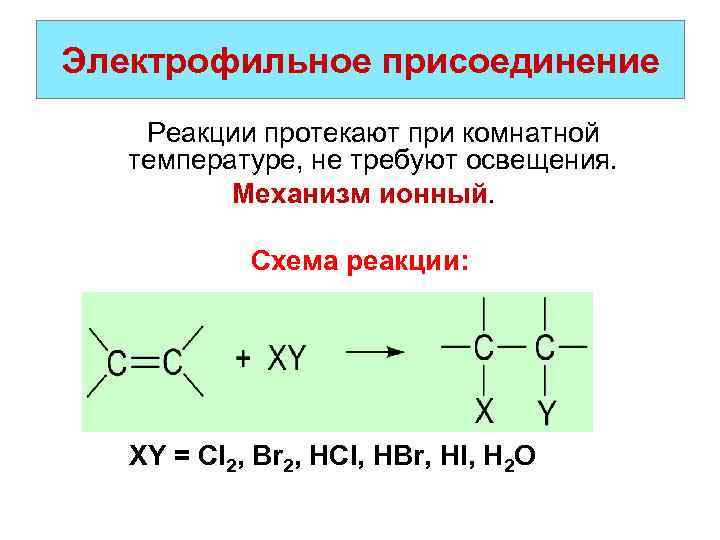 Электрофильное присоединение Реакции протекают при комнатной температуре, не требуют освещения. Механизм ионный. Схема реакции: XY = Cl 2, Br 2, HCl, HBr, HI, H 2 O
Электрофильное присоединение Реакции протекают при комнатной температуре, не требуют освещения. Механизм ионный. Схема реакции: XY = Cl 2, Br 2, HCl, HBr, HI, H 2 O
 Механизм электрофильного присоединения lim - комплекс σ- комплекс
Механизм электрофильного присоединения lim - комплекс σ- комплекс
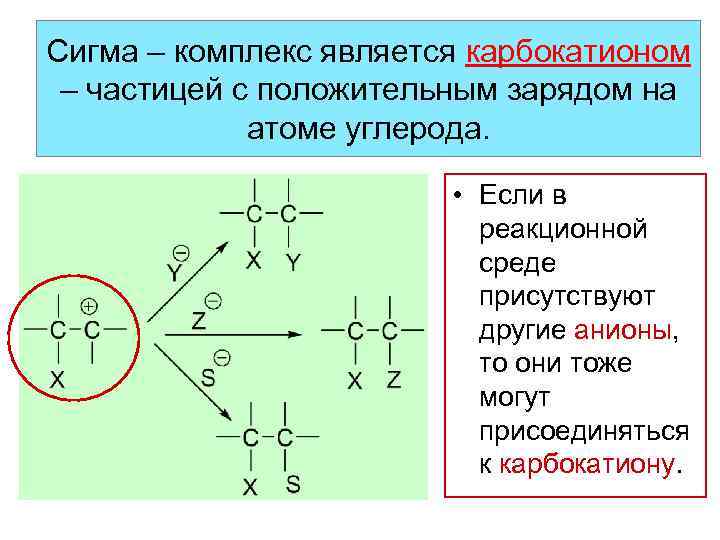 Сигма – комплекс является карбокатионом – частицей с положительным зарядом на атоме углерода. • Если в реакционной среде присутствуют другие анионы, то они тоже могут присоединяться к карбокатиону.
Сигма – комплекс является карбокатионом – частицей с положительным зарядом на атоме углерода. • Если в реакционной среде присутствуют другие анионы, то они тоже могут присоединяться к карбокатиону.
 Например, присоединение брома, растворенного в воде. • Эта качественная реакция на двойную С=С-связь протекает с обесцвечиванием раствора брома и образованием двух продуктов:
Например, присоединение брома, растворенного в воде. • Эта качественная реакция на двойную С=С-связь протекает с обесцвечиванием раствора брома и образованием двух продуктов:
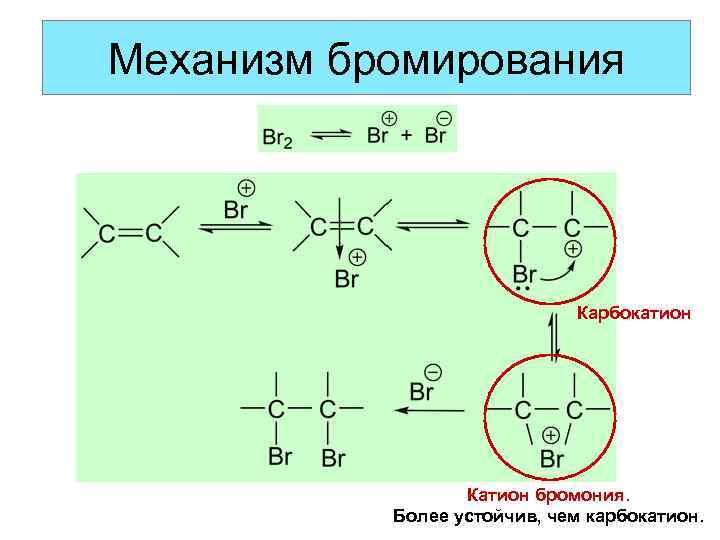 Механизм бромирования Карбокатион Катион бромония. Более устойчив, чем карбокатион.
Механизм бромирования Карбокатион Катион бромония. Более устойчив, чем карбокатион.
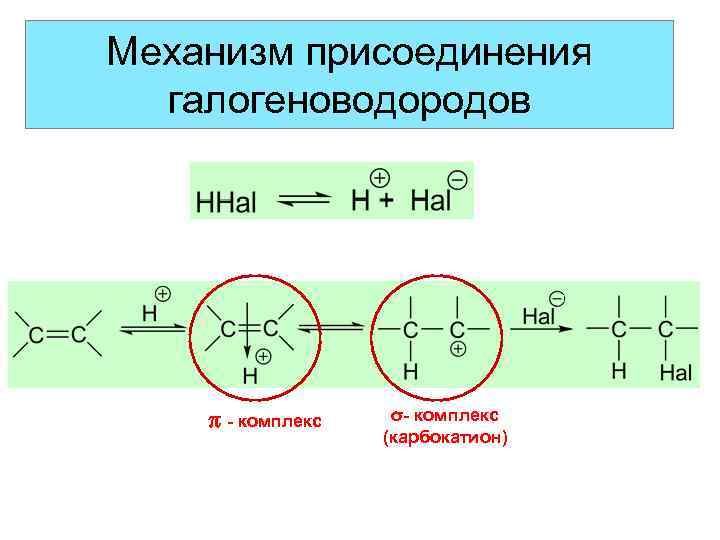 Механизм присоединения галогеноводородов - комплекс σ- комплекс (карбокатион)
Механизм присоединения галогеноводородов - комплекс σ- комплекс (карбокатион)
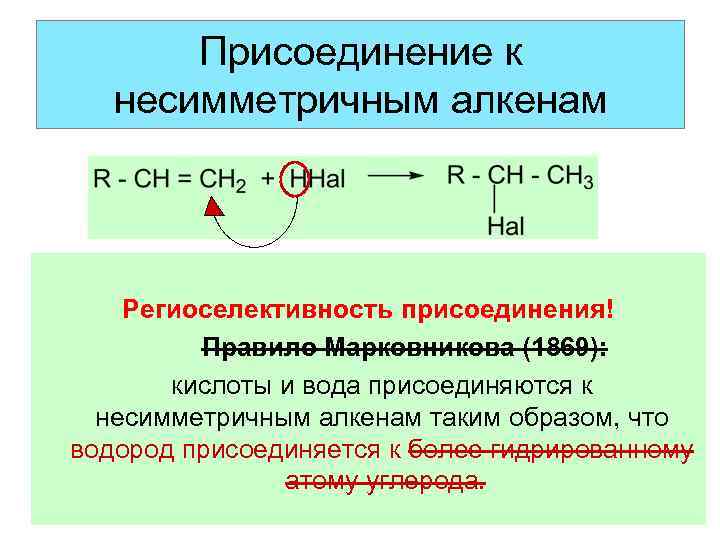 Присоединение к несимметричным алкенам Региоселективность присоединения! Правило Марковникова (1869): кислоты и вода присоединяются к несимметричным алкенам таким образом, что водород присоединяется к более гидрированному атому углерода.
Присоединение к несимметричным алкенам Региоселективность присоединения! Правило Марковникова (1869): кислоты и вода присоединяются к несимметричным алкенам таким образом, что водород присоединяется к более гидрированному атому углерода.
 Марковников Владимир Васильевич (1837 - 1904) • Выпускник Казанского университета. • С 1869 года – профессор кафедры химии. • Основатель научной школы. Рис. Источник: http: //images. yandex. ru.
Марковников Владимир Васильевич (1837 - 1904) • Выпускник Казанского университета. • С 1869 года – профессор кафедры химии. • Основатель научной школы. Рис. Источник: http: //images. yandex. ru.
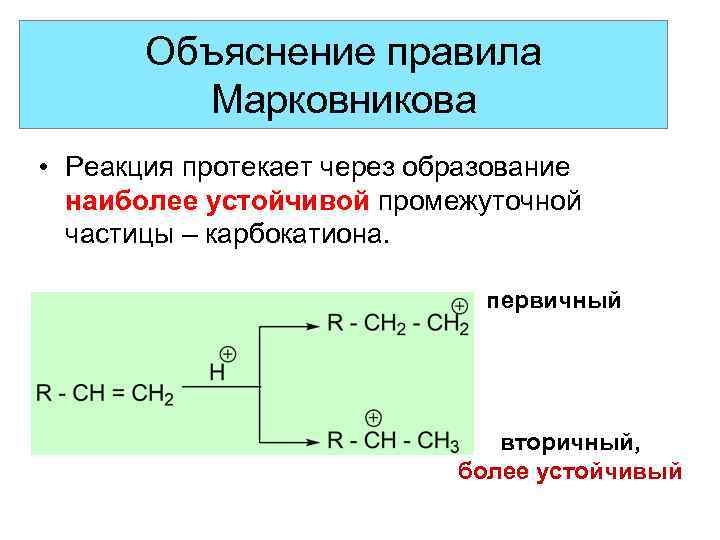 Объяснение правила Марковникова • Реакция протекает через образование наиболее устойчивой промежуточной частицы – карбокатиона. первичный вторичный, более устойчивый
Объяснение правила Марковникова • Реакция протекает через образование наиболее устойчивой промежуточной частицы – карбокатиона. первичный вторичный, более устойчивый
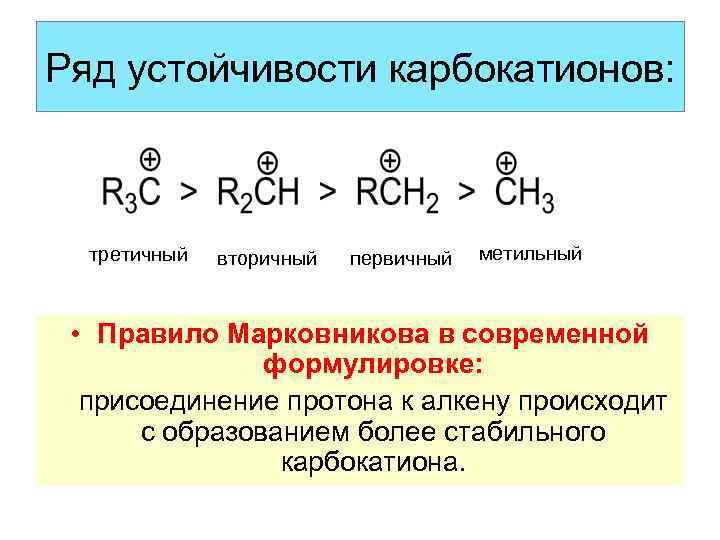 Ряд устойчивости карбокатионов: третичный вторичный первичный метильный • Правило Марковникова в современной формулировке: присоединение протона к алкену происходит с образованием более стабильного карбокатиона.
Ряд устойчивости карбокатионов: третичный вторичный первичный метильный • Правило Марковникова в современной формулировке: присоединение протона к алкену происходит с образованием более стабильного карбокатиона.
 Третичный карбокатион Устойчивы за счет электронодонорного влияния радикалов
Третичный карбокатион Устойчивы за счет электронодонорного влияния радикалов
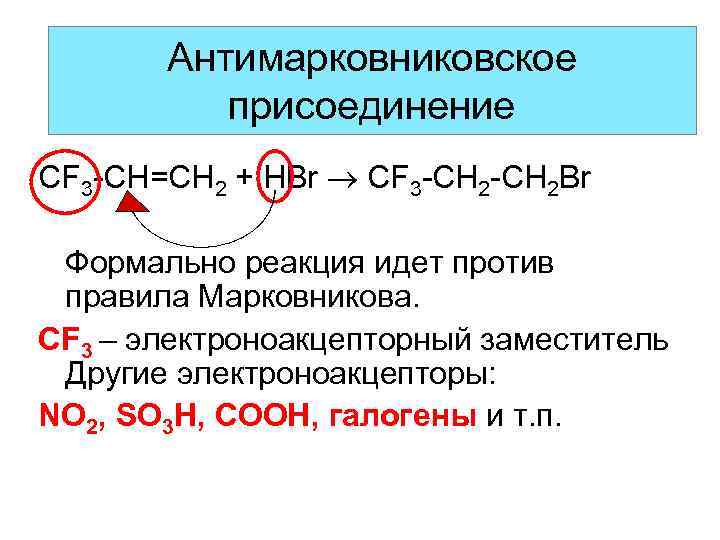 Антимарковниковское присоединение CF 3 -CH=CH 2 + HBr CF 3 -CH 2 Br Формально реакция идет против правила Марковникова. CF 3 – электроноакцепторный заместитель Другие электроноакцепторы: NO 2, SO 3 H, COOH, галогены и т. п.
Антимарковниковское присоединение CF 3 -CH=CH 2 + HBr CF 3 -CH 2 Br Формально реакция идет против правила Марковникова. CF 3 – электроноакцепторный заместитель Другие электроноакцепторы: NO 2, SO 3 H, COOH, галогены и т. п.
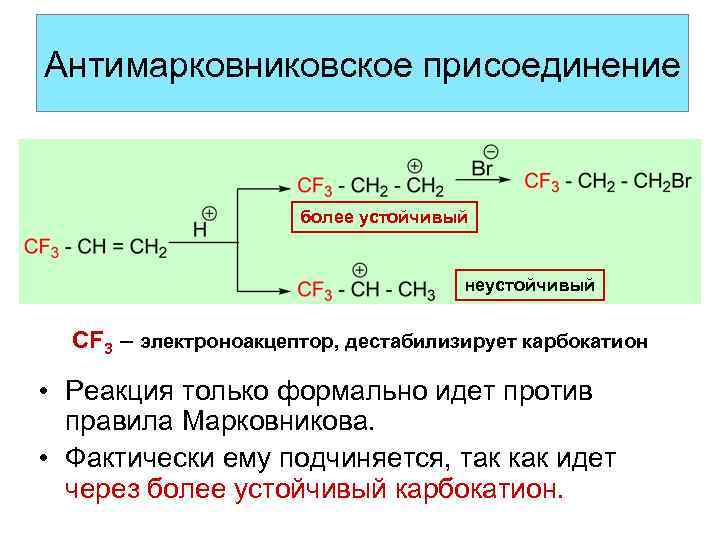 Антимарковниковское присоединение более устойчивый неустойчивый CF 3 – электроноакцептор, дестабилизирует карбокатион • Реакция только формально идет против правила Марковникова. • Фактически ему подчиняется, так как идет через более устойчивый карбокатион.
Антимарковниковское присоединение более устойчивый неустойчивый CF 3 – электроноакцептор, дестабилизирует карбокатион • Реакция только формально идет против правила Марковникова. • Фактически ему подчиняется, так как идет через более устойчивый карбокатион.
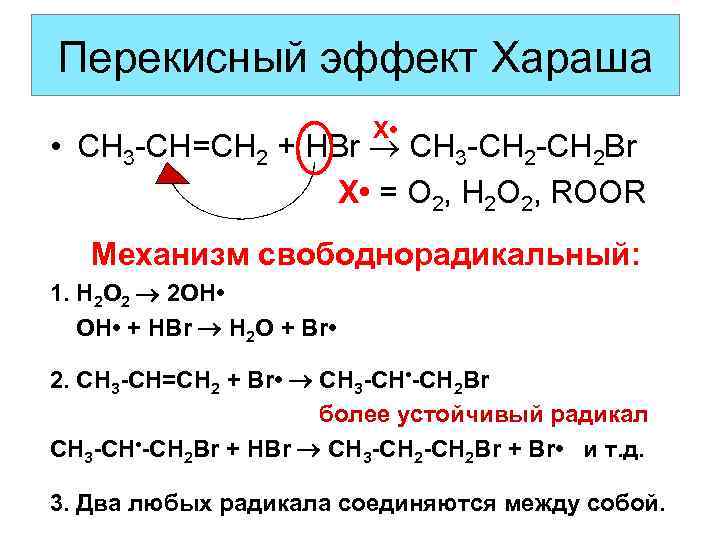 Перекисный эффект Хараша X • • CH 3 -CH=CH 2 + HBr CH 3 -CH 2 Br X • = O 2, H 2 O 2, ROOR Механизм свободнорадикальный: 1. H 2 O 2 2 OH • + HBr H 2 O + Br • 2. CH 3 -CH=CH 2 + Br • CH 3 -CH • -CH 2 Br более устойчивый радикал CH 3 -CH • -CH 2 Br + HBr CH 3 -CH 2 Br + Br • и т. д. 3. Два любых радикала соединяются между собой.
Перекисный эффект Хараша X • • CH 3 -CH=CH 2 + HBr CH 3 -CH 2 Br X • = O 2, H 2 O 2, ROOR Механизм свободнорадикальный: 1. H 2 O 2 2 OH • + HBr H 2 O + Br • 2. CH 3 -CH=CH 2 + Br • CH 3 -CH • -CH 2 Br более устойчивый радикал CH 3 -CH • -CH 2 Br + HBr CH 3 -CH 2 Br + Br • и т. д. 3. Два любых радикала соединяются между собой.
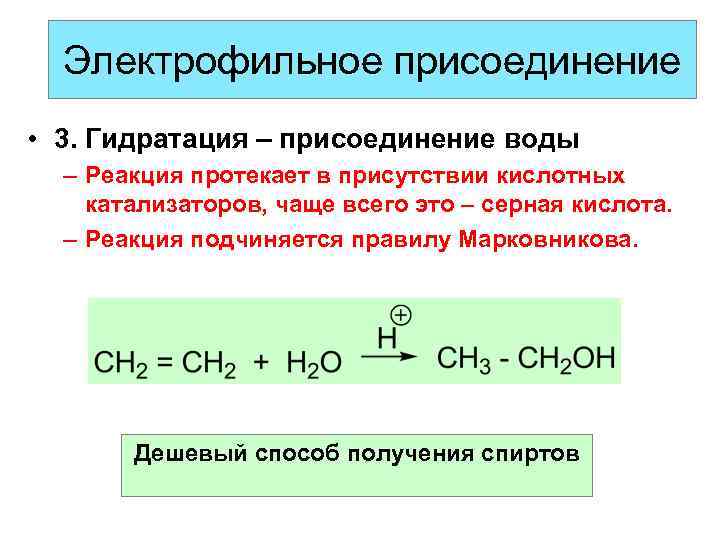 Электрофильное присоединение • 3. Гидратация – присоединение воды – Реакция протекает в присутствии кислотных катализаторов, чаще всего это – серная кислота. – Реакция подчиняется правилу Марковникова. Дешевый способ получения спиртов
Электрофильное присоединение • 3. Гидратация – присоединение воды – Реакция протекает в присутствии кислотных катализаторов, чаще всего это – серная кислота. – Реакция подчиняется правилу Марковникова. Дешевый способ получения спиртов
 На экзамене академик Иван Алексеевич Каблуков просит студента рассказать, как в лаборатории получают водород. • «Из ртути» , — отвечает тот. • «Как это "из ртути"? ! Обычно говорят "из цинка", а вот из ртути — это что-то оригинальное. Напишите-ка реакцию» . Студент пишет: • Hg = Н + g • И говорит: «Ртуть нагревают; она разлагается на Н и g. Н — водород, он легкий и поэтому улетает, а g — ускорение силы тяжести, тяжелое, остается» . • «За такой ответ надо ставить "пятерку", — говорит Каблуков. — Давайте зачетку. Только "пятерку" я сначала тоже подогрею. "Три" улетает, а "два" остается» .
На экзамене академик Иван Алексеевич Каблуков просит студента рассказать, как в лаборатории получают водород. • «Из ртути» , — отвечает тот. • «Как это "из ртути"? ! Обычно говорят "из цинка", а вот из ртути — это что-то оригинальное. Напишите-ка реакцию» . Студент пишет: • Hg = Н + g • И говорит: «Ртуть нагревают; она разлагается на Н и g. Н — водород, он легкий и поэтому улетает, а g — ускорение силы тяжести, тяжелое, остается» . • «За такой ответ надо ставить "пятерку", — говорит Каблуков. — Давайте зачетку. Только "пятерку" я сначала тоже подогрею. "Три" улетает, а "два" остается» .
 Приведите схему и механизм реакции гидробромирования бутена-1.
Приведите схему и механизм реакции гидробромирования бутена-1.
 Двое химиков в лаборатории: - Вась, опусти руку в этот стакан. - Опустил. - Что-нибудь чувствуешь? - Нет. - Значит серная кислота в другом стакане.
Двое химиков в лаборатории: - Вась, опусти руку в этот стакан. - Опустил. - Что-нибудь чувствуешь? - Нет. - Значит серная кислота в другом стакане.
 Ароматические углеводороды • Ароматический – душистый? ? • Ароматические соединения – это бензол и вещества, напоминающие его по химическому поведению!
Ароматические углеводороды • Ароматический – душистый? ? • Ароматические соединения – это бензол и вещества, напоминающие его по химическому поведению!
 Бензоидные ароматические углеводороды бензол нафталин антрацен Рис. Источник: http: //images. yandex. ru. фенантрен
Бензоидные ароматические углеводороды бензол нафталин антрацен Рис. Источник: http: //images. yandex. ru. фенантрен
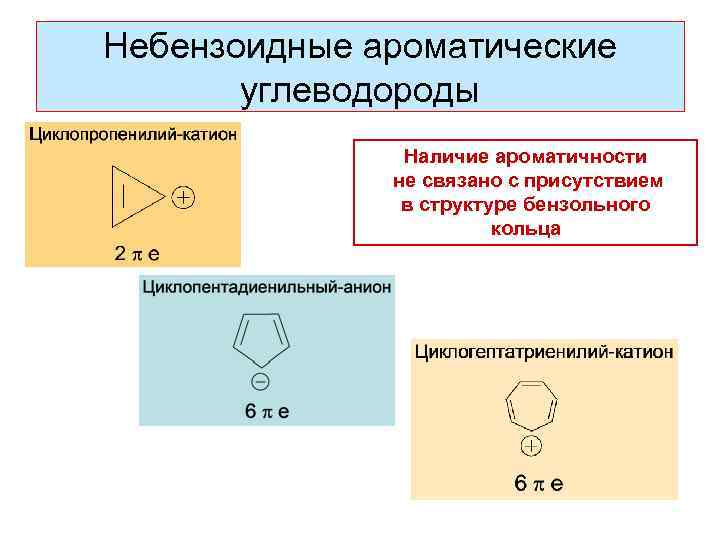 Небензоидные ароматические углеводороды Наличие ароматичности не связано с присутствием в структуре бензольного кольца
Небензоидные ароматические углеводороды Наличие ароматичности не связано с присутствием в структуре бензольного кольца
 История вопроса С 6 Н 6 Структуры Кекуле: Формула Кекуле. Почему она не удовлетворяла химиков? ? ?
История вопроса С 6 Н 6 Структуры Кекуле: Формула Кекуле. Почему она не удовлетворяла химиков? ? ?
 Рис. Источник: http: //images. yandex. ru.
Рис. Источник: http: //images. yandex. ru.
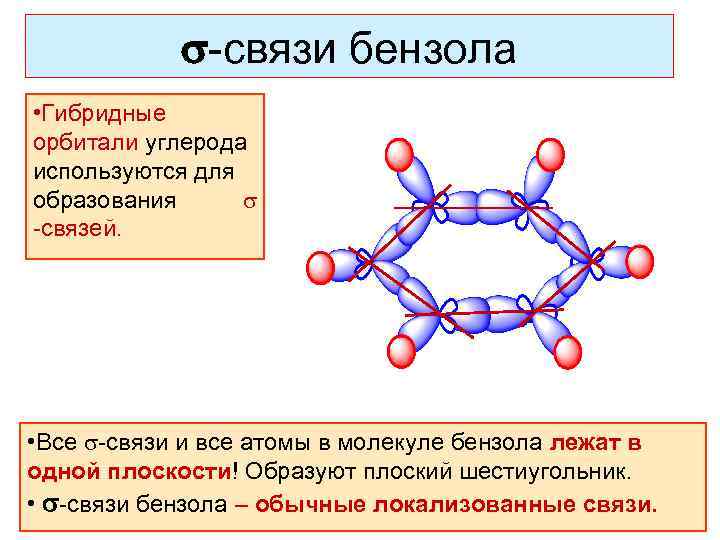 -связи бензола • Гибридные орбитали углерода используются для образования -связей. • Все -связи и все атомы в молекуле бензола лежат в одной плоскости! Образуют плоский шестиугольник. • -связи бензола – обычные локализованные связи.
-связи бензола • Гибридные орбитали углерода используются для образования -связей. • Все -связи и все атомы в молекуле бензола лежат в одной плоскости! Образуют плоский шестиугольник. • -связи бензола – обычные локализованные связи.
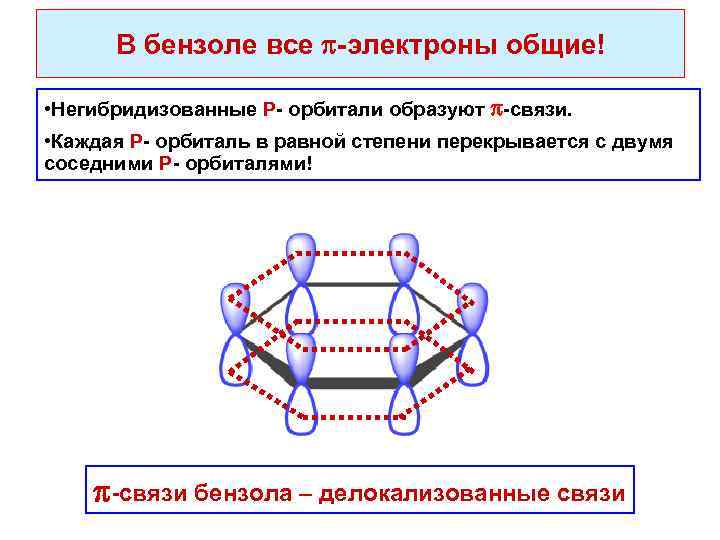 В бензоле все -электроны общие! • Негибридизованные Р- орбитали образуют -связи. • Каждая Р- орбиталь в равной степени перекрывается с двумя соседними Р- орбиталями! -связи бензола – делокализованные связи
В бензоле все -электроны общие! • Негибридизованные Р- орбитали образуют -связи. • Каждая Р- орбиталь в равной степени перекрывается с двумя соседними Р- орбиталями! -связи бензола – делокализованные связи
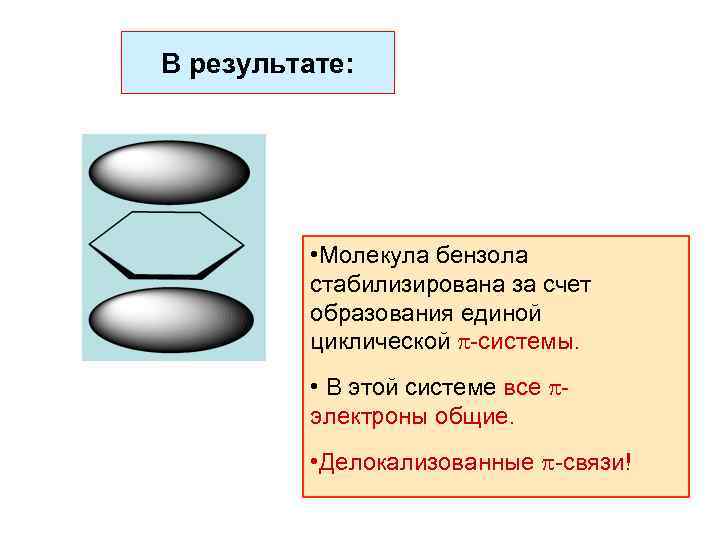 В результате: • Молекула бензола стабилизирована за счет образования единой циклической -системы. • В этой системе все электроны общие. • Делокализованные -связи!
В результате: • Молекула бензола стабилизирована за счет образования единой циклической -системы. • В этой системе все электроны общие. • Делокализованные -связи!
 Рис. Источник: http: //images. yandex. ru.
Рис. Источник: http: //images. yandex. ru.
 Что такое ароматичность? Ароматичность – это свойство циклической сопряженной молекулы приобретать аномальную стабильность за счет образования замкнутой делокализованной -электронной системы.
Что такое ароматичность? Ароматичность – это свойство циклической сопряженной молекулы приобретать аномальную стабильность за счет образования замкнутой делокализованной -электронной системы.
 Химические свойства бензола • I. Реакции замещения • II. Реакции, (характерные реакции). приводящие к неароматическим – Нитрование соединениям. – Сульфирование – Гидрирование – Хлорирование – Присоединение – Бромирование хлора – Алкилирование – Окисление – Ацилирование - Изомеризация
Химические свойства бензола • I. Реакции замещения • II. Реакции, (характерные реакции). приводящие к неароматическим – Нитрование соединениям. – Сульфирование – Гидрирование – Хлорирование – Присоединение – Бромирование хлора – Алкилирование – Окисление – Ацилирование - Изомеризация
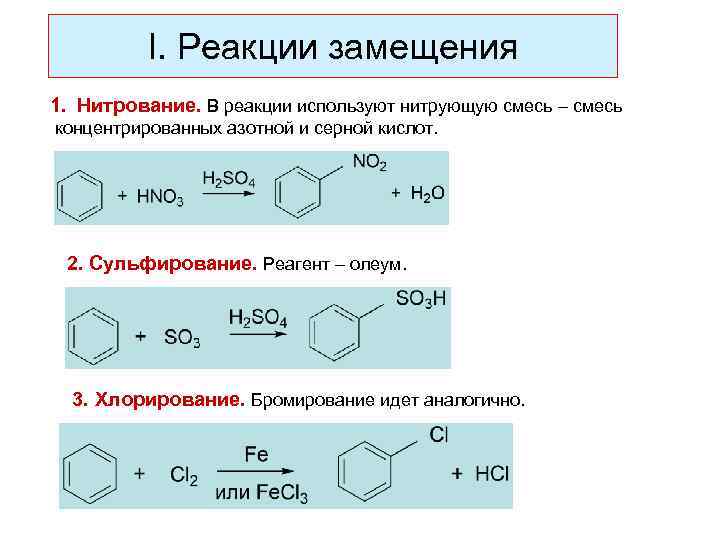 I. Реакции замещения 1. Нитрование. В реакции используют нитрующую смесь – смесь концентрированных азотной и серной кислот. 2. Сульфирование. Реагент – олеум. 3. Хлорирование. Бромирование идет аналогично.
I. Реакции замещения 1. Нитрование. В реакции используют нитрующую смесь – смесь концентрированных азотной и серной кислот. 2. Сульфирование. Реагент – олеум. 3. Хлорирование. Бромирование идет аналогично.
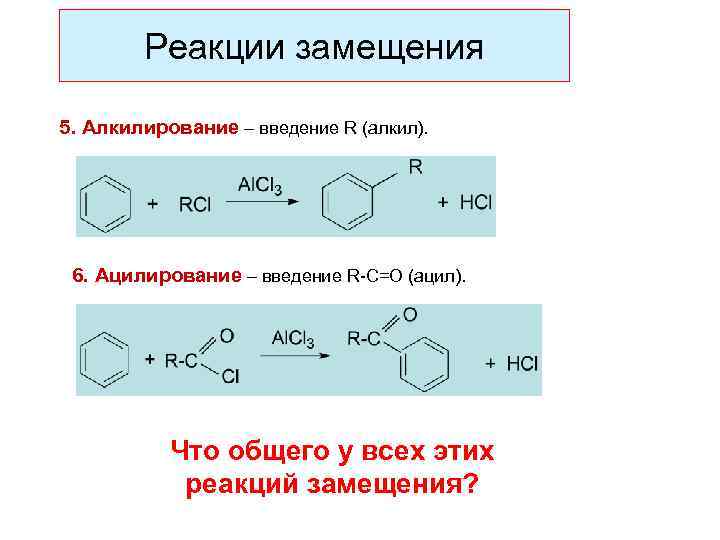 Реакции замещения 5. Алкилирование – введение R (алкил). 6. Ацилирование – введение R-C=O (ацил). Что общего у всех этих реакций замещения?
Реакции замещения 5. Алкилирование – введение R (алкил). 6. Ацилирование – введение R-C=O (ацил). Что общего у всех этих реакций замещения?
 1. Сохранение устойчивой ароматической структуры. 2. Использование кислотных катализаторов: минеральных кислот – H 2 SO 4, HNO 3 или кислот Льюиса – Fe. Cl 3, Al. Cl 3. Общий механизм – электрофильное ароматическое замещение.
1. Сохранение устойчивой ароматической структуры. 2. Использование кислотных катализаторов: минеральных кислот – H 2 SO 4, HNO 3 или кислот Льюиса – Fe. Cl 3, Al. Cl 3. Общий механизм – электрофильное ароматическое замещение.
 Генерация электрофильных реагентов
Генерация электрофильных реагентов
 Механизм ароматического электрофильного замещения lim -комплекс, -комплекс результат электростатич. притяжения Рис. Источник: http: //images. yandex. ru. ? ? ?
Механизм ароматического электрофильного замещения lim -комплекс, -комплекс результат электростатич. притяжения Рис. Источник: http: //images. yandex. ru. ? ? ?
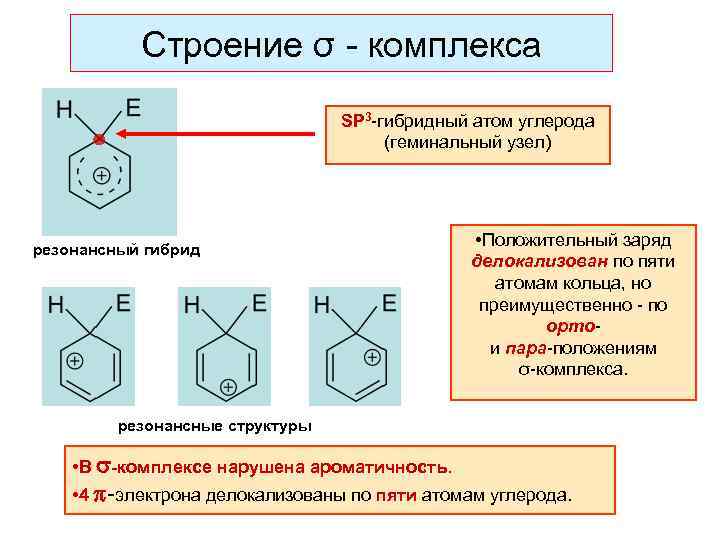 Строение σ - комплекса SP 3 -гибридный атом углерода (геминальный узел) резонансный гибрид • Положительный заряд делокализован по пяти атомам кольца, но преимущественно - по ортои пара-положениям σ-комплекса. резонансные структуры • В -комплексе нарушена ароматичность. • 4 -электрона делокализованы по пяти атомам углерода.
Строение σ - комплекса SP 3 -гибридный атом углерода (геминальный узел) резонансный гибрид • Положительный заряд делокализован по пяти атомам кольца, но преимущественно - по ортои пара-положениям σ-комплекса. резонансные структуры • В -комплексе нарушена ароматичность. • 4 -электрона делокализованы по пяти атомам углерода.
 Закономерности электрофильного замещения • Реакция происходит через образование комплекса и σ-комплекса. • Образование σ-комплекса –самая медленная (лимитирующая) стадия реакции. • Положительный заряд в σ–комплексе делокализован. • Стабилизация σ–комплекса (при введении электронодонорных заместителей) облегчает реакцию электрофильного замещения.
Закономерности электрофильного замещения • Реакция происходит через образование комплекса и σ-комплекса. • Образование σ-комплекса –самая медленная (лимитирующая) стадия реакции. • Положительный заряд в σ–комплексе делокализован. • Стабилизация σ–комплекса (при введении электронодонорных заместителей) облегчает реакцию электрофильного замещения.
 Пример CH 3 Br + Al. Br 3 CH 3 . . . Al. Br 4 – CH 3+ + Al. Br 4 - -комплекс
Пример CH 3 Br + Al. Br 3 CH 3 . . . Al. Br 4 – CH 3+ + Al. Br 4 - -комплекс
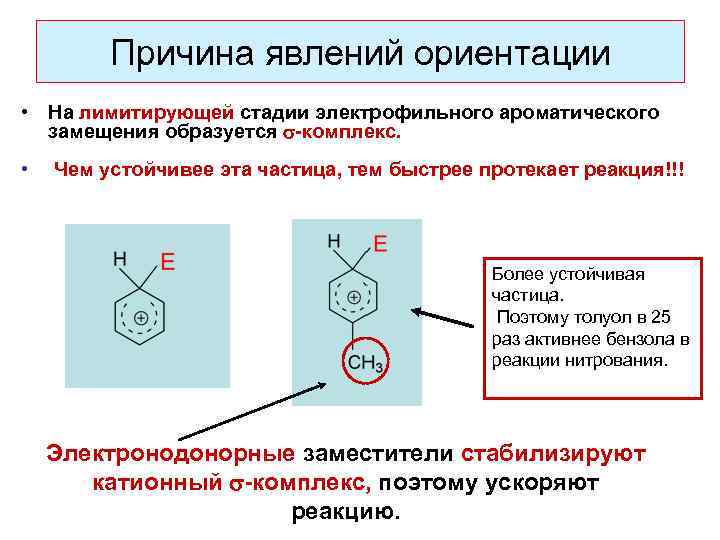 Причина явлений ориентации • На лимитирующей стадии электрофильного ароматического замещения образуется -комплекс. • Чем устойчивее эта частица, тем быстрее протекает реакция!!! Более устойчивая частица. Поэтому толуол в 25 раз активнее бензола в реакции нитрования. Электронодонорные заместители стабилизируют катионный -комплекс, поэтому ускоряют реакцию.
Причина явлений ориентации • На лимитирующей стадии электрофильного ароматического замещения образуется -комплекс. • Чем устойчивее эта частица, тем быстрее протекает реакция!!! Более устойчивая частица. Поэтому толуол в 25 раз активнее бензола в реакции нитрования. Электронодонорные заместители стабилизируют катионный -комплекс, поэтому ускоряют реакцию.
 Приведите схему и механизм реакции мононитрования бензойной кислоты.
Приведите схему и механизм реакции мононитрования бензойной кислоты.
 Как определить в каждом конкретном случае механизм реакции? Рис. Источник: http: //images. yandex. ru.
Как определить в каждом конкретном случае механизм реакции? Рис. Источник: http: //images. yandex. ru.
 • Однажды физик, биолог и химик впервые оказались на берегу океана. • – Ого, какие волны! – произнес физик, направляясь в пучину. – Если построить теорию динамики волн в жидкости, можно будет найти способ спокойно гулять по волнам. • – Смотрите-ка, в океане есть жизнь: рыбы, медузы, ракушки! – воскликнул биолог и тоже погрузился в воду. • Химик долго ожидал их на берегу, затем сделал вывод: - Физики и биологи способны полностью растворяться в океанской воде.
• Однажды физик, биолог и химик впервые оказались на берегу океана. • – Ого, какие волны! – произнес физик, направляясь в пучину. – Если построить теорию динамики волн в жидкости, можно будет найти способ спокойно гулять по волнам. • – Смотрите-ка, в океане есть жизнь: рыбы, медузы, ракушки! – воскликнул биолог и тоже погрузился в воду. • Химик долго ожидал их на берегу, затем сделал вывод: - Физики и биологи способны полностью растворяться в океанской воде.
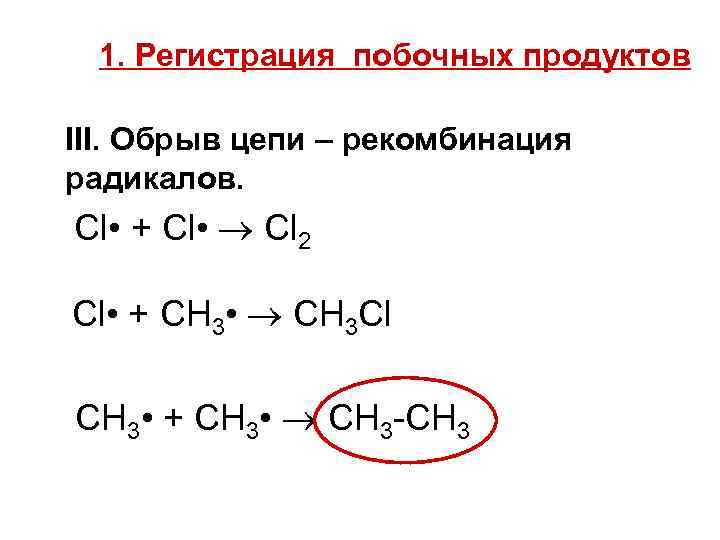 1. Регистрация побочных продуктов III. Обрыв цепи – рекомбинация радикалов. Cl • + Cl • Cl 2 Cl • + CH 3 • CH 3 Cl CH 3 • + CH 3 • CH 3 -CH 3
1. Регистрация побочных продуктов III. Обрыв цепи – рекомбинация радикалов. Cl • + Cl • Cl 2 Cl • + CH 3 • CH 3 Cl CH 3 • + CH 3 • CH 3 -CH 3
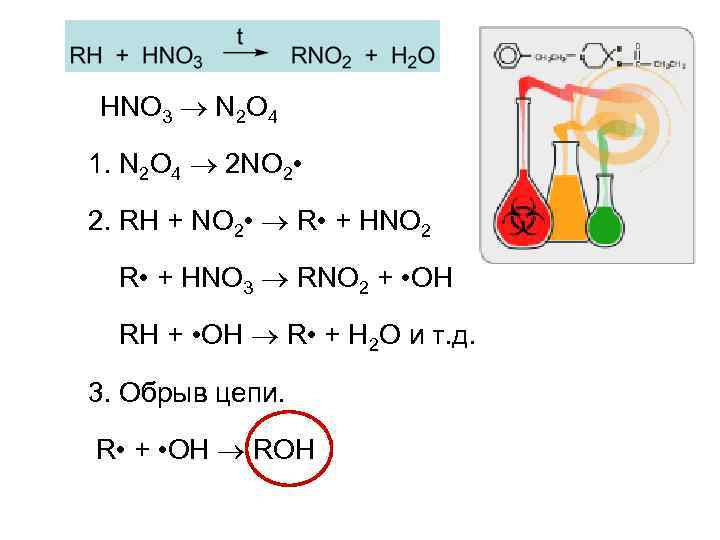 HNO 3 N 2 O 4 1. N 2 O 4 2 NO 2 • 2. RH + NO 2 • R • + HNO 2 R • + HNO 3 RNO 2 + • OH RH + • OH R • + H 2 O и т. д. 3. Обрыв цепи. R • + • OH ROH
HNO 3 N 2 O 4 1. N 2 O 4 2 NO 2 • 2. RH + NO 2 • R • + HNO 2 R • + HNO 3 RNO 2 + • OH RH + • OH R • + H 2 O и т. д. 3. Обрыв цепи. R • + • OH ROH
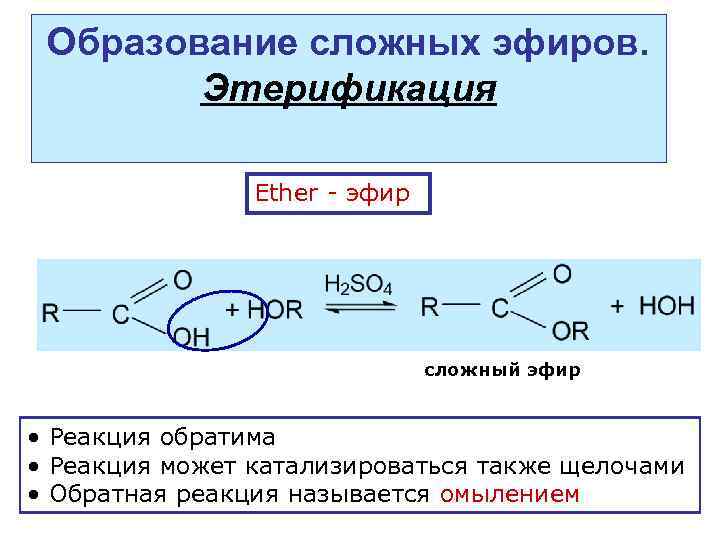 Образование сложных эфиров. Этерификация Ether - эфир сложный эфир • Реакция обратима • Реакция может катализироваться также щелочами • Обратная реакция называется омылением
Образование сложных эфиров. Этерификация Ether - эфир сложный эфир • Реакция обратима • Реакция может катализироваться также щелочами • Обратная реакция называется омылением
 2. Использование радиоактивных изотопов Механизм реакции этерификации
2. Использование радиоактивных изотопов Механизм реакции этерификации
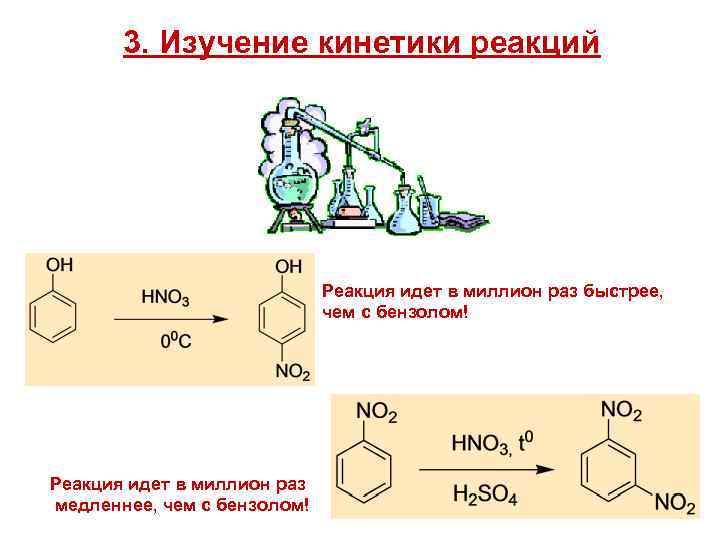 3. Изучение кинетики реакций Реакция идет в миллион раз быстрее, чем с бензолом! Реакция идет в миллион раз медленнее, чем с бензолом!
3. Изучение кинетики реакций Реакция идет в миллион раз быстрее, чем с бензолом! Реакция идет в миллион раз медленнее, чем с бензолом!
 Рис. Источник: http: //images. yandex. ru.
Рис. Источник: http: //images. yandex. ru.


