лекция 9 Oxidative Phosphorylation.pptx
- Количество слайдов: 34

Механизмы получения энергии Гликолиз Цикл Кребса Окислительное фосфорилирование Окисление жирных кислот
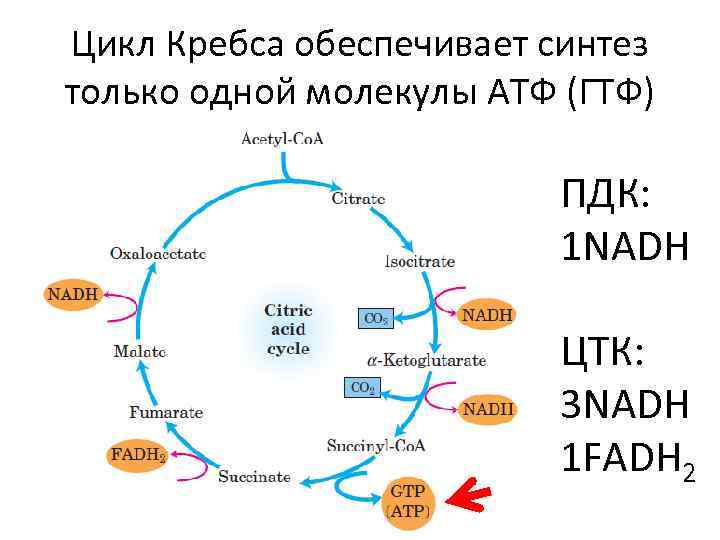
Цикл Кребса обеспечивает синтез только одной молекулы АТФ (ГТФ) ПДК: 1 NADH ЦТК: 3 NADH 1 FADH 2
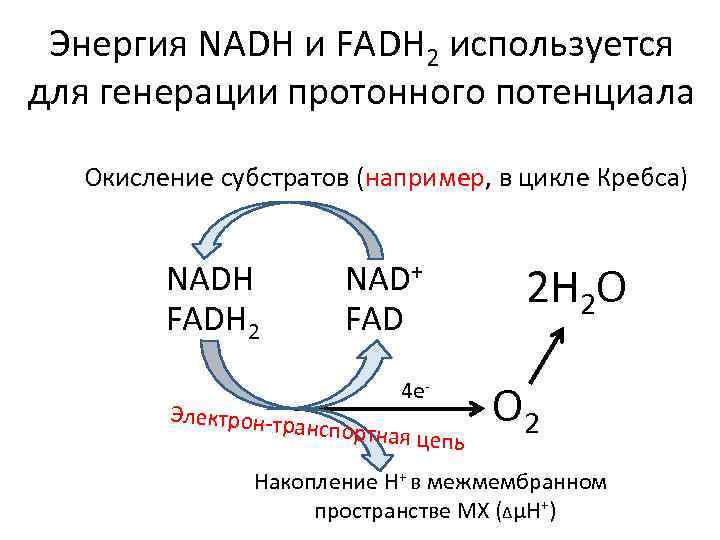
Энергия NADH и FADH 2 используется для генерации протонного потенциала Окисление субстратов (например, в цикле Кребса) NADH FADH 2 Электрон-тр NAD+ FAD 4 eанспортная цепь 2 H 2 O O 2 Накопление H+ в межмембранном пространстве МХ (∆μН+)

Градиент протонов служит для синтеза АТФ (хемиосмотическая теория Митчела) ü Внутренняя мембрана не проницаема для протонов ü Электрон-транспортная цепь генерирует градиент протонов ü Мембранная обратимая Н+-АТФаза синтезирует АТФ, используя градиент протонов ü Энергия = химическая (разница концентраций протонов) + электрическая (разница зарядов) Питер Митчелл
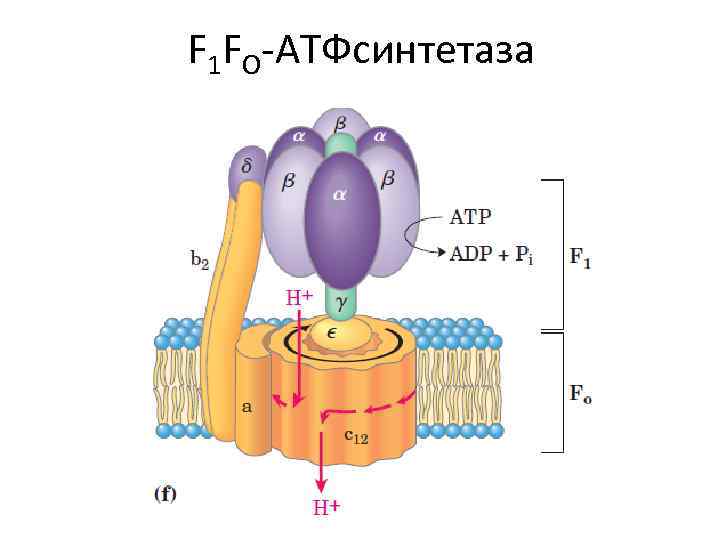
F 1 FO-АТФсинтетаза
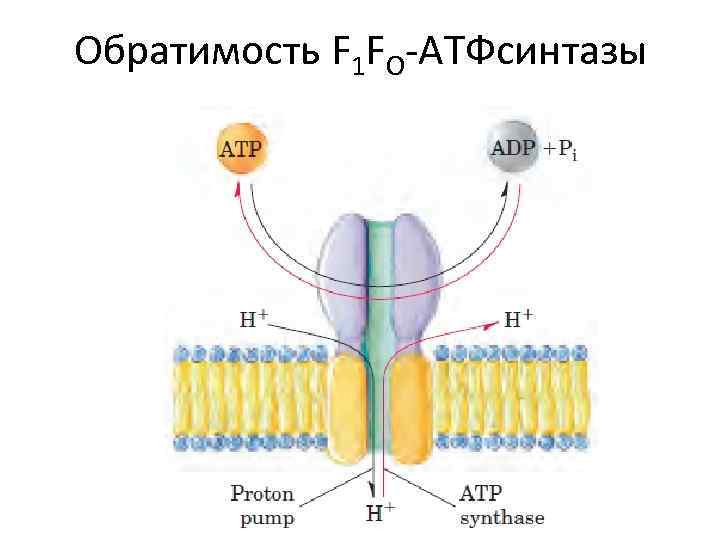
Обратимость F 1 FO-АТФсинтазы
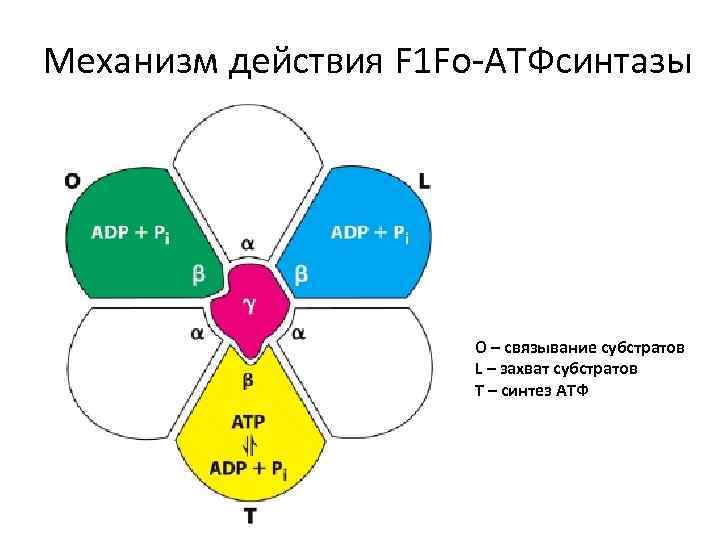
Механизм действия F 1 Fo-АТФсинтазы О – связывание субстратов L – захват субстратов Т – синтез АТФ
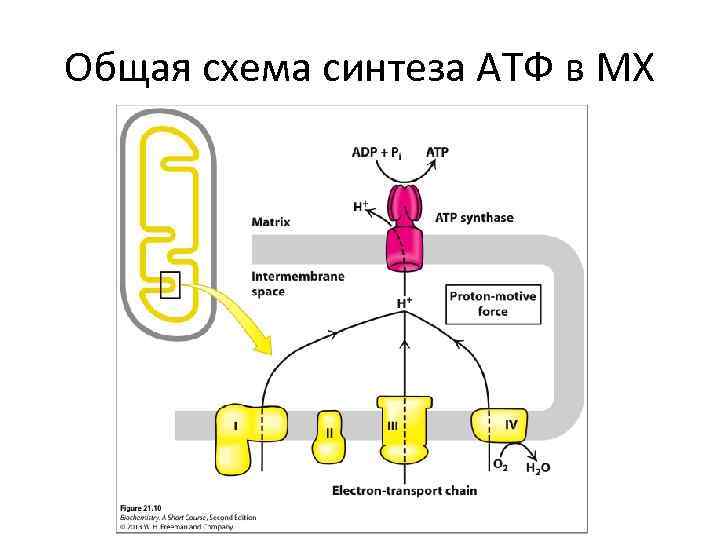
Общая схема синтеза АТФ в МХ
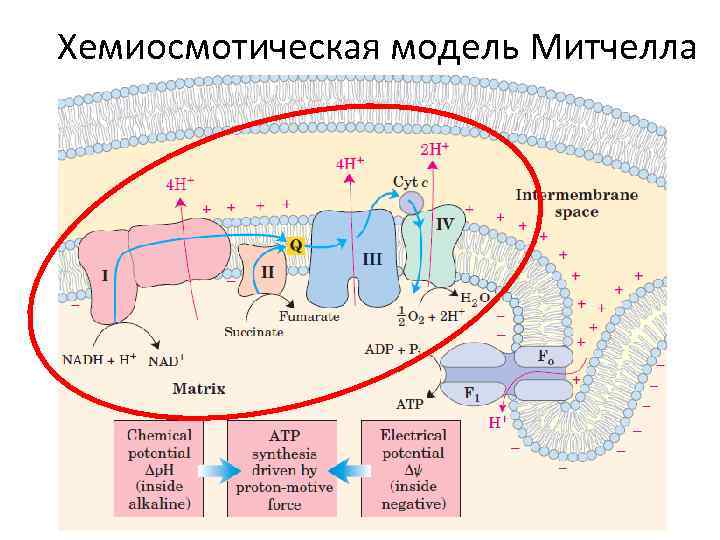
Хемиосмотическая модель Митчелла
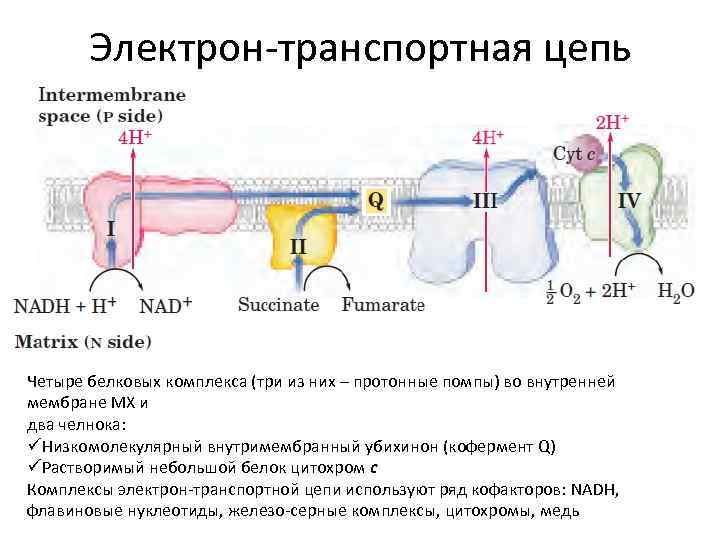
Электрон-транспортная цепь Четыре белковых комплекса (три из них – протонные помпы) во внутренней мембране МХ и два челнока: üНизкомолекулярный внутримембранный убихинон (кофермент Q) üРастворимый небольшой белок цитохром с Комплексы электрон-транспортной цепи используют ряд кофакторов: NADH, флавиновые нуклеотиды, железо-серные комплексы, цитохромы, медь
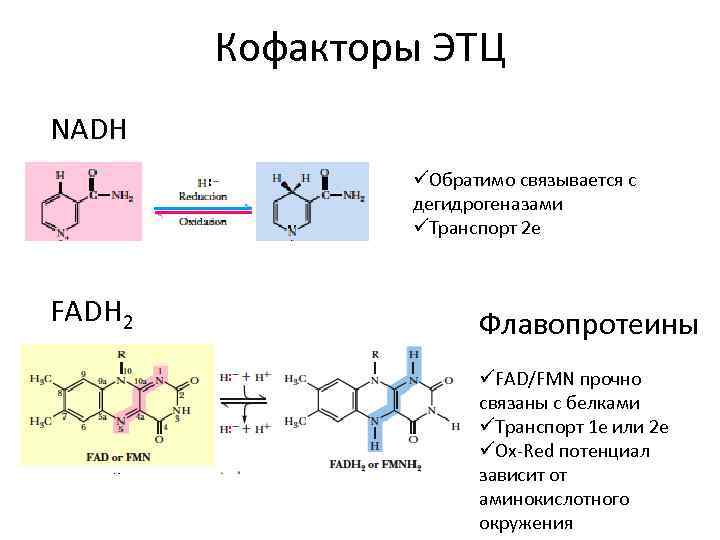
Кофакторы ЭТЦ NADH üОбратимо связывается с дегидрогеназами üТранспорт 2 е FADH 2 Флавопротеины üFAD/FMN прочно связаны с белками üТранспорт 1 е или 2 е üOx-Red потенциал зависит от аминокислотного окружения
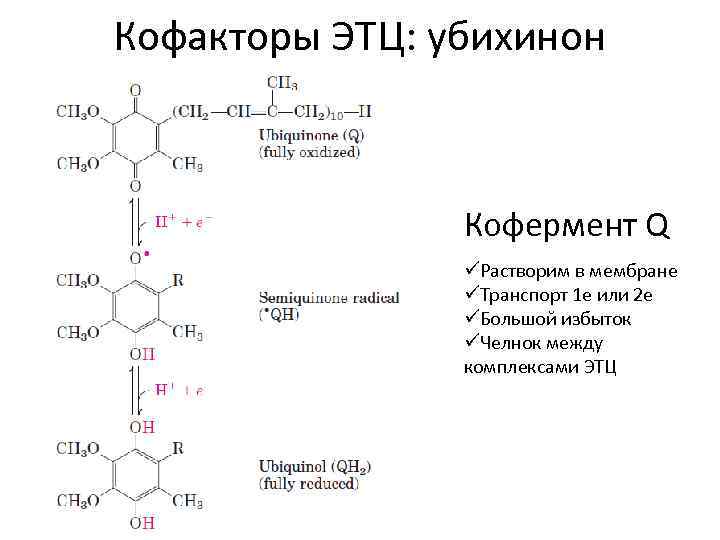
Кофакторы ЭТЦ: убихинон Кофермент Q üРастворим в мембране üТранспорт 1 е или 2 е üБольшой избыток üЧелнок между комплексами ЭТЦ
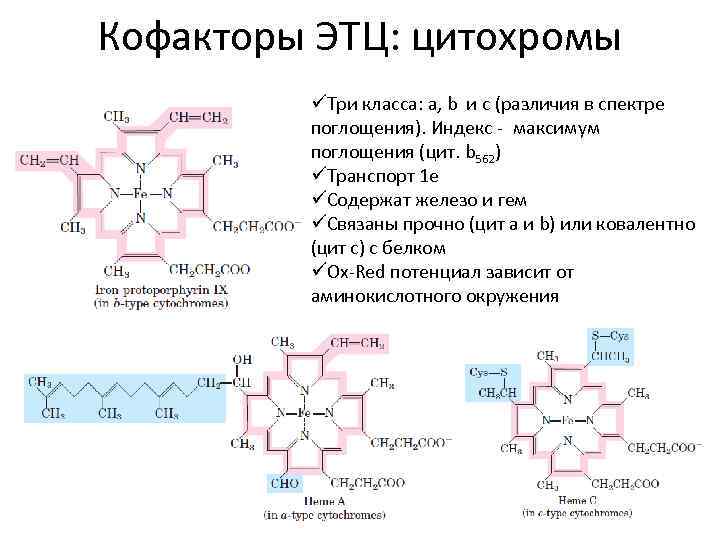
Кофакторы ЭТЦ: цитохромы üТри класса: a, b и с (различия в спектре поглощения). Индекс - максимум поглощения (цит. b 562) üТранспорт 1 е üСодержат железо и гем üСвязаны прочно (цит а и b) или ковалентно (цит с) с белком üOx-Red потенциал зависит от аминокислотного окружения
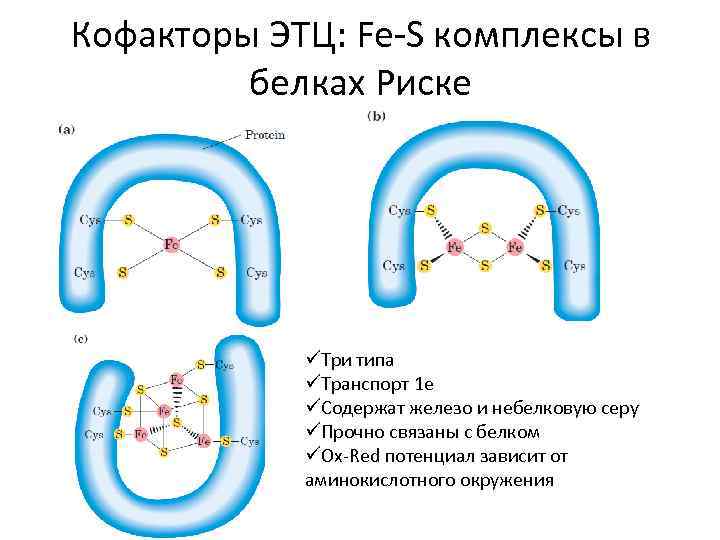
Кофакторы ЭТЦ: Fe-S комплексы в белках Риске üТри типа üТранспорт 1 е üСодержат железо и небелковую серу üПрочно связаны с белком üOx-Red потенциал зависит от аминокислотного окружения
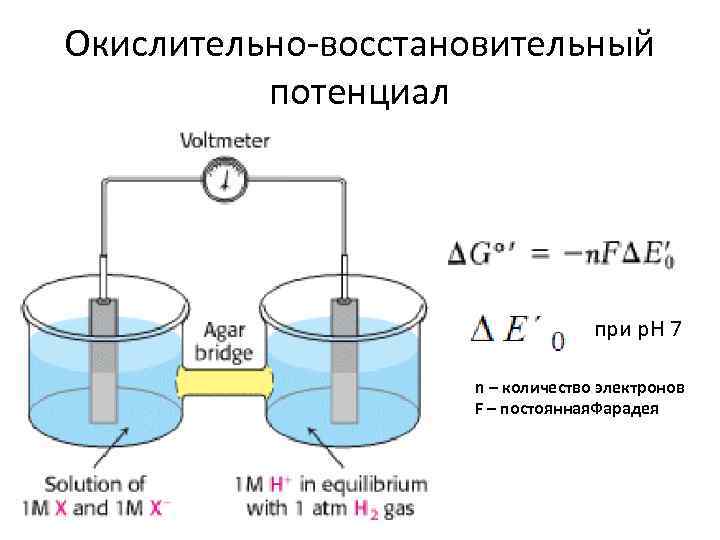
Окислительно-восстановительный потенциал при р. Н 7 n – количество электронов F – постоянная. Фарадея

Окислительно-восстановительные потенциалы компонентов ЭТЦ
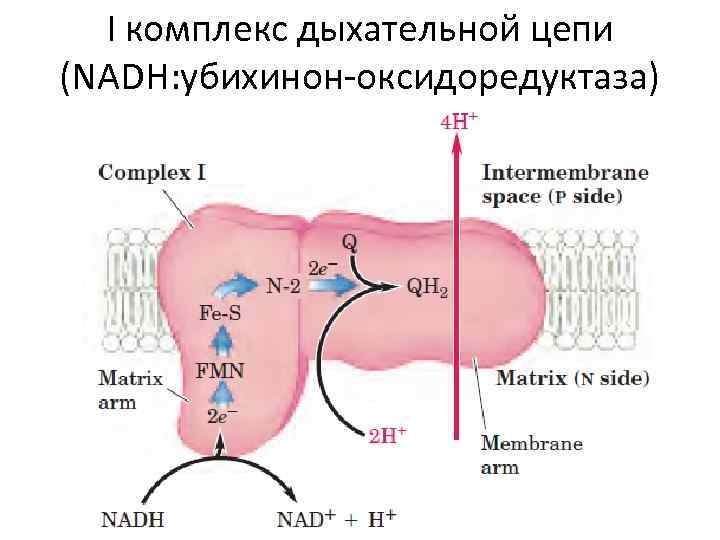
I комплекс дыхательной цепи (NADH: убихинон-оксидоредуктаза)
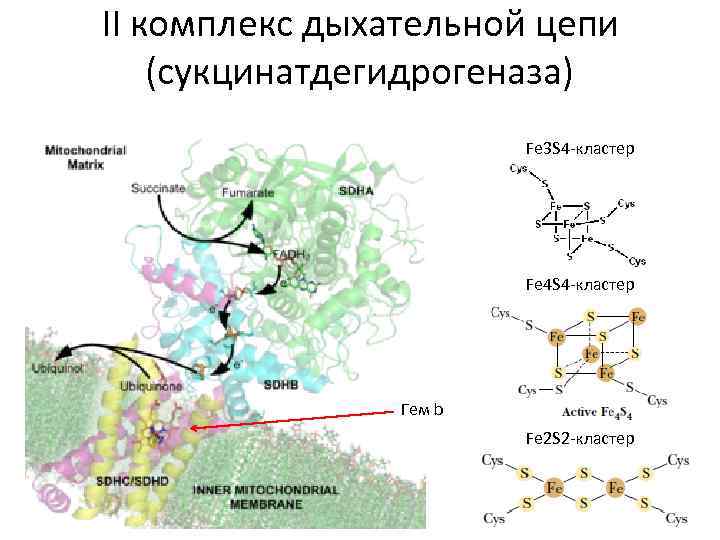
II комплекс дыхательной цепи (сукцинатдегидрогеназа) Fe 3 S 4 -кластер Fe 4 S 4 -кластер Гем b Fe 2 S 2 -кластер
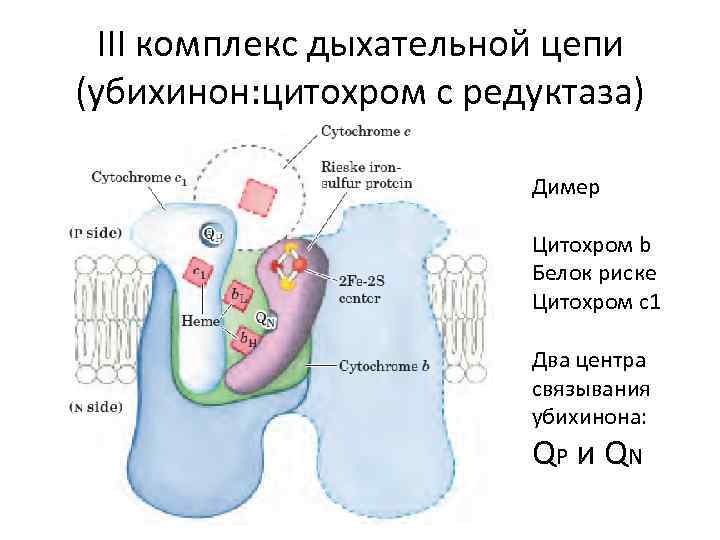
III комплекс дыхательной цепи (убихинон: цитохром с редуктаза) Димер Цитохром b Белок риске Цитохром с1 Два центра связывания убихинона: QP и QN
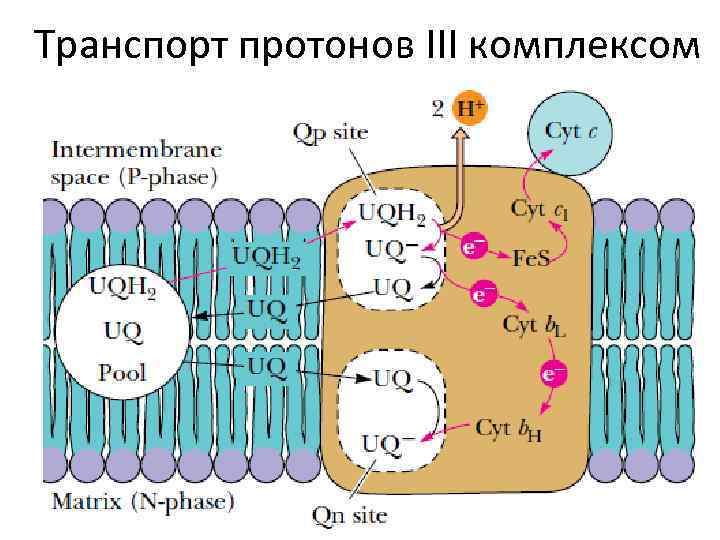
Транспорт протонов III комплексом
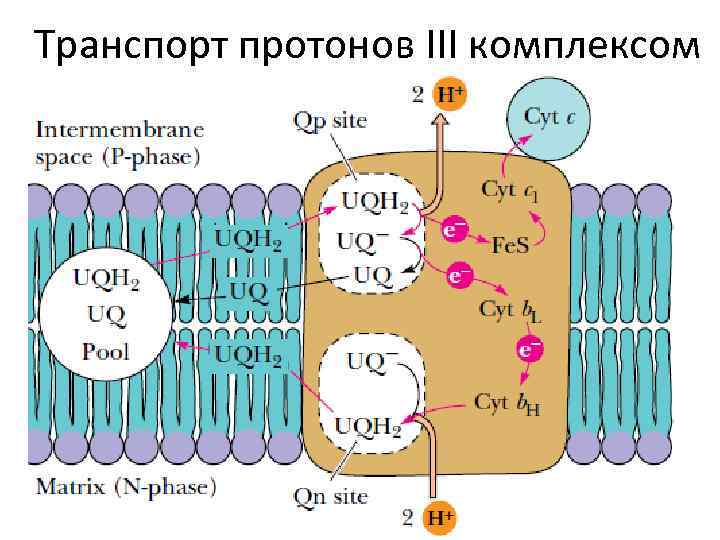
Транспорт протонов III комплексом
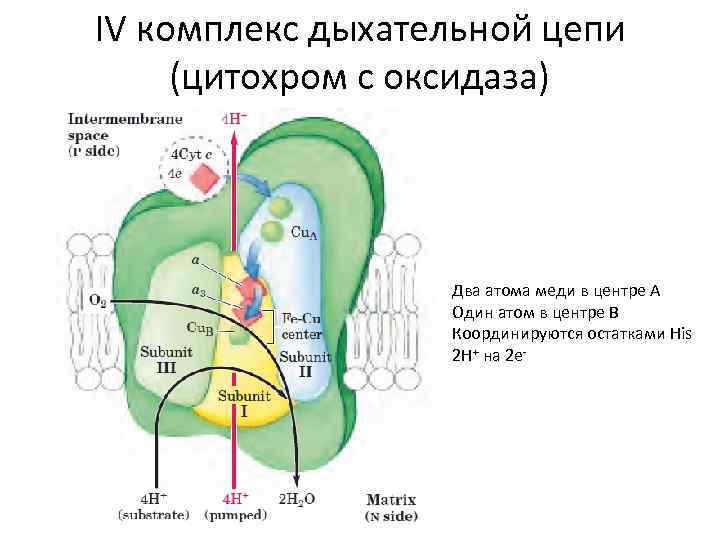
IV комплекс дыхательной цепи (цитохром с оксидаза) Два атома меди в центре А Один атом в центре В Координируются остатками His 2 H+ на 2 e-
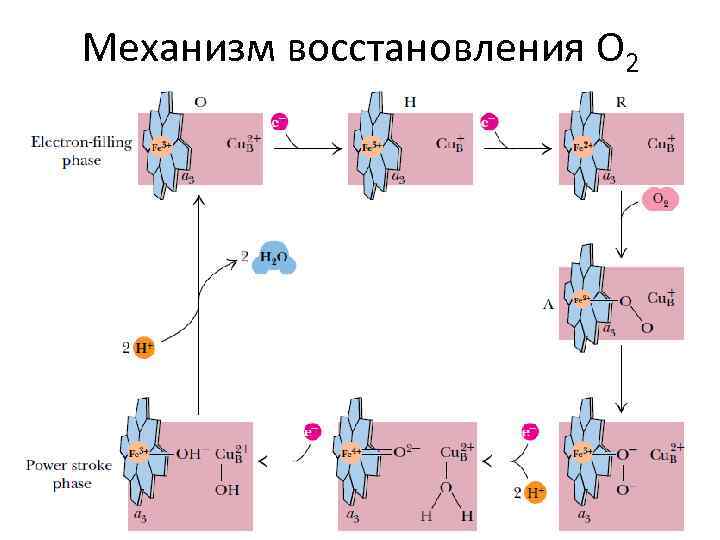
Механизм восстановления O 2
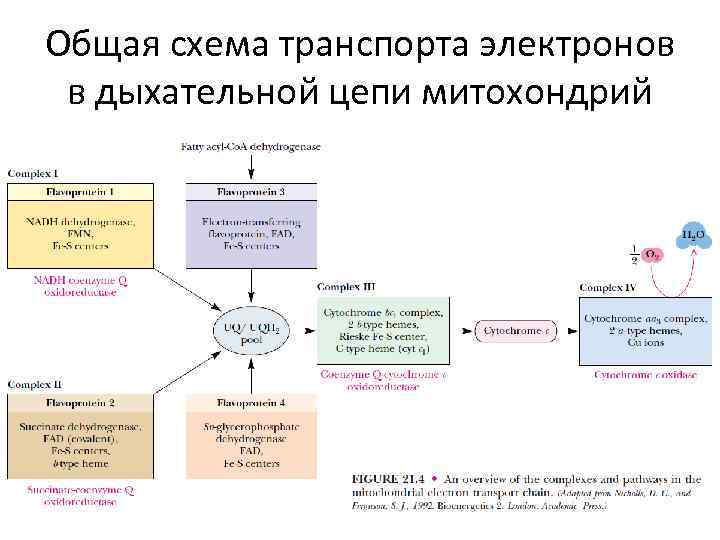
Общая схема транспорта электронов в дыхательной цепи митохондрий
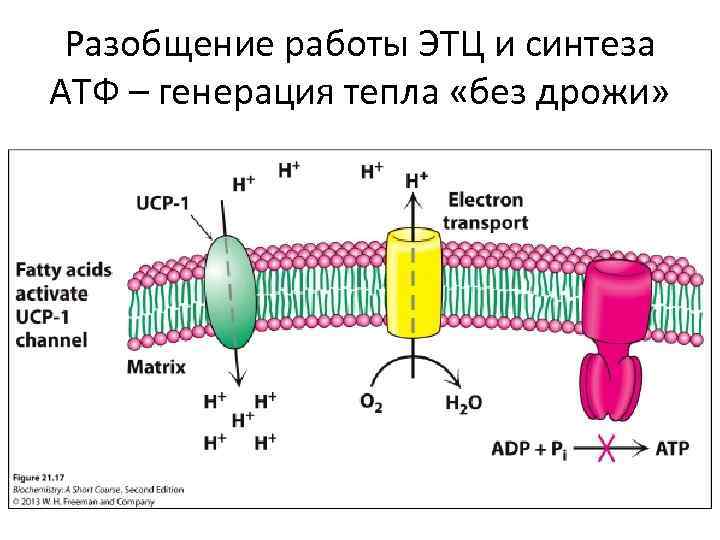
Разобщение работы ЭТЦ и синтеза АТФ – генерация тепла «без дрожи»
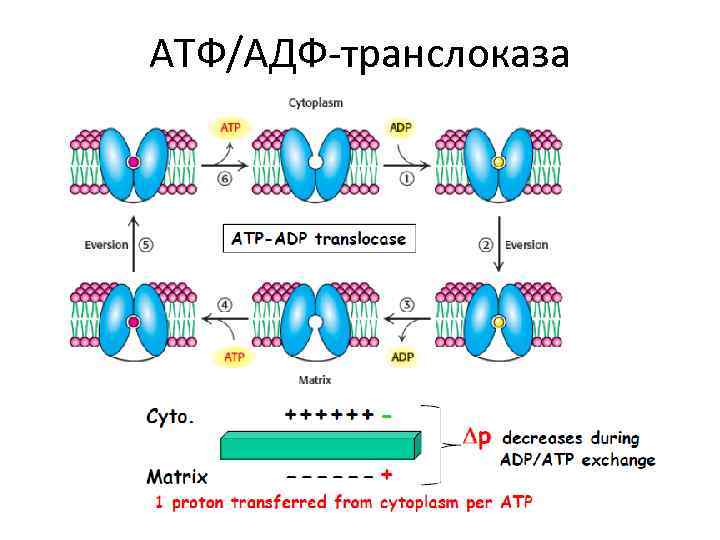
АТФ/АДФ-транслоказа
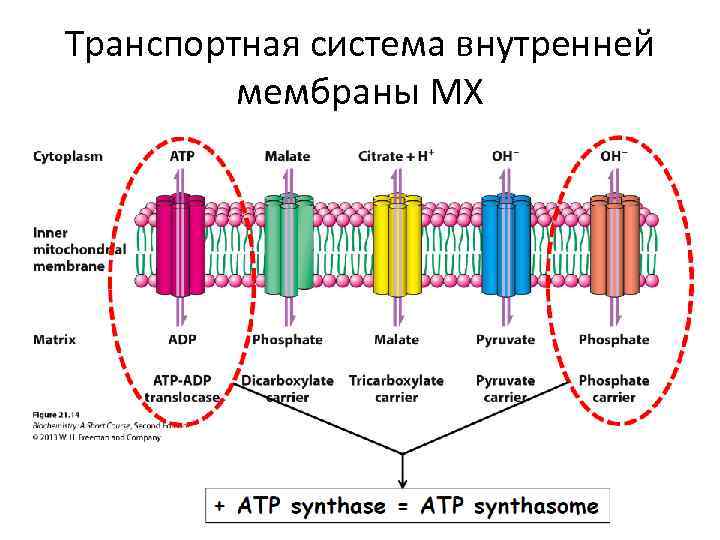
Транспортная система внутренней мембраны МХ
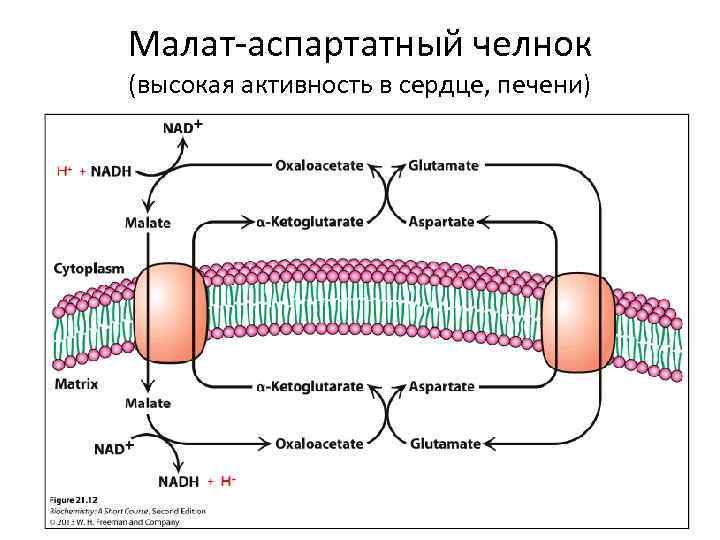
Малат-аспартатный челнок (высокая активность в сердце, печени)
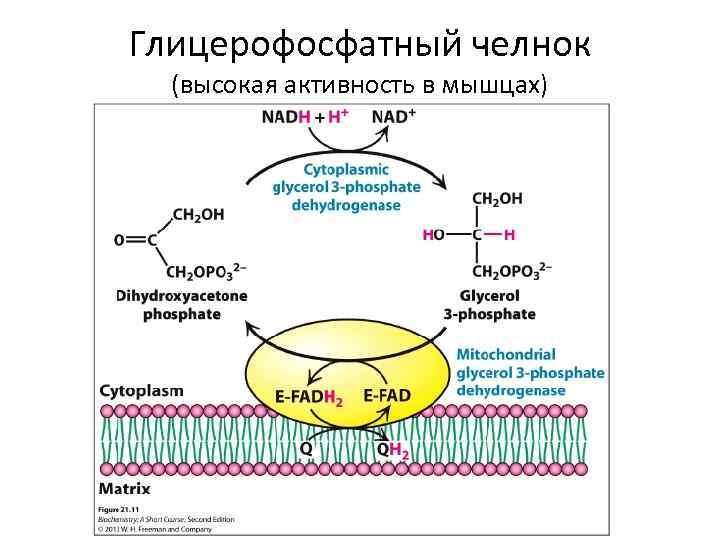
Глицерофосфатный челнок (высокая активность в мышцах)

Выход АТФ при полном окислении глюкозы 1 NADH - перенос 10 Н+ в трансмембранное пространство 3 Н+ = синтез 1 АТФ F 1 Fo-АТФсинтазой и 1 Н+ для переноса АТФ в цитоплазму, т. е. , 1 NADHмх = 2. 5 АТФ, 1 FADH 2 = 1. 5 АТФ, 1 NADHцито = 2. 5 или 1. 5 АТФ
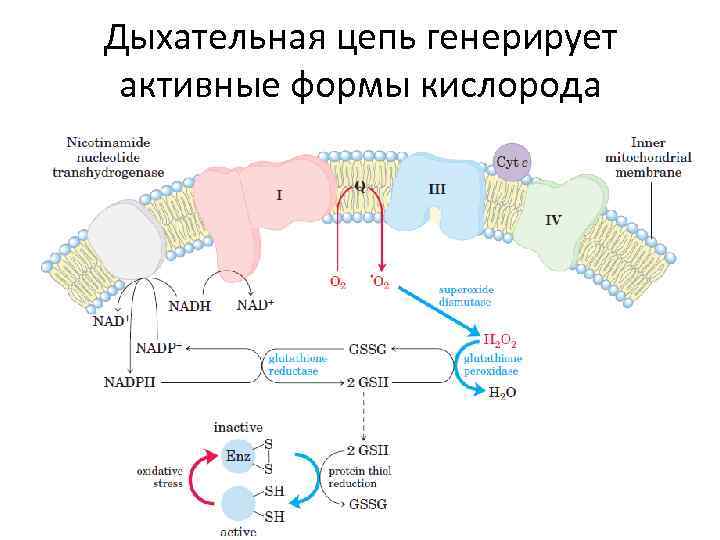
Дыхательная цепь генерирует активные формы кислорода
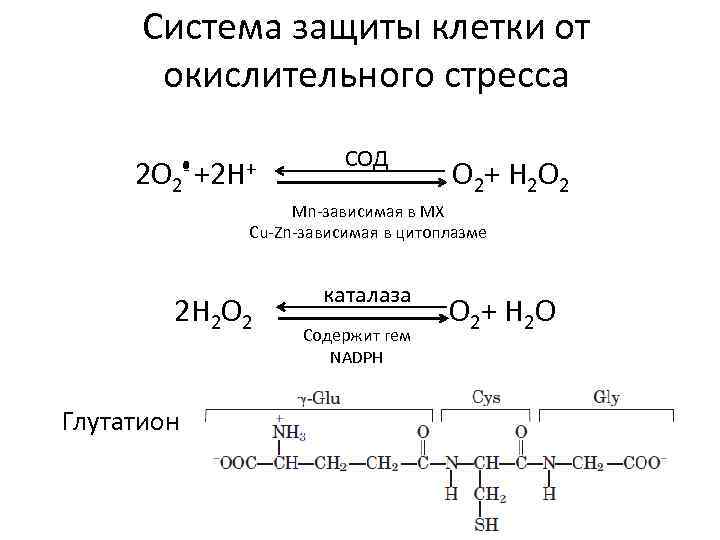
Система защиты клетки от окислительного стресса 2 O 2 - +2 H+ СОД O 2 + H 2 O 2 Mn-зависимая в МХ Cu-Zn-зависимая в цитоплазме 2 H 2 O 2 Глутатион каталаза Содержит гем NADPH O 2 + H 2 O
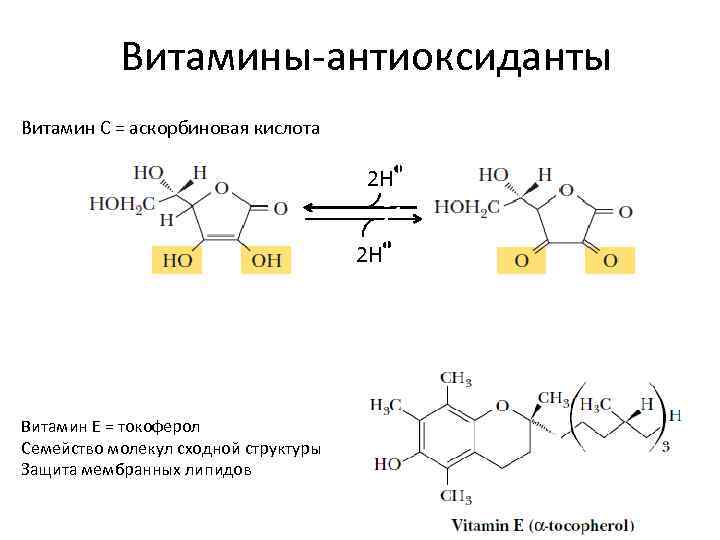
Витамины-антиоксиданты 1 Витамин С = аскорбиновая кислота Витамин Е = токоферол Семейство молекул сходной структуры Защита мембранных липидов 1 1 1 1 1 2 H 1 1 1 1 1
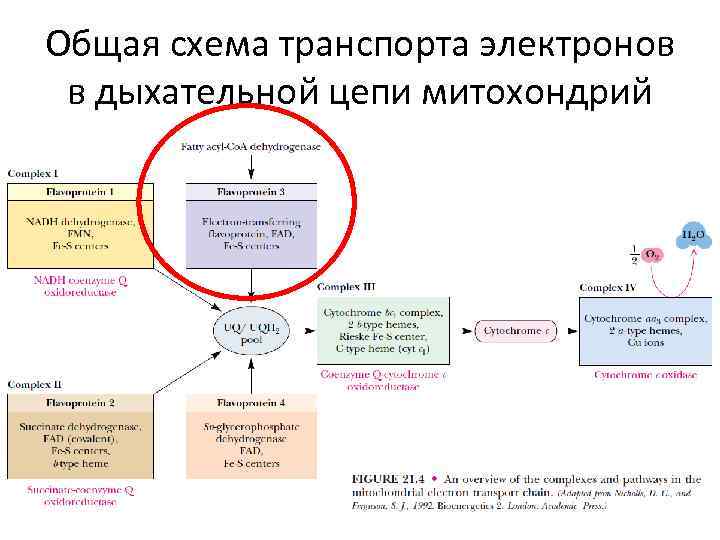
Общая схема транспорта электронов в дыхательной цепи митохондрий
лекция 9 Oxidative Phosphorylation.pptx