2014_Лекция_Неспецифическая защита.ppt
- Количество слайдов: 33
 Механизмы неспецифической защиты макроорганизма
Механизмы неспецифической защиты макроорганизма
 Иммунный ответ • Типовая реакция организма на антиген, который реализуется в виде иммунитета (защиты, физиологической иммунногенной реактивности) или в виде аллергии (патологической иммунногенной реактивности)
Иммунный ответ • Типовая реакция организма на антиген, который реализуется в виде иммунитета (защиты, физиологической иммунногенной реактивности) или в виде аллергии (патологической иммунногенной реактивности)
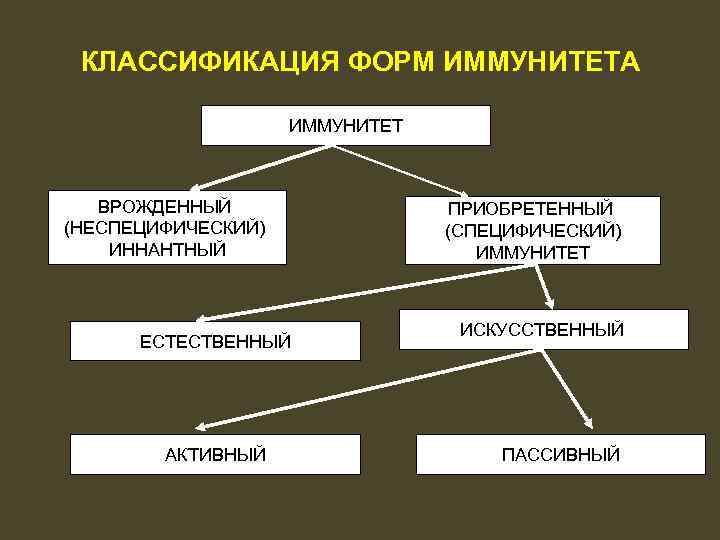 КЛАССИФИКАЦИЯ ФОРМ ИММУНИТЕТА ИММУНИТЕТ ВРОЖДЕННЫЙ (НЕСПЕЦИФИЧЕСКИЙ) ИННАНТНЫЙ ЕСТЕСТВЕННЫЙ АКТИВНЫЙ ПРИОБРЕТЕННЫЙ (СПЕЦИФИЧЕСКИЙ) ИММУНИТЕТ ИСКУССТВЕННЫЙ ПАССИВНЫЙ
КЛАССИФИКАЦИЯ ФОРМ ИММУНИТЕТА ИММУНИТЕТ ВРОЖДЕННЫЙ (НЕСПЕЦИФИЧЕСКИЙ) ИННАНТНЫЙ ЕСТЕСТВЕННЫЙ АКТИВНЫЙ ПРИОБРЕТЕННЫЙ (СПЕЦИФИЧЕСКИЙ) ИММУНИТЕТ ИСКУССТВЕННЫЙ ПАССИВНЫЙ
 ВРОЖДЕННЫЙ (НЕСПЕЦИФИЧЕСКИЙ) ИММУНИТЕТ • РЕЗИСТЕНТНОСТЬ (устойчивости организма к антигенам) – КОЖА И СЛИЗИСТЫЕ, КАШЕЛЬ, ЧИХАНИЕ, РВОТА, ПОНОС • РЕАКТИВНОСТЬ – КЛЕТОЧНЫЕ И ГУМОРАЛЬНЫЕ ФАКТОРЫ
ВРОЖДЕННЫЙ (НЕСПЕЦИФИЧЕСКИЙ) ИММУНИТЕТ • РЕЗИСТЕНТНОСТЬ (устойчивости организма к антигенам) – КОЖА И СЛИЗИСТЫЕ, КАШЕЛЬ, ЧИХАНИЕ, РВОТА, ПОНОС • РЕАКТИВНОСТЬ – КЛЕТОЧНЫЕ И ГУМОРАЛЬНЫЕ ФАКТОРЫ
 ВРОЖДЕННЫЙ (НЕСПЕЦИФИЧЕСКИЙ) ИННАНТНЫЙ 1 Распознавание антигена происходит по общим для большого числа микробов структурным компонентам 2 Быстрая скорость развития 3 Не происходит формирования иммуологической памяти 4 Гуморальный иммунитет представлен системой комплемента 5 Клеточный иммунитет представлен нейтрофилами, макрофагами, NK-клетками, В-лимфоцитами
ВРОЖДЕННЫЙ (НЕСПЕЦИФИЧЕСКИЙ) ИННАНТНЫЙ 1 Распознавание антигена происходит по общим для большого числа микробов структурным компонентам 2 Быстрая скорость развития 3 Не происходит формирования иммуологической памяти 4 Гуморальный иммунитет представлен системой комплемента 5 Клеточный иммунитет представлен нейтрофилами, макрофагами, NK-клетками, В-лимфоцитами
 НЕСПЕЦИФИЧЕСКИЕ ФАКТОРЫ ЗАЩИТЫ ОРГАНИЗМА ЧЕЛОВЕКА Внешние барьеры Нормальная микрофлора Кожа Слизистые Внутренние барьеры Лимфоузлы Тканевые, Клеточные барьеры Клеточные факторы Гуморальные факторы Фагоциты Комплемент Естественные Лизоцим киллеры Интерфероны Белки острой фазы Другие цитокины
НЕСПЕЦИФИЧЕСКИЕ ФАКТОРЫ ЗАЩИТЫ ОРГАНИЗМА ЧЕЛОВЕКА Внешние барьеры Нормальная микрофлора Кожа Слизистые Внутренние барьеры Лимфоузлы Тканевые, Клеточные барьеры Клеточные факторы Гуморальные факторы Фагоциты Комплемент Естественные Лизоцим киллеры Интерфероны Белки острой фазы Другие цитокины
 Эшелоны иммунного ответа • Первым этапом, или «линией обороны» являются слизистые оболочки. • Второй линией защиты являются иммуноглобулины s. Ig. A. • Третий этап иммунного ответа происходит с участием клеточных и гуморальных факторов. • Четвертый этап – специфическая иммунная защита
Эшелоны иммунного ответа • Первым этапом, или «линией обороны» являются слизистые оболочки. • Второй линией защиты являются иммуноглобулины s. Ig. A. • Третий этап иммунного ответа происходит с участием клеточных и гуморальных факторов. • Четвертый этап – специфическая иммунная защита
 СЛИЗИСТЫЕ ОБОЛОЧКИ • На этом уровне включаются механизмы неспецифической защиты, которые препятствуют адгезии и колонизации патогенов. • Слизь механически защищает эпителий слизистой оболочки желудка от адгезии, поскольку является физическим барьером между патогеном и эпителием. • Соляная кислота желудочного сока обладает бактерицидным действием и защищает от колонизации бактерий. • Перистальтика создает механическое препятствие для экспозиции патогена в слизистой оболочке желудка.
СЛИЗИСТЫЕ ОБОЛОЧКИ • На этом уровне включаются механизмы неспецифической защиты, которые препятствуют адгезии и колонизации патогенов. • Слизь механически защищает эпителий слизистой оболочки желудка от адгезии, поскольку является физическим барьером между патогеном и эпителием. • Соляная кислота желудочного сока обладает бактерицидным действием и защищает от колонизации бактерий. • Перистальтика создает механическое препятствие для экспозиции патогена в слизистой оболочке желудка.
 ВТОРАЯ ЛИНИЯ ЗАЩИТЫ • Если все-таки патоген преодолевает предыдущий барьер, то на следующем этапе при помощи поверхностных антигенов возбудитель пытается закрепиться на слизистой оболочке. • Протективную роль в этот момент играют иммуноглобулины s. Ig. A: • блокируют поверхностные антигены бактерии, • ингибирует адсорбцию и размножение бактерии. • Образование комплекса s. Ig. A-антигены приводит к высвобождению тучными клетками медиаторов воспаления. • Цитокины и хемокины (IL-8, IL-12) являются стимулами для привлечения эффекторных клеток и молекул воспаления. • Развивается неспецифическое острое локальное воспаление.
ВТОРАЯ ЛИНИЯ ЗАЩИТЫ • Если все-таки патоген преодолевает предыдущий барьер, то на следующем этапе при помощи поверхностных антигенов возбудитель пытается закрепиться на слизистой оболочке. • Протективную роль в этот момент играют иммуноглобулины s. Ig. A: • блокируют поверхностные антигены бактерии, • ингибирует адсорбцию и размножение бактерии. • Образование комплекса s. Ig. A-антигены приводит к высвобождению тучными клетками медиаторов воспаления. • Цитокины и хемокины (IL-8, IL-12) являются стимулами для привлечения эффекторных клеток и молекул воспаления. • Развивается неспецифическое острое локальное воспаление.
 ТРЕТИЙ ЭТАП ИММУННОГО ОТВЕТА • • • К гуморальным факторам неспецифической защиты организма относят систему комплемента, лизины, естественные антитела, которые секретируются киллерными клетками. Клеточная миграция, пока еще также неспецифическая, тем не менее, реализуется в строго определенном порядке. Первыми в очаге воспаления появляются нейтрофилы. Необходимым условием для их хемотаксиса является постепенное создание по ходу миграции клетки градиента концентрации хемоаттрактантов (MIP-1α, MIP-1β, IL-8, RANTES). Примерно на вторые сутки в очаг начинают поступать мононуклеарные фагоциты и лимфоциты. Основным эффектом неспецифической клеточной защиты является генерация продуктов респираторного взрыва (О–, ОН–, Н 2 О 2) и метаболизма окиси азота, а также продуктов, высвобождаемых из гранул лейкоцитов. В частности, при дегрануляции нейтрофилов в очаге воспаления появляются ферменты, обладающие пероксидазной активностью; белки, повреждающие микробные мембраны (катионные белки, катепсин D, лизоцим); лактоферрин. Цитокин-зависимая миграция нейтрофилов и макрофагов в очаг воспаления способствует презентации бактериального антигена иммунным клеткам.
ТРЕТИЙ ЭТАП ИММУННОГО ОТВЕТА • • • К гуморальным факторам неспецифической защиты организма относят систему комплемента, лизины, естественные антитела, которые секретируются киллерными клетками. Клеточная миграция, пока еще также неспецифическая, тем не менее, реализуется в строго определенном порядке. Первыми в очаге воспаления появляются нейтрофилы. Необходимым условием для их хемотаксиса является постепенное создание по ходу миграции клетки градиента концентрации хемоаттрактантов (MIP-1α, MIP-1β, IL-8, RANTES). Примерно на вторые сутки в очаг начинают поступать мононуклеарные фагоциты и лимфоциты. Основным эффектом неспецифической клеточной защиты является генерация продуктов респираторного взрыва (О–, ОН–, Н 2 О 2) и метаболизма окиси азота, а также продуктов, высвобождаемых из гранул лейкоцитов. В частности, при дегрануляции нейтрофилов в очаге воспаления появляются ферменты, обладающие пероксидазной активностью; белки, повреждающие микробные мембраны (катионные белки, катепсин D, лизоцим); лактоферрин. Цитокин-зависимая миграция нейтрофилов и макрофагов в очаг воспаления способствует презентации бактериального антигена иммунным клеткам.
 ФАГОЦИТОЗ Фагоцитоз - захват и «переваривание» бактерий
ФАГОЦИТОЗ Фагоцитоз - захват и «переваривание» бактерий
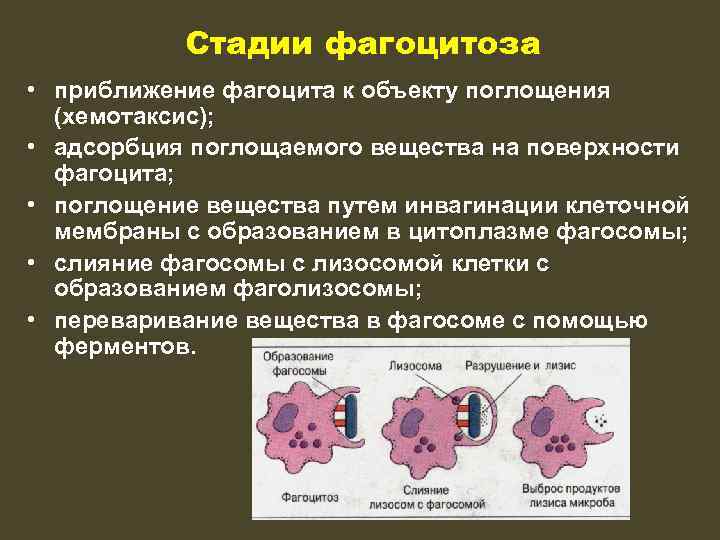 Стадии фагоцитоза • приближение фагоцита к объекту поглощения (хемотаксис); • адсорбция поглощаемого вещества на поверхности фагоцита; • поглощение вещества путем инвагинации клеточной мембраны с образованием в цитоплазме фагосомы; • слияние фагосомы с лизосомой клетки с образованием фаголизосомы; • переваривание вещества в фагосоме с помощью ферментов.
Стадии фагоцитоза • приближение фагоцита к объекту поглощения (хемотаксис); • адсорбция поглощаемого вещества на поверхности фагоцита; • поглощение вещества путем инвагинации клеточной мембраны с образованием в цитоплазме фагосомы; • слияние фагосомы с лизосомой клетки с образованием фаголизосомы; • переваривание вещества в фагосоме с помощью ферментов.
 Различают Эндоцитоз – это энергетически зависимый процесс, связанный с преобразованием энергии химических связей молекулы АТФ в сократительную активность внутриклеточных актина и миозина. Фагоцитоз – в отношении частиц с диаметром не менее 0, 1 мкм Пиноцитоз – в отношении более мелких частиц и молекул.
Различают Эндоцитоз – это энергетически зависимый процесс, связанный с преобразованием энергии химических связей молекулы АТФ в сократительную активность внутриклеточных актина и миозина. Фагоцитоз – в отношении частиц с диаметром не менее 0, 1 мкм Пиноцитоз – в отношении более мелких частиц и молекул.
 Окружение фагоцитируемого вещества двуслойной ЦПМ и образование изолированного внутриклеточного пузырька – фагосомы напоминает «застегивание молнии» (зипперный механизм). Внутри фагосомы продолжается атака поглощенного вещества перикисными радикалами. После слияния фагосомы и лизосомы и образования в цитоплазме фаголизосомы происходит активация лизосомальных ферментов. Эти ферменты разрушают поглощенное вещество. При этом случайный небольшой фрагмент перевариваемого вещества (размером до 9 аминокислот) может быть выставлен (экспрессирован) на поверхности фагоцита для «ознакомления» с ним Тхелперов.
Окружение фагоцитируемого вещества двуслойной ЦПМ и образование изолированного внутриклеточного пузырька – фагосомы напоминает «застегивание молнии» (зипперный механизм). Внутри фагосомы продолжается атака поглощенного вещества перикисными радикалами. После слияния фагосомы и лизосомы и образования в цитоплазме фаголизосомы происходит активация лизосомальных ферментов. Эти ферменты разрушают поглощенное вещество. При этом случайный небольшой фрагмент перевариваемого вещества (размером до 9 аминокислот) может быть выставлен (экспрессирован) на поверхности фагоцита для «ознакомления» с ним Тхелперов.
 Механизмы микробицидности фагоцитов 1. Кислород зависимые механизмы: v «Респираторный взрыв» –усиление потребления кислорода и глюкозы с одновременным выбросом нестабильных продуктов восстановления кислорода: пероксида водорода Н 2 О 2, супероксиданионов О 2, гидроксильных радикалов ОН–. v Система миелопероксидаз. 2. Кислород независимые – через лизоцим, лактоферрин, гидролазы. v Цикл оксида азота (NO–) – промежуточный продукт превращения L-аргинина, токсичен в отношении микробов. Это основной микробицидный фактор при макрофагальном фагоцитозе. v Антиоксидная защита тканей (каталаза, витамин С, Е, ненасыщенные жирные кислоты).
Механизмы микробицидности фагоцитов 1. Кислород зависимые механизмы: v «Респираторный взрыв» –усиление потребления кислорода и глюкозы с одновременным выбросом нестабильных продуктов восстановления кислорода: пероксида водорода Н 2 О 2, супероксиданионов О 2, гидроксильных радикалов ОН–. v Система миелопероксидаз. 2. Кислород независимые – через лизоцим, лактоферрин, гидролазы. v Цикл оксида азота (NO–) – промежуточный продукт превращения L-аргинина, токсичен в отношении микробов. Это основной микробицидный фактор при макрофагальном фагоцитозе. v Антиоксидная защита тканей (каталаза, витамин С, Е, ненасыщенные жирные кислоты).
 Виды фагоцитоза Фагоцитоз, заканчивающийся «перевариванием» захваченных бактерий, называется завершенным. Некоторые бактерии (гонококки) или вирусы (возбудитель ВИЧ-инфекции, натуральной оспы) блокируют ферментативную активность фагоцита, не погибают, не разрушаются и даже размножаются в фагоцитах. Такой процесс назван незавершенным фагоцитозом. Выживание фагоцитированных микроорганизмов могут обеспечить различные механизмы
Виды фагоцитоза Фагоцитоз, заканчивающийся «перевариванием» захваченных бактерий, называется завершенным. Некоторые бактерии (гонококки) или вирусы (возбудитель ВИЧ-инфекции, натуральной оспы) блокируют ферментативную активность фагоцита, не погибают, не разрушаются и даже размножаются в фагоцитах. Такой процесс назван незавершенным фагоцитозом. Выживание фагоцитированных микроорганизмов могут обеспечить различные механизмы
 Механизмы выживания фагоцитированных микроорганизмов препятствование слияния лизосом с фагосомами (токсоплазмы, микобактерии туберкулеза); устойчивость к действию лизосомных ферментов (гонококки, стафилококки, стрептококки группы А и др. ); могут покидать фагосому, избегая действие микробицидных факторов (риккетсии и др. ).
Механизмы выживания фагоцитированных микроорганизмов препятствование слияния лизосом с фагосомами (токсоплазмы, микобактерии туберкулеза); устойчивость к действию лизосомных ферментов (гонококки, стафилококки, стрептококки группы А и др. ); могут покидать фагосому, избегая действие микробицидных факторов (риккетсии и др. ).
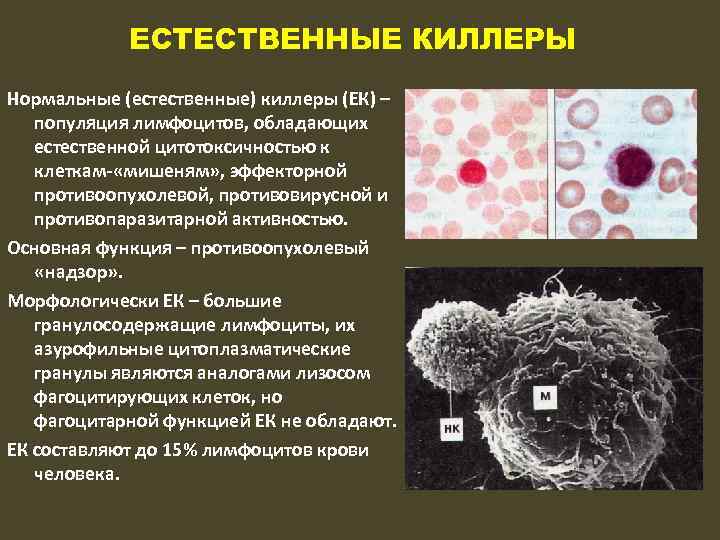 ЕСТЕСТВЕННЫЕ КИЛЛЕРЫ Нормальные (естественные) киллеры (ЕК) – популяция лимфоцитов, обладающих естественной цитотоксичностью к клеткам- «мишеням» , эффекторной противоопухолевой, противовирусной и противопаразитарной активностью. Основная функция – противоопухолевый «надзор» . Морфологически ЕК – большие гранулосодержащие лимфоциты, их азурофильные цитоплазматические гранулы являются аналогами лизосом фагоцитирующих клеток, но фагоцитарной функцией ЕК не обладают. ЕК составляют до 15% лимфоцитов крови человека.
ЕСТЕСТВЕННЫЕ КИЛЛЕРЫ Нормальные (естественные) киллеры (ЕК) – популяция лимфоцитов, обладающих естественной цитотоксичностью к клеткам- «мишеням» , эффекторной противоопухолевой, противовирусной и противопаразитарной активностью. Основная функция – противоопухолевый «надзор» . Морфологически ЕК – большие гранулосодержащие лимфоциты, их азурофильные цитоплазматические гранулы являются аналогами лизосом фагоцитирующих клеток, но фагоцитарной функцией ЕК не обладают. ЕК составляют до 15% лимфоцитов крови человека.
 ТРОМБОЦИТЫ Тромбоциты образуются из мегакариоцитов, пролиферацию которых усиливает ИЛ-11. Тромбоциты имеют на своей поверхности рецепторы для Ig. G и Ig. E, компонентов комплемента (С 1 и С 3), а также антигены гистосовместимости I класса. На тромбоциты влияют образующиеся в организме иммунные комплексы антиген-антитело и активированный комплемент. В результате тромбоциты выделяют биологически активные вещества (гистамин, лизоцим, β-лизины, лейкоплакины, простагландины и др. ), которые участвуют в процессах иммунитета и воспаления. В случае повреждения эндотелия тромбоциты прилипают к субэпителиальной поверхности поврежденной сосудистой стенки, образуя агрегаты. При этом из тромбоцитарных гранул двух типов высвобождается их содержимое, в том числе серотонин и фибриноген, что приводит к повышению проницаемости капилляров, активации комплемента и к привлечению лейкоцитов.
ТРОМБОЦИТЫ Тромбоциты образуются из мегакариоцитов, пролиферацию которых усиливает ИЛ-11. Тромбоциты имеют на своей поверхности рецепторы для Ig. G и Ig. E, компонентов комплемента (С 1 и С 3), а также антигены гистосовместимости I класса. На тромбоциты влияют образующиеся в организме иммунные комплексы антиген-антитело и активированный комплемент. В результате тромбоциты выделяют биологически активные вещества (гистамин, лизоцим, β-лизины, лейкоплакины, простагландины и др. ), которые участвуют в процессах иммунитета и воспаления. В случае повреждения эндотелия тромбоциты прилипают к субэпителиальной поверхности поврежденной сосудистой стенки, образуя агрегаты. При этом из тромбоцитарных гранул двух типов высвобождается их содержимое, в том числе серотонин и фибриноген, что приводит к повышению проницаемости капилляров, активации комплемента и к привлечению лейкоцитов.
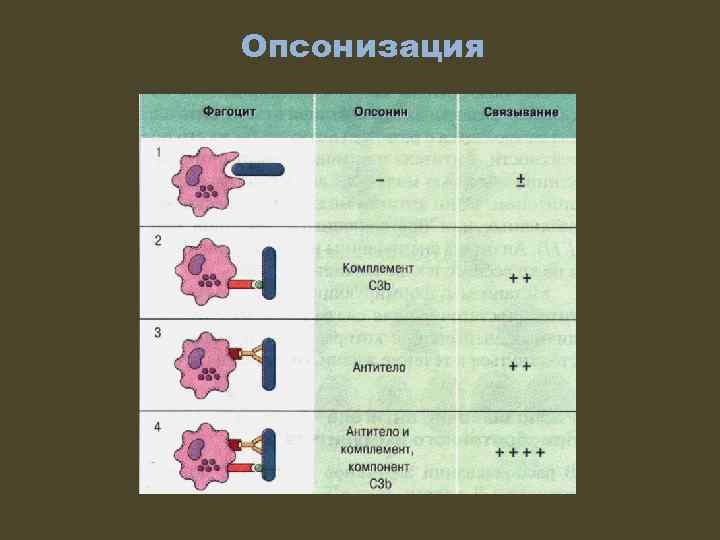 Опсонизация
Опсонизация
 ГУМОРАЛЬНЫЕ ФАКТОРЫ v. Нормальные антитела; vкомплемент; vлизоцим; vинтерферон; vцитокины; vзащитные белки сыворотки крови и др.
ГУМОРАЛЬНЫЕ ФАКТОРЫ v. Нормальные антитела; vкомплемент; vлизоцим; vинтерферон; vцитокины; vзащитные белки сыворотки крови и др.
 КОМПЛЕМЕНТ Комплемент был открыт в 1899 г. французским иммунологом Ж. Барде, назвавшим его «алексином» . Современное название комплементу дал П. Эрлих. Система комплемента – одна из основных систем врожденного иммунитета. Комплемент – сложный комплекс белков сыворотки крови, активирующийся при образовании комплекса АГ-АТ или при агрегации АГ, т. е. в начале иммунного процесса. В состав комплемента входят 20 взаимодействующих между собой белков, 9 из которых являются основными компонентами (фракциями) комплемента, их обозначают как С 1, С 2, С 3 … С 9. Белки комплемента относятся к глобулинам и различаются по ряду физико-химических свойств. Компоненты комплемента синтезируются в большом количестве (составляют 5 -10% всех белков крови), часть из них образуют фагоциты, часть клетки печени. Система комплемента – многокомпонентная самособирающаяся система белков сыворотки крови, которая играет важную роль в поддержании гомеостаза
КОМПЛЕМЕНТ Комплемент был открыт в 1899 г. французским иммунологом Ж. Барде, назвавшим его «алексином» . Современное название комплементу дал П. Эрлих. Система комплемента – одна из основных систем врожденного иммунитета. Комплемент – сложный комплекс белков сыворотки крови, активирующийся при образовании комплекса АГ-АТ или при агрегации АГ, т. е. в начале иммунного процесса. В состав комплемента входят 20 взаимодействующих между собой белков, 9 из которых являются основными компонентами (фракциями) комплемента, их обозначают как С 1, С 2, С 3 … С 9. Белки комплемента относятся к глобулинам и различаются по ряду физико-химических свойств. Компоненты комплемента синтезируются в большом количестве (составляют 5 -10% всех белков крови), часть из них образуют фагоциты, часть клетки печени. Система комплемента – многокомпонентная самособирающаяся система белков сыворотки крови, которая играет важную роль в поддержании гомеостаза
 ФУНКЦИИ КОМПЛЕМЕНТА v Комплемент участвует в лизисе микробных и других клеток (цитотоксическое действие); v обладает хемотаксической активностью; v участвует в анафилаксии; v участвует в фагоцитозе. v является компонентом многих иммунолитических реакций, направленных на освобождение организма от микробов и других чужеродных клеток и антигенов (например, опухолевых клеток, трансплантата).
ФУНКЦИИ КОМПЛЕМЕНТА v Комплемент участвует в лизисе микробных и других клеток (цитотоксическое действие); v обладает хемотаксической активностью; v участвует в анафилаксии; v участвует в фагоцитозе. v является компонентом многих иммунолитических реакций, направленных на освобождение организма от микробов и других чужеродных клеток и антигенов (например, опухолевых клеток, трансплантата).
 Механизм активации комплемента Это каскад ферментативных протеолитических реакций, в результате которых образуется активный цитотоксический комплекс, разрушающий стенку бактерии и других клеток. Существуют три пути активации комплемента: классический, лектиновый и альтернативный. Порядок вступления белков комплемента при активации по классическому пути : С 1 q→C 1 r → C 1 s → C 4 → C 2 → C 3 → C 5 → C 6 → C 7 → C 8 → C 9 По классическому пути комплемент активируется комплексом АГ-АТ (иммунным комплексом). Fc-фрагменты Ig. G и Ig. M в составе иммунных комплексов связываются с С 1, который распадается на субъединицы С 1 q, C 1 r и C 1 s. Далее последовательно активируюстя «ранние» компоненты комплемента: С 4→С 2→С 3. С 3 b активирует компонент С 5, который прикрепляется к мембране клетки. На компоненте С 5 путем последовательного присоединения «поздних» компонентов С 6, С 7, С 8 и С 9 образуется литический или мембранатакующий комплекс, в результате чего клетка погибает.
Механизм активации комплемента Это каскад ферментативных протеолитических реакций, в результате которых образуется активный цитотоксический комплекс, разрушающий стенку бактерии и других клеток. Существуют три пути активации комплемента: классический, лектиновый и альтернативный. Порядок вступления белков комплемента при активации по классическому пути : С 1 q→C 1 r → C 1 s → C 4 → C 2 → C 3 → C 5 → C 6 → C 7 → C 8 → C 9 По классическому пути комплемент активируется комплексом АГ-АТ (иммунным комплексом). Fc-фрагменты Ig. G и Ig. M в составе иммунных комплексов связываются с С 1, который распадается на субъединицы С 1 q, C 1 r и C 1 s. Далее последовательно активируюстя «ранние» компоненты комплемента: С 4→С 2→С 3. С 3 b активирует компонент С 5, который прикрепляется к мембране клетки. На компоненте С 5 путем последовательного присоединения «поздних» компонентов С 6, С 7, С 8 и С 9 образуется литический или мембранатакующий комплекс, в результате чего клетка погибает.
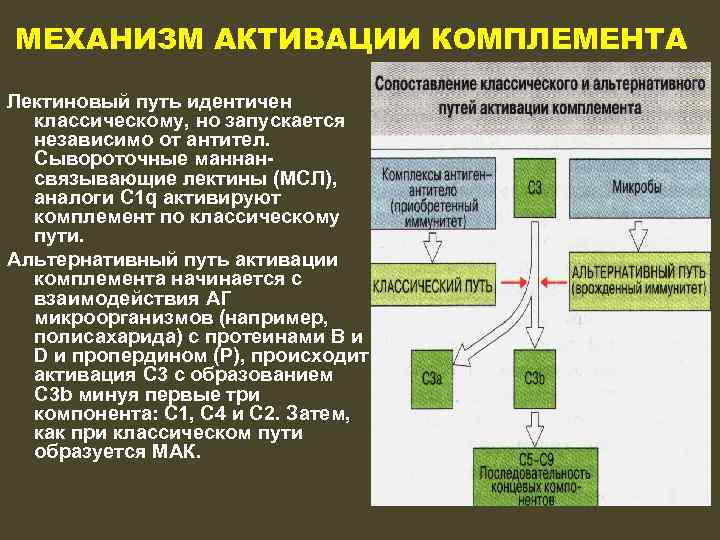 МЕХАНИЗМ АКТИВАЦИИ КОМПЛЕМЕНТА Лектиновый путь идентичен классическому, но запускается независимо от антител. Сывороточные маннансвязывающие лектины (МСЛ), аналоги С 1 q активируют комплемент по классическому пути. Альтернативный путь активации комплемента начинается с взаимодействия АГ микроорганизмов (например, полисахарида) с протеинами B и D и пропердином (Р), происходит активация С 3 с образованием С 3 b минуя первые три компонента: С 1, С 4 и С 2. Затем, как при классическом пути образуется МАК.
МЕХАНИЗМ АКТИВАЦИИ КОМПЛЕМЕНТА Лектиновый путь идентичен классическому, но запускается независимо от антител. Сывороточные маннансвязывающие лектины (МСЛ), аналоги С 1 q активируют комплемент по классическому пути. Альтернативный путь активации комплемента начинается с взаимодействия АГ микроорганизмов (например, полисахарида) с протеинами B и D и пропердином (Р), происходит активация С 3 с образованием С 3 b минуя первые три компонента: С 1, С 4 и С 2. Затем, как при классическом пути образуется МАК.
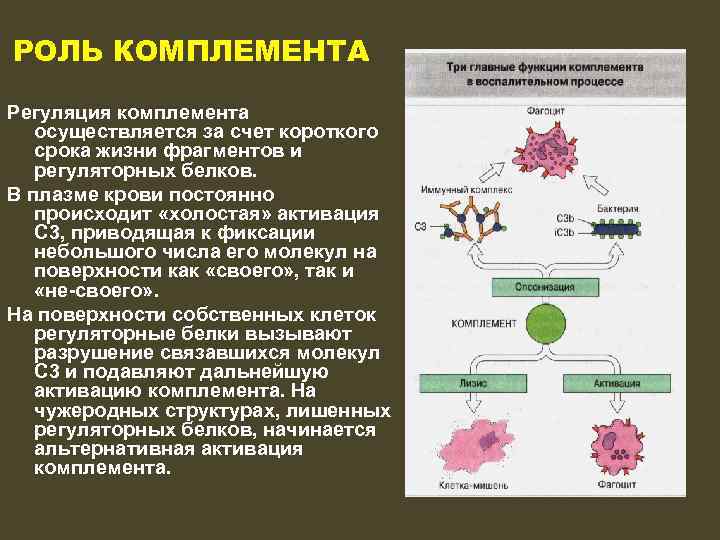 РОЛЬ КОМПЛЕМЕНТА Регуляция комплемента осуществляется за счет короткого срока жизни фрагментов и регуляторных белков. В плазме крови постоянно происходит «холостая» активация С 3, приводящая к фиксации небольшого числа его молекул на поверхности как «своего» , так и «не-своего» . На поверхности собственных клеток регуляторные белки вызывают разрушение связавшихся молекул С 3 и подавляют дальнейшую активацию комплемента. На чужеродных структурах, лишенных регуляторных белков, начинается альтернативная активация комплемента.
РОЛЬ КОМПЛЕМЕНТА Регуляция комплемента осуществляется за счет короткого срока жизни фрагментов и регуляторных белков. В плазме крови постоянно происходит «холостая» активация С 3, приводящая к фиксации небольшого числа его молекул на поверхности как «своего» , так и «не-своего» . На поверхности собственных клеток регуляторные белки вызывают разрушение связавшихся молекул С 3 и подавляют дальнейшую активацию комплемента. На чужеродных структурах, лишенных регуляторных белков, начинается альтернативная активация комплемента.
 УЧАСТИЕ КОМПЛЕМЕНТА В ПАТОЛОГИЧЕСКИХ ПРОЦЕССАХ Системная активация комплемента приводит к образованию больших количеств анафилатоксинов (шок при бактериемии). Тканевый некроз активирует комплемент. Активация комплемента вследствие образования иммунных комплексов приводит к повреждениям тканей.
УЧАСТИЕ КОМПЛЕМЕНТА В ПАТОЛОГИЧЕСКИХ ПРОЦЕССАХ Системная активация комплемента приводит к образованию больших количеств анафилатоксинов (шок при бактериемии). Тканевый некроз активирует комплемент. Активация комплемента вследствие образования иммунных комплексов приводит к повреждениям тканей.
 ЛИЗОЦИМ Лизоцим открыт в 1909 г. П. Л. Лащенко и выделен и изучен в 1922 г. А. Флемингом. Лизоцим – это протеолитический фермент мурамидаза (от лат. murus – стенка) с молекулярной массой 14000 -16000, синтезируется макрофагами, нейтрафилами и другими фагоцитирующими клетками, содержится в крови, лимфе, слезах, молоке, сперме, в урогенитальном тракте, на слизистых оболочках дыхательных путей, в ЖКТ. Лизоцим отсутствует лишь только в СМЖ и передней камере глаза. Лизоцим содержится в гранулах нейтрофилов и макрофагов. Механизм действия: разрушение гликопротеинов (мурамилдипептида) клеточной стенки бактерий, что приводит к их лизису; способствует фагоцитозу поврежденных клеток. Лизоцим активирует фагоцитоз и образование антител.
ЛИЗОЦИМ Лизоцим открыт в 1909 г. П. Л. Лащенко и выделен и изучен в 1922 г. А. Флемингом. Лизоцим – это протеолитический фермент мурамидаза (от лат. murus – стенка) с молекулярной массой 14000 -16000, синтезируется макрофагами, нейтрафилами и другими фагоцитирующими клетками, содержится в крови, лимфе, слезах, молоке, сперме, в урогенитальном тракте, на слизистых оболочках дыхательных путей, в ЖКТ. Лизоцим отсутствует лишь только в СМЖ и передней камере глаза. Лизоцим содержится в гранулах нейтрофилов и макрофагов. Механизм действия: разрушение гликопротеинов (мурамилдипептида) клеточной стенки бактерий, что приводит к их лизису; способствует фагоцитозу поврежденных клеток. Лизоцим активирует фагоцитоз и образование антител.
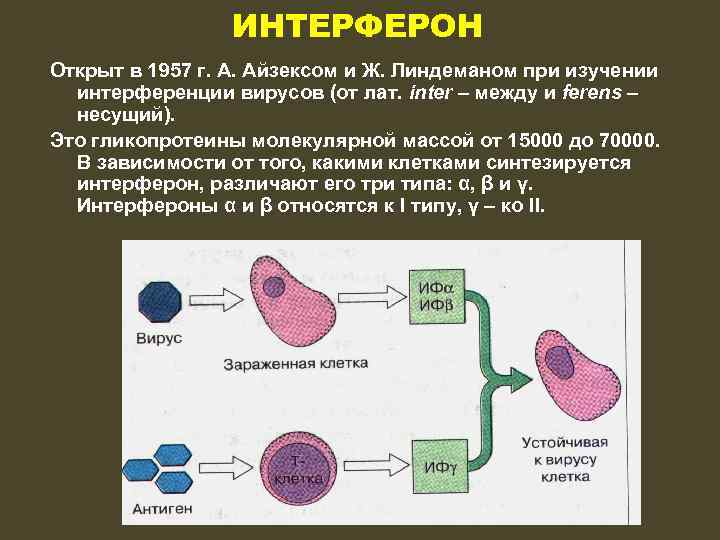 ИНТЕРФЕРОН Открыт в 1957 г. А. Айзексом и Ж. Линдеманом при изучении интерференции вирусов (от лат. inter – между и ferens – несущий). Это гликопротеины молекулярной массой от 15000 до 70000. В зависимости от того, какими клетками синтезируется интерферон, различают его три типа: α, β и γ. Интерфероны α и β относятся к I типу, γ – ко II.
ИНТЕРФЕРОН Открыт в 1957 г. А. Айзексом и Ж. Линдеманом при изучении интерференции вирусов (от лат. inter – между и ferens – несущий). Это гликопротеины молекулярной массой от 15000 до 70000. В зависимости от того, какими клетками синтезируется интерферон, различают его три типа: α, β и γ. Интерфероны α и β относятся к I типу, γ – ко II.
 ИНФ – индуцибельные белки клеток позвоночных; как цитокины в организме они выполняют контрольно-регуляторные функции, направленные на сохранение клеточного гомеостаза; важнейшие из них – антивирусная, противоопухолевая, иммуномодулирующая и радиопротекторная активности. α-ИФН синтезируют лейкоциты периферической крови (лейкоцитарный ИНФ); β-ИНФ синтезируют фибробласты (фибробластный ИНФ); γ-ИНФ – продукт стимулированных Т-лимфоцитов, NK-клеток и макрофагов (иммунный ИНФ). Интерферон-γ – полифункциональный иммуномодулирующий лимфокин, влияющий на рост и дифференцировку клеток разных типов, напротив вызывает активацию макрофагов и лимфоцитов. На макрофагах усиливается адгезия молекул, усиливаются иммунные реакции. Лимфоциты начинаю активно экспрессировать молекулы специфического иммунного ответа. Интерферон-γ обладает провоспалительной активностью.
ИНФ – индуцибельные белки клеток позвоночных; как цитокины в организме они выполняют контрольно-регуляторные функции, направленные на сохранение клеточного гомеостаза; важнейшие из них – антивирусная, противоопухолевая, иммуномодулирующая и радиопротекторная активности. α-ИФН синтезируют лейкоциты периферической крови (лейкоцитарный ИНФ); β-ИНФ синтезируют фибробласты (фибробластный ИНФ); γ-ИНФ – продукт стимулированных Т-лимфоцитов, NK-клеток и макрофагов (иммунный ИНФ). Интерферон-γ – полифункциональный иммуномодулирующий лимфокин, влияющий на рост и дифференцировку клеток разных типов, напротив вызывает активацию макрофагов и лимфоцитов. На макрофагах усиливается адгезия молекул, усиливаются иммунные реакции. Лимфоциты начинаю активно экспрессировать молекулы специфического иммунного ответа. Интерферон-γ обладает провоспалительной активностью.
 МЕХАНИЗМ АНТИВИРУСНОГО ДЕЙСТВИЯ ИНТЕРФЕРОНА 1. ИНФ индуцирует антивирусное состояние клетки. ИНФ не действует непосредственно на вирионы или их нуклеиновые кислоты и активны лишь после проникновения их в клетку, угнетая трансляцию вирусной м. РНК. 2. ИНФ не обладает вирусспецифичностью, что объясняет их универсально широкий спектр антивирусной активности. Образующийся ИНФ взаимодействует с интактными клетками, блокируя репродуктивный цикл вирусов за счет активации клеточных ферментов, экспрессия которых регулируется ИНФ. 3. Основной биологический эффект ИНФ – подавление синтеза вирусных белков, возможны также действия на другие этапы репродукции, включая отпочковывание дочерних популяций.
МЕХАНИЗМ АНТИВИРУСНОГО ДЕЙСТВИЯ ИНТЕРФЕРОНА 1. ИНФ индуцирует антивирусное состояние клетки. ИНФ не действует непосредственно на вирионы или их нуклеиновые кислоты и активны лишь после проникновения их в клетку, угнетая трансляцию вирусной м. РНК. 2. ИНФ не обладает вирусспецифичностью, что объясняет их универсально широкий спектр антивирусной активности. Образующийся ИНФ взаимодействует с интактными клетками, блокируя репродуктивный цикл вирусов за счет активации клеточных ферментов, экспрессия которых регулируется ИНФ. 3. Основной биологический эффект ИНФ – подавление синтеза вирусных белков, возможны также действия на другие этапы репродукции, включая отпочковывание дочерних популяций.
 ЗАЩИТНЫЕ БЕЛКИ СЫВОРОТКИ КРОВИ Это протеины, участвующие в защите организма от микробов и других антигенов: белки острой фазы, опсонины, пропердин, β-лизин, фибронектин и др. «Острофазная» реакция – это ранняя (первые часы) реакция, при которой повышается концентрация белков плазмы. Макрофаги секретируют ИЛ-1, который инициирует воспалительную реакцию, может вызывать системные реакции: лихорадку, гипотонию, шок, инициирует синтез остальных белков острой. Белки острой фазы – большая группу белков, обладающих антимикробным действием, способствующих фагоцитозу, активации комплемента, формированию и ликвидации воспалительного очага. Белки острой фазы продуцируются в печени при действии цитокинов, в основном ИЛ-1, ФНО-α и ИЛ-6. Основную массу белков острой фазы составляют С-реактивный белок и сывороточные амилоиды А и Р, а также – факторы свертывания крови, металлосвязывающие белки, ингибиторы протеаз, компоненты комплемента и некоторые другие.
ЗАЩИТНЫЕ БЕЛКИ СЫВОРОТКИ КРОВИ Это протеины, участвующие в защите организма от микробов и других антигенов: белки острой фазы, опсонины, пропердин, β-лизин, фибронектин и др. «Острофазная» реакция – это ранняя (первые часы) реакция, при которой повышается концентрация белков плазмы. Макрофаги секретируют ИЛ-1, который инициирует воспалительную реакцию, может вызывать системные реакции: лихорадку, гипотонию, шок, инициирует синтез остальных белков острой. Белки острой фазы – большая группу белков, обладающих антимикробным действием, способствующих фагоцитозу, активации комплемента, формированию и ликвидации воспалительного очага. Белки острой фазы продуцируются в печени при действии цитокинов, в основном ИЛ-1, ФНО-α и ИЛ-6. Основную массу белков острой фазы составляют С-реактивный белок и сывороточные амилоиды А и Р, а также – факторы свертывания крови, металлосвязывающие белки, ингибиторы протеаз, компоненты комплемента и некоторые другие.
 ЗАЩИТНЫЕ БЕЛКИ СЫВОРОТКИ КРОВИ v Сывороточный амилоидный белок А – липопротеин, обладающий способностью к хематтракции нейтрофилов, моноцитов и лимфоцитов, вызывает временную репарацию повреждений клетки и тканей при воспалении. v Сывороточный амилоид Р близок по структуре к СРБ, обладает способностью к активации комплемента. v Фибронектин – белок плазмы крови и тканевых жидкостей, синтезируемый макрофагами, обеспечивает опсонизацию антигенов и связывание фагоцитов с антигенами и микробами, «экранирует» дефекты эндотелия сосудов, препятствуя тромбообразованию. v Белки, связывающие железо – гаптоглобин, гемопексин, трансферрин – препятствуют размножению микроорганизмов, нуждающихся в железе. v Ингибиторы протеаз (антитрипсин, антихимотрипсин, церулоплазмин и макроглобулин) препятствуют разрушению тканей протеазами нейтрофилов в очагах воспаления.
ЗАЩИТНЫЕ БЕЛКИ СЫВОРОТКИ КРОВИ v Сывороточный амилоидный белок А – липопротеин, обладающий способностью к хематтракции нейтрофилов, моноцитов и лимфоцитов, вызывает временную репарацию повреждений клетки и тканей при воспалении. v Сывороточный амилоид Р близок по структуре к СРБ, обладает способностью к активации комплемента. v Фибронектин – белок плазмы крови и тканевых жидкостей, синтезируемый макрофагами, обеспечивает опсонизацию антигенов и связывание фагоцитов с антигенами и микробами, «экранирует» дефекты эндотелия сосудов, препятствуя тромбообразованию. v Белки, связывающие железо – гаптоглобин, гемопексин, трансферрин – препятствуют размножению микроорганизмов, нуждающихся в железе. v Ингибиторы протеаз (антитрипсин, антихимотрипсин, церулоплазмин и макроглобулин) препятствуют разрушению тканей протеазами нейтрофилов в очагах воспаления.


