Стерилизация мед.изделий.ppt
- Количество слайдов: 70
 «МЕТОДЫ СТЕРИЛИЗАЦИИ МЕДИЦИНСКИХ ИЗДЕЛИЙ И АППАРАТУРЫ» . Работу выполнили: Студентки 5 курса 374 группы Власова Е. А. Гаврик Т. Л.
«МЕТОДЫ СТЕРИЛИЗАЦИИ МЕДИЦИНСКИХ ИЗДЕЛИЙ И АППАРАТУРЫ» . Работу выполнили: Студентки 5 курса 374 группы Власова Е. А. Гаврик Т. Л.
 НОРМАТИВНАЯ ДОКУМЕНТАЦИЯ ГОСТ 25375 -82. Методы, средства и режимы стерилизации и дезинфекции изделий медицинского назначения. Термины и определения. ГОСТ Р ИСО 11737 -1 -95. Стерилизация медицинской продукции. Микробиологические методы. Часть 1. Оценка популяции микроорганизмов в продукте. ГОСТ Р 51609 -2000. Изделия медицинские. Классификация в зависимости от потенциального риска применения. Общие требования. ГОСТ Р ИСО Ш 38 -1 -2000. Стерилизация медицинской продукции. Биологические индикаторы. Часть1. Технические требования. ГОСТ Р 51935 -2002. Стерилизаторы паровые большие. Общие технические требования и методы испытаний. ГОСТ Р ИСО 13683 -2000. Стерилизация медицинской продукции. Требования к валидации и текущему контролю. Стерилизация влажным теплом в медицинских учреждениях. ГОСТ Р ИСО Ш 40 -1 -2000. Стерилизация медицинской продукции. Химические индикаторы. Часть 1. Общие требования. ГОСТ Р ИСО 11607 -2003. Упаковка для медицинских изделий, подлежащих финишной стерилизации. Общие требования. ГОСТ Р ИСО 11140 -2 -2001. Стерилизация медицинской продукции. Химические индикаторы. Часть 2. Оборудование и методы. ГОСТ Р ИСО 11138 -3 -2000. Стерилизация медицинской продукции. Биологические индикаторы Часть 3. Биологические индикаторы для стерилизации влажным теплом (паровой стерилизации). ГОСТ Р ИСО 11134 -2000. Стерилизация медицинской продукции. Требования к валидации и текущему контролю. Промышленная стерилизация влажным теплом.
НОРМАТИВНАЯ ДОКУМЕНТАЦИЯ ГОСТ 25375 -82. Методы, средства и режимы стерилизации и дезинфекции изделий медицинского назначения. Термины и определения. ГОСТ Р ИСО 11737 -1 -95. Стерилизация медицинской продукции. Микробиологические методы. Часть 1. Оценка популяции микроорганизмов в продукте. ГОСТ Р 51609 -2000. Изделия медицинские. Классификация в зависимости от потенциального риска применения. Общие требования. ГОСТ Р ИСО Ш 38 -1 -2000. Стерилизация медицинской продукции. Биологические индикаторы. Часть1. Технические требования. ГОСТ Р 51935 -2002. Стерилизаторы паровые большие. Общие технические требования и методы испытаний. ГОСТ Р ИСО 13683 -2000. Стерилизация медицинской продукции. Требования к валидации и текущему контролю. Стерилизация влажным теплом в медицинских учреждениях. ГОСТ Р ИСО Ш 40 -1 -2000. Стерилизация медицинской продукции. Химические индикаторы. Часть 1. Общие требования. ГОСТ Р ИСО 11607 -2003. Упаковка для медицинских изделий, подлежащих финишной стерилизации. Общие требования. ГОСТ Р ИСО 11140 -2 -2001. Стерилизация медицинской продукции. Химические индикаторы. Часть 2. Оборудование и методы. ГОСТ Р ИСО 11138 -3 -2000. Стерилизация медицинской продукции. Биологические индикаторы Часть 3. Биологические индикаторы для стерилизации влажным теплом (паровой стерилизации). ГОСТ Р ИСО 11134 -2000. Стерилизация медицинской продукции. Требования к валидации и текущему контролю. Промышленная стерилизация влажным теплом.
 1. 2. Медицинские изделия (МИ) - приборы, аппараты, инструменты, устройства, комплекты, системы с программными средствами, оборудование, приспособления, перевязочные и шовные средства, стоматологические материалы, наборы реагентов, контрольные материалы и стандартные образцы, изделия из полимерных, резиновых и иных материалов, которые применяют в медицинских целях по отдельности или в сочетании между собой и которые предназначены для: профилактики, диагностики, лечения заболеваний, реабилитации, проведения медицинских процедур, исследований медицинского характера, замены или модификации частей тканей, органов и организма человека, восстановления или компенсации нарушенных или утраченных физиологических функций, контроля над зачатием; воздействия на организм человека таким образом, что их функциональное назначение не реализуется путем химического, фармакологического, иммунологического или метаболического взаимодействия с организмом человека.
1. 2. Медицинские изделия (МИ) - приборы, аппараты, инструменты, устройства, комплекты, системы с программными средствами, оборудование, приспособления, перевязочные и шовные средства, стоматологические материалы, наборы реагентов, контрольные материалы и стандартные образцы, изделия из полимерных, резиновых и иных материалов, которые применяют в медицинских целях по отдельности или в сочетании между собой и которые предназначены для: профилактики, диагностики, лечения заболеваний, реабилитации, проведения медицинских процедур, исследований медицинского характера, замены или модификации частей тканей, органов и организма человека, восстановления или компенсации нарушенных или утраченных физиологических функций, контроля над зачатием; воздействия на организм человека таким образом, что их функциональное назначение не реализуется путем химического, фармакологического, иммунологического или метаболического взаимодействия с организмом человека.
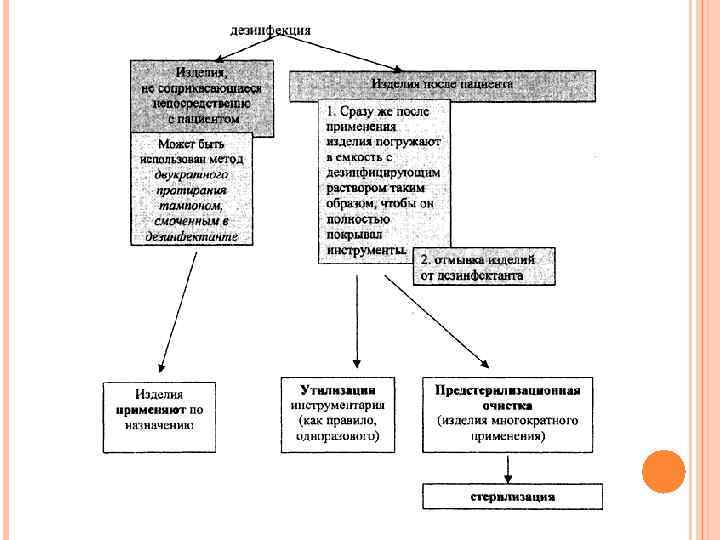
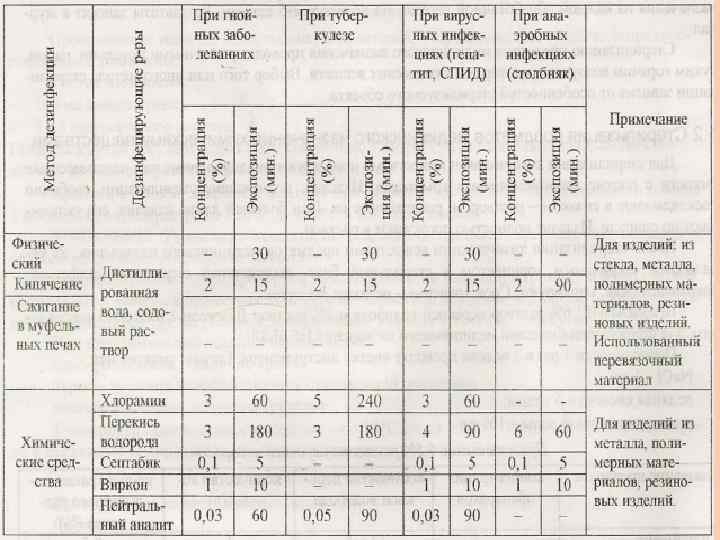
 ДЕЗИНФЕКЦИЯ 1. 2. Дезинфекция изделий медицинского назначения - умерщвление на изделиях или удаление с изделий медицинского назначения патогенных микроорганизмов. Дезинфекцию изделий осуществляют физическим (кипячение, водяной насыщенный пар под избыточным давлением, сухой горячий воздух) и химическим (использование растворов химических средств) методами. Выбор метода дезинфекции зависит от особенностей изделия и его назначения. Дезинфекцию с использованием физического метода выполняют: способом кипячения в дистиллированной воде или в воде с добавлением натрия двууглекислого (сода пищевая); паровым методом (в паровом стерилизаторе - автоклаве) и воздушным методом (в воздушном стерилизаторе).
ДЕЗИНФЕКЦИЯ 1. 2. Дезинфекция изделий медицинского назначения - умерщвление на изделиях или удаление с изделий медицинского назначения патогенных микроорганизмов. Дезинфекцию изделий осуществляют физическим (кипячение, водяной насыщенный пар под избыточным давлением, сухой горячий воздух) и химическим (использование растворов химических средств) методами. Выбор метода дезинфекции зависит от особенностей изделия и его назначения. Дезинфекцию с использованием физического метода выполняют: способом кипячения в дистиллированной воде или в воде с добавлением натрия двууглекислого (сода пищевая); паровым методом (в паровом стерилизаторе - автоклаве) и воздушным методом (в воздушном стерилизаторе).
 3. 4. Дезинфекции способом кипячения подвергают изделия из стекла, металлов, термостойких полимерных материалов и резин. Перед кипячением изделия очищают от органических загрязнений, промывая водопроводной водой с соблюдением мер противоэпидемической защиты. Паровым методом дезинфицируют изделия из стекла, металлов, резин, латекса, термостойких полимерных материалов. Предварительная очистка изделий не требуется. Их складывают в стерилизационные коробки и помещают в паровой стерилизатор. Дезинфекция осуществляется воздействием водяного насыщенного пара под избыточным давлением.
3. 4. Дезинфекции способом кипячения подвергают изделия из стекла, металлов, термостойких полимерных материалов и резин. Перед кипячением изделия очищают от органических загрязнений, промывая водопроводной водой с соблюдением мер противоэпидемической защиты. Паровым методом дезинфицируют изделия из стекла, металлов, резин, латекса, термостойких полимерных материалов. Предварительная очистка изделий не требуется. Их складывают в стерилизационные коробки и помещают в паровой стерилизатор. Дезинфекция осуществляется воздействием водяного насыщенного пара под избыточным давлением.

 ПРЕДСТЕРИЛИЗАЦИОННАЯ ОЧИСТКА Предстерилизационная очистка – удаление загрязнений с изделий медицинского назначения, подлежащих стерилизации. 1. Предстерилизационную очистку изделий медицинского назначения осуществляют после их дезинфекции и отмывания остатков дезинфицирующих средств проточной питьевой водой. Предстерилизационную очистку лигатурного шовного материала (нити хирургические шелковые крученые, нити хирургические капроновые крученые, шнуры хирургические полиэфирные) в ЛПУ не проводят. 2. Предстерилизационную очистку проводят ручным или механизированным (с помощью специального оборудования) способом.
ПРЕДСТЕРИЛИЗАЦИОННАЯ ОЧИСТКА Предстерилизационная очистка – удаление загрязнений с изделий медицинского назначения, подлежащих стерилизации. 1. Предстерилизационную очистку изделий медицинского назначения осуществляют после их дезинфекции и отмывания остатков дезинфицирующих средств проточной питьевой водой. Предстерилизационную очистку лигатурного шовного материала (нити хирургические шелковые крученые, нити хирургические капроновые крученые, шнуры хирургические полиэфирные) в ЛПУ не проводят. 2. Предстерилизационную очистку проводят ручным или механизированным (с помощью специального оборудования) способом.
 3. При наличии у средства, наряду с моющими, также и антимикробных свойств (в т. ч. в отношении возбудителей парентеральных вирусных гепатитов и ВИЧ-инфекции) предстерилизационная очистка изделий на этапе замачивания или кипячения в растворе может быть совмещена с их дезинфекцией. Разъемные изделия подвергают предстерилизационной очистке в разобранном виде. При замачивании или кипячении в моющем растворе изделия полностью погружают в раствор моющего средства, заполняя им каналы и полости изделий. Мойку изделий осуществляют с помощью ерша, ватномарлевых тампонов, тканевых салфеток; каналы изделий промывают с помощью шприца. Использование ерша при очистке резиновых изделий не допускается. 4.
3. При наличии у средства, наряду с моющими, также и антимикробных свойств (в т. ч. в отношении возбудителей парентеральных вирусных гепатитов и ВИЧ-инфекции) предстерилизационная очистка изделий на этапе замачивания или кипячения в растворе может быть совмещена с их дезинфекцией. Разъемные изделия подвергают предстерилизационной очистке в разобранном виде. При замачивании или кипячении в моющем растворе изделия полностью погружают в раствор моющего средства, заполняя им каналы и полости изделий. Мойку изделий осуществляют с помощью ерша, ватномарлевых тампонов, тканевых салфеток; каналы изделий промывают с помощью шприца. Использование ерша при очистке резиновых изделий не допускается. 4.


 СТЕРИЛИЗАЦИЯ 1. § § § Стерилизация изделий медицинского назначения умерщвление на изделиях или в изделиях медицинского назначения микроорганизмов всех видов, находящихся на всех стадиях развития. Стерилизацию осуществляют следующими методами: физическими (паровой, воздушный, в среде нагретых шариков); химическими (применение растворов химических средств, газовый); в промышленных условиях используют радиационный метод (гамма-излучения). Выбор адекватного метода стерилизации зависит от особенностей стерилизуемых изделий. При стерилизации паровым, воздушным и газовым методами изделия, как правило, стерилизуют упакованными в стерилизационные упаковочные материалы; при паровом методе, кроме того, используют стерилизационные коробки без фильтров и с фильтрами. При воздушном методе, а также в отдельных случаях при паровом и газовом методах, допускается стерилизация инструментов в неупакованном виде (в открытых лотках).
СТЕРИЛИЗАЦИЯ 1. § § § Стерилизация изделий медицинского назначения умерщвление на изделиях или в изделиях медицинского назначения микроорганизмов всех видов, находящихся на всех стадиях развития. Стерилизацию осуществляют следующими методами: физическими (паровой, воздушный, в среде нагретых шариков); химическими (применение растворов химических средств, газовый); в промышленных условиях используют радиационный метод (гамма-излучения). Выбор адекватного метода стерилизации зависит от особенностей стерилизуемых изделий. При стерилизации паровым, воздушным и газовым методами изделия, как правило, стерилизуют упакованными в стерилизационные упаковочные материалы; при паровом методе, кроме того, используют стерилизационные коробки без фильтров и с фильтрами. При воздушном методе, а также в отдельных случаях при паровом и газовом методах, допускается стерилизация инструментов в неупакованном виде (в открытых лотках).
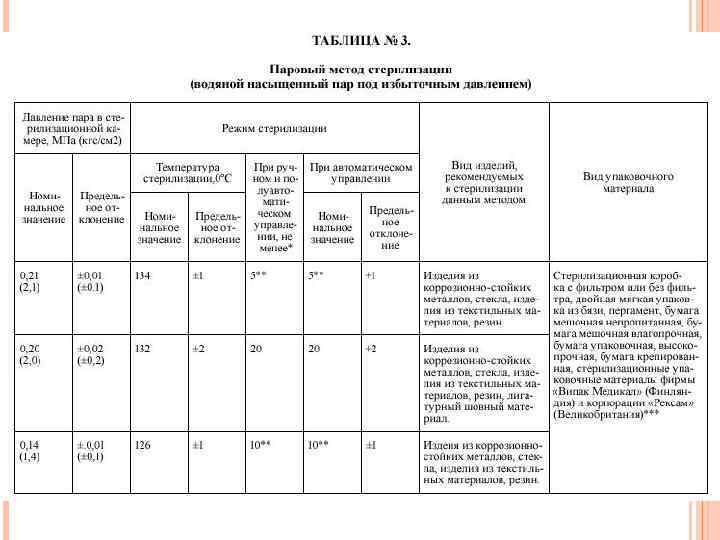
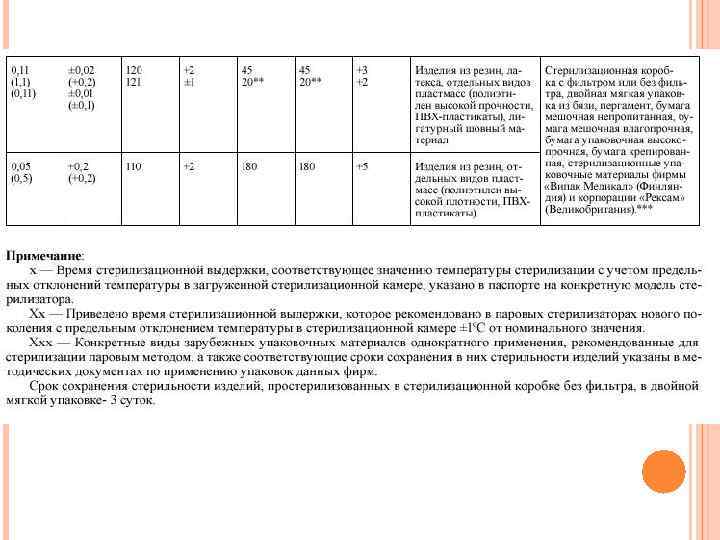
 ПАРОВОЙ МЕТОД СТЕРИЛИЗАЦИИ 1. 2. 3. 4. Стерилизующим средством является водяной насыщенный пар под избыточным давлением 0, 05 МПа - 0, 21 МПа температурой 110 -135 град. С; стерилизацию осуществляют в паровых стерилизаторах (автоклавах). Паровым методом стерилизуют общие хирургические и специальные инструменты, детали приборов и аппаратов из коррозионностойких металлов, стекла, шприцы с пометкой 200 град. С, хирургическое белье, перевязочный и шовный материал, изделия из резин (перчатки, трубки, катетеры, зонды и т. д. ), латекса, отдельных видов пластмасс. Стерилизационные коробки (биксы) не являются упаковкой для хранения простерилизованных изделий. Хирургическое белье, перевязочный материал укладывают в стерилизационные коробки параллельно движению пара. Срок сохранения стерильности изделий, простерилизованных в коробке без фильтра, в двойной мягкой упаковке - 3 суток, в пергаменте, бумаге мешочной непропитанной, бумаге мешочной влагопрочной, бумаге упаковочной высокопрочной, бумаге крепированной, стерилизационной коробке с фильтром - 20 суток.
ПАРОВОЙ МЕТОД СТЕРИЛИЗАЦИИ 1. 2. 3. 4. Стерилизующим средством является водяной насыщенный пар под избыточным давлением 0, 05 МПа - 0, 21 МПа температурой 110 -135 град. С; стерилизацию осуществляют в паровых стерилизаторах (автоклавах). Паровым методом стерилизуют общие хирургические и специальные инструменты, детали приборов и аппаратов из коррозионностойких металлов, стекла, шприцы с пометкой 200 град. С, хирургическое белье, перевязочный и шовный материал, изделия из резин (перчатки, трубки, катетеры, зонды и т. д. ), латекса, отдельных видов пластмасс. Стерилизационные коробки (биксы) не являются упаковкой для хранения простерилизованных изделий. Хирургическое белье, перевязочный материал укладывают в стерилизационные коробки параллельно движению пара. Срок сохранения стерильности изделий, простерилизованных в коробке без фильтра, в двойной мягкой упаковке - 3 суток, в пергаменте, бумаге мешочной непропитанной, бумаге мешочной влагопрочной, бумаге упаковочной высокопрочной, бумаге крепированной, стерилизационной коробке с фильтром - 20 суток.
 5. Резиновые перчатки перед стерилизацией пересыпают внутри и снаружи тальком для предохранения их от склеивания. Между перчатками прокладывают марлю или бумагу, каждую пару перчаток заворачивают отдельно в марлю или бумагу и в таком виде помещают в стерилизационную коробку или в другую упаковку. В целях уменьшения неблагоприятного воздействия пара резиновые перчатки, как и другие изделия из резин, стерилизуют при температуре 120 -122 град. С. Паровым методом стерилизуют лигатурный шовный материал. Готовят к стерилизации в виде косичек, мотков, наматывая на катушки, стеклянные палочки и т. д. Затем лигатурный шовный материал заворачивают в два слоя упаковочного материала (при размещении в стерилизационной коробке - в один слой упаковочного материала) в количестве, рассчитанном на одну операцию. На упаковке отмечают вид шовного материала и его номер. Нити хирургические капроновые крученые стерилизуют паром только при температуре 120 -122 град. С; лигатурный шовный материал других видов допускается стерилизовать при температуре 130 -134 гр. С. Лигатурный шовный материал хранят в той же упаковке, в которой он был простерилизован, в специальных шкафах для стерильных изделий. Неиспользованный стерильный лигатурный шовный материал в случае нарушения условий или истечения срока хранения может быть повторно (еще лишь один раз) простерилизован паровым методом при температуре 120 -122 град. С. 6.
5. Резиновые перчатки перед стерилизацией пересыпают внутри и снаружи тальком для предохранения их от склеивания. Между перчатками прокладывают марлю или бумагу, каждую пару перчаток заворачивают отдельно в марлю или бумагу и в таком виде помещают в стерилизационную коробку или в другую упаковку. В целях уменьшения неблагоприятного воздействия пара резиновые перчатки, как и другие изделия из резин, стерилизуют при температуре 120 -122 град. С. Паровым методом стерилизуют лигатурный шовный материал. Готовят к стерилизации в виде косичек, мотков, наматывая на катушки, стеклянные палочки и т. д. Затем лигатурный шовный материал заворачивают в два слоя упаковочного материала (при размещении в стерилизационной коробке - в один слой упаковочного материала) в количестве, рассчитанном на одну операцию. На упаковке отмечают вид шовного материала и его номер. Нити хирургические капроновые крученые стерилизуют паром только при температуре 120 -122 град. С; лигатурный шовный материал других видов допускается стерилизовать при температуре 130 -134 гр. С. Лигатурный шовный материал хранят в той же упаковке, в которой он был простерилизован, в специальных шкафах для стерильных изделий. Неиспользованный стерильный лигатурный шовный материал в случае нарушения условий или истечения срока хранения может быть повторно (еще лишь один раз) простерилизован паровым методом при температуре 120 -122 град. С. 6.
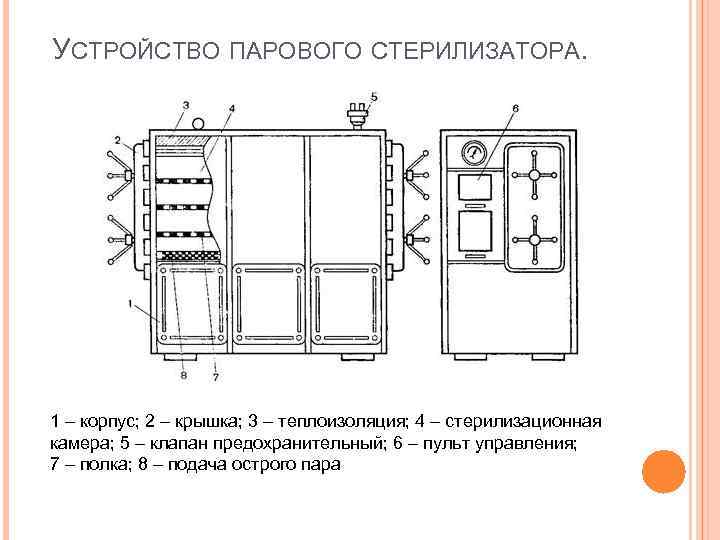 УСТРОЙСТВО ПАРОВОГО СТЕРИЛИЗАТОРА. 1 – корпус; 2 – крышка; 3 – теплоизоляция; 4 – стерилизационная камера; 5 – клапан предохранительный; 6 – пульт управления; 7 – полка; 8 – подача острого пара
УСТРОЙСТВО ПАРОВОГО СТЕРИЛИЗАТОРА. 1 – корпус; 2 – крышка; 3 – теплоизоляция; 4 – стерилизационная камера; 5 – клапан предохранительный; 6 – пульт управления; 7 – полка; 8 – подача острого пара
 ПАРОВОЙ СТЕРИЛИЗАТОР.
ПАРОВОЙ СТЕРИЛИЗАТОР.
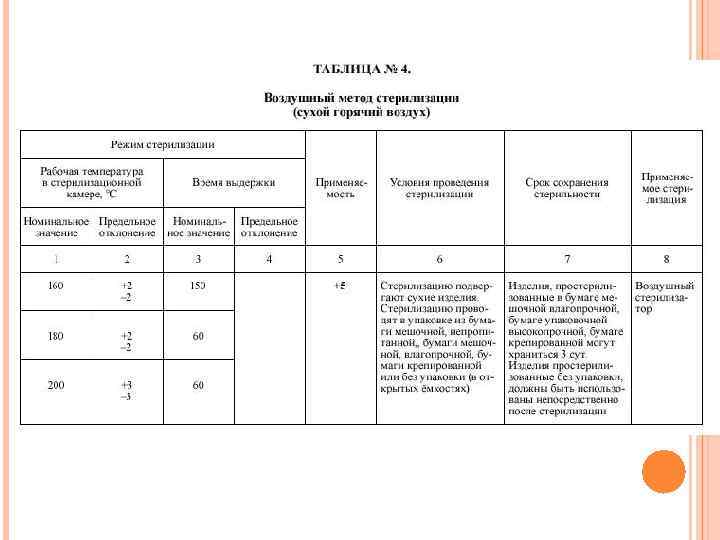
 ВОЗДУШНЫЙ МЕТОД СТЕРИЛИЗАЦИИ 1. 2. 3. Стерилизующим средством является сухой горячий воздух температурой 160 град. С и 180 град. С; стерилизацию осуществляют в воздушных стерилизаторах. Воздушным методом стерилизуют хирургические, гинекологические, стоматологические инструменты, детали приборов и аппаратов, в том числе изготовленные из коррозионнонестойких металлов, шприцы с пометкой 200 град. С, инъекционные иглы, изделия из силиконовой резины. Срок сохранения стерильности изделий, простерилизованных в бумаге мешочной влагопрочной, бумаге упаковочной высокопрочной, бумаге крепированной - 20 суток. Изделия, простерилизованные без упаковки, помещают на "стерильный стол" и используют в течение одной рабочей смены. Перед стерилизацией воздушным методом изделия после предстерилизационной очистки обязательно высушивают в сушильном шкафу при температуре 85 град. С до исчезновения видимой влаги.
ВОЗДУШНЫЙ МЕТОД СТЕРИЛИЗАЦИИ 1. 2. 3. Стерилизующим средством является сухой горячий воздух температурой 160 град. С и 180 град. С; стерилизацию осуществляют в воздушных стерилизаторах. Воздушным методом стерилизуют хирургические, гинекологические, стоматологические инструменты, детали приборов и аппаратов, в том числе изготовленные из коррозионнонестойких металлов, шприцы с пометкой 200 град. С, инъекционные иглы, изделия из силиконовой резины. Срок сохранения стерильности изделий, простерилизованных в бумаге мешочной влагопрочной, бумаге упаковочной высокопрочной, бумаге крепированной - 20 суток. Изделия, простерилизованные без упаковки, помещают на "стерильный стол" и используют в течение одной рабочей смены. Перед стерилизацией воздушным методом изделия после предстерилизационной очистки обязательно высушивают в сушильном шкафу при температуре 85 град. С до исчезновения видимой влаги.
 3. 4. 5. Качество стерилизации воздушным методом зависит от равномерности распределения горячего воздуха в стерилизационной камере, что достигается правильной загрузкой стерилизатора. Изделия загружают в таком количестве, которое допускает свободную подачу воздуха к стерилизуемому изделию. Стерилизуемые изделия, равномерно распределяя, укладывают горизонтально поперек пазов кассет (полок); не допускается перекрывать продувочные окна и решетки вентиляции. Объемные изделия следует класть на верхнюю металлическую решетку, чтобы они не препятствовали потоку горячего воздуха. При загрузке необходимо следить за тем, чтобы стерилизуемые изделия не попадали в зону вращения крыльчатки. Загрузку и выгрузку изделий проводят при температуре в стерилизационной камере 40 -50 град. С. Изделия стерилизуют завернутыми в стерилизационные упаковочные материалы. Шприцы стерилизуют в разобранном виде. Во время стерилизации металлических инструментов без упаковки их располагают так, чтобы они не касались друга.
3. 4. 5. Качество стерилизации воздушным методом зависит от равномерности распределения горячего воздуха в стерилизационной камере, что достигается правильной загрузкой стерилизатора. Изделия загружают в таком количестве, которое допускает свободную подачу воздуха к стерилизуемому изделию. Стерилизуемые изделия, равномерно распределяя, укладывают горизонтально поперек пазов кассет (полок); не допускается перекрывать продувочные окна и решетки вентиляции. Объемные изделия следует класть на верхнюю металлическую решетку, чтобы они не препятствовали потоку горячего воздуха. При загрузке необходимо следить за тем, чтобы стерилизуемые изделия не попадали в зону вращения крыльчатки. Загрузку и выгрузку изделий проводят при температуре в стерилизационной камере 40 -50 град. С. Изделия стерилизуют завернутыми в стерилизационные упаковочные материалы. Шприцы стерилизуют в разобранном виде. Во время стерилизации металлических инструментов без упаковки их располагают так, чтобы они не касались друга.
 ВОЗДУШНЫЙ СТЕРИЛИЗАТОР.
ВОЗДУШНЫЙ СТЕРИЛИЗАТОР.
 СТЕРИЛИЗАЦИЯ В СРЕДЕ НАГРЕТЫХ СТЕКЛЯННЫХ ШАРИКОВ Гласперленовый метод предназначен для быстрой стерилизации небольших цельнометаллических инструментов, не имеющих полостей, каналов и замковых частей. Метод крайне прост - инструмент погружается в среду мелких стеклянных шариков, нагретых до температуры 190 2900 С на 20 - 180 секунд, в зависимости от размера и массы инструмента. Этот метод используется, в основном, стоматологами для экспресс-стерилизации мелких инструментов - боров, пульпоэкстракторов, корневых игл, алмазных головок и др. , а также рабочих частей более крупных - зондов, гладилок, экскаваторов, шпателей и т. д. Так же можно стерилизовать акупунктурные иглы.
СТЕРИЛИЗАЦИЯ В СРЕДЕ НАГРЕТЫХ СТЕКЛЯННЫХ ШАРИКОВ Гласперленовый метод предназначен для быстрой стерилизации небольших цельнометаллических инструментов, не имеющих полостей, каналов и замковых частей. Метод крайне прост - инструмент погружается в среду мелких стеклянных шариков, нагретых до температуры 190 2900 С на 20 - 180 секунд, в зависимости от размера и массы инструмента. Этот метод используется, в основном, стоматологами для экспресс-стерилизации мелких инструментов - боров, пульпоэкстракторов, корневых игл, алмазных головок и др. , а также рабочих частей более крупных - зондов, гладилок, экскаваторов, шпателей и т. д. Так же можно стерилизовать акупунктурные иглы.
 Преимущества метода - короткое время стерилизации и отсутствие расходных материалов.
Преимущества метода - короткое время стерилизации и отсутствие расходных материалов.
 СТЕРИЛИЗАЦИЯ РАСТВОРАМИ ХИМИЧЕСКИХ СРЕДСТВ Стерилизация изделий растворами химических средств является вспомогательным методом, поскольку изделия нельзя простерилизовать в упаковке, а по окончании стерилизации их необходимо промыть стерильной жидкостью (питьевая вода, 0, 9% раствор натрия хлорида), что при нарушении правил асептики может привести к вторичному обсеменению простерилизованных изделий микроорганизмами. Метод следует применять для стерилизации изделий из термолабильных материалов. Конструкция изделия должна позволять стерилизовать его растворами химических средств. При этом необходим хороший доступ стерилизующего средства и промывной жидкости ко всем стерилизуемым поверхностям изделия. 1.
СТЕРИЛИЗАЦИЯ РАСТВОРАМИ ХИМИЧЕСКИХ СРЕДСТВ Стерилизация изделий растворами химических средств является вспомогательным методом, поскольку изделия нельзя простерилизовать в упаковке, а по окончании стерилизации их необходимо промыть стерильной жидкостью (питьевая вода, 0, 9% раствор натрия хлорида), что при нарушении правил асептики может привести к вторичному обсеменению простерилизованных изделий микроорганизмами. Метод следует применять для стерилизации изделий из термолабильных материалов. Конструкция изделия должна позволять стерилизовать его растворами химических средств. При этом необходим хороший доступ стерилизующего средства и промывной жидкости ко всем стерилизуемым поверхностям изделия. 1.
 2. 3. 4. Для стерилизации растворами химических средств используют средства, указанные в табл. 4. 4. , в т. ч. электрохимически активированные р-ры, вырабатываемые в диафрагменных электрохимических установках типа "СТЭЛ", а также в других уста-новках, разрешенных к выпуску, согласно инструк-тивнометодическим документам, утвержденным в установленном порядке в Российской Федерации. При стерилизации растворами химических средств используют стерильные емкости из стекла, металлов, термостойких пластмасс, выдерживающих стерилизацию паровым методом, или покрытые эмалью (эмаль без повреждений). Температура растворов, за исключением специаль-ных режимов применения перекиси водорода и средства Лизоформин 3000, должна составлять не менее 20 град. С для альдегидсодержащих средств и не менее 18 град. С - для остальных средств.
2. 3. 4. Для стерилизации растворами химических средств используют средства, указанные в табл. 4. 4. , в т. ч. электрохимически активированные р-ры, вырабатываемые в диафрагменных электрохимических установках типа "СТЭЛ", а также в других уста-новках, разрешенных к выпуску, согласно инструк-тивнометодическим документам, утвержденным в установленном порядке в Российской Федерации. При стерилизации растворами химических средств используют стерильные емкости из стекла, металлов, термостойких пластмасс, выдерживающих стерилизацию паровым методом, или покрытые эмалью (эмаль без повреждений). Температура растворов, за исключением специаль-ных режимов применения перекиси водорода и средства Лизоформин 3000, должна составлять не менее 20 град. С для альдегидсодержащих средств и не менее 18 град. С - для остальных средств.
 5. 6. 7. 8. Стерилизацию проводят при полном погружении изделий в раствор, свободно их раскладывая. Длинные изделия укладывают по спирали. Разъемные изделия стерилизуют в разобранном виде. Каналы и полости заполняют раствором. Во избежание разбавления рабочих растворов, погружаемые в них изделия должны быть сухими. После стерилизации все манипуляции проводят, соблюдая правила асептики. Изделия извлекают из раствора с помощью стерильных пинцетов (корнцангов), удаляют раствор из каналов и полостей, промывают в стерильной жидкости, налитой в стерильные емкости. При каждом переносе из одной емкости в другую освобождение каналов и полостей и их заполнение свежей жидкостью осуществляют с помощью стерильного шприца, пипетки или иного приспособления. Промытые стерильные изделия после удаления остатков жидкости из каналов и полостей используют сразу по назначению или помещают (с помощью стерильных пинцетов, корнцангов) на хранение в стерильную стерилизационную коробку, выложенную стерильной простыней, на срок не более 3 суток.
5. 6. 7. 8. Стерилизацию проводят при полном погружении изделий в раствор, свободно их раскладывая. Длинные изделия укладывают по спирали. Разъемные изделия стерилизуют в разобранном виде. Каналы и полости заполняют раствором. Во избежание разбавления рабочих растворов, погружаемые в них изделия должны быть сухими. После стерилизации все манипуляции проводят, соблюдая правила асептики. Изделия извлекают из раствора с помощью стерильных пинцетов (корнцангов), удаляют раствор из каналов и полостей, промывают в стерильной жидкости, налитой в стерильные емкости. При каждом переносе из одной емкости в другую освобождение каналов и полостей и их заполнение свежей жидкостью осуществляют с помощью стерильного шприца, пипетки или иного приспособления. Промытые стерильные изделия после удаления остатков жидкости из каналов и полостей используют сразу по назначению или помещают (с помощью стерильных пинцетов, корнцангов) на хранение в стерильную стерилизационную коробку, выложенную стерильной простыней, на срок не более 3 суток.
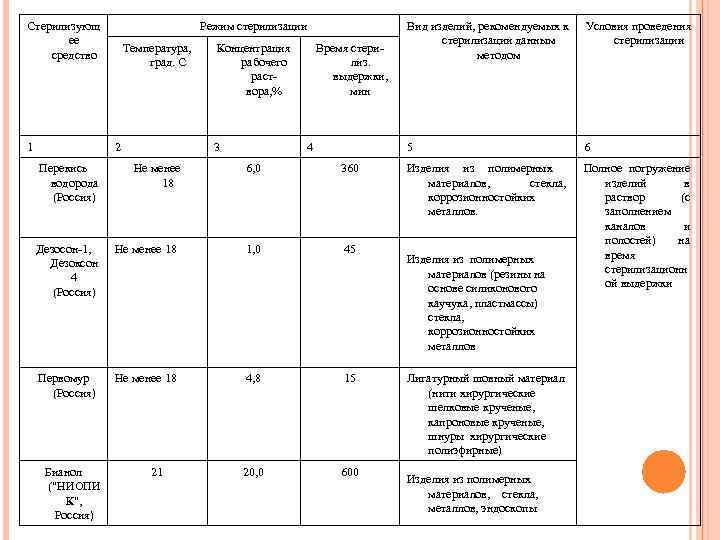 Стерилизующ ее средство 1 Режим стерилизации Температура, град. С 2 Перекись водорода (Россия) Концентрация рабочего раствора, % 3 Не менее 18 4 6, 0 360 Дезосон-1, Дезоксон 4 (Россия) Не менее 18 1, 0 45 Первомур (Россия) Не менее 18 4, 8 15 20, 0 600 Бианол ("НИОПИ К", Россия) 21 Условия проведения стерилизации 5 Время стерилиз. выдержки, мин Вид изделий, рекомендуемых к стерилизации данным методом 6 Изделия из полимерных материалов, стекла, коррозионностойких металлов. Полное погружение изделий в раствор (с заполнением каналов и полостей) на время стерилизационн ой выдержки Изделия из полимерных материалов (резины на основе силиконового каучука, пластмассы) стекла, коррозионностойких металлов Лигатурный шовный материал (нити хирургические шелковые крученые, капроновые крученые, шнуры хирургические полиэфирные) Изделия из полимерных материалов, стекла, металлов, эндоскопы
Стерилизующ ее средство 1 Режим стерилизации Температура, град. С 2 Перекись водорода (Россия) Концентрация рабочего раствора, % 3 Не менее 18 4 6, 0 360 Дезосон-1, Дезоксон 4 (Россия) Не менее 18 1, 0 45 Первомур (Россия) Не менее 18 4, 8 15 20, 0 600 Бианол ("НИОПИ К", Россия) 21 Условия проведения стерилизации 5 Время стерилиз. выдержки, мин Вид изделий, рекомендуемых к стерилизации данным методом 6 Изделия из полимерных материалов, стекла, коррозионностойких металлов. Полное погружение изделий в раствор (с заполнением каналов и полостей) на время стерилизационн ой выдержки Изделия из полимерных материалов (резины на основе силиконового каучука, пластмассы) стекла, коррозионностойких металлов Лигатурный шовный материал (нити хирургические шелковые крученые, капроновые крученые, шнуры хирургические полиэфирные) Изделия из полимерных материалов, стекла, металлов, эндоскопы
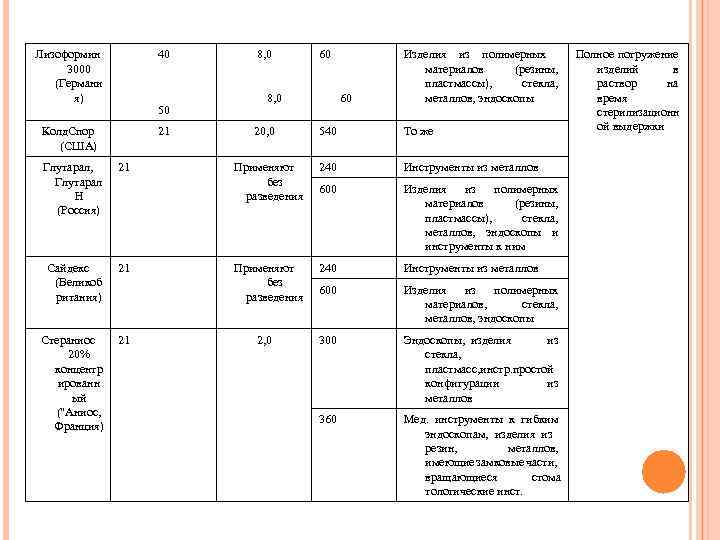 Лизоформин 3000 (Германи я) 40 Колд. Спор (США) 21 50 Глутарал, Глутарал Н (Россия) 21 Сайдекс (Великоб ритания) 21 Стераниос 20% концентр ированн ый ("Аниос, Франция) 21 8, 0 60 8, 0 20, 0 60 Изделия из полимерных материалов (резины, пластмассы), стекла, металлов, эндоскопы 540 То же Применяют без разведения 240 Инструменты из металлов 600 Изделия из полимерных материалов (резины, пластмассы), стекла, металлов, эндоскопы и инструменты к ним Применяют без разведения 240 Инструменты из металлов 600 Изделия из полимерных материалов, стекла, металлов, эндоскопы 300 Эндоскопы, изделия из стекла, пластмасс, инстр. простой конфигурации из металлов 360 Мед. инструменты к гибким эндоскопам, изделия из резин, металлов, имеющие замковые части, вращающиеся стома тологические инст. 2, 0 Полное погружение изделий в раствор на время стерилизационн ой выдержки
Лизоформин 3000 (Германи я) 40 Колд. Спор (США) 21 50 Глутарал, Глутарал Н (Россия) 21 Сайдекс (Великоб ритания) 21 Стераниос 20% концентр ированн ый ("Аниос, Франция) 21 8, 0 60 8, 0 20, 0 60 Изделия из полимерных материалов (резины, пластмассы), стекла, металлов, эндоскопы 540 То же Применяют без разведения 240 Инструменты из металлов 600 Изделия из полимерных материалов (резины, пластмассы), стекла, металлов, эндоскопы и инструменты к ним Применяют без разведения 240 Инструменты из металлов 600 Изделия из полимерных материалов, стекла, металлов, эндоскопы 300 Эндоскопы, изделия из стекла, пластмасс, инстр. простой конфигурации из металлов 360 Мед. инструменты к гибким эндоскопам, изделия из резин, металлов, имеющие замковые части, вращающиеся стома тологические инст. 2, 0 Полное погружение изделий в раствор на время стерилизационн ой выдержки
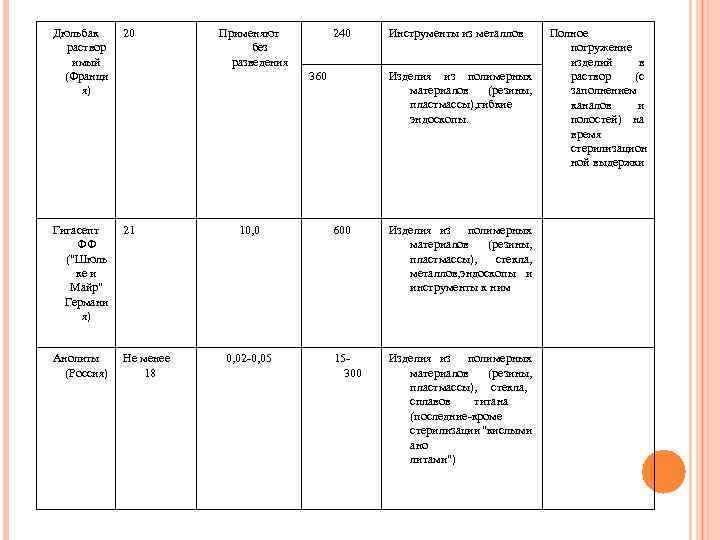 Дюльбак раствор имый (Франци я) 20 Гигасепт ФФ ("Шюль ке и Майр" Германи я) 21 Анолиты (Россия) Не менее 18 Применяют без разведения 240 360 10, 02 -0, 05 Инструменты из металлов Изделия из полимерных материалов (резины, пластмассы), гибкие эндоскопы. 600 Изделия из полимерных материалов (резины, пластмассы), стекла, металлов, эндоскопы и инструменты к ним 15300 Изделия из полимерных материалов (резины, пластмассы), стекла, сплавов титана (последние-кроме стерилизации "кислыми ано литами") Полное погружение изделий в раствор (с заполнением каналов и полостей) на время стерилизацион ной выдержки
Дюльбак раствор имый (Франци я) 20 Гигасепт ФФ ("Шюль ке и Майр" Германи я) 21 Анолиты (Россия) Не менее 18 Применяют без разведения 240 360 10, 02 -0, 05 Инструменты из металлов Изделия из полимерных материалов (резины, пластмассы), гибкие эндоскопы. 600 Изделия из полимерных материалов (резины, пластмассы), стекла, металлов, эндоскопы и инструменты к ним 15300 Изделия из полимерных материалов (резины, пластмассы), стекла, сплавов титана (последние-кроме стерилизации "кислыми ано литами") Полное погружение изделий в раствор (с заполнением каналов и полостей) на время стерилизацион ной выдержки
 СТЕРИЛИЗАЦИЯ ГАЗОВЫМ МЕТОДОМ 1. Используют смесь ОБ (смесь окиси этилена и бромистого метила в весовом соотношении 1: 2, 5), окись этилена, пары раствора формальдегида в этиловом спирте, а также озон. 2. Стерилизацию смесью ОБ и окисью этилена проводят при комнатной температуре (не менее 18°С), при температуре 35°С и 55°С, парами раствора формальдегида в этиловом спирте при температуре 80°С. Стерилизацию газовым методом осуществляют в стационарных газовых стерилизаторах, разрешенных к применению в уста-новленном порядке, а также в портативных аппаратах (микроанаэростаты объемом 2, 0 куб. дм и 2, 7 куб. дм). Для поддержания температуры стерилизации (35, 55°С) в портативных аппаратах их помещают в термостат или водяную баню. 3. 4. Перед газовой стерилизацией изделия вытирают чистой салфеткой либо подсушивают при комнатной температуре или температуре 35°С до исчезновения видимой влаги. Удаление влаги из каналов полимерных (резиновые, пластмассовые) катетеров, трубок проводят с использованием централизованного вакуума, при его отсутствии - с помощью водоструйного насоса, подсоединенного к водопроводному крану.
СТЕРИЛИЗАЦИЯ ГАЗОВЫМ МЕТОДОМ 1. Используют смесь ОБ (смесь окиси этилена и бромистого метила в весовом соотношении 1: 2, 5), окись этилена, пары раствора формальдегида в этиловом спирте, а также озон. 2. Стерилизацию смесью ОБ и окисью этилена проводят при комнатной температуре (не менее 18°С), при температуре 35°С и 55°С, парами раствора формальдегида в этиловом спирте при температуре 80°С. Стерилизацию газовым методом осуществляют в стационарных газовых стерилизаторах, разрешенных к применению в уста-новленном порядке, а также в портативных аппаратах (микроанаэростаты объемом 2, 0 куб. дм и 2, 7 куб. дм). Для поддержания температуры стерилизации (35, 55°С) в портативных аппаратах их помещают в термостат или водяную баню. 3. 4. Перед газовой стерилизацией изделия вытирают чистой салфеткой либо подсушивают при комнатной температуре или температуре 35°С до исчезновения видимой влаги. Удаление влаги из каналов полимерных (резиновые, пластмассовые) катетеров, трубок проводят с использованием централизованного вакуума, при его отсутствии - с помощью водоструйного насоса, подсоединенного к водопроводному крану.
 5. 6. 7. Изделия после подсушивания упаковывают в разобранном виде в пакеты из рекомендованных упаковочных материалов, затем помещают их в стационарный или в портативный аппараты и закрывают крышкой, которую прижимают зажимом. При стерилизации смесью ОБ и окисью этилена из портативного аппарата удаляют воздух до давления 0, 9 кгс/кв. Дозирование газов осуществляют по парциальному давлению непосредственно из баллона через штуцер микроанаэростата. При использовании портативного аппарата после окончания стерилизационной выдержки его открывают в вытяжном шкафу и выдерживают 5 часов.
5. 6. 7. Изделия после подсушивания упаковывают в разобранном виде в пакеты из рекомендованных упаковочных материалов, затем помещают их в стационарный или в портативный аппараты и закрывают крышкой, которую прижимают зажимом. При стерилизации смесью ОБ и окисью этилена из портативного аппарата удаляют воздух до давления 0, 9 кгс/кв. Дозирование газов осуществляют по парциальному давлению непосредственно из баллона через штуцер микроанаэростата. При использовании портативного аппарата после окончания стерилизационной выдержки его открывают в вытяжном шкафу и выдерживают 5 часов.
 8. 9. Озоном, вырабатываемым в "Стерилизаторе озоновом СО-01 -С. -Пб. ", стерилизуют инструменты простой конфигурации из коррозионностойких сталей и сплавов, применяемые в хирургии и стоматологии (скальпели, пинцеты, зеркала цельнометаллические, гладилки, зонды, шпатели, боры стоматологические твердосплавные). После стерилизации инструменты используют по назначению сразу (без дополнительного проветривания). При контакте с ним могут повреждаться изделия из стали, меди, резины и др. Кроме того, озон токсичен, а имеющиеся сегодня аппараты не позволяют обезопасить персонал от контакта с ним. Для контролирования процесса существуют только индикаторы первого класса.
8. 9. Озоном, вырабатываемым в "Стерилизаторе озоновом СО-01 -С. -Пб. ", стерилизуют инструменты простой конфигурации из коррозионностойких сталей и сплавов, применяемые в хирургии и стоматологии (скальпели, пинцеты, зеркала цельнометаллические, гладилки, зонды, шпатели, боры стоматологические твердосплавные). После стерилизации инструменты используют по назначению сразу (без дополнительного проветривания). При контакте с ним могут повреждаться изделия из стали, меди, резины и др. Кроме того, озон токсичен, а имеющиеся сегодня аппараты не позволяют обезопасить персонал от контакта с ним. Для контролирования процесса существуют только индикаторы первого класса.
 10. 11. Стерилизация термолабильных изделий формальдегидом стоит на втором месте после этиленоксида. Оптимальный диапазон температуры при формальдегидной стерилизации должен быть 60 800 С, давление - от 0, 25 до 0, 475 бар, при концентрации формальдегида от 8 до 15 мг/л. Реально формальдегид используется в концентрации около 30 мг/л, экспозиция до 60 минут; при этом общая продолжительность цикла составляет 3, 5 часа (с учетом дегазации простерилизованных изделий (аэрации)). Не все изделия, стерилизуемые этиленоксидом, можно стерилизовать формальдегидом. Рекомендованное исключение составляют оптические инструменты, имплантируемые изделия, эндоскопическая аппаратура.
10. 11. Стерилизация термолабильных изделий формальдегидом стоит на втором месте после этиленоксида. Оптимальный диапазон температуры при формальдегидной стерилизации должен быть 60 800 С, давление - от 0, 25 до 0, 475 бар, при концентрации формальдегида от 8 до 15 мг/л. Реально формальдегид используется в концентрации около 30 мг/л, экспозиция до 60 минут; при этом общая продолжительность цикла составляет 3, 5 часа (с учетом дегазации простерилизованных изделий (аэрации)). Не все изделия, стерилизуемые этиленоксидом, можно стерилизовать формальдегидом. Рекомендованное исключение составляют оптические инструменты, имплантируемые изделия, эндоскопическая аппаратура.
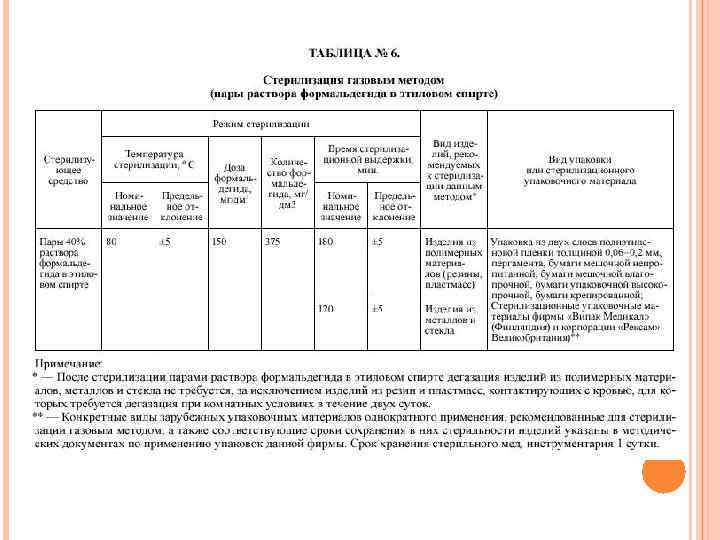
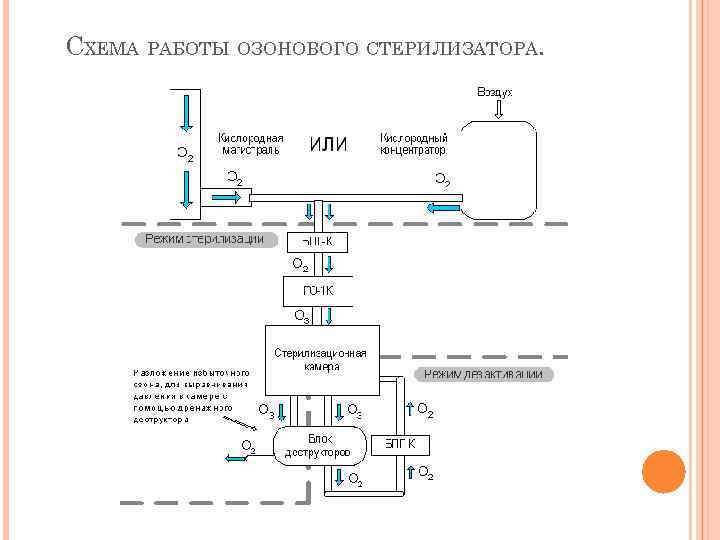 СХЕМА РАБОТЫ ОЗОНОВОГО СТЕРИЛИЗАТОРА.
СХЕМА РАБОТЫ ОЗОНОВОГО СТЕРИЛИЗАТОРА.

 ПЛАЗМЕННАЯ СТЕРИЛИЗАЦИЯ Стерилизующий агент - пары перекиси водорода в сочетании с низкотемпературной плазмой, представляющей собой продукты распада пероксида водорода (гидроксильные группы ОН, ООН), образующиеся под воздействием электромагнитного излучения с выделением видимого и ультрафиолетового излучения. Пероксид водорода и плазма не обладают такими проникающими способностями, как этиленоксид, но распадается на нетоксичные продукты - воду и кислород. Стерилизация проводится при температуре 46 - 500 С за 54 - 72 минуты. Метод позволяет за короткое время (в пределах 70 -80 мин) простерилизовать в упакованном виде сложные медицинские изделия (определенные типы гибких эндоскопов, изделия с электропроводными шнурами, волоконные световодные кабели), к которым в ряде случаев не удается применить ни один из известных методов стерилизации. Высокая стоимость оборудования и расходных материалов сужает спектр применения данного метода стерилизации. Кроме того, стерилизация полых многоканальных изделий требует применения дополнительных расходных приспособлений, еще более увеличивающих стоимость цикла стерилизации. В настоящее время в России наиболее известна система плазменной стерилизации Стеррад, производимая фирмой ASP (США), включающая три установки разного объема: 50, 100 и 200 литров. Более 95% медицинских изделий могут подвергаться стерилизации в этих установках. Не подлежат стерилизации плазмой изделия из полиамида, некоторые сульфиды, хирургическое белье, перевязочный материал, изделия из целлюлозы, порошки, жидкости.
ПЛАЗМЕННАЯ СТЕРИЛИЗАЦИЯ Стерилизующий агент - пары перекиси водорода в сочетании с низкотемпературной плазмой, представляющей собой продукты распада пероксида водорода (гидроксильные группы ОН, ООН), образующиеся под воздействием электромагнитного излучения с выделением видимого и ультрафиолетового излучения. Пероксид водорода и плазма не обладают такими проникающими способностями, как этиленоксид, но распадается на нетоксичные продукты - воду и кислород. Стерилизация проводится при температуре 46 - 500 С за 54 - 72 минуты. Метод позволяет за короткое время (в пределах 70 -80 мин) простерилизовать в упакованном виде сложные медицинские изделия (определенные типы гибких эндоскопов, изделия с электропроводными шнурами, волоконные световодные кабели), к которым в ряде случаев не удается применить ни один из известных методов стерилизации. Высокая стоимость оборудования и расходных материалов сужает спектр применения данного метода стерилизации. Кроме того, стерилизация полых многоканальных изделий требует применения дополнительных расходных приспособлений, еще более увеличивающих стоимость цикла стерилизации. В настоящее время в России наиболее известна система плазменной стерилизации Стеррад, производимая фирмой ASP (США), включающая три установки разного объема: 50, 100 и 200 литров. Более 95% медицинских изделий могут подвергаться стерилизации в этих установках. Не подлежат стерилизации плазмой изделия из полиамида, некоторые сульфиды, хирургическое белье, перевязочный материал, изделия из целлюлозы, порошки, жидкости.
 РАДИАЦИОННАЯ СТЕРИЛИЗАЦИЯ Стерилизующим агент - проникающее гамма- или бета-излучение. Наиболее широко используется гамма-излучающий изотоп кобальта 60, реже изотоп цезия-137. Бета-излучающие изотопы используются крайне редко, так как бета-излучение обладает гораздо меньшей проникающей способностью. Эффективность метода зависит от общей дозы излучения и не зависит от времени. Средняя летальная доза для микроорганизмов всегда одинакова, проводится ли облучение при низкой интенсивности в течение длительного промежутка времени или недолго при высокой интенсивности излучения. Доза 25 к. Гр (2, 5 Мрад) гарантирует уничтожение высокорезистентных споровых форм микроорганизмов. Радиационная стерилизация обладает рядом технологических преимуществ: высокая степень инактивации микроорганизмов, возможность стерилизации больших партий материалов, автоматизация процесса, возможность стерилизации материалов в любой герметичной упаковке (кроме радионепрозрачной). Температура стерилизуемых изделий в ходе стерилизации не повышается. Радиационный метод используется для промышленной стерилизации одноразовых изделий из полимерных материалов, режущих инструментов, шовного и перевязочного материала, некоторых лекарственных препаратов. В лечебно-профилактических учреждениях радиационная стерилизация не применяется в связи с большой дороговизной установок и по соображениям безопасности
РАДИАЦИОННАЯ СТЕРИЛИЗАЦИЯ Стерилизующим агент - проникающее гамма- или бета-излучение. Наиболее широко используется гамма-излучающий изотоп кобальта 60, реже изотоп цезия-137. Бета-излучающие изотопы используются крайне редко, так как бета-излучение обладает гораздо меньшей проникающей способностью. Эффективность метода зависит от общей дозы излучения и не зависит от времени. Средняя летальная доза для микроорганизмов всегда одинакова, проводится ли облучение при низкой интенсивности в течение длительного промежутка времени или недолго при высокой интенсивности излучения. Доза 25 к. Гр (2, 5 Мрад) гарантирует уничтожение высокорезистентных споровых форм микроорганизмов. Радиационная стерилизация обладает рядом технологических преимуществ: высокая степень инактивации микроорганизмов, возможность стерилизации больших партий материалов, автоматизация процесса, возможность стерилизации материалов в любой герметичной упаковке (кроме радионепрозрачной). Температура стерилизуемых изделий в ходе стерилизации не повышается. Радиационный метод используется для промышленной стерилизации одноразовых изделий из полимерных материалов, режущих инструментов, шовного и перевязочного материала, некоторых лекарственных препаратов. В лечебно-профилактических учреждениях радиационная стерилизация не применяется в связи с большой дороговизной установок и по соображениям безопасности
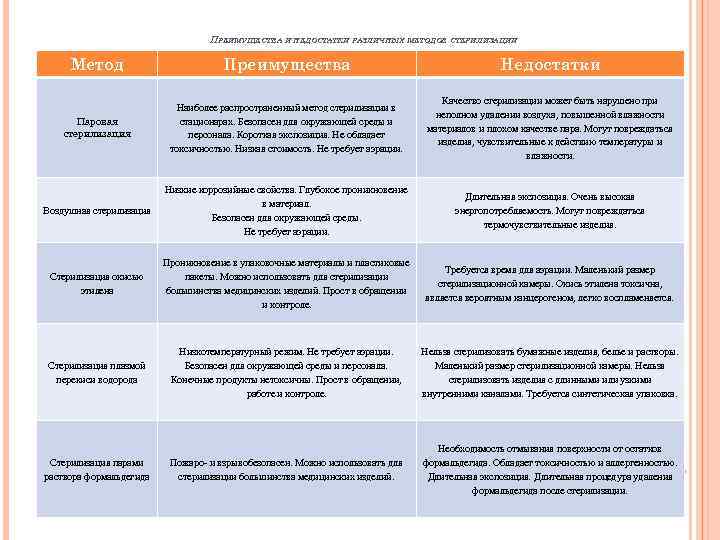 ПРЕИМУЩЕСТВА И НЕДОСТАТКИ РАЗЛИЧНЫХ МЕТОДОВ СТЕРИЛИЗАЦИИ Метод Преимущества Недостатки Паровая стерилизация Наиболее распространенный метод стерилизации в стационарах. Безопасен для окружающей среды и персонала. Короткая экспозиция. Не обладает токсичностью. Низкая стоимость. Не требует аэрации. Качество стерилизации может быть нарушено при неполном удалении воздуха, повышенной влажности материалов и плохом качестве пара. Могут повреждаться изделия, чувствительные к действию температуры и влажности. Воздушная стерилизация Низкие коррозийные свойства. Глубокое проникновение в материал. Безопасен для окружающей среды. Не требует аэрации. Длительная экспозиция. Очень высокая энергопотребляемость. Могут повреждаться термочувствительные изделия. Стерилизация окисью этилена Проникновение в упаковочные материалы и пластиковые пакеты. Можно использовать для стерилизации большинства медицинских изделий. Прост в обращении и контроле. Требуется время для аэрации. Маленький размер стерилизационной камеры. Окись этилена токсична, является вероятным канцерогеном, легко воспламеняется. Стерилизация плазмой перекиси водорода Низкотемпературный режим. Не требует аэрации. Безопасен для окружающей среды и персонала. Конечные продукты нетоксичны. Прост в обращении, работе и контроле. Нельзя стерилизовать бумажные изделия, белье и растворы. Маленький размер стерилизационной камеры. Нельзя стерилизовать изделия с длинными или узкими внутренними каналами. Требуется синтетическая упаковка. Стерилизация парами раствора формальдегида Пожаро- и взрывобезопасен. Можно использовать для стерилизации большинства медицинских изделий. Необходимость отмывания поверхности от остатков формальдегида. Обладает токсичностью и аллергенностью. Длительная экспозиция. Длительная процедура удаления формальдегида после стерилизации.
ПРЕИМУЩЕСТВА И НЕДОСТАТКИ РАЗЛИЧНЫХ МЕТОДОВ СТЕРИЛИЗАЦИИ Метод Преимущества Недостатки Паровая стерилизация Наиболее распространенный метод стерилизации в стационарах. Безопасен для окружающей среды и персонала. Короткая экспозиция. Не обладает токсичностью. Низкая стоимость. Не требует аэрации. Качество стерилизации может быть нарушено при неполном удалении воздуха, повышенной влажности материалов и плохом качестве пара. Могут повреждаться изделия, чувствительные к действию температуры и влажности. Воздушная стерилизация Низкие коррозийные свойства. Глубокое проникновение в материал. Безопасен для окружающей среды. Не требует аэрации. Длительная экспозиция. Очень высокая энергопотребляемость. Могут повреждаться термочувствительные изделия. Стерилизация окисью этилена Проникновение в упаковочные материалы и пластиковые пакеты. Можно использовать для стерилизации большинства медицинских изделий. Прост в обращении и контроле. Требуется время для аэрации. Маленький размер стерилизационной камеры. Окись этилена токсична, является вероятным канцерогеном, легко воспламеняется. Стерилизация плазмой перекиси водорода Низкотемпературный режим. Не требует аэрации. Безопасен для окружающей среды и персонала. Конечные продукты нетоксичны. Прост в обращении, работе и контроле. Нельзя стерилизовать бумажные изделия, белье и растворы. Маленький размер стерилизационной камеры. Нельзя стерилизовать изделия с длинными или узкими внутренними каналами. Требуется синтетическая упаковка. Стерилизация парами раствора формальдегида Пожаро- и взрывобезопасен. Можно использовать для стерилизации большинства медицинских изделий. Необходимость отмывания поверхности от остатков формальдегида. Обладает токсичностью и аллергенностью. Длительная экспозиция. Длительная процедура удаления формальдегида после стерилизации.
 СТЕРИЛИЗАЦИЯ АППАРАТОВ ЭКСТРАКОРПОРАЛЬНОГО (ИСКУССТВЕННОГО) КРОВООБРАЩЕНИЯ. 1. 2. 3. Аппараты искусственного кровообращения стерилизуют в разобранном и в собранном виде. Отдельные блоки и детали аппарата (оксигенераторы, резервуар для донорской крови, резервный сосуд, артериальные канюли, венозные катетеры, тройник, ловушки, трубки из полимерных мате-риалов и т. д. ) стерилизуют паровым методом при температуре 120 -122°С. Трубки из полимерных материалов при стерилизации приобретают молочный цвет, исчезающий после подсушивания в сушильном шкафу при температуре 60 -80°С в течение 10 часов. Стерилизацию аппаратов экстракорпорального кровообращения в собранном виде проводят газо-вым методом окисью.
СТЕРИЛИЗАЦИЯ АППАРАТОВ ЭКСТРАКОРПОРАЛЬНОГО (ИСКУССТВЕННОГО) КРОВООБРАЩЕНИЯ. 1. 2. 3. Аппараты искусственного кровообращения стерилизуют в разобранном и в собранном виде. Отдельные блоки и детали аппарата (оксигенераторы, резервуар для донорской крови, резервный сосуд, артериальные канюли, венозные катетеры, тройник, ловушки, трубки из полимерных мате-риалов и т. д. ) стерилизуют паровым методом при температуре 120 -122°С. Трубки из полимерных материалов при стерилизации приобретают молочный цвет, исчезающий после подсушивания в сушильном шкафу при температуре 60 -80°С в течение 10 часов. Стерилизацию аппаратов экстракорпорального кровообращения в собранном виде проводят газо-вым методом окисью.
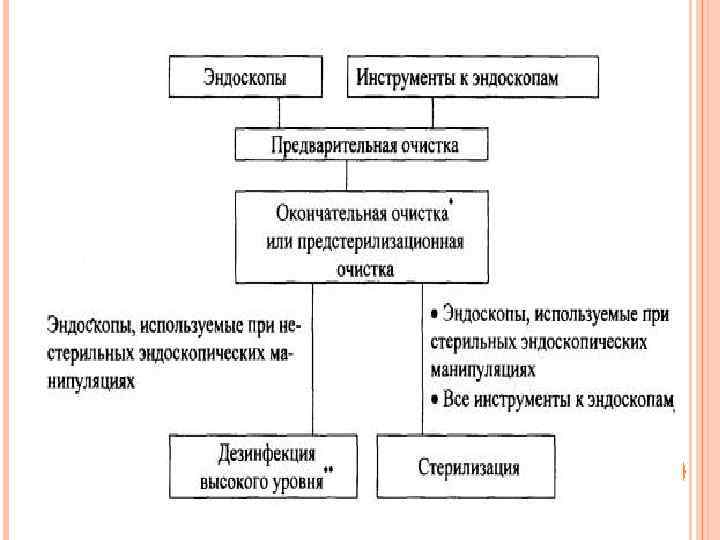
 ОЧИСТКА, ДЕЗИНФЕКЦИЯ И СТЕРИЛИЗАЦИЯ ЭНДОСКОПОВ И ИНСТРУМЕНТОВ К НИМ 1. ОБЩИЕ ПОЛОЖЕНИЯ 1. Эндоскопы и инструменты к ним предназначены для визуализации органов и тканей, а также для проведения диагностических и лечебных манипуляций у пациентов, в процессе чего эти изделия контактируют со слизистыми оболочками и/или проникают в стерильные ткани и полости организма. 2. Применяемые в настоящее время в лечебно-профилактических учреждениях (ЛПУ) эндоскопы и большее число инструментов к ним относятся к изделиям многократного применения и между эндоскопическими манипуляциями у пациентов подлежат обработке. 3. Варианты обработки эндоскопов Эндоскопы подвергают обработке по одному из двух вариантов, отличающихся завершающей стадией: либо дезинфекцией высокого уровня (далее - ДВУ), либо стерилизацией. Соответствующий вариант обработки выбирают в зависимости от типа проводимой эндоскопической манипуляции (нестерильная или стерильная). Перед нестерильной эндоскопической манипуляцией, эндоскоп на завершающей стадии обработки подлежит ДВУ с целью уничтожения патогенных и условнопатогенных микроорганизмов, в т. ч. вегетативных форм всех бактерий (включая микобактерии туберкулеза), вирусов и грибов, а также значительного числа споровых форм бактерий. Процесс обработки состоит из последовательно выполняемых стадий предварительной очистки, окончательной очистки и ДВУ.
ОЧИСТКА, ДЕЗИНФЕКЦИЯ И СТЕРИЛИЗАЦИЯ ЭНДОСКОПОВ И ИНСТРУМЕНТОВ К НИМ 1. ОБЩИЕ ПОЛОЖЕНИЯ 1. Эндоскопы и инструменты к ним предназначены для визуализации органов и тканей, а также для проведения диагностических и лечебных манипуляций у пациентов, в процессе чего эти изделия контактируют со слизистыми оболочками и/или проникают в стерильные ткани и полости организма. 2. Применяемые в настоящее время в лечебно-профилактических учреждениях (ЛПУ) эндоскопы и большее число инструментов к ним относятся к изделиям многократного применения и между эндоскопическими манипуляциями у пациентов подлежат обработке. 3. Варианты обработки эндоскопов Эндоскопы подвергают обработке по одному из двух вариантов, отличающихся завершающей стадией: либо дезинфекцией высокого уровня (далее - ДВУ), либо стерилизацией. Соответствующий вариант обработки выбирают в зависимости от типа проводимой эндоскопической манипуляции (нестерильная или стерильная). Перед нестерильной эндоскопической манипуляцией, эндоскоп на завершающей стадии обработки подлежит ДВУ с целью уничтожения патогенных и условнопатогенных микроорганизмов, в т. ч. вегетативных форм всех бактерий (включая микобактерии туберкулеза), вирусов и грибов, а также значительного числа споровых форм бактерий. Процесс обработки состоит из последовательно выполняемых стадий предварительной очистки, окончательной очистки и ДВУ.
 - Перед стерильной эндоскопической манипуляцией, эндоскоп на завершающей стадии обработки подлежит стерилизации с целью уничтожения микроорганизмов всех видов, находящихся на всех стадиях развития (включая споровые формы). Процесс обработки состоит из стадий предварительной очистки, предстерилизационной очистки и стерилизации. 4. Процесс обработки инструментов к эндоскопам во всех случаях (независимо от варианта обработки) состоит из последовательно выполняемых стадий предварительной очистки, предстерилизационной очистки и стерилизации. 5. Обработку эндоскопов и инструментов к ним после применения при манипуляциях у инфекционного больного проводят с учетом требований противоэпидемического режима для инфекционных стационаров. При этом изделия после предварительной очистки подлежат дезинфекции, которая может быть совмещена с окончательной (перед ДВУ эндоскопов) или предстерилиза-ционной очисткой. 6. Инструменты к эндоскопам, выпускаемые в стерильном виде с пометкой "только для однократного применения", не должны подвергаться очистке и стерилизации в ЛПУ и использоваться повторно.
- Перед стерильной эндоскопической манипуляцией, эндоскоп на завершающей стадии обработки подлежит стерилизации с целью уничтожения микроорганизмов всех видов, находящихся на всех стадиях развития (включая споровые формы). Процесс обработки состоит из стадий предварительной очистки, предстерилизационной очистки и стерилизации. 4. Процесс обработки инструментов к эндоскопам во всех случаях (независимо от варианта обработки) состоит из последовательно выполняемых стадий предварительной очистки, предстерилизационной очистки и стерилизации. 5. Обработку эндоскопов и инструментов к ним после применения при манипуляциях у инфекционного больного проводят с учетом требований противоэпидемического режима для инфекционных стационаров. При этом изделия после предварительной очистки подлежат дезинфекции, которая может быть совмещена с окончательной (перед ДВУ эндоскопов) или предстерилиза-ционной очисткой. 6. Инструменты к эндоскопам, выпускаемые в стерильном виде с пометкой "только для однократного применения", не должны подвергаться очистке и стерилизации в ЛПУ и использоваться повторно.
 2. ПРЕДВАРИТЕЛЬНАЯ ОЧИСТКА 1. 2. 3. альный Для предварительной очистки эндоскопов и инструментов к ним следует использовать растворы средств, разрешенных для предстерилизационной очистки этих изделий. Предварительную очистку эндоскопов и инструментов к ним проводят ручным способом сразу же после окончания эндоскопической манипуляции, не допуская подсыхания загрязнений на/в изделиях. Рабочую (вводимую в тело пациента) часть эндоскопа протирают одноразовой марлевой (тканевой) салфеткой, увлажненной моющим раствором, удаляя видимые загрязнения по направлению к дистальному концу. водой и промывают каналы согласно инструкции по обработке, предоставляемой производителем эндоскопа. После завершения предварительной очистки эндоскоп отключают от источника света и эндоскопического отсоса. Клапаны и заглушки снимают с эндоскопа и погружают их в моющий раствор, обеспечивая контакт всех поверхностей с раствором. Жесткие эндоскопы перед очисткой разбирают на комплектующие детали.
2. ПРЕДВАРИТЕЛЬНАЯ ОЧИСТКА 1. 2. 3. альный Для предварительной очистки эндоскопов и инструментов к ним следует использовать растворы средств, разрешенных для предстерилизационной очистки этих изделий. Предварительную очистку эндоскопов и инструментов к ним проводят ручным способом сразу же после окончания эндоскопической манипуляции, не допуская подсыхания загрязнений на/в изделиях. Рабочую (вводимую в тело пациента) часть эндоскопа протирают одноразовой марлевой (тканевой) салфеткой, увлажненной моющим раствором, удаляя видимые загрязнения по направлению к дистальному концу. водой и промывают каналы согласно инструкции по обработке, предоставляемой производителем эндоскопа. После завершения предварительной очистки эндоскоп отключают от источника света и эндоскопического отсоса. Клапаны и заглушки снимают с эндоскопа и погружают их в моющий раствор, обеспечивая контакт всех поверхностей с раствором. Жесткие эндоскопы перед очисткой разбирают на комплектующие детали.
 3. ДЕЗИНФЕКЦИЯ ЭНДОСКОПОВ И ИНСТРУМЕНТОВ К НИМ 1. 2. 3. 4. Эндоскоп и инструменты к ним, использованные при манипуляциях у инфекционного больного, после предварительной очистки подвергают дезинфеции. Дезинфекцию эндоскопов и инструментов к ним проводят в "грязной зоне" специально отведенного помещения для обработки (моечно-дезинфекционная эндоскопической аппаратуры). Дезинфекцию осуществляют химическим методом ручным или механизированным способом с использованием разрешенных для этих целей. Дезинфекцию изделий растворами химических средств ручным способом проводят в эмалированных (без повреждения эмали) или пластмассовых емкостях, закрывающихся крышками.
3. ДЕЗИНФЕКЦИЯ ЭНДОСКОПОВ И ИНСТРУМЕНТОВ К НИМ 1. 2. 3. 4. Эндоскоп и инструменты к ним, использованные при манипуляциях у инфекционного больного, после предварительной очистки подвергают дезинфеции. Дезинфекцию эндоскопов и инструментов к ним проводят в "грязной зоне" специально отведенного помещения для обработки (моечно-дезинфекционная эндоскопической аппаратуры). Дезинфекцию осуществляют химическим методом ручным или механизированным способом с использованием разрешенных для этих целей. Дезинфекцию изделий растворами химических средств ручным способом проводят в эмалированных (без повреждения эмали) или пластмассовых емкостях, закрывающихся крышками.
 4. ПРЕДСТЕРИЛИЗАЦИОННАЯ/ОКОНЧАТЕЛЬ НАЯ ОЧИСТКА Наименование этапа Особенности осуществления этапа Замачивание в растворе средства Полное погружение в раствор с тщательным заполнением полостей и каналов Мойка в той же порции раствора средства Манипуляции проводят под поверхностью растворов в емкости. Гибкие эндоскопы: - инструментальный канал очищают щеткой для очистки инструментального канала; - все внутренние каналы поочередно промывают раствором через адаптер для заполнения каналов с помощью шприца; - наружную поверхность моют с помощью марлевой (тканевой) салфетки. Жесткие эндоскопы: поверхности каждой детали моют с помощью ерша или марлевой (тканевой) салфетки; - каналы промывают с помощью шприца. Инструменты к эндоскопам: - наружные(внешние) поверхности, в т. ч. замковые части, моют с помощью маленькой щеточки или марлевой (тканевой) салфетки; - внутренние открытые каналы моют с помощью шприца Ополаскивание проточной питьевой водой Ополаскивание проводят при полном погружении эндоскопов (у частично погруженных эндоскопов окунают рабочую часть и детали, разрешенные к погружению) и инструментов к ним в воду. Каналы промывают через адаптер для заполнения каналов с помощью шприца Ополаскивание дистиллированной водой Ополаскивание проводят при полном погружении эндоскопов (у частично погруженных эндоскопов окунают рабочую часть и детали, разрешенные к погружению) и инструментов к ним в воду. Каналы промывают через адаптер для заполнения каналов с помощью шприца
4. ПРЕДСТЕРИЛИЗАЦИОННАЯ/ОКОНЧАТЕЛЬ НАЯ ОЧИСТКА Наименование этапа Особенности осуществления этапа Замачивание в растворе средства Полное погружение в раствор с тщательным заполнением полостей и каналов Мойка в той же порции раствора средства Манипуляции проводят под поверхностью растворов в емкости. Гибкие эндоскопы: - инструментальный канал очищают щеткой для очистки инструментального канала; - все внутренние каналы поочередно промывают раствором через адаптер для заполнения каналов с помощью шприца; - наружную поверхность моют с помощью марлевой (тканевой) салфетки. Жесткие эндоскопы: поверхности каждой детали моют с помощью ерша или марлевой (тканевой) салфетки; - каналы промывают с помощью шприца. Инструменты к эндоскопам: - наружные(внешние) поверхности, в т. ч. замковые части, моют с помощью маленькой щеточки или марлевой (тканевой) салфетки; - внутренние открытые каналы моют с помощью шприца Ополаскивание проточной питьевой водой Ополаскивание проводят при полном погружении эндоскопов (у частично погруженных эндоскопов окунают рабочую часть и детали, разрешенные к погружению) и инструментов к ним в воду. Каналы промывают через адаптер для заполнения каналов с помощью шприца Ополаскивание дистиллированной водой Ополаскивание проводят при полном погружении эндоскопов (у частично погруженных эндоскопов окунают рабочую часть и детали, разрешенные к погружению) и инструментов к ним в воду. Каналы промывают через адаптер для заполнения каналов с помощью шприца
 5. СТЕРИЛИЗАЦИЯ Стерилизацию проводят в "чистой зоне" помещения для обработки. 2. Для стерилизации эндоскопов и инструментов к ним в ЛПУ используют разрешенные в установленном порядке химические (газовый, плазменный и использование химических средств в виде растворов) и физические (паровой) методы исходя из их приемлемости с точки зрения влияния на материалы изделий с учетом рекомендаций производителей этих изделий. Преимущество следует отдавать методам, которые позволяют стерилизовать эндоскопы и инструменты к ним в упакованном виде. Сроки хранения эндоскопов и инструментов к ним в упаковках, в которых проводили стерилизацию, не должны превышать допустимые сроки, указанные для конкретных упаковочных материалов определенного производителя. 3. Стерилизацию эндоскопов и инструментов к ним раствором одного из средств, разрешенных для этой цели, осуществляют ручным или механизированным. 1.
5. СТЕРИЛИЗАЦИЯ Стерилизацию проводят в "чистой зоне" помещения для обработки. 2. Для стерилизации эндоскопов и инструментов к ним в ЛПУ используют разрешенные в установленном порядке химические (газовый, плазменный и использование химических средств в виде растворов) и физические (паровой) методы исходя из их приемлемости с точки зрения влияния на материалы изделий с учетом рекомендаций производителей этих изделий. Преимущество следует отдавать методам, которые позволяют стерилизовать эндоскопы и инструменты к ним в упакованном виде. Сроки хранения эндоскопов и инструментов к ним в упаковках, в которых проводили стерилизацию, не должны превышать допустимые сроки, указанные для конкретных упаковочных материалов определенного производителя. 3. Стерилизацию эндоскопов и инструментов к ним раствором одного из средств, разрешенных для этой цели, осуществляют ручным или механизированным. 1.
 Стерилизацию изделий растворами химических средств ручным способом проводят в стерильных эмалированных (без повреждения эмали) или пластмассовых емкостях, закрывающихся крышками. Эндоскопы и инструменты к ним полностью погружают в раствор (у частично погруженных в раствор эндоскопов окунают рабочую часть, разрешенную к погружению); заполняют все каналы раствором через адаптер с помощью шприца, избегая образования воздушных пробок. Инструмент большой длины к гибким эндоскопам сворачивают кольцом, учитывая рекомендации производителя. Инструменты к эндоскопам, имеющие замковые части, погружают раскрытыми, предварительно сделав ими в растворе несколько рабочих движений для лучшего проникновения смеси в область замка. Толщина слоя раствора над изделиями должна быть не менее 1 см. 4. При проведении стерилизации растворами все манипуляции осуществляют в асептических условиях. После окончания стерилизационной выдержки изделия извлекают из средства и отмывают от его остатков, соблюдая правила асептики: используют стерильные емкости со стерильной питьевой водой и стерильные инструменты (шприцы, корнцанги); работу проводят, надев на руки стерильные перчатки. Емкости, используемые для стерилизации и при отмыве стерильных изделий от остатков средства, предварительно стерилизуют паровым методом. Воду для отмыва стерилизуют паровым методом. 5.
Стерилизацию изделий растворами химических средств ручным способом проводят в стерильных эмалированных (без повреждения эмали) или пластмассовых емкостях, закрывающихся крышками. Эндоскопы и инструменты к ним полностью погружают в раствор (у частично погруженных в раствор эндоскопов окунают рабочую часть, разрешенную к погружению); заполняют все каналы раствором через адаптер с помощью шприца, избегая образования воздушных пробок. Инструмент большой длины к гибким эндоскопам сворачивают кольцом, учитывая рекомендации производителя. Инструменты к эндоскопам, имеющие замковые части, погружают раскрытыми, предварительно сделав ими в растворе несколько рабочих движений для лучшего проникновения смеси в область замка. Толщина слоя раствора над изделиями должна быть не менее 1 см. 4. При проведении стерилизации растворами все манипуляции осуществляют в асептических условиях. После окончания стерилизационной выдержки изделия извлекают из средства и отмывают от его остатков, соблюдая правила асептики: используют стерильные емкости со стерильной питьевой водой и стерильные инструменты (шприцы, корнцанги); работу проводят, надев на руки стерильные перчатки. Емкости, используемые для стерилизации и при отмыве стерильных изделий от остатков средства, предварительно стерилизуют паровым методом. Воду для отмыва стерилизуют паровым методом. 5.
 При отмывании от остатков стерилизующего средства изделия должны быть полностью погружены в стерильную воду при соотношении объема воды к объему, занимаемому изделиями, не менее чем 3: 1. Через каналы изделий с помощью электроотсоса пропускают не менее 20 мл воды в каждой емкости, не допуская попадания пропущенной воды в емкость с отмываемыми изделиями. Отмытые от остатков средства стерильные изделия помещают на стерильную ткань, из их каналов и полостей удаляют воду с помощью стерильного шприца или иного приспособления. Для более полного удаления остатков влаги из каналов эндоскопов может использоваться 70%-ный этиловый спирт путем пропускания 50 мл его через каналы с помощью шприца. Срок хранения изделий, простерилизованных раствором средства, не должен превышать 3 суток. 6.
При отмывании от остатков стерилизующего средства изделия должны быть полностью погружены в стерильную воду при соотношении объема воды к объему, занимаемому изделиями, не менее чем 3: 1. Через каналы изделий с помощью электроотсоса пропускают не менее 20 мл воды в каждой емкости, не допуская попадания пропущенной воды в емкость с отмываемыми изделиями. Отмытые от остатков средства стерильные изделия помещают на стерильную ткань, из их каналов и полостей удаляют воду с помощью стерильного шприца или иного приспособления. Для более полного удаления остатков влаги из каналов эндоскопов может использоваться 70%-ный этиловый спирт путем пропускания 50 мл его через каналы с помощью шприца. Срок хранения изделий, простерилизованных раствором средства, не должен превышать 3 суток. 6.
 УСТАНОВКА ДЕЗИНФЕКЦИОННАЯ ЭНДОСКОПИЧЕСКАЯ.
УСТАНОВКА ДЕЗИНФЕКЦИОННАЯ ЭНДОСКОПИЧЕСКАЯ.

 МЕРЫ ПРЕДОСТОРОЖНОСТИ ПРИ РАБОТЕ С ДЕЗИНФИЦИРУЮЩИМИ, МОЮЩИМИ И СТЕРИЛИЗУЮЩИМИ СРЕДСТВАМИ 1. 2. 3. 4. 5. 6. К работе со средствами не допускаются лица моложе 18 лет, страдающие аллергическими заболеваниями, беременные женщины и кормящие матери. Приготовление рабочих растворов средств, дезинфекцию, предстерилизационную очистку и стерилизацию изделий меди-цинского назначения проводят в специальном помещении с естественной или искусственной (приточновытяжной) вентиляцией. Емкости с рабочими растворами в процессе обработки должны быть плотно закрыты крышками. Все работы со средствами необходимо выполнять с защитой кожи рук резиновыми перчатками. Если в Методических указаниях по применению средства имеются рекомендации по защите органов дыхания респираторами (РУ-60 М или РПГ-67), следует неукоснительно их соблюдать. После окончания работ со средствами помещение необходимо проветрить. Хранить средства следует в отдельном помещении, в прохладном месте, закрытыми в шкафу отдельно от лекарственных препаратов, в местах, недоступных детям.
МЕРЫ ПРЕДОСТОРОЖНОСТИ ПРИ РАБОТЕ С ДЕЗИНФИЦИРУЮЩИМИ, МОЮЩИМИ И СТЕРИЛИЗУЮЩИМИ СРЕДСТВАМИ 1. 2. 3. 4. 5. 6. К работе со средствами не допускаются лица моложе 18 лет, страдающие аллергическими заболеваниями, беременные женщины и кормящие матери. Приготовление рабочих растворов средств, дезинфекцию, предстерилизационную очистку и стерилизацию изделий меди-цинского назначения проводят в специальном помещении с естественной или искусственной (приточновытяжной) вентиляцией. Емкости с рабочими растворами в процессе обработки должны быть плотно закрыты крышками. Все работы со средствами необходимо выполнять с защитой кожи рук резиновыми перчатками. Если в Методических указаниях по применению средства имеются рекомендации по защите органов дыхания респираторами (РУ-60 М или РПГ-67), следует неукоснительно их соблюдать. После окончания работ со средствами помещение необходимо проветрить. Хранить средства следует в отдельном помещении, в прохладном месте, закрытыми в шкафу отдельно от лекарственных препаратов, в местах, недоступных детям.
 МЕТОДЫ КОНТРОЛЯ ЭФФЕКТИВНОСТИ СТЕРИЛИЗАЦИИ Контроль эффективности работы стерилизационного оборудования осуществляется физическими, химическими и биологическим (бактериологическим) методами. Надежность этих методов неодинакова. Физические и химические методы предназначены для оперативного контроля и позволяют контролировать соблюдение параметров режимов паровой, газовой, воздушной стерилизации, температуру, давление, экспозицию. Недостаток этих методов заключается в том, что они не могут служить доказательством эффективной стерилизации. Достоверным для определения эффективности является только бактериологический метод.
МЕТОДЫ КОНТРОЛЯ ЭФФЕКТИВНОСТИ СТЕРИЛИЗАЦИИ Контроль эффективности работы стерилизационного оборудования осуществляется физическими, химическими и биологическим (бактериологическим) методами. Надежность этих методов неодинакова. Физические и химические методы предназначены для оперативного контроля и позволяют контролировать соблюдение параметров режимов паровой, газовой, воздушной стерилизации, температуру, давление, экспозицию. Недостаток этих методов заключается в том, что они не могут служить доказательством эффективной стерилизации. Достоверным для определения эффективности является только бактериологический метод.
 ФИЗИЧЕСКИЕ МЕТОДЫ Физические методы контроля осуществляются с помощью средств измерения температуры (термометры, термопары), давления (манометры, мановакуумметры) и времени (таймеры). Современные стерилизаторы оснащены также записывающими устройствами, фиксирующими отдельные параметры каждого цикла стерилизации.
ФИЗИЧЕСКИЕ МЕТОДЫ Физические методы контроля осуществляются с помощью средств измерения температуры (термометры, термопары), давления (манометры, мановакуумметры) и времени (таймеры). Современные стерилизаторы оснащены также записывающими устройствами, фиксирующими отдельные параметры каждого цикла стерилизации.
 ХИМИЧЕСКИЕ МЕТОДЫ В течение десятков лет для проведения химического контроля применялись химические вещества, изменяющие свое агрегатное состояние или цвет при температуре, близкой к температуре стерилизации (бензойная кислота для контроля паровой стерилизации, сахароза, гидрохинон и ряд других веществ - для контроля воздушной стерилизации). При изменении цвета и расплавлении указанных веществ результат стерилизации признавался удовлетворительным. Однако многолетние наблюдения и данные литературы указывают, что при удовлетворительных результатах химического контроля с помощью названных индикаторов, бактериологический контроль в ряде случаев (до 12%) выявляет неудовлетворительный результат стерилизации.
ХИМИЧЕСКИЕ МЕТОДЫ В течение десятков лет для проведения химического контроля применялись химические вещества, изменяющие свое агрегатное состояние или цвет при температуре, близкой к температуре стерилизации (бензойная кислота для контроля паровой стерилизации, сахароза, гидрохинон и ряд других веществ - для контроля воздушной стерилизации). При изменении цвета и расплавлении указанных веществ результат стерилизации признавался удовлетворительным. Однако многолетние наблюдения и данные литературы указывают, что при удовлетворительных результатах химического контроля с помощью названных индикаторов, бактериологический контроль в ряде случаев (до 12%) выявляет неудовлетворительный результат стерилизации.
 Кроме того, эти вещества имеют существенный недостаток. Переход их в другое агрегатное состояние не дает представления о продолжительности воздействия температуры, при которой происходит их расплавление. Принимая во внимание недостаточную достоверность использования указанных индикаторов для контроля, а также значительную трудоемкость и неудобство их практического применения, в 70 -х годах были разработаны химические индикаторы, изменение цвета которых происходит при воздействии температуры, принятой для данного режима, в течение времени, необходимого для стерилизации. По изменению окраски этих индикаторов можно судить о том, что основные параметры процесса стерилизации температура и время - выдержаны. Длительное применение таких индикаторов показало их высокую надежность.
Кроме того, эти вещества имеют существенный недостаток. Переход их в другое агрегатное состояние не дает представления о продолжительности воздействия температуры, при которой происходит их расплавление. Принимая во внимание недостаточную достоверность использования указанных индикаторов для контроля, а также значительную трудоемкость и неудобство их практического применения, в 70 -х годах были разработаны химические индикаторы, изменение цвета которых происходит при воздействии температуры, принятой для данного режима, в течение времени, необходимого для стерилизации. По изменению окраски этих индикаторов можно судить о том, что основные параметры процесса стерилизации температура и время - выдержаны. Длительное применение таких индикаторов показало их высокую надежность.
 Более сложные индикаторы предназначены для контроля критических параметров процесса стерилизации. Критическими параметрами являются: для парового метода стерилизации температура, время воздействия данной температуры, водяной насыщенный пар; для воздушного метода стерилизации - температура и время воздействия данной температуры; для газовых методов стерилизации - концентрация используемого газа, температура, время воздействия, уровень относительной влажности; для радиационной стерилизации - полная поглощенная доза.
Более сложные индикаторы предназначены для контроля критических параметров процесса стерилизации. Критическими параметрами являются: для парового метода стерилизации температура, время воздействия данной температуры, водяной насыщенный пар; для воздушного метода стерилизации - температура и время воздействия данной температуры; для газовых методов стерилизации - концентрация используемого газа, температура, время воздействия, уровень относительной влажности; для радиационной стерилизации - полная поглощенная доза.
 С ЯНВАРЯ 2002 ГОДА В РОССИИ ВВЕДЕН В ДЕЙСТВИЕ ГОСТ Р ИСО 11140 -1 "СТЕРИЛИЗАЦИЯ МЕДИЦИНСКОЙ ПРОДУКЦИИ. ХИМИЧЕСКИЕ ИНДИКАТОРЫ. ОБЩИЕ ТРЕБОВАНИЯ". СОГЛАСНО ЭТОМУ ДОКУМЕНТУ ХИМИЧЕСКИЕ ИНДИКАТОРЫ РАСПРЕДЕЛЕНЫ НА ШЕСТЬ КЛАССОВ.
С ЯНВАРЯ 2002 ГОДА В РОССИИ ВВЕДЕН В ДЕЙСТВИЕ ГОСТ Р ИСО 11140 -1 "СТЕРИЛИЗАЦИЯ МЕДИЦИНСКОЙ ПРОДУКЦИИ. ХИМИЧЕСКИЕ ИНДИКАТОРЫ. ОБЩИЕ ТРЕБОВАНИЯ". СОГЛАСНО ЭТОМУ ДОКУМЕНТУ ХИМИЧЕСКИЕ ИНДИКАТОРЫ РАСПРЕДЕЛЕНЫ НА ШЕСТЬ КЛАССОВ.
 ИНДИКАТОРЫ 1 -ГО КЛАССА. Являются индикаторами ("свидетелями") процесса. Обычно выпускаются в виде свернутых в рулон клейких лент (наподобие скотча) с нанесенным на их лицевую поверхность химическим индикатором (в виде полосок или надписей). Применяются для удобства отличия изделий, подвергнутых процессу стерилизации, от нестерильных. Кусочки ленты наклеиваются на подготовленные к стерилизации упаковки, контейнеры, свертки. Могут применяться для закрепления краев упаковочных материалов. Должны характеризоваться отчетливым необратимым изменением цвета индикатора, нанесенного на полоски.
ИНДИКАТОРЫ 1 -ГО КЛАССА. Являются индикаторами ("свидетелями") процесса. Обычно выпускаются в виде свернутых в рулон клейких лент (наподобие скотча) с нанесенным на их лицевую поверхность химическим индикатором (в виде полосок или надписей). Применяются для удобства отличия изделий, подвергнутых процессу стерилизации, от нестерильных. Кусочки ленты наклеиваются на подготовленные к стерилизации упаковки, контейнеры, свертки. Могут применяться для закрепления краев упаковочных материалов. Должны характеризоваться отчетливым необратимым изменением цвета индикатора, нанесенного на полоски.
 ИНДИКАТОРЫ 2 -ГО КЛАССА. предназначен для использования в специальных тестовых процедурах Самый характерный представитель этого класса индикаторов - индикатор теста Бовье. Дика (Bowie-Dick). Он предназначен для испытания эффективности вакуумной системы парового стерилизатора. Выполняемый ежедневно, этот тест должен первым сигнализировать о неисправности стерилизатора. Тест не определяет качество стерилизации как таковое, но является неотъемлемой частью всесторонней программы гарантии стерилизации. С помощью теста пользователь определяет, что вакуумная стадия стерилизатора удаляет достаточное количество воздуха до введения пара в камеру, а также проверяется герметичность камеры в течение цикла стерилизации.
ИНДИКАТОРЫ 2 -ГО КЛАССА. предназначен для использования в специальных тестовых процедурах Самый характерный представитель этого класса индикаторов - индикатор теста Бовье. Дика (Bowie-Dick). Он предназначен для испытания эффективности вакуумной системы парового стерилизатора. Выполняемый ежедневно, этот тест должен первым сигнализировать о неисправности стерилизатора. Тест не определяет качество стерилизации как таковое, но является неотъемлемой частью всесторонней программы гарантии стерилизации. С помощью теста пользователь определяет, что вакуумная стадия стерилизатора удаляет достаточное количество воздуха до введения пара в камеру, а также проверяется герметичность камеры в течение цикла стерилизации.
 ИНДИКАТОРЫ 3 -ГО КЛАССА. Являются индикаторами одного параметра. Они оценивают максимальную температуру, но не дают представления о времени ее воздействия. Термохимический индикатор представляет собой стеклянную трубку с химическим веществом, изменяющим свое агрегатное состояние или цвет при температуре, близкой к температуре стерилизации. В современном виде это - полоска бумаги, на которую нанесена термоиндикаторная краска. Определение параметров, достигнутых в процессе стерилизации, основано на изменении цвета термоиндикаторной краски при достижении "температуры перехода", строго определенной для каждой краски.
ИНДИКАТОРЫ 3 -ГО КЛАССА. Являются индикаторами одного параметра. Они оценивают максимальную температуру, но не дают представления о времени ее воздействия. Термохимический индикатор представляет собой стеклянную трубку с химическим веществом, изменяющим свое агрегатное состояние или цвет при температуре, близкой к температуре стерилизации. В современном виде это - полоска бумаги, на которую нанесена термоиндикаторная краска. Определение параметров, достигнутых в процессе стерилизации, основано на изменении цвета термоиндикаторной краски при достижении "температуры перехода", строго определенной для каждой краски.
 ИНДИКАТОРЫ 4 -ГО КЛАССА. это многопараметровые индикаторы. Они содержат красители, изменяющие свой цвет при сочетанном воздействии нескольких параметров стерилизации, чаще всего температуры и времени. Примером таких индикаторов служат термовременные индикаторы для контроля воздушной стерилизации. Они отличаются от предыдущего класса только тем, что индикаторная краска меняет свой цвет только в течении определенного времени воздействия контролируемого фактора. Поэтому чаще всего маркируются двумя цифрами, например: 180 -60 (180 градусов, 60 минут).
ИНДИКАТОРЫ 4 -ГО КЛАССА. это многопараметровые индикаторы. Они содержат красители, изменяющие свой цвет при сочетанном воздействии нескольких параметров стерилизации, чаще всего температуры и времени. Примером таких индикаторов служат термовременные индикаторы для контроля воздушной стерилизации. Они отличаются от предыдущего класса только тем, что индикаторная краска меняет свой цвет только в течении определенного времени воздействия контролируемого фактора. Поэтому чаще всего маркируются двумя цифрами, например: 180 -60 (180 градусов, 60 минут).
 ИНДИКАТОРЫ 5 -ГО КЛАССА. Интегрирующие индикаторы. Эти индикаторы реагируют на все критические параметры метода стерилизации. Характеристика этого класса индикаторов сравнивается с инактивацией высокорезистентных микроорганизмов. Цвет контрольной метки интегратора должен необратимо изменяться в ходе стерилизации только при соответствии всех критических параметров примененного процесса необходимым требованиям. К примеру, при температуре 132 -1350 С цвет метки полностью изменится в течение от 3, 0 до 3, 5 минут при условии воздействия на интегратор насыщенного водяного пара. Аналогично работают интеграторы этиленоксидной стерилизации. Одновременные испытания химических интеграторов и биологических индикаторов показали, что цвет химического индикатора изменяется не раньше, чем пройдет время, необходимое для полного уничтожения контрольных микроорганизмов биологического индикатора. Цветной стандарт для сравнения должен быть напечатан на каждой полоске интегратора.
ИНДИКАТОРЫ 5 -ГО КЛАССА. Интегрирующие индикаторы. Эти индикаторы реагируют на все критические параметры метода стерилизации. Характеристика этого класса индикаторов сравнивается с инактивацией высокорезистентных микроорганизмов. Цвет контрольной метки интегратора должен необратимо изменяться в ходе стерилизации только при соответствии всех критических параметров примененного процесса необходимым требованиям. К примеру, при температуре 132 -1350 С цвет метки полностью изменится в течение от 3, 0 до 3, 5 минут при условии воздействия на интегратор насыщенного водяного пара. Аналогично работают интеграторы этиленоксидной стерилизации. Одновременные испытания химических интеграторов и биологических индикаторов показали, что цвет химического индикатора изменяется не раньше, чем пройдет время, необходимое для полного уничтожения контрольных микроорганизмов биологического индикатора. Цветной стандарт для сравнения должен быть напечатан на каждой полоске интегратора.
 ИНДИКАТОРЫ 6 -ГО КЛАССА. Индикаторы-эмуляторы. Эти индикаторы должны реагировать на все контрольные значения критических параметров метода стерилизации.
ИНДИКАТОРЫ 6 -ГО КЛАССА. Индикаторы-эмуляторы. Эти индикаторы должны реагировать на все контрольные значения критических параметров метода стерилизации.
 БИОЛОГИЧЕСКИЙ МЕТОД Наряду с физическими и химическими применяется бактериологический метод контроля стерилизации. Он предназначается для контроля эффективности стерилизационного оборудования. До недавнего времени для контроля паровой и воздушной стерилизации использовались пробы садовой земли, содержащей микроорганизмы, высокорезистентные к воздействию стерилизующих факторов. Однако устойчивость микроорганизмов в различных пробах неодинакова, что не позволяет стандартизировать результаты контроля. В настоящее время для проведения бактериологического контроля используются биотесты, имеющие дозированное количество спор тесткультуры. Контроль эффективности стерилизации с помощью биотестов рекомендуется проводить 1 раз в 2 недели. В зарубежной практике принято применять биологическое тестирование не реже 1 раза в неделю. В ряде случаев возникает необходимость проведения контроля с помощью биотестов каждой загрузки стерилизатора. Прежде всего, речь идет о стерилизации инструментов, используемых для выполнения сложных оперативных вмешательств, требующих применения высоконадежных стерильных материалов. Каждая загрузка имплантируемых изделий также должна подвергаться бактериологическому контролю. При этом использование простерилизованных материалов задерживается до получения отрицательных результатов контроля. Тех же принципов при определении периодичности контроля рекомендуется придерживаться в отношении газовой стерилизации, являющейся по сравнению с другими методами более сложной.
БИОЛОГИЧЕСКИЙ МЕТОД Наряду с физическими и химическими применяется бактериологический метод контроля стерилизации. Он предназначается для контроля эффективности стерилизационного оборудования. До недавнего времени для контроля паровой и воздушной стерилизации использовались пробы садовой земли, содержащей микроорганизмы, высокорезистентные к воздействию стерилизующих факторов. Однако устойчивость микроорганизмов в различных пробах неодинакова, что не позволяет стандартизировать результаты контроля. В настоящее время для проведения бактериологического контроля используются биотесты, имеющие дозированное количество спор тесткультуры. Контроль эффективности стерилизации с помощью биотестов рекомендуется проводить 1 раз в 2 недели. В зарубежной практике принято применять биологическое тестирование не реже 1 раза в неделю. В ряде случаев возникает необходимость проведения контроля с помощью биотестов каждой загрузки стерилизатора. Прежде всего, речь идет о стерилизации инструментов, используемых для выполнения сложных оперативных вмешательств, требующих применения высоконадежных стерильных материалов. Каждая загрузка имплантируемых изделий также должна подвергаться бактериологическому контролю. При этом использование простерилизованных материалов задерживается до получения отрицательных результатов контроля. Тех же принципов при определении периодичности контроля рекомендуется придерживаться в отношении газовой стерилизации, являющейся по сравнению с другими методами более сложной.
 БИОЛОГИЧЕСКИЕ ИНДИКАТОРЫ. Они представляют собой пластиковый контейнер с крышечкой, содержащий хрупкую ампулу с восстанавливающей средой и бумажную полоску, зараженную спорами контрольных микроорганизмов. Индикатор размещается непосредственно в стерилизационной камере, либо закладывается в контейнеры и упаковки, предназначенные к стерилизации, в процессе их подготовки. Никаких предварительных манипуляций с индикатором производить не требуется - он полностью готов к применению. После окончания стерилизационного цикла индикатор должен быть извлечен и подвергнут инкубации для контроля инактивации содержащихся в нем спор микроорганизмов. После извлечения из камеры стерилизатора надо раздавить находящуюся внутри ампулу и инкубировать при рекомендованной температуре в течение необходимого времени - обычно это 24 часа. Ошибка стерилизации проявляется изменением цвета и/или помутнением среды.
БИОЛОГИЧЕСКИЕ ИНДИКАТОРЫ. Они представляют собой пластиковый контейнер с крышечкой, содержащий хрупкую ампулу с восстанавливающей средой и бумажную полоску, зараженную спорами контрольных микроорганизмов. Индикатор размещается непосредственно в стерилизационной камере, либо закладывается в контейнеры и упаковки, предназначенные к стерилизации, в процессе их подготовки. Никаких предварительных манипуляций с индикатором производить не требуется - он полностью готов к применению. После окончания стерилизационного цикла индикатор должен быть извлечен и подвергнут инкубации для контроля инактивации содержащихся в нем спор микроорганизмов. После извлечения из камеры стерилизатора надо раздавить находящуюся внутри ампулу и инкубировать при рекомендованной температуре в течение необходимого времени - обычно это 24 часа. Ошибка стерилизации проявляется изменением цвета и/или помутнением среды.
 ЗАКЛЮЧЕНИЕ Пути совершенствования процесса стерилизации определяют: разработка оборудования, позволяющего реализовать новые методы стерилизации с более короткими или более щадящими режимами; разработка новых химических средств и оптимальных режимов применения, обеспечивающих эффект стерилизации в приемлемые сроки; увеличение номенклатуры химических средств на основе действующих веществ, пригодных для стерилизации изделий из разнородных материалов; разработка химических индикаторов различных классов, позволяющих осуществлять в стерилизаторах разных типов оперативный внешний и внутренний контроль стерилизации.
ЗАКЛЮЧЕНИЕ Пути совершенствования процесса стерилизации определяют: разработка оборудования, позволяющего реализовать новые методы стерилизации с более короткими или более щадящими режимами; разработка новых химических средств и оптимальных режимов применения, обеспечивающих эффект стерилизации в приемлемые сроки; увеличение номенклатуры химических средств на основе действующих веществ, пригодных для стерилизации изделий из разнородных материалов; разработка химических индикаторов различных классов, позволяющих осуществлять в стерилизаторах разных типов оперативный внешний и внутренний контроль стерилизации.
 СПАСИБО ЗА ВНИМАНИЕ!
СПАСИБО ЗА ВНИМАНИЕ!


