 Методы решения ОВР с участием органических соединений Выполнил: Морозов Максим Алексеевич, ученик 9 класса, МБОУ «Сотниковская СОШ» Руководитель: Дружинин Викторович, учитель химии и биологии МБОУ «Сотниковская СОШ» Место выполнения: Канский район, с. Сотниково, МБОУ «Сотниковская СОШ» Цель работы- познакомиться с методом решения ОВР с участием органических веществ. Задачи: - изучить методы решения ОВР; - оценить пригодность методов для решения ОВР с участием органических веществ; - научиться решать ОВР с участием органических веществ.
Методы решения ОВР с участием органических соединений Выполнил: Морозов Максим Алексеевич, ученик 9 класса, МБОУ «Сотниковская СОШ» Руководитель: Дружинин Викторович, учитель химии и биологии МБОУ «Сотниковская СОШ» Место выполнения: Канский район, с. Сотниково, МБОУ «Сотниковская СОШ» Цель работы- познакомиться с методом решения ОВР с участием органических веществ. Задачи: - изучить методы решения ОВР; - оценить пригодность методов для решения ОВР с участием органических веществ; - научиться решать ОВР с участием органических веществ.
 Химия- важнейшая наука в жизни человека!
Химия- важнейшая наука в жизни человека!
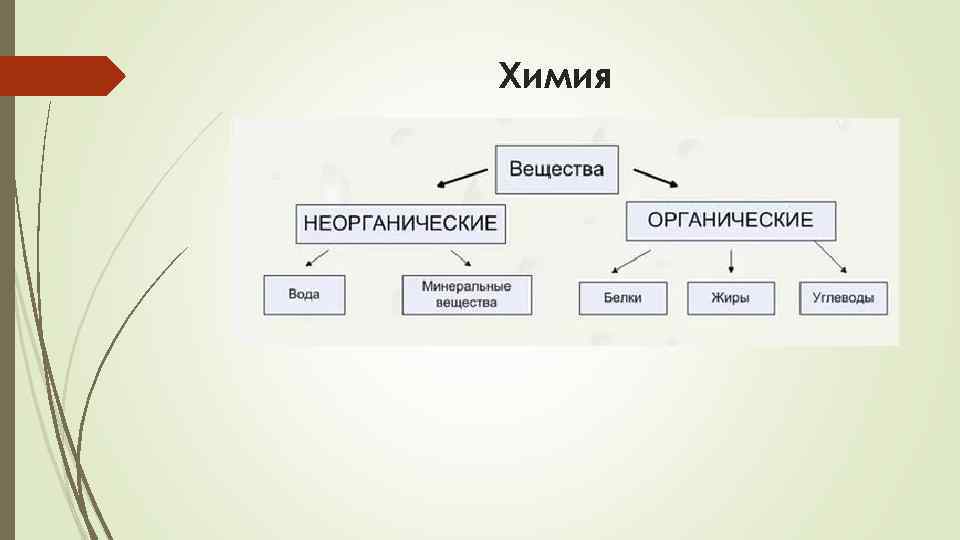 Химия
Химия
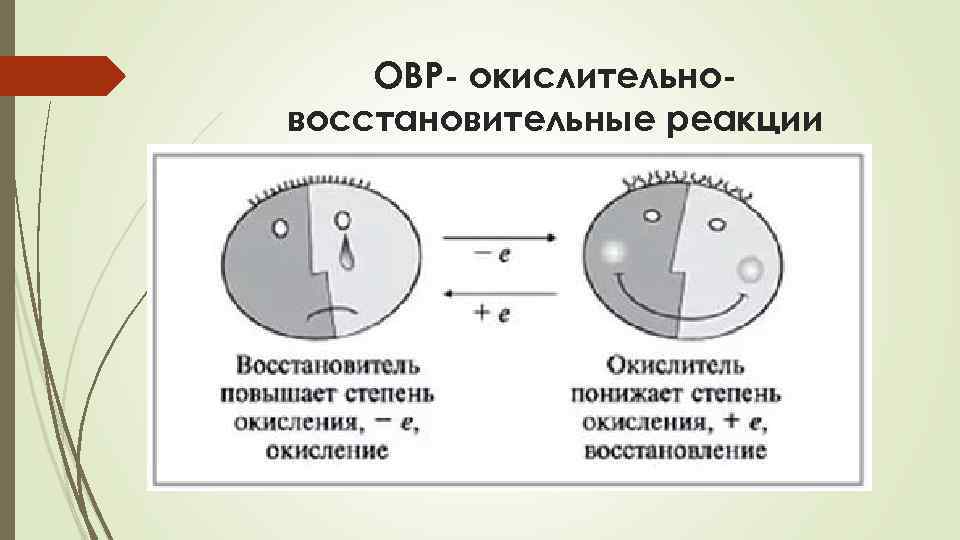 ОВР- окислительновосстановительные реакции
ОВР- окислительновосстановительные реакции
 Цель работы- познакомиться с методом решения ОВР с участием органических веществ. - изучить методы решения ОВР; - оценить пригодность методов для решения ОВР с участием органических веществ; - научиться решать ОВР с участием органических веществ. Гипотеза: органические ОВР решаемы на базовом уровне изучения химии.
Цель работы- познакомиться с методом решения ОВР с участием органических веществ. - изучить методы решения ОВР; - оценить пригодность методов для решения ОВР с участием органических веществ; - научиться решать ОВР с участием органических веществ. Гипотеза: органические ОВР решаемы на базовом уровне изучения химии.
 ОВР
ОВР
 Способы решения ОВР. Метод ионно-электронного баланcа Метод полуреакций Метод подстановки
Способы решения ОВР. Метод ионно-электронного баланcа Метод полуреакций Метод подстановки
 Выводы по работе В ходе работы были рассмотрены методы решения ОВР, проанализированы возможности решения с их помощью реакций с участием органических веществ. Наиболее подходящим способом оказался метод макроподстановки. Метод этот довольно сложный, но позволяет решать ОВР с участием органических соединений с использованием базовых знаний химии и математики.
Выводы по работе В ходе работы были рассмотрены методы решения ОВР, проанализированы возможности решения с их помощью реакций с участием органических веществ. Наиболее подходящим способом оказался метод макроподстановки. Метод этот довольно сложный, но позволяет решать ОВР с участием органических соединений с использованием базовых знаний химии и математики.
 Пример 1 CH 3 -CH 2 -CH=CH 2 + KMn. O 4 + H 2 O = С 2 Н 5 -СООК + Mn. O 2 + KOH+ КНСО 3 С -1 – 4 е =С+3 С -2 – 6 е = С+4 10 Mn+7 + 3 е = Mn+4 10 3 восстановитель Окисление окислитель Восстановление 3 CH 3 -CH 2 -CH=CH 2 + 10 KMn. O 4 + H 2 O = 3 С 2 Н 5 -СООК + 10 Mn. O 2 + KOH+ 3 КНСО 3 3 CH 3 -CH 2 -CH=CH 2 + 10 KMn. O 4 + H 2 O = 3 С 2 Н 5 -СООК + 10 Mn. O 2 + 4 KOH+ 3 КНСО 3 = 3 К 2 СО 3 + КOH + 3 H 2 O 3 СН 3 -СН 2 -СН=СН 2 + 10 KMn. O 4 + Н 2 О = 3 С 2 Н 5 -СООК + 10 Mn. O 2 + 4 KOH + 3 К 2 СО 3 Проверка: 3 СН 3 -СН 2 -СН=СН 2 + 10 KMn. O 4 = 3 С 2 Н 5 -СООК + 10 Mn. O 2 + 4 KOH + 3 К 2 СО 3 + 4 Н 2 О
Пример 1 CH 3 -CH 2 -CH=CH 2 + KMn. O 4 + H 2 O = С 2 Н 5 -СООК + Mn. O 2 + KOH+ КНСО 3 С -1 – 4 е =С+3 С -2 – 6 е = С+4 10 Mn+7 + 3 е = Mn+4 10 3 восстановитель Окисление окислитель Восстановление 3 CH 3 -CH 2 -CH=CH 2 + 10 KMn. O 4 + H 2 O = 3 С 2 Н 5 -СООК + 10 Mn. O 2 + KOH+ 3 КНСО 3 3 CH 3 -CH 2 -CH=CH 2 + 10 KMn. O 4 + H 2 O = 3 С 2 Н 5 -СООК + 10 Mn. O 2 + 4 KOH+ 3 КНСО 3 = 3 К 2 СО 3 + КOH + 3 H 2 O 3 СН 3 -СН 2 -СН=СН 2 + 10 KMn. O 4 + Н 2 О = 3 С 2 Н 5 -СООК + 10 Mn. O 2 + 4 KOH + 3 К 2 СО 3 Проверка: 3 СН 3 -СН 2 -СН=СН 2 + 10 KMn. O 4 = 3 С 2 Н 5 -СООК + 10 Mn. O 2 + 4 KOH + 3 К 2 СО 3 + 4 Н 2 О
 Пример 2 + KMn. O 4 + H 2 SO 4 = + CO 2 + CH 3 COOH + Mn. SO 4 + K 2 SO 4 + H 2 O С -1 – 4 е =С+3 С +1 – 2 е = С+3 С -1 – 4 е = С+3 С -3 – 7 е = С+4 С -2 – 5 е = С+3 Mn+7 + 5 е = Mn+2 С -1 +С +1 +С -3 +С -2 – 22 е = 4 С+3 + С+4 5 С 12 Н 16 О 2+ 22 Л KMn. O 4+ 33 H 2 SO 4 = 5 С 9 Н 6 О 6 + 5 CO 2 + 5 CH 3 COOH + 22 Mn. SO 4 + 11 K 2 SO 4 + 38 Н 2 О 22 5 22 восстановитель окислитель Окисление Восстановление
Пример 2 + KMn. O 4 + H 2 SO 4 = + CO 2 + CH 3 COOH + Mn. SO 4 + K 2 SO 4 + H 2 O С -1 – 4 е =С+3 С +1 – 2 е = С+3 С -1 – 4 е = С+3 С -3 – 7 е = С+4 С -2 – 5 е = С+3 Mn+7 + 5 е = Mn+2 С -1 +С +1 +С -3 +С -2 – 22 е = 4 С+3 + С+4 5 С 12 Н 16 О 2+ 22 Л KMn. O 4+ 33 H 2 SO 4 = 5 С 9 Н 6 О 6 + 5 CO 2 + 5 CH 3 COOH + 22 Mn. SO 4 + 11 K 2 SO 4 + 38 Н 2 О 22 5 22 восстановитель окислитель Окисление Восстановление
 Практическая значимость Эта работа может быть интересна ученикам, собирающимся сдавать ЕГЭ по химии и (или) готовящимся к олимпиадам и конкурсам, а также их преподавателям.
Практическая значимость Эта работа может быть интересна ученикам, собирающимся сдавать ЕГЭ по химии и (или) готовящимся к олимпиадам и конкурсам, а также их преподавателям.
 Спасибо за внимание!
Спасибо за внимание!