МЕТОДЫ ПРОБОПОДГОТОВКИ И ИСПОЛЬЗОВАНИЕ ДРОБНОГО


МЕТОДЫ ПРОБОПОДГОТОВКИ И ИСПОЛЬЗОВАНИЕ ДРОБНОГО МЕТОДА В ХТА НА «МЕТАЛЛИЧЕСКИЕ ЯДЫ» Ст. преподаватель, к. ф. н. Петухов А. Е,

ВИДЫ БИООБЪЕКТОВ ХТА «МЕТАЛЛИЧЕСКИХ ЯДОВ» n Кровь, моча (живой пациент) n Внутренние органы (труп) n Волосы, ногти (при хронических отравлениях) n Вещественные доказательства (продукты питания, земля с места захоронения, доски гроба).

МЕТОДЫ ПРОБОПОДГОТОВКИ БИОМАТЕРИАЛА ПРИ ХТА «МЕТАЛЛИЧЕСКИХ ЯДОВ» n Сухое озоление n Сжигание n Сплавление с нитратом и карбонатом натрия n Влажное озоление n Концентрированными кислотами n Деструкция n СВЧ - пробоподготовка

СУХОЕ ОЗОЛЕНИЕ метод сжигания n Метод сухого озоления основан на нагревании органических веществ до высокой температуры при доступе воздуха. n Сухое озоление производят в фарфоровых, кварцевых или платиновых тиглях до постоянной массы. n При разрушении органических веществ с помощью этого метода на исследование берут относительно небольшие навески (1 — 10 г) исследуемых объектов. Увеличение навесок исследуемых объектов является нежелательным, так как это значительно увеличивает время озоления. n Метод применяется крайне редко, когда имеется специальное задание исследовать объекты биологического происхождения на наличие марганца, меди, висмута, цинка и некоторых других металлов.

МЕТОДИКА СУХОГО ОЗОЛЕНИЯ n Исследуемые объекты измельчают, высушивают исследуемую пробу. Затем обугливают эту пробу. Обуглившийся биоматериал охлаждают, смачивают азотной кислотой. Опять высушивают пробу, и переносят в фарфоровый тигель вместимостью 30— 50 мл, и осторожно нагревают на слабом пламени. При этом пламя не должно соприкасаться с дном тигля. n Для полноты сгорания содержимого тигля его смачивают концентрированным раствором н нитрата аммония, высушивают и прокаливают. После этого тигель охлаждают, а к его содержимому прибавляют раствор кислоты (соляной или азотной) для переведения оксидов металлов в их соли. После обработки кислотой содержимое тигля фильтруют. Фильтрат выпаривают досуха. Сухие остатки растворяют в 3 — 5 мл воды и полученные растворы подвергают ХТА.

НЕДОСТАТКИ СУХОГО ОЗОЛЕНИЯ n Улетучивание некоторых металлов или их соединений в процессе нагревания (соединения ртути, таллия, меди, никеля, хрома и др. ) n Взаимодействие отдельных металлов с материалом тиглей.

ВЛАЖНОЕ ОЗОЛЕНИЕ n Для минерализации органических веществ методом влажного озоления применяют кислоты-окислители (азотную, серную). n При помощи этих окислителей происходит разрушение биологического материала с образованием более простых химических соединений. n При минерализации биологического материала, содержащего металлы, связанные в организме с многими жизненно важными органическими соединениями, образуются соли этих металлов, которые можно обнаружить в минерализатах при помощи соответствующих реакций и методов.

МЕТОДИКА ВЛАЖНОГО ОЗОЛЕНИЯ n В начале минерализации концентрированная серная кислота играет роль водоотнимающего средства. Ее роль как водоотнимающего средства усиливается с повышением температуры. Благодаря водоотнимающему действию концентрированная серная кислота нарушает структуру клеток и тканей биологического материала. При повышении температуры (выше 110°С) и концентрации (до 60— 70 %) серной кислоты она проявляет окислительные свойства и разлагается с выделением оксида серы (IV). n Азотная кислота, находящаяся в смеси с серной кислотой, вначале минерализации является слабым окислителем. Со временем часть азотной кислоты при окислении биологического материала превращается в оксиды азота и азотистую кислоту, которые являются автокатализаторами дальнейшего более интенсивного процесса окисления органических веществ азотной кислотой. С образованием оксидов азота и азотистой кислоты, а также с повышением температуры азотная кислота проявляет себя как сильный окислитель.

МЕТОДИКА ВЛАЖНОГО ОЗОЛЕНИЯ n В первой стадии минерализации происходит деструкция биологического материала азотной и серной кислотами, которая заканчивается за 30— 40 мин. В результате деструкции получается прозрачная жидкость (деструктат), имеющая желтоватую или бурую окраску. n Во второй стадии минерализации происходит разрушение (окисление) органических веществ, находящихся в жидкой фазе (деструктате), полученной после деструкции биологического материала. Эта стадия разрушения более длительная, чем стадия деструкции.

МЕТОДИКА ВЛАЖНОГО ОЗОЛЕНИЯ n Для окончательного разрушения органических веществ, находящихся в жидкой фазе, к ней при нагревании по каплям прибавляют азотную кислоту. От прибавления больших количеств азотной кислоты происходит обильное выделение оксидов азота, выходящих из колбы и загрязняющих атмосферу лаборатории. От прибавления в колбу недостаточных количеств азотной кислоты находящиеся в ней органические вещества обугливаются горячей серной кислотой, о чем свидетельствует потемнение жидкости в колбе. При обугливании органических веществ серной кислотой из жидкости с выходящими газами могут улетучиваться соединения мышьяка и ртути. n Разрушение биологического материала азотной и серной кислотами считается законченным тогда, когда после прекращения добавления азотной кислоты (при нагревании колбы) будут выделяться белые пары серной кислоты и не будет происходить почернение минерализата.

ДЕНИТРАЦИЯ Денитрация — процесс освобождения минерализатов от азотной и азотистой кислот и оксидов азота. Денитрацию проводят формальдегидом. При взаимодействии формальдегида с азотной кислотой, которая почти всегда находится в минерализате, выделяется азот: 4 HNO 3 + 5 НСНО → 2 N 2 + 5 СО 2 + 7 Н 2 О. В результате взаимодействия азотистой кислоты с формальдегидом выделяются азот, оксид азота (II), оксид углерода (IV) и вода: 4 HNO 2 + 2 НСНО → Ν 2 + 2ΝΟ + 2 СО 2 + 4 Н 2 О.

ДЕНИТРАЦИЯ Оксид азота (II) окисляется кислородом воздуха до оксида азота (IV), который при взаимодействии с водой дает азотную и азотистую кислоты: ΝΟ + Ο 2 → ΝΟ 2 2ΝΟ 2 + Н 2 О → ΗΝΟ 2 + ΗΝΟ 3 Образовавшиеся при этом азотная и азотистая кислоты реагируют с формальдегидом, как указано выше. Избыток формальдегида, не вступившего в реакцию с азотной и азотистой кислотами, удаляют нагреванием жидкости в течение 5— 10 мин. Для проверки полноты денитрации минерализатов проводят реакцию с раствором дифениламина

ДЕСТРУКЦИЯ Деструкция — нарушение структуры биологического материала под влиянием азотной, серной и других кислот, обладающих окислительными свойствами, без полного разрушения органических веществ, переходящих в деструктаты. Ртуть в биологическом материале находится в связанном виде с сульфгидрильными и некоторыми другими функциональными группами белковых веществ. В результате деструкции ртуть переходит в деструктат в виде ионов, которые можно обнаружить и определить с помощью соответствующих реакций и физико-химических методов. Таким образом, после деструкции биологического материала в деструктате в различных количествах находятся ионы ртути, белки, пептиды, аминокислоты, липиды и др.

МЕТОДИКА ДЕСТРУКЦИИ 20 г измельченных органов вносят в колбу, в которую прибавляют 5 мл воды, 1 мл этилового спирта и 10 мл концентрированной азотной кислоты. Затем в колбу малыми порциями прибавляют 20 мл концентрированной серной кислоты с такой скоростью, чтобы оксиды азота не выделялись из колбы. После окончания прибавления концентрированной серной кислоты колбу оставляют на 5— 10 мин при комнатной температуре (до прекращения выделения оксидов азота). Затем колбу устанавливают на кипящую водяную баню и нагревают в течение 10— 20 мин. Если после нагревания колбы на кипящей водяной бане останутся неразрушенными кусочки биологического материала, то их осторожно растирают стеклянной палочкой о стенки колбы.

ДЕСТРУКЦИЯ Для ускорения деструкции к биологическому материалу прибавляют этиловый спирт, который является катализатором этого процесса. Для удаления из деструктата азотной, азотистой кислот и оксидов азота, образующихся в процессе деструкции, прибавляют мочевину. 2 HNO 2 + OC(NH 2) → 2 N 2 + СО 2 + 3 Н 2 О 2 HNO 3 + OC(NH 2) → N 2 + 2 NO + СО 2 + 3 Н 2 О

МЕТОДИКА ДЕСТРУКЦИИ При бурном протекании реакции с выделением оксидов азота в колбу прибавляют 30— 50 мл горячей воды. Полученный горячий деструктат смешивают с двойным объемом кипящей воды и, не охлаждая жидкость, фильтруют ее через двойной увлажненный фильтр. Фильтр, через который фильтровали деструктат, и остатки жира на нем 2— 3 раза промывают горячей водой. Промывные воды присоединяют к профильтрованному деструктату. Полученную при этом жидкость собирают в колбу, содержащую 20 мл насыщенного раствора мочевины, предназначенной для денитрации деструктата. Затем деструктат охлаждают, доводят водой до определенного объема и исследуют его на наличие ртути.

СОВРЕМЕННЫЕ МЕТОДЫ ПРОБОПОДГОТОВКИ n СВЧ – пробоподготовка n Пробоподготовка в приборах ААС и АЭС

Дробный анализ в ХТА «Металлических яов»

Дробный метод n В 30 -х годах XX столетия среди бессероводородных методов появилось новое направление – дробные методы анализа. Одним из создателей дробных методов анализа в аналитической химии был советский ученый проф. Николай Александрович Тананаев. n Дробный метод анализа предусматривает обнаружение того или иного иона в присутствии всех других ионов без их предварительного разделения на группы и особенно удобен в случаях с «лимитированными заданиями» , т. е. в таких, когда задача химика-аналитика ограничена заданием произвести исследование лишь на определенное число (2 -4) элементов.

История метода n В основу дробного метода анализа Н. А Тананаев положил «правило рядов» , согласно которому «выделение ионов из раствора в осадок производится действием другого аналогичного по составу осадка, но обладающего большей величиной произведения растворимости» . Примером правила рядов Н. А. Тананаева может служить ряд сульфидов. n Позднее другие авторы применили правило рядов к солям металлов с органическими кислотами и к их комплексам. n А. Х. Баталин в целях повышения специфичности реакций, их селективности и создания новых дробных реакций использовал учение о маскировке ионов (учение о подавлении ионов). С этой целью он использовал комплексообразование, изменение р. Н среды и т. п. n Дробный метод анализа для решения задач токсикологической химии разработан в Научно-исследовательском институте судебной медицины МЗ СССР А. Н. Крыловой.

Сущность метода n Дробный метод анализа включает качественный и количественный анализ на 12 элементов, относящихся к группе «металлических» ядов. Количественное определение имеет особое значение, так как чувствительность дробного метода анализа лежит на границе с естественным содержанием большинства токсикологически важных элементов. n Дробный метод основан на использовании специфичных реакций, экстракции и реэкстракции металлов в виде комплексов с органическими реагентами, такими как дитизон, диэтилдитиокарбаминаты и др. , комплексировании мешающих ионов. Методы количественного определения основаны на принципах дробного метода.

Трудности проведении дробного метода n Основные трудности проведении качественного анализа связаны с тем, что минерализат представляет собой кислую жидкость, содержащую большое количество железа, намного превосходящее количество искомых элементов, что во многих случаях мешает их обнаружено. Поэтому проведение многих реакций бывает невозможным без предварительного выделения искомых элементов из минерализата. С этой целью широко используются приемы селективной экстракции с последующей реэкстракцией различными органическими реагентами, такими как дитизон, соли диэтилдитиокарбаминатов и др. , образующие с металлами комплексы, растворимые в органических растворителях.

Органические комплексообразователи n Экстракция в виде диэтилдитиокарбаминатов применена для Cu, Zn, Cd, Bi с последующей реэкстракцией в водную фазу. n Селективная экстракция в виде дитизонатов применена для обнаружения и определения Pb, Ag, Hg, Zn. n Экстракция с красителями трифенилметанового ряда использована для дробного обнаружения Sb и Tl. n 8 -оксихинолин, для Bi.

Приемы маскировки мешающих ионов - введение комплексообразователей. Например, при исследовании на ионы Mn, Cr, Sb ион железа маскируется фосфат-ионами; - использование окислительно-востановительных реакций при исследовании на марганец, хром, мышьяк; - соблюдение определенных значений p. H среды при проведении химических реакций; - использование малых объемов и разбавление минерализата до пределов чувствительности реакций обнаружения, чтобы понизить концентрацию мешающих ионов.
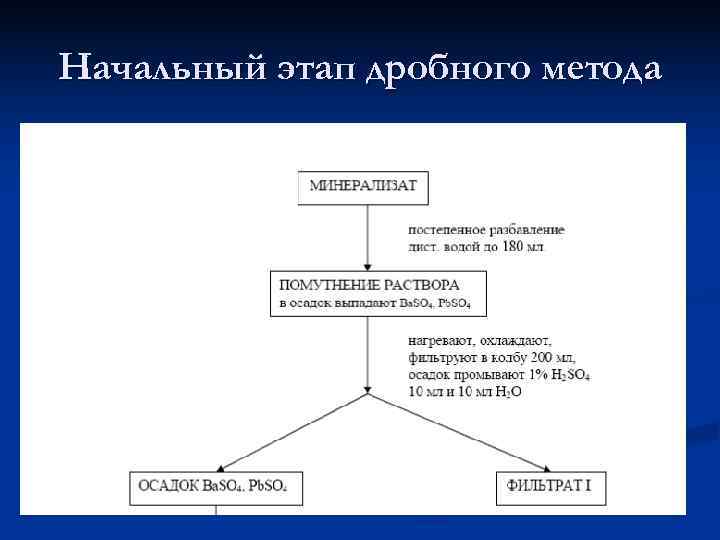
Начальный этап дробного метода

Использование дитизона в дробном методе n Дифенилтиокарбазон (сокращённо, дитизон [H 2 Dz]), представляет собой слабую кислоту, при р. Н=7, не растворимую в воде (сине-чёрные хлопья), и растворимую при р. Н › 7 (раствор жёлто- оранжевого цвета). [p. Ka=4, 5] n В органических растворителях дитизон растворяется относительнохорошо. При этом растворы дитизона окрашены в интенсивный зелёныйцвет.

Образование дитизонатов металлов n Дитизон образует внутрикомплексные соединения в определённом интервале р. Н со многими металлами. Образование дитизонатов происходит на границе раздела двух фаз при встряхивании водного раствора соли металла с раствором дитизона в органическом растворителе. Они почти не растворимы в воде и, поэтому количественно переходят в фазу органического растворителя (в качестве органических растворителей широко применяют CCl 4, CHCl 3).

Разделение дитизонатов металлов достигается различнымианалитическими приёмами: n Селективная экстракция анализируемого иона в определённоминтервале р. Н; n Добавление маскирующих веществ, которые образуют сопределёнными катионами труднодиссоциируемые соли или комплексныесоединения.

СПАСИБО ЗА ВНИМАНИЕ!
Лекция Металлы - вечерника.ppt
- Количество слайдов: 29

